Данное изобретение относится к применению тризамещенных бензопиранонов для лечения или профилактики патологических состояний, ассоциируемых с окислительным стрессом и/или воспалительными реакциями, и к новым тризамещенным бензопиранонам и их физиологически приемлемым солям. Данное изобретение относится также к растительным экстрактам, лекарственным веществам, диетическим пищевым продуктам и фармацевтическим препаратам.
Свободные радикалы представляют собой атомы молекул, имеющие неспаренный электрон на их внешней орбите. Для биологических процессов важнейшим свободным радикалом является молекулярный кислород, способный к образованию различных метаболитов путем восстановления. Эти метаболиты обычно охватываются собирательным термином "реакционноспособные кислородные группы" (ROS). Примеры ROS включают анион надокиси, гидроксильный радикал, перекись водорода, анион перекиси, синглетную форму кислорода, гипохлорид, окись азота и пероксинитрит.
ROS образуются спонтанно при протекании различных биологических процессов. Так называемый "окислительный взрыв" лейкоцитов, когда после стимулирования клеток микроорганизмами, ксенобиотиками или эндогенными веществами образуются надокисный радикал и другие ROS в качестве продуктов реакции из молекулярного кислорода за счет активации мембранной NADPH - оксидазы, имеет особенное значение. Респираторный взрыв представляет собой один из наиболее важных механизмов ранней неспецифической иммунной защиты и служит в основном для уничтожения проникших инфекционных агентов и опухолевых клеток. Кроме того, ROS в основном образуются при проникновении электронов, возникающих при недостаточно происшедших реакциях сочетания. Это происходит, например, при синтезе простагландинов и лейкотриенов из арахидоновой кислоты, во время митохондриального дыхания, при катализированном ксантин-оксидазой окислении гипоксантина в ишемических условиях или в процессе цитохром - Р450 - опосредованной метаболизации ксенобиотиков.
В то время как окислительный взрыв является в основном желательной реакцией при защите от инфекции, повышенное и непрерывное образование ROS представляет собой обычно нежелательное явление, поскольку окислительная атака не ограничивается инвазией микроорганизмов, собственная ткань организма также подвергается воздействию их токсичности. Это в особенности относится к неинфекционным болезням, например, повышенное образование ROS при аутоиммунных заболеваниях, при дегенеративных болезнях, во время ишемии или при метаболизации фармацевтических агентов. Нежелательное действие свободных радикалов и ROS основано на их взаимодействии с нуклеиновыми кислотами (например, индуцирование разрывов нитей ДНК), белками (например, денатурация, инактивация систем ферментов), углеводами (например, деполимеризация гиалуроновых кислот) или частично с липидами (например, перокисление липидов, повреждение мембран, образование провоспалительных простагландинов и лейкотриенов).
После того как около 50 лет тому назад было установлено, что реакционноспособные кислородные группы (ROS) участвуют в патогенезе различных болезней, в настоящее время считается доказанным, что эти молекулы играют важную роль в патогенезе многочисленных заболеваний, таких как сахарный диабет I и II типа, воспалительные болезни (например, ревматоидный артрит, астма, язвенный колит, псориаз), бактериальные и вирусные инфекции (например, грипп, СПИД, вирусный гепатит), атеросклероз, ишемия, неврологические заболевания, например, болезнь Альцгеймера, болезнь Паркинсона и другие нейродегенеративные заболевания), катаракта, серповидно-клеточная анемия и опухолевые болезни, и что они, кроме этого, ответственны также за процессы старения (A.Bendich (1994) in: B.Frei (ed.) "Natural Antioxidants in Human Health and Disease", Academic Press, San Diego, p.447; T.Peterhans (1997) J. Nutr. 127, 962 S; D.V.Parke (1999) in: T.K.Basu et al. (ed.) "Antioxidants in Human Health", CAB International, p.1).
В организме имеются различные системы защиты для защиты от вредного воздействия свободных радикалов и ROS. Они включают витамины (например, витамин Е и витамин С) и другие низкомолекулярные соединения (например, глютатионы, мочевая кислота), антиокислительные ферменты (например, надокись дисмутазы, каталаза и глютатионпероксидаза), а также белки, связывающие металлы (например, трансферрин, церулоплазмин). Однако собственные антиокислительные системы организма часто активны во время начальной фазы патологического процесса только потому, что повышенная концентрация ROS, образовавшихся в развивающемся патологическом процессе, превышает намного способность эндогенных механизмов защиты.
Следовательно, считается, что окислительный стресс представляет собой диспропорцию между концентрацией ROS и антиокислительными системами защиты. Таким образом, благодаря исключительному значению ROS в отношении многочисленных болезней существует огромный интерес к веществам, имеющим антиокислительные свойства, которые могут быть использованы для профилактики и лечения таких патологических состояний.
Так как ROS имеют особенное значение для воспалительных реакций, и окислительный стресс часто сопровождается ускоренным синтезом провоспалительных эйкозаноидов (например, простагландинов, лейкотриенов) и цитокинов (например IL-1, TNF-α, IL-6), к веществам, которые обладают антиокислительными свойствами и, кроме того, предотвращают образование этих медиаторов воспаления, проявляется особенный интерес.
Цель настоящего изобретения состоит в создании соединений для лечения или профилактики патологических состояний, связанных с окислительным стрессом и/или воспалительными реакциями.
Эта цель достигается за счет применения соединений общей формулы I
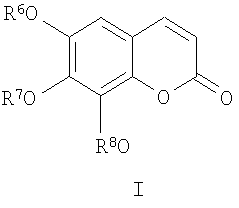
где остатки R6, R7 и R8 независимо обозначают Н или SO3H и их физиологически приемлемых солей для лечения или профилактики патологических болезней, связанных с окислительным стрессом и/или воспалительными реакциями.
Неожиданно было обнаружено, что 6,7,8-тригидрокси-2Н-1-бензопиран-2-он (соединение II) обладает особенно благоприятными фармакологическими свойствами. В добавление к сильному антиокислительному действию это соединение также ингибирует синтез лейкотриенов и простагландинов, а также синтез провоспалительных цитокинов IL-1β, TNF-α и IL-6. Так, соединение II в основном пригодно для лечения или профилактики болезней, сопровождающихся окислительным стрессом, таких как сахарный диабет I типа и/или II типа, атеросклероз и эндотелиальная дисфункция, ишемия, неврологические болезни (например, болезнь Альцгеймера, болезнь Паркинсона и другие нейродегенеративные болезни), катаракта и опухолевые болезни. Однако соединение II особенно благоприятно для патологических болезней, имеющих воспалительный компонент, таких как ревматоидный артрит, астма, язвенный колит, болезнь Крона, псориаз, нейродермит и инфекции, вызванные бактериями, вирусами (например, грипп, СПИД, вирусный гепатит) и другими патогенами (например, паразитами, грибками и прионами). Соединение II уже было описано в литературе (O.Kayser и H.Kolodziej, Phytochemistry 39, 1181-1185 (1995); S.Kumar, A.B.Ray, C.Konno, Y.Oshima и H.Hikino, Phytochemistry 27, 636-638 (1988); K.P.Lattem O.Kayser, N.Ntan, M.Kaloga и H.Kolodziej, Z.Naturforsch. 55 c, 528-533 (2000)), однако фармакологическое действие соединения II до сих пор неизвестно. Соединение II содержится в Pelargonium sidoides только в концентрации 0,0004% (Kayser et al.; Latte et al.; см. выше) и в Pelargonium reniforme только в концентрации 0,02% (Latte et al., см. выше). Следовательно, нужно сделать вывод, что соединение II не вносит значительного вклада в биологическую эффективность Pelargonium sidoides и reniforme в этих низких концентрациях.
Предметом данного изобретения является применение соединения II для лечения или профилактики патологических состояний, связанных с окислительным стрессом и/или воспалительными реакциями.
Можно также применять соединение II в виде эфиров серной кислоты общей формулы I, так как соединение II высвобождается из этих соединений при пероральном введении. По этой причине соединения общей формулы I также пригодны для лечения или профилактики вышеуказанных патологических состояний. Предпочтительные соединения общей формулы I представляют собой 6,7-дигидрокси-8-сульфокси-2Н-1-бензопиран-2-он (R6=R7=Н; R8=SO3H) и 7,8-дигидрокси-6-сульфокси-2Н-1-бензопиран-2-он (R7=R8=Н; R6=SO3H). Особенно предпочтительным является соединение 6,8-бис-(сульфокси)-7-гидрокси-2Н-1-бензопиран-2-он (R6=R8=SO3H; R7=Н; соединение III). Соединения общей формулы I, где по меньшей мере один из радикалов R6, R7 или R8 представляет собой SO3H, являются новыми. Поэтому эти соединения и особенно соединение формулы III, а также их применение для лечения или профилактики патологических состояний, связанных с окислительным стрессом и/или воспалительными реакциями, также составляют часть данного изобретения.

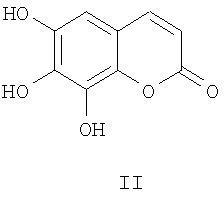
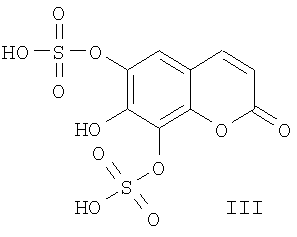
В общей формуле I радикалы R6, R7 и R8 независимо обозначают атом водорода или остаток SO3H. Соединения общей формулы I, а также соединения формулы II и формулы III могут быть в виде физиологически приемлемых солей с щелочными металлами, щелочноземельными металлами и других солей, например калиевых солей. Эти соли также являются предметом данного изобретения.
Далее, растительные экстракты, в частности, из Pelargonium species, содержащие одно или несколько соединений формулы I, где по меньшей мере один из радикалов R6, R7 и R8 обозначает SO3H, и фармацевтические препараты, полученные на их основе, также составляют часть данного изобретения. При этом экстракты, содержащие по меньшей мере одно из соединений общей формулы I в сухом веществе растительного экстракта в концентрации между 0,1% и 10%, являются предпочтительными, а экстракты с концентрацией этих соединений между 0,5% и 5% особенно предпочтительны. Количество сухого вещества соответствует сухому остатку согласно Ph. Eur. (жидкие экстракты), причем определение можно проводить непосредственно, например, в жидком экстракте и сухой остаток можно определить путем расчета.
Получение соединения II проводят путем гидролиза и/или расщепления эфирной связи, например, коммерчески доступного фраксина или соединения формулы I, где по меньшей мере один из остатков R6, R7 и R8 является SO3H.
Получение тех соединений общей формулы I, где по меньшей мере один из радикалов R6, R7 и R8 обозначает остаток SO3H, можно осуществить путем взаимодействия соединения II с комплексом трехокись серы - триметиламин или в случае соединения III путем выделения из соответствующего растительного материала, например, из высушенных корней Pelargonium sidoides. Соединения 6,7-дигидрокси-8-сульфоокси-2Н-1-бензопиран-2-он (общая формула I; R6=R7=Н; R8=SO3H) и 7,8-дигидрокси-6-сульфоокси-2Н-1-бензопиран-2-он (общая формула I; R7=R8=Н; R6=SO3H) могут быть также получены путем частичного гидролиза соединения формулы III.
Согласно данному изобретению экстракты могут быть получены с разным составом из растений пеларгонии или их частей известными методами с применением растворителей, таких как вода, метанол, этанол, ацетон и т.д., и их смесей при температурах от комнатной до 60°С при перемешивании от слабого до энергичного или путем перколяции в течение промежутка времени от 10 мин до 24 ч. Предпочтительными растворителями для экстракции являются вода или смеси этанола и воды с содержанием воды по меньшей мере 50 вес.%, особенно предпочтительным является отношение этанол/вода от 10/90 до 15/85 (вес./вес.). Для дальнейшего увеличения концентрации соединений общей формулы I согласно данному изобретению может быть проведено дополнительное концентрирование, например, распределение жидкость - жидкость, с применением смесей 1-бутанол/вода или этилацетат/вода, адсорбция - десорбция с применением ионообменников, LH20, НР20 и других смол, или хроматографическое выделение с применением RP18, силикагеля и т.п. Если желательно, проводится дальнейшая обработка с получением сухих экстрактов в соответствии с методами, известными как таковые путем удаления растворителя при повышенной температуре и/или пониженном давлении или путем замораживания - сушки. Согласно European Pharmacopoeia сухие экстракты содержат сухой остаток, равный по меньшей мере 95 вес.%.
Соединения общей формулы I в соответствии с данным изобретением и экстракты, содержащие по меньшей мере одно из этих соединений соответственно, предпочтительно вводятся перорально в виде порошков, гранул, таблеток, драже или капсул или в виде раствора.
Доза составляет от 0,1 мг/день до 250 мг/день, предпочтительно 0,3-50 мг/день для одного или нескольких соединений общей формулы I.
Для приготовления таблеток по меньшей мере одно из соединений общей формулы I или соответствующий экстракт смешиваются с подходящими фармацевтически приемлемыми добавками, такими как лактоза, целлюлоза, двуокись кремния, кроскармелоза и стеарат магния, и затем осуществляется прессование в таблетки, которые могут быть снабжены подходящим покрытием, изготовленным, например, из гидроксиметилпропилцеллюлозы, полиэтиленгликоля, красителей (например, двуокиси титана, окиси железа) и талька.
Эффективность соединения формулы II в случае патологических состояний, связанных с окислительным стрессом и/или воспалительными реакциями, подтверждается экспериментами, описанными ниже.
Антиокислительные свойства
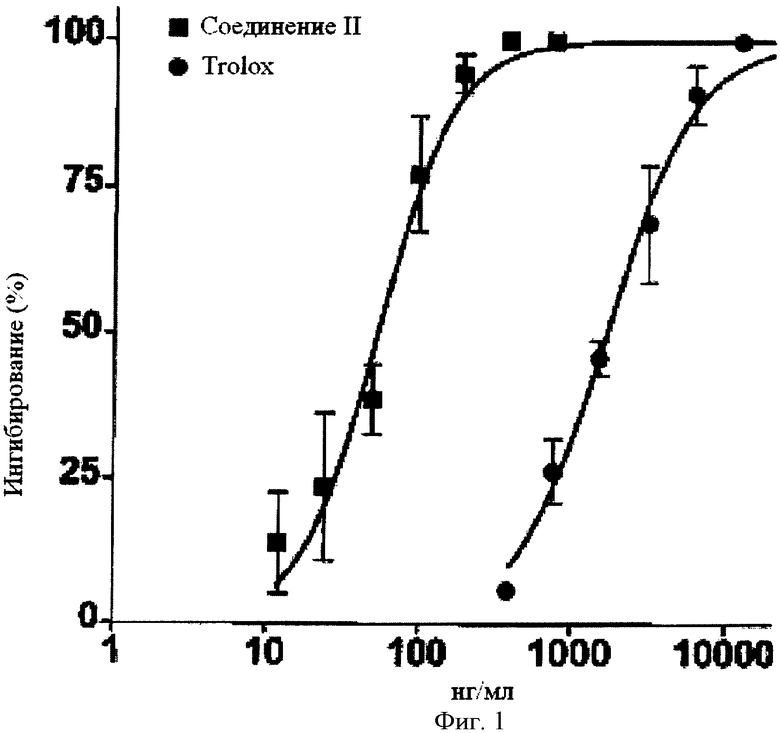
Аутоокисление липидов связано с эмиссией света. Определение этой чрезвычайно слабой хемолюминесценции может быть использовано как для количественного определения перекисей, так и для оценки эффективности антиоксидантов. Мозговая ткань самца мыши (NMRI; 20-30 г; Centre d'Elevage Janvier, Le Genest - Saint Isle, France) служила в качестве обогащенной липидами ткани при проведении исследований. После экстракции мозг промывали ледяным физиологическим раствором, содержащим фосфатный буфер (PBS, pH 7,4) и освобождали от мозговой оболочки и остаточной крови. Образцы ткани гомогенизировали в 4-х кратном объеме (об/вес) PBS и центрифугировали при 1000x г и 4°С в течение 10 мин. Надосадочные жидкости сразу же разбавляли тем же самым буфером до 3-х кратного объема и хранили на льду. 250 мкл разбавленной надосадочной жидкости помещали в пробирку для испытаний и инкубировали в течение 10 мин при 37°С в 6-канальном люминометре (Multi - Biolumat LB 9505 С, Berthold, Bad Wildbad). После добавления 25 мкл соединения II в PBS с добавлением 2,5% ДМСО инкубацию продолжали еще 10 мин. Затем определяли интенсивность хемолюминесценции (CL) в течение 60 мин. Процент ингибирования аутоокисления определяли по сравнению с растворителем (PBS с добавлением 2,5% ДМСО), при этом ингибирование в случае растворителя определяли одновременно. Соединение II ингибировало аутоокисление липидов с превосходной активностью при полумаксимальной концентрации, равной 53 нг/мл (Фигура 1). В противоположность этому Trolox, который часто используют в качестве эталонного вещества при определении антиокислительных свойств, имел полумаксимальную концентрацию ингибирования, равную 1665 нг/мл.
На Фигуре 1 показано влияние соединения II и Trolox'a на аутоокисление липидов. Величина ингибирования перокисления липидов сравнивалась с соответствующей величиной для растворителя в трех независимых опытах (средняя величина ±SD).
Ингибирование синтеза провоспалительных цитокинов
Влияние соединения II на синтез провоспалительных цитокинов IL-1β, TNF-α и IL-6 определяли с применением активированных перитонеальных макрофагов грызунов. Для выделения активированных макрофагов самцам мышей NMRI (Centre d'Elevage Janvier, Le Genest - Saint Isle, France) парентерально вводили 3×109 умерщвленных дифтериеподобных бактерий parvum (Changzhou Yanshen Co. Ltd., Changzhou, China) в 0,5 мл PBS. Через 6 дней брюшную полость промывали 2,5 мл сбалансированного физиологического раствора Хэнкса (HBSS), не содержащего кальция и магния и содержащего 10 ед/мл добавленного гепарина. Клетки снова суспендировали при концентрации 2×106 кл/мл в полной среде RPMI, дополненной 10% фетальной телячьей сыворотки. Лунки 96-луночного микротитрационного планшета заполняли 200 мкм суспензии клеток. Через 2 ч инкубирования неприлипшие клетки удаляли и оставшиеся клетки дважды промывали культуральной средой (37°С). Макрофаги предварительно инкубировали в течение 30 мин с соединением II и затем индуцировали синтез провоспалительных цитокинов путем добавления 1 мкг/мл липосахарида E.coli (серотип 0127: В8, Sigma, Deisenhofen). После инкубирования в течение 24 ч (37°С, 5% СО2 в воздухе) клетки подвергали лизису путем трехкратного замораживания и оттаивания, надосадочные жидкости отделяли и замораживали при -80°С до проведения анализа. Определение концентрации цитокинов в надосадочной жидкости проводили при помощи коммерческих наборов (Duosets IL-1β, TNF-α и IL-6, R и D, Wiesbaden) в соответствии с инструкциями производителя. Все определения проводили 3 раза. Влияние соединения II на синтез цитокинов оценивали по сравнению с контрольным растворителем (0,1% ДМСО в полной среде RPMI), определение проводили одновременно. Как видно из Таблицы I ниже, соединение II с концентрацией 100 мкг/мл ингибировало синтез всех трех испытанных цитокинов, ингибирование продуцирования IL-6 было наибольшим.
Влияние соединения II на синтез провоспалительных цитокинов в активированных перитонеальных макрофагах мышей. Показаны средние величины + SD для трех параллельных опытов. Влияние соединения II определяли как изменение в процентах по сравнению с контрольным растворителем (* вероятность ошибки Р<0,05, t - тест)
Ингибирование активности циклооксигеназы и липоксигеназы в цельной крови человека
Для опытов применяли гепаринизированную цельную кровь человека. 100 мкл цельной крови добавляли в каждую лунку микротитрационных планшетов с 96 лунками. Отделенные планшеты использовали для определения активности циклооксигеназы 1 (СОХ1) и липоксигеназы (LO), а также индукции циклооксигеназы 2 (СОХ2).
Соединение II разбавляли в среде DME (DMEM) 1% раствором антибиотиков/антимикотиков и 2 мМ L - глютамина (Sigma, Deisenhofen), применяя ДМСО (конечная концентрация 0,1%) в качестве промотора растворимости. После добавления 50 мкл соединения II среду культивировали в течение 60 мин при 37°С. Затем для стимулирования синтеза эйкозаноидов добавляли 50 мкл кальцийионофора А23187 (конечная концентрация 50 мкМ). После культивирования еще в течение 30 мин при 37°С микротитрационные планшеты центрифугировали в течение 5 мин при 4°С, 1500 г. Плазму отбирали пипеткой и замораживали при -80°С до начала проведения анализа.
Для того чтобы доказать активность СОХ2 образцы крови (100 мкл/лунку) вначале обрабатывали аспирином (50 мкл в DMEM, конечная концентрация 12 мкг/мл) в течение 6 ч при 37°С для инактивации СОХ1. Затем добавляли соединение II и растворитель (DMEM с 1% ДМСО) до объема 25 мкл. Более того, для индуцирования экспрессии СОХ2 добавляли 25 мкл липополисахарида E.coli (серотип 0127: В8, конечная концентрация 10 мкг/мл). После культивирования в течение 18 ч при 37°С выделяли плазму, как описано выше, и также хранили при -80°С до начала определения.
В образцах плазмы в качестве параметров активности для СОХ1, СОХ2 и LO определяли ТХВ2, PGE2 и цистениллейкотриены (цистенил - LT). В соответствии с инструкциями производителей для анализа применяли наборы EIA (ТХВ2 и PGE2: Caymann/IBL, Hamburg; цистениллейкотриены: CAST - 2000, Milenia, Bad Nauheim). По результатам (см. Таблицу 2) видно, что соединение II в значительной степени ингибирует активность СОХ2 и LO.
С другой стороны, активность СОХ1 почти не изменяется. Спектр эффективности должен рассматриваться как чрезвычайно благоприятный, так как при терапевтическом применении соединения II побочные эффекты, типичные для ингибиторов СОХ1, такие как заболевания желудочно-кишечного тракта (эрозия, язвы) или кровотечения благодаря ингибированию агрегации тромбоцитов можно не принимать во внимание.
Влияние соединения II на синтез цистенил - LT, TXB2 и PGE2 в цельной крови человека. Приведены средние величины ±SD для двух параллельных опытов. Действие соединения II определяли как изменение величины в % по сравнению с растворителем (контроль)
Пример 1: Получение 6,7,8-тригидрокси-2Н-1-бензопиран-2-она (соединение II)
20 г (42,7 ммол) калиевой соли 6,8-бис-(сульфокси)
-7-гидрокси-2Н-1-бензопиран-2-она перемешивали в 480 мл примерно 2 N соляной кислоты в течение 20 ч при 40-50°С. После охлаждения осажденный сырой продукт отфильтровывали и перекристаллизовывали из воды (горячая фильтрация). Кристаллы отфильтровывали, промывали и сушили под вакуумом при 100°С: 5,9 г (71%), точка плавления: разложение начинается при 260°С; 1Н и 13С ЯМР совпадают с указанными O.Kayser и H.Kolodziej (Phytochemistry 39, 1181-1185 (1995)).
Пример 2: Выделение и определение структуры калиевой соли 6,8-бис-(сульфоокси)-7-гидрокси-2Н-1-бензопиран-2-она (калиевая соль соединения III)
15 кг измельченных корней Pelargonium sidoides подвергали перколяции при комнатной температуре, применяя 75 л и 40 л воды, соответственно. Водный экстракт концентрировали примерно до 1/3 объема, к нему добавляли 7 кг сульфата аммония и экстрагировали несколько раз 3/2 смесью 2-бутанона/этанола. Органические фазы соединяли и концентрировали выпариванием.
Полученный остаток хроматографировали на колонке НР20 (элюент - вода). Фракции 6,8-бис-(сульфоокси)-7-гидрокси-2Н-1-бензопиран-2-она концентрировали, устанавливали величину pH, равную 8, при помощи раствора гидроокиси калия и разбавляли этанолом в отношении 1/1. Осадок отфильтровывали и суспендировали в воде. При помощи раствора гидроокиси калия устанавливали величину pH, равную 10,7, и разбавляли продукт этанолом в отношении 1/1. Полученный в результате осадок снова растворяли в горячей воде. Горячий раствор отфильтровывали и разбавляли этанолом в отношении 1/1. Осажденные кристаллы отфильтровывали, промывали и высушивали под вакуумом при температуре 50°С: 27,6 г (0,14% в расчете на растительный материал, определен как свободная кислота).
Точка плавления: разложение начинается при 216°С; C9H3K3O11S2 (468.55) найдено: C 23.08%, H 0.70%, K 24.65%, S 13.9% - рассчитано: C 23.07%, H 0.65%, K 25.04%, O 37.56%, S 13.69%; 1Н ЯМР (DMSO-d6): δ=7.62 (d, J=9.1 Hz, H-4), 7.03 (s, Н-5), 5.59 (d, J=9.1 Hz, H-3); 13С NMR (DMSO-d6): δ=162.9 (C-7), 161.9 (C-2), 147.7 (C-8), 145.1 (C-4), 142.2 (C-6), 130.4 (С-8a), 115.5 (С-5), 102.4 (С-3), 101.5 (С-4а).
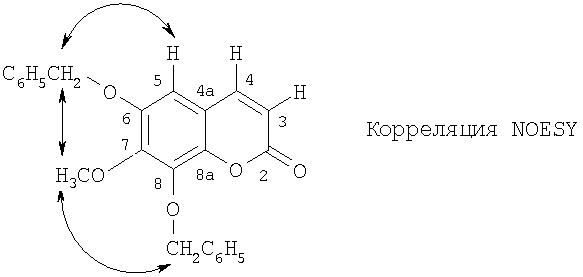
Кислотный гидролиз калиевой соли тригидроксикумариндисульфата приводит к получению 6,7,8-тригидроксикумарина (см. Пример 1). Для дальнейшего определения структуры соединение III подвергали дериватизации в соответствии со следующей схемой реакции:
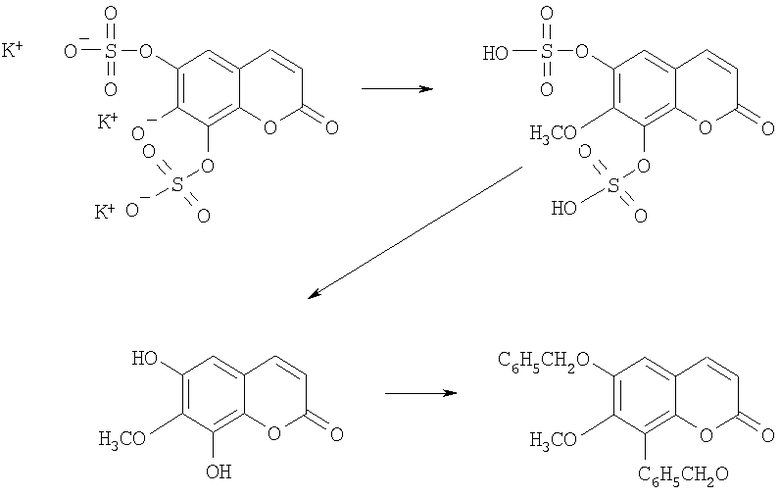
Для этой цели калиевую соль тригидроксикумариндисульфата подвергали взаимодействию с метилйодидом в присутствии карбоната калия при 60°С в DMF для получения соответствующего 7-метилэфира. После подкисления концентрированной соляной кислотой реакционную смесь перемешивали в течение 24 ч при 50°С, экстрагировали этилацетатом и осуществляли хроматографию на силикагеле (элюент: гептан/этилацетат 7/3): 6,8-дигидрокси-7-метоксикумарин. Этот продукт подвергали реакции с бензилбромидом в присутствии карбоната калия и йодида калия в DMF при комнатной температуре. Смесь концентрировали и остаток распределяли между водой и ТВМЕ. Органическую фазу концентрировали и осуществляли хроматографию на силикагеле (элюент: толуол/этанол 95/5): 6,8-дибензилокси-7-метоксикумарин.
Смесь продуктов замещения полученного соединения определяли методом одноразмерной и двухразмерной ЯМР-спектроскопии в CDCl3. Четкая корреляция NOESY между Н-5 и одним из СН2-сигналов позволяет сделать однозначный вывод о наличии бензилоксигруппы в положении 6. Далее, ОСН3-сигнал коррелирует с СН2-сигналами, что указывает на то, что метокси-группа расположена между двумя бензилоксигруппами, то есть в положении 7. Корреляция НМВС между C-7 и Н-5, а также ОСН3, а также между С-8 и Н-4 и 8-СН2 подтверждает схему замещения по NOESY. Можно сделать четкий вывод, исходя из последовательности стадий получения данного производного и его структуры, что сульфооксигруппы дисульфата тригидроксикумарина присоединены в положениях 6 и 8.
Пример 3: Растительный экстракт с содержанием 6,8-бис-(сульфоокси)-7-гидрокси-2Н-1-бензопиран-2-она (соединение III)
500 г измельченных корней Pelargonium sidoides экстрагировали 3 кг воды в течение 4 ч при комнатной температуре. Экстрагированный растительный материал отфильтровывали и еще раз экстрагировали 2 кг воды, как описано выше, и отфильтровывали. Фильтраты соединяли и концентрировали при температуре около 35°С и замораживали - оттаивали: 58,7 г (11,7%) сухого экстракта, содержащего 1,54% соединения III.
Пример 4: Растительный экстракт с содержанием 6,8-бис-(сульфоокси)-7-гидрокси-2Н-1-бензопиран-2-она (соединение III)
Около 1,25 кг измельченных корней Pelargonium sidoides экстрагировали при помощи примерно 12,5 кг смеси этанола/воды 11/89 (вес/вес) при комнатной температуре. После фильтрования фильтрат концентрировали при температуре около 45°С и замораживали/оттаивали: 90,4 г (7,2%) сухого экстракта, содержащего 1,86% соединения III.
Пример 5: Таблетки
Для приготовления таблеток, содержащих 5-250 мг активного ингредиента в зависимости от желательной эффективности, необходимо следующее:
Активный ингредиент необязательно измельчали, смешивали с добавками и прессовали в таблетки весом 250 мг и диаметром 9 мм, соответственно, обычным способом. В случае доз, превышающих 125 мг, прессованием получали таблетки весом 500 мг и диаметром 11 мм. В случае необходимости получали на таблетках пленочное покрытие.
Результаты биологических испытаний
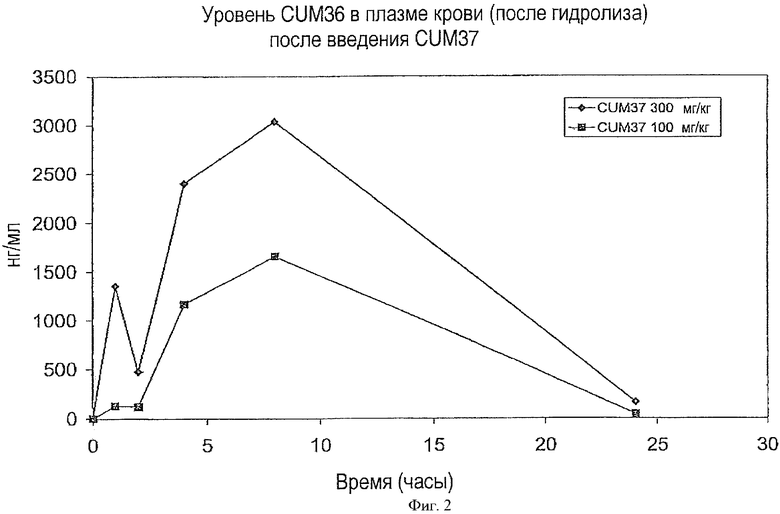
Крысам вводили перорально 100 мг/кг и 300 мг/кг калиевой соли соединения III (=CUM0037), соответственно. Методом жидкостной хроматографии высокого разрешения определяли количество соединения II (=CUM0036) в плазме крови животных после ферментативного расщепления (=гидролиза) арил-сульфатазой/глюкоронидазой. Фигура 2 показывает, что в плазме крови можно обнаружить значительное количество соединения II.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СТАБИЛЬНЫХ ПРИ ХРАНЕНИИ РАСТВОРОВ ЭКСТРАКТОВ ПЕЛАРГОНИИ | 2008 |
|
RU2454246C2 |
| ПРИМЕНЕНИЕ ЭКСТРАКТОВ ИЗ ПЕЛАРГОНИИ | 2004 |
|
RU2342941C2 |
| 2-2-ДИАЛКИЛ- ИЛИ ТРАНС-2,2-ДИАЛКИЛ-3,4-ДИГИДРО-3-ГИДРОКСИ-6-(ПИРИДИН-4-ИЛ)-2Н-1-БЕНЗОПИРАН | 1992 |
|
RU2104277C1 |
| БЕНЗОПИРАНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 1996 |
|
RU2160735C2 |
| СОЕДИНЕНИЯ ФЛАВОНОИДОВ И ИХ ПРИМЕНЕНИЕ | 2006 |
|
RU2431634C2 |
| НОВЫЕ СОЕДИНЕНИЯ ФЛАВОНОИДОВ И ИХ ПРИМЕНЕНИЕ | 2013 |
|
RU2647842C2 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛИНДИОНА КАК ИНГИБИТОРЫ НАДФН-ОКСИДАЗЫ | 2010 |
|
RU2569855C2 |
| ПРОИЗВОДНЫЕ ИНДОЛА | 1992 |
|
RU2061694C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ БЕНЗОЦИКЛОАЛКЕНИЛДИГИДРООКСИАЛКАНОВЫХ КИСЛОТ | 1990 |
|
RU2012554C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ, ВКЛЮЧАЯ ТРАНС-7-ОКСО-6-(СУЛЬФОКСИ)-1,6-ДИАЗАБИЦИКЛО[3.2.1]ОКТАН-2-КАРБОКСАМИД И ЕГО СОЛИ | 2012 |
|
RU2769076C2 |
Данное изобретение относится к применению бензопиранонов формулы II для изготовления фармацевтического препарата для лечения и/или профилактики патологических состояний, связанных с окислительным стрессом и/или воспалительными реакциями. Изобретение также относится к калиевой соли 6,8-бис-(сульфокси)-7-гидрокси-2Н-1-бензопиран-2-она. Технический результат - бензопираноны, обладающие антиокислительными свойствами, полезные для профилактики и лечения патологических состояний, ассоциируемых с окислительным стрессом и/или воспалительными реакциями. 3 н. и 4 з.п. ф-лы, 2 табл., 2 ил.
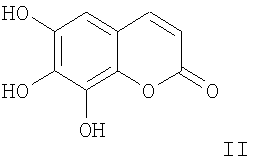
1. Применение соединения формулы II
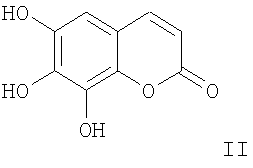
и его физиологически приемлемых солей для изготовления фармацевтического препарата для лечения и/или профилактики патологических состояний, связанных с окислительным стрессом и/или воспалительными реакциями.
2. Применение по п.1, отличающееся тем, что соединение формулы II содержится в растительном экстракте.
3. Применение по п.2, отличающееся тем, что растительный экстракт получен из Pelargonium species.
4. Применение по п.3, отличающееся тем, что растительный экстракт получен из Pelargonium sidoides.
5. Фармацевтический препарат для лечения или профилактики патологических состояний, связанных с окислительным стрессом и/или воспалительными реакциями, содержащий соединение формулы II
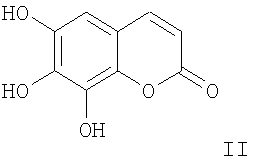
в качестве активного ингредиента и фармацевтически приемлемый носитель.
6. Фармацевтический препарат по п.5, в виде оральной формы введения.
7. Калиевая соль 6,8-бис-(сульфокси)-7-гидрокси-2Н-1-бензопиран-2-она.
| Klaus Peter Latte et al.: "Unusual coumarin patterns of Pelargonium species forming the origin of the traditional herbal medicine Umckaloabo", ZEITSCHRIFT FUER NATURFORSCHUNG, C: JOURNAL OF BIOSCIENCES, 2000, v.55 (7/8), p.528-533 | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| НОВЫЕ ГИДРОКСИ- И ПОЛИГИДРОКСИПРОИЗВОДНЫЕ КУМАРИНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1998 |
|
RU2207338C2 |
| ПРОИЗВОДНЫЕ КУМАРИНА, ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ PLA-ИНГИБИТОРОВ И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 1994 |
|
RU2133745C1 |
Авторы
Даты
2010-03-10—Публикация
2005-06-30—Подача