ОБЛАСТЬ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Данное изобретение относится к ингибированию αv интегринов, в частности αvβ3 и αvβ6 интегринов, с помощью специфических антагонистов, предпочтительно непептидных антагонистов, таких как EMD 409915 и EMD 409849, родственных соединений и соединений со сравнимой специфичностью, которые осуществляют понижающую регуляцию фиброгенеза с помощью ингибирования клеточной миграции и продукции профиброгенных молекул (например, коллагеназы, ТМР-1) и цитокинов (например, CTGF, TGFβ1,2) с помощью активированных печеночных звездчатых клеток, активированных миофибробластов и активированного фибробластами эпителия и эндотелия. Эти антагонисты в отдельности или в комбинации с другими агентами могут эффективно предотвращать, уменьшать или даже вызывать обратное развитие прогрессивного фиброза, такого как фиброз/цирроз печени, а также фиброз других органов, таких как легкие, почки, кишечник, поджелудочная железа, кожа и артерии.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ И УРОВЕНЬ ТЕХНИКИ
Активированные печеночные звездчатые клетки и миофибробласты играют центральную роль в развитии хронических заболеваний печени. Они депонируют избыток компонентов экстрацеллюлярного матрикса, что приводит к фиброзу и, в конце концов, к циррозу. Цирроз определяется как искажение структуры печени тяжелыми сосудистыми и функциональными аномалиями. Последствиями этого являются гипертензия воротной вены с развитием асцитов и пищеводного варикозного кровотечения, печеночная энцефалопатия и предрасположенность к частым летальным инфекциям. Определенные рецепторы клетка-клетка и, особенно, клетка-матрикс, главным образом интегрины, подвергаются повышающей регуляции на активированном эндотелии и HSC/MF, передавая сигналы миграции, усиления роста и другие профиброгенные сигналы.
Таким образом, активация интегрина αvβ3 опосредует активацию и миграцию HSC/MF в ответ на профиброгенные цитокины, такие как PDGF-АВ/ВВ, и индуцирует повышающую регуляцию экспрессии HSC/MF профиброгенных цитокинов, таких как CTGF, фактор, который стимулирует синтез коллагена ауто- и паракринным путем.
Подобно этому, значительная повышающая регуляция интегрина αvβ6 была обнаружена в активированных эпителиальных клетках, в частности в пролиферирующем эндотелии желчного протока фиброзной печени, что дополнительно усиливает фиброгенез путем запуска секреции основной мембраны и других профиброгенных белков и ростовых факторов, которые активируют HSC/MF.
Лечение фиброзных заболеваний печени и цирроза с помощью специфических антагонистов интегринов αvβ3 и αvβ6 может блокировать миграцию и активацию эндотелиальных клеток, HSC/MF и эпителиальных клеток и, таким образом, замедлять или даже вызывать обратное развитие фиброгенеза. Поскольку аналогично печени, активированные миофибробластоподобные клетки и эпителиальные клетки играют центральную роль в патогенезе других прогрессивных фиброзных заболеваний, специфические антагонисты интегринов αvβ3 и αvβ6 также могут использоваться для лечения фиброзных расстройств других органов, например поджелудочной железы, кишечника, легких, сердца, почек, артерий или кожи.
Интегрины представляют собой семейство трансмембранных клеточных рецепторов, которые опосредуют взаимодействия между клетками и между клетками и экстрацеллюлярным матриксом. Потеря опосредуемых интегринами контактов обычно приводит к апоптозу. Рецепторы интегринов состоят из α и β субъединиц, которые могут существовать, по крайней мере, в 24 различных комбинациях, каждая из которых имеет свои собственные специфичности связывания и свойства передачи сигналов. Подсемейство β3 цепей состоит из двух интегринов, αIIβ3 и αvβ3. αIIβ3 экспрессируется на тромбоцитах и мегакариоцитах и участвует в процессе образования тромбов, αvβ3 представляет собой нетромбоцитарный интегрин, который экспрессируется эндотелиальными и миофибробластными клетками, определенными активированными фибробластами/миофибробластами, а также некоторыми воспалительными клетками (1-3). Цепь β6 интегрина, в основном, обнаруживается на эпителиальных клетках и некоторых активированных фибробластах/миофибробластах, она образует гетеродимер только с субъединицей αv (4).
Некоторые сообщения продемонстрировали, что экспрессия αvβ3, которая происходит, тесно ассоциирована с онкогенной трансформацией и развитием опухоли, то есть инвазивными и метастатическими свойствами опухолевых клеток человека. Индуцированная экспрессия интегрина αvβ3 на поверхности эндотелитальных клеток, как предполагают, является существенной для миграции эндотелиальных клеток, пролиферации и образования трубчатых структур (5). В последние годы стало очевидным, что адгезия к белкам экстрацеллюлярного матрикса (ЕСМ), опосредованная интегринами, необходима для роста и выживания большинства типов клеток (2). Нарушение адгезии задерживает клетки в фазе G1 и вызывает апоптоз. Было обнаружено, что интегрин αvβ3 играет фундаментальную роль в процессе ангиогенеза путем ингибирования апоптоза эндотелиальных клеток (6). Сверхэкспрессия αvβ3 в клетках яичника китайского хомячка повышает активность Rho и усиливает образование волокон (7), факторов, которые связаны с адгезией, миграцией и активацией.
Понижающая регуляция рецепторной системы PDFG (BB)-PDGFBβ играет важную роль в процессе фиброгенеза, то есть при de novo образовании и отложении экстрацеллюлярного матрикса (ЕСМ) в таких органах, как печень (8). Активированный рецептор PDGFβ может быть подвергнут совместной иммунопреципитации вместе с αvβ3 (9) интегрином. Недавно было показано, что αvβ3 взаимодействует с фрагментом RGD пептида, трансформирующего ростового фактора бета (TGFβ) (10), ассоциированного с латентным состоянием (LAPβ1), который может быть вовлечен в раковый процесс и в ряд воспалительных и фиброзных заболеваний, при которых экспрессия обоих белков играет важную роль.
αvβ3 является существенным для гладкой мускулатуры и миграции эндотелиальных клеток, а также при образовании кровеносных сосудов в ткани с протекающими процессами грануляции. До настоящего времени потенциальная роль αvβ3 при фиброзе печени и фиброзе других органов оставалась в значительной степени неисследованной (11-19).
Интегрин αvβ6, в основном, обнаруживается в активированных эпителиальных и фибробластных клетках. Он подвергается значительной повышающей регуляции во время повреждения тканей (20-22). Мыши, у которых отсутствует эта субъединица интегрина, демонстрируют удивительную устойчивость к индукции легочного фиброза (20). Активация и пролиферация эпителиальных клеток желчного протока регулярно обнаруживается при хроническом повреждении печени и фиброзе, а пролиферирующий эпителий желчного протока представляет собой основной источник профиброгенных факторов, таких как TGFβ1, TGFβ2 и CTGF, а также некоторых белков ЕСМ, при фиброзе печени, в частности фиброзе желчного протока (23, 24).
HSC/MF и миофибробласты считаются основными типами клеток, которые отвечают за избыток депонирования ЕСМ во время активного печеночного фиброгенеза. Как было показано, они синтезируют и высвобождают несколько типов коллагенов, в частности коллагены типа I и типа III, образующие фибрилл, которые свойственны для рубцевых тканей, ламинин-2, фибронектин и TIMP-1, основной ингибитор коллагеназ, и другие (12-19, 25-27). Миграция этих клеток является критической для их аккумуляции в сайтах печеночного повреждения. После активации культивируемые HSC/MF мигрируют в ответ на некоторые стимулы, включая ростовые факторы, такие как PDGF-AB, PDGF-ВВ, вазоактивные вещества, такие как эндотелин-1, и хемокины, такие как хемотаксический белок моноцитов (МСР-1) (28-30).
HSC/MF экспрессируют ряд интегринов, лигандами которых, в первую очередь, являются молекулы ЕСМ, которые трансдуцируют экстрацеллюлярные сигналы от ЕСМ в клетки в соответствии с цитокинами/ростовыми факторами (перекрестная передача сигнала) (1-3). Некоторые активности HSC/MF могут регулироваться с помощью интегринов, включая клеточную пролиферацию, сжатие, миграцию и синтез ЕСМ (1-3). Более того, интегрины также могут активировать латентный TGFβ, усиливая, таким образом, фиброгенную активность этого ключевого цитокина (10, 22). Таким образом, фармакологическое модулирование взаимодействия между HSC/MF и окружающим ЕСМ путем влияния путем интегриновой передачи сигналов является потенциальной стратегией для ограничения фиброза печени и фиброза других органов.
Несмотря на то, что миграция HSC/MF in vivo является сложной для измерения, вещества, которые ингибируют HSC/MF in vitro, являются главными кандидатами для снижения их аккумуляции в поврежденной печени. Кроме того, ингибирование активации, миграции и пролиферации эндотелиальных и эпителиальных клеток желчного протока может дополнительно подавлять фиброгенез в хронически поврежденной печени.
Приведенное ниже иллюстрирует клиническое воздействие на хронические фиброзные заболевания, как представлено на примере печеночного фиброза. Сценарий является подобным для всех фиброзных заболеваний, таких как те, что поражают легкие, почки, кишечник, поджелудочную железу, кожу или артерии. Так, по оценкам, только в Германии с населением 100 миллионов приблизительно 500000 людей страдают от цирроза печени, от хронических заболеваний печени на последней стадии, а ежегодный показатель смертности по причине цирроза колеблется от 50000 до 100000 человек (12, 31). Цирроз может быть определен как нарушение структуры печени при избыточной аккумуляции экстрацеллюлярного матрикса (ЕСМ), что приводит к образованию аномальных узелков печеночных клеток, перисинусоидальному склерозу и шунтированию крови от метаболически активных гепатоцитов. Пациенты с циррозом печени легко могут войти в состояние декомпенсированного заболевания печени со всеми последствиями поврежденной синтетической функции печени (расстройства коагуляции, нарушенный синтез альбумина и питательных веществ), что приводит к общему истощению, эдеме, портальной гипертензии, что ведет к возникновению асцитов и пищеводного варикозного кровотечения, предрасположенности к тяжелым инфекциям и к развитию печеночной энцефалопатии. Цирроз сам по себе способствует значительному увеличению распространенности первичной карциномы печеночных клеток.
В то время как на Западе приблизительно половина случаев цирроза возникает по причине алкогольной зависимости, другая половина имеет разнообразные другие причины, такие как (в порядке снижения значимости) хронический вирусный гепатит С и В, аутоиммунные заболевания (первичный желчный цирроз, классический иммунный гепатит, первичный склерозирующий холангит), метаболические заболевания (гемохроматоз, болезнь Вилсона, дефицит по α1-антитрипсину, тиросенемия, гликогенная гепатомегалия), фиброз желчного пузыря, индуцированный лекарственными средствами фиброз (индуцированный, например, метотрексатом), врожденные аномалии (врожденный печеночный фиброз, билиарная атрезия, синдром Алагилла), послеоперационные осложнения (вторичный билиарный цирроз), или васкулярные заболевания (синдром Бада Киари). Эти заболевания и причины цирроза печени могут быть легко экстраполированы на другие западные страны. Это количество может быть даже более высоким, чем в западных странах, с более высоким значением вирусных гепатитов В и С. Каузальное лечение этих заболеваний печени является ограниченным (12, 31). Так, даже самые лучшие доступные фармакологические терапии могут устранять вирус гепатита В только у 40%, а вирус гепатита С только у 30-40-50% пациентов с хроническим вирусным гепатитом. Эти терапии всегда включают введение интерферона на протяжении 6-12 месяцев и, таким образом, являются дорогостоящими и обремененными значительными побочными эффектами. Увеличивающаяся проблема здоровья представляет собой эпидемии гепатита С (32), который становится хроническим у 80-90% инфицированных лиц и который имеет распространенность от 0,5 до 1% в Западной Европе, от 1 до 1,5% в США, приблизительно 2% в Восточной Европе и Азии и до 20% в некоторых странах, подобных Египту. Некоторые заболевания печени, такие как иммунные расстройства, могут лечиться симптоматически или, возможно, слабо замедляться в своем развитии до цирроза с помощью агентов, таких как кортикостероиды (при классическом аутоиммунном гепатите) и урсодезоксихолевая кислота (при первичном билиарном циррозе). В других случаях такое развитие может предотвращаться, когда заболевания обнаружены на ранней стадии. Примерами являются венесекция при гемохроматозе и использование хелатирующих агентов, таких как D-пеницилламин при болезни Вилсона, по причине нехватки доноров и высокой стоимости трансплантация печени является возможной только в некоторых, отдельных случаях печеночного заболевания на последней стадии.
Упомянутые неблагоприятные стимулы, такие как гепатотоксины, включая алкоголь, гепатотропные вирусы, иммунные реакции, ассоциированные с печенью, метаболические заболевания и застой желчи, могут осуществлять запуск фиброгенеза печени, то есть избыточный синтез и депонирование экстрацеллюлярного матрикса (ЕСМ). При острых заболеваниях печени, таких как самоограниченный вирусный гепатит, фиброгенез уравновешивается с помощью фибролиза, то есть удаления избытка ЕСМ. Однако повторяющиеся инсульты средней степени тяжести или дополнительные вредные влияния, например хронический гепатит С в сочетании с потреблением алкоголя, что возникает при многих хронических заболеваниях печени, сдвигают метаболизм ЕСМ к фиброгенезу, приводя, таким образом, к фиброзу или циррозу (12-19, 32). При фиброгенезе повреждения гепатоцитов или эпителия желчного протока ведет к активации мононуклеарных клеток, высвобождению фиброгенных факторов и активации клеток мезенхимы печени. Активированные клетки Купфера, то есть специфические для печени макрофаги, а также пролиферирующий эпителий желчного протока, как полагают, являются первичными источниками потенциально фиброгенных цитокинов и ростовых факторов, которые, в конечном счете, нацеливают HSC/MF, то есть те типы клеток, которые отвечают за избыток депонирования ЕСМ в печени (12-19, 32). Как было упомянуто выше, оба этих типа клеток находятся в связи со всеми другими мезенхимально-эпителиальными и васкулярными органами (14, 33-44). При активации с помощью фиброгенных ростовых факторов и нарушении их нормального трехмерного окружения матриксом покоящиеся HSC/MF подвергаются трансформации в клеточный фенотип, который характеризуется высоким пролиферативным потенциалом и способностью вырабатывать избыток молекул ЕСМ. Эта трансформация, которая обычно характеризуется приобретением миофибробластного маркера α актина гладкой мускулатуры, играет центральную роль в защитной программе, которая направлена на быстрое закрытие потенциально летальной раны.
В обычном случае эта программа является самоограниченной, если нарушающий нормальное функционирование агент присутствует только в течение короткого периода времени, но эта программа может приводить к фиброзу и циррозу, когда она подвергается непрерывной активации. Еще раз следует подчеркнуть, что клетки и факторы, которые приводят к фиброзу и циррозу печени, являются почти идентичными тем, что лежат в основе процессов, которые приводят к фиброзу и рубцеванию других органов.
Таким образом, при многих хронических заболеваниях печени (12-19, 32) и других органов, таких как сердце, почки, легкие, артерии, кожа, кишечник и поджелудочная железа (14, 33-44), которые приводят к фиброзу, непрерывное повреждение не может быть предотвращено или хотя бы снижено, в лучшем случае. Кроме того, пациенты обычно имеют уже развитую стадию структурного и функционального нарушения. Это требует развития способов лечения, которые могут или остановить развитие фиброза органа, или даже вызвать обратное развитие прогрессирующего рубцевания. Такие способы лечения должны предполагать пероральное введение, должны быть экономически приемлемыми и быть свободными от нежелательных побочных эффектов.
КОРОТКОЕ ОПИСАНИЕ СУТИ ИЗОБРЕТЕНИЯ
Задача настоящего изобретения заключается в обеспечении способа лечения патологических состояний, при которых активированные фибробласты, миофибробластные клетки и миофибробласты, а также активированные эндотелиальные и эпителиальные клетки вырабатывают и/или индуцируют выработку избытка экстрацеллюлярного матрикса, что приводит к нежелательному рубцеванию. Это относится к фиброзу и циррозу печени, а также фиброзу других органов, таких как легкие, почки, кишечник, поджелудочная железа, кожа и артерии, которые могут подвергаться почти идентичным патологическим процессам.
Другая задача настоящего изобретения заключается в обеспечении композиций вещества для лечения патологических состояний, с помощью которых ингибируются активированные фибробласты, миофибробластные клетки и миофибробласты, а также активированные эндотелиальные и эпителиальные клетки и, таким образом, рубцевание, по крайней мере, частично ингибируется. Было обнаружено, что указанные выше заболевания и патологические состояния могут успешно подвергаться лечению с помощью ингибиторов интегринов, предпочтительно ингибиторов интегринов αβ, более предпочтительно антагонистов αvβ3 и αvβ6, в соответствии с чем включаются как пептидные, так и непептидные молекулы. Предпочтительно, когда ингибиторы EMD 409915 и EMD 409849, известные из предшествующего уровня техники, или такие, которые легко могут быть получены в соответствии со стандартными способами, представляют собой эффективные лекарственные средства в указанном контексте.
EMD 409915 является 3-бензо[1,2,5]тиадиазол-5-ил-3-{6-[2-(6-метиламинопиридин-2-ил)этокси]-1H-индол-3-ил} пропионовой кислотой.
EMD 409849 является 3-{3-бензиокси-2-[5-(пиридин-2-иламино)пентаноиламино]пропаноиламино}-3-(3,5-дихлорфенил)пропионовой кислотой.
Эти антагонисты отдельно или в сочетании с другими агентами могут эффективно предотвращать, уменьшать или даже вызывать обратное развитие прогрессивного фиброза, такого как фиброз/цирроз печени и фиброз других органов, таких как легкие, почки, кишечник, поджелудочная железа, кожа и артерии.
КОРОТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг.1. Эффект EMD 409915 при концентрации 10-9-10-6 М на а) клетки CFSC-2G, линия HSC крыс и b) первичные крысиные HSC/MF, обработанные с помощью PDGF-BB (10 нг/мл). Миграцию клеток оценивали в течение 20 часов. Данные представляют один из ≥3 независимых экспериментов, осуществленных в трехкратной повторности и представленных как среднее значение ± SEM (% по отношению к исходному уменьшению ширины царапины).
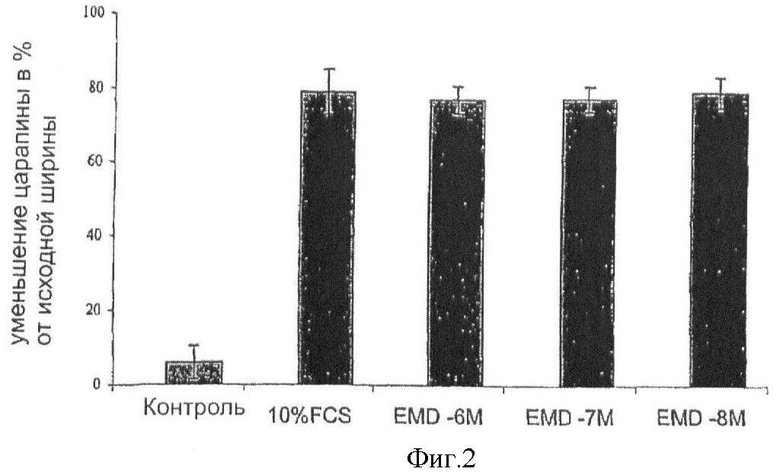
Фиг.2. Эффект EMD 409915 при концентрации 10-10-10-6 М на миграцию клеток HSC/MF, стимулированных фетальной сывороткой теленка (FCS). Данные представляют один из ≥3 независимых экспериментов, осуществленных в трехкратной повторности и представленных как среднее значение ± SEM (% по отношению к исходному уменьшению ширины царапины).
Фиг.3. Синтез ДНК, измеренный с помощью встраивания BrdU в HSC/MF, стимулированные с помощью PDGF-BB (10 нг/мл), в течение 24 часов в присутствии EMD 409915 при концентрации 10-6М - 10-8М. Данные представляют один из ≥3 независимых экспериментов, осуществленных в четырехкратной повторности и представленных как среднее значение ± SEM (произвольные единицы).
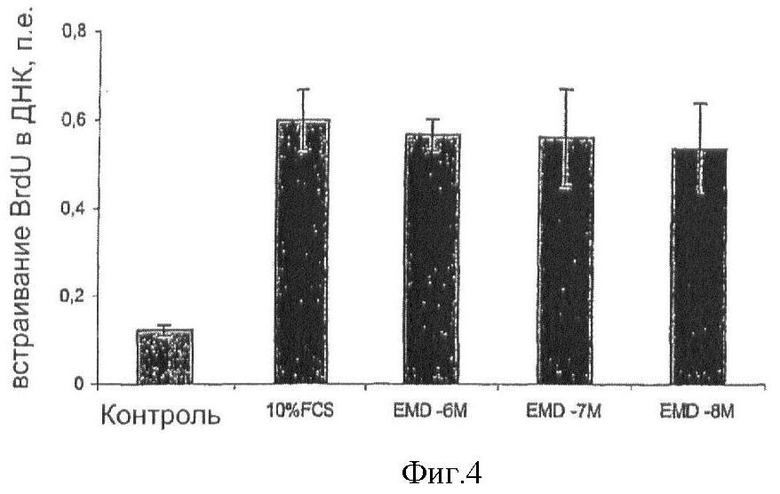
Фиг.4. Синтез ДНК, измеренный с помощью встраивания BrdU в HSC/MF, стимулированные с помощью FCS, в течение 24 часов в присутствии EMD 409915 при концентрации 10-6М - 10-8М. Данные представляют один из ≥3 независимых экспериментов, осуществленных в четырехкратной повторности и представленных как среднее значение ± SEM (произвольные единицы).
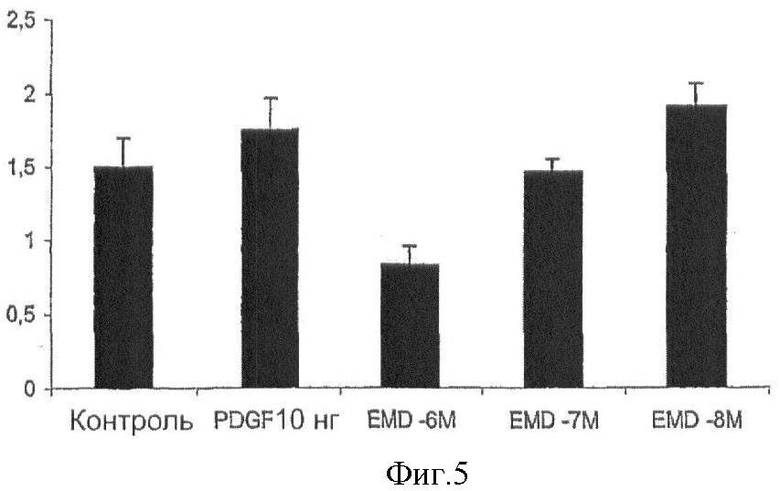
Фиг.5. Экспрессия CTGF в клетках CFSC-2G, обработанных EMD 409915 при концентрации 10-6М - 10-8М в присутствии PDGF-BB (10 нг/мл), в течение 24 часов. Данные представляют один из ≥3 независимых экспериментов, осуществленных в четырехкратной повторности и представленных как среднее значение ± SEM (произвольные единицы).
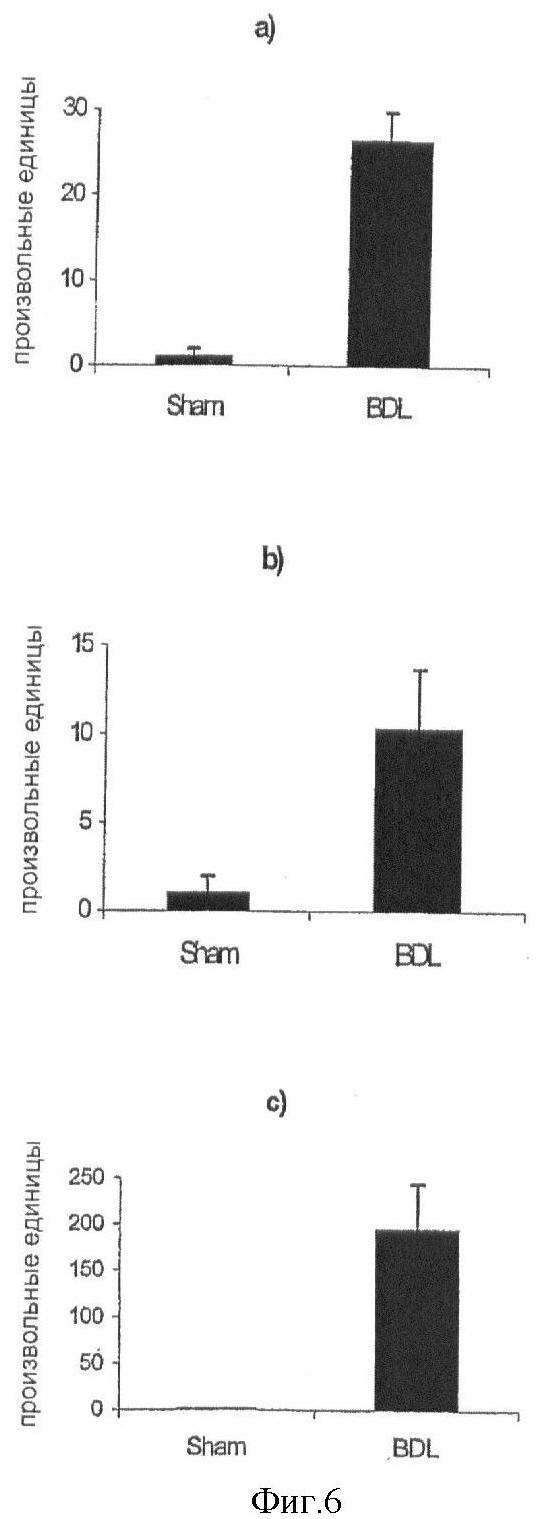
Фиг.6. Экспрессия а) проколлагена α1(I), b) TGFβ1 и с) CTGF при первичном билиарном фиброзе. Экспрессию измеряли при осуществлении ПЦР в реальном времени при использовании общей РНК, полученной из печени крыс: крыс, подвергшихся ложной операции (Sham), и крыс с фиброзом по причине окклюзии желчного протока в течение 6 недель (BDL). Каждый прямоугольник представляет образцы РНК из печени, полученные от трех индивидуальных животных, данные представлены как среднее значение ± SEM (произвольные единицы).
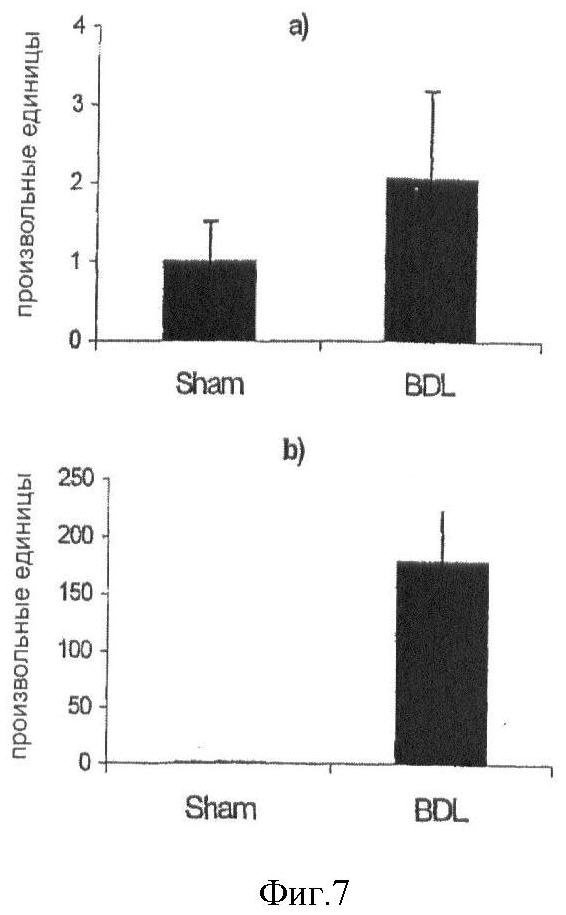
Фиг.7. Экспрессия а) бета 3 интегрина и b) бета 6 интегрина при фиброзе печени. Экспрессию измеряли при осуществлении ПЦР в реальном времени при использовании общей РНК, полученной из печени крыс: крыс, подвергшихся ложной операции (Sham), и крыс с фиброзом по причине окклюзии желчного протока в течение 6 недель (BDL). Каждый прямоугольник представляет образцы РНК из печени, полученные от трех индивидуальных животных, данные представлены как среднее значение ± SEM (произвольные единицы).
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВОПЛОЩЕНИЙ
Способы
Изоляция HSC и культура
Кратко, печень подвергали перфузии in situ через воротную вену при использовании канюли 16-18 G с HBSS, не содержащим кальция (Gybco, UK), в течение 5 минут, после чего использовали 0,1% проназу Е (Sigma), а потом 0,025% коллагеназу типа IV (Sigma) в модифицированной Дюльбекко среде Игла в течение 10-15 минут каждая среда. Вычленяли разложившуюся печень, осторожно измельчали и инкубировали в дальнейшем с 0,04% проназы, 0,025% коллагеназы, 0,002% ДНКазы (Sigma) в модифицированной Дюльбекко среде Игла, дополненной 25 мМ HEPES при температуре 37°С в течение 10-30 минут при осторожном перемешивании. После фильтрации через 100 мкм нейлоновую марлю паренхимные клетки удаляли при центрифугировании при низкой скорости. Фракцию HSC собирали на границе раздела градиента после обогащения путем двухэтапного центрифугирования в градиенте 11 и 13% Nycodenz (Sigma) при 1500 g в течение 15 минут без торможения и высаживали при плотности 0,5×106/см2 в DMEM с добавлением 10% FCS, пенициллина и стрептомицина. Среду меняли каждые 24 часа, а в дальнейшем каждые 48 часов. Жизнеспособность изолированных клеток оценивали с помощью вытеснения трепановым голубым, при этом она была большей, чем 95-98%. Чистоту изолятов HSC подтверждали с помощью их типичного морфологического внешнего вида: липидные капли в цитоплазме, демонстрация зеленоватой аутофлуоресценции при возбуждении 390 нм и форма, напоминающая звезду. Контаминацию клетками Купфера оценивали по способности поглощать латексные бусинки размером 3 мкм, она была ниже 3-5% после изоляции и почти не определялась после первого пассажа. Для экспериментов использовали клетке в промежутке между первым и третьим пассажем, если не указано другое.
В дополнение использовали HSC линии клеток CFSC-2G (умеренно активированные, которые были любезно предоставлены доктором М. Ройкиндом, Вашингтон DC, США).
Опыты на животных
Взрослых самцов крыс Wistar со средним весом 206±19 г подвергали следующей микрохирургической процедуре под оперативным микроскопом (OPMI6-S, Zeiss, Germany) (45-47): 1) после анестезии с помощью 100 мг/кг гидрохлорида кетамина (Ketanest®, Parke-Davis, Germany) и 10 мг/кг гидрохлорида 5,6-дигидро-2-(2,6-ксилидино)-4Н-1,3-тиазина (Rompun®, Bayer, Germany) делали надрез по средней линии живота; 2) проводили иссечение общего желчного протока, ставили тефлоновый катетер (Abbocath®-T 26 G, Venisystems, USA), размещали его дистально и проксимально не полностью накладывали лигатуру с помощью 5-0 шелка (Perma-hand®, Ethicon, Germany); 3) осуществляли ретроградную инъекцию натрий-амидотриазоата (Ethibloc®, Ethicon, Germany) при дозе 0,02 мл/100 г веса тела; 4) удаляли катетер, закрывали проксимальную лигатуру, разъединяли желчный проток между лигатурами и смыкали края раны. После окклюзии желчного протока (BDO) животные получали нормальный корм (Altromin®, Lage, Germany), а также свободный доступ к воде. Ранняя смертность (в пределах 1 часа-3 дней) у крыс происходила по причине подтекания желчи и составляла до 9%. Поскольку на этой модели фиброз становится явным только через две недели BDO, животные, которые умерли ранее, не учитывались для статистического анализа. Через 6 недель крыс умерщвляли при использовании анестезии кетанест/ромпан и с помощью пунктуры правого желудочка осуществляли обескровливание. Печень и селезенку взвешивали, и кусочки весом 1-2 г левой и правой печеночных долей фиксировали в 4% формалине или быстро замораживали в жидком азоте для осуществления гистологии, определяли мРНК и гидроксипролин (HYP).
Анализ царапины
Миграцию клеток оценивали путем измерения уменьшения площади царапины. Клетки высевали на планшет на 24 ячейки при плотности 60000 клеток/ячейка. После достижения конфлюэнтности клетки истощали на среде, не содержащей сыворотки, в течение 24 часов перед нанесением царапины через монослой клеток при использовании кончика стерильной пипетки. После повреждения клетки предварительно обрабатывали с помощью ингибитора интегрина αvβ3 в увеличивающихся концентрациях (10-10М - 10-6М) в течение 30 минут, а потом обрабатывали PDGF-BB в концентрации 10 нг/мл и при отсутствии сыворотки. Уменьшение площади царапины измеряли в трех различных точках на ячейку при использовании специального окуляра с микрометром, содержащим сетку, спустя 15-20 часов.
Встраивание BrdU
Для оценки клеточной пролиферации de novo синтез ДНК оценивали как встраивание BrdU. Клетки высевали при плотности 20000 клеток/ячейка в планшеты на 96 ячеек в ростовую среду, содержащую 10% фетальной сыворотки теленка (FCS). Через 24 часа среду заменяли до 0% FCS и осуществляли инкубацию в течение последующих 24 часов, после чего осуществляли инкубацию в среде, содержащей PDGF-BB в концентрации 10 нг/мл, ингибитор интегрина αvβ3 (10-9-10-5) или без ингибитора в течение 20 часов. В течение последних часов инкибируемые клетки импульсно метили с помощью BrdU, и его встраивание измеряли при использовании набора ELISA (Roche) и считывающего устройства для микротитровальных планшетов.
ПЦР в реальном времени
Общую РНК изолировали из клеточных лизатов при использовании коммерческого набора RNApure (PeqLab, Erlangen, Germany) в соответствии с рекомендациями производителя. Матричную кДНК получали с помощью обратной транскрипции 0,5 мг общей РНК.
Относительные транскрипционные уровни количественно оценивали с помощью RT-ПЦР, применяя систему LightCycler (Roche), при использовании 1,5 мкл разведения матричной кДНК в общем реакционном объеме 15 мкл, который включал Taq ДНК-полимеразу, дНТФ-смесь, реакционный буфер и 3,0 мМ MgCl2, которые обеспечивались с помощью набора «LightCycler FastStart DNA Master Hybridization Probes» (Roche Molecular Biochemicals, Mannheim, Germany) в соответствии с инструкциями производителя. Для каждого измеренного транскрипта использовали как стандарт серии разведении одного образца от 1:2 до 1:32. Данные анализировали с помощью программы LightCycler при использовании опции «пропорциональный максимум второй производной». Амплифицировали вспомогательные гены бета-2 микроглобулина или GAPDH в параллельной реакции для нормализации результатов.
TaqMan зонды и наборы праймеров определяли при использовании программного обеспечения Primer Express (Perkin Elmer) на основе опубликованных последовательностей. Смысловые и антисмысловые праймеры (каждый в концентрации 0,5 мкМ) и 0,125 мкМ 5'-фосфорилированного зонда, меченного на своем 5'-конце с помощью опознавательного красителя (FAM), a на 3'-конце - молекулой гасителя (TAMRA), синтезировали на MWG Biotech AG (Ebersberg, Germany). Наборы праймеров, которые использовали для измерения экспрессии специфических целевых генов, представлены в таблице.

Для количественного определения транскрипционных уровней интегринов β3 и β6 в стационарной фазе роста использовали ПЦР с SYBR зеленым в качестве флуорофора (Molecular Probes, Eugene, OR). Для разграничения специфического продукта ПЦР от неспецифических продуктов и димеров праймеров осуществляли анализ кривых плавления. Так как различные продукты ДНК плавятся при различных температурах, является возможным разграничить подлинные продукты димеров праймеров и неспецифические продукты.
Все эксперименты осуществляли в клеточной культуре с миофибробластоподобной клеточной линией CFSC-2G (клеточная линия HSC, полученная из цирротической печени) и первичными HSC/MF. Для оценки влияния ингибитора интегрина αvβ3 на миграцию клетки высевали на планшеты на 24 ячейки и после достижения конфлюэнтности подвергали истощению при отсутствии FCS в течение 24 часов. Наносили царапины на клетки, обработанные с помощью PDFG-BB в концентрации 10 нг/мл в присутствии или в отсутствие ингибитора αvβ3 при концентрации 10-6-10-9М. Значение миграции измеряли спустя 17-20 часов как уменьшение исходной ширины царапины.
Ингибитор αvβ3 сильно ингибирует клеточную миграцию, индуцированную PDGF-BB, в участок зоны царапины зависимым от дозы образом. Полное устранение миграции наблюдали при концентрации 10-6 М во всех использованных типах клеток (Фиг.1). При этом неожиданно было обнаружено, что отсутствует влияние ингибитора интегрина αvβ3 на миграцию клеток, стимулированных FCS (Фиг.2), что могло быть по причине стимуляции других, вероятно, более нормальных путей метаболизма, вовлеченных в миграцию, которые запускаются FCS. EMD 409915 не выявил какого-либо значительного ингибирования миграции даже при пониженных концентрациях FCS (0,25%) (данные не представлены). Эти наблюдения дают возможность предположить, что миграция HSC/MF, индуцированная PDGF, является специфически зависимой от αvβ3 и находится под его сильным влиянием. Таким образом, является заманчивым блокировать HSCMF миграцию в фиброзной печени и других фиброзных органах весьма специфическим образом, не препятствуя в значительной степени процессу «нормальной» миграции путем использования ингибирования β3 интегрина.
Для проверки, демонстрирует ли ингибитор αvβ3 подобное влияние на клеточную пролиферацию, клетки истощали на среде без сыворотки в течение 24 часов, а потом обрабатывали с помощью PDGF-BB в концентрации 10 нг/мл и при содержании ингибитора αvβ3 в концентрации 10-8М - 10-6М на протяжении 24 часов. При этих условиях ингибитор αvβ3 не оказывает никакого влияния на клеточную пролиферацию, стимулированную PDGF-BB, во всех типах клеток (Фиг.3). Такое же отсутствие эффекта наблюдали для клеточной пролиферации, стимулированной сывороткой (Фиг.4).
Для исследования, оказывает ли ингибитор интегрина αvβ3 какой-либо эффект на экспрессию мРНК в HSC/MF, измеряли экспрессию спектра основных про- и анти-фиброгенных молекул, подобных проколлагену α1(I) I, TGFβ1, TGFβ2, ММР-3, ММР-13, ММР-2, ростового фактора соединительной ткани (CTGF) и ТЕМР-1 с помощью ПЦР в реальном времени. Клетки, выращенные до стадии конфлюэнтности, истощали в течение 24 часов в среде, не содержащей сыворотки, потом предварительно обрабатывали с помощью ингибитора αvβ3 в течение 30 минут и стимулировали при использовании PDFG-BB (10 нг/мл) на протяжении последующих 24 часов. Как показано на Фиг.5, ингибитор αvβ3 понижает регуляцию CTGF в клетках CFSC-2G зависимым от дозы образом, при этом максимальное ингибирование наблюдается при концентрации 10-6. Не наблюдали никаких изменений транскрипционных уровней других ЕСМ молекул (данные не показаны). Для исследования моделей экспрессии интегринов во время фиброза печени использовали крысиную модель полной непроходимости желчного протока в течение 6 недель, что приводило к циррозу с 4- или 10-12-кратной аккумуляцией относительного (на г печени) и абсолютного (на общий вес печени) печеночного коллагена, соответственно. Через 6 недель после окклюзии желчного протока наблюдали значительную понижающую регуляцию экспрессии мРНК проколлагена α1(I) I, TGFβ1, TGFβ2 и CTGF (25-, 10-, 200- и 190-кратную, соответственно) по сравнению с ложно прооперированными животными (Фиг.6). В то же время мРНК αvβ3 подвергалась умеренной понижающей регуляции (Фиг.7а), в то время как очень высокую (180-кратную) сверхэкспрессию субъединицы интегрина р6 наблюдали в образцах цирротической печени (Фиг.7b). Сильную понижающую регуляцию интегрина αvβ3 никогда не наблюдали при фиброзных заболеваниях и при печеночном фиброзе, в частности. Клетки, ответственные за эту понижающую регуляцию, в основном, представляют собой пролиферирующие эпителиальные клетки желчного протока (а также активированные HSC/миофибробласты), такие клетки, которые секретируют большие количества профиброгенных цитокинов, таких как TGFβ и CTGF, и которые, таким образом, представляют собой первичные мишени для терапии печеночного фиброза, в отличие от активированных HSC/MF. Кроме того, наши недавние пилотные исследования на модели неослабевающего прогрессивного фиброза печени крыс вследствие окклюзии желчного протока (5-6 животных на группу) дают возможность предположить, что специфическое ингибирование β6 интегрина с помощью EMD 409849 может значительно улучшить вторичный билиарный печеночный фиброз путем снижения общего коллагена печени на 50-70% после 5-6-недельной окклюзии желчного протока. Взятые вместе эти данные показывают, что ингибирование интегринов αvβ3 и αvβ6 с помощью специфических низкомолекулярных пептидов и, в частности, их непептидных аналогов, является мощным орудием для улучшения, блокирования или даже обеспечения обратного развития фиброза печени и других органов, лечение которых остается в большой степени труднодостижимым (11-19, 33-44).
Соединения для применения в соответствии с настоящим изобретением, и/или их физиологически приемлемые соли, и/или их физиологически приемлемые производные могут, таким образом, использоваться для получения фармацевтических композиций или препаратов путем введения их в приемлемой дозе вместе, по крайней мере, с одним наполнителем или вспомогательным веществом и, если это является желательным, с одним или более дополнительными активными соединениями. Композиции или препараты, полученные таким образом, могут использоваться в качестве лекарственных средств в медицине и ветеринарии. Приемлемые наполнители представляют собой органические или неорганические вещества, которые являются приемлемыми для энтерального (например, перорального или ректального) или парентерального введения и не вступают в реакцию с соединениями, которые используются в соответствии с настоящим изобретением. Они представляют собой, например, воду, растительные масла, бензиловые спирты, полиэтиленгликоли, глицеринтриацетат или другие глицериды жирных кислот, желатин, соевый лецитин, углеводы, такие как лактоза или крахмал, стеарат магния, тальк или целлюлоза. Для перорального введения, в частности, используют таблетки, покрытые оболочкой таблетки, капсулы, сиропы, соки или капли. Особый интерес представляют покрытые оболочкой таблетки и капсулы, имеющие энтерические покрытия или капсульные оболочки. Для ректального введения используют суппозитории, а для парентерального введения - растворы, предпочтительно масляные или водные растворы, а также суспензии, эмульсии или имплантаты.
Соединения для применения в соответствии с данным изобретением могут также быть лиофилизированы, и полученные таким образом лиофилизаты используют для производства препаратов для инъекций. Такие указанные композиции или препараты могут быть стерилизованными и/или могут содержать вспомогательные вещества, такие как консерванты, стабилизаторы и/или смачивающие агенты, эмульгаторы, соли для регулирования осмотического давления, буферные вещества, красители или вкусовые агенты. Если это является желательным, то они могут также содержать одно или более дополнительных активных соединений, например один или более витаминов, диуретиков, противовоспалительных соединений, антидиабетических агентов, анальгетиков, противовоспалительных агентов или соединений, отличных от соединений, которые используются в соответствии с настоящим изобретением, таких как соединения, которые не составляют предмет настоящего изобретения, и могут использоваться в диагностике, профилактике и/или лечении расстройств, клинических картин и/или симптомов, как описано в данной заявке, например, для улучшения и усиления терапевтического эффекта и/или переносимости дополнительных соединений.
Фармацевтические композиции в соответствии с изобретением могут быть получены или произведены в соответствии со способами, известными в области техники, или аналогичными с ними. Обычно фармацевтические композиции в соответствии с изобретением получают с помощью нехимических способов, например, путем перемешивания активных ингредиентов, например, с физиологически приемлемыми наполнителями, вспомогательными веществами, дополнительными веществами и носителями, и превращения смеси в желаемую дозированную форму, например в таблетки, с помощью методов прессования, или превращения в растворы с помощью растворения активных ингредиентов в растворителе. В общем случае активные ингредиенты превращают в фармацевтическую композицию вместе с одним или более наполнителями, например твердым, жидким и/или полужидким наполнителем, или одним или более вспомогательным веществом, в сочетании с одним или более дополнительными активными ингредиентами.
Эти препараты могут использоваться в качестве лекарственного средства в медицине и ветеринарии. Приемлемые наполнители представляют собой органические или неорганические вещества, которые являются приемлемыми для энтерального (например, перорального), парентерального или местного введении и не реагируют с новыми соединениями. Они представляют собой, например, воду, растительные масла, бензиловые спирты, алкиленгликоли, полиэтиленгликоли, глицеринтриацетат или другие глицериды жирных кислот, желатин, соевый лецитин, углеводы, такие как лактоза или крахмал, стеарат магния, тальк или вазелин. Приемлемыми для перорального введения, в частности, являются таблетки, пилюли, покрытые оболочкой таблетки, капсулы, порошки, гранулы, сиропы, соки или капли, приемлемыми для ректального введения являются суппозитории, приемлемыми для парентерального введения являются растворы, предпочтительно масляные или водные растворы, а также суспензии, эмульсии или имплантаты, а предпочтительными для местного применения являются мази, кремы или порошки. Новые соединения могут также быть лиофилизированы, а полученные лиофилизаты использованы, например, для получения инъекционных препаратов. Указанные препараты могут быть стерилизованными и/или могут содержать вспомогательные вещества, такие как лубриканты, консерванты, стабилизаторы и/или смачивающие агенты, эмульгаторы, соли для регулирования осмотического давления, буферные вещества, красители, вкусовые агенты и/или множество дополнительных активных ингредиентов, например один или более витаминов.
Для введения в виде ингаляционного аэрозоля является возможным использовать аэрозоли, в которых активные ингредиенты либо растворены, либо суспендированы в газе-вытеснителе или смеси газов-вытеснителей (например, СО2 или хлорфторуглероды). Активный ингредиент предпочтительно использовать в данной заявке в тонкоизмельченной форме, в случае которой могут присутствовать один или более дополнительных физиологически приемлемых растворителей, например этанол. Ингаляционные растворы могут вводиться с помощью традиционных ингаляторов.
В соответствии с этим антагонисты предпочтительно вводятся в дозах от приблизительно 0,001 мг до 200 мг, более предпочтительно от приблизительно 0,01 мг до 100 мг, даже более предпочтительно от приблизительно 0,01 мг до 50 мг и, в частности, от 0,01 до 30 мг, на одну единичную дозу.
Суточная доза предпочтительно является большей или равной приблизительно 0,0001 мг/кг, более предпочтительно большей или равной приблизительно 0,001 мг/кг, даже более предпочтительно большей или равной приблизительно 0,005 мг/кг, большей или равной приблизительно 0,01 мг/кг или большей или равной приблизительно 0,1 мг/кг. Суточная доза предпочтительно является меньшей или равной приблизительно 30 мг/кг, более предпочтительно меньшей или равной приблизительно 20 мг/кг, даже более предпочтительно меньшей или равной приблизительно 15 мг/кг, меньшей или равной приблизительно 5 мг/кг или меньшей или равной приблизительно 1 мг/кг веса тела.






Предложено применение антагониста интегрина αvβ для получения лекарственного средства для лечения вторичного билиарного фиброза печени, где указанный антагонист является 3-{3-бензилокси-2-[5-(пиридин-2-иламино)пентаноиламино]пропаноиламино}-3-(3,5-дихлорфенил)-пропионовой кислотой. Показано, что данное соединение ингибирует интегрины αv, в частности αvβ3 и αvβ6 интегрины, осуществляет понижающую регуляцию фиброгенеза путем ингибирования клеточной миграции и продукции молекул профиброгена (например, коллагеназ, ТМР-1) и цитокинов (например, CTGF) с помощью активированных печеночных звездчатых клеток/миофибробластов, активированных эпителия и эндотелия. Этот антагонист может эффективно предотвращать, уменьшать или даже вызывать обратное развитие вторичного билиарного фиброза печени путем снижения общего коллагена печени на 50-70% после 5-6-недельной окклюзии желчного протока. 7 ил., 1 табл.
Применение антагониста αvβ интегрина для получения лекарственного средства для лечения вторичного билиарного фиброза печени, где указанный антагонист является 3-{3-бензилокси-2-[5-(пиридин-2-иламино)пентаноиламино]пропаноиламино}-3-(3,5-дихлорфенил)пропановой кислотой.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| DE 10063173 A1, 20.06.2002 | |||
| DE 19933173 A1, 18.01.2001 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| АМИДЫ СУЛЬФАМИДО- И СУЛЬФАМИДОКАРБОНИЛПИРИДИН-2-КАРБОНОВЫХ КИСЛОТ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2129545C1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| DE 10006139 A1, 16.08.2001 | |||
| STN on the web, база данных CAS AN 139: 191476, AN138:180760 RN 497955-40-5 [online] [найдено 11.09.2008] | |||
| STN on the web, база данных CAS AN 142: 441882 RN 851333-14-7 [on line] [найдено 11.09.2008]. | |||
Авторы
Даты
2010-05-10—Публикация
2004-09-16—Подача