Предлагаемое изобретение относится к области фармацевтической промышленности, более конкретно к средству для лечения и профилактики неалкогольной жировой болезни печени.
Жировой гепатоз или неалкогольная жировая болезнь печени - НАЖБП (стеатоз печени, жировая инфильтрация, жировое перерождение печени) - это состояние, при котором более 5% массы печени составляет жир, преимущественно триглицериды. Если содержание жира превышает 10% веса органа, то более 50% печеночных клеток содержат жир, и жировые скопления распределены по всей ткани печени.
Причиной жирового гепатоза является метаболический синдром - нарушение обмена веществ и гормональные изменения. При этом развивается сахарный диабет и повышение уровня липидов в крови с угрозой формирования сердечно-сосудистых осложнений.
Жировое перерождение клеток печени может быть вызвано:
- злоупотреблением алкоголем,
- ожирением,
- некоторыми вирусными инфекциями (вирусы гепатитов В и С),
- нарушением питания,
- нарушением обмена веществ при сахарном диабете,
- увеличением печеночных ферментов (АЛТ, ACT, ГГТ),
- наследственными дефектами цикла мочевины и окисления жирных кислот,
- генетическими факторами,
- некоторыми лекарственными средствами, например, нестероидными противовоспалительными препаратами.
В основе НАЖБП лежит инсулинорезистентность (невосприимчивость клеток к инсулину) и нарушение обмена веществ, главным образом липидного и углеводного. Жировая дистрофия печени возникает из-за повышенного поступления в печень жирных кислот либо с пищей, либо при усилении липолиза (расщепления жира в жировой ткани).
НАЖБП - это многофакторное заболевание при воздействии совокупности факторов риска:
- абдоминальное ожирение (объем талии у мужчин - более 94 см и у женщин - более 80 см);
- злоупотребляющие алкоголем и вредной пищей;
- страдающие атеросклерозом, в результате высокого уровня липидов в крови, повышение уровня триглицеридов в крови более 1,7 ммоль/л, повышение уровня холестерина и снижение уровня липопротеидов высокой плотности;
- повышение артериального давления более 130/85 мм.рт.ст.;
- нарушение толерантности к глюкозе, длительная гипергликемия (сахарный диабет 2 типа);
- инсулинорезистентность;
- работа с токсическими веществами;
- прием множества лекарственных препаратов;
- после операций желудочно-кишечного тракта;
- страдающие некоторыми хроническими заболеваниями наследственного характера.
НАЖБП включает в себя следующие этапы развития:
1) стеатоз печени - в гепатоците накапливается жировое включение;
2) неалкогольный стеатогепатит - количество жировых включений, приобретает большие размеры;
3) фиброз - избыточное количество жировых включений разрывает клетку печени, и образуется жировая киста, которая способствует замене ткани печени на фиброзную ткань;
4) цирроз печени, как исход НАЖБП, с повышенным риском развития гепатоцеллюлярной карциномы.
Проявляется в следующих стадиях:
- ожирение гепатоцита - клетки печени не разрушаются, функционирование органа практически не нарушается;
- некробиоз гепатоцитов - из-за накапливания жиров клетки отмирают, образуются кисты, происходит мезенхимально-клеточная реакция;
- предцирротическая стадия - соединительная ткань органа заменяется на мезенхимальную;
- цирротическая стадия
Неалкогольная жировая болезнь печени (НАЖБП) является одним из наиболее широко распространенных заболеваний печени в мире. Так, по данным эпидемиологических исследований НАЖБП страдает 10-40% населения земного шара [Буеверов А.О. Хронические заболевания печени: краткое руководство для практикующих врачей. 2 изд. - М.: Медицинское информационное агентство, 2014. - 137 с.; Жировое перерождение печени и ишемическая болезнь сердца. Гериатрические аспекты: монография / ред. Хорошинина Л.П. - М.: ООО «Концепт дизайн», 2014 - 346 с.; Мехтиев С.Н и др. Неалкогольная жировая болезнь печени в вопросах и ответах (этиология, современная концепция патогенеза, особенности клиники, принципы диагностики и лечения) / Учебное пособие. - СПб., 2011 - 53 с.; Трухан Д.И. Неалкогольная жировая болезнь печени в практике врача «первого контакта» / Клинические перспективы гастроэнтерологии, гепатологии, 2012, №1, с. 3-9]. НАЖБП порой является первым органным поражением при метаболическом синдроме и серьезным предиктором развития и прогрессирования сахарного диабета, кардиоваскулярной патологии [Жировое перерождение печени и ишемическая болезнь сердца. Гериатрические аспекты: монография / ред. Хорошинина Л.П. - М.: ООО «Концепт дизайн», 2014 - 346 с.; Азизов В.А. и др. Неалкогольная жировая болезнь печени и кардиоваскулярные осложнения: в чем взаимосвязь? / Евразийский кардиологический журнал, 2013, №1, с. 63-69; Шифф Ю.Р. и др. Алкогольные, лекарственные, генетические и метаболические заболевания / пер. с англ. под ред. Мухина Н.А. и др. - М: ГЭОТАР-Медиа, 2011. - 480 с.]. Жировая болезнь развивается, как правило, в возрасте 40-60 лет, при этом женщины болеют чаще. Заболевание также затрагивает и детей. При избыточном весе с индексом 30 (масса в килограммах, деленная на рост в м2) вероятность жирового гепатоза составляет 40%.
НАЖБП объединяет спектр поражений печени, включающий стеатоз печени, неалкогольный стеатогепатит (НАСГ), стеатофиброз и стеатоцирроз [Жировое перерождение печени и ишемическая болезнь сердца. Гериатрические аспекты: монография / ред. Хорошинина Л.П. - М.: ООО «Концепт дизайн», 2014 - 346 с.; Трухан Д.И. Неалкогольная жировая болезнь печени в практике врача «первого контакта» / Клинические перспективы гастроэнтерологии, гепатологии, 2012, №1, с. 3-9; Шифф Ю.Р. и др. Алкогольные, лекарственные, генетические и метаболические заболевания / пер. с англ. под ред. Мухина Н.А. и др. - М.: ГЭОТАР-Медиа, 2011. - 480 с.; Корнеева Е.В. и др. Патофизиология метаболического синдрома / Монография. - М.: Изд. Дом «Высшее образование и Наука», 2012. - 136 с.]. Известно, что НАСГ коморбидное состояние метаболического синдрома и по сути это печеночная манифестация данной патологии [Жировое перерождение печени и ишемическая болезнь сердца. Гериатрические аспекты: монография / ред. Хорошинина Л.П. - М.: ООО «Концепт дизайн», 2014 - 346 с.; Корнеева Е.В. и др. Патофизиология метаболического синдрома / Монография. - М.: Изд. Дом «Высшее образование и Наука», 2012. - 136 с.; Стельмах В.В. и др. Энерготропная патогенетически ориентированная терапия сукцинатсодержащими препаратами при неалкогольной жировой болезни печени: Методические рекомендации. - СПб.: Тактик-Студио, 2014. - 40 с.]. Развитие НАСГ при метаболическом синдроме составляет 37,5% случаев [Арапкина О.М. Неалкогольная жировая болезнь печени метаболический синдром / Медицинский альманах, 2010, №1, с. 162-163]. При ожирении НАСГ имеет место в 20-47% случаев, при сахарном диабете 2 типа - 15% случаев, при дислипидемии - в 20-80% случаев. Как известно, в случае игнорирования и отсутствия лечения НАСГ в 5-25% случаев прогрессирует до исхода в цирроз печени с развитием портальной гипертензии, печеночно-клеточной недостаточности и гепатоцеллюлярной карциномы [Жировое перерождение печени и ишемическая болезнь сердца. Гериатрические аспекты: монография / ред. Хорошинина Л.П. - М.: ООО «Концепт дизайн», 2014 - 346 с.; Шифф Ю.Р. и др. Алкогольные, лекарственные, генетические и метаболические заболевания / пер. с англ. под ред. Мухина Н.А. и др. - М.: ГЭОТАР-Медиа, 2011. - 480 с.; Шапошников А.В. Гепатоонкопревенция. Концепция и принципы реализации / Пособие для врачей. - М.: Форте принт, 2013. - 80 с.].
НАСГ активно участвует в манифестации и усугублении атерогенной дислипидемии [Жировое перерождение печени и ишемическая болезнь сердца. Гериатрические аспекты: монография / ред. Хорошинина Л.П. - М.: ООО «Концепт дизайн», 2014 - 346 с.; Шифф Ю.Р. и др. Алкогольные, лекарственные, генетические и метаболические заболевания / пер. с англ. под ред. Мухина Н.А. и др. - М.: ГЭОТАР-Медиа, 2011. - 480 с.; Драпкина О.М. и др. Атерогенная дислипидемия и печень / Медицинский алфавит, 2012, Т. 4, №24, с. 30-35], что повышает вероятность развития ишемической болезни сердца (ИБС) и соответствующих этой патологии осложнений - острый инфаркт миокарда (ОИМ) и острое нарушение мозгового кровообращения (ОНМК) [Жировое перерождение печени и ишемическая болезнь сердца. Гериатрические аспекты: монография / ред. Хорошинина Л.П. - М.: ООО «Концепт дизайн», 2014 - 346 с.; Азизов В.А. и др. Неалкогольная жировая болезнь печени и кардиоваскулярные осложнения: в чем взаимосвязь? / Евразийский кардиологический журнал, 2013, №1, с. 63-69]. НАСГ также имеет большое значение в прогрессии нарушений углеводного обмена [Жировое перерождение печени и ишемическая болезнь сердца. Гериатрические аспекты: монография / ред. Хорошинина Л.П. - М.: ООО «Концепт дизайн», 2014 - 346 с.; Шифф Ю.Р. и др. Алкогольные, лекарственные, генетические и метаболические заболевания / пер. с англ. под ред. Мухина Н.А. и др. - М.: ГЭОТАР-Медиа, 2011. - 480 с.]. Хроническая гипергликемия аналогично провоцирует высокий риск кардиоваскулярных патологий.
С биологической точки зрения НАСГ объясняется так называемой гипотезой «параллельных множественных ударов» (multiple parallel hits), согласно которой патогенез НАЖБП есть модель взаимодействия таких факторов как инсулинорезистентность, активация процессов перекисного окисления липидов, персистирующая продукция провоспалительных цитокинов, таких как ФНОα, ИЛ-6, ИЛ-8 и др. и продукция так называемых адипоцитокинов жировой тканью: лептин, резистин, адипонектин [Буеверов А.О. Хронические заболевания печени: краткое руководство для практикующих врачей. 2 изд. - М.: Медицинское информационное агентство, 2014. - 137 с.].
Ключевыми источниками развития неалкогольной жировой болезни печени (НАЖБП) являются инсулинорезистентность и оксидативный стресс. Поскольку в организме возникает ситуация резистентности к инсулину, а, следовательно, и невозможность использовать глюкозу как источник энергии, то это компенсируется активацией липолиза и извлечением из периферических тканей жирных кислот. Большое количество свободных жирных кислот (СЖК) поступает в печень, что приводит к жировой нагрузке печеночной паренхимы и формированию стеатоза.
НАЖБП, как правило, прогрессирует постепенно и опасна возможностью перерастания в цирроз. Предполагается, что жировая болезнь печени в ближайшие 20-30 лет станет наиболее частой причиной цирроза печени, требующей трансплантации [«Трансплантация печени» Национальные клинические рекомендации, 2013, 42 с.].
Гепатоциты представляют собой главные функциональные клетки печени, и каждый отдельный гепатоцит составляет 15-30 микрон в диаметре. В печени человека находится примерно 250 миллиардов гепатоцитов. Критическое повреждение гепатоцита заканчивается некрозом клетки. В случае некроза гепатоциты способны регенерировать за счет деления неповрежденных гепатоцитов. Тем не менее, чередование некроза и регенерации запускает процесс фиброза печени, что ведет к циррозу печени, портальной гипертензии, печеночной энцефалопатии, кровотечению и другим осложнениям.
Эти заболевания развиваются после стадии фиброза печени. Фиброз печени - это разрастание соединительной ткани, которое возникает из-за чрезмерного накопления белков внеклеточного матрикса, включая коллаген. Известно, что клетки печени состоят из гепатоцитов, синусоидальных эндотелиальных клеток, клеток Купфера и звездчатых клеток печени. Звездчатые клетки печени играют наиболее важную роль в фиброзе печени [Francis J.E. et al. Fibrogenesis I. New insights into hepatic stellate cell activation: the simple becomes complex / American Journal of Physiology-Gastrointestinal and Liver Physiology, 2000, V. 279, N. 1, pp. G7-G11]. Звездчатые клетки печени это 15% всех клеток печени, которые в норме осуществляют функцию запасания ретиноида, являющегося предшественником витамина А. В случае повреждения или гибели гепатоцитов клетки Купфера начинают канибализировать поврежденные гепатоциты и секретировать цитокины (TGF-бета, PDGF, FGF, HGF, PAF и ЕТ-1) для пролиферации звездчатых клеток печени. Звездчатые клетки печени дифференцируются в миофибробласты. Миофибробласты синтезируют коллаген, который накапливается в межклеточном матриксе, что и приводит к фиброзу печени. Следовательно, активация звездчатых клеток печени играет главенствующую роль в прогрессировании фиброза печени.
Активация звездчатых клеток печени идет в три стадии. Предвоспалительная стадия; воспалительная стадия; поствоспалительная стадия.
В предвоспалительной стадии повреждение гепатоцитов провоцирует синтез гормона, стимулирующего пролиферацию звездчатых клеток печени, или пролиферация звездчатых клеток печени усиливается посредством уменьшения активности аргиназы, ингибитора клеточной пролиферации. Образование ацетальдегида или пероксида липидов стимулирует экспрессию генов матрикса.
На воспалительной стадии под воздействием цитокинов [TGF-бета, PDGF, FGF, HGF, PAF и ЕТ-1), которые секретируются возбужденными клетками Купфера и тромбоцитами, звездчатые клетки печени пролиферируют и далее дифференцируются в миофибробласты, способные превращаться в фиброциты [Marie-Reine Losser et al. Mechanisms of Liver Damage / Seminars in Liver Disease, 1996, V. 16, N. 4, pp. 357-367; Anke M.B.C. Tiggelman et al. Transforming growth factor-β-induced collagen synthesis by human liver myofibroblasts is inhibited by α2-macroglobulin / Journal of Hepatology, 1997, V. 26, N. 6, pp. 1220-1228).
На поствоспалительном этапе цитокины и факторы роста секретируются уже дифференцированными миофибробластами для активации недифференцированных звездчатых клеток печени и для секреции внеклеточных матриксов. Миофибробласты, активированные и дифференцированные под воздействием звездчатых клеток печени, образуют коллаген, затем скапливающийся в межклеточном матриксе. Мономер коллагена очень нестабилен и легко распадается при температуре тела, и распавшиеся мономеры полимеризуются, вызывая фиброз печени [Brenner D.A. et al. Type I collagen gene regulation and the molecular pathogenesis of cirrhosis / American Journal of Physiology-Gastrointestinal and Liver Physiology, 1993, V. 264, N. 4, pp. G589-G595].
Цирроз печени, как исход фиброза печени, развивается по причине полимеризации накапливающегося коллагена. Образующийся коллаген переходит в нерастворимые волокна. Цирроз печени также провоцируется и/или поддерживается перманентным воспалением в печени, в случае, когда происходит деструкция гепатоцитов, регенерация замещением соединительной тканью, при потреблении алкоголя, гепатите, токсическом воздействии и т.д. Цирроз печени является серьезной патологией и приводит к смертельным осложнениям, таким как портальная гипертензия, пищеводное и желудочное кровотечение, гепатома, печеночная энцефалопатия, кома и т.д. [Gines P. et al. Management of cirrhosis and ascites / The New England Journal of Medicine, 2004, V. 350, N. 16, pp. 1646-1654].
В связи с вышесказанным профилактика и лечение неалкогольной жировой болезни печени, в том числе на всех стадиях ее развития, является актуальным и социально значимым фактором.
Задача предлагаемого изобретения состояла в поиске нового средства, которое было бы эффективным в отношении профилактики и терапии неалкогольной жировой болезни печени.
В качестве такого средства в настоящем изобретении предлагается использовать лактитол.
Лактитол (систематическое наименование: 4-O-альфа-D-галактопиранозил-D-глюцитол) - сахарный спирт, синтезируемый из молочного сахара (лактозы), относится к дисахаридам, имеет длительный опыт применения и обладает уникальными характеристиками.
В странах ЕС, США, Японии лактитол используется в качестве подсластителя в пищевой промышленности, при этом он обладает низкой энергетической ценностью - 2 ккал/г. Поэтому его считают идеальным подсластителем для продуктов функционального питания нового поколения. Главным преимуществом лактитола по сравнению с другими пребиотиками является также его устойчивость к воздействию высоких температур и низких значений рН. Эти свойства позволяют использовать его для пищевых продуктов, подвергающихся воздействию высокотемпературной обработки, в частности, в хлебопечении и кондитерской промышленности [Артюхова С.И. и др. Использование лактитола в биотехнологии функциональных продуктов питания / Современные наукоемкие технологии, 2013, №3, с. 87-88].
По фармакологическому указателю лактитол относится к группе «Слабительные средства», по АТХ - к группе «Осмотические слабительные» и имеет код A06AD12. Отличием лактитола от других осмотических слабительных средств (за исключением препаратов на основе лактулозы) является то, что осмотическими свойствами обладает не само действующее вещество, а продукты его метаболизма в толстой кишке. В кишечнике человека отсутствуют ферментные системы, способные расщеплять Лактитол, поэтому он не всасывается в тонкой кишке и попадает в практически неизмененном виде в толстую кишку. Уже в восходящей ободочной кишке лактитол активно ассимилируется сахаролитической микрофлорой. Образующиеся в процессе микробного метаболизма короткоцепочные карбоновые кислоты алифатического ряда (КЦЖК) с низкой молекулярной массой (молочная, уксусная, масляная, пропионовая) приводят: 1) к снижению внутрикишечного рН, что способствует активизации пропульсивной перистальтики; 2) к увеличению объема и разжижению кишечного содержимого за счет повышения осмотического давления и задержки жидкости, что облегчает его продвижение по кишечнику.
Лактитол помимо своего дозозависимого слабительного эффекта обладает пребиотическим эффектом (пребиотики - это компоненты пищи, которые не перевариваются и не усваиваются в верхних отделах желудочно-кишечного тракта, но ферментируются микрофлорой толстого кишечника человека и стимулируют ее рост и жизнедеятельность). Его пребиотический эффект связан с тем, что, попадая в толстую кишку без изменений, он используется пробиотической микрофлорой кишечника как источник энергии, не расщепляется бактериями группы кишечной палочки и подавляет рост протеолитических бактерий за счет ингибирования их адгезии на клеточных стенках эпителия. Лактитол усиливает синтез белка бактериями, тормозит образование токсинов. По типу метаболизма лактитол похож на пищевые волокна, он не гидролизуется и не всасывается в желудке и тонком кишечнике, а в толстом кишечнике ферментируется сахаролитической микрофлорой, преобразовываясь, как уже известно, в низшие жирные кислоты, углекислый газ, водород и биомассу. Продуктами метаболизма лактитола являются КЦЖК, в первую очередь уксусная кислота и масляная кислота в соотношении 2:1. Принципиальным отличием лактитола от других дисахаридов является разный профиль синтезируемых микрофлорой КЦЖК. Так, по сравнению с лактулозой при метаболизме лактитола в 10 раз больше образуется масляной кислоты. В дальнейшем органические кислоты усваиваются организмом и обеспечивают энергетическую ценность, равную 2 ккал/г. Суммарная энергетическая ценность лактитола равна 2,4-2,6 ккал/г (в отличие от углеводов - 4 ккал/г). Молекулы уксусной кислоты проходят через стенки кишечника и попадают в печень, откуда распространяются в качестве энергетического субстрата к мышечным тканям и внутренним органам (сердце, почки, головной мозг и др.). КЦЖК являются главным энергетическим донором и модулятором метаболизма колоноцитов.
Поскольку лактитол представляет собой источник питания для бактерий толстой кишки, расщепляющих сахара {Lactobacillus spp., Lactobacillus bifidus, Lactobacillus acidophilus, Bifidobacteria), то при его применении избирательно увеличивается биомасса сахаролитической микрофлоры и угнетается рост протеолитических бактерий Enterobacteria и Enterococci, численность которых обычно приумножается при запорах. При сравнительном изучении влияния лактитола и лактулозы на пробиотические и условно патогенные и патогенные бактерии было установлено, что действие лактитола носит более избирательный характер. В частности, он, в отличие от лактулозы, не ферментируется кишечной палочкой (Е. coli) и расщепляется значительно меньшим количеством штаммов стафилококка (St. aureus) и клостридий (Cl. perfringens). Рандомизированные клинические исследования по сравнительному анализу эффективности и безопасности лактитола и лактулозы в лечении запоров [Amit Maydeo. Lactitol or lactulose in the treatment of chronic constipation: Result of a systematic / Journal of the Indian Medical Association, 2010, V. 108, N. 11, pp. 789-792] показали, что при практически одинаковом послабляющем действии лактитол переносится пациентами лучше. Лактитол показал меньшее число побочных эффектов по сравнению с лактулозой (31,20±0,80% и 62,10±1,10% соответственно, р=0,0019). Кроме того, в педиатрии эффективные используемые дозы лактитола практически в 2 раза меньше эффективных доз лактулозы (250-400 мг/кг/день и 500-750 мг/кг/день соответственно).
В уровне техники [международная заявка на патент WO 0239832 А1, дата публ.: 23.05.2002] предложено применение лактитола, предпочтительно при его суточной дозе 5-15 г, в качестве пищевого продукта (или пищевой добавки) для улучшения микрофлоры кишечника, а также для профилактики кишечных инфекций, рака толстой кишки, диареи или повышения иммунитета.
Лактитол также имеет одобренное применение при печеночной энцефалопатии и гипераммониемии в качестве агента, способствующего уменьшению образования и всасывания аммиака в кишечнике.
Так, в документе [патент GB 2113998 А, дата публ.: 17.08.1983] предлагается использовать лактитол, предпочтительно при дозировке 20-200 г в сутки, для лечения порто-системной энцефалопатии, которая является расстройством центральной нервной системы, возникающим как осложнение расширенного цирроза печени. У пациентов, страдающих от этого заболевания, вырабатываемые в кишечники азотсодержащие токсические вещества, предпочтительно аммиак, не обезвреживаются печенью, попадая в циркуляцию крови и в мозг, повреждая нервные клетки. В данном документе указанный терапевтически эффект лактитола также связан с уменьшением образования и всасывания аммиака.
Однако из уровня техники неизвестно применение лактитола при неалкогольной жировой болезни печени (НАЖБП). До настоящего времени прямых исследований в отношении эффективности лактитола именно при жировом гепатозе не проводилось.
Технический результат настоящего изобретения заключается в расширении арсенала средств, используемых для профилактики и лечения неалкогольной жировой болезни печени.
Указанный технический результат достигается применением 4-О-альфа-D-галактопиранозил-D-глюцитола (лактитола) в терапевтически эффективном количестве для профилактики и лечения неалкогольной жировой болезни печени у млекопитающего, нуждающегося в этом.
В предпочтительном варианте млекопитающим является человек.
Терапевтически эффективным количеством (или терапевтической дозой) является то количество (или та доза) активного агента, в котором его используют с лечебными или профилактическими целями. Например, терапевтически эффективное количество лактитола может составлять 1-20 г в сутки.
Лактитол может быть введен млекопитающему, предпочтительно человеку, на всех стадиях развития неалкогольной жировой болезни печени.
Кроме того, в одном из вариантов настоящего изобретения лактитол в дозировке 1-20 г в сутки может быть также предназначен для профилактики и лечения цирроза печени, который является исходом неалкогольной жировой болезни печени.
В одном из вариантов применение лактитола может быть осуществлено в виде пероральной лекарственной формы.
Такой пероральной лекарственной формой может быть порошок, который (помимо активного агента - лактитола) не содержит дополнительных вспомогательных веществ и/или активных веществ. Порошок может быть помещен в саше. Либо пероральная лекарственная форма (помимо лактитола) может дополнительно содержать фармацевтически приемлемые вспомогательные вещества и быть выбрана из порошка, таблетки (включая таблетки с модифицированным высвобождением), капсулы, гранул, сиропа, напитка, геля, пластинки, мягкой желатиновой конфеты и тому подобное. В качестве фармацевтически приемлемых вспомогательных веществ могут быть использованы различные добавки, используемые при производстве готовых лекарственных пероральных форм, совместимые как с активным агентом, так и с другими вспомогательными вещества и не оказывающие неблагоприятное воздействие на пациента, которому проводят профилактику или терапию.
Для подтверждения возможности применения лактитола в качестве средства для лечения и профилактики неалкогольной жировой болезни печени, в том числе для профилактики и лечения цирроза печени, являющегося исходом НАЖБП, были проведены следующие испытания.
Пример 1.
Для проведения исследования были взяты мыши, имеющие дефект гена лептина - белка, который является гиперфаговым при ожирении. У таких мышей достаточно быстро формируется ожирение печени.
Мыши самцы с дефектом гена и с ожирением возрастом около 8 недель были случайным образом распределены на группы по 7 животных. Обычные белые лабораторные мыши в количестве 7 штук выступали в качестве группы сравнения. Всех животных содержали при постоянной температуре 23±0,5°С, влажности 50±5% и освещении, соответствующем световому дню (7:00-19:00 часов). Животные имели свободный доступ к воде и питанию. Все процедуры и опыты на мышах проводились в соответствии с международными правилами обращения с животными.
Мышей распределяли на группы исследования и ежедневно вводили им (для соответствующей группы) перорально дозы лактитола (7,5; 15,0 или 30,0 мг/кг), и аналогичные дозы L-орнитина-L-аспартата. Известно [Журавлева Л.В. и др. L-орнитин-L-аспартат в лечении неалкогольной жировой болезни печени у больных ожирением с признаками метаболического синдрома / Практикуючий лiкар, 2015, №4, с. 25-31], что L-орнитина-L-аспартат используется для лечения стеатоза и стеатогепатита (различного генеза).
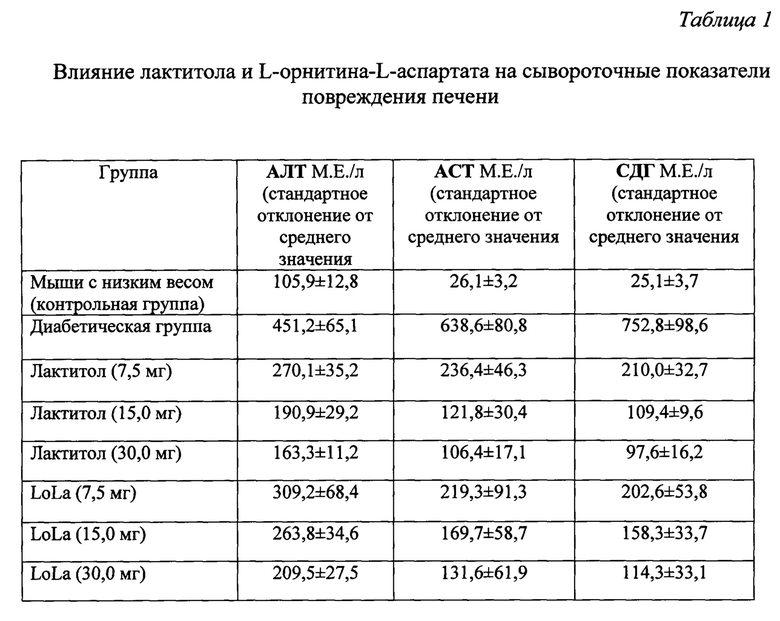
У мышей с дефектом гена лептина развивается хроническое воспалительное ожирение печени, и они представляют собой животную модель неалкогольного стеатогепатита (НАСГ). При НАСГ происходит увеличение жировых включений и повышается вероятность воспалительных повреждений. Важным критерием НАСГ являются, в отсутствие вирусной инфекции или алкоголизма, повышенные уровни в сыворотке крови показателей трансфераз, которые высвобождаются из поврежденных клеток печени: аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (ACT) и сорбитдегидрогеназы (СДГ). Содержание данных ферментов повышено у мышей с дефектом гена как следствие ожирения печени и сопутствующего вторичного воспаления.
В таблицу 1 сведены показатели АЛТ, ACT и СДГ в сыворотке крови, полученной у мышей, которым давали Лактитол, L-орнитина-L-аспартат (LoLa), а также уровни указанных ферментов в сыворотке крови, полученной у нормальных мышей с низким весом (контрольная группа) и у диабетических мышей, которым давали физиологический раствор (диабетическая группа). Уровни АЛТ, ACT и СДГ существенно повышены у страдающих ожирением диабетических мышей с дефектом гена по сравнению с нормальными мышами.
Полученные данные, которые сведены в таблицу 1, свидетельствуют о том, что при введении L-орнитина-L-аспартата в дозе от 7,5 до 30,0 мг/кг/день происходило снижение показателей АЛТ, ACT и СДГ. В то же время обработка лактитолом в дозе 7,5-30,0 мг/кг/день также приводила к дозозависимому снижению указанных ферментов печени в сыворотке крови.
Полученные профили ферментов печени в сыворотке крови коррелировали с гистологией печени. Так, у страдавших ожирением диабетических мышей с дефектом гена в диабетической группе, которым давали физиологический раствор, отмечалось внутриклеточное накопление жира в печени в виде жировых капелек. Ежедневное введение лактитола в терапевтических и субтерапевтических дозах в течение 4 недель вызывало заметное снижение накопления жира в печени, также как и в группе мышей, которым вводили L-орнитина-L-аспартат (LoLa).
Пример 2.
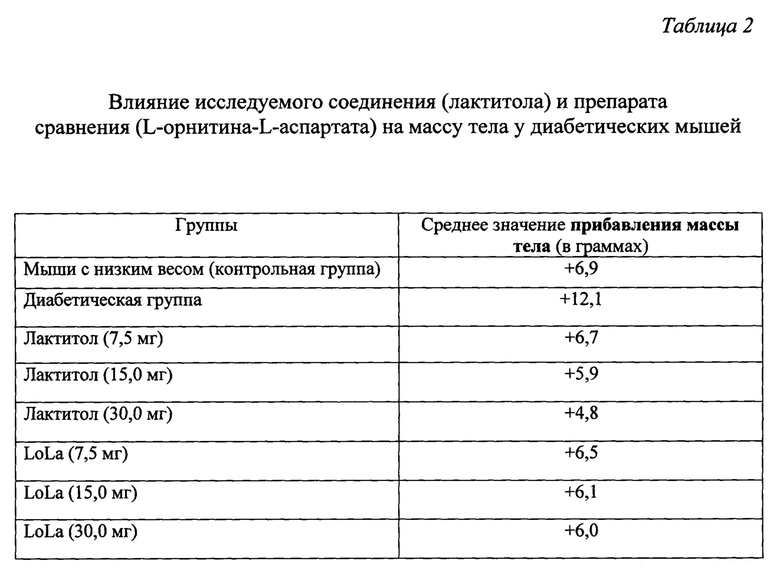
Кроме того, у мышей всех групп исследования примера 1 оценивали прибавление массы тела. Полученные данные показаны в таблице 2.
Мыши диабетической группы увеличились в весе во время всего четырехнедельного периода исследования. Кроме того, диабетические мыши без лечения (которым не вводили ни лактитол, ни LoLa) прибавляли в весе относительно мышей, которых лечили либо препаратом исследования (лактитолом), либо препаратом сравнения (LoLa). Полученные данные показывают, что введение лактитола диабетическим мышам индуцирует дозозависимое ослабление набора веса.
Пример 3.
Самцов мышей, подверженных ожирению, возрастом примерно 8 недель случайным образом распределяли на группы по 5-7 животных, так чтобы масса тела (50-55 г) и уровень глюкозы в сыворотке крови (>300 мг/декалитр в накормленном состоянии) были схожими между группами. Самцы тощих мышей выступали в качестве контрольной группы. Для адаптации после прибытия мышей оставляли в покое минимум на 7 дней. Все животные содержались при контролируемой температуре (23±0,5°С), относительной влажности (50±5%) и световом периоде суток (7:00-19:00 часов). Животные имели свободный доступ к корму и воде.
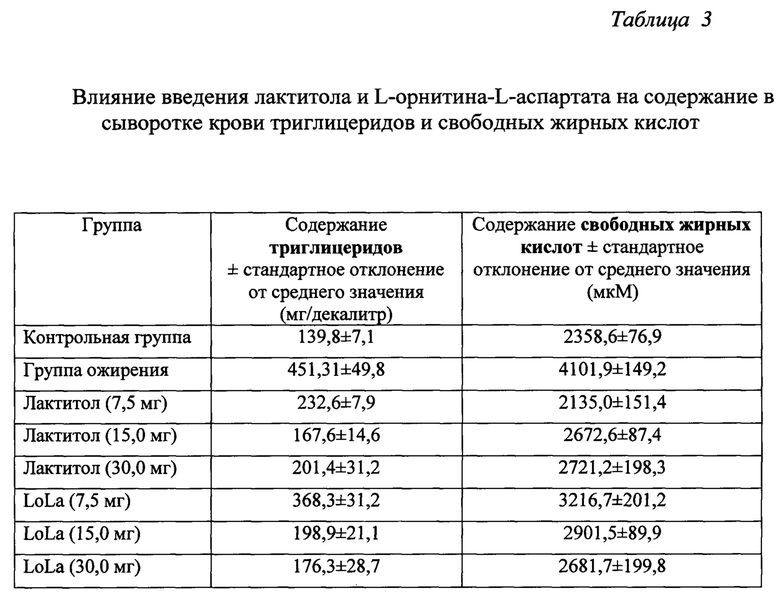
Одной из групп мышей, подверженных ожирению, не вводили никакие препараты (группа ожирения). Остальные группы мышей, подверженных ожирению, были группами обработки, которые получали ежедневно перорально дозы лактитола или LoLa в течение 2 недель. В конце периода обработки у мышей всех групп исследования отбирали по 100 мкл венозной крови в гепаринизированную капиллярную пробирку из ретробульбарной пазухи мышей для химического анализа сыворотки крови на содержание триглицеридов и свободных жирных кислот.
На основании полученных результатов, сведенных в таблицу 3, показано, что введение лактитола мышам, подверженных ожирению, приводит к дозозависимому снижению содержания триглицеридов и свободных жирных кислот.
Таким образом, проведенные испытания и исследования достоверно свидетельствуют о том, что лактитол оказывает влияние на течение жирового перерождения печени и обладает положительным и терапевтическим, и профилактическим эффектом при жировых заболеваниях печени неалкогольного генеза.
Пример 4.
В рамках настоящего изобретения также проведены испытания, чтобы подтвердить предположение о том, что введение лактитола будет оказывать терапевтический эффект, препятствующий развитию цирроза печени.
Эксперименты были проведены на беспородных белых лабораторных крысах. Цирроз моделировали внутрижелудочным введением 50%-го раствора CCl4 (гепатотропный яд) на оливковом масле при дозе 2 мл/кг в течение 3-х недель 2 раза в неделю, всего 6 раз. Для усиления патологического воздействия на печень животные в течение всего периода эксперимента получали 10%-ый раствор этилового спирта.
Группам животных за 4 недели до моделирования патологии печени каждый день перорально вводили лактитол (15 мг). Введение лактитола продолжили и после начала индукции цирроза печени. Контрольной группе животных по той же схеме в эквивалентном объеме вместо лактитола вводили дистиллированную воду.
Состояния печени оценивали после гибели крыс. Проводились биохимические исследования на аспартатаминотрансферазу (АсАТ), аланинаминотрансферазу (АлАТ), щелочную фосфатазу (ЩФ) в сыворотке крови на 41-е сутки. Помимо этого оценивали и морфологическое состояние печени на 41-е сутки опыта. Активность ферментов сыворотки крови определяли общепринятыми методами, используя биохимический анализатор и стандартные наборы к нему. Кровь для исследования получали из бедренной артерии через катетер. На гистологических препаратах печени, окрашенных гематоксилином и эозином, определяли количество клеток инфильтрата с помощью окулярной сетки Автандилова, содержащей 25 тест-точек. В 20 полях зрения подсчитывали количество клеток, попадающих на тест-точки сетки. Относительную площадь инфильтрации высчитывали через отношение точек сетки, приходящихся на клетки инфильтрата, ко всем точкам сетки в 20 полях зрения. Площадь соединительной ткани определяли с помощью средств компьютерной обработки графических данных. Для этого на стандартной площади среза печени (последовательные микрофотографии 10 полей зрения, выполненные микровидеокамерой с программой передачи изображения на компьютер) измеряли площадь структур, окрашенных пикрофуксином, и вычисляли процентное отношение к выбранной стандартной площади. Обработку результатов проводили методом вариационной статистики с использованием t-критерия Стьюдента и непараметрического U-критерия Вилкоксона-Манна-Уитни.
Проведенные эксперименты показали значительную гибель крыс в контрольной группе - 48,9%, в то время как в группе крыс, которым вводили лактитол на фоне моделирования цирроза печени, гибель имела место в весьма незначительном количестве - 4,2%.
Биохимические исследования сыворотки крови выявили повышение активности АлАТ, АсАТ и ЩФ на 40-е сутки опыта после начала введения CCl4 в контрольной группе (таблица 4). В то же время для группы введения лактитола была показана стабилизация ферментативной активности сыворотки крови.
При гистологическом исследовании печени в группе крыс без лечения (не получавших лактитол) имелось выраженное нарушение долькового строения органа. Происходили структурные изменения печеночных венул, артериол и желчных протоков. Грануляционная ткань замещала погибшие гепатоциты, интенсивно протекало новообразование сосудов и печеночных протоков, формировались фиброзные тяжи и микроузлы, так называемые псевдодоли. Последние представляли собой группы гепатоцитов, окруженных участками фиброза. В оставшихся гепатоцитах фиксировалась масштабная крупнокапельная жировая дистрофия. Введение лактитола препятствовало наступлению морфологических признаков цирроза. Сохранялось дольковое строение печени. Стоит отметить, что признаки мелкокапельной жировой дистрофии и портальной инфильтрации фиксировались вплоть до конца периода наблюдения.
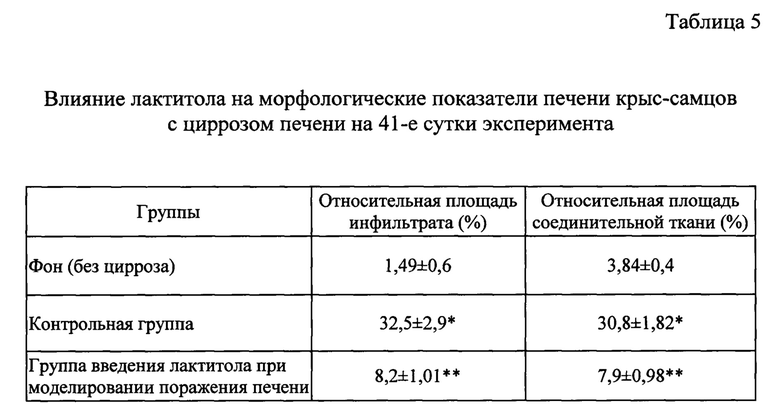
Демонстрировалось значимое уменьшение содержания клеток инфильтрата и площади соединительной ткани в группе крыс, получавших лактитол (таблица 5).
Пример 5.
Получение пероральной лекарственной формы лактитола в виде порошка, упакованного в саше.
Просеянный порошок лактитола моногидрата без вспомогательных веществ упаковывали в саше в количестве 10 г и помещали в картонные пачки.
Пример 6.
Получение пероральной лекарственной формы лактитола в виде капсул.
Порошок лактитола моногидрата просеивают и тщательно смешивают с порошком лактозы в соотношении 2:1. Полученной смесью в количестве 500 мг заполняют твердые желатиновые капсулы подходящего размера.
Пример 7.
Получение пероральной лекарственной формы лактитола в виде таблеток.
Смешивают 1600 мг крахмала, 1600 мг измельченной лактозы, 400 мг талька и 1000 мг лактитола и спрессовывают в брусок. Полученный брусок измельчают в гранулы и просеивают через сита, собирая гранулы размером 14-16 меш. Полученные гранулы таблетируют в подходящую форму таблетки весом 560 мг каждая.
Таким образом, в рамках настоящей заявки достоверно подтверждено, что введение лактитола способствует, в том числе, предотвращению циррозных изменений печени, которые являются следствием НАЖБП.

* отмечена достоверность различия показателя от его фонового значения при р<0,05.
** отмечена достоверность различия показателя от его контрольного значения при р<0,05.
* отмечена достоверность различия показателя от его фонового значения при p<0,05.
** отмечена достоверность различия показателя от его контрольного значения при р<0,05.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ ДЛЯ ПРЕДОТВРАЩЕНИЯ ИЛИ ЛЕЧЕНИЯ ЖИРОВЫХ БОЛЕЗНЕЙ ПЕЧЕНИ | 2015 |
|
RU2664696C2 |
| ПРОФИЛАКТИЧЕСКОЕ И ТЕРАПЕВТИЧЕСКОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО ОТ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ | 2018 |
|
RU2820552C2 |
| НАЛМЕФЕН, НАЛТРЕКСОН ИЛИ ИХ ПРОИЗВОДНЫЕ ДЛЯ ПРИМЕНЕНИЯ В ЛЕЧЕНИИ (НЕ)АЛКОГОЛЬНОГО СТЕАТОГЕПАТИТА ИЛИ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ | 2017 |
|
RU2717677C1 |
| ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ПЕЧЕНИ | 2018 |
|
RU2723686C1 |
| НОВОЕ ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ СОЕДИНЕНИЙ ТИЕНО[3,2-D]ПИРИМИДИН-4-ОНА | 2019 |
|
RU2768828C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ СТЕАТОЗА И НЕАЛКОГОЛЬНОГО СТЕАТОГЕПАТИТА У ЖЕНЩИН | 2020 |
|
RU2744021C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ НЕАЛКОГОЛЬНЫМ СТЕАТОГЕПАТИТОМ НА ФОНЕ МЕТАБОЛИЧЕСКОГО СИНДРОМА | 2015 |
|
RU2595815C1 |
| Способ дифференциальной диагностики стеатоза печени и неалкогольного стеатогепатита у мужчин | 2020 |
|
RU2753455C1 |
| НОВЫЕ ПРИМЕНЕНИЯ И СПОСОБЫ | 2017 |
|
RU2765804C2 |
| Способ прогнозирования эффективности литолиза при желчнокаменной болезни в сочетании с неалкогольной жировой болезнью печени | 2023 |
|
RU2813033C1 |
Изобретение относится к области фармацевтической промышленности, а именно к применению лактитола в терапевтически эффективном количестве (1-20 г в сутки) для лечения и профилактики неалкогольной жировой болезни печени у млекопитающего. Изобретение обеспечивает расширение арсенала средств для данной терапии и профилактики. 8 з.п. ф-лы, 7 пр., 5 табл.
1. Применение 4-O-альфа-D-галактопиранозил-D-глюцитола (лактитола) в терапевтически эффективном количестве для профилактики и лечения неалкогольной жировой болезни печени у млекопитающего, нуждающегося в этом.
2. Применение по п.1, характеризующееся тем, что млекопитающим является человек.
3. Применение по п.1 или 2, характеризующееся тем, что терапевтически эффективное количество лактитола составляет 1-20 г в сутки.
4. Применение по п.1 или 2, характеризующееся тем, что лактитол предназначен для введения млекопитающему, нуждающемуся в этом, на всех стадиях развития неалкогольной жировой болезни печени в дозировке 1-20 г в сутки.
5. Применение по п.1 или 2, характеризующееся тем, что лактитол в дозировке 1-20 г в сутки предназначен для профилактики и лечения цирроза печени, являющегося исходом неалкогольной жировой болезни печени.
6. Применение по п.1 или 2, характеризующееся тем, что лактитол применяют в дозировке 1-20 г в сутки в виде пероральной лекарственной формы.
7. Применение по п.6, характеризующееся тем, что пероральная лекарственная форма не содержит дополнительных активных веществ.
8. Применение по п.6, характеризующееся тем, что пероральная лекарственная форма представляет собой порошок, который не содержит дополнительных вспомогательных веществ.
9. Применение по п.6, характеризующееся тем, что пероральная лекарственная форма может быть выбрана из порошка, таблеток, капсул, гранул, сиропа, напитка, геля, пластинок, мягких желатиновых конфет и дополнительно содержит фармацевтически приемлемые вспомогательные вещества.
| ПРЕСС-ФОРМА ДЛЯ ИЗГОТОВЛЕНИЯ АРМИРОВАННЫХ РЕЗИНОТЕХНИЧЕСКИХ ИЗДЕЛИЙ | 1996 |
|
RU2113998C1 |
| Лекарственный препарат "Экспортал" (порошок для приготовления раствора для приема внутрь) / Зарегистрирован в государственном реестре лекарственных средств, регистрационный номер: ЛСР-003898/07, дата регистрации: 19.11.2007 | |||
| Lanthier P.L | |||
| et al | |||
| Lactitol in the treatment of chronic hepatic encephalopathy: an open comparison with lactulose / Gut, 1985, V.26, pp.415-420 | |||
| Гальченко О.Е | |||
| и др | |||
| Современные возможности применения гепатопротекторов в лечении хронических диффузных заболеваний печени / Лекарственный вестник, 2015, Т.9, N.2 (58), c.7-17. | |||
Авторы
Даты
2019-06-24—Публикация
2018-04-03—Подача