[0001] По настоящей заявке испрашивается приоритет Китайской патентной заявки No. 201811114946.5, поданной в Китайское национальное управление интеллектуальной собственности 25 сентября 2018 г., озаглавленной « Применение чиглитазара и родственных ему соединений», полное содержание которой, таким образом, приведено в качестве ссылки.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
[0002] Настоящее изобретение относится к области медицинской технологии, и конкретно относится к применению чиглитазара и родственных ему соединений.
УРОВЕНЬ ТЕХНИКИ
[0003] Чиглитазар представляет собой активный продукт чиглитазара натрия. Чиглитазар натрия, новое соединение с независимым правом интеллектуальной собственности в Китае, предназначено для лечения диабета типа II. Посредством тестовых моделей ex vivo и in vivo, подтверждено, что чиглитазар натрия оказывает фармакологический эффекты увеличения чувствительности к инсулину, уменьшения уровня глюкозы в крови и улучшения метаболических синдромов. Структурные формулы этих двух соединений являются следующими:
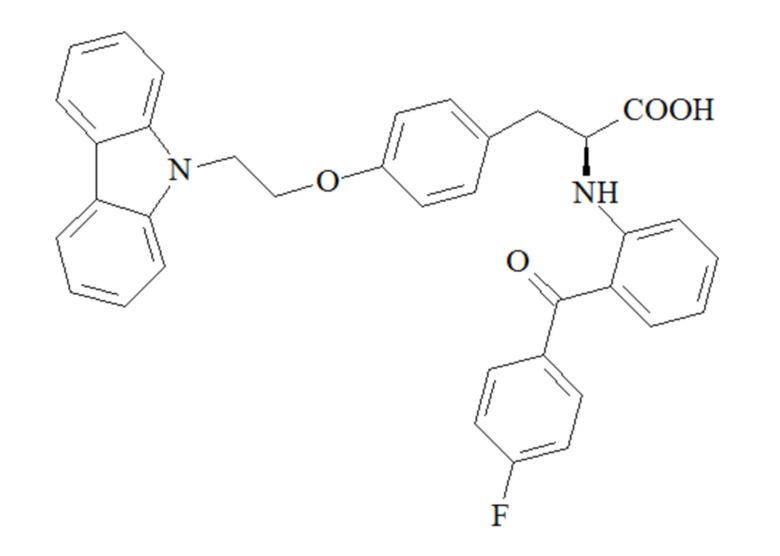
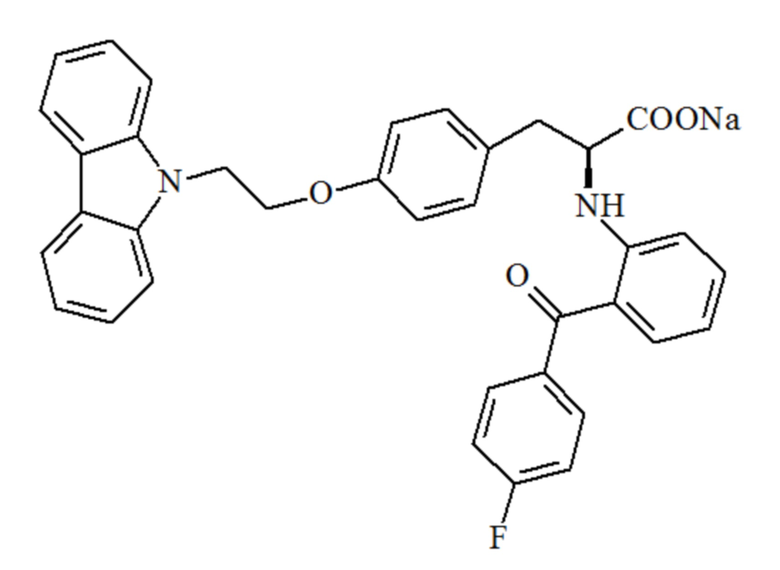
[0004] Опубликованным в настоящее время показанием для чиглитазара является диабет типа II, но не существует относящихся к делу сообщений для фиброзных заболеваний.
[0005] Фиброз представляет собой патофизиологический процесс, который может возникать во множестве тканей и органов в организме. Он проявляет патологические характеристики увеличения количества фиброзной соединительной ткани и уменьшения количества паренхимных клеток в тканях и органах. Продолжающееся прогрессирование фиброза может приводить к разрушению структуры органа, гипофункции и даже органной недостаточности, которая принадлежит к патологическому типу с угрозой для жизни. Органы организма состоят из паренхимы и интерстиция. Паренхимный компонент относится к основной структуре и функциональным клеткам органа, в то время как интерстициальный компонент состоит из интерстициальных клеток и внеклеточного матрикса, которые в основном поддерживают морфологическую структуру и нормальную функцию тканей и органов.
[0006] Повреждение клеток тканей, вызванное экзогенными или эндогенными факторами, может индуцировать местный воспалительный ответ и процесс репарации. В случае незначительного повреждения, процесс репарации включает ограниченную пролиферацию функциональных клеток и восполнение интерстиция, в то время как, в случае значительного повреждения или персистенции факторов, процесс репарации также индуцируется, и внеклеточный матрикс, продуцированный посредством активации интерстициальных клеток, может занимать положения паренхимных функциональных клеток, таким образом, изменять структуру ткани и снижать нормальные физиологические функции. Таким образом, фиброз является по существу нормальным ответом репарации на повреждение ткани для защиты относительной целостности тканей и органов. Однако, избыточный фиброз может изменять нормальную морфологию тканей и органов, и ослаблять их функции.
[0007] Почти во всех главных органах организма человека могут развиваться фиброзные очаги, включая легкое (например, при идиопатической интерстициальной пневмонии и т.д.), сердце (например, при гипертрофической кардиомиопатии и т.д.), печень (например, при неалкогольной жировой инфильтрации печени и циррозе и т.д.), почку (например, при хроническом нефрите и т.д.), костный мозг (например, при миелофиброзе и т.д.), кожу (например, при системной склеродермии и т.д.), и другие ткани и органы могут быть затронуты.
[0008] Фиброзные очаги представляют собой многофакторный и многозвенный патологический процесс, включающий по меньшей мере повреждение клеток паренхимной ткани, воспалительный ответ, активацию интерстициальных клеток и образование матрикса. Повреждение паренхимных клеток вызвано экзогенными факторами, например, повреждение посредством лекарственных средств, и эндогенными факторами, например, аутоиммунное повреждение и метаболическая токсичность (например, липотоксичность). Нормальный воспалительный ответ организма обычно поддается контролю и может быть остановлен посредством факторов петли отрицательной обратной связи после устранения факторов иммунной активации (например, экзогенной инфекции и повреждения клеток ткани). Однако, хроническое воспаление может развиваться в случае персистенции стимулирующих факторов (например, хронической инфекции и аутоантигенов, и т.д.) или иммунодефицита. Поврежденные клетки и иммуноциты продуцируют различные факторы (например, трансформирующий фактор роста TGFβ или тромбоцитарный фактор роста PDGFα/β и т.д.) для стимуляции активации и пролиферации интерстициальных клеток, и продукции внеклеточного матрикса, такого как коллаген. Персистенция вышеуказанной стимуляции вызывает накопление матрикса и фиброз ткани. Таким образом, процесс вмешательства при фиброзных заболеваниях требует участия множества звеньев. При современном клиническом лечении, фиброз все еще имеет необратимое прогрессирование заболевания. Общепринятые виды лечения включают кортикостероиды и другие противовоспалительные лекарственные средства, химиотерапевтические лекарственные средства и лекарственные средства против рецептора тромбоцитарного фактора роста, которые обычно только частично улучшают симптомы пациентов. Главной целью таких видов лечения фиброза все еще является замедление прогрессирования заболевания и поддержание нормальных физиологических функций, и для пациентов на поздних стадиях, трансплантация органов является единственной возможностью для спасения. Таким образом, в клинике существует огромная необходимость в клиническом лечении.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0009] Ввиду этого, целью настоящего изобретения является предоставление серий применений чиглитазара и родственных ему соединений в области фиброзных заболеваний.
[0010] В настоящем описании, чиглитазар и родственные ему соединения включают чиглитазар или его стереоизомеры, геометрические изомеры, таутомеры, сольваты, метаболиты, кристаллические формы, аморфные формы, или их фармацевтически приемлемые соли.
[0011] Его фармацевтически приемлемая соль представляет собой чиглитазар натрия или чиглитазар калия, и их структурные формулы являются следующими:
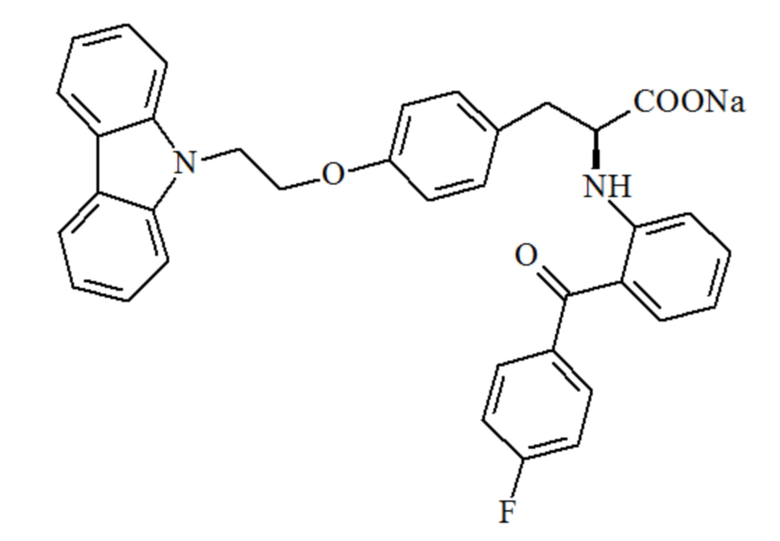
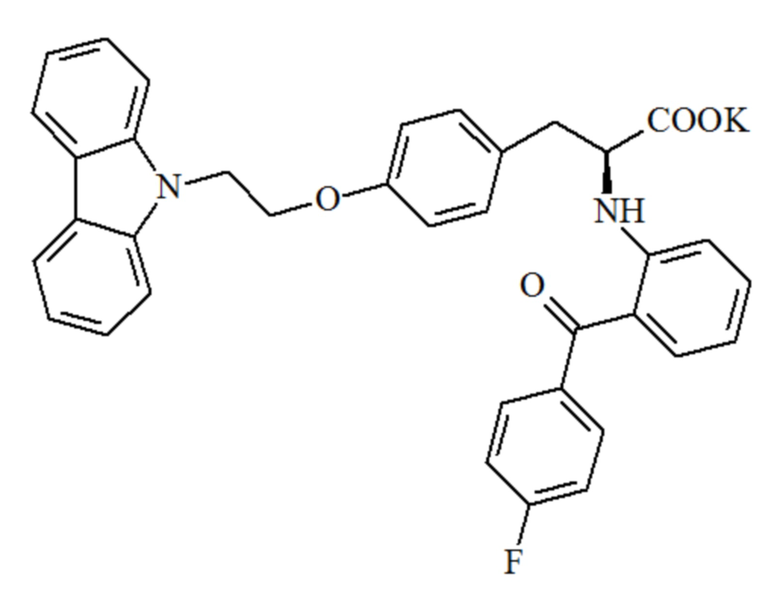
[0012] Активация и пролиферация фибробластов является важным патологическим процессом в прогрессировании фиброзных заболеваний. Ингибирование пролиферации фибробластов имеет потенциал для лечения фиброзных заболеваний. По настоящему изобретению, используют первичные звездчатые клетки печени человека и первичные фибробласты кожи человека в качестве тестируемых объектов для детекции ингибирующих эффектов in vitro чиглитазара натрия и эталонных соединений на оба типа клеток. Результаты показали, что чиглитазар натрия имел активность in vitro ингибирования пролиферации происходящих из кожи и печени человека фибробластов, в отличие от эталонного соединения, пиоглитазона, для которого не показано очевидной ингибирующей активности. Чиглитазар натрия специфически ингибирует пролиферацию фибробластов in vitro, что значительно отличается от других известных агонистов PPAR, таких как пиоглитазон. На основании этого, настоящее изобретение относится к применению чиглитазара и родственных ему соединений в изготовлении ингибиторов фибробластов.
[0013] Трансформирующий фактор роста β (TGF-β) может активировать фибробласты и индуцировать экспрессию связанных с внеклеточным матриксом генов, что играет важную роль в патологическом процессе фиброзных заболеваний. TGF-β1 стимулирует активацию фибробластов и индуцирует экспрессию в матриксе, включая экспрессию гладкомышечного α-актина (α-SMA) и фактора роста соединительной ткани (CTGF), посредством взаимодействия с рецепторами TGF-β. По настоящему изобретению, первичные звездчатые клетки печени человека культивировали в культуральной среде, содержащей TGF-β1 и чиглитазар натрия или эталонное соединение, и затем детектировали уровни экспрессии генов гладкомышечного α-актина (α-SMA) и фактора роста соединительной ткани (CTGF). Результаты показывают, что при стимуляции трансформирующего фактора роста TGFβ, экспрессия связанных с матриксом генов в фибробластах была значительно увеличена, что было значительно ингибировано посредством чиглитазара натрия. В случае экспрессии гладкомышечного α-актина, двойной агонист PPARα/δ GFT505 оказывал определенный ингибирующий эффект, но все еще не такой хороший, как чиглитазар натрия, в то время как двойной агонист PPARγ/α пиоглитазон не оказывал эффекта. В случае экспрессии фактора роста соединительной ткани, только чиглитазар натрия оказывал значительный и зависимый от дозы ингибирующий эффект. Это показывает, что чиглитазар натрия оказывал лучший и неожиданный ингибирующий эффект на пролиферацию фибробластов и экспрессию связанных с фиброзом генов, чем другие агонисты PPAR, такие как пиоглитазон и GFT505. На основании этого, настоящее изобретение относится к применению чиглитазара и родственных ему соединений в изготовлении ингибитора опосредованной TGFβ активации внеклеточного матрикса фибробластов.
[0014] Моноциты вовлечены в местное воспаление, индуцированное посредством повреждения клеток. Они индуцируются хемокинами, высвобождаемыми посредством повреждения, для достижения участка повреждения, и активируются до макрофагов, которые, в свою очередь, продуцируют различные воспалительные факторы (такие как фактор некроза опухоли TNFα и моноцитарный хемоаттрактантный белок MCP-1, и т.д.) для инициации последующего воспалительного ответа, и персистирующий воспалительный ответ индуцирует активацию фибробластов и продукцию внеклеточного матрикса, что является важным патологическим процессом фиброзных заболеваний. Ингибирование этого процесса имеет терапевтические применения для фиброзных заболеваний. По настоящему изобретению, линия мононуклеарных клеток острого моноцитарного лейкоза человека (THP-1) принята в качестве тестируемого объекта, который активировали посредством определенной концентрации форболовых сложных эфиров (форбол-12-миристат-13-ацетата, PMA), и подвергали дифференцировке в макрофаги. Посредством этой клеточной модели, детектировали активирующие эффекты чиглитазара натрия и других соединений на экспрессию связанных с THP-1 воспалительных факторов. Результаты показывают, что как чиглитазар натрия, так и контрольное соединение GFT505 могут значительно ингибировать опосредованную форболовыми сложными эфирами активацию моноцитов и экспрессию связанных генов, но эффект контрольного соединения GFT505 был меньше, чем эффект чиглитазара натрия. На основании этого, настоящее изобретение относится к применению чиглитазара и родственных ему соединений в изготовлении ингибитора воспалительного фактора.
[0015] Хемотаксис моноцитов в кровотоке, индуцированный хемокинами, к участку повреждения, таким образом, для инициации и участия в последующем воспалительном ответе, является одним из важных патологических процессов фиброза ткани. По настоящему изобретению, этот процесс имитировали с использованием технологии Transwell и тестировали эффект чиглитазара натрия или контрольных соединений на индуцированный хемокинами хемотаксис линии моноцитарных клеток THP-1. Результаты показали, что чиглитазар натрия значительно ингибировал активность миграции (transwell) моноцитов THP-1, индуцированной хемокинами моноцитов, по сравнению с контрольными соединениями. Пиоглитазон имел частичную ингибирующую активность, в то время как для двух других контрольных соединений не показано очевидной ингибирующей активности. Для различных агонистов PPAR показаны различные характеристики активности, и чиглитазар натрия имеет более сильную ингибирующую активность. На основании этого, настоящее изобретение относится к применению чиглитазара и родственных ему соединений в изготовлении ингибитора хемотаксиса моноцитов.
[0016] Эндогенные или экзогенные факторы повреждения (такие как химические токсичные вещества) вызывают гибель клеток ткани и индуцируют воспалительный ответ и репарацию ткани, что является типичной патологией фиброзных заболеваний. Тетрахлорметан (CCl4) обычно используют в качестве химического фактора повреждения для имитации фиброза печени, а также широко используют в исследовательской модели фиброза печени грызунов. По настоящему изобретению, используют эту модель для тестирования ингибирующего эффекта чиглитазара натрия в различных дозах на фиброз печени. Результаты показывают, что в модели на мышах, тетрахлорметан (CCl4) может индуцировать гибель паренхимных клеток печени, воспалительную инфильтрацию и фиброз ткани, что согласуется с клиническим патологическим феноменом. Чиглитазар натрия во всех высоких, средних и низких дозах может частично ингибировать воспалительную активность и степень фиброза ткани печени, и таким образом, имеет фармакодинамическую активность для лечения фиброзных заболеваний. На основании этого и вышеупомянутых экспериментальных результатов, настоящее изобретение относится к применению чиглитазара и родственных ему соединений в изготовлении лекарственного средства для лечения фиброзных заболеваний.
[0017] На основании серий экспериментальных результатов по настоящему описанию, можно заключить, что чиглитазар и родственные ему соединения имеют явные эффекты в лечении фиброзных заболеваний, особенно фиброзного заболевания, вызванного повреждением клеток ткани в результате хронического воспаления. Фиброзные заболевания, вызванные повреждением клеток ткани в результате хронического воспаления, включают, но без ограничения, системную склеродермию, хронический нефрит и фиброз почек, миелофиброз, идиопатический пульмонарный фиброз и неалкогольную жировую инфильтрацию печени.
[0018] Можно понять из вышеуказанных технических решений, что посредством моделей in vitro и моделей на животных, настоящее описание иллюстрирует то, что чиглитазар и родственные ему соединения ингибировали активацию фибробластов, продукцию матрикса, активацию моноцитов и хемотактическую активность in vitro, и уменьшали воспалительную активность и площадь фиброза ткани в моделях фиброза печени на животных. По сравнению с известными сходными соединениями, для чиглитазара натрия показаны более значительные и различные характеристики активности, и он имел лучший потенциал к применению для лечения фиброзных заболеваний.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
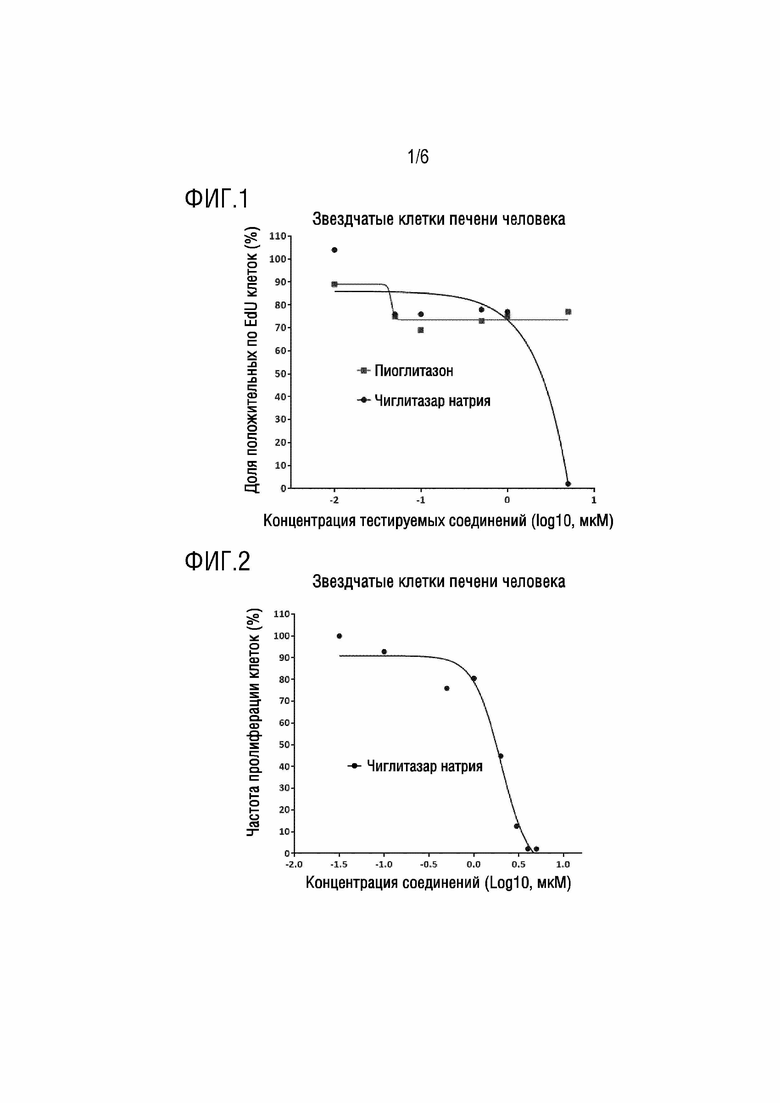
[0019] На ФИГ. 1 показана кривая ингибирования роста in vitro звездчатых клеток печени человека, опосредованного чиглитазаром натрия (анализ EdU);
[0020] На ФИГ. 2 показана кривая ингибирования роста in vitro звездчатых клеток печени человека, опосредованного чиглитазаром натрия (анализ MTT);
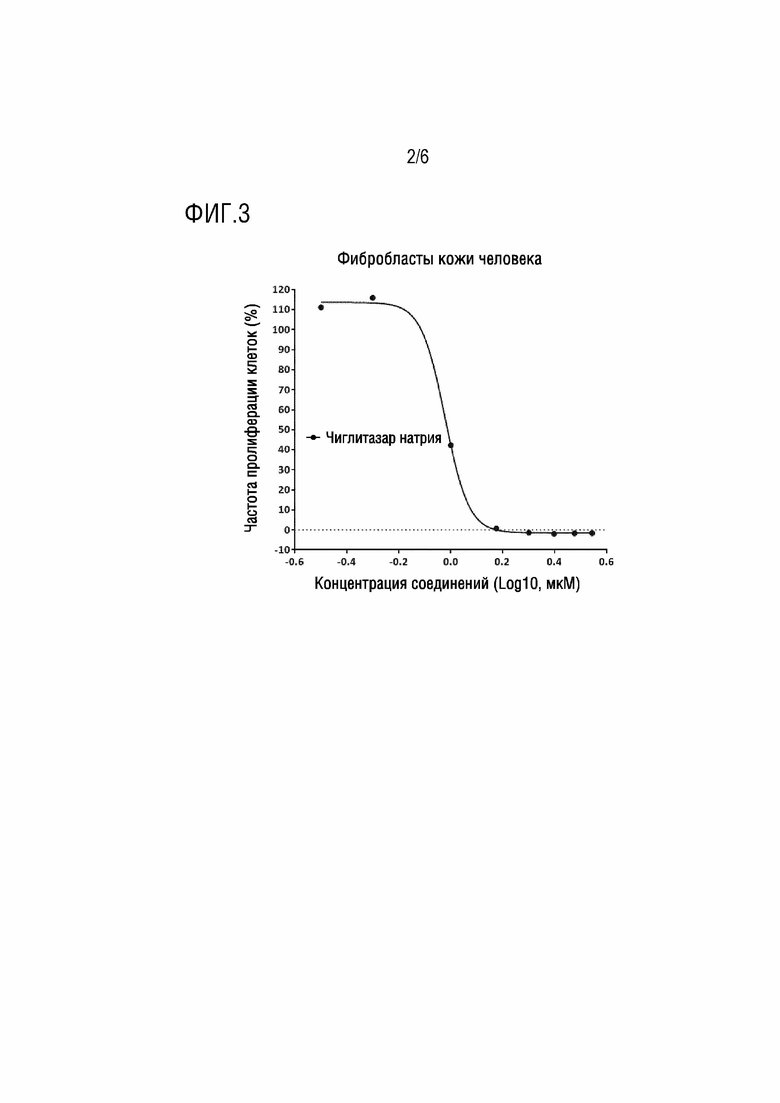
[0021] На ФИГ. 3 показана кривая ингибирования роста in vitro фибробластов кожи человека, опосредованного чиглитазаром натрия (анализ MTT);
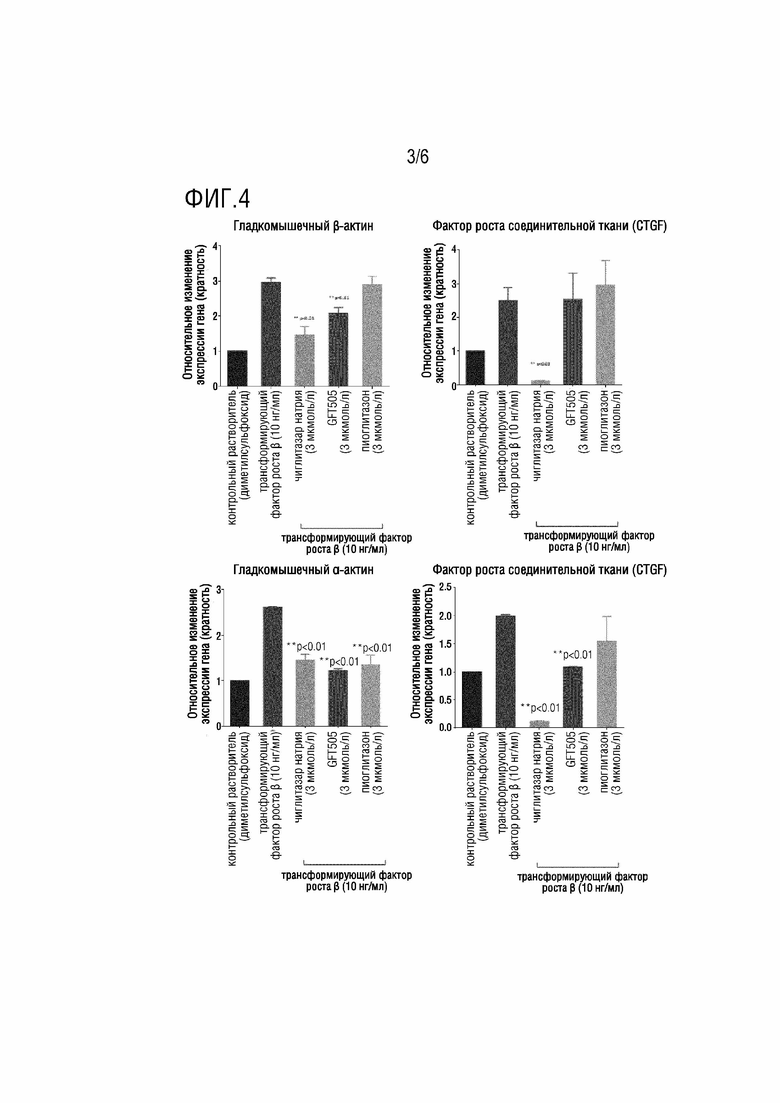
[0022] На ФИГ. 4 показаны эффекты чиглитазара натрия в различных концентрациях и контрольных соединений GFT505 и пиоглитазона на экспрессию генов-мишеней в активированных посредством TGFβ фибробластах;
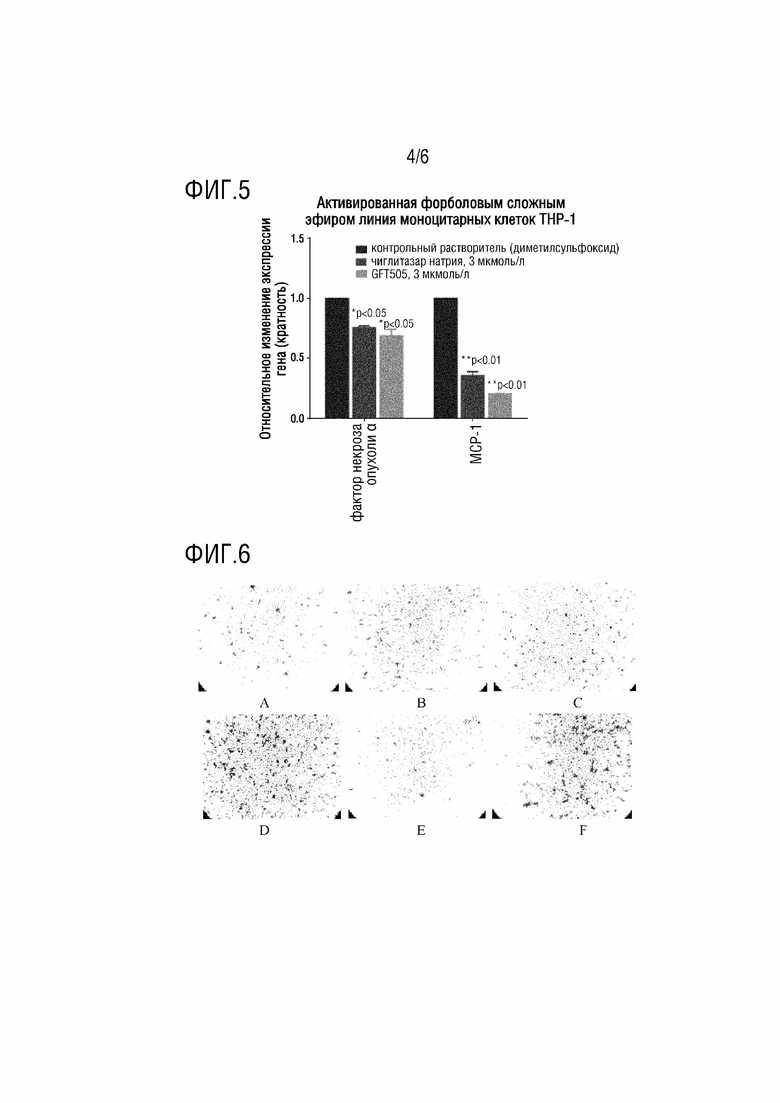
[0023] На ФИГ. 5 показаны эффекты чиглитазара натрия и контрольного соединения GFT505 на экспрессию генов-мишеней в активированных форболовыми сложными эфирами моноцитах, где столбцы в каждой группе слева направо представляют собой контрольный растворитель (диметилсульфоксид), чиглитазар натрия (3 мкмоль/л) и GFT505 (3 мкмоль/л), соответственно;
[0024] На ФИГ. 6 показаны эффекты чиглитазара натрия и контрольных соединений на хемотаксис и миграцию клеток THP-1 (показано как окрашивание клеток кристаллическим фиолетовым), где A представляет собой контрольный растворитель (диметилсульфоксид), B представляет собой контрольный растворитель+MCP-1 (10 нг/мл), C представляет собой чиглитазар натрия (3 мкмоль/л) + MCP-1 (10 нг/мл), D представляет собой GFT505 (3 мкмоль/л) + MCP-1 (10 нг/мл), E представляет собой пиоглитазон (3 мкмоль/л) + MCP-1 (10 нг/мл), и F представляет собой розиглитазон (3 мкмоль/л) + MCP-1 (10 нг/мл), соответственно;
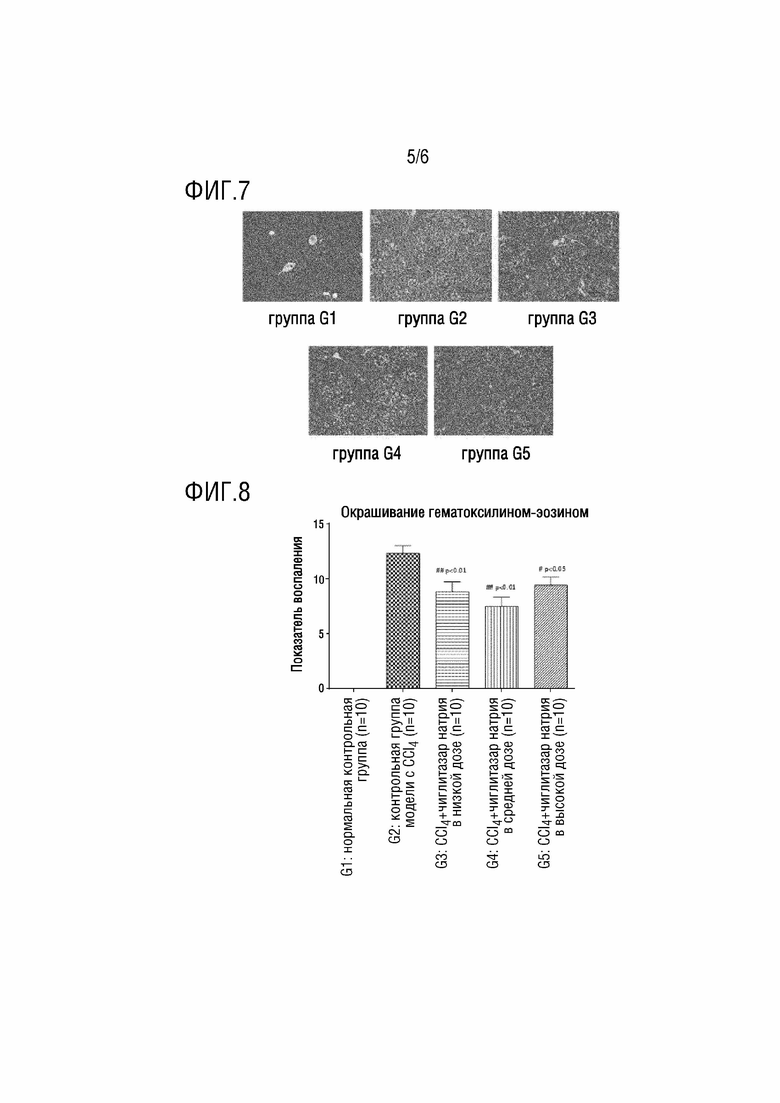
[0025] На ФИГ. 7 показаны микроскопические изображения патологических срезов ткани печени, окрашенных с использованием H&E;
[0026] На ФИГ. 8 показаны основанные на воспалении показатели патологических срезов ткани печени, окрашенных с использованием H&E;
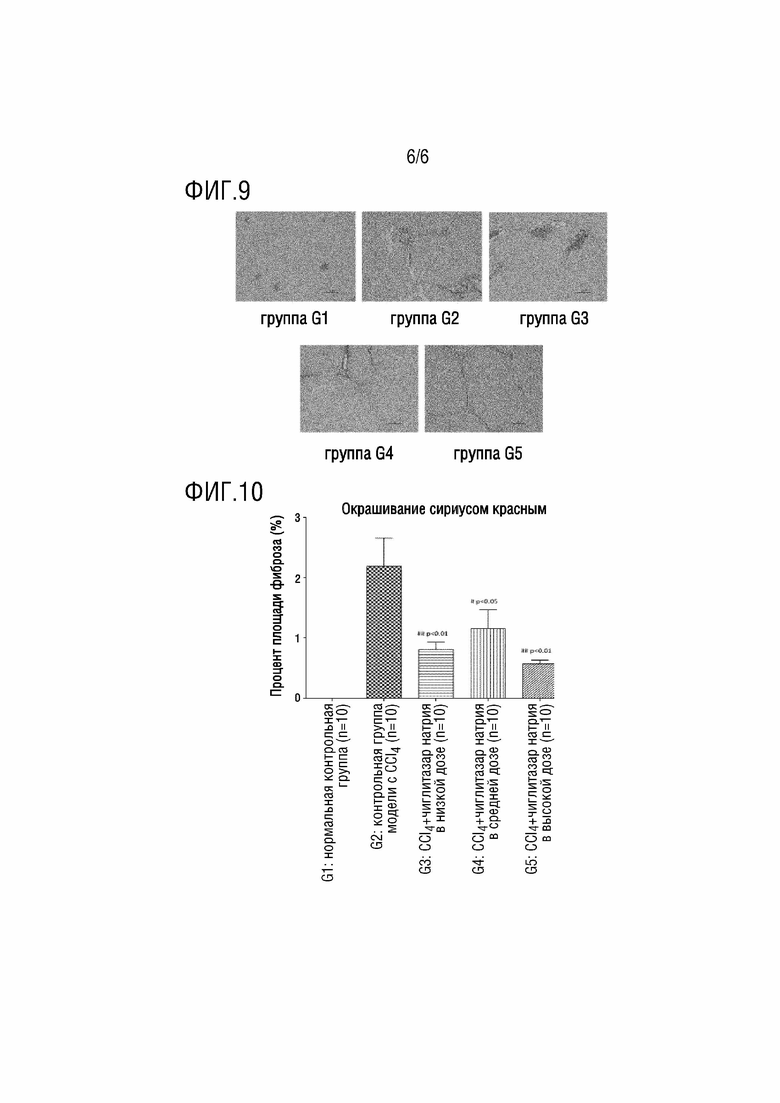
[0027] На ФИГ. 9 показаны микроскопические изображения патологических срезов ткани печени, окрашенных пикросириусом красным; и
[0028] На ФИГ. 10 показаны показатели фиброза патологических срезов ткани печени, окрашенных пикросириусом красным.
ПОДРОБНОЕ ОПИСАНИЕ
[0029] Настоящее изобретение относится к применению чиглитазара и родственных ему соединений. Специалист в данной области может узнать из содержания настоящего описания и подходящим образом улучшать параметры производства. Следует, в частности, указать, что специалисту в данной области очевидны все сходные замены и изменения, которые, как подразумевают, включены в настоящее изобретение. Применения настоящего изобретения описаны посредством предпочтительных вариантов осуществления, и очевидно, специалист в данной области может осуществлять изменения или подходящие модификации и комбинации применений, как описано в настоящем описании, для осуществления и применения технологии по настоящему описанию без отклонения от его содержания, сущности и объема.
[0030] Далее представлено дальнейшее описание применения чиглитазара и родственных ему соединений, представленного по настоящему изобретению.
Пример 1: Активация рецептора PPAR человека посредством чиглитазара натрия
[0031] Модель репортерного гена PPAR содержит три подтипа экспрессирующих плазмид, экспрессирующую RXR плазмиду, плазмиду с репортерным геном люциферазы и экспрессирующую GFP плазмиду в качестве внешнего эталона. Линию клеток гепатоцитов человека L-02 рассевали в 96-луночные планшеты при плотности 15000 клеток/лунку с приблизительно 50% плотностью рассева, с последующим культивированием в течение 24 часов при 37°C. Клетки в каждой лунке трансфицировали соответствующей экспрессирующей плазмидой (плазмида pHD с репортерным геном люциферазы+экспрессирующая PPARα плазмида+экспрессирующая GFP плазмида для детекции активности PPARα; плазмида pACOX с репортерным геном люциферазы+экспрессирующая PPARγ плазмида+экспрессирующая RXR плазмида+экспрессирующая GFP плазмида для детекции активности PPARγ; и плазмида pGL3-PPRE с репортерным геном люциферазы+экспрессирующая PPARδ плазмида+экспрессирующая RXR плазмида+экспрессирующая GFP плазмида для детекции активности PPARδ), с использованием FuGENE 6 от Roche.
[0032] После трансфекции в течение 48 часов, различные концентрации лекарственных средств, подлежащие тестированию, добавляли к культивируемым клеткам с DMSO в качестве контрольного растворителя, и организовывали три лунки повторов для каждой группы обработки.
[0033] После добавления лекарственных средств на 24 часа, культуральную среду отбрасывали и удаляли полностью посредством помещения 96-луночных планшетов вверх дном на адсорбирующую бумагу, и затем 80 мкл лизатов клеток (Promega, E153A) добавляли в каждую лунку. Клеткам позволяли стоять в течение 5 минут при комнатной температуре до использования пипетки, чтобы хорошо перемешать. 60 мкл лизатов клеток из каждой лунки переносили в белые планшеты для детекции (Corning, 3693).
[0034] Интенсивность флуоресценции (при длине волны 485-527 нм) зеленого флуоресцентного белка (GFP) в каждой лунке сначала детектировали в качестве внутреннего стандарта посредством детектора флуоресценции, и затем 30 мкл субстратов люциферазы (Promega, E151A) добавляли в каждую лунку. После слабого встряхивания, чтобы хорошо перемешать, детектировали значения оптической плотности при 562 нм. Относительную интенсивность активации репортерного гена получали посредством соотношения сигнала детекции флуоресценции для лекарственных средств, подлежащих тестированию, и сигнала для контрольного растворителя, где оба сигнала нормализовали по сигналу внутреннего стандарта GFP. Половину максимальной активации (AC50) для лекарственных средств, подлежащих тестированию, рассчитывали с использованием активности при различных концентрациях (показано в таблице 1).
Таблица 1. Активность активации чиглитазара натрия для трех подтипов рецепторов PPAR в модели репортерного гена.
AC50(мкМ)
[0035] Результат показал, что чиглитазар натрия имел активность активации для всех трех подтипов PPAR.
Пример 2: Ингибирование пролиферации фибробластов посредством чиглитазара натрия
[0036] Первичные звездчатые клетки печени человека (HSC), закупленные из Sciencell Research Laboratories, Inc., рассевали в 96-луночные планшеты с использованием полной среды для роста (Stellate Cell Medium) в течение 24 часов, с последующим культивированием в течение ночи в культуральных средах, не содержащих сыворотки и факторов роста, и затем культуральные среды заменяли на свежие среды, содержащие тромбоцитарный фактор роста (PDGF-BB) и соединения, подлежащие тестированию, (чиглитазар натрия или эталонное соединение двойной агонист PPARγ/α пиоглитазон, закупленный из Selleck Chemicals LLC), в различных концентрациях, и клетки культивировали в течение 24 часов. Когда клетки обрабатывали соединениями в течение последних 17 часов, EdU (5-этинил-2’-дезоксиуридин) добавляли к клеткам. Наконец, культуральные среды удаляли, и клетки фиксировали формальдегидом. Количество EdU, включенного в ДНК клеток, количественно оценивали посредством флуоресцентного анализа Click-it EdU, в соответствии с инструкциями производителя (Beyotime). Результаты показаны как процент положительных по EdU клеток среди общего количества клеток, с использованием среднего значения для трех биологических повторов. Ингибирование пролиферации клеток посредством соединений определяли посредством сравнения с значением для включенного EdU в контрольной группе (ФИГ. 1).
[0037] Первичные звездчатые клетки печени человека или первичные фибробласты кожи человека (HDF), и те, и другие закупленные из Sciencell, рассевали в 96-луночные планшеты с полными средами для роста (Stellate Cell Medium или Fibroblast Cell Medium) в течение 24 часов, с последующим культивированием в течение ночи в культуральных средах, не содержащих сыворотку и факторы роста, и затем культуральные среды заменяли на свежую среду, содержащую тромбоцитарный фактор роста (PDGF-BB) и соединения, подлежащие тестированию, в различных концентрациях, и клетки культивировали в течение следующих 72 часов. Измерение проводили с использованием общепринятого набора для анализа MTT (Promega). Результаты показаны как относительная оптическая плотность (OD490) для MTT субстрата, с использованием среднего значения для трех биологических повторов. Ингибирование пролиферации клеток посредством соединений определяли посредством сравнения с значением оптической плотности для контрольной группы (ФИГ. 2, 3).
[0038] Можно видеть из ФИГ. 1-3, что чиглитазар натрия имел ингибирующую активность для пролиферации in vitro фибробластов, происходящих из кожи и печени человека, по сравнению с эталонным соединением пиоглитазоном, для которого не показано очевидной ингибирующей активности. Чиглитазар натрия специфически ингибирует пролиферацию фибробластов in vitro, что значительно отличается от других известных агонистов PPAR, таких как пиоглитазон.
Пример 3: Эффект чиглитазара натрия и контрольных соединений на опосредованную трансформирующим фактором роста TGFβ активацию генов фибробластов
[0039] Первичные звездчатые клетки печени человека рассевали в 6-луночные планшеты с полными средами для роста (Stellate Cell Medium) в течение 24 часов, и затем культуральные среды заменяли на свежие среды (не содержащие сыворотки и факторов роста), содержащие TGF-β1 и соединение, подлежащее тестированию (чиглитазар натрия), или эталонное соединение двойной агонист PPARγ/α пиоглитазон или двойной агонист PPARα/δ GFT505 (оба закупленные из Selleck), и клетки культивировали в течение 24 часов. Тотальные РНК из образцов выделяли, и проводили реакцию обратной транскрипции. После этого, набор для общепринятой амплификации ПЦР (FastStart Universal SYBR@ Green Master (ROX), Roche) использовали для дальнейшей детекции, где праймеры для ПЦР разрабатывали на основании стандартной последовательности мРНК генов-мишеней из NCBI (таблица 2). Реакцию ПЦР и детекцию проводили в устройстве для количественной ПЦР с детекцией в реальном времени ABI StepOnePlus.
Таблица 2. Праймеры для генов-мишеней, используемые для детекции (включая внутренний эталонный ген)
[0040] Посредством расчета относительного количества транскриптов, рассчитанного «способом дельта-дельта CT» (Livak et al. Methods 2001), и с использованием ACTB в качестве гена домашнего хозяйства для нормализации и средних данных для необработанных звездчатых клеток печени человека в качестве эталонного контроля, получали кратность относительного изменения экспрессии гена (ФИГ. 4).
[0041] Результаты, показанные на ФИГ. 4, показывают, что при стимуляции трансформирующего фактора роста TGFβ, экспрессия связанных с матриксом генов в фибробластах была значимо увеличена, что было значимо ингибировано посредством чиглитазара натрия. В случае экспрессии гладкомышечного α-актина, двойной агонист PPARα/δ GFT505 имел определенный ингибирующий эффект, в то время как двойной агонист PPARγ/α пиоглитазон не имел эффекта. В случае экспрессии фактора роста соединительной ткани, только чиглитазар натрия имел значимый и зависимый от дозы ингибирующий эффект. Это показывает, что чиглитазар натрия оказывал лучший и неожиданный ингибирующий эффект на пролиферацию фибробластов и экспрессию связанных с фиброзом генов, чем другие агонисты PPAR, такие как пиоглитазон и GFT505.
Пример 4: Эффект чиглитазара натрия и контрольных соединений на экспрессию связанных воспалительных факторов при опосредованной форболовыми сложными эфирами активации линии моноцитарных клеток THP-1
[0042] Клетки линии мононуклеарных клеток острого моноцитарного лейкоза человека (THP-1) активировали посредством определенной концентрации форболовых сложных эфиров (форбол-12-миристат-13-ацетата, PMA) и подвергали дифференцировке в макрофаги. В рамках этой модели на клетках, детектировали активирующие эффекты чиглитазара натрия и других соединений на экспрессию связанных с THP-1 воспалительных факторов.
[0043] Клетки THP-1 рассевали в 6-луночные планшеты с полными средами для роста в течение 24 часов, и затем культуральные среды заменяли на свежие среды, содержащие PMA и соединение, подлежащее тестированию (чиглитазар натрия), или эталонное соединение GFT505 (двойной агонист PPARα/δ), и клетки культивировали в течение 6 часов. Тотальные РНК из образцов выделяли, и кДНК-матрицы синтезировали посредством реакции обратной транскрипции (набор для синтеза первой цепи кДНК Transcriptor First Strand cDNA Synthesis Kit, Roche). После этого, набор для общепринятой амплификации ПЦР (FastStart Universal SYBR@ Green Master (ROX), Roche) использовали для полуколичественной детекции экспрессии генов в устройстве для количественной ПЦР с детекцией в реальном времени ABI StepOnePlus. Праймеры для генов-мишеней показаны в таблице 2.
[0044] Относительное изменение экспрессии генов-мишеней получали с использованием внутреннего эталонного гена β-актина (ACTB) в качестве стандарта для нормализации, сравнивали с образцами клеток без обработки, и рассчитывали кратность относительного изменения экспрессии (ФИГ. 5).
[0045] Результаты, показанные на ФИГ. 5, показывают, что как чиглитазар натрия, так и контрольное соединение GFT505, могут значимо ингибировать опосредованную форболовыми сложными эфирами активацию моноцитов и экспрессию связанных генов, однако, эффект контрольного соединения GFT505 был не настолько хорошим, как у чиглитазара натрия.
Пример 5: Эффект чиглитазара натрия и контрольных соединений на индуцированный хемокинами хемотаксис линии моноцитарных клеток THP-1
[0046] В модели in vitro, миграцию линии моноцитарных клеток THP-1 индуцировали посредством определенной концентрации хемокинов (таких как моноцитарный хемотактический белок 1, MCP-1), и соответственно, имитировали такой процесс in vivo. Технология Transwell, в соответствии с инструкциями производителя от Corning Inc., подразумевает, что Traswell представляет собой вид поликарбонатного мембранного фильтра, так же как проницаемый носитель. Поликарбонатная мембрана разделяет культуральную камеру на верхнюю и нижнюю, где компоненты культуральной среды в нижней камере могут влиять на рост, дифференцировку и движение клеток в верхней камере. Наконец, способность клеток к миграции может отражать окрашивание и подсчет клеток в нижней камере.
[0047] Во время культивирования на стадии логарифмической фазы, клетки THP-1 ресуспендировали, доводили концентрацию и рассевали в 24-луночные планшеты, с последующей предварительной обработкой культуральными средами, содержащими соединение, подлежащее тестированию (чиглитазар натрия), или эталонное соединение GFT505, пиоглитазон или одинарный агонист PPARγ розиглитазон (все закупленные из Selleck), в течение 24 часов. Transwell использовали в соответствии с инструкциями производителя. Культуральные среды, содержащие хемокин MCP-1, добавляли в нижнюю камеру (т.е., на дно 24-луночных планшетов), и суспензию клеток добавляли в верхнюю камеру и культивировали в течение 4 часов. Позже, клетки, культивированные на поверхности «потолка» из поликарбонатной мембраны, фиксировали и окрашивали раствором кристаллического фиолетового (ФИГ. 6), и затем количество клеток в нижней камере подсчитывали (таблица 3).
Таблица 3 Количество клеток в нижней камере в эксперименте transwell
[0048] Можно видеть в таблице 3 и на ФИГ. 6, что чиглитазар натрия значительно ингибировал активность миграции моноцитов THP-1, индуцированной хемокином моноцитов, по сравнению с контрольными соединениями (transwell). Пиоглитазон имел частичную ингибирующую активность, которая очевидно являлась не настолько хорошей, как у чиглитазара натрия, в то время как для двух других контрольных соединений не показано очевидной ингибирующей активности. Для различных агонистов PPAR показаны различные характеристики активности, и чиглитазар натрия имеет более сильную ингибирующую активность.
Пример 6: Ингибирующий эффект чиглитазара натрия в модели индуцированного тетрахлорметаном фиброза печени на мышах
[0049] Мышам BALB/c инъецировали внутрибрюшинно 25% CCl4 (4 мл/кг массы тела) дважды в неделю, что может вызывать повреждение печени и хронический фиброз печени за 3 недели. Модельных животных подвергали непрерывному введению в течение 6 недель, и в не модельной контрольной группе вводили контрольный растворитель оливковое масло в течение такого же периода. Модельных животных случайным образом разделяли на группы, начиная с третьей недели. В контрольной группе вводили растворитель (0,2% метилцеллюлозу натрия) внутрижелудочно, начиная с четвертой недели, и в группах чиглитазара натрия при высокой, средней и низкой дозе вводили 40, 20 и 10 мг/кг массы тела активного ингредиента чиглитазара натрия внутрижелудочно, соответственно (таблица 4), до окончания эксперимента на 7й неделе. После умерщвления экспериментальных животных, образцы ткани плазмы и печени собирали для измерения содержания трансаминазы плазмы, массы ткани печени и соотношения массы печени и массы тела, соответственно. Ткани печени фиксировали для получения патологических срезов, и затем проводили окрашивание гематоксилином-эозином (окрашивание H&E) и окрашивание пикросириусом красным, соответственно. Первый использовали для оценки повреждения клеток и воспаления, и последний использовали для оценки фиброза ткани.
Таблица 4 Разбиение на группы для тестирования и обработка лекарственным средством
[0050] Показатели тканей печени на основании воспаления получали посредством микроскопического исследования и оценки в баллах патологических срезов, окрашенных гематоксилином и эозином (окрашивание H&E). Односторонне слепое тестирование и оценку в баллах проводили патологи, с использованием системы оценки в баллах Metavir для воспалительной активности, сравнивающей четыре независимых показателя, то есть, портальное воспаление, лобулярное воспаление, мелкоочаговый некроз и мостовидный некроз (ФИГ. 8).
[0051] Срезы ткани печени окрашивали пикросириусом красным для морфологического исследования (ФИГ. 9), и измеряли с использованием полуавтоматической цифровой системы анализа изображений и программного обеспечения для измерения (OsteoMetrics, Inc.). Патолог проводил односторонне слепое тестирование и вручную обводил целые срезы, и затем измерял площадь фиброза в целых срезах по прямым линиям. Программное обеспечение автоматически рассчитывало общую площадь измерения. % площади фиброза=общая площадь фиброза ÷ общая площадь среза ткани печени *100 (ФИГ. 10).
[0052] Можно видеть из результатов на ФИГ. 7-10, что в модели на мышах, тетрахлорметан (CCl4) может индуцировать гибель паренхимных клеток печени, воспалительную инфильтрацию и фиброз ткани. Чиглитазар натрия во всех высоких, средних и низких дозах может частично ингибировать воспалительную активность и степень фиброза тканей печени, и таким образом, имел фармакодинамическую активность лечения фиброзных заболеваний.
[0053] Вышеуказанное представляет собой предпочтительные варианты осуществления настоящего изобретения, однако, следует отметить, что специалист в данной области может осуществлять некоторые их улучшения и модификации без отклонения от принципов настоящего описания, и эти улучшения и модификации следует также подразумевать как входящие в объем патентной охраны по настоящему изобретению.
Изобретение относится к применению чиглитазара или его фармацевтически приемлемых солей для изготовления лекарственного средства для лечения фиброзных заболеваний, в том числе фиброзных заболеваний, вызванных повреждением клеток ткани в результате хронического воспаления, таких как системная склеродермия, хронический нефрит и фиброз почек, миелофиброз, идиопатический пульмонарный фиброз и неалкогольная жировая инфильтрация печени, а также для изготовления ингибитора фибробластов, для изготовления ингибитора опосредованной TGFβ активации внеклеточного матрикса фибробластов, для изготовления ингибитора воспалительного фактора в изготовлении ингибитора хемотаксиса моноцитов. По сравнению с известными сходными соединениями чиглитазар демонстрирует более значительные и различные характеристики активности и имеет лучший потенциал применения для лечения фиброзного заболевания. 5 н. и 3 з.п. ф-лы, 10 ил., 4 табл., 6 пр.
1. Применение чиглитазара или его фармацевтически приемлемых солей в изготовлении лекарственного средства для лечения фиброзных заболеваний.
2. Применение чиглитазара или его фармацевтически приемлемых солей в изготовлении ингибитора фибробластов.
3. Применение чиглитазара или его фармацевтически приемлемых солей в изготовлении ингибитора опосредованной TGFβ активации внеклеточного матрикса фибробластов.
4. Применение чиглитазара или его фармацевтически приемлемых солей в изготовлении ингибитора воспалительного фактора.
5. Применение чиглитазара или его фармацевтически приемлемых солей в изготовлении ингибитора хемотаксиса моноцитов.
6. Применение по любому из пп. 1-5, где фармацевтически приемлемая соль чиглитазара представляет собой чиглитазар натрия или чиглитазар калия.
7. Применение по любому из пп. 1-5, где фиброзное заболевание представляет собой фиброзное заболевание, вызванное повреждением клеток ткани в результате хронического воспаления.
8. Применение по п. 7, где фиброзное заболевание, вызванное повреждением клеток ткани в результате хронического воспаления, включает системную склеродермию, хронический нефрит и фиброз почек, миелофиброз, идиопатический пульмонарный фиброз и неалкогольную жировую инфильтрацию печени.
| CN 102056606 A, 11.05.2011 | |||
| CN 102883721 A, 16.01.2013 | |||
| WO 2011002012 A1, 06.01.2011 | |||
| US 20170174718 A1, 22.06.2017 | |||
| Антифибролитическое средство | 2016 |
|
RU2621163C1 |
Авторы
Даты
2022-03-31—Публикация
2019-09-20—Подача