Изобретение относится к области наноматериалов, в том числе биомедицинского применения, и направлено на создание эффективных нанотехнологий, с целью предотвращения деградации, т.е. агрегации оксидных наночастиц фосфатов кальция состава xCaO·yP2Os·zH2O.
Для стабилизации наночастиц, т.е. для предотвращения агрегации, применяют синтез наночастиц в мезопористых матрицах, например алюмосиликатных (1) или стеклянных матрицах (2). Однако извлечение наночастиц из таких матриц требует применения агрессивных жидкостей (кислот, щелочей).
Известны способы формирования порошкового композита «наночастицы/солевая матрица» в результате механохимического твердофазного синтеза нанопорошков СеО (3) в результате обменной реакции, ZnO в результате разложения Zn5(NO3)2(OH)8·2Н2О (4), и соединения Na0.5Bi0.5TiO3 с использованием топохимического метода (5) в солевых матрицах. Солевая матрица формируется в твердой фазе отчасти вследствие обменной реакции (3), а также вносится при составлении исходной шихты (3, 4, 5). Однако такие способы не могут быть использованы для формировании порошкового композита «наночастицы/солевая матрица» нанокристаллических фосфатов кальция из-за необходимости при синтезе поддержания постоянной величины рН.
Наиболее близким к предлагаемому изобретению является способ формирования солевой матрицы для стабилизации оксидных наночастиц, включающий синтез порошкового композита, содержащего солевую матрицу (6), в котором как наночастицы, так и солевая матрица формируются в результате обменной реакции. Недостатком указанного способа также является невозможность регулирования уровня рН, необходимого для синтеза нерастворимых фосфатов.
Целью настоящего изобретения является разработка способа получения наночастиц фосфатов кальция, стабилизированных солевой матрицей. Поставленная цель была достигнута настоящим изобретением.
В способе получения наночастиц фосфатов кальция, стабилизированных солевой матрицей, взаимодействием компонентов, первый из которых содержит катион металла, а второй - содержит анион, согласно изобретению в качестве первого компонента используют растворимую в воде соль кальция, а в качестве второго компонента растворимый ортофосфат, при этом образуются наночастицы нерастворимого в воде фосфатата кальция, а солевая матрица формируется из растворимого сопутствующего продукта.
Для формирования солевой матрицы с включенными в нее наночастицами фосфата кальция состава xCaO·yP2O5·zH2O (или порошкового композита «наночастицы фосфата кальция/солевая матрица») готовят исходные растворы с концентрацией 0,25-1,00 М для [Са2+] и 0,15-0,60 М для [(РО4)-3]. Порошки после взаимодействия реагентов, отделения осадка и сушки содержат от 8 до 35% адсорбированного сопутствующего продукта реакции, что соответствует содержанию оксидных наночастиц в композите 65-82 мас.%.
При использовании более разбавленных растворов (менее 0,25М для [Са2+] и 0,15 М для [РО4 3-]) количество адсорбированного сопутствующего растворимого продукта реакции будет недостаточным для предотвращения агрегации наночастиц в порошковом композите. При использовании более концентрированных растворов (более 1,0 М для [Са2+] и 0,6 М для [(РО4)3-]) количество адсорбированного продукта практически не возрастает, что связано с ограниченной адсорбционной емкостью поверхности наночастиц фосфата кальция.
Пример 1
1 л 0,5 М раствора хлорида кальция CaCl2 приливают к 1 л 0,3 М раствору Na2HPO4, содержащему в качестве регулятора рН среды NaOH, взятый в 1,2-кратном избытке относительно рассчитанного по реакции, при рН=8-10, Т=60°С (1)

Синтезированный порошок после отделения осадка и сушки представляет собой порошковый композит «наночастицы фосфата кальция/солевая матрица», в котором наночастицы фосфата кальция - это наночастицы гидроксиапатита, а солевая матрица - хлорид натрия. Порошковый композит содержит 80% Са10(PO4)6(ОН)2 и 20% NaCl. Хлорид натрия в данном случае представляет собой физическое препятствие для протекания агрегации наночастиц гидроксиапатиата. Хранение наночастиц гидроксиапатита в солевой матрице сопутствующего продукта возможно в течение длительного времени при нормальных условиях, без нагревания до температуры плавления солевой матрицы. Извлечение нанопорошка из солевой матрицы проводят промыванием полученного порошка водой. Аналогично были извлечены нанопорошки гидроксиапатита, синтезированные по реакции (1) из растворов других концентраций (Таблица 1). Из таблицы следует, что при указанных условиях извлечения нанопорошка из солевой матрицы размер частиц составляет 20-40 нм. Для получения нанокерамики предпочтительно коллоидное формование из суспензии наночастиц гидроксиапатита, извлеченных из солевой матрицы.
Пример 2
1 л 0,3 М раствора (NH4)2HPO4 приливают к 1 л 0,5 М раствора нитрата кальция Са(NO3)2, содержащему в качестве регулятора рН среды NH4OH, взятый в 1,2-кратном избытке относительно рассчитанного по реакции (2), при рН=9, Т=60°С.
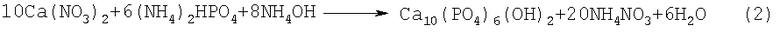
Синтезированный порошок после отделения осадка и сушки представляет собой порошковый композит «наночастицы фосфата кальция/солевая матрица», в котором наночастицы фосфата кальция - это наночастицы гидроксиапатита, а солевая матрица - нитрата аммония. Порошковый композит «наночастицы фосфата кальция/солевая матрица» содержит 80% Са10(PO4)6(ОН)2 и 20% NH4NO3. Нитрат аммония в данном случае представляет собой физическое препятствие для протекания агрегации наночастиц гидроксиапатиата. Хранение наночастиц гидроксиапатита в солевой матрице сопутствующего продукта возможно в течение длительного времени при нормальных условиях, без нагревания до температуры плавления или термического разложения солевой матрицы. Извлечение нанопорошка из солевой матрицы проводят промыванием полученного порошка водой.
Аналогично были извлечены нанопорошки гидроксиапатита, синтезированные по реакции (2) из растворов других концентраций (Таблица 2). Из таблицы следует, что при указанных условиях извлечения нанопорошка из солевой матрицы размер частиц составляет 20-40 нм. Для получения нанокерамики предпочтительно коллоидное формование из суспензии наночастиц гидроксиапатита, извлеченных из солевой матрицы.
Для извлечения нанопорошка гидроксиапатита из солевой матрицы нитрата аммония возможен также другой способ извлечения, который связан с относительно низкой температурой разложения нитрата аммония, которая лежит в интервале 150-250°С. Для такого способа извлечения нанопорошка гидроксиапатиата в солевой матрице нитрата аммония проводят в интервале 300-400°С в течение 3-6 часов. При обработке при температуре ниже 300°С и менее 3 часов не удается полностью освободить порошок от солевой матрицы. При обработке при температуре выше
400°С и дольше 6 часов возможно протекание начальной стадии спекания, ведущей как к уменьшению удельной поверхности, так и к увеличению размера частиц.
Аналогично были извлечены нанопорошки гидроксиапатита, синтезированные по реакции (2) из растворов других концентраций (Таблица 3). Из таблицы следует, что при указанных условиях извлечения нанопорошка из солевой матрицы удельная поверхность порошка составляет 40-60 м2/г. Восстановленный порошок гидроксиапатита может быть использован для получения нанокерамики с использованием холодного гидростатического прессования.
Пример 3
1 л 0,5 М раствора ацетата кальция Са(СН3СОО)2 приливают к 1 л 0,3 М раствора K2HPO4, содержащему в качестве регулятора рН среды КОН, взятый в 1,2-кратном избытке относительно рассчитанного по реакции, рН=8-11, Т=60°С (3)

Синтезированный порошок после отделения осадка и сушки представляет собой порошковый композит «наночастицы фосфата кальция/солевая матрица», в котором наночастицы фосфата кальция - это наночастицы гидроксиапатита, солевая матрица - ацетат калия. Порошковый композит «наночастицы фосфата кальция/солевая матрица» содержит 80% Са10(PO4)6(ОН)2 и 20% KCH3COO. Ацетат калия в данном случае представляет собой физическое препятствие для протекания агрегации наночастиц гидроксиапатиата. Хранение наночастиц гидроксиапатита в солевой матрице сопутствующего продукта возможно в течение длительного времени при нормальных условиях, без нагревания до температуры термического разложения солевой матрицы. Извлечение нанопорошка гидроксиапатита из солевой матрицы проводят промыванием полученного порошка водой.
Аналогично были извлечены нанопорошки гидроксиапатита, синтезированные по реакции (3) из растворов других концентраций (Таблица 4). Из таблицы следует, что при указанных условиях извлечения нанопорошка гидроксиапатита из солевой матрицы размер частиц составляет 30-50 нм. Для получения нанокерамики предпочтительно коллоидное формование из суспензии наночастиц гидроксиапатита, извлеченных из солевой матрицы.
Пример 4
1 л 0,5 М раствора хлорида кальция CaCl2 приливают к 1 л 0,5 М раствора Na2HPO4, по реакции рН=4, Т=40°С (4)

Синтезированный порошок после отделения осадка и сушки представляет собой порошковый композит «наночастицы фосфата кальция/солевая матрица», в котором наночастицы фосфата кальция - это наночастицы брушита CaHPO4·2H2O, солевая матрица - хлорида натрия NaCl. Порошковый композит «наночастицы фосфата кальция/солевая матрица» содержит 80% CaHPO4·2H2O и 20% NaCl. Хлорид натрия в данном случае представляет собой физическое препятствие для протекания агрегации наночастиц монетита. Хранение наночастиц брушита в солевой матрице сопутствующего продукта возможно в течение длительного времени при нормальных условиях, без нагревания до температуры плавления солевой матрицы. Извлечение нанопорошка из солевой матрицы проводят промыванием полученного порошка водой.
Аналогично были извлечены нанопорошки брушита, синтезированные по реакции (4) из растворов других концентраций (Таблица 5). Из таблицы следует, что при указанных условиях извлечения нанопорошка из солевой матрицы размер частиц составляет 40-60 нм. Для получения нанокерамики предпочтительно коллоидное формование из суспензии наночастиц брушита, извлеченных из солевой матрицы.
Литература
1. Третьяков Ю.Д., Лукашин А.В., Елисеев А.А. Синтез функциональных нанокомпозитов на основе твердофазных нанореакторов. // Успехи химии. 2004, Т.73, №9, С.974-998.
2. Matthew J. Dejneka, Christy Powell, Nick Borrelli, Dimitre Ouzounov, Alex Gaeta Transparent Magnetic Glass-Ceramics II J. Am. Ceram. Soc. 2005, Vol.88. №9. P.2435-2441.
3. T.Tsuzuki and P.G. McCormick, Synthesis of ultrafine ceria powder by mechanochemical processing// J. Am. Ceram. Soc. 2001, Vol.84, №7 P.1453-1458.
4. Chong Phui Fah, Junmin Xue, John Wang nanosized Zinc-oxide particle derived from mechanical activation of Zn5(NO3)8*2H2O in sodium cloride // J. Am. Ceram. Soc. 2002, Vol.85. №1. P.273-275.
5. J.T.Zeng, K.W.Kwok, W.K.Tam, H.Y.Tian, X.P.Jiang, and H.L.W.Chan, Plate-like Na0.5Bi0.5TiO3 template synthesized by topochemical method // J. Am. Ceram. Soc. 2006. Vol.89, №12, P.3850-3853.
6. T.Tsuzuki, W.T.A.Harrison, P.G.McCormick. Synthesis of ultrafine gadolinium oxide powder by mechanochemical processing // J. Alloys and compounds, 1998, Vol.281, P.146-151.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОДГОТОВКИ ШИХТЫ ДЛЯ ПОЛУЧЕНИЯ КЕРАМИЧЕСКОГО БИОДЕГРАДИРУЕМОГО МАТЕРИАЛА | 2010 |
|
RU2456253C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТОГО КЕРАМИЧЕСКОГО МАТЕРИАЛА НА ОСНОВЕ ПИРОФОСФАТА КАЛЬЦИЯ | 2012 |
|
RU2531377C2 |
| СПОСОБ ПОЛУЧЕНИЯ КЕРАМИЧЕСКОГО КОМПОЗИЦИОННОГО БИОДЕГРАДИРУЕМОГО МАТЕРИАЛА НА ОСНОВЕ ДВОЙНОГО ФОСФАТА КАЛИЯ КАЛЬЦИЯ | 2008 |
|
RU2395303C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИОННОГО МАТЕРИАЛА ДЛЯ ЗАМЕЩЕНИЯ КОСТНЫХ ДЕФЕКТОВ С ИСПОЛЬЗОВАНИЕМ ГИДРОЛИТИЧЕСКОЙ КОНВЕРСИИ | 2015 |
|
RU2599022C1 |
| Высокопрочный антифрикционный композит на основе полиэфирэфиркетона для медицины и способ его изготовления | 2020 |
|
RU2729653C1 |
| СПОСОБ ПОДГОТОВКИ ШИХТЫ ДЛЯ ПОЛУЧЕНИЯ БИОКЕРАМИКИ | 2009 |
|
RU2431627C2 |
| СПОСОБ ПОЛУЧЕНИЯ КЕРАМИЧЕСКОГО БИОДЕГРАДИРУЕМОГО МАТЕРИАЛА, СОСТОЯЩЕГО ИЗ ПИРОФОСФАТА КАЛЬЦИЯ И ТРИКАЛЬЦИЙФОСФАТА | 2008 |
|
RU2391316C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУБМИКРОННОЙ БИФАЗНОЙ КЕРАМИКИ НА ОСНОВЕ ТРИКАЛЬЦИЙФОСФАТА И ГИДРОКСИАПАТИТА | 2013 |
|
RU2555685C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКОВОГО МАТЕРИАЛА НА ОСНОВЕ КАРБОНАТГИДРОКСИАПАТИТА И БРУШИТА | 2014 |
|
RU2546539C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСОВМЕСТИМОЙ ПОРИСТОЙ КЕРАМИКИ НА ОСНОВЕ ДИОКСИДА ЦИРКОНИЯ ДЛЯ ЭНДОПРОТЕЗИРОВАНИЯ | 2020 |
|
RU2741918C1 |
Изобретение относится к медицине. Описан способ получения наночастиц фосфатов кальция, стабилизированных солевой матрицей, взаимодействием компонентов, первый из которых содержит катион металла, а второй - содержит анион. Согласно изобретению в качестве первого компонента используют растворимую в воде соль кальция, а в качестве второго компонента растворимый ортофосфат, при этом образуются наночастицы нерастворимого в воде фосфатата кальция, а солевая матрица формируется из растворимого сопутствующего продукта. Содержание наночастиц фосфатов кальция в порошковом композите «оксидные наночастицы/солевая матрица» составляет 65-82 мас.%. Способ направлен на создание эффективных нанотехнологий, с целью предотвращения деградации, то есть агрегации оксидных наночастиц фосфатов кальция. 5 табл.
Способ получения порошкового композита - наночастицы фосфата кальция/солевая матрица - взаимодействием компонентов, первый из которых содержит катион металла, а второй - содержит анион, отличающийся тем, что в качестве первого компонента используют растворимую в воде соль кальция с концентрацией 0,25-1,00 М для [Са2+], а в качестве второго компонента растворимый ортофосфат с концентрацией 0,15-1,00 М для [(PO4)3-], при этом образуются наночастицы нерастворимого в воде фосфатата кальция, а солевая матрица формируется из растворимого сопутствующего продукта, содержание наночастиц фосфатов кальция в порошковом композите составляет 65-82 мас.%.
| T.TSUZUKI, Synthesis of ultrafine gadolinium oxide powder by mechanochemical processing, J | |||
| Alloys and compounds, 1998, vol.281, p.146-151 | |||
| WO 2005123579 A1, 29.12.2005 | |||
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИАПАТИТА | 1993 |
|
RU2077475C1 |
Авторы
Даты
2010-06-10—Публикация
2008-10-09—Подача