Изобретение относится к медицине, конкретно к технологии получения биосовместимых композитных материалов, которые могут быть использованы для изготовления костных имплантатов в восстановительной хирургии.
Керамические материалы в настоящее время занимают приоритетное положение на мировом рынке, широко востребованы в разных областях промышленности и медицины. Это обусловлено их высокой коррозионной, химической, радиационной стойкостью, термостойкостью, низкой теплопроводностью, что делает возможным продолжительную эксплуатацию керамических элементов в условиях воздействия химически-агрессивных сред и повышенных температур без деградации свойств. При этом наилучшие свойства обнаруживают керамические материалы из частично стабилизированного диоксида циркония (t-ZrO2), который получают путем добавления на стадии синтеза порошка-прекурсора стабилизирующих добавок, таких как оксид иттрия, церия и др. [1-3]. Привлекательность керамики на основе t-ZrO2 для медицинского применения по сравнению с металлами и полимерами обусловлена исключительной химической инертностью, высокой прочностью и хорошей совместимостью с организмом человека.
Для изготовления эндопротезов используют износостойкую керамику, металлы и сплавы, различные полимеры. Они легко поддаются обработке для достижения хорошего сопряжения частей конструкции протеза. Наиболее популярным материалом для создания протезов является нержавеющие стальные сплавы благодаря низкой стоимости изделия. Однако металлические конструкции часто вызывают аллергические реакции и отторгаются организмом, что уменьшает их срок службы и приводит к необходимости повторного хирургического вмешательства и замены протеза. Полимерные материалы также не всегда совместимы с организмом. Кроме того, они обладают низкими показателями износостойкости и способны разрушаться из-за воздействия биологических жидкостей в организме человека [4, 5].
В последние годы все больше внимания уделяется разработкам биосовместимой керамики для заместительной хирургии и эндопротезирования. Создание отечественных конкурентоспособных керамических композиций на основе диоксида циркония связано с использованием нанодисперсных порошков. В последние годы для получения нанодисперсных порошков на основе t-ZrO2 широко используются так называемые методы «мягкой» химии, основанные на синтезе наночастиц из водных растворов солей соответствующих металлов при относительно низких (~300°С) температурах. Возможность контроля и управления условиями протекания процесса позволяет получать порошки-прекурсоры заданного химического, фазового и гранулометрического состава [2, 6-8].
При создании композита для имплантатов, обладающего характеристиками, близкими к характеристикам костной ткани, оптимальным является комбинирование материалов с требуемыми механическими и биологическими свойствами. Развитая поровая структура композита обеспечивает прочное сцепление имплантата с тканями, что является важным условием для обеспечения высоких прочностных характеристик и долговечности конструкции, например, при протезировании тазобедренного сустава. Керамика на основе t-ZrO2 используется в медицине для реконструкции и замещения костной ткани, т.к. она не оказывает токсического влияния на организм и способна длительное время сохранять механические характеристики, пребывая в биологически среде [9].
Пористые керамические материалы - особый класс материалов, эксплуатационные характеристики которых определяются объемом порового пространства и размером пор. Структура материала должна позволять костной ткани прорастать вглубь, что требует наличия развитой системы пор. Современные технологические приемы увеличения пористости керамики довольно разнообразны [8, 10-12].
Высокопористую керамику обычно получают простым и эффективным методом твердофазного спекания с введением порообразующих добавок. В качестве порообразователей используют активированный уголь, спирты, амины, а также карбонаты и нитраты аммония и другие соединения, которые при нагревании разлагаются с образованием газообразных продуктов, формируя при спекании материала пористую структуру. Одним из высокоэффективных и безопасных порообразователей является карбонат аммония (NH4)2CO3, при разложении одного моля которого выделяются три моля газообразной фазы, что способствует образованию развитой поровой структуры в керамической матрице [13-14].
При пористости керамики свыше 40% ее прочность резко падает, поэтому интерес представляют такие добавки, которые могут обладать как порообразующими, так и армирующими свойствами, например, гидроксид алюминия.
Открытая пористость трубчатых костей человека составляет 40-50%, модуль упругости ~100 ГПа. Использование керамических эндопротезов подразумевает постоянно возникающие упругие напряжения/релаксации в месте контакта имплантата с костной и мышечной тканями человека. Для наиболее долговечного использования имплантата необходимо, чтобы упругие свойства кости и керамики были сопоставимы для предотвращения возможного взаимного разрушения. С медицинской точки зрения одним из наиболее перспективных материалов для изготовления имплантатов является гидроксиапатит кальция Ca10(PO4)6(OH)2 (ГАП) благодаря своему подобию костной ткани [15].
В современной научной литературе известны работы, посвященные созданию биоматериалов, как из диоксида циркония, так и из ГАП. Однако долговечные цельнокерамические конструкции из этих материалов изготовить сложно из-за недостаточно прочного сцепления имплантата из t-ZrCO2 с костной и мышечной тканью и низкой прочностью и трещиностойкостью ГАП. Поэтому в последние годы особое внимание уделяется созданию и изучению комбинированных материалов из смеси t-ZrO2 и ГАП. Получение отечественных t-ZrO2/ГАП композитов для реконструктивной медицины, сочетающих в себе высокую прочность и биосовместимость, простым и эффективным методом является в настоящее время актуальной проблемой [4, 16-18].
Недостатки известных способов получения биосовместимой пористой керамики на основе диоксида циркония заключаются в следующем.
Использование сложной многоступенчатой технологии синтеза оксидных нанопорошков-прекурсоров, включающей несколько стадий помола, влечет за собой необходимость очистки порошков от нежелательных примесей, что увеличивает энергозатраты и, как следствие, себестоимость материала. Кроме того, использование в качестве исходных реагентов хлоридов циркония и иттрия приводит к отрицательному влиянию ионов хлора кристаллическую структуру керамики, что также влечет за собой введение дополнительной стадии очистки.
Зачастую в качестве порообразователей и спекающих добавок используют органические вещества (спирты, амины и др.), которые могут оказывать негативное влияние на организм человека. Кроме того, порообразователи способствуют разрыхлению материала и снижают его прочность, что приводит к необходимости увеличивать температуру спекания или вводить дополнительные спекающие добавки, загрязняющие конечный материал.
Ввиду особенностей механических свойств керамик из диоксида циркония и гидроксиапатита, использование их отдельно может приводить к получению итогового материала с низкой прочностью и трещиностойкостью при пористости выше 40%.
Задачей изобретения является разработка полностадийного способа получения прочной высокопористой керамики на основе диоксида циркония с открытой пористостью не менее 45%, модулем упругости не менее 90 ГПа с возможностью варьирования этих показателей, перспективной для использования в качестве материала для эндопротезирования.
Согласно изобретению способ получения биосовместимой пористой керамики на основе диоксида циркония для эндопротезирования включает несколько стадий: жидкофазный направленный синтез порошков-прекурсоров, введение порообразующих добавок, консолидация нанопорошков для получения итоговой керамики заданного химического состава, при этом жидкофазный направленный синтез порошков-прекурсоров в системе ZrO2-Y2O3-Al2O3 осуществляют путем выбора в качестве исходных реагентов солей ZrO(NO3)2⋅2H2O, Y(NO3)3⋅5H2O и Al(NO3)3⋅9H2O, из которых приготавливают разбавленные растворы и осуществляют двухэтапное осаждение гидроксидов из соответствующих солей водным раствором аммиака NH4OH до полного осаждения всех гидроксидов, смешения и получения осадка с высокой степенью гомогенности, затем гелеобразный осадок фильтруют и подвергают быстрому замораживанию при -25°С в течение 24 часов, после чего синтезированный порошок состава [(ZrO2)0,97(Y2O3)0,03]0,8(Al2O3)0,2 высушивают и подвергают термообработке при 800°С, затем осуществляют введение порообразующих добавок, для чего с помощью механического смешения к синтезированному порошку добавляют оптимальную композицию порообразующей добавки с содержанием 10 масс. % гидроксиапатита кальция Ca10(PO4)6(ОН)2 ГАП и 30 масс. % (NH4)2CO3, после чего для получения итоговой керамики заданного химического состава полученные смеси формуют в компакты методом холодного одноосного прессования при давлении 100 МПа и спекают на воздухе при 1300°С с изотермической выдержкой в 2 ч и скоростью нагрева - 350-400°/ч.
Технический результат, достигаемый при использовании заявленной совокупности существенных признаков, заключается в следующем.
Использование разбавленных растворов азотнокислых солей при осаждении более целесообразно, чем концентрированных, так как это позволяет получить более дисперсный и однородный продукт осаждения. Контролируя скорость поступления их в маточный раствор достигается равномерное рН во всем объеме и обеспечивается удаленность центров зародышеобразования.
Параллельное двухэтапное осаждение обеспечивает полное осаждение всех гидроксидов и получения осадка с высокой степенью гомогенности. Быстрое замораживание геля ослабляет силы взаимодействия кристаллических частиц осадка между собой и способствует снижению степени его агломерации.
Твердофазное спекание с добавлением в шихту порообразующих выгорающих добавок для получения высокопористой керамики является доступным и эффективным. Для получения пористой керамики медицинского назначения необходимо учитывать, что спекающие добавки и порообразователи должны быть нетоксичны и безопасны для человека, не вызывать аллергию и отторжение организма.
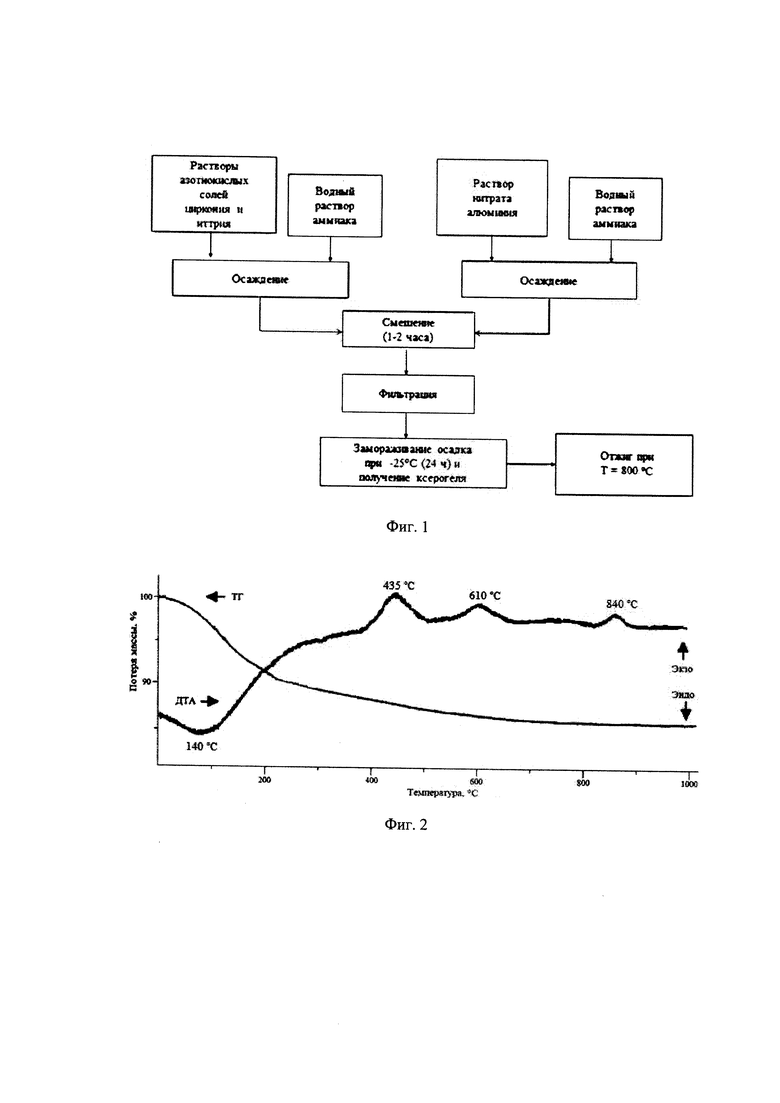
Сущность изобретения поясняется чертежами, где на фиг. 1 представлена схема синтеза порошков на основе t-ZrO2 - Al2O3, на фиг. 2 - результаты дифференциально-термического анализа ксерогеля состава 80 мол.% (ZrO2)0,97(Y2O3)0,03 - 20 мол. % Al2O3; на фиг. 3 - последовательность образования керамического нанокомпозита в системе ZrO2-Y2O3-Al2O3, полученного методом совместного осаждения: 1 - ксерогель после замораживания при -25°С и сушки при 110°С; 2 - порошок, полученный после обжига при 800°С; 3 - керамика, спеченная при 1300°С. Обозначения: ■ - тетрагональный твердый раствор на основе ZrO2, • - кубический твердый раствор на основе ZrO2 типа флюорита, на фиг. 4 - дифференциальное распределение пор по размерам пористой структуры керамики на основе t-ZrO2 с добавлением порообразующих композиций (1300°С, 2 ч).
Заявленный способ осуществляют следующим образом.
В качестве исходных реагентов выбирают азотнокислые соли ZrO(NO3)2⋅2H2O, Y(NO3)3⋅5H2O и Al(NO3)3⋅9H2O, из которых приготавливают разбавленные растворы (~0.1 М). Использование разбавленных растворов при осаждении более целесообразно, чем концентрированных, так как это позволяет получить более дисперсный продукт осаждения. Осаждение оксогидроксида циркония происходит при рН 2.3-4.2, гидроксида иттрия - 7.0-7.4. Значения рН осаждения гидроксида алюминия лежит в интервале 4.0-5.2, при достижении значений рН 7.8 начинается процесс растворения осадка гидроксида алюминия, вплоть до полного растворения при рН 10.8 [19]. Поэтому процесс осаждения проводят в два параллельных этапа: 1-й этап - соосаждение азотнокислых солей циркония и иттрия, 2-й этап-осаждение нитрата алюминия. После осаждения смеси гидроксидов циркония и иттрия осадок промывают декантацией до достижения значения рН раствора ~7.0, добавляли свежеосажденный гидроксид алюминия и перемешивали. Гидроксид циркония является основным компонентом продукта совместного осаждения в системе [(ZrO2)0,97(Y2O3)0,03]0,8(Al2O3)0,2 и для него характерны реакции гидролиза и полимеризации с образованием тетрамерных гидроксильных комплексов [Zr(OH)2⋅nH2O]48+, которые приводят к образованию «жестких» агломератов. Поэтому необходимо, чтобы время нахождения осадка в маточном растворе было минимальным [20, 21].
Гелеобразный осадок фильтруют, а затем замораживают при -25°С (24 ч), в результате получают рентгеноаморфный ксерогель, фиг. 3, кривая 1, с площадью удельной поверхности 150 м2/г и средним размером пор ~3-4 нм. Быстрое замораживание геля ослабляет силы взаимодействия кристаллических частиц осадка между собой и способствует снижению степени его агломерации.
Процессы термолиза полученного ксерогеля исследовали методом ДТА, фиг. 2. На термограмме в интервале температур 110-150°С наблюдается эндоэффект, соответствующий основной стадии дегидратации осадка. Ксерогели содержат значительное количество адсорбированной воды в виде молекул H2O и структурной - в виде ОН--групп. Кроме того, для порошков на основе системы ZrO2(Y2O3) - Al2O3 характерно повышенное содержание структурно связанной воды по сравнению с порошками на основе ZrO2(Y2O3). Для увеличения эффективности дегидратации осадок подвергают низкотемпературной обработке при -25°С (24 ч), способствующей вымораживанию большей части воды и интенсификации процесса дегидратации на стадии сушки. Это позволяет снизить потерю массы в ксерогеле до 10%. Экзоэффект при 435°С свидетельствует о начале процесса кристаллизации метастабильного кубического твердого раствора на основе диоксида циркония (c-ZrO2). Экзоэффект при 610°С соответствует кристаллизации γ-Al2O3. Широкий экзоэффект при 840°С указывает на протекание фазового перехода γ-Al2O3 → δ-Al2O3. Средний размер кристаллитов в синтезированном порошке состава [(ZrO2)0,97(Y2O3)0,03]0,8(Al2O3)0,2 составляет 8-10 нм.
Для получения поровой структуры керамики на основе синтезированных ксерогелей и порошков выбирают нетоксичные и доступные порообразующие добавки: карбонат аммония (NH4)2CO3 марки «ч» и синтезированные нами гидроксид алюминия Al(ОН)3 и гидроксиапатит кальция Са10(РО4)6(ОН)2, а также их смеси.
Для получения пористой керамики медицинского назначения необходимо учитывать, что спекающие добавки и порообразователи должны быть безопасны для человека, не вызывать аллергию и отторжение организма, препятствующих остеоинтеграции конструкции.
Известно, что при достижении пористости свыше 40% за счет порообразующих добавок, прочность материала резко падает, поэтому наибольший интерес представляет гидроокись алюминия не только в качестве порообразователя, но и в качестве спекающей добавки.
Кроме того, одним из безопасных и высокоэффективных порообразователей является карбонат аммония. Один моль (NH4)2CO3 при разложении дает три моля газообразной фазы, что способствует образованию развитой пористой структуры.
С медицинской точки зрения одним из наиболее перспективных материалов для изготовления имплантатов является гидроксиапатит кальция (Са10(PO4)6(ОН)2) благодаря биосовместимости с организмом человека.
Исходные порошки смешивают с выбранными (оптимальными) композициями порообразующих добавок на основе Al(ОН)3, (NH4)2CO3 и ГАП в планетарной мельнице Fritsch Pulverisette в корундовых стаканах с корундовыми мелющими телами в течение 2 часов. Полученные смеси формуют сухим одноосным прессованием на гидравлическом прессе ПГР-400 в стальной пресс-форме и спекают на воздухе на корундовых подложках в печи SNOL 6,7/1300 при 1300°С с изотермической выдержкой 2 ч, скоростью нагрева - 350-400°С/ч. Достаточно большую скорость нагрева выбирают, чтобы уменьшить скорость роста кристаллитов.
На основании исследования влияния добавления индивидуальных порообразователей (NH4)2CO3 и Al(ОН)3 в исходные порошки не удалось получить высокую пористость керамики с сохранением ее прочности. Анализируя полученные результаты, были выбраны порообразующие добавки в виде композиций Al(ОН)3+(NH4)2CO3 и ГАП+(NH4)2CO3 - табл. 1.


Введение порообразующей композиции состава 15 масс. % Al(ОН)3 + 20 масс. % (NH4)2CO3 в исходные порошки I и II показало, что свойства керамики в значительной степени зависят от состава цирконий содержащей матрицы. Оксид алюминия способствует торможению роста зерен диоксида циркония, что позволяет увеличить прочность материала за счет протекания процесса трансформационного упрочнения, характерного для наноразмерной керамики из t-ZrO2.
В связи с вышеизложенным, изучение влияния состава порообразующих композиций на свойства керамики проводили с использованием исходного порошка II.
В порообразователе на основе смеси Al(ОН)3 и (NH4)2CO3 увеличение количества карбоната аммония до 30 масс. % приводит к незначительному возрастанию открытой пористости керамики (состав 3), а уменьшение количества гидроксида алюминия до 10 масс. % не оказывает отрицательного влияния на величину модуля упругости.
Для исследования влияния гидроксиапатита кальция на свойства керамики используют порообразующую композицию, в которой гидроксид алюминия заменяют таким же количеством гидроксиапатита кальция (10 масс. %), содержание карбоната аммония уменьшают также до 10 масс. %. После спекания модуль упругости образцов керамики (состав 4) возрастает до значений, необходимых при использовании керамики для эндопротезирования. Увеличение значений модуля упругости обусловлено формированием твердого раствора Ca0.10Zr0.90O2, образующегося вследствие полного разложения гидроксиапатита кальция после обжига при 1300°С и частичной термической диффузии ионов Са2+ в решетку ZrO2 [16]. Снижение значения открытой пористости при этом связано со значительным уменьшением содержания (NH4)2CO3.
Увеличение в смеси порообразователей количества карбоната аммония до 30 масс. % при сохранении количества гидроксиапатита кальция (состав 5) позволяет получить после спекания керамику со свойствами, наиболее приближенными к параметрам трубчатой костной ткани человека: открытая пористость - 48%) и модуль упругости - 98 ГПа. Закрытая пористость всех полученных керамических образцов была незначительна и не превышала 0,16%.
Методом ртутной порометрии были получены данные о размерах и распределении пор в образце полученного керамического материала (фиг. 4).
Из фиг. 4 следует, что данная керамика имеет бимодальное распределение мезо- и макропор по размерам в интервале 40-800 нм. Первый максимум обусловлен мезопорами менее 100 нм, размер которых соизмерим с размером зерна. Второй максимум образуют макропоры размером от 100 нм и выше. Столь крупные пустоты в керамике обусловлены образованием в процессе прессования каркаса из агломератов используемых порошков, размеры которых определяют размер макропор между ними. Значительная доля пор имеет радиус менее 200 нм. Средний размер пор по полученным данным составил ~180 нм.
Полученная высокопористая прочная керамика на основе t-ZrO2/ГАП по своим механическим (открытая пористость 48%, модуль упругости 94 ГПа) и медико-биологическим (биосовместимость с тканями организма человека) свойствам перспективна в качестве материала для эндопротезирования и может быть рекомендована для использования в трансплантологии [22].
При создании новых материалов медицинского назначения для современной заместительной хирургии и эндопротезирования ключевым вопросом является разработка технологий получения высококачественных оксидных нанокомпозитов с заданными физико-химическими и механическими свойствами. Заявленное изобретение представляет собой технологию жидкофазного синтеза многокомпонентного биосовместимого керамического материала в системе ZrO2-Y2O3-Al2O3 для создания керамического имплантата для эндопротезирования.
Подобрано соотношение оксидов и оптимальные условия получения нанокристаллического порошка на основе диоксида циркония и выявлены условия его консолидации. Подобраны комплексные порообразующие добавки для получения высокопористой керамики на основе диоксида циркония: карбонат аммония, гидроксид алюминия, гидроксиапатит кальция и их смесь в различном процентном соотношении. Такой выбор обусловлен тем, что карбонат аммония и гидроксид алюминия доступны, экологически чисты и не загрязняют конечный продукт, безопасны для организма человека, а гидроксиапатит кальция (ГАП) является неорганической составляющей костной ткани человека. Выбран оптимальный состав порообразующей добавки с содержанием 10 масс. % ГАП и 30 масс. % (NH4)2СО3. На основе исходных порошков состава [(ZrO2)0,97(Y2O3)0,03]0,8(Al2O3)0,2 с порообразующими добавками получена высокопористая прочная керамика с открытой пористостью 48%, модулем упругости 94 ГПа, перспективная для использования в качестве материала для эндопротезирования. Установлено, что, изменяя содержание разных компонентов комплексного порообразователя: (NH4)2CO3 и ГАП, можно в широких пределах варьировать пористость и прочность материала.
Все вышеупомянутое свидетельствует о перспективности применения предложенной технологии синтеза нанопорошков состава [(ZrO2)0,97(Y2O3)0,03]0,8(Al2O3)0,2 и получения на их основе высокопористой, прочной керамики медицинского назначения для заместительной хирургии и трансплантологии.
Список использованной литературы
1. Рутман Д.С., Торопов Ю.С., Плинер С.Ю. Высокоогнеупорные материалы из диоксида циркония. М.: Металлургия, 1985, 136 с.
2. Шевченко А.В., Рубан А.К., Дудник Е.В. Высокотехнологичная керамика на основе диоксида циркония. // Огнеупоры и техническая керамика, 2000, №9, с. 2-8.
3. Анциферов В.Н., Порозова С.Е., Кульметьева В.Б., Торсунов М.Ф. Фазовый состав нанодисперсных порошков диоксида циркония, стабилизированных оксидами иттрия и церия. // Огнеупоры и техническая керамика, 2012, №4-5, с. 17-21.
4. Рыбакова У.С., Ивасев С.С., Раводина Д.В. Технология создания биосовместимых покрытий на имплантаты // Решетневские чтения. 2016. №20. Т. 2. С. 341-342.
5. Садовой М.А., Ларионов П.М., Самохин А.Г., Рожнова О.М. Клеточные матрицы (скаффолды) для целей регенерации кости: современное состояние проблемы // Хирургия позвоночника. 2014. №2. С. 79-86.
6. Михайлина Н.А., Подзорова Л.И., Румянцева М.Н., Шворнева Л.И., Овчинникова О.А., Анисимова С.В., Лебеденко И.Ю., Лебеденко А.И., Хван B.И. Керамика на основе тетрагонального диоксида циркония для реставрационной стоматологии. // Перспективные материалы, 2010, №3, с. 44-48.
7. Жуков И.А., Буякова С.П., Кульков С.Н., Третьяков Д.А. Пористая керамика ZrO2-Al2O3. // Изв. вузов. Физика, 2011, т. 54, №9/2, С. 120-124.
8. Максимов А.И., Мошников В.А., Таиров Ю.М., Шилова О.А. Основы золь-гель технологии нанокомпозитов. СПб: Изд-во «Элмор», 2007, 255 с.
9.  Santa Cruz,
Santa Cruz,  Spino, Georg Grathwohl. Nanocrystalline ZrO2 ceramics with idealized macropores // Journal of the European Ceramic Society. 2008. Vol. 28. Iss. 9. Pp 1783-1791.
Spino, Georg Grathwohl. Nanocrystalline ZrO2 ceramics with idealized macropores // Journal of the European Ceramic Society. 2008. Vol. 28. Iss. 9. Pp 1783-1791.
10. Буякова С.П., Хлусов И.А., Кульков С.Н. Пористая циркониевая керамика для эндопротезирования костной ткани. // Физическая мезомеханика, 2004, т. 7, ч. 2, с. 127-130.
11. Кульков С.Н., Буякова С.П., Смолин А.Ю., Роман Н.В., Кинеловский C.А. Перколяционные переходы в поровой структуре керамики и ее физико-механические свойства // Письма в ЖТФ, 2011, т. 37, вып. 8, с. 34-40.
12. Кульков С.Н., Масловский В.И., Буякова С.П., Никитин Д.С. Негуковское поведение пористого диоксида циркония при активной деформации сжатием. // Журнал технической физики, 2002, том 72, вып. 3, с. 38-42.
13. Гузман И.Я. Некоторые принципы образования пористых керамических структур, свойств и применение // Стекло и керамика. 2003. №9. С28-31.
14. Гращенков Д.В., Балинова Ю.А., Тинякова Е.В. Керамические волокна оксида алюминия и материалы на их основе // Стекло и керамика. 2012. №4. С. 32-35.
15. Путляев В.И. Современные биокерамические материалы // Соросовский образовательный журнал. 2004. Т. 8. №1. С. 44-50.
16. Оковитый В.А., Пантелеенко Ф.И., Пантелеенко А.Ф., Оковитый В.В., Кулак А.И., Уласевич С.А. Процесс получения композиционного порошка на основе гидроксиапатита и диоксида циркония для нанесения плазменных биокерамических покрытий // Наука и техника. 2013. №1. С. 31-38.
17. Крутько В.К., Кулак А.И., Мусская О.Н. Термические превращения в композитах на основе гидроксиапатита и диоксида циркония // Неорганические материалы. 2017. Т. 53. №4. С. 427-434.
18. H.W., Noh Y.J., Koh Y.H., Kim Н.Е., Kim H.M. Effect of CaF2 on densification and properties of hydroxyapatite-zirconia composites for biomedical applications // Biomaterials. 2002. Vol. 23. Pp. 4113-4121.
19. Koval'ko N.Yu., Dolgin A.S., Efimova L.N., Arsent'ev M.Yu., Shilova O.A. Liquid-phase Synthesis and Investigation of Powders Based on Zirconium Dioxide // Glass Physics and Chemistry. 2018. Vol. 44. No. 6. Pp. 611-616.
20. Koval'ko N.Yu., Kalinina M.V., Maslennikova T.P., Morozova L.V., Myakin S.V., Khamova T.V., Arsent'ev M.Yu., Shilova O.A. Comparative Study of Powders Based on the ZrO2-Y2O3-CeO2 System Obtained by Various Liquid Phase Methods of Synthesis // Glass Physics and Chemistry, 2018. Vol. 44. No. 5. pp. 433-439. DOI: 10.1134/S1087659618050103.
21. Федоренко Н.Ю., Мякин С.В., Франк В.М., Долгий А.С, Христюк Н.А., Полякова И.Г., Калинина М.В., Шилова О.А. Влияние условий синтеза ксерогелей в системе ZrO2-Y2O3-CeO2 на свойства керамики на их основе // Физика и химия стекла. 2020. №2. С. 206-212.
22. Ковалько Н.Ю., Калинина М.В., Суслов Д.Н., Галибин О.В., Юкина Г.Ю., Арсентьев М.Ю., Шилова О.А. Исследование влияния биокерамических образцов на основе t-ZrO2 на состояние мышечной и соединительной тканей экспериментальных животных при внутримышечном введении. // Перспективные материалы, 2019, №5, с. 41-49.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения многослойных металлокерамических покрытий на поверхности эндопротезов | 2021 |
|
RU2790959C1 |
| СПОСОБ ПОЛУЧЕНИЯ КЕРАМИКИ НА ОСНОВЕ ДИОКСИДА ЦИРКОНИЯ ДЛЯ РЕСТАВРАЦИОННОЙ СТОМАТОЛОГИИ | 2013 |
|
RU2536593C1 |
| Способ получения нанопористой керамики на основе муллита | 2020 |
|
RU2737298C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТОЙ БИОАКТИВНОЙ КЕРАМИКИ НА ОСНОВЕ ОКСИДА ЦИРКОНИЯ | 2015 |
|
RU2595703C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТЫХ МЕМБРАН НА ОСНОВЕ ДИОКСИДА ЦИРКОНИЯ ДЛЯ ФИЛЬТРАЦИИ ЖИДКОСТЕЙ И ГАЗОВ | 2017 |
|
RU2640546C1 |
| Способ получения остеопластического дисперсного биокомпозита | 2020 |
|
RU2741015C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОАКТИВНОЙ КЕРАМИКИ НА ОСНОВЕ ДИОКСИДА ЦИРКОНИЯ | 2021 |
|
RU2771017C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЛОТНОЙ НАНОКЕРАМИКИ НА ОСНОВЕ ОКСИДА АЛЮМИНИЯ В СИСТЕМЕ AlO-ZrO(YO) | 2018 |
|
RU2685604C1 |
| Способ жидкофазного синтеза многокомпонентного керамического материала в системе ZrO-YO-GdO-MgO для создания электролита твердооксидного топливного элемента | 2015 |
|
RU2614322C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИСПЕРСНЫХ МЕЗОПОРИСТЫХ ПОРОШКОВ НА ОСНОВЕ ОКСИДА АЛЮМИНИЯ ДЛЯ НОСИТЕЛЕЙ КАТАЛИЗАТОРОВ | 2018 |
|
RU2665038C1 |

Изобретение относится к медицине, конкретно к технологии получения биосовместимых композитных материалов, которые могут быть использованы для изготовления костных имплантатов в восстановительной хирургии. Жидкофазный направленный синтез порошков-прекурсоров в системе ZrO2-Y2O3-Al2O3 осуществляют путем выбора в качестве исходных реагентов солей ZrO(NO3)2⋅2H2O, Y(NO3)3⋅5H2O и Al(NO3)3⋅9H2O, из которых приготавливают разбавленные растворы и осуществляют двухэтапное осаждение гидроксидов из соответствующих солей водным раствором аммиака NH4OH до полного осаждения всех гидроксидов, смешения и получения осадка с высокой степенью гомогенности. Гелеобразный осадок фильтруют и подвергают быстрому замораживанию при -25°С в течение 24 часов, после чего синтезированный порошок состава [(ZrO2)0,97(Y2O3)0,03]0,8(Al2O3)0,2 высушивают и подвергают термообработке при 800°С. К синтезированному порошку добавляют оптимальную композицию порообразующей добавки с содержанием 10 мас.% гидроксиапатита кальция Са10(PO4)6(ОН)2 и 30 мас.% (NH4)2CO3, после чего полученные смеси нанопорошков формуют в компакты методом холодного одноосного прессования при давлении 100 МПа и спекают на воздухе при 1300°C с изотермической выдержкой в 2 ч и скоростью нагрева - 350-400°/ч. Заявленный способ обеспечивает синтез и получение на основе нанопорошков состава [(ZrO2)0,97(Y2O3)0,03]0,8(Al2O3)0,2 высокопористой прочной керамики медицинского назначения для заместительной хирургии и трансплантологии. 1 табл., 4 ил.
Способ получения биосовместимой пористой керамики на основе диоксида циркония для эндопротезирования включает несколько стадий: жидкофазный направленный синтез порошков-прекурсоров, введение порообразующих добавок, консолидация нанопорошков для получения итоговой керамики заданного химического состава, при этом жидкофазный направленный синтез порошков-прекурсоров в системе ZrO2-Y2O3-Al2O3 осуществляют путем выбора в качестве исходных реагентов солей ZrO(NO3)2⋅2H2O, Y(NO3)3⋅5H2O и Al(NO3)3⋅9H2O, из которых приготавливают разбавленные растворы и осуществляют двухэтапное осаждение гидроксидов из соответствующих солей водным раствором аммиака NH4OH до полного осаждения всех гидроксидов, смешения и получения осадка с высокой степенью гомогенности, затем гелеобразный осадок фильтруют и подвергают быстрому замораживанию при -25°С в течение 24 часов, после чего синтезированный порошок состава [ZrO2)0,97(Y2O3)0,03]0,8(Al2O3)0,2 высушивают и подвергают термообработке при 800°С, затем осуществляют введение порообразующих добавок, для чего с помощью механического смешения к синтезированному порошку добавляют оптимальную композицию порообразующей добавки с содержанием 10 мас.% гидроксиапатита кальция Ca10(PO4)6(OH)2 ГАП и 30 мас.% (NH4)2СО3, после чего для получения итоговой керамики заданного химического состава полученные смеси нанопорошков формуют в компакты методом холодного одноосного прессования при давлении 100 МПа и спекают на воздухе при 1300°С с изотермической выдержкой в 2 ч и скоростью нагрева - 350-400°/ч.
| СПОСОБ ПОЛУЧЕНИЯ ДИСПЕРСНЫХ МЕЗОПОРИСТЫХ ПОРОШКОВ НА ОСНОВЕ ОКСИДА АЛЮМИНИЯ ДЛЯ НОСИТЕЛЕЙ КАТАЛИЗАТОРОВ | 2018 |
|
RU2665038C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТОЙ КЕРАМИКИ С БИМОДАЛЬНЫМ РАСПРЕДЕЛЕНИЕМ ПОРИСТОСТИ | 2017 |
|
RU2691207C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТОГО КЕРАМИЧЕСКОГО БИОМАТЕРИАЛА НА ОСНОВЕ ДИОКСИДА ЦИРКОНИЯ | 2015 |
|
RU2585291C1 |
| JP 2018524251 A, 30.08.2018 | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
Авторы
Даты
2021-01-29—Публикация
2020-06-29—Подача