Область изобретения
Данное изобретение относится к области медицины. Более конкретно, данное изобретение касается производных темозоломид-8-карбоксилата, способа их получения, композиций на их основе, а также применения производных и композиций в производстве лекарственного средства для лечения опухоли, конкретно применения соединения и композиции в препарате для перорального или трансдермального применения, предназначенного для лечения опухоли, такой как карцинома кожи, карцинома мозга и лимфома.
Уровень техники
Темозоломид (в данном описании имеет название "ТМЗ"), алкилирующее средство для лечения карциномы, обладает противоопухолевой биологической активностью широкого спектра действия [L.H.Tsang, et al. Cancer Chemother Pharmacol. 27 (1991): 342-346] и, в частности, обладает биологической активностью, пригодной для лечения нейроглиомы (карцинома мозга) и злокачественной меланомы (карцинома кожи). В некоторых западных странах ТМЗ в капсулах зарегистрирован для применения в лечении злокачественной нейроглиомы. WO 0057867 описывает способ применения ТМЗ в циклический схеме. ТМЗ в капсулах также зарегистрирован для клинического применения в Китае. Фаза II клинических испытаний показала, что ТМЗ обладает способностью излечивать злокачественную меланому [N.M.Bleehen, et al. J. Clin. Oncol. 13 (1995): 910-913], а недавние клинические испытания фазы III показали, что, с точки зрения лечения злокачественной меланомы, ТМЗ обладает такой же активностью, как дакарбазин [M.R.Middleton, et al. J. Clin. Oncol. 18 (2000): 158-166], даже с подобными побочными эффектами, такими как лейкоцитопения, тошнота, рвота, выпадение волос, красная сыпь и запор. Кроме того, пероральное введение ТМЗ продемонстрировало ограничивающую дозу миелотоксичность [А.M.Heimberger, et al. Clin. Can. Res. 6 (2000): 4148-4153]. Предыдущее исследование различных лекарственных форм продемонстрировало, что интратекальное инъекционное введение раствора ТМЗ может уменьшить побочные эффекты [J.H.Sampson, et al. Clin. Can. Res. 5 (1999): 1183-1188]. По-видимому, препарат ТМЗ для трансдермального введения является идеальным для излечения карциномы кожи, особенно на ранних стадиях. Несколько исследований показали, что местное применение торемифена в месте карциномы может обеспечивать высокие местные концентрации при снижении системной концентрации [L.Soe, et al. Cancer Chemother. Pharmacol., 39 (1997): 513-520], что способствует снижению системной токсичности.
В целом, подкожное введение обусловливается как барьером кожи, так и физико-химическими свойствами лекарственного средства. Нестабильность и нерастворимость указанного лекарственного средства препятствуют введению его в лекарственные формы. Например, опубликованное в WO 0057867 исследование показало, что неспособность лекарственного средства проникать сквозь искусственную кожу (силиконовая мембрана), кожу человека и кожу крысы делает невозможным введение данного лекарственного средства в лекарственные формы для трансдермального введения. Ввиду этого сфера применения ТМЗ будет в существенной мере ограничена.
Раньше с целью модификации структуры были синтезированы многочисленные производные, большинство из которых касалось замены группы при атоме азота №3 и модификации группы при атоме азота амидной группы №8. Общая формула, описанная в ЕР 0252682 (1987), заявляет метил-, этил-, пропил- и бутилтемозоломид-8-карбоксилаты, но не раскрывает их фармакологическое действие и активность, с точки зрения лечения различных видов карциномы.
С другой стороны, соединения имидазо[5,1-d]-1,2,3,5-тетразин-4-она, обычно представленные ТМЗ, имеют общую особенность чрезвычайно низкой растворимости; они с трудом растворяются в распространенных растворителях, таких как этилацетат, дихлорметан и вода. Они демонстрируют слабую растворимость (приблизительно 1~5%) в смеси органического растворителя и воды, например в водном растворе уксусной кислоты, ацетонитрила, ацетона, метанола или этанола, с концентрацией 1~10%. Даже в апротонном полярном растворителе ДМСО их растворимость составляет приблизительно 5%. Другой особенностью данных соединений является их нестабильность, что сказывается не просто в их чувствительности к действию света, но более того, в их чувствительности к щелочным средам со значением рН более 7 и средам, которые содержат нуклеофильные группы, например соединения, содержащие амидогенные, гидроксильные и меркаптогруппы. Например, среда со значением рН более 7 приводит к быстрому разложению и изменению цвета (красный) указанных соединений; то же может происходить в метаноле и этаноле. Таким образом, применение метанола и этанола как солюбилизаторов в производстве препаратов является ограниченным. Следовательно, в высокой степени желательным выглядит создание нового биологически активного соединения и поиск способов повышения его стабильности и растворимости для использования в фармацевтической промышленности.
Подробное описание изобретения
Таким образом, объектом данного изобретения является получение производных 3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата общей формулы (I) и способы их получения, а также композиции, содержащие указанные производные и способы получения таких композиций.
Изобретателями было обнаружено, что производные 3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата общей формулы (I) и содержащие их композиции обладают противоопухолевой активностью и могут применяться для лечения различных видов карциномы, особенно карциномы кожи, карциномы мозга и лимфатической карциномы, и т.п. Таким образом, другим объектом изобретения является применение производных 3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата общей формулы (I) и содержащих их композиций в производстве лекарственных средств для лечения различных видов карциномы, где указанные виды карциномы включают карциному кожи, карциному мозга и лимфатическую карциному, и т.п.
Другой объект изобретения заключается в создании разнообразных препаратов, обладающих биологической противоопухолевой активностью и содержащих производные темозоломид-8-карбоксилата общей формулы (I) как активный(е) ингредиент(ы), особенно препаратов для перорального применения и трансдермальных пластырей для местного применения (проникновение сквозь кожу). Указанные трансдермальные пластыри для местного применения включают пластырь с контролируемым высвобождением матричного типа, пластырь с контролируемым высвобождением по типу резервуара твердого вещества или пластырь с контролируемым высвобождением по типу резервуара жидкого вещества.
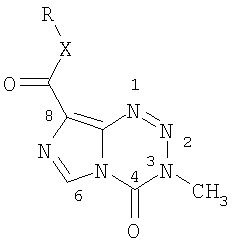
Структура указанного 3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата по данному изобретению представлена общей формулой (I) следующим образом:
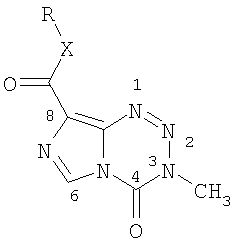
где Х представляет собой О или S;
R представляет собой замещенный или незамещенный С3~С10 алкил с неразветвленной или разветвленной цепью, С3~С10 циклоалкил, С3~С10 алкенил с неразветвленной или разветвленной цепью или С3~С10 алкинил с неразветвленной или разветвленной цепью;
Дополнительно, R может содержать заместитель(и), где указанные заместитель(и) могут представлять собой С1~С6 алкил, С1~С6 алкокси, С1~С6 алкилтиогрупу, С1~С6 алкиламиногрупу, фенил или фенил, замещенный галогеном.
Предпочтительно, X представляет собой О.
В приведенном выше определении термин С3~С10 алкил с неразветвленной или разветвленной цепью в данном описании представляет собой насыщенный углеводородный радикал с неразветвленной или разветвленной цепью, содержащий 3-10 атомов углерода, например пропил, бутил, амил, гексил, гептил, октил, нонил или децил и т.п., и все их изомеры, такие как изопропил, изобутил, трет-бутил, изо-гексил или изо-гептил, и т.д. Предпочтительно, R выбран из группы, состоящей из метила, этила, пропила, изопропила, н-бутила, 1-метил-пропила, 2-метил-пропила, амила, 1-метил-бутила, 2-метил-бутила, 3-метил-бутила, гексила, 1-метил-амила, 2-метил-амила, 3-метил-амила, 4-метил-амила, гептила, 1-метил-гексила, 2-метил-гексила, 3-метил-гексила, 4-метил-гексила, 5-метил-гексила, октила, 1-метил-гептила, 2-метил-гептила, 3-метил-гептила, 4-метил-гептила, 5-метил-гептила, 6-метил-гептила, 1-этил-пропила, 1-этил-бутила, 1-этил-амила, 2-этил-амила или 3-этил-амила. Более предпочтительно, R представляет собой н-гексил, изогексил и циклогексил. Наиболее предпочтительно, R представляет собой н-гексил.
В соответствии с описанными выше группами производные ТМЗ-8-карбоновой кислоты включают:
метил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
этил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
пропил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
бутил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
1-метил-бутил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
1-этил-бутил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
1-этил-пропил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
1-этил-амил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
1-метил-гексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
2-метил-гексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
3-метил-гексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
4-метил-гексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
5-метил-гексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
1-метил-гептил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
2-метил-гептил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
3-метил-гептил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
4-метил-гептил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
5-метил-гептил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
6-метил-гептил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
амил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
н-гексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
циклогексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
изогексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат;
гептил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат и
октил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат.
Более предпочтительными являются н-гексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат, изогексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат и циклогексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат; наиболее предпочтительным является н-гексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат.
В приведенном выше определении общей формулы термин С3~С10 циклоалкил в данном описании обозначает циклический насыщенный углеводородный радикал, содержащий 3-10 атомов углерода, такой как циклопропил, циклобутил, циклоамил, циклогексил, циклогептил, циклооктил, циклононил или циклодецил, и т.д.
В приведенном выше определении общей формулы термин С3~С10 алкенильная цепь обозначает углеводородный радикал, содержащий 1, 2 или 3 ненасыщенных двойных связи и 3-10 атомов углерода, такой как пропенил, бутенил, пентенил, гексенил, гептенил и гептадиенил, и т.д.
В приведенном выше определении общей формулы термин С3~С10 алкинильная цепь обозначает углеводородный радикал, содержащий 1, 2 или 3 ненасыщенных тройных связи и 3-10 атомов углерода, такой как пропинил, бутинил, пентинил, гексинил и гептинил, и т.д.
В приведенном выше определении общей формулы термин С1~С6 алкил, как определено выше, обозначает алкил с неразветвленной или разветвленной цепью, содержащий 1-6 атомов углерода, такой как метил, этил, пропил, бутил, амил, гексил и т.п., и также все их изомеры.
В приведенном выше определении общей формулы термин С1~С6 алкокси обозначает алкил, приведенный выше, содержащий атом кислорода, такой как метокси, этокси, пропокси, бутокси, пентокси, гексилокси и т.п., а также все их изомеры.
В приведенном выше определении общей формулы термин С1~С6 алкилтиогрупа обозначает алкоксил, приведенный выше, в котором атом кислорода заменен на атом серы, такой как метилтио, этилтио, пропилтио, бутилтио, амилтио, гексилтио и т.п., а также все их изомеры.
В приведенном выше определении общей формулы термин С1~С6 алкиламиногрупа обозначает аминогруппу, содержащую один или два алкильных радикала, как определено выше, такую как метиламино, этиламино, диметиламино, бутиламино, амиламино, гексиламино и т.п., а также все их изомеры.
В приведенном выше определении общей формулы термин галоген обозначает фтор, хлор, бром или йод.
Соединения общей формулы (I) получают по следующему способу.
При перемешивании ТМЗ смешивают с концентрированной серной кислотой. Натрия нитрит растворяют в воде и потом по каплям добавляют к описанной выше смеси на ледяной бане при температуре ниже 15°С, после чего перемешивают при комнатной температуре в течение ночи. К полученной смеси непрерывно добавляют лед и охлаждают на ледяной бане в течение 1 час. Полученный твердый продукт ТМЗ кислоту отделяют фильтрацией и сушат под вакуумом.
Смесь безводных ДМФА и ТГФ впрыскивают в колбу, заполненную ТМЗ кислотой и Pybrop, и перемешивают до полного растворения твердого вещества, после чего в условиях ледяной бани добавляют 4-диметиламинопиридин (DMAP). Далее соответствующее количество безводного углеводородного спирта или меркаптана впрыскивают в полученную смесь и дают реакции протекать в течение 30 минут, после чего перемешивают при комнатной температуре в течение ночи. После завершения реакции суспензию фильтруют сквозь воронку Бюхнера. Полученный маточник подвергают дистилляции; к остатку добавляют лед и экстрагируют этилацетатом (10 мл×3). Этилацетатные фракции объединяют и сушат с помощью безводного магния сульфата. Этилацетат удаляют с помощью роторного испарителя с получением остатка. Остаток, который представляет собой конечный продукт, далее очищают на колонке с силикагелем, после испарения растворителей получают целевое соединение.
Продукт идентифицирован с помощью данных ИК-спектра, 1Н-ЯМР, 13С-ЯМР и МС.
В соответствии с другим аспектом изобретения предлагаются композиции, содержащие указанные производные 3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата, и способы их получения.
Фармацевтические композиции по изобретению обладают противоопухолевой активностью, причем указанные композиции содержат терапевтически эффективное количество одного или больше соединений общей формулы (I), как активные ингредиенты, вместе с традиционными фармацевтически приемлемыми носителями. Указанные фармацевтически приемлемые носители представляют собой носители, известные из уровня техники, такие как жидкие или твердые вспомогательные вещества, разбавители, увлажняющие средства, консерванты, средства для маскировки вкуса и красители, и т.д.
Композиции по изобретению включают одно или больше соединений приведенной общей формулы (I) как активный(е) ингредиент(ы). Предпочтительные соединения общей формулы (I) выбраны из группы, которая состоит из:
метил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
этил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
пропил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
бутил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
1-метил-бутил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
1-этил-бутил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
1-этил-пропил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
1-этил-амил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
1-метил-гексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
2-метил-гексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
3-метил-гексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
4-метил-гексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
5-метил-гексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
1-метил-гептил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
2-метил-гептил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
3-метил-гептил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
4-метил-гептил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
5-метил-гептил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
6-метил-гептил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
амил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
н-гексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
изо-гексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
циклогексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата,
гептил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата и
октил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата.
Более предпочтительными соединениями являются н-гексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат, изо-гексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат и циклогексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат. Наиболее предпочтительным соединением является н-гексил-3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат.
Дополнительно, композиции по изобретению могут включать фармацевтически приемлемые компоненты кислотной природы, например вспомогательные вещества кислотной природы, которые используются в фармацевтической промышленности, такие как олеиновая кислота, стеариновая кислота, линоленовая кислота, фумаровая кислота, бензойная кислота, винная кислота, сорбиновая кислота, молочная кислота, лимонная кислота, уксусная кислота, ЭДТА, и т.д. Такие субстанции кислотной природы выполняют роль стабилизатора для соединений общей формулы (I).
Изобретателями также было выявлено, что растворимость и количество в среде ТМЗ-8-карбоксилата, активного ингредиента композиций, будет увеличиваться при добавлении 0,5~20% (масс.), преимущественно 1~10% (масс.), фармацевтически приемлемого вторичного спирта или третичного спирта на основе общей массы композиции. Причем предпочтительным спиртом является С3~С8 вторичный спирт или третичный спирт, такой как изопропанол, изобутиловый спирт, изоамиловый спирт, трет-бутиловый спирт или их эфирные производные, такие как триглицерид и полигликолевый эфир. Между тем указанные субстанции могут использоваться как солюбилизатор для композиции и лекарственных форм другого типа, содержащих производные ТМЗ-8-карбоксилата или другие имидазо[5,1-d]-1,2,3,5-тетразин-4-оны.
Композиция по изобретению может быть изготовлена в любой из традиционных фармацевтических лекарственных форм. Конкретно, лекарственные формы разрабатывают с учетом следующих факторов: желательный эффект, свойства активных ингредиентов, дозировка, возраст, пол и состояние заболевания пациентов. Указанные лекарственные формы включают лекарственные формы, пригодные для введения, например таблетку, пилюлю, диспергированный порошок, капсулу, гранулы, эмульсию, раствор, суспензию, сироп, твердый суппозиторий для вагинального или ректального введения, а также пластырь для местного применения. Предпочтительной является трансдермальная лекарственная форма для местного применения или лекарственная формула для перорального применения. Наиболее предпочтительной является трансдермальная лекарственная форма для местного применения.
Композиция и все ее лекарственные формы по изобретению могут быть изготовлены любым способом, хорошо известным в фармацевтической отрасли.
В соответствии с изобретением одна из лекарственных форм, пригодных для введения производных 3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата, представляет собой препарат для перорального применения, в том числе твердые и жидкие препараты, в частности твердые препараты для перорального применения включают таблетку, пилюлю, диспергированный порошок, капсулу и гранулы, и т.д. В ходе процесса изготовления твердых лекарственных форм биологически активный агент, производные ТМЗ-8-карбоксилата, может не быть смешан с другими ингредиентами или может быть смешан как минимум с одним инертным разбавителем, в том числе кальция карбонатом, крахмалом, альгиновой кислотой или лактозой, и т.д., а также с субстанцией кислотной природы, такой как фумаровая кислота, винная кислота, сорбиновая кислота и лимонная кислота, и т.д., которые могут быть добавлены в лекарственную форму. Кроме перечисленных выше компонентов, лекарственные формы могут включать другие компоненты, например смазующее вещество, такое как стеарат магния. Кроме того, производные ТМЗ-8-карбоксилата могут быть введены в жидкие лекарственные формы для перорального применения, в том числе эмульсию, раствор, суспензию и сироп, и т.д. В упомянутых выше жидких лекарственных формах всегда присутствует водная жидкость, которая содержит поверхностно-активное вещество или жидкий парафин как инертные разбавители. Кроме инертных разбавителей, также могут быть включены другие добавки, например увлажняющие агенты, суспендирующие агенты, такие как поливинилпиролидон (ПВП), подсластители, агенты для маскировки вкуса, консерванты и ароматизаторы.
Другой фармацевтической лекарственной формой, пригодной для введения производных 3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата, является суппозиторий, в том числе твердый суппозиторий для вагинального и ректального введения. Кроме традиционных вспомогательных веществ, с целью обеспечения пролонгированного и контролируемого высвобождения указанный суппозиторий обычно включает полимер, который разлагается в биологической среде, такой как полимолочная кислота (PLGA), полиангидрид и поли(смешанный ангидрид) (полиангидридный сополимер поли(1,3-бис-(n-карбоксифеноксипропан)-ко-(себациновый ангидрид) или (CPP:SA)).
С учетом свойств производных 3,4-дигидро-3-метил-4-оксоимидазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилата, способных проникать сквозь кожу, наиболее предпочтительными лекарственными формами для них являются трансдермальные лекарственные формы для местного применения, в том числе настойка, суспензия, эмульсия, мазь, гель, суппозиторий, пленка и пластырь, и т.д. Как правило, трансдермальные лекарственные формы для местного применения включают такие вспомогательные вещества, как масляная среда, поверхностно-активное вещество и т.п.
Указанную масляную среду, которая используется в трансдермальных лекарственных формах для местного применения, выбирают из группы, состоящей из олеиновой кислоты, изопропилмиристата (ИПМ), лауриновой кислоты, воска, цетилового спирта, стеарилового спирта, жидкого парафина, вазелина, безводного ланолина, стеариновой кислоты, хлопкового масла, касторового масла, линоленовой кислоты и триглицерида, и т.п. Указанное широко применяемое поверхностно-активное вещество выбирают из группы, состоящей из фосфолипида, субстанции по типу Myrj, субстанции по типу Brij, субстанции по типу Твина, акациевой камеди, трагакантовой камеди, глютина и витамина Е ТПГС (BE ТПГС) и т.д.
Предпочтительные трансдермальные пластыри ТМЗ-8-карбоксилата для местного применения делятся на две группы: резервуарного и матричного типа. Матричный тип может быть разделен на единую матрицу (AM) и полиматрицу (РМ). Тип резервуара включает систему резервуара жидкости (LRS) и систему резервуара твердого вещества (SRS), которая состоит из многослойной липкой (MLA) и многослойной полимерной матрицы (MLM). В основном, трансдермальные лекарственные формы ТМЗ-8-карбоксилатов для местного применения как матричного типа, так и резервуарного типа в существенной мере включают: матрицу, полимерные материалы, резервуар лекарственного средства (раствор или суспензию лекарственного средства), замедляющую скорость высвобождения мембрану, чувствительные к давлению клейкие вещества (PSAs) и слой высвобождения для защиты PSAs. Дополнительное обсуждение приведено ниже.
Пластырь по типу резервуара твердой жидкости: матрица представляет собой прозрачную и стабильную микроэмульсию и ее лекарственные формы, образованные водной фазой, масляной фазой и поверхностно-активными веществами в различных соотношениях, которые подразделяются на пластырь по типу резервуара жидкости и пластырь по типу резервуара твердого вещества. В указанном пластыре по типу резервуара твердого вещества в качестве масляной фазы может быть выбрана олеиновая кислота или изопропилмиристат (ИПМ), а также лауриновая кислота, воск, цетиловый спирт, стеариловый спирт, жидкий парафин, вазелин, безводный ланолин, стеариновая кислоты, хлопковое масло, касторовое масло и линоленовая кислота могут быть выбраны в качестве масляной фазы.
Предпочтительная масляная фаза для пластыря по типу резервуара твердого вещества ТМЗ-8-карбоксилата по изобретению представляет собой изопропилмиристат (ИПМ) или олеиновую кислоту, предпочтительная водная фаза представляет собой воду и предпочтительное поверхностно-активное вещество представляет собой BE ТПГС и лимонную кислоту.
Пластырь с контролируемым высвобождением по типу резервуара для жидкости изготавливают путем термического плавления непроницаемой матрицы (или так называемой матрицы), жидкого лекарственного средства, замедляющей скорость высвобождения мембраны, PSAs и слоя высвобождения.
Структура каждой части пластыря по типу резервуара жидкости ТМЗ-8-карбоксилата по изобретению является следующей.
Матрица, то есть непроницаемая матрица, в целом может быть синтезирована из полимерных материалов, которые обладают проницаемостью или непроницаемостью, таких как полиэстер, полиэтилен, поливинилхлорид (ПВХ), поли(винилиденхлорид) (ПВДХ) и полиуретан и т.д., а также из природных полимерных материалов, таких как хлопок или шерсть и т.п. Матрица по изобретению может быть выбрана из группы, которая состоит из ПВХ, нитроглицерина (Transdermal®), полидиметилсилоксана (Nitrodisc®), ПВП, поливинилового спирта (Nitro-Dur® I), комплекса полиэтеноксида, ПЭГ, всех производных ПЭГ, таких как монометиловый эфир полиэтиленгликоля или диметиловый эфир полиэтиленгликоля, полиэтиленгликоль сукцинат (ТПГС) и BE ТПГС и т.д. Предпочтительными являются полиэтилен, поливинилхлорид, ПВДХ, полиуретан или хлопок.
Предпочтительно, замедляющая скорость высвобождения мембрана представляет собой мембрану, образованную сополимером этилена и винилацетата, или гомогенные мембраны, такие как мембрана из полиуретана и мембрана из гликольдиацетата. PSAs представляет собой уникальную биоадгезивную, преимущественно чувствительную к давлению полисилоксановую или чувствительную к давлению полиакрилатную смолу.
Пластырь с контролируемым высвобождением по типу резервуара по изобретению может быть изготовлен по способу, который включает следующие стадии: взвешивание соответствующего количества н-гексил-ТМЗ-8-карбоксилата и измельчение его до состояния тонкого порошка, добавление водной фазы, такой как вода, масляной фазы, такой как олеиновая кислота и т.д., и поверхностно-активного вещества, такого как BE ТПГС и т.д.; тщательное смешивание; добавление измельченного лекарственного средства, помол полученной смеси с образованием микроэмульсии; с последующим добавлением замедляющей скорость высвобождения мембраны, такой как мембрана, образованная сополимером этилена и винилацетата, и соответствующего количества PSAs, тщательное перемешивание; дегазацию путем сохранения тепла с использованием водяной бани и распределение на полиэтиленовой матрице; сушку и разрезание на маленькие кусочки с получением целевого продукта.
Указанные пластыри матричного типа по изобретению с единой клейкой матрицей изготавливают по способу, который включает следующие стадии: диспергирование лекарственного средства в PSAs, из которого будет осуществляться контролируемое высвобождение лекарственного средства. Особенности системы с контролируемым высвобождением: более тонкий объем, более простой технический процесс и более легкая промышленная воспроизводимость. Состав вспомогательных веществ клейкой матрицы лекарственного средства по изобретению выбирают из группы, состоящей из природных или синтетических полимеров, в том числе поливинилхлорида, полиакрилата, полидиметилсилоксана, и гидрофильных полимеров, таких как ПВП, поливиниловый спирт, водный гель, изготовленный из геля (например, Prostep®), комплекса ПВП и полиэтеноксида, ПЭГ и его производных, таких как монометиловый эфир полиэтиленгликоля или диметиловый эфир полиэтиленгликоля, полиэтиленгликоль сукцината и BE ТПГС. Предпочтительным является полиакрилат.
Обычно указанный ТМЗ-8-карбоксилат вводят в дозах 0,1~200 мг/кг массы тела/день, преимущественно 1~20 мг/кг массы тела/день.
Исследование растворимости в липидах, стабильности и растворимости ТМЗ-8-карбоксилата
Исследования показали, что по сравнению с ТМЗ растворимость производных ТМЗ-8-карбоксилата в липидах является значительно лучшей. Например, если взять Log P в качестве стандарта, Log Р для ТМЗ составляет -0,66, тогда как Log P для н-гексил-ТМЗ-8-карбоксилата составляет 2,56. Это означает, что н-гексил-ТМЗ-8-карбоксилат представляет собой идеальное лекарственное средство для местного трансдермального применения (способ измерения Log Р см. в Leo and Hansch. Chemical Reviews 71 No.6, December 1971; Partition Coefficients and Their Uses, Leo A., Hansch C. and Elkins D.).
Изобретателями было обнаружено, что стабильность может быть существенно повышена в случае производных ТМЗ-8-карбоксилата отдельно или вместе с другими имидазо[5,1-d]-1,2,3,5-тетразин-4-онами в кислых условиях (рН 1~6,5), полученных добавлением фармацевтически приемлемых компонентов кислотной природы. Следовательно, стабильность активных ингредиентов будет в существенной мере повышаться, если производные ТМЗ-8-карбоксилата будут применяться как активные ингредиенты в жидкой лекарственной форме, такой как настойка, суспензия, эмульсия и инъекционные лекарственные формы, а также в твердой лекарственной форме, такой как мазь, суппозиторий и пленка. Указанные субстанции кислотной природы включают олеиновую кислоту, стеариновую кислоту, линоленовую кислоту, фумаровую кислоту, бензойную кислоту, винную кислоту, сорбиновую кислоту, молочную кислоту, лимонную кислоту, уксусную кислоту, ЭДТА и т.п.
Кроме того, изобретателями также было обнаружено, что растворимость и количество ТМЗ-8-карбоксилата, активного ингредиента композиции, в среде будет увеличиваться при добавлении 0,5~20% фармацевтически приемлемого вторичного спирта или третичного спирта, такого как изопропанол, изобутиловый спирт, изоамиловый спирт, трет-бутиловый спирт или их эфирные производные, такие как триглицерид, полигликолевый эфир. Соответственно, вторичный спирт или третичный спирт, такой как изопропанол, изобутиловый спирт, изоамиловый спирт, трет-бутиловый спирт и т.д., может использоваться как солюбилизатор в композиции, содержащей производные ТМЗ-8-карбоксилата и другие имидазо[5,1-d]-1,2,3,5-тетразин-4-оны.
Полученные данные подтверждают, что изобретение обеспечивает противоопухолевую композицию, которая содержит одно или больше производных ТМЗ-8-карбоксилата, фармацевтически приемлемые вещества кислотной природы, необязательно содержит фармацевтически приемлемый вторичный спирт или третичный спирт и их производные, а также фармацевтически приемлемые вспомогательные вещества и/или носители. Изобретение также предлагает разнообразные препараты, изготовленные на основе композиции по изобретению.
Следующие эксперименты по исследованию фармацевтической активности метил-ТМЗ-8-карбоксилата, бутил-ТМЗ-8-карбоксилата и н-гексил-ТМЗ-8-карбоксилата in vitro против карциномы приведены с целью иллюстрации их эффективности.
Изучение способности ТМЗ-8-карбоксилата убивать опухолевые клетки in vitro
Эксперимент проводили для метил-ТМЗ-8-карбоксилата, бутил-ТМЗ-8-карбоксилата, н-гексил-ТМЗ-8-карбоксилата и ТМЗ кислоты, которая известна как активное соединение против карциномы, с использованием инъекции фторурацила (10 мл: 0,25 г, приобретен у Xudong Pharmaceutical Co. Ltd, номер серии 000612) в качестве лекарственного средства для положительного контроля. Штаммы раковых клеток, которые использовали в экспериментах, включали НСТ-8 (клетки карциномы ободочной кишки человека), А549 (клетки карциномы легких человека), MCF-7 (клетки карциномы молочной железы человека), Bel7402 (клетки карциномы печени человека), BGC-823 (клетки карциномы желудка человека) и МV3 (клетки меланомы человека).
Лекарственные средства и реактивы
ТМЗ кислота представляет собой белый порошок; метил-ТМЗ-8-карбоксилат, бутил-ТМЗ-8-карбоксилат и н-гексил-ТМЗ-8-карбоксилат, белые чешуйные кристаллы получали по способу, описанному в Примере 2; фторурацил для инъекций (10 мл: 0,25 г): как лекарственное средство для позитивного контроля, производитель Xudong Pharmaceutical Co. Ltd, номер серии 000612; RPMI: производитель GIBCO; телячья сыворотка: производитель Sijiqing bio-engineer material Co. Ltd, Hangzhou и MTT: производитель Bebco.
Штаммы клеток
Все штаммы раковых клеток - НСТ-8, А549, MCF-7, Bel-7402, BGC-823, MV3 и В16 - были выращены и культуры переданы из Institute of Materia Medica, Chinese Academy of Medical Sciences и Peking Union Medical College.
Прибор: BIORAD 550 для меченых ферментов.
Метод
Использовали пробу восстановления соли тетразолия [3-(4,5-диметилтиазол-2-ил)-2,5-дифенил-тетразолия-бромид, МТТ]. Все выращенные клетки карциномы собирали, готовили суспензию клеток 1×104/мл в растворе для культивирования RPMI 1640, содержащем 10% телячьей сыворотки, и инокулировали в 96-ячейковые планшеты для культивирования по 100 мкл на ячейку (содержит 1000 раковых клеток). После 24 час культивирования в термосном инкубаторе с 5% СО2 при температуре 37°С добавляли лекарственные средства. В исследовании принимала участие группа холостого контроля, лекарственным средством для положительного контроля был фторурацил. Исследуемые лекарственные средства были разделены на пять групп с разными концентрациями, которые исследовались в трех параллельных повторениях. Культуры клеток помещали в термосный инкубатор с 5% СО2 при температуре 37°С для культивирования в течение 4 дней. Среду культивирования отбрасывали и добавляли 100 мкл раствора МТТ (0,4 мг/мл, приготовленный в RPMI 1640) на ячейку и продолжали культивирование в течение 4 час при температуре 37°С. Супернатант отбрасывали и добавляли 150 мкл диметилсульфоксида для растворения гранул Fomazan. После осторожного перемешивания измеряли значение оптической плотности с помощью прибора для меченых ферментов BIORAD 550 при длине волны 540 нм и длине волны сравнения 450 нм.
Результаты
Данные ингибирования клеток наносили на график и строили кривую зависимости "доза-реакция", с помощью которой вычисляли 50% ингибирующую концентрацию IC50 (см. Таблицу 1 и Таблицу 2).
Результат (см. Таблицу 1) продемонстрировал, что интервалы IC50 четырех лекарственных средств (метил-ТМЗ-8-карбоксилат, бутил-ТМЗ-8-карбоксилат, н-гексил-ТМЗ-8-карбоксилат и ТМЗ кислота) составляли для выбранных штаммов клеток 10~30 мкг/мл, причем не наблюдалось значительных отличий между ними, с точки зрения действия на клетки.
Влияние местного применения гексил-ТМЗ-8-карбоксилата на рост ксенотрансплантированой меланомы человека у голых мышей MV3
Гексил-ТМЗ-8-карбоксилат был выбран в качестве репрезентативного соединения для исследования влияния производных ТМЗ-8-карбоксилата на рост ксенотрансплантированой меланомы человека у голых мышей MV3.
Гексил-ТМЗ-8-карбоксилат растворяли в ДМСО с получением раствора 50 мг/мл. Осуществляли ксенотрансплантацию меланомы человека голым мышам BALB/c-nu и позволяли ей развиваться. Когда опухоль достигала объема 100-300 мм3, всех животных разделяли на две группы в соответствии с размером опухоли, по 8 мышей в каждой группе.
Из указанных двух групп одна представляла собой группу лекарственного средства, в которой осуществляли лечение нанесением раствора гексил-ТМЗ-8-карбоксилата; другая группа служила контролем, где опухоли развивались естественным образом.
В группе лекарственного средства его применяли путем нанесения в месте опухоли и окружающей области (2 см×2 см) дважды в день (один раз в субботу и воскресенье). Каждый раз, когда раствор высыхал, нанесение повторяли 1-2 раза. Средняя суточная доза введенного мыши гексил-ТМЗ-8-карбоксилата в целом составляла приблизительно 20 мг.
Объем опухоли у мыши измеряли дважды на неделю таким образом, чтобы наблюдать и регистрировать ее рост в динамике. Когда опухоли в контрольной группе достигли определенного объема, всех мышей забивали, опухоли извлекали и взвешивали, была вычислена степень ингибирования роста. Пролиферацию опухоли (Т/С (%)) вычисляли с использованием относительного объема опухоли в двух группах.
Объем опухоли (TV) вычисляли с помощью следующего уравнения:
Длина×ширина2÷2
Относительный объем опухоли вычисляли с помощью следующего уравнения:
Vt/Vo,
где Vo представляет собой TV, измеренный в точке времени, где животных распределяли в отдельные клетки, и Vt представляет собой TV, измеренный в дальнейшем в каждой точке времени.
t-Тест применяли для сравнения статистических различий между двумя группами для нескольких показателей, таких как масса опухоли, TV и RTV. Относительную скорость пролиферации опухоли (Т/С (%)) использовали как показатель противоопухолевой биологической активности, которую вычисляли следующим образом:

Критерии оценки эффекта:
Эффект оценивали с помощью статистического анализа. Эффект считали недостоверным, если Т/С (%) составляло более 60, и считали достоверным, если Т/С (%) составляло ≤60 при р<0,05.
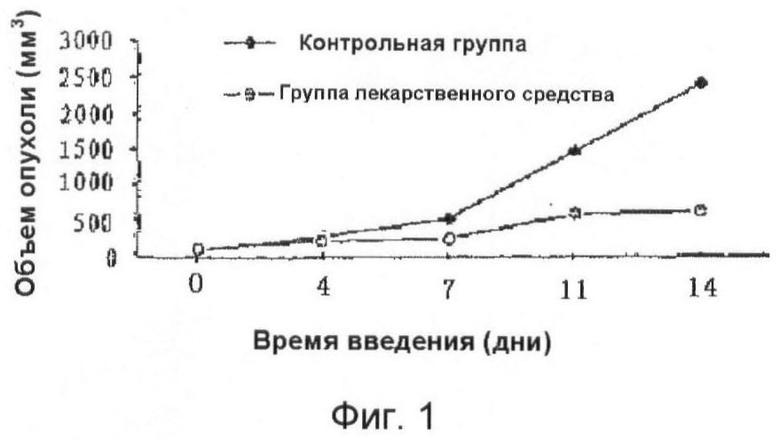
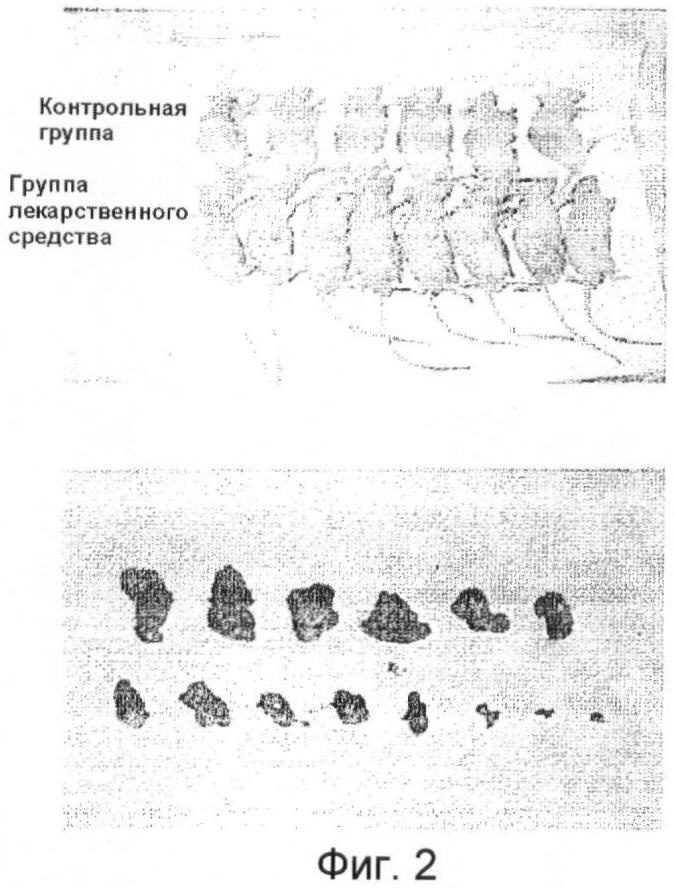
Результаты показали, что гексил-ТМЗ-8-карбоксилат осуществляет выраженное ингибирующее действие на рост различных видов карциномы у мышей и выраженное цитотоксическое действие на клетки карциномы, такие как меланома человека MV3; при ежедневном внешнем применении у мышей 20 мг указанного средства оказывали выраженный эффект ингибирования пересаженной карциномы. К концу эксперимента наблюдалось статистически значимое отличие массы и объема опухолей по сравнению с контрольной группой. Результаты можно увидеть на Фигурах 1, 2 и в Таблице 2. Фигура 1 демонстрирует влияние нанесения гексил-ТМЗ-8-карбоксилата на рост различных видов меланомы человека, которое можно увидеть из данных роста меланомы человека в группе лекарственного средства, который заметно ингибировался по сравнению с контрольной группой или группой отрицательного контроля. Фигура 2 демонстрирует реальное изображение мышей из двух групп. В верхней части изображения показаны мыши из контрольной группы, в нижней части - мыши из группы лекарственного средства. Верхняя часть второй фотографии демонстрирует вид опухолей в контрольной группе, а нижняя часть демонстрирует вид опухолей в группе лекарственного средства. В Таблице 2 показано влияние нанесения гексил-ТМЗ-8-карбоксилата на рост опухолей у мышей с MV3.
Краткое описание фигур
Фигура 1 представляет кривую роста опухоли, показывая ингибирующее влияние н-гексил-ТМЗ-8-карбоксилата на рост различных видов меланом человека.
Фигура 2 представляет реальное изображение тела мыши из группы исследуемого препарата и контрольной группы.
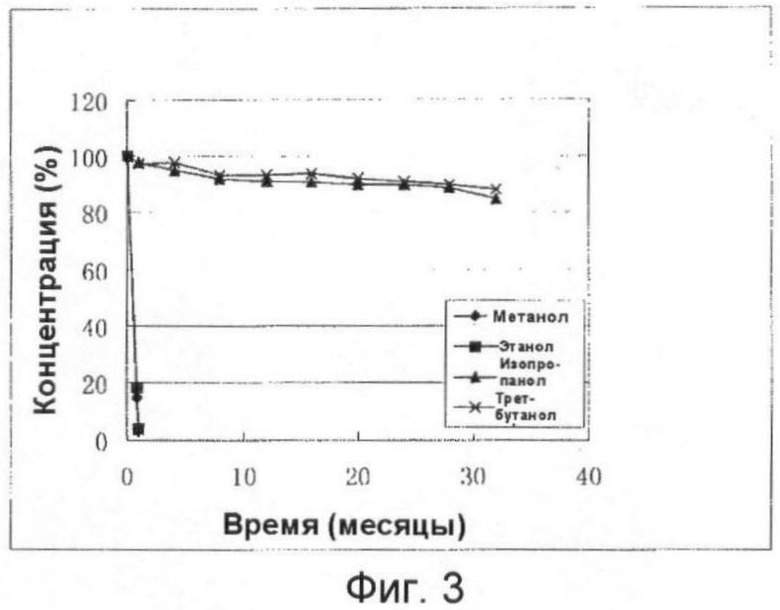
Фигура 3 демонстрирует результаты изучения стабильности н-гексил-ТМЗ-8-карбоксилата в широко применяемых спиртах.
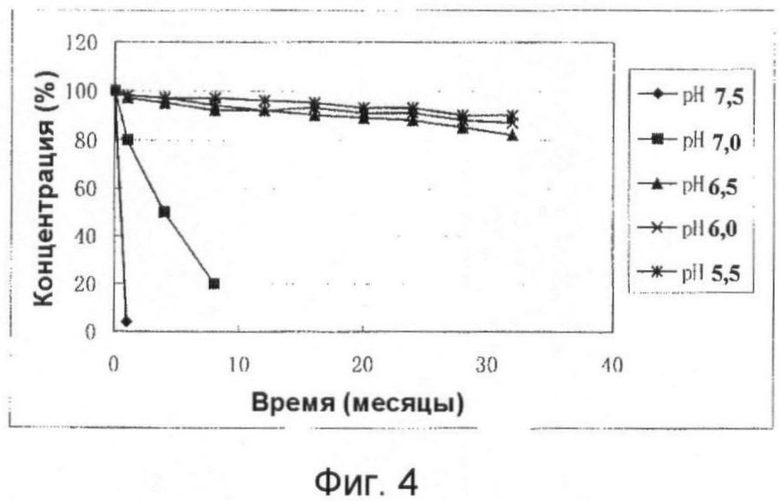
Фигура 4 демонстрирует влияние значения рН среды на стабильность н-гексил-ТМЗ-8-карбоксилата.
Предпочтительные варианты изобретения
Следующие примеры иллюстрируют изобретение без какого-либо сужения его границ.
Пример 1. Получение ТМЗ кислоты (ЕР 0252682)
При перемешивании ТМЗ (2,577 ммоль, 0,5 г) смешивают с концентрированной серной кислотой (4 мл). Натрия нитрит (9,4 ммоль, 0,65 г) растворяют в 2,6 мл воды и по каплям добавляют к описанной выше смеси на ледяной бане при температуре ниже 15°С, после чего перемешивают при комнатной температуре в течение ночи. К полученной смеси добавляют 10 г льда и охлаждают в течение 1 час на ледяной бане. Твердый продукт отделяют и сушат под вакуумом с получением 0,493 г ТМЗ кислоты. Выход составляет 98,6%.
Пример 2. Получение ТМЗ-8-карбоксилата
Смесь безводных ДМФА (2 мл) и ТГФ (3 мл) вводят в колбу, заполненную ТМЗ кислотой (1 ммоль, 0.195 г), полученной в соответствии с Примером 1, и Pybrop (1 ммоль, 0.466 г) и перемешивают до полного растворения твердого вещества, к которому в условиях ледяной бани добавляют 4-диметиламинопиридин (DMAP, 2 ммоль, 0.244 г). Далее в полученную смесь вводят соответствующее количество безводного углеводородного спирта или меркаптана 2,2 (ммоль) и дают реакции протекать в течение 30 минут, после чего перемешивают при комнатной температуре в течение ночи. После завершения реакции суспензию фильтруют сквозь воронку Бюхнера. Полученный маточный раствор подвергают дистилляции; к остатку добавляют 10 г льда и экстрагируют этилацетатом (10 мл×3). Этилацетатные фракции объединяют и сушат с помощью безводного магния сульфата. Этилацетат удаляют с помощью роторного испарителя с получением остатка. Затем остаток очищают на колонке с силикагелем и получают целевое соединение после испарения растворителя.
Продукт идентифицирован с помощью ИК-спектра, 1Н-ЯМР, 13С-ЯМР и МС. Типичные данные были такими, как показано ниже:
1. Метил-ТМЗ-8-карбоксилат
1Н ЯМР (d6-ДМСО/промилле) δ 8,86 (с, 1, Н-6), 3,90 (с, 3, СН 3-O), 3,87 (с, 3, СН 3-N)
13С ЯМР (d6-ДМСО/промилле) δ 161 (COO), 139 (C-4), 137 (C-6), 129 (C-9), 126 (C-8), 52,2 (ОСН2), 36,4 (NCH3)
νmax (KBr): 3489, 2961 (C-H), 1752 (С=O), 1727 (С=O), 1214 (С-O), 1062 (С-O), 828,556 см-1
МС: + ионизация электрораспылением (соотношение массы и заряда) = 232 [M+H]+, 214 [М+Н-H2O]+
2. Этил-ТМЗ-8-карбоксилат
1Н ЯМР (CDCl3/промилле) δ 8,45 (с, 1, Н-6), 4,52 (к, 2, J=7,1 Гц, СН 2-О), 4,04 (с, 3, СН 3-N), 1,45 (т, 3, J=7,1 Гц, СН2-СН 3)
13С ЯМР (d6-ДМСО/промилле) δ 161 (COO), 139 (C-4), 137 (C-6), 129 (C-9), 127 (C-8), 60,9 (ОСН2), 36,4 (NCH3), 14,3 (СН2 СН3)
νmax (KBr): 3478, 2991 (C-H), 1754 (C=O), 1700 (C=O), 1467 (C-O), 1258 (С-O), 1060 (С-O), 844,561 см-1
МС: + ионизация электрораспылением (соотношение массы и заряда) = 246 [М+
Н]+, 228 [М+Н-H2O]+
3. Пропил-ТМЗ-8-карбоксилат
1H ЯМР (CDCl3/промилле) δ 8,46 (с, 1, Н-6), 4,41 (т, 2, J=6,7 Гц, СН 2-О), 4,03 (с, 3, СН 3-N), 1,83 (секстет, 2, J=7,1 Гц, C-CH 2-C), 1,03 (т, 3, J=7,4 Гц, С-СН 3)
13С ЯМР (CDCl3/промилле) δ 160 (COO), 138 (C-4), 136 (C-6), 130 (C-9), 128 (C-8), 67,1 (OCH2), 36,5 (NCH3), 21,7 (CH2CH3), 8,87 (CH2 CH3)
νmax (KBr): 3122, 2960 (C-H), 1729 (C=O), 1700 (С=O), 1457 (С-O), 1200 (С-O), 1174 (С-O), 1052,942 см-1
МС: + ионизация электрораспылением (соотношение массы и заряда) = 260 [М+
Н]+, 242 [М+Н-Н2О]+
4. Бутил-ТМЗ-8-карбоксилат
1Н ЯМР (CDCl3/промилле) δ 8,45 (с, 1 Н-6), 4,45 (т, 2, J=7,1 Гц, СН 2-О), 4,03 (с, 3, СН 3-N), 1,79 (квинтет, 2, J=7,4 Гц, С-СН 2-С), 1,46 (секстет, 2, J=7,3 Гц, С-СН 2-СН3), 0,95 (т, 3, J=7,3 Гц, С-СН 3)
13С ЯМР (d6-ДМСО/промилле) δ 161 (COO), 139 (C-4), 137 (C-6), 129 (C-9), 127 (C-8), 64,5 (ОСН2), 36,4 (NCH3), 30,3 (OCH2 CH2), 18,7 (СН2СН3), 13,6 (СН2 СН3)
νmax (KBr): 3156, 2967 (C-H), 1746 (С=O), 1467 (С-O), 1261 (С-O), 1054 (С-O), 823,561 см-1
МС: + ионизация электрораспылением (соотношение массы и заряда) = 274 [М+
Н]+, 256 [M+H-H2O]+
5. Амил-ТМЗ-8-карбоксилат
1Н ЯМР (CDCl3/промилле) δ 8,46 (с, 1, Н-6), 4,45 (т, 2, J=7,0 Гц, СН 2-О), 4,03 (с, 3, СН 3-N), 1,79 (квинтет, 2, J=7,1 Гц, С-СН 2-С), 1,29-1,40 (м, 4, С-(СН 2)2-СН3), 0,96 (т, 3, J=6,9 Гц, С-СН 3)
13С ЯМР (d6-ДМСО/промилле) δ 161 (COO), 139 (C-4), 137 (C-6), 129 (C-9), 127 (C-8), 64,6 (OCH2), 36,4 (NCH3), 30,9 (ОСН2 СН2), 28,2 (O(СН2)2 СН2), 22,8 (СН2СН3), 14,0 (СН2 СН3)
νmax (KBr): 3136, 2967 (C-H), 1736 (C=O), 1459 (С-O), 1231 (С-O), 1154 (С-O),
923,761 см-1
МС: + ионизация электрораспылением (соотношение массы и заряда) = 288 [М+
Н]+, 270 [М+Н-Н2О]+
6. Гексил-ТМЗ-8-карбоксилат
1Н ЯМР (CDCl3/промилле) δ 8,49 (с, 1, Н-6), 4,45 (т, 2, J=6,9 Гц, СН 2-O), 4,04 (с, 3, СН 3-N), 1,79 (квинтет, 2, J=7,1 Гц, С-СН 2-С), 1,29-1,40 (м, 6, С-(СН 2)3-СН3), 0,87 (т, 3, J=6,9 Гц, С-СН 3)
13С ЯМР (d6-ДМСО/промилле) δ 161 (COO), 139 (C-4), 137 (C-6), 129 (C-9), 127 (C-8), 64,8 (OCH2), 36,4 (NCH3), 30,9 (OCH2 CH2), 28,2 (O(СН2)2 СН2), 25,1 (СН2СН2СН3), 22,1 (СН2СН3), 13,9 (СН2 СН3)
νmax (KBr): 3156, 2967 (C-H), 1746 (С=O), 1467 (С-O), 1261 (С-O), 1054 (С-O), 823,561 см-1
МС: + ионизация электрораспылением (соотношение массы и заряда) = 302 [М+
Н]+, 284 [М+Н-Н2О]+
7. Гептил-ТМЗ-8-карбоксилат
1Н ЯМР (CDCl3/промилле) δ 8,39 (с, 1, Н-6), 4,38 (с, 2, СН 2-О), 4,00 (с, 3, СН 3-N), 1,75 (с, 2, С-СН 3-С), 1,19 (с, 8, С-(СН 2)4-С), 0,83 (с, 3, С-СН 3)
13С ЯМР (d6-ДМСО/промилле) δ 161 (COO), 139 (C-4), 137 (C-6), 129 (C-9), 127 (C-8), 64,8 (ОСН2), 36,4 (NCH3), 31,1 (ОСН2 СН2), 2×28,4 (ОСН2СН2(СН2)2), 25,3 (СН2СН2СН3), 22,1 (СН2СН3), 13,8 (СН2 СН3)
νmax (KBr): 3146, 2927 (C-H), 2858 (C-H), 1748 (C=O), 1718 (C=O), 1457 (С-O), 1245 (С-O), 828, 566 см-1
МС: + ионизация электрораспылением (соотношение массы и заряда) = 316 [М+
Н]+, 398 [М+Н-H2O]+
8. Октил-ТМЗ-8-карбоксилат
1Н ЯМР (CDCl3/промилле) δ 8,36 (с, 1, Н-6), 4,36 (с, 2, СН 2-O), 3,95 (с, 3, СН 3-N), 1,74 (с, 2, С-СН 3-С), 1,19 (с, 10, С-(СН 2)5-С), 0,78 (с, 3, С-СН 3)
13С ЯМР (d6-ДМСО/промилле) δ 160 (COO), 139 (C-4), 137 (C-6), 129 (C-9), 127 (C-8), 64,8 (OCH2), 36,4 (NCH3), 31,2 (OCH2 CH2), 2×28,6 (OCH2CH2(CH2)2), 28,2 (O(СН2)4 СН2), 25,4 (СН2СН2СН3), 22,1 (СН2СН3), 13,9 (СН2 СН3)
νmax (KBr): 2925, 2853, 1758, 1720, 1467, 1255, 838, 556 см-1
МС: + ионизация электрораспылением (соотношение массы и заряда) = 330 [М+
Н]+, 312 [М+Н-Н2О]+
Пример 3. Исследование стабильности производных ТМЗ-8-карбоксилата в спиртах
Точную навеску н-гексил-ТМЗ-8-карбоксилата разбавляют соответственно метанолом, этанолом, изопропанолом и трет-бутиловым спиртом, чтобы получить 1% раствор. По три образца растворов (20 мл) отбирают из каждого из описанных выше растворов и помещают в бутыль коричневого стекла объемом 50 мл, закупоривают и оставляют стоять при комнатной температуре. В точках времен 1, 4, 8, 12, 16, 20, 24, 28, 32 месяцев после начала эксперимента отбирают образцы исследуемых растворов и определяют концентрацию н-гексил-ТМЗ-8-карбоксилата с помощью ВЭЖХ для вычисления среднего значения трех параллельных определений и построения графика. Полученные результаты продемонстрировали, что н-гексил-ТМЗ-8-карбоксилат быстро разлагается в метаноле и этаноле, тогда как в изопропаноле и трет-бутиловом спирте он остается стабильным (см. Фигуру 3).
Пример 4. Исследование стабильности ТМЗ-8-карбоксилата в кислой среде
Точные навески натрия гидроксида и лимонной кислоты разбавляют водой с получением растворов, которые имеют значения рН 7,5, 7,0, 6,5, 6,0 и 5,5 соответственно. Точную навеску н-гексил-ТМЗ-8-карбоксилата растворяют в указанных водных растворах с разными значениями рН, получая серию 1% растворов н-гексил-ТМЗ-8-карбоксилата. Три образца раствора (по 20 мл) отбирают из каждого из описанных выше растворов и помещают в мерные бутыли коричневого стекла объемом 50 мл, закупоривают и оставляют стоять при комнатной температуре. Через 1, 4, 8, 12, 16, 20, 24, 28, 32 месяца после начала эксперимента отбирают образцы исследуемых растворов и определяют концентрацию н-гексил-ТМЗ-8-карбоксилата с помощью ВЭЖХ для вычисления среднего значения трех параллельных определений и построения графика. Полученные результаты продемонстрировали, что н-гексил-ТМЗ-8-карбоксилат быстро разлагается в слабощелочной (рН 7,5) или нейтральной (рН 7,0) среде, тогда как в кислой (рН<7,0) среде он остается относительно стабильным (см. Фигуру 4).
Пример 5. Получение системы по типу резервуара твердого вещества метил-ТМЗ-8-карбоксилата
Навеску 3 г метил-ТМЗ-8-карбоксилата измельчают до состояния тонкого порошка и смешивают с 20 г воды, 50 г олеиновой кислоты, 30 г BE ТПГС и соответствующим количеством лимонной кислоты, получая микроэмульсию путем помола. Добавляют соответствующее количество замедляющей скорость высвобождения мембраны (сополимер этилена и винилацетата) и PSAs (чувствительная к давлению полисилоксановая смола). Полученную смесь тщательно перемешивают, дегазируют путем сохранения тепла с использованием водяной бани и распределяют на полимерной матрице. Высушивают и разрезают на 50 пластырей с получением целевого продукта.
Пример 6. Получение системы по типу резервуара твердого вещества пропил-ТМЗ-8-карбоксилата
Данную систему изготавливают по способу, описанному в Примере 5, с получением 50 кусков пластыря, где метил-ТМЗ-8-карбоксилат, как активный ингредиент, заменен пропил-ТМЗ-8-карбоксилатом.
Пример 7. Получение системы по типу резервуара твердого вещества бутил-ТМЗ-8-карбоксилата
Данную систему изготавливают по способу, описанному в Примере 5, с получением 50 кусков пластыря, где метил-ТМЗ-8-карбоксилат, как активный ингредиент, заменен бутил-ТМЗ-8-карбоксилатом.
Пример 8. Получение системы по типу резервуара твердого вещества гептил-ТМЗ-8-карбоксилата
Данную систему изготавливают по способу, описанному в Примере 5, с получением 50 кусков пластыря, где метил-ТМЗ-8-карбоксилат, как активный ингредиент, заменен гептил-ТМЗ-8-карбоксилатом.
Пример 9. Получение системы по типу резервуара твердого вещества н-гексил-ТМЗ-8-карбоксилата
Данную систему изготавливают по способу, описанному в Примере 5, с получением 50 кусков пластыря, где метил-ТМЗ-8-карбоксилат, как активный ингредиент, заменен н-гексил-ТМЗ-8-карбоксилатом.
Пример 10. Получение системы по типу резервуара твердого вещества этил-ТМЗ-8-карбоксилата
Данную систему изготавливают по способу, описанному в Примере 5, с получением 50 кусков пластыря, где метил-ТМЗ-8-карбоксилат, как активный ингредиент, заменен этил-ТМЗ-8-карбоксилатом.
Пример 11. Получение пластыря амил-ТМЗ-8-карбоксилата
Данную систему изготавливают по способу, описанному в Примере 5, с получением 50 кусков пластыря, где метил-ТМЗ-8-карбоксилат, как активный ингредиент, заменен амил-ТМЗ-8-карбоксилатом
Пример 12. Получение капсулы бутил-ТМЗ-8-карбоксилата
Навеску 5 мг бутил-ТМЗ-8-карбоксилата мелют до состояния тонкого порошка и наполняют полученным порошком твердую желатиновую капсулу с получением препарата в капсулах.
Пример 13. Получение капсулы гептил-ТМЗ-8-карбоксилата
Навеску 10 мг гептил-ТМЗ-8-карбоксилата мелют до состояния тонкого порошка и наполняют полученным порошком твердую желатиновую капсулу с получением препарата в капсулах
Пример 14. Получение капсулы октил-ТМЗ-8-карбоксилата
Навеску 10 мг октил-ТМЗ-8-карбоксилата мелют до состояния тонкого порошка и наполняют полученным порошком твердую желатиновую капсулу с получением препарата в капсулах
Пример 15. Получение капсулы н-гексил-ТМЗ-8-карбоксилата
Рецептура, мг
н-Гексил-ТМЗ-8-карбоксилат, лактозу, прежелатинизированный крахмал, натрий кроскармеллозу (поперечно-сшитая натрий карбоксиметилцелюлоза) соответственно просеивают сквозь сито 65 меш для последующего использования. Навеску н-гексил-ТМЗ-8-карбоксилата в соответствии с указанным в рецептуре количеством смешивают с другими вспомогательными веществами методом пропорционального увеличения количеств. Смесь трижды просеивают сквозь сито 65 меш. Измеренное значение угла естественного откоса составляло меньше 30°. После проведения анализа содержания и определения вместимости получают капсулы, помещая смесь в капсулы №3.
Пример 16. Получение капсулы октил-ТМЗ-8-карбоксилата
Рецептура, мг
Способ изготовления описан в Примере 14, за исключением того, что н-гексил-ТМЗ-8-карбоксилат, как активный ингредиент, заменен октил-ТМЗ-8-карбоксилатом. Получают целевую капсулу.
Пример 17. Получение капсулы 3-метил-гептил-ТМЗ-8-карбоксилата
Рецептура, мг
Способ изготовления описан в Примере 14, за исключением того, что н-гексил-ТМЗ-8-карбоксилат, как активный ингредиент, заменен 3-метил-гептил-ТМ3-8-карбоксилатом. Получают целевую капсулу.
Пример 18. Получение пластыря 2-этил-амил-ТМЗ-8-карбоксилата
Рецептура
Субстанции из приведенного выше перечня тщательно перемешивают с получением микроэмульсии, к которой добавляют соответствующее количество замедляющей скорость высвобождения мембраны (сополимер этилена и винилацетата), и добавляют PSAs (чувствительная к давлению полисилоксановая смола). Полученную смесь тщательно перемешивают, дегазируют путем сохранения тепла с использованием водяной бани и распределяют на полимерной матрице. Высушивают и разрезают на 50 пластырей с получением целевого продукта.
Пример 19. Получение трансдермальной эмульсии н-гексил-ТМЗ-8-карбоксилата для местного применения
Навеску 3 г н-гексил-ТМЗ-8-карбоксилата измельчают до состояния тонкого порошка и смешивают с 20 г воды, 50 г олеиновой кислоты, 30 г фосфолипида, соответствующим количеством лимонной кислоты или сорбиновой кислоты (рН 5,5), витамина Е и изопропанола для получения микроэмульсии. Она может быть использована непосредственно в полученном виде или разделена на 50 частей для изготовления 25 пластырей.
Пример 20. Получение трансдермальной эмульсии н-гексил-ТМЗ-8-карбоксилата для местного применения
Навеску 3 г н-гексил-ТМЗ-8-карбоксилата измельчают до состояния тонкого порошка и смешивают с 20 г воды, 35 г BE ТПГС, 45 г триглицеридов с умеренной или длинной цепью, соответствующим количеством молочной кислоты или бензойной кислоты (рН 5,0) и изопропанола для получения микроэмульсии. Она может быть использована непосредственно в полученном виде или разделена на 50 частей для изготовления 25 пластырей.
Пример 21. Получение трансдермальной мази н-гексил-ТМЗ-8-карбоксилата для местного применения
Навеску 3 г н-гексил-ТМЗ-8-карбоксилата измельчают до состояния тонкого порошка и смешивают с 15 г воды, 50 г BE ТПГС, 35 г изопропилмиристата, соответствующим количеством яблочной кислоты или бензойной кислоты (рН 6,0) и изобутилового спирта для получения мази. Она может быть использована непосредственно в полученном виде или может быть превращена в микроэмульсию и разделена на 50 частей для изготовления 25 пластырей.
| название | год | авторы | номер документа |
|---|---|---|---|
| АРИЛ-КОНДЕНСИРОВАННОЕ СОЕДИНЕНИЕ ИЗОСЕЛЕНАЗОЛА, СОДЕРЖАЩЕЕ ТЕТРАЗИНОВЫЙ ЗАМЕСТИТЕЛЬ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2818486C1 |
| Фармацевтическая композиция на основе 3-(4-Метилимидазол-1-ил)имидазо[1,2-b][1,2,4,5]тетразина в качестве противоопухолевого средства | 2015 |
|
RU2614234C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С АНТИОПУХОЛЕВОЙ АКТИВНОСТЬЮ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1994 |
|
RU2148401C1 |
| ПИРИМИДИЛЦИКЛОПЕНТАНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ AKT-ПРОТЕИНКИНАЗЫ | 2008 |
|
RU2486178C2 |
| ТРАНСДЕРМАЛЬНАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ДОНЕПЕЗИЛ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2015 |
|
RU2713207C2 |
| СОЕДИНЕНИЯ БЕНЗОКСАЗИНОНА В КАЧЕСТВЕ ДВОЙНЫХ ИНГИБИТОРОВ KLK5/7 | 2020 |
|
RU2831430C1 |
| ГИДРОКСИЛИРОВАННЫЙ ПИРИМИДИЛ ЦИКЛОПЕНТАН В КАЧЕСТВЕ ИНГИБИТОРА ПРОТЕИНКИНАЗЫ (АКТ) | 2009 |
|
RU2520735C2 |
| СОЕДИНЕНИЕ, ОБЛАДАЮЩЕЕ ИНГИБИРУЮЩЕЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ KDM5, И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2021 |
|
RU2840256C1 |
| КОМБИНАЦИИ АЛЬФА-2-ДЕЛЬТА-ЛИГАНДА С СЕЛЕКТИВНЫМ ИНГИБИТОРОМ ЦИКЛООКСИГЕНАЗЫ-2 | 2003 |
|
RU2286151C2 |
| ЗАМЕЩЕННЫЕ СОЕДИНЕНИЯ ХИНОЛИНА И СПОСОБЫ ИХ ИСПОЛЬЗОВАНИЯ | 2012 |
|
RU2568258C2 |
Данное изобретение раскрывает фармацевтические композиции на основе соединений темозоломид-8-карбоксилата общей формулы I, а также способ их получения. Заявляемые композиции содержат наряду с традиционными фармацевтическими носителями еще и компонент кислой природы, обуславливающий повышенную устойчивость фармацевтической композиции к колебаниям рН. Представленная композиция обладает противоопухолевым действием и может быть особенно полезна при трансдермальном применении. 2 н. и 14 з.п. ф-лы, 4 ил., 2 табл.
1. Фармацевтическая композиция, обладающая противоопухолевой активностью, отличающаяся тем, что содержит терапевтически эффективное количество одного или больше из соединений формулы 1, как активный ингредиент, обусловленное фармацевтически приемлемыми носителями и одним или более фармацевтически приемлемыми компонентами кислотной природы, где указанный компонент кислотной природы выбран из группы, состоящей из олеиновой кислоты, стеариновой кислоты, линолевой кислоты, фумаровой кислоты, бензойной кислоты, винной кислоты, сорбиновой кислоты, молочной кислоты, лимонной кислоты, уксусной кислоты и ЭДТА,
отличающаяся тем, что Х является S или О;
R представляет собой замещенный или незамещенный С3~С10 алкил с неразветвленной или разветвленной цепью, С3~С10 циклоалкил, С3~С10 алкенил с неразветвленной или разветвленной цепью или С3~С10 алкинил с неразветвленной или разветвленной цепью;
и R может содержать заместитель(и), где указанные заместитель(и) могут представлять собой С1~С6 алкил, С1~С6 алкокси, С1~С6 алкилтиогруппу, С1~С6 алкиламиногруппу, фенил или фенил, замещенный галогеном.
2. Фармацевтическая композиция по п.1, отличающаяся тем, что указанная композиция дополнительно может содержать один или больше фармацевтически приемлемых С3~С8 третичных спиртов или вторичных спиртов, или их эфирных производных.
3. Фармацевтическая композиция по п.1 или 2, отличающаяся тем, что указанный активный ингредиент вводят пациентам в дозе 0,1-200 мг/кг массы тела/сутки.
4. Фармацевтическая композиция по п.3, отличающаяся тем, что указанный интервал доз активного ингредиента составляет 1-20 мг/кг массы тела/сутки.
5. Фармацевтическая композиция по п.1, отличающаяся тем, что указанная композиция может быть изготовлена в любой из фармацевтически приемлемых лекарственных форм.
6. Фармацевтическая композиция по п.5, отличающаяся тем, что указанная композиция может быть изготовлена в виде трансдермальной лекарственной формы для местного применения или лекарственной формы для перорального применения.
7. Фармацевтическая композиция по п.6, отличающаяся тем, что указанная трансдермальная лекарственная форма для местного применения представляет собой трансдермальный пластырь для местного применения.
8. Фармацевтическая композиция по п.7, отличающаяся тем, что указанный трансдермальный пластырь представляет собой пластырь с контролируемым высвобождением матричного типа, пластырь с контролируемым высвобождением по типу резервуара твердого вещества или пластырь с контролируемым высвобождением по типу резервуара жидкого вещества.
9. Фармацевтическая композиция по п.8, отличающаяся тем, что указанный трансдермальный пластырь представляет собой пластырь с контролируемым высвобождением по типу резервуара твердого вещества, в котором водная фаза представляет собой воду, и масляная фаза представляет собой одну или больше субстанций, выбранных из группы, состоящей из олеиновой кислоты, изопропилмиристата, лауриновой кислоты, воска, цетилового спирта, стеарилового спирта, жидкого парафина, вазелина, безводного ланолина, стеариновой кислоты, хлопкового масла, касторового масла и линоленовой кислоты.
10. Фармацевтическая композиция по п.9, отличающаяся тем, что указанная масляная фаза представляет собой олеиновую кислоту или изопропилмиристат.
11. Фармацевтическая композиция по п.8, отличающаяся тем, что указанный трансдермальный пластырь представляет собой пластырь с контролируемым высвобождением по типу резервуара, который содержит непроницаемую матрицу, жидкое лекарственное средство, замедляющую скорость высвобождения мембрану, PSAs и слой высвобождения, где:
непроницаемая матрица состоит из одной или больше субстанций, выбранных из группы, состоящей из полиэтилена, поливинилхлорида, нитроглицерина, полидиметилсилоксана, поливинилпирролидона, поливинилового спирта, комплекса полиэтеноксида, полиэтиленгликоля, монометилового эфира полиэтиленгликоля или диметилового эфира полиэтиленгликоля, полиэтиленгликоля сукцината и витамина Е ТПГС, хлопка и шерсти;
указанная мембрана, замедляющая скорость высвобождения, выбрана из группы, состоящей из мембраны из сополимера этилена и винилацетата, мембраны из полиуретана или мембраны из гликольдиацетата; и
указанный PSAs, выбранный из группы, состоящей из чувствительной к давлению полисилоксановой смолы или чувствительной к давлению полиакрилатной смолы.
12. Фармацевтическая композиция по п.11, отличающаяся тем, что указанная матрица представляет собой матрицу из полиэтилена или поливинилхлора.
13. Фармацевтическая композиция по п.8, отличающаяся тем, что указанный трансдермальный пластырь для местного применения представляет собой пластырь с контролируемым высвобождением матричного типа, где вспомогательная клейкая матрица лекарственного средства выбрана из группы, состоящей из поливинилхлорида, полиакрилата, полидиметилсилоксана, поливинилпирролидона, поливинилового спирта, водного геля, изготовленного из поливинилпирролидона, комплекса поливинилпирролидона и полиэтиленоксида, монометилового эфира полиэтиленгликоля или диметилового эфира полиэтиленгликоля, полиэтиленгликоля сукцината и BE ТПГС.
14. Фармацевтическая композиция по п.13, отличающаяся тем, что вспомогательная липкая матрица лекарственного средства представляет собой полиакрилат.
15. Фармацевтическая композиция по п.5, отличающаяся тем, что указанная лекарственная форма представляет собой таблетку, пилюлю, диспергированный порошок, капсулу, гранулу, эмульсию, раствор, суспензию, сироп, твердый суппозиторий для вагинального или ректального введения.
16. Способ получения композиции по п.9, который отличается тем, что включает следующие стадии:
взвешивание соответствующего количества соединения по п.1 как активного ингредиента и измельчение его до состояния тонкого порошка, тщательное перемешивание водной фазы, масляной фазы, поверхностно-активного вещества и необходимых носителей с последующим смешиванием с измельченным порошком лекарственного средства, перемешивание полученной смеси и помол с образованием микроэмульсии; добавление к смеси соответствующего количества мембраны, замедляющей скорость высвобождения, и чувствительной к давлению клейкой субстанции с тщательным перемешиванием; дегазация путем сохранения тепла с использованием водяной бани и распределение на полиэтиленовой матрице; сушка и разрезание на маленькие кусочки с получением указанного пластыря с контролируемым высвобождением по типу резервуара твердого вещества.
| CN 1485327 A, 31.03.2004 | |||
| ДАТЧИК ДЛЯ ИЗМЕРЕНИЯ УСИЛИЙ|П HATEHT.ffO- | 0 |
|
SU252682A1 |
| Wang Yongfeng et al, 1997, J.Org | |||
| Chem, 62, 7288-7294 | |||
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С АНТИОПУХОЛЕВОЙ АКТИВНОСТЬЮ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1994 |
|
RU2148401C1 |
Авторы
Даты
2010-06-27—Публикация
2005-09-15—Подача