Изобретение может найти применение как общий метод окисления спиртов до карбонильных соединений и может быть использовано в фармацевтике.
Известен электрохимический способ окисления спиртов в системе KJ-вода-сорастворитель (Tetrahedron Letters, 1979, №2, pp.165-168, Т.Shono, Y.Matsumura, J.Hayashi и М.Mizoguchi). При этом первичные спирты окисляются до эфиров кислот, а вторичные - до кетонов.
Например, в ячейку, снабженную мешалкой и рубашкой охлаждения и платиновыми электродами, помещают раствор 2,49 г (0,015 моль) йодида калия в 15 мл воды, 0,06 моль 2-метилциклогексанола и 15-20 мл сорастворителя (трет-бутиловый спирт или гексан). Процесс ведут при постоянном токе (плотность тока 0,02 А/см2) и заканчивают после того, как будет пропущено 20 Ф/моль электричества. Органический слой отделяют, а водный слой трижды экстрагируют эфиром; органические вытяжки объединяют, промывают водой и водным тиосульфатом натрия. Затем растворитель удаляют, а продукт очищают перегонкой и идентифицируют, сравнивая с заведомым образцом. Выход 2-метилциклогексанона - 52% по веществу и 6% по току.
Недостатком этого метода является высокий удельный расход электричества, т.к. на один моль конечного продукта приходится пропускать до 20 Ф/моль электричества, кроме этого первичные спирты в этих условиях окисляются не до альдегидов, а до эфиров кислот.
Наиболее близким является способ окисления спиртов в двухфазной системе вода-толуол в присутствии кристаллического йода и нитроксильного радикала. (Ross A. Miller and R Scott Hoerrer. Organic Letters, 2003, V.5, №3, pp 285-287).
Например, в колбу емкостью 100 мл, снабженную магнитной мешалкой, помещают 0,75 г (3,98 ммоль) цинамоилового спирта, 10 мл толуола и раствор 1 г (11,94 ммоль) бикарбоната натрия в 10 мл дистиллированной воды. Затем при перемешивании добавляют 0,06 г (0,398 ммоль) 2,2,6,6-тетраметилпиперидин-1-оксила и 2,02 г (7,96 ммоль) кристаллического йода. Смесь перемешивают в течение 16 часов при 20°С. Затем смесь охлаждают до 5°С, обрабатывают этилацетатом (10 мл) и добавляют водный раствор сульфата натрия (0,501 г Na2SO4 в 5 мл дистиллированной воды). Затем смесь переносят в делительную воронку и отделяют водный слой. Органический слой промывают 10 мл раствора бикарбоната калия, сушат безводным сульфатом натрия и упаривают в вакууме до объема 10 мл, а затем - в среде инертного газа до объема 10 мл. Выпавший осадок отфильтровывают, промывают толуолом (3 мл) и сушат в вакууме. В результате выделяют 0,69 г (85%) соответствующего альдегида.
Недостатком приведенного выше способа является большой расход йода (на 1 моль спирта требуется 2 моль йода), который достаточно дорог, а также образование побочного продукта - йодида калия.
Задача изобретения - усовершенствование процесса окисления спиртов до карбонильных соединений в энергоэкономическом отношении.
Поставленная задача достигается тем, что готовится реакционная смесь при комнатной температуре, состоящей из окисляемого спирта, воды, бикарбоната натрия, органического растворителя и нитроксильного радикала, в качестве органического растворителя используют хлористый метилен, а в качестве нитроксильного радикала используют - 4-ацетиламино-2,2,6,6-тетраметилпиперидин-1-оксил формулы:
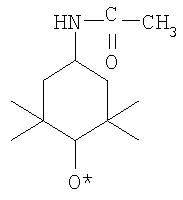
при соотношении спирт и нитроксильный радикал 10:1, добавляют йодид калия, а электролиз проводят на платиновых электродах при силе тока 1 А и температуре 20-25°С. При этом затраты электрической энергии на окисление 1 моль спирта в 5 раз меньше. Так же в отличие от прототипа и аналога в синтезе вместо кристаллического йода используется йодид калия, который в процессе окисления не расходуется, что позволяет использовать на окисление 1 моля спирта в 8 раз меньшее количество йодида калия, чем кристаллического йода. Причем первичные спирты окисляются только до альдегидов, а не кислот, что очень важно, т.к. остановить процесс на этой стадии удается не всегда. Кроме того, в предложенном способе используются каталитические количества нитроксильного радикала - 4-ацетиламино-2,2,6,6-тетраметилпиперидин-1-оксила (в 100 раз меньше, чем в аналоге), что, однако, не мешает проводить процесс с высоким выходом по веществу и по току.
Процесс проводят в бездиафрагменном электролизере на платиновых электродах, в двухфазной системе хлористый метилен - водный раствор йодида калия, в присутствии нитроксильного радикала. На аноде образуется йод, окисляющий нитроксильный радикал до оксоаммониевой соли, которая выступает одноэлектронным окислителем спирта до соответствующего карбонильного соединения. При этом соль оксоаммония превращается в гидроксиламин, который легко окисляется до исходного нитроксильного радикала, таким образом каталитический цикл замыкается. При этом на 1 моль целевого продукта требуется от 2 до 4 Ф электричества.
Эти условия повышают технологичность процесса, сокращают сроки получения целевого продукта, т.к. окисление проводится значительно быстрее и требуется меньшее количество электричества.
Предлагаемый метод позволяет окислять первичные и вторичные спирты электрогенерируемым йодом в присутствии 4-ацетиламино-2,2,6,6-тетраметилпиперидин-1-оксила, являющегося медиатором процесса окисления. Электрогенирируемый йод имеет преимущество перед другими реагентами, т.к. в процессе окисления им не затрагиваются другие легкоокисляющиеся группы.
Пример 1
Окисление вторичных спиртов на примере окисления циклогексанола до циклогексанона
В бездиафрагменный электролизер емкостью 150 мл, снабженный механической мешалкой, водяной рубашкой охлаждения и двумя платиновыми электродами (пластины, площадью анод - 20 см2, катод - 15 см2), помещают 4,5 мл (0,042 моль) циклогексанола, который растворяют в 30 мл хлористого метилена. Затем прибавляют 5 г (0,06 моль) NаНСО3 и 2 г (0,01 моль) KJ, растворенных в 70 мл дистиллированной воды. Последним добавляют 1,1 г (0,005 моль) 4-ацетиламино-2,2,6,6-тетраметилпиперидин-1-оксила. Условия электролиза: температура 20-25°С, сила тока 1 А (плотность 0,05 А/см2). Синтез заканчивают после пропускания 4 Ф/моль электричества. После окончания электролиза содержимое электролизера сливают, избыток йода нейтрализуют раствором щелочи или прибавлением кристаллического Na2S2O3, после чего отделяют органический слой. Водный слой экстрагируют хлористым метиленом (2×50 мл), органические вытяжки объединяют и сушат безводным сульфатом натрия. По данным ТСХ реакционная смесь содержит два вещества - исходный спирт и продукт. Содержание циклогексанона и циклогексанола определяют методом ГЖХ. Степень конверсии циклогексанола до кетона по данным ГЖХ составила 85%. Для выделения кетона хлористый метилен удаляют, а остаток перегоняют в вакууме, собирая фракцию 48°С (7 мм рт.ст.). Выход циклогексанона 3,05 г (78%).
Пример 2
Окисление первичных спиртов на примере окисления фенилэтилового спирта до α-толуилового альдегида.
В бездиафрагменный электролизер емкостью 150 мл, снабженный механической мешалкой, водяной рубашкой охлаждения и двумя платиновыми электродами (пластины площадью: анод - 20 см2, катод - 15 см2), помещают 4,5 мл (0,042 моль) фенилэтилового спирта, растворенного в 30 мл хлористого метилена. Затем прибавляем 5 г (0,06 моль) NaHCO3 и 2 г (0,01 моль) KJ, растворенных в 70 мл дистиллированной воды. Последним добавляют 1,1 г (0,005 моль) 4-ацетиламино-2,2,6,6-тетраметилпиперидин-1-оксила. Условия электролиза: температура 20-25°С, сила тока 1 А (плотность 0,05 А/см2), интенсивное перемешивание. Синтез заканчивают после пропускания 4 Ф/моль электричества. После окончания электролиза содержимое электролизера сливают, избыток йода восстанавливают кристаллическим Na2S2O3, после чего отделяют органический слой. Водный слой экстрагируют хлористым метиленом (2×50 мл), органические вытяжки объединяют и сушат безводным сульфатом натрия. По данным ТСХ реакционная смесь содержит два вещества - исходный спирт и продукт. Содержание α-толуилового альдегида и фенилэтилового спирта определяют методом ГЖХ. Степень конверсии фенилэтилового спирта до α-толуилового альдегида по данным ГЖХ составила 90%. Для выделения альдегида хлористый метилен удаляют, а остаток перегоняют в вакууме, собирая фракцию 41-42°С (7 мм рт.ст.). Выход α-толуилового альдегида 4,01 г (80%).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ электрохимического окисления спиртов | 2018 |
|
RU2671827C1 |
| Способ электрохимического окисления спиртов в нитрилы | 2021 |
|
RU2778929C1 |
| Способ электрохимического окисления спиртов в нитрилы | 2020 |
|
RU2724898C1 |
| СПОСОБ ОКИСЛЕНИЯ СПИРТОВ ДО КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ | 2007 |
|
RU2351693C1 |
| ЭЛЕКТРОХИМИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ 2,2,6,6-ТЕТРАМЕТИЛПИПЕРИДИН-1-ОКСИЛА | 2006 |
|
RU2302410C1 |
| Катализатор селективного окисления первичных спиртов, способ приготовления катализатора и способ селективного окисления первичных спиртов до альдегидов | 2021 |
|
RU2788871C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИСНОРАЛЬДЕГИДА | 1994 |
|
RU2131437C1 |
| СПОСОБЫ ПОЛУЧЕНИЯ ФТОРИРОВАННЫХ КАРБОНОВЫХ КИСЛОТ И ИХ СОЛЕЙ | 2010 |
|
RU2545172C2 |
| НЕПРЕРЫВНЫЙ СПОСОБ ПОЛУЧЕНИЯ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ ПОСРЕДСТВОМ СОДЕРЖАЩЕГО НИТРОКСИЛЬНЫЙ РАДИКАЛ КАТАЛИЗАТОРА | 2011 |
|
RU2579510C2 |
| Способ получения комплексов платины (IV) с аминонитроксильными радикалами | 2015 |
|
RU2613513C2 |
Настоящее изобретение относится к электрохимическому способу окисления спиртов до карбонильных соединений, который может быть использован в фармацевтике. Способ включает приготовление реакционной смеси при комнатной температуре, состоящей из окисляемого спирта, воды, бикарбоната натрия, органического растворителя и нитроксильного радикала. При этом электролиз проводят на платиновых электродах при силе тока 1 А и температуре 20-25°С, в реакционную смесь добавляют йодид калия, в качестве органического растворителя используют хлористый метилен, а в качестве нитроксильного радикала - 4-ацетиламино-2,2,6,6-тетраметилпиперидин-1-оксил формулы:
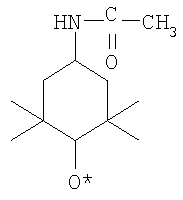
при соотношении спирт и нитроксильный радикал 10:1. Изобретение позволяет при сокращенных сроках и меньших затратах электричества высокотехнологичным способом получить целевые продукты с высоким выходом.
Электрохимический способ окисления спиртов до карбонильных соединений, включает приготовление реакционной смеси при комнатной температуре, состоящей из окисляемого спирта, воды, бикарбоната натрия, органического растворителя и нитроксильного радикала, отличающийся тем, что электролиз проводят на платиновых электродах при силе тока 1А и температуре 20-25°С, в реакционную смесь добавляют йодид калия, в качестве органического растворителя используют хлористый метилен, а в качестве нитроксильного радикала - 4-ацетиламино-2,2,6,6-тетраметилпиперидин-1-оксил формулы:
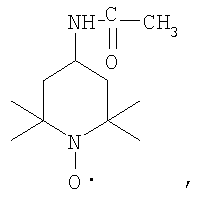
при соотношении спирт и нитроксильный радикал 10:1.
| R.A.Miller et al | |||
| Iodine as a Chemoselective Reoxidant of TEMPO: Application to the Oxidation of Alcohols to Aldehydes and Ketones | |||
| Organic Letters, 2003, т.5, №3, с.285-287 | |||
| Жукова И.Ю | |||
| и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| ун-т | |||
| Новочеркасск: Деп | |||
| в ВИНИТИ, 13.12.2000, № 3127-В2000 | |||
| US 6776894 B1, 17.08.2004 | |||
| US 6069282 A, 30.05.2000. | |||
Авторы
Даты
2010-06-27—Публикация
2008-10-29—Подача