ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к раствору для консервирования, перфузии и/или реперфузии любого органа, особенно сердца, с целью трансплантации. Раствор содержит пептидный(ые) ингибитор(ы) протеинкиназы С бета II (ПКС βII) и/или протеинкиназы С зета (ПКС ζ) и/или пептидный(ые) активаторы протеинкиназы С дельта (ПКС δ).
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Успеху трансплантации органов нередко препятствует их повреждение ввиду ишемии/реперфузии. Изолированные человеческие сердца, лишенные кислорода на более чем 4 часа, прогрессивно теряют жизнеспособность и часто не приживаются у реципиентов. Прочие органы, такие как почки, печень, поджелудочная железа и легкие, будучи удаленными из организма перед трансплантацией, также подвержены тканевому и клеточному повреждению. Причиной этого повреждения являются гипоксия и недостаток кровообращения, которые в физиологических условиях осуществляют поддержание необходимых концентраций кислорода и питательных веществ и устраняют токсические продукты метаболизма клеток. Трансплантаты органов чаще благополучно приживаются, если пересадка происходит немедленно после взятия органа.
Последние научные достижения позволили увеличить частоту успешных пересадок органов и успешных операций на органах, например, таких как аортокоронарное шунтирование. Эти успешные хирургические вмешательства стали возможны благодаря появлению растворов для консервации и перфузии органов. Кроме того, усовершенствовались способы и устройства доставки перфузионного раствора к органу.
Краткосрочная консервация миокарда в настоящее время осуществляется с помощью охлаждения после кардиоплегии. Тем не менее, существует множество способов, различающихся составом используемого раствора, температурой консервации и протокола введения.
С целью защиты миокарда при операциях на сердце были разработаны различные растворы, останавливающие и консервирующие сердце. Примерами могут служить растворы Krebs-Henseleit, UW, St.Thomas II, растворы Collins и Stanford (см., например, патенты США №№4798824 и 4938961; Southard и Belzer, Ann. Rev. Med. 46:235-247 (1995); и Donnelly и Djuric, Am. J. Hosp. Pharm. 48:2444-2460 (1991)). Тем не менее, проблема отторжения органов, обусловленная повреждением трансплантата за период времени, проходящий между его удалением и восстановлением кровотока в организме реципиента, сохраняется.
Восстановление кровотока является первоочередной задачей при воздействии на органы и ткани, испытывающие длительную ишемию, например, при трансплантации. Тем не менее, реперфузия вызывает повреждение эндотелия и миоцитов, что приводит к органной дисфункции (Buerke и др., Am JPhysiol 266: Н128-136, 1994; Lucchesi и Mullne, Ann. Rev. Pharmacol. Toxicol. 26: 2011-2024, 1986; и Lucchesi и др., J.Mol. Cell. Cardiol. 21: 1241-1251, 1989). Последовательность событий, ассоциирующихся с реперфузионным повреждением, начинается с дисфункции эндотелия, которая характеризуется снижением базальной секреции клетками эндотелия оксида азота (NO) в течение первых 2.5-5 минут после восстановления кровотока (Tsao и Lefer, Am. J.phyiol. 259: Н1660-1666, 1990). Уменьшение высвобождения NO эндотелием ассоциируется с повышением концентрации молекул адгезии на мембранах эндотелиальных клеток и полиморфноядерных лейкоцитов (ПЯЛ) (Ma и др., Circ Res 72: 403-412, 1993; и Weyrich и др., J.Leuko. Biol. 57: 45-55, 1995). Это в свою очередь приводит к взаимодействию между ПЯЛ и эндотелием, которое имеет место через 10-20 минут после восстановления кровотока, с последующей инфильтрацией миокарда ПЯЛ, что можно наблюдать уже через 30 минут (Lefer и Hayward, B The Role of Nitric Oxide in Ischemia-Reperfusion: Contemporary Cardiology, Loscalzo и др. (Eds.), Humana Press, Totowa, NJ, pp.357-380, 2000; Lefer и Lefer, Cardiovadc. Res. 32: 743-751, 1996; T-sao и др., Circulation 82. 1402-1412, 1990; и Weyrich и соавт., J.Leuko. Biol. 57: 45-55, 1995).
Из реперфузированной ткани высвобождаются молекулы хемотаксиса, которые вкупе с плазменными факторами активируют ПЯЛ, что способствует высвобождению из последних цитотоксических соединений (т.е., супероксид аниона) и усугубляет органную дисфункцию, следующую за ишемией/реперфузией (Lucchesi и др. L.Mol. Cell. Cardiol. 21: 1241-1251, 1989; Ma и др., Circ Res 69: 95-106, 1991; Tsao и др., Circulation 82: 1402-1412, 1990; и Tsao и др., Am Heart J.123: 1464-1471, 1992). Супероксид взаимодействует с NO с образованием пероксинитрит аниона и, таким образом, снижает биодоступность NO и усугубляет дисфункцию эндотелия и инфильтрацию ПЯЛ после ишемии/реперфузии миокарда (Clancey и др., J. Clin. Invest. 90: 1116-1121, 1992; Hansen, Circulation 91: 1872-85, 1995; Lucchesi и др., J.Mol. Cell. Cardiol. 21: 1241-1251, 1989; Rubanyi и Vanhoutte, Am LPhysiol 250: Н815-821, 1986; Tsao и др., Am Heart J123: 1464-1471, 1992; и Weiss, New Eng.J.Med. 320: 365-375, 1989).
Таким образом, в настоящее время сохраняется потребность в более качественных растворах, которые могли бы увеличить время консервации трансплантируемого органа и защитить его от реперфузионного повреждения после ишемии, с тем чтобы орган мог должным образом функционировать после восстановления кровотока.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение представляет собой раствор для консервации, перфузии и/или реперфузии органов, особенно сердца, содержащий пептидный(ые) ингибитор(ы) протеинкиназы С βII (ПКС βII) и/или протеинкиназы С ζ (ПКС ζ) и/или пептидного(ых) активатора(ов) протеинкиназы Сδ (ПКС δ). Раствор предохраняет ткани и клетки органа от повреждения в случаях, когда орган изолирован от кровообращения или испытывает снижение кровотока (ишемию). Авторы обнаружили, что пептидные ингибиторы ПКС βII и/или ПКС ζ, и/или пептидный(ые) активатор(ы) ПКС δ способствуют образованию NО или подавляют высвобождение супероксида эндотелием и ПЯЛ, что может приводить к защитному воздействию на органы, подвергающиеся ишемии/реперфузии.
Данный раствор содержит около 5-10 µM пептидного ингибитора ПКС βII и/или около 2.5-5 µM пептидного ингибитора ПКС ζ и/или 5-10 µM пептидного активатора ПКС δ, растворенных в растворе хлорида натрия. Пептидный ингибитор ПКС βII представляет собой SEQ:ID No:1, пептидный активатор ПКС δ представляет собой SEQ: ID No:3, а пептидный ингибитор ПКС ζ выбран из группы, состоящей из EEQ:ID No: 2 и Go6983. Указанные ингибиторы/активатор могут быть меристилированны.
Данный раствор может быть использован как перфузионная среда или как консервирующий раствор. В качестве перфузионного раствора он вводится в сосудистое русло органа с целью защиты тканей и клеток. При использовании в качестве консерванта орган погружается в раствор целиком. Желательно, чтобы орган и перфузировался раствором, и был погружен в него. Далее, данный раствор также служит и раствором для реперфузии при восстановлении кровотока в органе после ишемии.
Настоящее изобретение включает также способы использования данного раствора. К ним относятся способы консервации органа для трансплантации, способы защиты ишемизированного органа от повреждения, уменьшения степени органной дисфунции после ишемии, сохранения высвобождения оксида азота в ишемизированном органе и защиты изолированного от кровообращения органа от повреждения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
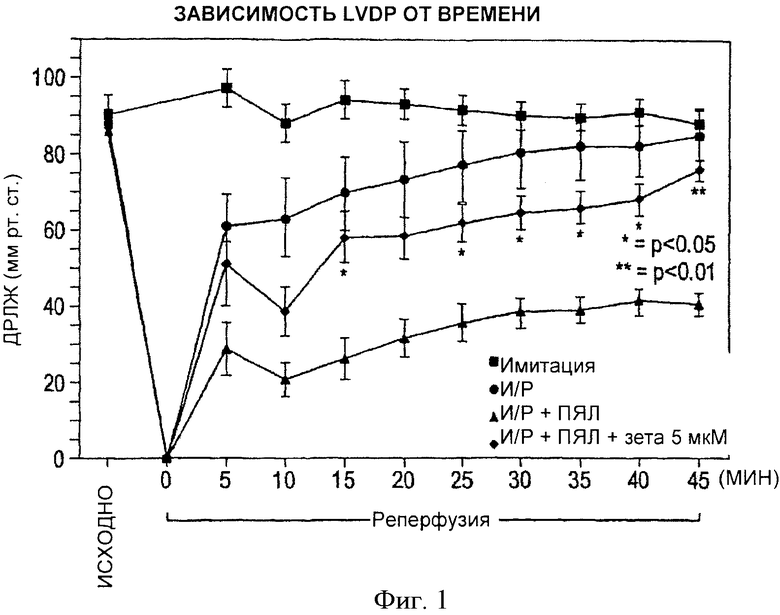
Фиг.1. Зависимость ДРЛЖ (давление, развиваемое левым желудочком = конечное систолическое давление в левом желудочке - конечное диастолическое давление в левом желудочке) от времени в сердцах-имитациях и сердцах крыс, перфузируемых в режимах И/Р (И/Р = ишемия/реперфузия), И/Р+ПЯЛ и И/Р+ПЯЛ+ПКСζ пептидными ингибиторами (5µM). Приводятся значения ДРЛЖ в начале, после 20-минутной ишемии и во время реперфузии от 0 до 45 минут. В группе имитаций (n=6) значение ДРЛЖ было одним и тем же в течение всего 80-минутного протокола. В группе И/Р (n=6) значения вернулись к исходным. В группе И/Р+ПЯЛ (n=6) произошло достоверное и стойкое уменьшение ДРЛЖ по сравнению с группой, получившей И/Р+ПЯЛ+ПКСζ пептидный ингибитор (n=6). Все значения представлены в виде среднего ±m (стандартная ошибка среднего). *p<0.05 и **p<0.01, группа, получившая 1/R-+ПЯЛ+ПКСζ пептидный ингибитор от группы И/Р+ПЯЛs.
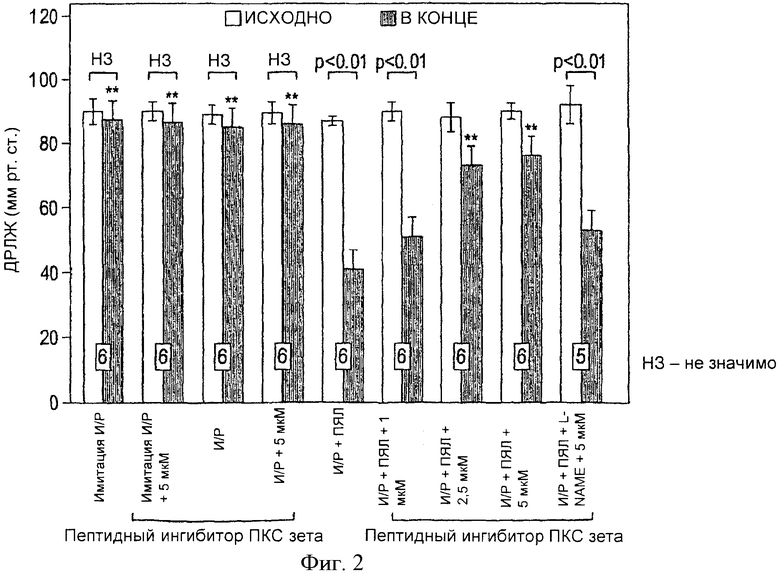
Фиг.2. Начальное и конечное ДРЛЖ, выраженное в мм рт.ст., развиваемое изолированными перфузируемыми сердцами крыс до ишемии (И) (исходно) и через 45 минут после реперфузии (Р) (конечное значение). Сердца перфузировались в присутствии или в отсутствии ПЯЛ. ПЯЛ вызывали значительную контрактильную дисфункцию, которая уменьшалась под действием пептидного ингибитора ПКСζ, но достоверно блокировалась A∧-нитро-L-аргинин метил эфиром (L-NAME). Все значения представлены в виде среднего ±m. Количество исследованных сердец представлено внизу столбиков. **p<0.01, по сравнению с конечным И/Р+ПЯЛ; нз = не значимо.
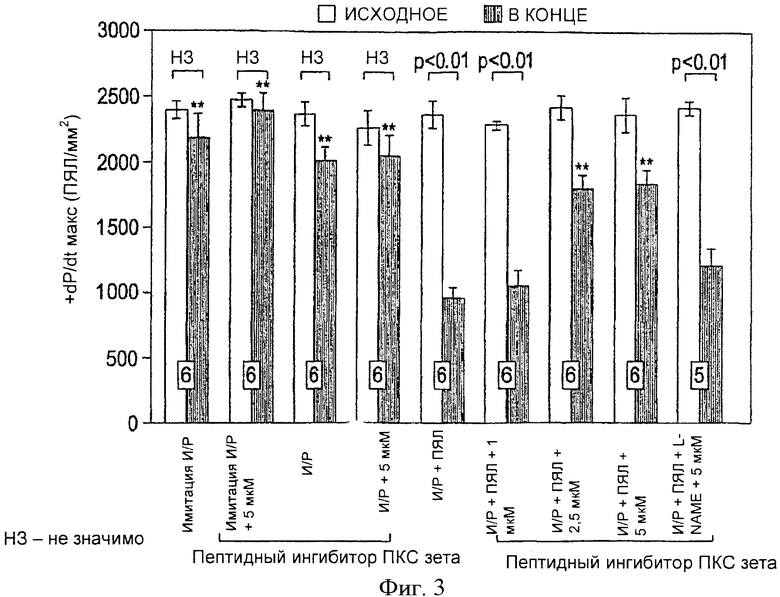
Фиг.3. Исходное и конечное максимальное ДРЛЖ (+dP/dt max), выраженное в мм рт.ст./с в изолированных перфузированных сердцах крыс до ишемии (И) и после реперфузии (Р). Сердца перфузировались в присутствии или в отсутствии ПЯЛ. ПЯЛ вызывали значительную контрактильную дисфункцию, которая уменьшалась под действием пептидного ингибитора ПКСζ, но блокировалась L-NАМЕ. Все значения представлены в виде среднего ±m. Количество исследованных сердец представлено внизу столбиков. **p<0.01, по сравнению с конечным И/Р+ПЯЛ; нз = не значимо.
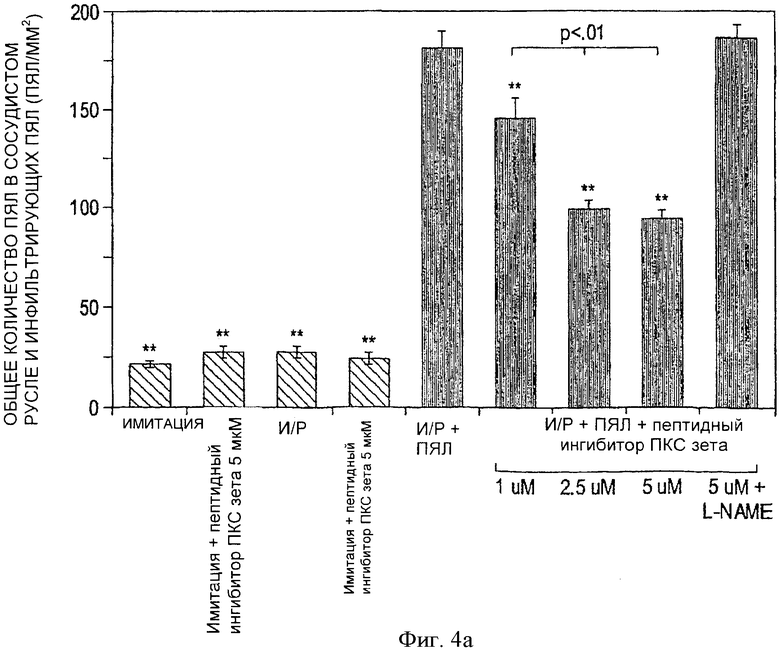
Фиг.4а. Гистологическая оценка общего числа внутрисосудистых и инфильтрирующих ПЯЛ в изолированных перфузированных сердцах крыс (образцы брались у 3 крыс из группы и из 10 участков сердца). Общее число внутрисосудистых и инфильтрирующих ПЯЛ в претерпевшей реперфузию ткани сердца и прилежащих к коронарному руслу значительно уменьшалось под действием пептидного ингибитора ПКСζ. Заштрихованные столбики касаются сердец, перфузированных без ПЯЛ, а черные столбики - сердец, перфузированных ПЯЛ. **Р<0.01, по сравнению с И/Р+ПЯЛ.
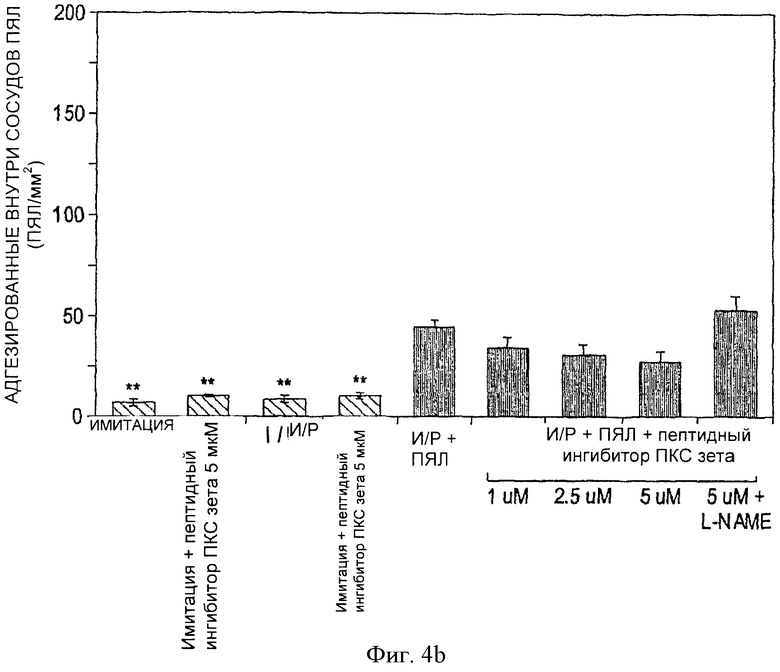
Фиг.4b. Гистологическая оценка внутрисосудистых ПЯЛ, прилежащих к коронарному руслу в изолированных перфузированных сердцах крыс (у 3 крыс из группы забиралось по 10 образцов из 10 участков миокарда). Число ПЯЛ, прилежащих к коронарному руслу не различалось достоверно в зависимости от И/Р+ПЯЛ. Заштрихованные столбики касаются сердец, перфузированных без ПЯЛ, а черные столбики - сердец, перфузированных ПЯЛ. Все значения представляют собой среднее количество ПЯЛ/мм площади сердца ±m.
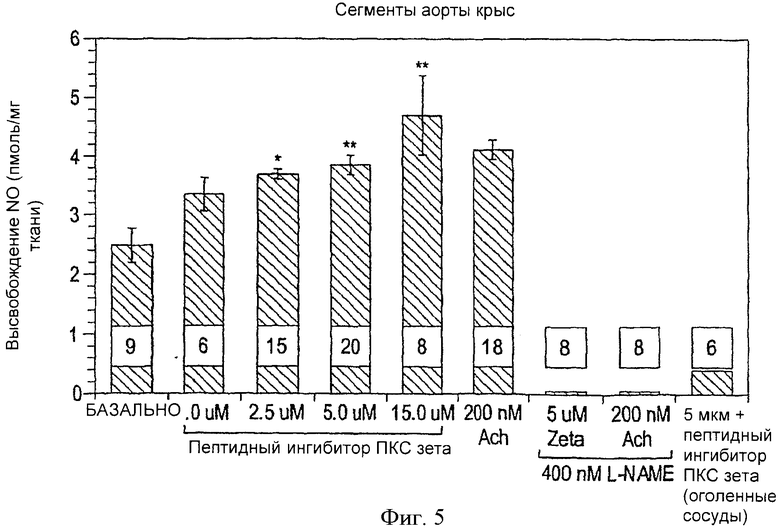
Фиг.5. Определение высвобождения NO из фрагментов аорты крыс. Высвобождение NO эндотелием достоверно увеличивалось по сравнению с базальным уровнем во фрагментах, обработанных пептидным ингибитором ПКС ζ (2.5-15 µM), равно как и ацетилхолином (Ach, 200 nM). Высвобождение NO достоверно уменьшалось в обеих группах, получавших 400 µM L-NAME, и в деэндотелизированных фрагментах. Все значения представляют собой среднее ±m. Цифры внизу столбиков означают количество отдельных экспериментов на группу. *p<0.05, **p<0.01, по сравнению с исходными значениями.
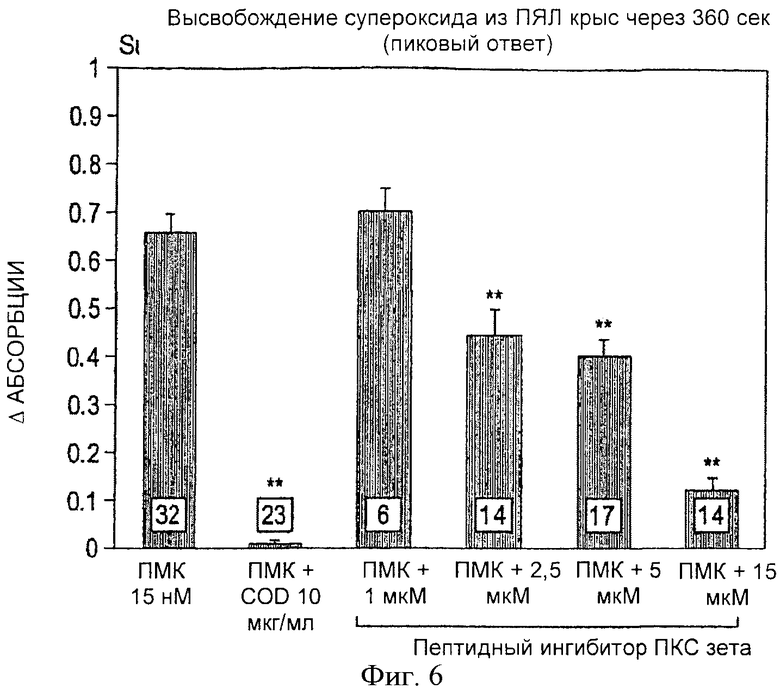
Фиг.6. Высвобождение супероксида из ПЯЛ крыс. Высвобождение супероксида исследовалось на 5×106 ПЯЛ после стимуляции форбол-12-миристат-13-ацетатом (FMA) (15 nM). В качестве положительного контроля использовалась супероксиддисмутаза (COD) (10 µg/ml). Изменение оптической плотности (Δ) измерялось через 360 сек после добавления FMA (пиковый ответ). Высвобождение супероксида достоверно подавлялось пептидным ингибитором ПКС ζ (**p<0.01, 2.5, 5 и 15 uM). Все значения представляют собой среднее ±m. Цифры внизу столбиков означают количество отдельных экспериментов на группу.
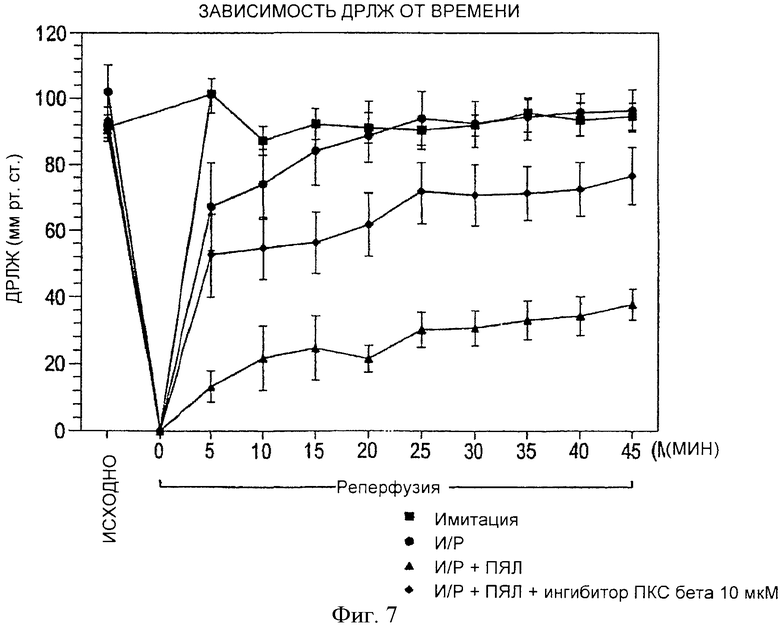
Фиг.7. Зависимость ДРЛЖ от времени в имитациях и сердцах крыс, перфузируемых в режимах И/Р, И/Р, И/Р+ПЯЛ и И/Р+ПЯЛ+βII пептидный ингибитор (10 µМ). Приводятся значения ДРЛЖ исходно, после 20-минутной ишемии и во время реперфузии от 0 до 45 минут. В группе имитаций (n=6) в течение 80-минутного протокола сохранялись стабильные значения ДРЛЖ. В группе И/Р+ПЯЛ (n=9) произошло достоверное и стойкое снижение ДРЛЖ по сравнению с группами И/Р (n=6) и И/Р+ПЯЛ+βII пептидный ингибитор (n=7). Все значения представляют собой среднее ±m. *p<0.05 и **p<0.01, по сравнению с И/Р+ПЯЛ.
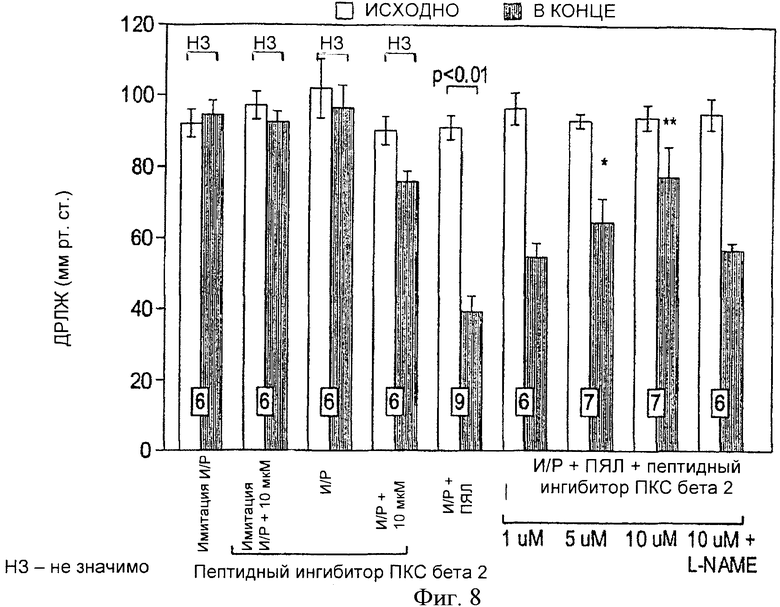
Фиг.8. Исходное и конечное ДРЛЖ в мм рт.ст. в изолированных перфузируемых сердцах крыс перед ишемией (И) (исходно) и через 45 минут после реперфузии (Р) (конечное значение). Сердца перфузировались в присутствии или в отсутствии ПЯЛ. ПЯЛ вызывали значительную контрактильную дисфункцию, которая уменьшалась под действием пептидного ингибитора ПКС βII, но достоверно блокировалась L-NAME. Все значения представляют собой среднее ±m. Число исследованных сердец указано внизу столбиков. *p<0.05 и **p<0.01, по сравнению с конечным значением И/Р+ПЯЛ; нз = не значимо.
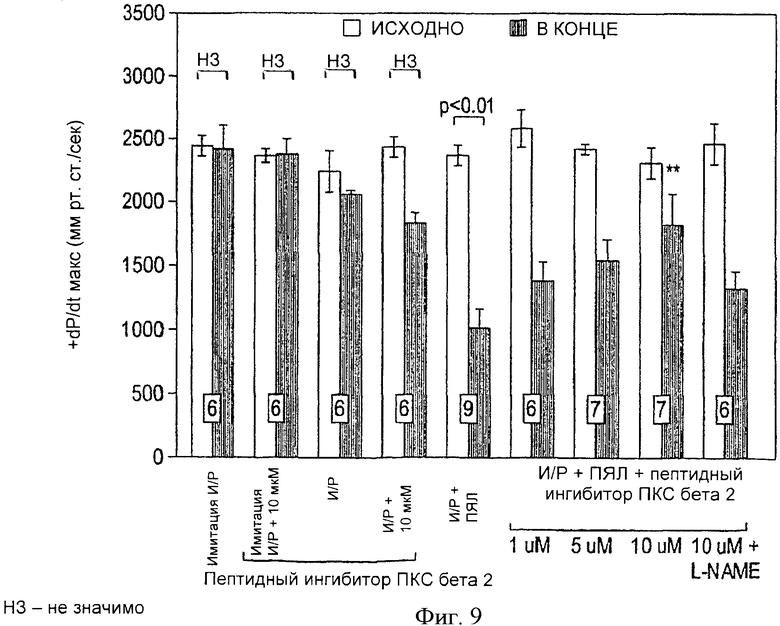
Фиг.9. Исходное и конечное ДРЛЖ+dP/dt max, выраженное в мм рт.ст./с в изолированных перфузированных сердцах крыс до ишемии (И) и после реперфузии (Р). Сердца перфузировались в присутствии или в отсутствие ПЯЛ. ПЯЛ вызывали значительную контрактильную дисфункцию, которая уменьшалась под действием пептидного ингибитора ПКС βII, но достоверно блокировалась L-NAME. Все значения представляют собой среднее ±m. Число исследованных сердец указано внизу столбиков. *p<0.05 и **P<0.01, по сравнению с конечным значением И/Р+ПЯЛ; нз = не значимо.
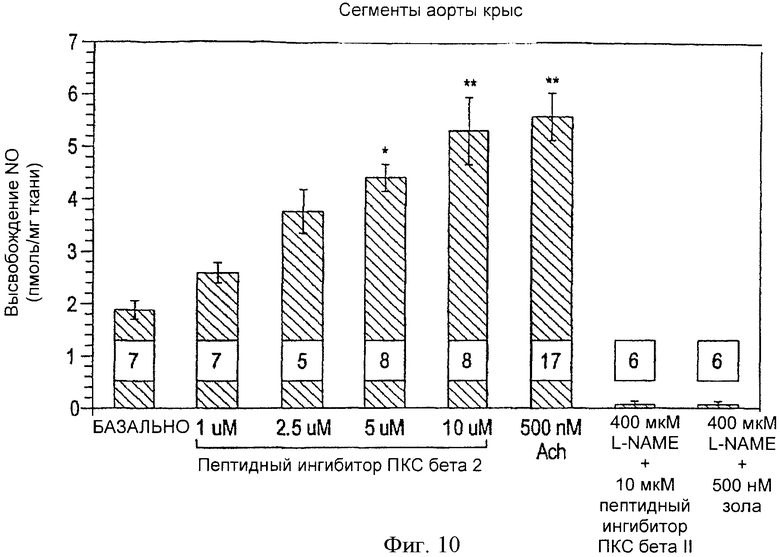
Фиг.10. Определение высвобождения NO из фрагментов аорты крыс; высвобождение NO эндотелием достоверно увеличивалось по сравнению с базальным уровнем во фрагментах, обработанных пептидным ингибитором ПКС βII (1, 2.5, 5 и 10 µM), равно как и ацетилхолином (Ach, 500 nM). Высвобождение NO достоверно уменьшалось в обеих группах, получавших 400 µM L-NAME. Все значения представляют собой среднее ±m. Цифры внизу столбиков означают количество отдельных экспериментов на группу; *p<0.05, **p<0.01, по сравнению с исходными значениями.
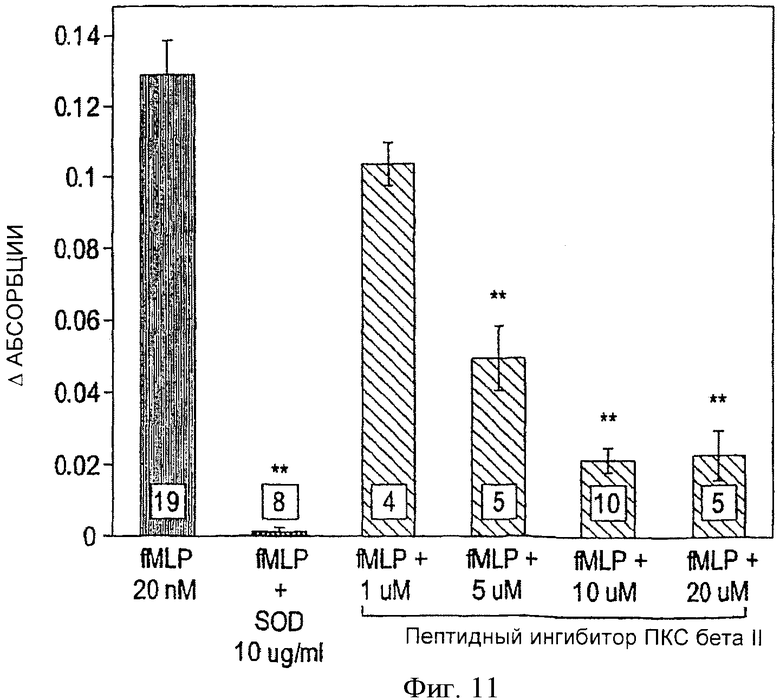
Фиг.11. Высвобождение супероксида из ПЯЛ крыс. Высвобождение супероксида исследовалось на 5×106 ПЯЛ после стимуляции формил-метионил-лейцил-фенилаланином (fMLF) (200 nM). COD (10 µg/ml) использовалась в качестве позитивного контроля. Изменение оптической плотности (Δ) измерялось через 90 сек после добавлении fMLF (пиковый ответ). Высвобождение супероксида достоверно подавлялось пептидным ингибитором ПКС βII (**p<0.01, 5,10 и 20 µM). Все значения представляют собой среднее ±m. Цифры внизу столбиков означают количество отдельных экспериментов на группу.
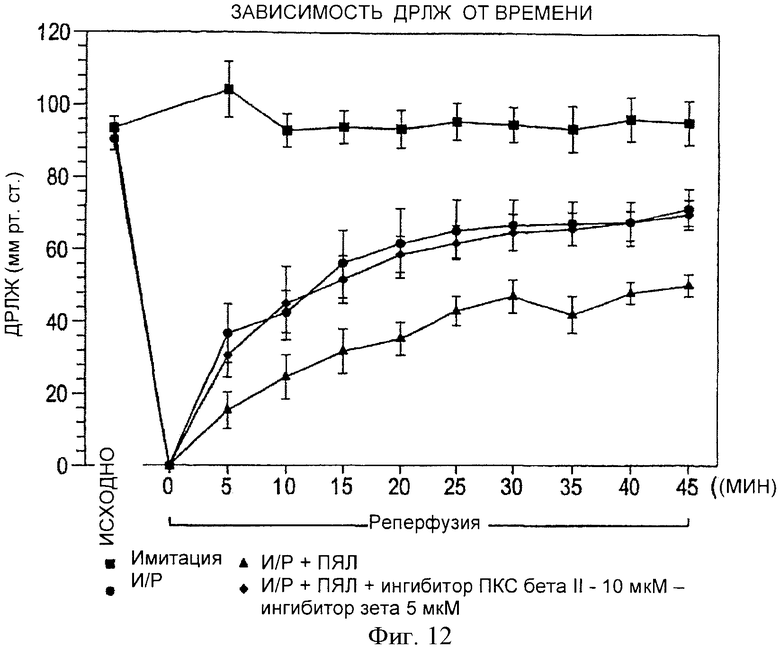
Фиг.12. Зависимость ДРЛЖ от времени в имитациях и сердцах крыс, перфузируемых в режимах И/Р, И/Р+ПЯЛ и И/Р+ПЯЛ+ПКС βII(10 µM)+ПКС ζ (5 µМ) пептидные ингибиторы. Приводятся значения ДРЛЖ исходно, после 20-минутной ишемии и во время реперфузии от 0 до 45 минут. В группе имитаций (n=6) в течение 80-минутного протокола сохранялись стабильные значения ДРЛЖ. В группе И/Р (n=6) отмечалось частичное восстановление исходных значений. В группе И/Р+ПЯЛ (n=11) отмечалось достоверное и стойкое снижение ДРЛЖ по сравнению с группой И/Р+ПЯЛ+ПКС β11 (10 µМ)+ПКС ζ (5 µМ) пептидные ингибиторы (n=7). Все значения представляют собой среднее ±m; *p<0.05 по отношению к И/Р+ПЯЛ.
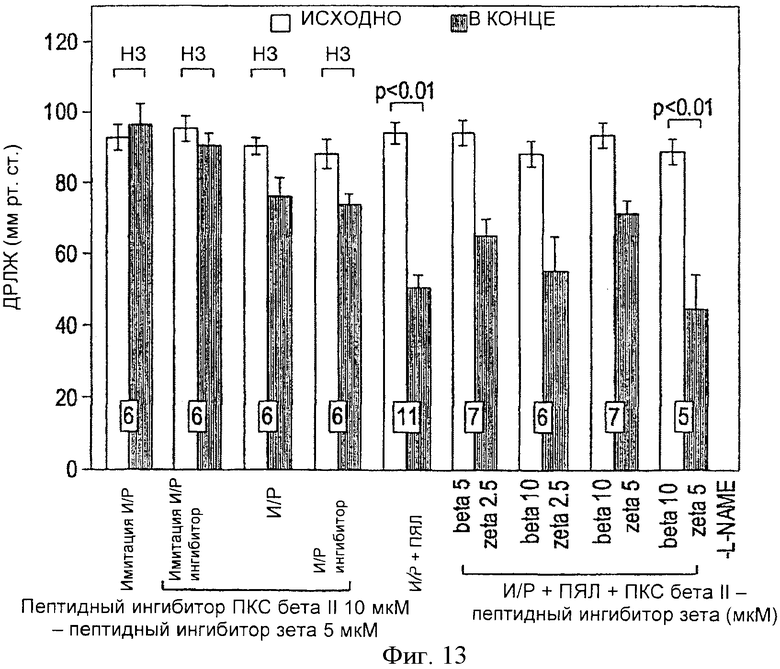
Фиг.13. Исходное и конечное ДРЛЖ в мм рт.ст. в изолированных перфузируемых сердцах крыс перед ишемией (И) (исходно) и через 45 минут после реперфузии (Р) (конечное значение). Сердца перфузировались в присутствии или в отсутствии ПЯЛ. ПЯЛ вызывали значительную контрактильную дисфункцию, которая уменьшалась под действием пептидных ингибиторов ПКС βII и ПКСζ. Этот защитный эффект блокировался L-NAME. Все значения представляют собой среднее ±m. Число исследованных сердец указано внизу столбиков; *p<0.05 по сравнению с конечным И/Р+ПЯЛ; нз = не значимо.
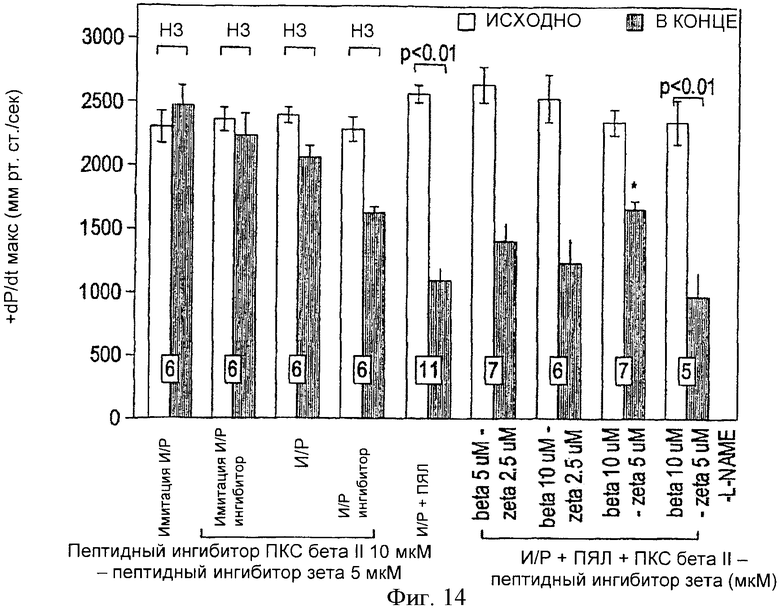
Фиг.14. Исходное и конечное ДРЛЖ+dP/dt max, выраженное в мм рт.ст./с в изолированных перфузированных сердцах крыс до ишемии (И) и после реперфузии (Р). Сердца перфузировались в присутствии или в отсутствии ПЯЛ. ПЯЛ вызывали значительную контрактильную дисфункцию, которая уменьшалась под действием пептидных ингибиторов ПКС βII и ПКСζ. Все значения представляют собой среднее ±m. Число исследованных сердец указано внизу столбиков; *р<0.05 по сравнению с конечным И/Р+ПЯЛ; нз = не значимо.
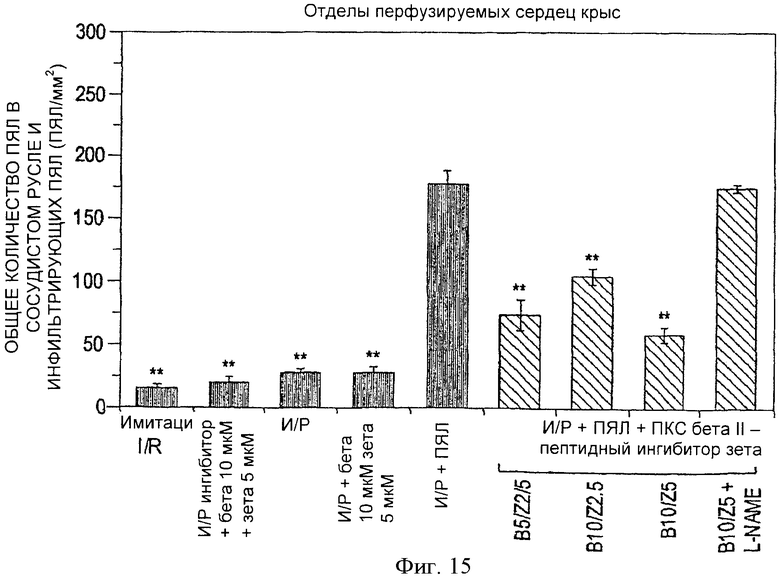
Фиг.15. Гистологическая оценка общего числа внутрисосудистых и инфильтрирующих ПЯЛ в изолированных перфузированных сердцах крыс (образцы брались у 3 крыс из группы и из 10 участков сердца). Общее число внутрисосудистых и инфильтрирующих ПЯЛ в претерпевшей реперфузию ткани сердца и прилежащих к коронарному руслу значительно уменьшалось под действием пептидных ингибиторов ПКС βII и ПКСζ. Заштрихованные столбики касаются сердец, перфузированных без ПЯЛ, а черные столбики - сердец, перфузированных ПЯЛ; **р<0.01, по сравнению с И/Р+ПЯЛ.
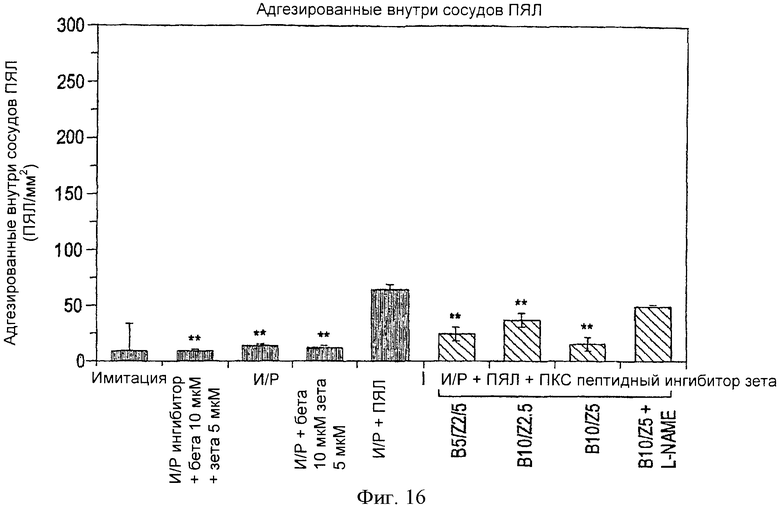
Фиг.16. Гистологическая оценка внутрисосудистых ПЯЛ, прилежащих к коронарному руслу в изолированных перфузированных сердцах крыс. Количество ПЯЛ, прилежащих к коронарному руслу в сердцах, обработанных пептидными ингибиторами ПКС βII и ПКСζ, было ниже, чем в сердцах группы И/Р+ПЯЛ. Заштрихованные столбики касаются сердец, перфузированных без ПЯЛ, а черные столбики - сердец, перфузированных ПЯЛ. Все значения представляют собой среднее количество ПЯЛ/мм2 площади сердца ±_SEM (сканирующая электронная микроскопия); р<0.01, по сравнению с И/Р+ПЯЛ.
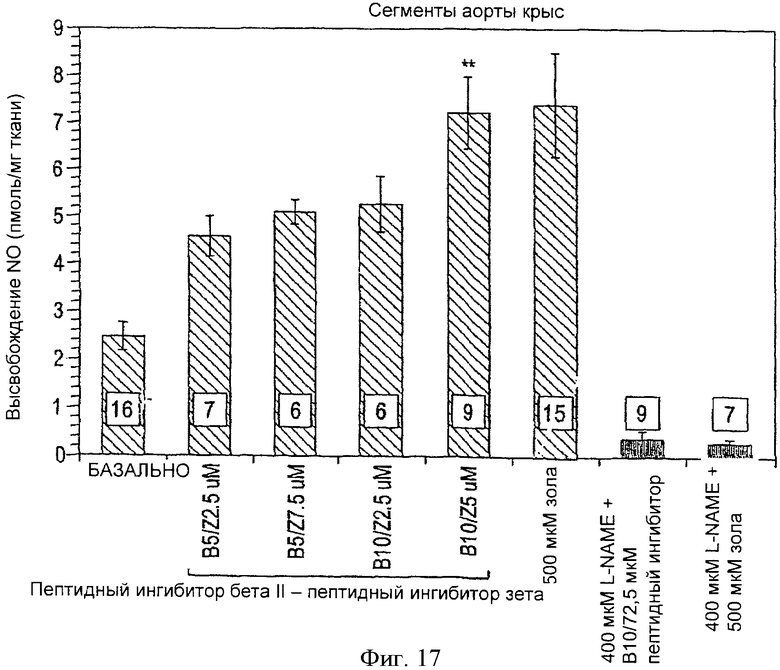
Фиг.17. Определение высвобождения NO из фрагментов аорты крыс. Высвобождение NO эндотелием достоверно увеличивалось по сравнению с базальным уровнем во фрагментах, обработанных пептидными ингибиторами ПКС βII и ПКС ζ, равно как и ацетилхолином (Ach, 500 nM). Высвобождение NO достоверно уменьшалось в обеих группах, получавших 400 µM L-NAME. Все значения представляют собой среднее ±m. Цифры внизу столбиков означают количество отдельных экспериментов на группу; **p<0.01, по сравнению с исходными значениями.
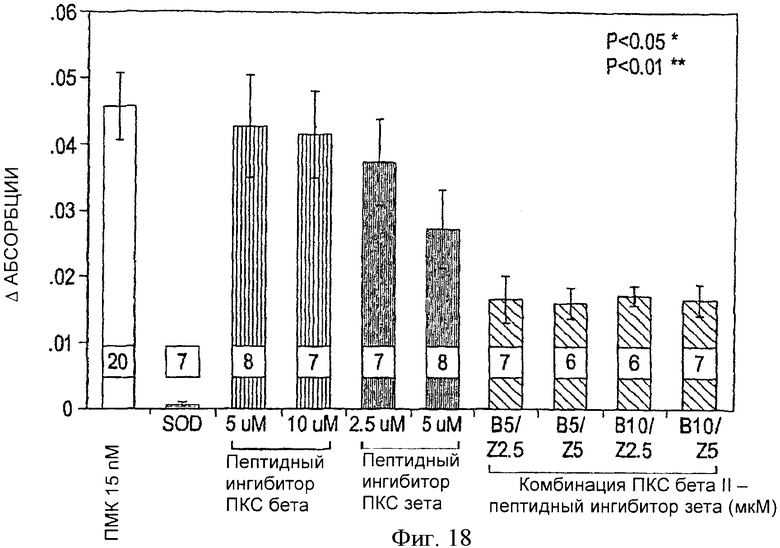
Фиг.18. Высвобождение супероксида из ПЯЛ крыс. Высвобождение супероксида исследовалось на 5×106 ПЯЛ после стимуляции FMA (15 nM). COD (10 µg/ml) использовалась в качестве позитивного контроля. Изменение оптической плотности (Δ) измерялось через 360 сек после добавлении FMA (пиковый ответ). Высвобождение супероксида достоверно подавлялось пептидными ингибиторами ПКС βII и ПКС ζ (*p<0.05, **p<0.01). Все значения представляют собой среднее ±m. Цифры внизу столбиков означают количество отдельных экспериментов на группу.
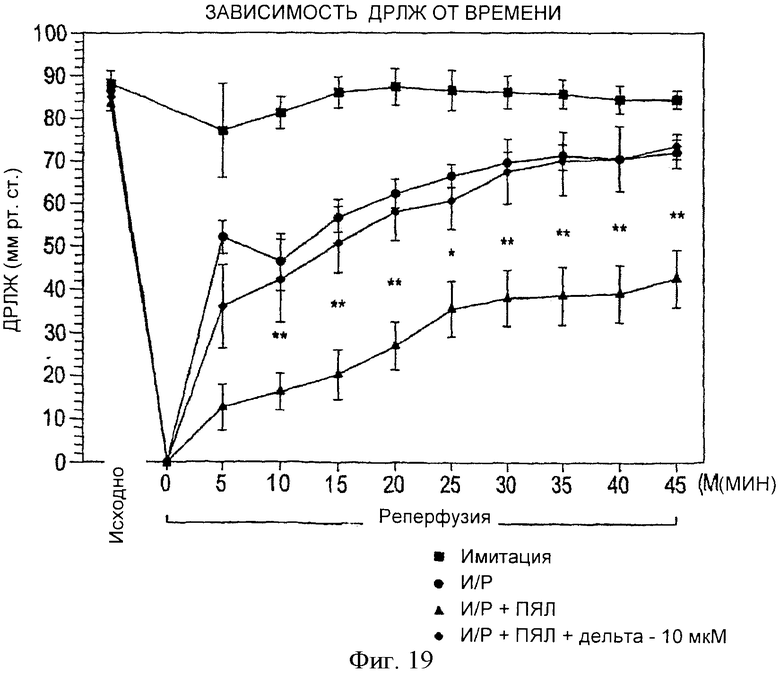
Фиг.19. Зависимость ДРЛЖ от времени в имитациях и сердцах крыс, перфузируемых в режимах И/Р, И/Р+ПЯЛ и И/Р+ПЯЛ+ПКС δ пептидный активатор (10 µM). Приводятся значения ДРЛЖ исходно, после 20-минутной ишемии и во время реперфузии от 0 до 45 минут. В группе имитаций (n=6) в течение 80-минутного протокола сохранялись стабильные значения ДРЛЖ. В группе И/Р (n=6) отмечалось восстановление исходных значений. В группе И/Р+ПЯЛ (n=6) отмечалось достоверное и стойкое снижение ДРЛЖ по сравнению с группой И/Р+ПЯЛ+ПКСδ пептидный активатор (n=6). Все значения представляют собой среднее ±SEM; **p<0.01, по отношению к И/Р+ПЯЛ.
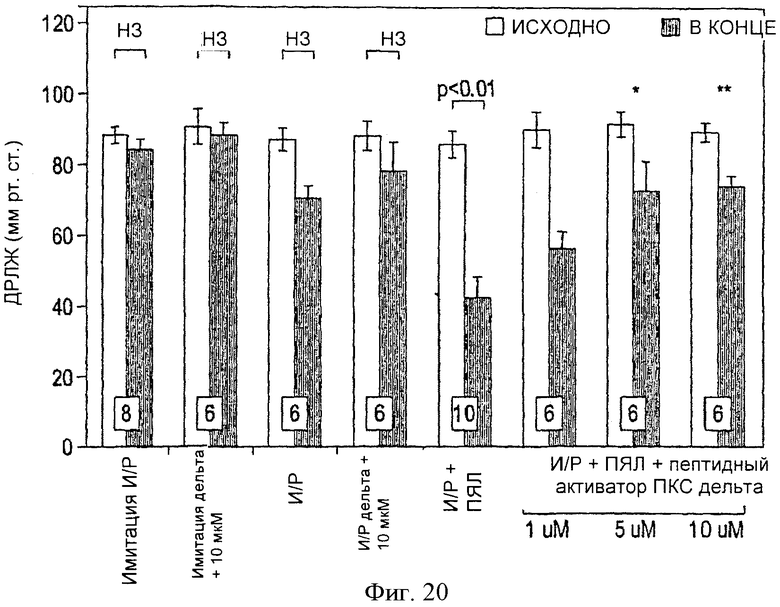
Фиг.20. Исходное и конечное ДРЛЖ в мм рт.ст. в изолированных перфузируемых сердцах крыс перед ишемией (И) (исходно) и через 45 минут после реперфузии (Р) (конечное значение). Сердца перфузировались в присутствии или в отсутствии ПЯЛ. ПЯЛ вызывали значительную контрактильную дисфункцию, которая уменьшалась под действием ПКСδ пептидного активатора. Все значения представляют собой среднее ±SEM. Количество исследованных сердец указано внизу столбиков; *p<0.05 и **p<0.01, по сравнению с конечным И/Р+ПЯЛ; нз = не значимо.
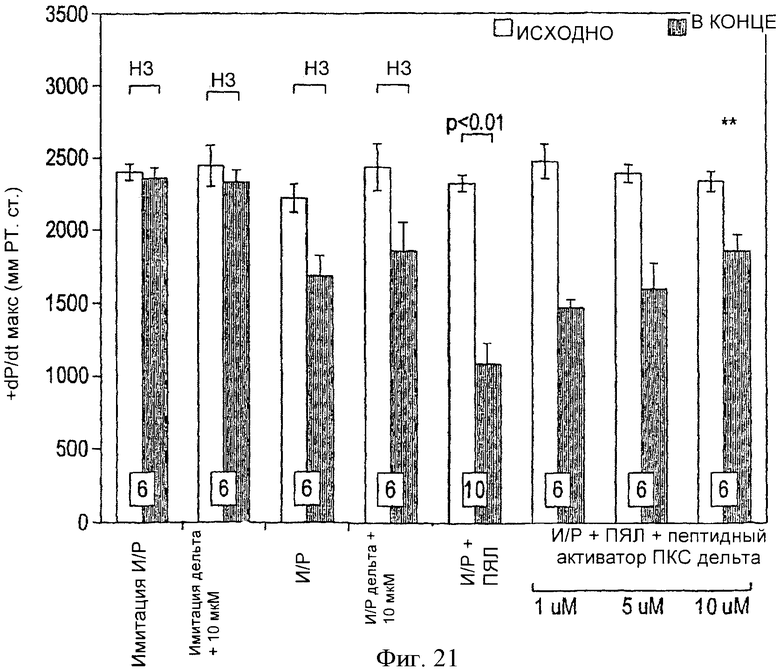
Фиг.21. Исходное и конечное ДРЛЖ+dP/dt max, выраженное в мм рт.ст./с в изолированных перфузированных сердцах крыс до ишемии (И) и после реперфузии (Р). Сердца перфузировались в присутствии или в отсутствии ПЯЛ; ПЯЛ вызывали значительную контрактильную дисфункцию, которая уменьшалась под действием ПКСδ пептидного активатора. Все значения представляют собой среднее ±m. Число исследованных сердец указано внизу столбиков; **р<0.01, по сравнению с конечным И/Р+ПЯЛ; нз = не значимо.
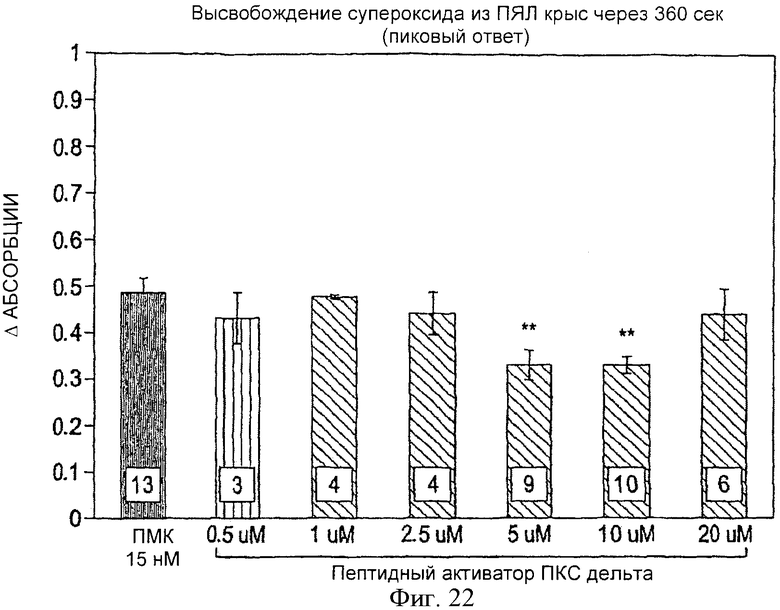
Фиг.22. Высвобождение супероксида из ПЯЛ крыс. Высвобождение супероксида исследовалось на 5×106 ПЯЛ после стимуляции FМА (15 nM). Изменение оптической плотности (Δ) измерялось через 360 сек после добавлении FMA (пиковый ответ). Высвобождение супероксида достоверно подавлялось пептидным активатором ПКС δ (**p<0.01, 5 и 10 µM). Все значения представляют собой среднее ±m. Цифры внизу столбиков означают количество отдельных экспериментов на группу.
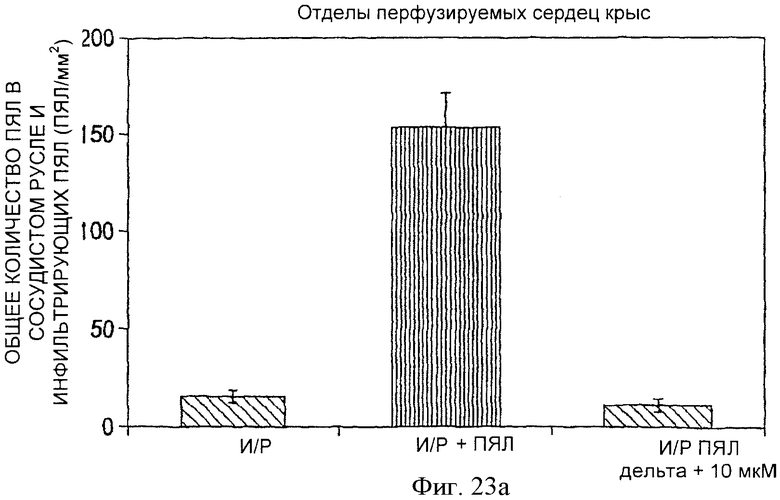
Фиг.23а. Гистологическая оценка общего числа внутрисосудистых и инфильтрирующих ПЯЛ в изолированных перфузированных сердцах крыс (образцы брались у 3 крыс из группы и из 10 участков сердца). Общее число внутрисосудистых и инфильтрирующих ПЯЛ в претерпевшей реперфузию ткани сердца и прилежащих к коронарному руслу уменьшалось под действием пептидного активатора ПКСδ. Заштрихованные столбики касаются сердец, перфузированных без ПЯЛ, а черные столбики - сердец, перфузированных ПЯЛ.
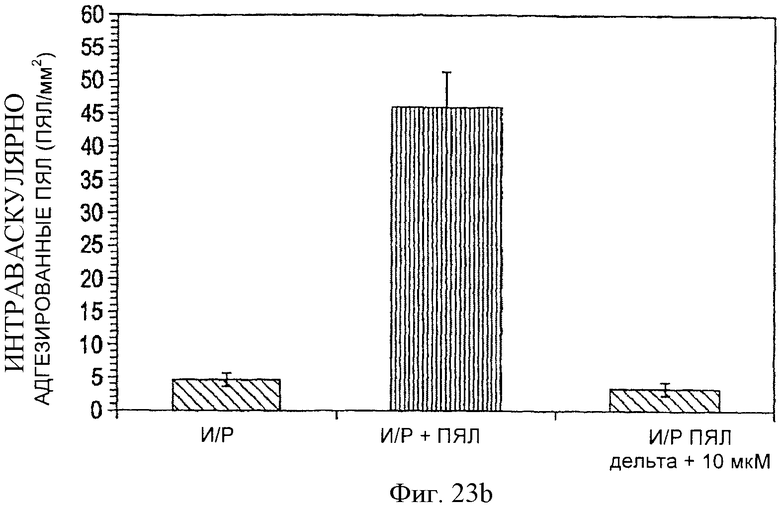
Фиг.23b. Гистологическая оценка внутрисосудистых ПЯЛ, прилежащих к коронарному руслу в образцах изолированных перфузированных сердец крыс, бравшихся у 3 крыс из группы и из 10 участков сердца. Количество ПЯЛ, прилежащих к коронарному руслу, уменьшалось под действием пептидного активатора ПКС δ. Заштрихованные столбики касаются сердец, перфузированных без ПЯЛ, а черные столбики - сердец, перфузированных ПЯЛ. Все значения представляют собой среднее количество ПЯЛ/мм2 площади сердца ±SEM.
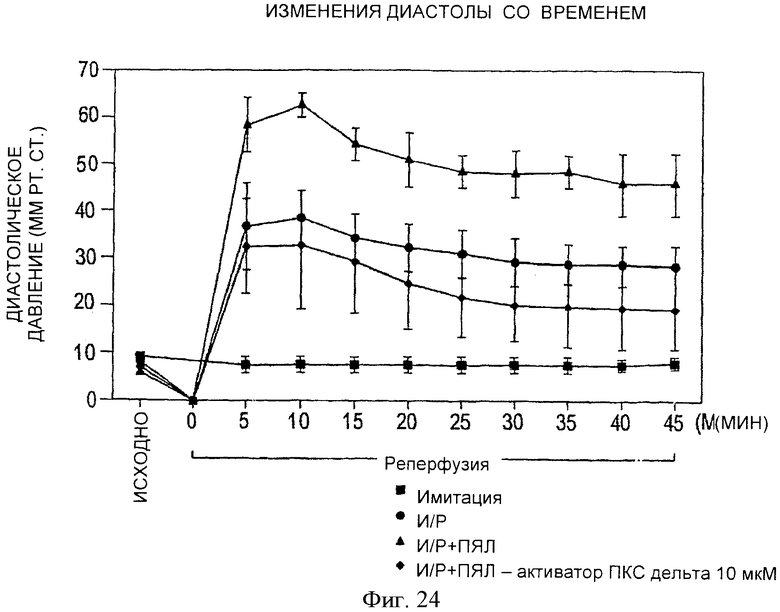
Фиг.24. Зависимость конечного диастолического давления в полости левого желудочка (ДДЛЖ) от времени в имитациях и сердцах крыс, перфузируемых в режимах И/Р, И/Р+ПЯЛ и И/Р+ПЯЛ+ПКС δ пептидный активатор (10 µМ). Приводятся значения ДДЛЖ исходно, после 20-минутной ишемии и во время реперфузии от 0 до 45 минут. В группе имитаций (n=6) в течение 80-минутного протокола сохранялись стабильные значения ДДЛЖ. В группе И/Р (n=6) отмечалось частичное восстановление исходных значений. В группе И/Р+ПЯЛ (n=6) отмечалось достоверное и стойкое повышение ДДЛЖ по сравнению с группой И/Р+ПЯЛ+ПКСδ пептидный активатор (n=6). Все значения представляют собой среднее ±SEM; *p<0.05 и **p<0.01, по отношению к И/Р+ПЯЛ.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение представляет собой раствор для консервации, перфузии и/или реперфузии органов, в особенности сердца. Раствор содержит пептидный(ые) ингибитор(ы) протеинкиназы С βII (ПКС βII) и/или протеинкиназы С ζ (ПКС ζ) и/или пептидный(ые) активатор(ы) ПКС δ. Желательно, чтобы пептидный ингибитор ПКС βII или пептидный активатор ПКС δ присутствовал в растворе в количестве около 5-10 µМ; и пептидный ингибитор ПКС ζ присутствовал в количестве приблизительно 2.5-5 µМ.
В предпочтительном воплощении пептидный ингибитор ПКС βII имеет аминокислотную последовательность SEQ ID NO: 1; пептидный ингибитор ПКС ζ имеет аминокислотную последовательность SEQ ID NO: 2; а пептидный активатор имеет аминокислотную последовательность SEQ ID NO: 3. Также желательно, чтобы пептидные ингибиторы/активаторы были миристилированы, чтобы облегчить абсорбцию в клетки органа.
В предпочтительном воплощении пептидный(ые) ингибитор(ы) или пептидный(ые) активатор(ы) растворены в растворе хлорида натрия, предпочтительно изотоническом (0.9% NaCl). Пептидные ингибитор(ы) могут также растворяться в известных консервирующих растворах, таких как растворы Кребса-Гензелейта, UW, Ст.Томас II, Коллинза, Станфордском и подобных. Раствор может также содержать натрий (Na+), калий (K+), кальций (Ca2+), магний (Mg2+), глутамат, аргинин, аденозин, маннитол, аллопуринол, глутатион, раффмозу и лактобиониковую кислоту в концентрациях приблизительно 4-7 мМ, приблизительно 0.2-0.3 мМ, приблизительно 108-132 мМ, приблизительно 13-16 мМ, приблизительно 18-22 мМ, приблизительно 2-4 мМ, приблизительно 0.5-1 мМ, приблизительно 27-33 мМ, приблизительно 0.9-1.1 мМ, приблизительно 2.7-3.3 мМ, приблизительно 25-35 мМ, и приблизительно 80-120 мМ, соответственно. Na+ может быть в форме NaOH; K+ - в форме KCl и/или KH2PO4, оптимально в соотношении примерно 2-3.5 мМ KCl и примерно 2-3.5 мМ KH2PO4; Ca2+ может присутствовать в форме CaCl2; и Mg2 может быть в форме MgCl2. Желательно поддерживать физиологический pH раствора - около 7,2-7,4.
Данный раствор может быть использован во время всех фаз трансплантации органов, особенно сердца, включая следующие (но не ограничиваясь ими): 1) изоляцию органа от донора (кардиоплегический раствор); 2) консервацию органа (хранение и транспортировка в условиях гипотермии); и 3) имплантация органа реципиенту (раствор для реперфузии).
Во время фазы перфузии или реперфузии, особенно это касается сердца, желательно поддерживать скорость перфузии органа около 1 мл/мин в течение приблизительно 5 мин. Скорость перфузии может меняться, но она не должна превышать приблизительно 25 мл/мин. В целом, скорость перфузии не должна быть столь высокой, чтобы создавать чрезмерное давление на сосудистую систему органа.
Раствор по изобретению можно приготовить следующим образом: 1) растворить пептидный(ые) ингибитор(ы) и другие компоненты в дистиллированной воде; 2) довести pH до приблизительно 7.2-7.4, например, с помощью NaOH; и 3) простерилизовать раствор, например с помощью фильтрации через 0.2 µm фильтр. Стерилизованный раствор должен затем храниться в условиях, изолированных от возможных загрязнителей окружающей среды.
Специалист может, используя предшествующее описание и следующие за ним иллюстрирующие примеры, без дальнейших пояснений приготовить и использовать компоненты настоящего изобретения и использовать заявленные способы. Следующий пример приведен для иллюстрации настоящего изобретения. Необходимо иметь в виду, что сфера применения настоящего изобретения не ограничивается специфическими условиями или деталями, описанными в примере.
Пример 1. Эффекты пептидного ингибитора ПКС ζ
Крысы-самцы Sprague Dawley (275-325 g, Ace Animals, Boyertown, PA) были подвергнуты анестезии пентобарбиталом натрия 60 мг/кг внутрибрюшинно (в/б). Также в/б вводилась натриевая соль гепарина (1,000 U). Сердца были быстро удалены, восходящие аорты канюлированы, после чего была начата ретроградная перфузия сердца модифицированными буфером Кребса при температуре 37°С и постоянном давлении 80 мм рт.ст. Буфер Кребса имел следующий состав, ммоль/л: 17 глюкозы, 120 NaCl, 25 NaHCO3, 2.5 CaCl2, 0.5 ЭДТА, 5.9 KCl, и 1.2 MgCL. Перфузирующий раствор аэрировался смесью из 95% O2 и 5% CO2, pH его поддерживалось на уровне 7.3-7.4. Два боковых разъема в перфузионной линии, находившихся проксимально по отношению к входной канюле позволяли вводить ПЯЛ, плазму без пептидного ингибитора ПКСζ (контрольные сердца) и плазму с разными концентрациями пептидного ингибитора ПКСζ (1, 2.5 или 5 µM) непосредственно в коронарное русло. Коронарный кровоток мониторировался с помощью водомера (Т106, Transonic System, Inc., Ithaca, NY). ДРЛЖ+dP/dtmax мониторировались с помощью датчика давления (SPR-524, Millar Instruments, Inc., Houston, TX), который устанавливался в полости левого желудочка. Сердца погружались в резервуар с водяной рубашкой, Содержащий 160 мл буфера Кребса, температура которого поддерживалась на уровне 37°С. Коронарный кровоток, ДРЛЖ и +dP/dt записывались с помощью регистрирующей системы Powerlab Station (ADInstruments, Grand Junction, CO), соединенной с компьютером.
ДРЛЖ, +dP/dtmax, и коронарный кровоток измерялись каждые 5 минут в течение 15 минут для того, чтобы уравновесить сердца и получить исходные измерения. ДРЛЖ определялось как конечное систолическое давление в левом желудочке минус конечное диастолическое давление в левом желудочке. Через 15 минут скорость циркуляции буфера Кребса снижалась до нуля на 20 минут с целью создания глобальной ишемии. После реперфузии в сердца вводились в течение 5 минут 200×106 ПЯЛ, взвешенных в 5 мл буфера Кребса плюс 5 мл плазмы со скоростью 1 мл/мин. В некоторых экспериментах пептидный ингибитор ПКС ζ (Genemed Synthesis, Inc., San Francisco, CA) добавлялся к плазме в конечной концентрации 1, 2.5 или 5 µM. Сердца-имитации И/Р не подвергались ишемии и не перфузировались ПЯЛ.
Использовались следующие группы изолированных перфузируемых сердец:
Группа 1: Сердца - имитации ишемии/реперфузии (И/Р) не подвергались ишемии и не перфузировались ПЯЛ, но перфузировались 5 мл плазмы (1 мл/мин) на 35-й минуте (в то же самое время, когда в сердца И/Р вводились бы 5 мл плазмы, 15 минут исходных записей плюс 20 минут ишемии). Эти сердца представляют собой контрольную группу, призванную установить, способно ли изолированное сердце крысы поддерживать ДРЛЖ и + dP/dtm в течение 80-минутного протокола (n=6).
Группа 2: Сердца - имитации И/Р + пептидный ингибитор ПКС ζ (5 µM) не подвергались ишемии и не перфузировались ПЯЛ. В эти сердца вводился пептидный ингибитор ПКС ζ (5 µM, получен при растворении в плазме 5 тМ водного раствора) на 35 минуте перфузии. Эта группа была призвана выяснить, обладает ли пептидный ингибитор ПКС ζ кардиотоническим или кардиодепрессиорным эффектом (n=6).
Группа 3: Сердца И/Р в течение 20 минут подвергались ишемии и перфузировались 5 мл плазмы (1 мл/мин) в течение первых 5 минут реперфузии, но не перфузировались ПЯЛ. Эти сердца представляли собой контрольную группу, призванную продемонстрировать, что 20-минутная ишемия с последующей реперфузией приводят к станнингу миокарда, но ДРЛЖ и + dP/dtmax восстановятся к исходным значениям максимум к концу 45-минутного периода реперфузии (n=6).
Группа 4: Сердца И/Р + пептидный ингибитор ПКС ζ (5 µM, растворенный в плазме) подвергались ишемии в течение 20 мин и не перфузировались ПЯЛ. Эти сердца перфузировались 5 мл плазмы+пептидный ингибиотор ПКС ζ в течение первых 5 мин реперфузии. Эта группа использовалась, чтобы определить, не обладает ли пептидный ингибитор ПКС ζ кардиодепрессорным эффектом в условиях И/Р при отсутствии ПЯЛ (n=6).
Группа 5: Сердца И/Р+ПЯЛ подвергались ишемии в течение 20 минут и перфузировались 5 мл плазмы (1 мл/мин) и ПЯЛ (взвешенными в 5 мл буфера Кребса) во время первых 5 минут реперфузии. Эти сердца представляли собой контрольную группу, призванную установить, приводит ли 20-минутная ишемия с последующей реперфузией в течение 45 минут в присутствии ПЯЛ (200×106) к стойкой сократительной дисфункции сердца в течение всего 45-минутного периода реперфузии по сравнению с исходными значениями (n=6).
Группа 6: Сердца И/Р+ПЯЛ + пептидный ингибитор ПКС (1 µM) подвергались ишемии в течение 20 минут и перфузировались 1 µM пептидного ингибитора ПКС ζ (растворенного в плазме) и ПЯЛ (200×106) в течение первых 5 минут реперфузии. Эти сердца представляли собой основную группу, призванную оценить эффективность ингибирования ПКС ζ для борьбы с ПЯЛ-индуцированной контрактильной дисфункцией сердца (n=6).
Группа 7: Сердца И/Р+ПЯЛ + пептидный ингибитор ПКС (2.5 µМ) подвергались ишемии в течение 20 минут и перфузировались 2.5 µМ пептидного ингибитора ПКС ζ (растворенного в плазме) и ПЯЛ (200×106) в течение первых 5 минут реперфузии. Эти сердца представляли собой группу, призванную оценить эффективность ингибирования ПКС ζ для борьбы с ПЯЛ-индуцированной контрактильной дисфункцией сердца (n=6).
Группа 8: Сердца И/Р+ПЯЛ + пептидный ингибитор ПКС (5 µМ) подвергались ишемии в течение 20 минут и перфузировались 5 µМ пептидного ингибитора ПКС ζ (растворенного в плазме) и ПЯЛ (200×106) в течение первых 5 минут реперфузии. Эти сердца представляли собой группу, призванную оценить эффективность ингибирования ПКС ζ с помощью большей концентрации пептидного ингибитора ПКСζ для борьбы с ПЯЛ-индуцированной контрактильной дисфункцией сердца (n=6).
Группа 9: Сердца И/Р+ПЯЛ + пептидный ингибитор ПКС ζ (5 µМ) + А∧-нитро-L-аргинин метил эфир (L-NAME, 50 µМ) подвергались ишемии в течение 20 минут и перфузировались 5 мин µM пептидного ингибитора ПКС ζ (растворенного в 5 мл плазмы) и 50 µM L-NAME (растворенного в буфере Клебса из 50 µМ водного препарата) и ПЯЛ (200×106) в течение первых 5 минут реперфузии. L-NAME (50 µМ) постоянно вводился в сердце в течение всего 45-минутного периода реперфузии. Эти сердца составляют группу, призванную установить, может ли кардиозащитный эффект пептидного ингибитора ПКС ζ блокироваться ингибитором синтазы оксида азота (L-NAME) (n=5).
Данные регистрировались каждые 5 минут в течение 45 минут после реперфузии. После завершения каждого эксперимента левый желудочек был изолирован, фиксирован в 4% растворе параформальдегида и хранился при температуре 4°С до последующего гистологического анализа.
На фиг.1 показана зависимость сократительной функции сердца (то есть, ДРЛЖ) от времени. Результаты, полученные в группах имитации И/Р, И/Р, И/Р+ПЯЛ + пептидный ингибитор ПКС ζ (5 µM) и И/Р+ПЯЛ демонстрируют относительные изменения ДРЛЖ во время 80-минутного периода перфузии. Как было показано, в группе имитации И/Р показатель ДРЛЖ оставался близким к или превышал 100% от исходного значения в течение всего периода перфузии. Сердца группы И/Р претерпели снижение ДРЛЖ в начале реперфузии, но восстановили до 95±7% от исходного значения к концу реперфузии. Напротив, сердца из группы И/Р+ПЯЛ претерпели тяжелую контрактильную дисфункцию, восстановившись к 45 минуте после реперфузии лишь до 47±7% от исходных значений. Наоборот, сердца из группы И/Р+ПЯЛ + пептидный ингибитор ПКСζ (5 µM) восстановились к 45 минутам после реперфузии до 84±4%.
Для того чтобы определить, не обладает ли пептидный ингибитор ПКС прямым инотропным действием на сократительную функцию сердца, неишемизированные сердца из группы имитации И/Р перфузировались пептидным ингибитором ПКСζ (5 µМ). Введение в сердца-имитации И/Р пептидного ингибитора ПКСζ, не привело к каким-либо достоверным изменениям ДРЛЖ (фиг.2) или + dP/dtmax (фиг.3) в течение 80-минутного периода перфузии, что указывает на то, что пептидный ингибитор в дозе 5 µМ не обладает непосредственным влиянием на сократительную функцию сердца. Вначале с этой целью тестировалась 15 µM концентрация пептидного ингибитора ПКС ζ, так как именно эта концентрация ассоциировалась со снижением высвобождения супероксида из ПЯЛ на 82%. Тем не менее, 15 µM обладали кардиодепрессорным эффектом (снижение ДРЛЖ на 50% в сердцах-имитациях И/Р) и не могли использоваться в этих экспериментах (данные не представлены).
На фиг.2 и 3 показаны исходные и конечные значения ДРЛЖ и + dP/dtmax в изолированных перфузируемых сердцах крыс. Исходные значения были сходными во всех группах. Тем не менее, конечные ДРЛЖ и + dP/dtmax (45 минут после реперфузии) сердец И/Р, реперфузированных с ПЯЛ, достоверно снизились (p<0.01) соответственно на 47±7% и 41±7% по сравнению с исходными значениями. Пептидный ингибитор ПКС ζ (концентрации 2.5 µМ и 5 µМ) достоверно уменьшал отрицательную динамику ДРЛЖ и + dP/dtmax, ассоциировавшуюся с постишемической реперфузией с ПЯЛ. В группе, получившей 5 µM препарата, сердца восстановили до 84±4% и 76±5% конечных ДРЛЖ и + dP/dtmax по сравнению с исходными значениями. Наименьшая эффективная доза составляла 2.5 µМ; эти сердца восстановили до 83±4% от исходного ДРЛЖ и до 75±5% от исходного + dP/dt. Кардиопротективные эффекты пептидного ингибитора ПКС ζ (5 µМ) блокировались в присутствии L-NAME (50 u-М). Эти сердца к 45 минуте после реперфузии восстановили только до 58±7% ДРЛЖ и до 54±9% + dP/dtmax. То есть эти сердца вели себя сходно с группой И/Р+ПЯЛ (47±7% и 41±7% ДРЛЖ, +dP/dtmax). Сердца, обработанные пептидным ингибитором ПКС ζ в дозе 1 µМ и подвергшиеся воздействию И/Р+ПЯЛ, восстановили к 45 минуте после реперфузии по сравнению с исходными значениями только до 57±10% и 46±6% ДРЛЖ и + dP/dtmax соответственно. Эти сердца, получившие более низкую дозу, к 45 минуте после реперфузии не отличались достоверно от контрольной группы И/Р+ПЯЛ.
Повреждение сердца, ассоциированное с И/Р, в этой модели тесно коррелировало со значительным количеством ПЯЛ, инфильтрировавших миокард в течение 45-минутного периода реперфузии. Во время реперфузии существенное число ПЯЛ мигрировало в миокард, где их число возросло к концу периода реперфузии от менее чем 25 ПЯЛ/мм2 в группе имитации И/Р до более чем 180 ПЯЛ/мм2 в сердцах группы И/Р+ПЯЛ (фиг.4а). Напротив, в сердцах, подвергшихся И/Р+ПЯЛ + пептидный ингибитор ПКС ζ, отмечалось достоверное снижение инфильтрации ткани сердца ПЯЛ на 20±6%, 46+4% и 48+3% соответственно в дозах 1, 2.5 и 5 µM (p<0.01), и этот эффект блокировался в присутствии L-NАМЕ. Более того, в сердцах, получивших дозы 2.5 и 5 µМ инфильтрация ПЯЛ была достоверно меньше выражена по сравнению с сердцами, в которые вводилась доза 1 µМ (p<0.01) (фиг.4а).
Прилегание ПЯЛ к эндотелию коронарных сосудов также исследовалось в рамках оценки общего количества внутрисосудистых и инфильтрирующих ПЯЛ. Как показано на фиг.4b, число прилежащих к коронарному эндотелию ПЯЛ достоверно не уменьшилось в сердцах группы И/Р+ПЯЛ + пептидный ингибитор ПКСζ (5 µМ) (43+10%, p<0.06) (фиг.4b). С целью выяснить, реализуется ли кардиозащитный эффект пептидного ингибитора ПКСζ за счет повышения высвобождения NO эндотелием, измерялось выделение NO эндотелием аорты крыс. На фиг.5 видно, что эндотелий, обработанный пептидным ингибитором ПКС ζ, вырабатывал достоверно больше NO на 47±2% (2.5 µМ, p<0.05), 54±5% (5 µМ, p<0.01), и 91±15% (15 µМ, p<0.01) по сравнению с базальным высвобождением NO. При использовании дозы 1 µM высвобождение NO достоверно не отличалось от базального уровня. Ацетилхолин (200 µМ) использовался в качестве положительного контроля при количественном определении М и достоверно повышал высвобождение NO на 67+4% (р0.01) по сравнению с его базальным высвобождением. Ингибитор эндотелиальной NО синтазы, L-NAME, использовался в качестве другого контроля с целью снижения базальной секреции NO до нуля. Продуцирование NO, индуцированное и ацетилхолином, и пептидным ингибитором ПКС ζ полностью подавлялось при обработке эндотелия L-NAME (400 µМ). Чтобы установить, что источником NO являлся именно эндотелий, образцы деэндотелизированных сегментов аорты крыс инкубировались с пептидным ингибитором ПКС ζ (5 µМ); результаты не отличались от сегментов, обработанных L-NAME.
Другой механизм кардиопротективного действия пептидного ингибитора ПКСζ может быть связан с подавлением высвобождения супероксида. Пептидный ингибитор ПКСζ достоверно снижал высвобождение супероксида на 33-82% (2,5-15 µМ, p<0.01), за исключением дозы в 1µМ, при которой результаты не отличались от суспензий, стимулированных FМА ПЯЛ крыс (фиг.6). COD (10 µg/mL) использовалась как положительный контроль при количественном анализе супероксида и деградировала выработанный стимулированными FМА крысиными ПЯЛ супероксид на 99% (p<0.01; фиг.6).
Пример 2. Действие пептидного ингибитора ПКС βII
Эксперименты с пептидными ингибиторами ПКС βII проводились в значительной мере аналогично описанному в Примере 1 для пептидных ингибиторов ПКСζ.
Использовались следующие группы изолированных перфузируемых сердцах крыс:
Группа 1: Сердца-имитации И/Р не подвергались ишемии и не перфузировались с ПЯЛ, но перфузировались с 5 мл плазмы (1 мл/мин) на 35 минуте перфузии (в то же самое время, когда в сердца из группы И/Р вводились бы 5 мл плазмы, 15 минут записи исходных значений плюс 20 минут ишемии). Эти сердца представляли собой контрольную группу, призванную установить, может ли изолированное сердце крысы поддерживать стабильный уровень ДРЛЖ и + dP/dtmax в течение 80-минутного протокола (n=6).
Группа 2: Имитация И/Р + пептидный ингибитор ПКС βII (10 µМ). Эти сердца не подвергались ишемии и не перфузировались с ПЯЛ. В эти сердца вводили пептидный ингибитор ПКС βII (10 µM, растворенный в плазме из 5 mM водного препарата) на 35 минуте перфузии. Эта группа была призвана определить, не обладает ли пептидный ингибитор ПКС βII кардиотоническим или кардиодепрессорным эффектом (n=6).
Группа 3: Сердца И/Р подвергались ишемии на 20 минут и перфузировались 5 мл плазмы (1 мл/мин) в течение первых 5 мин реперфузии, но не перфузировались с ПЯЛ. Эти сердца представляют собой контрольную группу, целью которой было установить, что 20 минут ишемии с последующей реперфузией вызывают станнинг миокарда, но ДРЛЖ и + dP/dtmax восстанавливаются к исходным значениям к концу 45-минутного периода реперфузии (n=6).
Группа 4: И/Р + пептидный ингибитор ПКС βII (10 µM, растворенный в плазме). Эти сердца подвергались 20-минутной ишемии, но не перфузировались ПЯЛ. Их перфузировали в течение первых 5 минут реперфузии с 5 мл плазмы + пептидным ингибитором ПКС βII. Эта группа предназначалась для того, чтобы установить, не обладает ли пептидный ингибитор ПКС βII кардиодепрессорным действием в условиях И/Р в отсутствие ПЯЛ (n=6).
Группа 5: Сердца группы И/Р+ПЯЛ подвергались 20-минутной ишемии и перфузировались в течение первых 5 минут реперфузии 5 мл плазмы (1 мл/мин) и ПЯЛ (в виде суспензии в 5 мл буфера Кребса). Эти сердца представляли собой контрольную группу, призванную установить, вызывает ли 20-минутная ишемия с последующей 45-минутной реперфузией в присутствии ПЯЛ (200×106) стойкую сократительную дисфункцию сердца, сохраняющуюся в течение всего 45-минутного периода реперфузии, по сравнению с исходными значениями (n=9).
Группа 6: И/Р+ПЯЛ + пептидный ингибитор ПКС βII (1 µM). Эти сердца подвергались 20-минутной ишемии и перфузировались в течение первых 5 минут реперфузии 1 µМ пептидного ингибитора ПКС βII (растворенного в плазме) и ПЯЛ (200×106). Целью этой группы сердец было установить эффективность ингибирования ПКС βII при борьбе с ПЯЛ-индуцированной контрактильной дисфункцией сердца (n=6).
Группа 7: И/Р+ПЯЛ + пептидный ингибитор ПКС βII (5 µМ). Сердца подвергались 20-минутной ишемии и перфузировались в течение первых 5 минут реперфузии 5цМ пептидного ингибитора ПКС βII (растворенного в плазме) и ПЯЛ (200×106).
Эти сердца представляли собой группу, призванную установить эффективность ингибирования ПКС βII с помощью большей концентрации пептидного ингибитора ПКС βII при борьбе с ПЯЛ-индуцированной контрактильной дисфункцией сердца (n=7).
Группа 8: И/Р+ПЯЛ + пептидный ингибитор ПКС βII (10 µМ). Сердца подвергались 20-минутной ишемии и перфузировались в течение первых 5 минут реперфузии 10 µM пептидного ингибитора ПКСβII (растворенного в плазме) и ПЯЛ (200×106). Эти сердца представляли собой группу, призванную установить эффективность ингибирования ПКС βII с помощью большей концентрации пептидного ингибитора ПКС βII при борьбе с ПЯЛ-индуцированной контрактильной дисфункцией сердца (n=7).
Группа 9: И/Р+ПЯЛ + пептидный ингибитор ПКС βII (10 µМ) + NG-нитро-L-аргинин метил эфир (L-NAME, 50 µМ). Сердца подвергались 20-минутной ишемии и перфузировались в течение первых 5 минут реперфузии 10 µМ пептидного ингибитора ПКС βII (растворенного в 5 мл плазмы), 50 µM L-NAME (растворенного в буфере Кребса из 50 µМ водного препарата) и ПЯЛ (200×106). L-NAME (50 µM) постоянно вводился в сердце в течение 45-минутного периода реперфузии. Эти сердца составляли группу, целью которой было определить, может ли кардиозащитный эффект пептидного ингибитора ПКСβII блокироваться добавлением ингибитора синтазы оксида азота (L-NAME) (n=6).
Предыдущие исследования показали, что сердца-имитации И/Р при введении ПЯЛ не претерпевали никаких изменений по сравнению с исходными контрольными значениями (Lefer и др., Circulation 100: 178-184, 1999). Результаты фиксировались каждые 5 минут в течение 45 минут после реперфузии. После каждого эксперимента левый желудочек изолировался, фиксировался в 4% параформальдегиде и хранился перед последующим гистрологическим анализом при 4°С.
Рисунок 7 демонстрирует зависимость сократительной функции сердца (ДРЛЖ) от времени в группах имитации И/Р, И/Р, И/Р+ПЯЛ + пептидный ингибитор ПКС βII (10 µM) и И/Р+ПЯЛ, и иллюстрирует динамику ДРЛЖ в течение 80 минут перфузии. Сердца группы имитации И/Р поддерживали 103±4% от исходных значений ДРЛЖ в течение всего периода перфузии. Сердца в группе И/Р претерпели снижение ДРЛЖ в течение начальных стадий реперфузии, но к концу этого периода восстановили до 94±6% от исходных значений. Однако в группе И/Р+ПЯЛ развилась тяжелая сократительная дисфункция сердец, и к концу периода реперфузии восстановилось только 43±5% от исходных значений. Напротив, сердца группы И/Р+ПЯЛ+пептидный ингибитор ПКС βII (10 µM), хотя и испытали вначале снижение ДРЛЖ на 61±10% от исходных значений на 15 минуте реперфузии, восстановились до 82±9% от исходного уровня.
Для того чтобы установить, обладает ли пептидный ингибитор ПКС βII какими-либо прямыми инотропным воздействием на сердце, сердца группы имитации И/Р перфорировались пептидным ингибитором ПКС βII (10 µM). Эта группа в исследовании играла роль одной из контрольных групп. Эти сердца не продемонстрировали сколько-нибудь значимой динамики ДРЛЖ (фиг.8) или + dP/dtmax (фиг.9) к концу 80 минуты периода реперфузии, что указывает на то, что данная доза пептидного ингибитора ПКС βII не обладает прямым влиянием на сократительную функцию сердца. Доза пептидного ингибитора ПКС βII тестировалась на сердце - имитации И/Р, и в этой дозе также не было отмечено никаких кардиодепрессорных эффектов.
Фиг.8 и 9 демонстрируют исходные и конечные значения ДРЛЖ и + dP/dtmax изолированных перфузируемых сердец крыс соответственно. Между исходными значениями во всех изучаемых группах не было достоверной разницы. Также не было достоверных различий между исходными и конечными значениями ДРЛЖ и + dP/dt в группах имитации И/Р, И/Р, имитации И/Р + пептидный ингибитор ПКС βII (5 µМ), и И/Р + пептидный ингибитор ПКС βII (10 µM). Однако разница между исходными и конечными значениями ДРЛЖ и + dP/dtmax в группе И/Р+ПЯЛ была достоверной. На 45 минуте постреперфузии отмечалось достоверное (p<0.01) снижение относительно исходного уровня ДРЛЖ на 43±5% и + dP/dtmax на 42±6%.
Присутствие пептидного ингибитора ПКС βII в дозах 5 µМ и 10 µМ уменьшало выраженность снижения ДРЛЖ и + dP/dtmax, ассоциированного с постишемической перфузией с ПЯЛ. Доза 10 µМ обладала наибольшим кардиопротективным эффектом, так как сердца группы И/Р+ПЯЛ + пептидный ингибитор ПКС βII (10 µM) к 45 минуте постреперфузии восстановили до 82±9% от исходного ДРЛЖ и до 79±10% от исходного + dP/dtmax. Эти значения достоверно отличались от показателей, полученных в группе И/Р+ПЯЛ на 45-й минуте постреперфузии (p<0.01). Доза в 5 µМ также демонстрировала кардиозащитный эффект, хотя и не столь выраженный, как при введении 10 µM, так как сердца из группы И/Р+ПЯЛ + пептидный ингибитор ПКС βII (5 µМ) к 45-й минуте постреперфузии восстановили до 69±7% от исходного ДРЛЖ и до 63±7% от исходного + dP/dtmax. Значения ДРЛЖ, полученные при введении дозы 5 µМ, к 45 минуте постреперфузии достоверно отличались от группы И/Р+ПЯЛ (p<0.05). Доза пептидного ингибитора ПКС βII 1 µМ не обладала кардиопротективным эффектом, так как сердца из группы И/Р+ПЯЛ + пептидный ингибитор ПКС βII (1 µM) восстановили только до 57±4% ДРЛЖ и 53±6%. Конечные значения ДРЛЖ и + dP/dtmax в группе, получившей дозу 1 µМ, достоверно не отличались от конечных значений в группе И/Р+ПЯЛ.
В группе И/Р+ПЯЛ + пептидный ингибитор ПКС βII (10 µМ) + L-NAME (50 µМ) кардиозащитный эффект 10 βII пептидного ингибитора ПКС βII блокировался в присутствии L-NAME (50 µМ), поскольку значения ДРЛЖ и + dP/dtmax к концу 45-й минуты реперфузионного периода составляли соответственно только 56±2% и 53±5% от исходных и достоверно не отличались от конечных показателей в группе И/Р+ПЯЛ (фиг.3 и 4).
Чтобы уточнить, реализуется ли кардиозащитный эффект пептидного ингибитора ПКС βII через увеличение продукции NO эндотелием, измерялось высвобождение NO из эндотелия аорты крыс. На фиг.10 показано, что обработанные пептидным ингибитором ПКС βII в дозах 5 µМ и 10 µМ фрагменты эндотелия генерировали достоверно больше NO по сравнению с базальным высвобождением NO (p<0.05 и p<0.01 соответственно). Зафиксированное базальное значение высвобождения NO составило 1.85±0.18 пмоль NO/мг ткани. При стимуляции эндотелия пептидным ингибитором ПКС βII отмечался четкий дозозависимый эффект, поскольку его дозы в 1 µМ, 2.5 µМ, 5 µМ и 10 µМ вызывали превышение базальных значений высвобождения NO соответственно на 0.75±0.19, 1.91±0.44, 2.54±0.29 и 3.49±0.62 пмоль NO)/мг ткани.
Ацетилхолин (Ach, 500 nM) использовался при данном количественном анализе в качестве положительного контроля и стимулировал эндотелий, вызывая превышение базальных значений на 3.75±0.58 пмоль NO/мг ткани. L-NAME использовался в качестве еще одного контроля с целью снижения базального высвобождения NO до нуля. Выработка NO, стимулированная и ацетилхолином, и пептидным ингибитором ПКС βII, полностью подавлялась при обработке эндотелия L-NAME (400 µM).
Еще одним механизмом реализации кардиозащитных эффектов (т.е. влияния на ДРЛЖ) пептидного ингибитора ПКС βII может быть подавление высвобождения супероксида из ПЯЛ. Пептидный ингибитор ПКС βII в дозах 5 µM, 10 µМ и 20 µМ достоверно снижал высвобождение супероксида (то есть оптическую плотность) суспензиями стимулированных фМЛФ крысиных ПЯЛ от 0.13±0.01 до 0.05±0.009 (p<0.01), 0.02±0.004 (p<0.01), и 0.02±.007 (p 0.01) соответственно (фиг.11). В дозе 1 µМ не отмечалось достоверного подавления выделения супероксида. SOD (10 мг/мл) использовалась в качестве положительного контроля и приводила к разложению супероксида, выделенного стимулированными фМЛФ крысиными ПЯЛ, уменьшая ответ до 0.0016±0.0006.
Пример 3. Эффекты комбинации пептидных ингибиторов ПКС βII и ПКСζ
Эксперименты с пептидными ингибиторами ПКС βII и ПКСζ проводились в значительной мере аналогично описанным в Примерах 1 и 2.
Использовались следующие группы изолированных перфузируемых сердец крыс:
Группа 1: Сердца-имитации И/Р не подвергались ишемии и не перфузировались с ПЯЛ, но перфузировались с 5 мл плазмы (1 мл/мин) на 35 минуте перфузии (в то же самое время, когда в сердца из группы И/Р вводились бы 5 мл плазмы, 15 минут записи исходных значений плюс 20 минут ишемии). Эти сердца представляли собой контрольную группу, призванную установить, может ли изолированное сердце крысы поддерживать стабильный уровень ДРЛЖ и + dP/dtmax в течение 80-минутного протокола (n=6).
Группа 2: Имитация И/Р + пептидные ингибиторы ИКС βII (10 µM) и ПКСζ (5 µМ). Эти сердца не подвергались ишемии и не перфузировались с ПЯЛ. В эти сердца вводили пептидные ингибиторы ПКС βII и ПКС ζ (соответственно 10 µМ и 5 µМ, растворенные в плазме из 5 mM водного препарата) на 35 минуте перфузии. Эта группа была призвана определить, не обладают ли пептидные ингибиторы кардиотоническим или кардиодепрессорным эффектом (n=6).
Группа 3: Сердца И/Р подвергались ишемии на 20 минут и перфузировались 5 мл плазмы (1 мл/мин) в течение первых 5 мин реперфузии, но не перфузировались с ПЯЛ. Эти сердца представляли собой контрольную группу, целью которой было установить, что 20 минут ишемии с последующей реперфузией вызывают станнинг миокарда, но ДРЛЖ и + dP/dtmax восстанавливаются к исходным значениям к концу 45-минутного периода реперфузии (n=6).
Группа 4: И/Р + пептидные ингибиторы ПКС βII (10 µМ) и ПКС ζ (5 µМ) (растворенные в плазме). Эти сердца подвергались 20-минутной ишемии, но не перфузировались ПЯЛ. Их перфузировали в течение первых 5 минут реперфузии с 5 мл плазмы + пептидными ингибиторами ПКС βII и ПКС ζ. Эта группа предназначалась для того, чтобы установить, не обладают ли пептидные ингибиторы кардиодепрессорным действием в условиях И/Р в отсутствие ПЯЛ (n=6).
Группа 5: Сердца группы И/Р+ПЯЛ подвергались 20-минутной ишемии и перфузировались в течение первых 5 минут реперфузии 5 мл плазмы (1 мл/мин) и ПЯЛ (в виде суспензии в 5 мл буфера Кребса). Эти сердца представляли собой контрольную группу, призванную установить, вызывает ли 20-минутная ишемия с последующей 45-минутной реперфузией в присутствии ПЯЛ (200×106) стойкую сократительную дисфункцию сердца, сохраняющуюся в течение всего 45-минутного периода реперфузии, по сравнению с исходными значениями (n=11).
Группа 6: И/Р+ПЯЛ + пептидные ингибиторы ПКС βII (5 µМ) и ПКС ζ (2.5 µМ). Эти сердца подвергались 20-минутной ишемии и перфузировались в течение первых 5 минут реперфузии 1 µМ пептидного ингибитора ПКС βII (растворенного в плазме) и ПЯЛ (200×106). Целью этого эксперимента было установить эффективность ингибирования ПКС βII при борьбе с ПЯЛ-индуцированной контрактильной дисфункцией сердца (n=7).
Группа 7: И/Р+ПЯЛ + пептидные ингибиторы ПКС βII (10 µМ) и ПКС ζ (2.5 µМ). Эти сердца подвергались 20-минутной ишемии и перфузировались в течение первых 5 минут реперфузии 5 цµМ пептидного ингибитора ПКС βII (растворенного в плазме) и ПЯЛ (200×106). Целью этого эксперимента было установить эффективность ингибирования ПКС βII с помощью большей концентрации пептидного ингибитора ПКС βII при борьбе с ПЯЛ-индуцированной контрактильной дисфункцией сердца (n=6).
Группа 8: И/Р+ПЯЛ + пептидные ингибиторы ПКС βII (10 µМ) и ПКС ζ (5 µМ). Эти сердца подвергались 20-минутной ишемии и перфузировались в течение первых 5 минут реперфузии 10 µМ пептидного ингибитора ПКС βII (растворенного в плазме) и ПЯЛ (200×106). Целью этого эксперимента было установить эффективность ингибирования ПКС βII с помощью большей концентрации пептидного ингибитора ПКС βII при борьбе с ПЯЛ-индуцированной контрактильной дисфункцией сердца (n=7).
Группа 9: И/Р+ПЯЛ + пептидные ингибиторы ПКС βII (10 µМ) и ПКС ζ (5 µМ) + N-нитро-L-аргинин метил эфир (L-NAME, 50 µМ). Сердца подвергались 20-минутной ишемии и перфузировались в течение первых 5 минут реперфузии 10 µМ пептидного ингибитора ПКС βII (растворенного в 5 мл плазмы), 50 µМ L-NAME (растворенного в буфере Кребса из 50 mМ водного препарата) и ПЯЛ (200×106). L-NAME (50 µМ) постоянно вводился в сердце в течение 45-минутного периода реперфузии. Эти сердца составляли группу, целью которой было определить, может ли кардиозащитный эффект пептидных ингибиторов блокироваться добавлением ингибитора синтазы оксида азота (L-NAME) (n=5).
Из графика на фиг.12 видно, что комбинация пептидных ингибиторов ПКС βII (10 µM) и ПКС ζ (5 µМ) привела к скорости восстановления, приближающейся к сердцам И/Р. Это не наблюдалось при использовании пептидных ингибиторов ПКС βII (10 µМ) или ПКС ζ (5 µМ) в режиме монотерапии (Примеры 1 и 2), в которых скорость восстановления сердца, обработанного пептидным ингибитором, была ниже, чем в группе И/Р.
На фиг.13 и 14 показаны начальные и конечные значения соответственно ДРЛЖ и + dP/dtmax изолированных перфузируемых сердец. Как и ожидалось, подобно наблюдавшемуся в Примерах 1 и 2, исходные и конечные значении ДРЛЖ и + dP/dtmax в группе И/Р+ПЯЛ достоверно различались, при этом ДРЛЖ к 45-й минуте постреперфузии снизилось приблизительно на 50%, а + dP/dtmax - на 45% по сравнению с исходными значениями (p<0.01).
Присутствие пептидных ингибиторов ПКС βII и ПКСζ уменьшало ассоциированное с постишемической перфузией с ПЯЛ снижение ДРЛЖ и+dР/dtmax.Дозы пептидных ингибиторов ПКС βII 10 µМ и ПКСζ 5 µM обладали наибольшим кардиозащитным действием. Увеличение дозы пептидного ингибитора ПКС βII с 5 µМ до 10 µМ не привело к достоверному увеличению кардиозащитного эффекта.
С другой стороны, повышение дозы пептидного ингибитора ПКС ζ с 2.5 µМ до 5 µМ привело к пограничному повышению кардиозащитной активности.
Кардиозащитные эффекты комбинации пептидных ингибиторов ПКС βII и ПКС ζ блокировались в присутствии L-NAME (50 µМ) в группе И/Р+ПЯЛ + пептидные ингибиторы ПКС β11 (10 µM) и ПКС ζ (5 µМ) + L-NAME (50 µМ), поскольку значения ДРЛЖ и + dP/dtmax к концу 45-минутного периода реперфузии составляли лишь соответственно около 50% и 40% от исходных значений, и достоверно не отличались от конечных значений в группе И/Р+ПЯЛ (фиг.13 и 14).
Ассоциированное с И/Р повреждение сердца в этой модели тесно коррелировало с существенным числом ПЯЛ, инфильтрировавших миокард в течение 45-минутного периода реперфузии. Во время реперфузии значительное количество ПЯЛ мигрировало в миокард, где их число к концу периода реперфузии возросло с менее 25 ПЯЛ /мм2 в группе имитации И/Р до более 175 ПЯЛ/мм2 в сердцах И/Р+ПЯЛ (фиг.15). Напротив, в сердцах группы И/Р+ПЯЛ + пептидные ингибиторы ПКС β11 и ПКС ζ отмечалось достоверное уменьшение выраженности инфильтрации ПЯЛ ткани сердца во время постреперфузии. Этот эффект блокировался в присутствии L-NAME. Более того, удвоение дозы пептидного ингибитора ПКС βII с 5 µМ до 10 µМ при константной дозе пептидного ингибитора ПКС ζ в 2.5 µМ, не приводило к достоверному уменьшению инфильтрации ПЯЛ. С другой стороны, удвоение дозы пептидного ингибитора ПКС ζ с 2.5 µМ до 5 µM при сохранении неизменной дозы пептидного ингибитора ПКС βII в 10 µМ приводит к пограничному уменьшению инфильтрации ПЯЛ (фиг.15).
Прилегание ПЯЛ к эндотелию коронарных сосудов также исследовалось в рамках оценки общего количества внутрисосудистых и инфильтрирующих ПЯЛ. Как показано на фиг.16, число прилегающих к коронарному эндотелию ПЯЛ уменьшалось в сердцах группы И/Р+ПЯЛ + пептидные ингибиторы ПКС βII и ПКС ζ. Этот защитный эффект терялся в присутствии L-NAME.
На фиг.17 в эндотелии сердец, обработанных пептидными ингибиторами ПКС βII и РКС ε, наблюдается достоверно более выраженное высвобождение NO, особенно при использовании дозы 10 мкМ.
Сравнение воздействия пептидных ингибиторов ПКС βII и ПКС ε 5 мкМ на базальное высвобождение NO.
В анализе на NO ацетилхолин (500 нМ) использовался в качестве положительного контроля. При его применении происходит достоверное увеличение высвобождения NO по сравнению с базальным высвобождением NO. L-NAME использовался в качестве другого контроля в целью снижения базального высвобождения NO до нуля. Продукция NO, вызванная как ацетилхолином, так и пептидными ингибиторами, полностью ингибировалась при обработке эндотелия при помощи L-NAME (400 мкМ).
Другой механизм кардиопротективных эффектов пептидных ингибиторов ПКС βII и ПКС ε может быть связан с ингибированием высвобождения супероксида. Как видно из фиг.18, при применении комбинации пептидных ингибиторов ПКС βII и ПКС ε происходит значительное ингибирование высвобождения супероксида по сравнению с применением суспензий ПЯЛ у крыс, стимулированных ПМК, или по сравнению с применением ингибиторов ПКС βII и ПКС ε по отдельности. COD (10 мкг/мл) использовалась в качестве положительного контроля в анализе на супероксид и приводила к снижению высвобождения супероксида в ПЯЛ у ПМК-стимулированных крыс на 99% (фиг.18).
Все примеры свидетельствуют о том, что присутствие достаточного количества пептидного ингибитора ПКС βII и/или пептидного ингибитора ПКС ε обеспечивает развитие выраженного кардиопротективного эффекта за счет ослабления ПЯЛ-индуцированной сердечной дисфункции.
Пример 4 - Эффекты пептидного активатора ПКС δ
Эксперименты с использованием пептидного активатора ПКС δ в большинстве случаев выполнялись, как описано в Примере 1 для пептидного ингибитора ПКС δ.
Использовались следующие группы изолированных перфузированных сердец крыс:
Группа 1: Сердца из группы с имитацией И/Р не подвергались воздействию ишемии и не перфузировались с ПЯЛ, но перфузировались 5 мл плазмы (1 мл/мин) в течение 35 минут (в тот момент, когда сердца, подвергающиеся И/Р, обрабатывались 5 мл плазмы, в течение 15 минут проводилась исходная регистрация, а в течение 20 мин создавались условия ишемии). Эти сердца составляли контрольную группу, которая служила для определения, способны ли изолированные сердца крыс поддерживать ДРЛЖ и + dP/dtmax по протоколу в течение 80 минут (n=6).
Группа 2: Сердца с имитацией И/Р + сердца с пептидным ингибитором ПКС δ (10 мкМ) не подвергались воздействию ишемии и не перфузировались ПЯЛ. На эти сердца воздействовали при помощи пептидного активатора ПКС δ (10 мкМ, исходно представленного в виде 5 мМ основного раствора в H2O, растворенного в плазме) при перфузии в течение 35 минут. Эта группа использовалась для решения вопроса о том, оказывает ли пептидный активатор ПКС 5 кардиотонический или кардиосупрессивный эффект (n=6).
Группа 3: Сердца, подвергающиеся И/Р, в течение 20 минут подвергались воздействию ишемии и перфузировались при помощи 5 мл плазмы (1 мл/мин) в течение первых 5 минут реперфузии, но не перфузировались ПЯЛ. Эти сердца представляли собой контрольную группу, используемую для решения вопроса о том, вызывает ли ишемия, действующая в течение 20 минут и следующая за ней реперфузия, эффект оглушения в сердце, однако ДРЛЖ и + dP/dtmax возвращались к исходным значениям (начальным значениям) к конце 45-минутного периода реперфузии (n=6).
Группа 4: Сердца, подвергавшиеся воздействию И/Р+обработанные пептидным активатором ПКС δ (10 мкМ, растворенный в плазме) подвергались воздействию ишемии в течение 20 минут и не перфузировались ПЯЛ. Сердца перфузировались с использованием 5 мл плазмы+пептидного активатора ПКС δ в течение первых 5 минут реперфузии. Эта группа использовалась для того, чтобы определить, оказывает ли пептидный активатор ПКС δ кардиосупрессивный эффект в условиях И/Р без воздействия ПЯЛ (n=6).
Группа 5: Сердца, на которые воздействовали с использованием И/Р и ПЯЛ, в течение 20 минут подвергались ишемии и перфузировались 5 мл плазмы (1 мл/мин) и ПЯЛ (в виде суспензии в 5 мл буфера Кребса) в течение первых 5 минут реперфузии. Эти сердца представляли контрольную группу, использующуюся для определения, приводит ли ишемия в течение 20 минут, за которой следует реперфузия в течение 45 минут в присутствии ПЯЛ (200×106), к развитию устойчивой сократительной дисфункции сердца в течение 45-минутного реперфузионного периода по сравнению с начальными и исходными значениями (n=10).
Группа 6: Сердца, на которые воздействовали с использованием И/Р+ПЯЛ + пептидного активатора (1 мкМ), подвергались воздействию ишемии в течение 20 минут и перфузировались с использованием пептидного ингибитора ПКС βII 1 мкМ (растворенного в плазме) и ПЯЛ (200×106) в течение первых 5 минут реперфузии. Эти сердца использовались в качестве группы для определения эффекта активации ПКС δ на ослабление ПЯЛ-индуцированной дисфункции сократительной способности сердца (n=6).
Группа 7: Сердца, на которые воздействовали с использованием И/Р+ПЯЛ + пептидного активатора ПКС δ (5 мкМ), подвергались ишемии в течение 20 минут и перфузировались пептидным ингибитором ПКС βII 1 мкМ (растворенным в плазме) и ПЯЛ (200×106) в течение первых 5 минут реперфузии. Эти сердца использовались в качестве группы для определения эффекта активации ПКС δ при более высокой концентрации пептидного активатора ПКС δ для ослабления ПЯЛ-индуцированной дисфункции сократительной способности сердца (n=6).
Группа 8: Сердца, на которые воздействовали с использованием И/Р+ПЯЛ + пептидного активатора ПКС δ (10 мкМ), подвергались ишемии в течение 20 минут и перфузировались пептидным ингибитором ПКС βII 1 мкМ (растворенным в плазме) и ПЯЛ (200×106) в течение первых 5 минут реперфузии. Эти сердца использовались в качестве группы для определения эффекта активации ПКС δ при более высокой концентрации пептидного активатора ПКС δ для ослабления ПЯЛ-индуцированной дисфункции сократительной способности сердца (n=6).
В предыдущих исследованиях было показано, что для сердец, подвергающихся воздействию И/Р и ПЯЛ, не наблюдается изменений по сравнению с исходными контрольными значениями (Lefer и др., Chirculation 100; 178-184, 1999). Данные регистрировались через каждые 5 минут в течение 45 минут после реперфузии. После каждого эксперимента проводилась изоляция левого желудочка и фиксация при помощи параформальдегида. Препараты сохранялись при температуре 4°С для проведения дальнейшего гистологического исследования.
На фиг.19 показан характер сократительной функции сердца (ДРЛЖ) для следующих групп: имитации И/Р, И/Р, И/Р+ПЯЛ + пептидный активатор ПКС δ (10 мкМ) и И/Р+ПЯЛ, и проиллюстрированы изменения ДРЛЖ в течение 80 мин периода перфузии. Для сердец из группы имитации И/Р значения ДРЛЖ находились в пределах 103±4% от начальных исходных значений в течение всего периода перфузии. Для сердец из группы И/Р наблюдалось снижение ДРЛЖ в течение начальных стадий реперфузии, но в конце периода реперфузии эти значения возвращались к уровню 82±3% от исходных базальных значений. Однако для сердец из группы И/Р+ПЯЛ отмечалась тяжелая дисфункция сократимости сердца, и к концу периода перфузии восстановление сократительной функции сердца происходило только на 46±9% от исходных значений. Напротив, для сердец из группы И/Р+ПЯЛ + пептидный активатор ПКС δ (10 мкМ), хотя и первоначально отмечалось снижение ДРЛЖ до 58±8% от исходных значений, через 15 минут проведения реперфузии, происходило восстановление этого показателя до 83±3%.
С целью установления, оказывает ли пептидный активатор ПКС δ прямые инотропные эффекты на сократительную функцию сердца, сердца с имитацией И/Р перфузировались при помощи пептидного активатора ПКС δ (10 мкМ). Эта группа служила в исследовании в качестве одной из контрольных групп. В сердцах не выявлялось каких-либо значительных изменений ДРЛЖ (фиг.20) или + dP/dtmax (фиг.21) в конце периода перфузии длительностью 80 минут, что указывает на то, что при использовании такой дозы пептидный активатор ПКС δ не обладает прямым влиянием на сократительную функцию сердца.
На фиг.20 и 21 показаны исходные и конечные значения ДРЛЖ и + dP/dtmax соответственно для перфузируемых изолированных сердец. Достоверных различий между начальными исходными значениями во всех исследуемых группах выявлено не было. Также не выявлялось достоверных различий между исходными и конечными значениями ДРЛЖ и + dP/dtmax для групп имитации И/Р, И/Р, имитации И/Р + пептидный активатор ИКС δ и И/Р+ИКС δ (10 мкМ). Однако выявлялись значительные различия в исходных и конечных значениях ДРЛЖ и + dP/dtmax для группы И/Р+ПЯЛ. Наблюдалось значительное снижение (p<0,01) от исходных базальных значений для ДРЛЖ до 46±9% и для +dP/dtmax до 45±8% через 45 минут после реперфузии.
Присутствие пептидного активатора ПКС δ в дозе 5 мкМ и 10 мкМ ослабляет снижение ДРЛЖ и + dP/dtmax, связанное с постишемической перфузией ПЯЛ. Доза 10 мкМ оказывала более выраженный кардиозащитный эффект, так как в сердцах из группы И/Р+ПЯЛ + пептидный активатор ПКС δ (10 мкМ) наблюдалось восстановление значений для ДРЛЖ и + dP/dtmax соответственно до 80±9% и 67±7% от исходных базальных значений через 45 минут после реперфузии. Значения достоверно отличались от значений, полученных для группы И/Р+ПЯЛ через 45 минут после реперфузии (p<0,01). Доза 5 мкМ также оказывала кардиозащитный эффект, но не в такой степени, как доза 10 мкМ, так как в группе сердец И/Р+ПЯЛ + пептидный активатор ПКСδ (5 мкМ) значения ДРЛЖ и + dP/dtmax восстанавливались соответственно до 80±9% до 67±7% от исходных начальных значений через 45 минут после реперфузии. Значения ДРЛЖ для дозы 5 мкМ статистически достоверно отличались от группы И/Р+ПЯЛ через 45 минут после реперфузии (p<0,05).
Доза 1 мкМ пептидного активатора ПКСδ не обладала кардиозащитным эффектом, так как значения ДРЛЖ и + dP/dtmax в группе сердец И/Р+ПЯЛ + пептидный активатор ПКС δ (1 мкМ) восстанавливались соответственно только до 60±13% и 51±5%. Конечные значения ДРЛЖ и + dP/dtmax в группе, где применялась доза 1 мкМ, достоверно не отличались от конечных значений в группе И/Р+ПЯЛ.
Механизм, который способствует кардиопротективным эффектам (т.е. ДРЛЖ) пептидного активатора ПКС δ, может быть связан с ингибированием высвобождения супероксиддисмутазы из ПЯЛ. Пептидный активатор ПКС δ значительно ингибирует высвобождение супероксида (т.е. абсорбцию) из суспензии ПЯЛ крыс, стимулированных ПМК, с 0,49±0,03 до 0,32±0,03 (p<0,01) для дозы 5 мкМ и 0,32+0,02 (p<0,01) для дозы 10 мкМ (фиг.22). Значительного ингибирования супероксида при дозе 1 мкМ не отмечалось.
Хотя некоторые из предпочтительных воплощений данного изобретения были описаны, для специалистов очевидно, что различные модификации описанных и показанных здесь воплощений могут быть выполнены без отклонения от его сути и объема. В соответствии с этим предполагается, что данное изобретение ограничивается только прилагаемой формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОНСЕРВАЦИИ ОРГАНОВ | 2006 |
|
RU2440131C2 |
| ПРИМЕНЕНИЕ КАРИПОРИДА ДЛЯ УМЕНЬШЕНИЯ НЕЖЕЛАТЕЛЬНЫХ ВОЗДЕЙСТВИЙ МАКРОЛИДНЫХ АНТИБИОТИКОВ ПРИ ИШЕМИИ И РЕПЕРФУЗИИ СЕРДЦА | 1998 |
|
RU2252754C2 |
| Способ рекондиционирования донорского сердца | 2021 |
|
RU2777097C1 |
| ПРИМЕНЕНИЕ РАСБУРИКАЗЫ ДЛЯ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ РАССТРОЙСТВ ИЛИ КОСВЕННЫХ ОСЛОЖНЕНИЙ НА СЕРДЦЕ, ВЫЗВАННЫХ ПРИСТУПАМИ ИШЕМИИ ИЛИ РЕПЕРФУЗИЕЙ | 2008 |
|
RU2482187C2 |
| СПОСОБ УМЕНЬШЕНИЯ ОКИСЛИТЕЛЬНОГО ПОВРЕЖДЕНИЯ (ВАРИАНТЫ) | 2005 |
|
RU2376028C2 |
| СПОСОБ ОЦЕНКИ СОСТОЯНИЯ МИОКАРДА ПРИ КАРДИОХИРУРГИЧЕСКИХ ВМЕШАТЕЛЬСТВАХ В УСЛОВИЯХ КАРДИОПЛЕГИЧЕСКОЙ ЗАЩИТЫ | 2017 |
|
RU2651364C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОИШЕМИЧЕСКОЙ АКТИВНОСТЬЮ В ЭКСПЕРИМЕНТАЛЬНОЙ КАРДИОЛОГИИ | 1988 |
|
RU2007985C1 |
| СПОСОБ ОЦЕНКИ КАРДИОПРОТЕКТИВНОЙ АКТИВНОСТИ ФАРМАКОЛОГИЧЕСКИХ СРЕДСТВ | 2017 |
|
RU2643104C1 |
| Способ защиты миокарда от ишемического и реперфузионного повреждения в эксперименте | 2021 |
|
RU2776770C1 |
| 5-ГИДРОКСИНИКОТИНАТ КАЛИЯ, ОБЛАДАЮЩИЙ КАРДИОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2017 |
|
RU2640580C1 |
Настоящее изобретение относится к области фармацевтической промышленности, в частности к раствору для перфузии, консервации и/или реперфузии органов, особенно сердца, с целью трансплантации. Раствор содержит, по меньшей мере, один пептидный ингибитор протеинкиназы СβII (ПКС βII), представляющий собой SEQ ID No:1, и/или, по меньшей мере, один пептидный ингибитор протеинкиназы С ζ (ПКС ζ), представляющий собой SEQ ID No:2 или Go6983, и/или, по меньшей мере, один пептидный активатор протеинкиназы С δ (ПКС δ), представляющий собой SEQ ID No:2. Описываются также способы применения раствора, включая способ консервации органа для трансплантации, защиты ишемизированного органа от повреждения, уменьшения дисфункции органа после ишемии, сохранения высвобождения оксида азота в ишемизированном органе и защиты органа от повреждения при изоляции от циркуляции. Настоящее изобретение позволяет более эффективно защитить трансплантируемый орган от реперфузионного повреждения после ишемии. 6 н. и 92 з.п. ф-лы, 26 ил.
1. Раствор для перфузии, консервации и/или реперфузии изъятого органа, содержащий по меньшей мере один пептидный ингибитор протеинкиназы С βII (ПКС βII) и/или по меньшей мере один пептидный ингибитор протеинкиназы С ζ (ПКС ζ) и/или по крайней мере один пептидный активатор ПКС δ, при этом по меньшей мере один пептидный ингибитор ПКС βII представляет собой SEQ ID No:1 и его концентрация составляет приблизительно 5-10 мкМ, по меньшей мере один пептидный активатор ПКС δ представляет собой SEQ ID No:3 и его концентрация составляет приблизительно 5-10 мкМ, по меньшей мере один пептидный ингибитор ПКС ζ выбран из группы, состоящей из SEQ ID No:2 и Go6983 и его концентрация составляет приблизительно 2,5-5 мкМ.
2. Раствор по п.1, в котором пептидные ингибиторы растворены в солевом растворе.
3. Раствор по п.1, дополнительно содержащий хлорид калия.
4. Раствор по п.1, где орган представляет собой сердце.
5. Раствор по п.1, где орган представляет собой орган млекопитающего.
6. Раствор по п.5, где орган млекопитающего представляет собой орган человека.
7. Раствор по п.1, где орган представляет собой орган, предназначенный для трансплантации.
8. Раствор по п.1, в котором пептидные ингибиторы/активатор меристилированы.
9. Способ сохранения органов, предназначенных для трансплантации, включающий перфузирование органа раствором по п.1.
10. Способ по п.9, при котором пептидные ингибиторы/активатор растворены в солевом растворе.
11. Способ по п.9, дополнительно включающий использование хлорида калия.
12. Способ по п.9, при котором по меньшей мере один ингибитор ПКС βII представляет собой SEQ ID NO:1.
13. Способ по п.9, при котором по меньшей мере один активатор ПКС δ представляет собой SEQ ID No:3.
14. Способ по п.9, при котором по меньшей мере один ингибитор ПКС ζ представляет собой SEQ ID No:2 и Go6983.
15. Способ по п.9, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС βII составляет приблизительно 5-10 мкМ.
16. Способ по п.9, при котором концентрация по меньшей мере одного пептидного активатора ПКС δ составляет приблизительно 5-10 мкМ.
17. Способ по п.9, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС ζ составляет приблизительно 2,5-5 мкМ.
18. Способ по п.9, при котором орган представляет собой сердце.
19. Способ по п.9, при котором орган представляет собой орган млекопитающего.
20. Способ по п.19, при котором орган млекопитающего представляет собой орган человека.
21. Способ по п.9, при котором орган представляет собой орган, предназначенный для трансплантации.
22. Способ по п.9, при котором пептидные ингибиторы/активатор меристилированы.
23. Способ по п.9, при котором перфузию проводят со скоростью менее 20 мл/мин.
24. Способ по п.9, при котором перфузию проводят со скоростью около 1 мл/мин.
25. Способ по п.9, при котором перфузия представляет собой ретроградную перфузию.
26. Способ по п.9, при котором перфузию проводят в течение примерно 5 мин.
27. Способ защиты ишемизированного органа от повреждений, включающий перфузию органа раствором по п.1.
28. Способ по п.27, при котором пептидные ингибиторы/активаторы растворены в солевом растворе.
29. Способ по п.27, дополнительно включающий использование хлорида калия.
30. Способ по п.27, при котором по меньшей мере один ингибитор ПКС βII представляет собой SEQ ID No:1.
31. Способ по п.27, при котором по меньшей мере один активатор ПКС δ представляет собой SEQ ID No:3.
32. Способ по п.27, при котором по меньшей мере один ингибитор ПКС ζ представляет собой SEQ ID No:2 и Go6983.
33. Способ по п.27, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС βII составляет приблизительно 5-10 мкМ.
34. Способ по п.27, при котором концентрация по меньшей мере одного пептидного активатора ПКС δ составляет приблизительно 5-10 мкМ.
35. Способ по п.27, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС ζ составляет приблизительно 2,5-5 мкМ.
36. Способ по п.27, при котором орган представляет собой сердце.
37. Способ по п.27, при котором орган представляет собой орган млекопитающего.
38. Способ по п.37, при котором орган представляет собой орган человека.
39. Способ по п.27, при котором орган представляет собой орган, предназначенный для трансплантации.
40. Способ по п.27, при котором пептидные ингибиторы/активатор меристилированы.
41. Способ по п.27, при котором перфузию проводят со скоростью менее 20 мл/мин.
42. Способ по п.27, при котором перфузию проводят со скоростью около 1 мл/мин.
43. Способ по п.27, при котором перфузия представляет собой ретроградную перфузию.
44. Способ по п.27, при котором перфузию проводят в течение примерно 5 мин.
45. Способ уменьшения дисфункции органа после ишемии, включающий перфузию органа раствором по п.1.
46. Способ по п.45, при котором пептидные ингибиторы/активаторы растворены в солевом растворе.
47. Способ по п.45, дополнительно включающий использование хлорида калия.
48. Способ по п.45, при котором по меньшей мере один ингибитор ПКС βII представляет собой SEQ ID №:1.
49. Способ по п.45, при котором по меньшей мере один активатор ПКС δ представляет собой SEQ ID №:3.
50. Способ по п.45, при котором по меньшей мере один ингибитор ПКС ζ представляет собой SEQ ID №:2 и Go6983.
51. Способ по п.45, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС βII составляет приблизительно 5-10 мкМ.
52. Способ по п.45, при котором концентрация по меньшей мере одного пептидного активатора ПКС δ составляет приблизительно 5-10 мкМ.
53. Способ по п.45, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС ζ составляет приблизительно 2,5-5 мкМ.
54. Способ по п.45, при котором орган представляет собой сердце.
55. Способ по п.45, при котором орган представляет собой орган млекопитающего.
56. Способ по п.55, при котором орган представляет собой орган человека.
57. Способ по п.45, при котором орган представляет собой орган, предназначенный для трансплантации.
58. Способ по п.45, при котором пептидные ингибиторы/активатор меристилированы.
59. Способ по п.45, при котором перфузию проводят со скоростью менее 20 мл/мин.
60. Способ по п.45, при котором перфузию проводят со скоростью менее 1 мл/мин.
61. Способ по п.45, при котором перфузия представляет собой ретроградную перфузию.
62. Способ по п.45, при котором перфузию проводят в течение примерно 5 мин.
63. Способ поддержания высвобождения оксида азота в ишемизированном органе, включающий перфузию органа раствором по п.1.
64. Способ по п.63, при котором пептидные ингибиторы/активаторы растворены в солевом растворе.
65. Способ по п.63, дополнительно включающий использование хлорида калия.
66. Способ по п.63, при котором по меньшей мере один ингибитор ПКС βII представляет собой SEQ ID №:1.
67. Способ по п.63, при котором по меньшей мере один активатор ПКС δ представляет собой SEQ ID №:3.
68. Способ по п.63, при котором по меньшей мере один ингибитор ПКС ζ представляет собой SEQ ID №:2 и Go6983.
69. Способ по п.63, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС βII составляет приблизительно 5-10 мкМ.
70. Способ по п.63, при котором концентрация по меньшей мере одного пептидного активатора ПКС δ составляет приблизительно 5-10 мкМ.
71. Способ по п.63, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС ζ составляет приблизительно 2,5-5 мкМ.
72. Способ по п.63, при котором орган представляет собой сердце.
73. Способ по п.63, при котором орган представляет собой орган млекопитающего.
74. Способ по п.73, при котором орган млекопитающего представляет собой орган человека.
75. Способ по п.63, при котором орган представляет собой орган, предназначенный для трансплантации.
76. Способ по п.63, при котором пептидные ингибиторы/активатор меристилированы.
77. Способ по п.63, при котором перфузию проводят со скоростью менее 20 мл/мин.
78. Способ по п.63, при котором перфузию проводят со скоростью менее 1 мл/мин.
79. Способ по п.63, при котором перфузия представляет собой ретроградную перфузию.
80. Способ по п.63, при котором перфузию проводят в течение примерно 5 минут.
81. Способ защиты органа от повреждения после изоляции от системы кровообращения, включающий перфузию органа раствором по п.1.
82. Способ по п.81, при котором пептидные ингибиторы/активаторы растворены в солевом растворе.
83. Способ по п.81, дополнительно включающий использование хлорида калия.
84. Способ по п.81, при котором по меньшей мере один ингибитор ПКС βII представляет собой SEQ ID №:1.
85. Способ по п.81, при котором по меньшей мере один активатор ПКС δ представляет собой SEQ ID №:3.
86. Способ по п.81, при котором по меньшей мере один ингибитор ПКС ζ представляет собой SEQ ID №:2 и Go6983.
87. Способ по п.81, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС βII составляет приблизительно 5-10 мкМ.
88. Способ по п.81, при котором концентрация по меньшей мере одного пептидного активатора ПКС δ составляет приблизительно 5-10 мкМ.
89. Способ по п.81, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС ζ составляет приблизительно 2,5-5 мкМ.
90. Способ по п.81, при котором орган представляет собой сердце.
91. Способ по п.81, при котором орган представляет собой орган млекопитающего.
92. Способ по п.91, при котором орган млекопитающего представляет собой орган человека.
93. Способ по п.81, при котором орган представляет собой орган, предназначенный для трансплантации.
94. Способ по п.81, при котором пептидные ингибиторы/активатор меристилированы.
95. Способ по п.81, при котором перфузию проводят со скоростью менее 20 мл/мин.
96. Способ по п.81, при котором перфузию проводят со скоростью менее 1 мл/мин.
97. Способ по п.81, при котором перфузия представляет собой ретроградную перфузию.
98. Способ по п.81, при котором перфузию проводят в течение примерно 5 мин.
| Сердечник для отливки полых металлических предметов | 1936 |
|
SU53007A1 |
| JP 5139992 A, 08.06.1993 | |||
| JP 2002060346 A, 26.02.2002 | |||
| JOHNSON JA et al | |||
| A protein kinase C translocation inhibitor as an isozyme-selective antagonist of cardiac function | |||
| J Biol Chem | |||
| Предохранительное устройство для паровых котлов, работающих на нефти | 1922 |
|
SU1996A1 |
| WO 9817299 A1, 30.04.1998. | |||
Авторы
Даты
2010-08-27—Публикация
2006-01-13—Подача