Изобретение относится к медицине, а именно к патофизиологии и трансплантологии, и может быть использовано для восстановления жизнеспособности донорских сердец, перенесших тепловую ишемию в эксперименте.
Ключевой проблемой, сдерживающей развитие клинической трансплантологии, остается глобальный дефицит донорских органов оптимального качества, что критически ограничивает доступность трансплантационной помощи [Резник О.Н., Скворцов А.Е., Мойсюк Я.Г. Сохранение и перфузионная реабилитация донорских органов: достижения последнего десятилетия. Альманах клинической медицины. 2020;48(3):193-206.]. В качестве одного из способов увеличения числа донорских органов предлагается использовать донорские сердца с так называемыми расширенными критериями, ранее считавшимися неприемлемыми для трансплантации, и, в частности, от доноров с необратимой остановкой кровообращения. Этот подход может увеличить пул донорских органов на 15-20% [Noterdaeme T, Detry O, Hans M-F, et al. What is the potential increase in the heart graft pool by cardiac donation after circulatory death? Transpl Int. 2013; 26(1):61-66.]. Существенным недостатком трансплантации органов от доноров после остановки кровообращения является снижение функциональных резервов и последующее повреждение внутренних органов вследствие тотальной тепловой ишемии, развивающейся в организме донора по мере угнетения системной гемодинамики, что ассоциировано с риском первичной дисфункции трансплантатов и высокой летальностью реципиентов таких органов [Stevenson R., Shapter O, Aitken E, Stevenson K, Shiels P., Kingsmore D. Has the Expansion in Extended Criteria Deceased Donors Led to a Different Type of Delayed Graft Function and Poorer Outcomes? Transplant Proc. 2018;50(10):3160-4.]. В современной литературе достаточно активно обсуждаются возможности восстановления и поддержания жизнеспособности исходно компрометированных и первоначально неприемлемых для трансплантации донорских органов; данные методики, разработанные в эксперименте, получили общее название “рекондиционирование органов” (“organ reconditioning”) [Ciubotaru A., Haverich A. Ex vivo Approach to Treat Failing Organs: Expanding the Limits. Eur Surg Res 2015; 54:64-74; Abdalla LG, Oliveira-Braga KA, Fernandes LM, Samano MN, Camerini PR, Pêgo-Fernandes PM. Evaluation and reconditioning of donor organs for transplantation through ex vivo lung perfusion. Einstein (São Paulo). 2019;17(4): eAO4288. http://dx.doi.org/ 10.31744/ einstein_journal/ 2019-AO4288].
Из существующего уровня техники известны следующие способы рекондиционирования донорских органов.
Способ восстановления жизнеспособности ишемически поврежденных донорских органов [Патент РФ 2423 931 МПК A61B 17/00; A61K 31/02; A61K 31/727; A61K 31/573; A61K 33/14; A61K 38/49; A61P 41/00 “Способ восстановления жизнеспособности ишемически поврежденных донорских органов” / Багненко С.Ф., Резник О. Н., Скворцов А.Е.; патентообладатель Государственное учреждение “Санкт-Петербургский научно-исследовательский институт скорой помощи им. И.И. Джанелидзе”. Заявка: 2009136319/14; заявл. 30.09.2009; опубл. 20.07.2011, Бюл. №20], отличающийся тем, что после изъятия органа проводят его экстракорпоральную перфузию раствором, в состав которого входит консервирующий раствор «Кустодиол», перфторан, стрептокиназа, гепарин, преднизолон в течение не менее 2-х часов, при этом из контура экстракорпоральной аппаратной перфузии с помощью лейкоцитарного фильтра удаляют активированные лейкоциты, а температуру перфузата снижают до 5-12°С.
Описан способ восстановления и поддержания жизнеспособности ишемически поврежденного донорского органа [Патент РФ 2 441608 МПК A61B 17/00; A61M 1/10; A61M 1/38; “Способ восстановления и поддержания жизнеспособности ишемически поврежденного донорского органа” / Готье С.В., Багненко С.Ф., Мойсюк Я.Г., Резник О. Н., Скворцов А.Е., Москвин А.Л.; патентообладатель Государственное учреждение “Санкт-Петербургский научно-исследовательский институт скорой помощи им. И.И. Джанелидзе”. Заявка: 2010126694/14; заявл. 29.06.2010; опубл. 10.02.2012, Бюл. №4], основанный на проведении нормотермической перфузии абдоминального региона кровоснабжения пульсирующим потоком, обогащенного кислородом перфузата на основе крови, из которого дополнительно удаляют активированные лейкоциты и недоокисленные продукты биохимического распада.
Общими недостатками указанных способов являются техническая сложность и дороговизна проведения нормотермической аппаратной перфузии органов, связанные с необходимостью использования мехатронного перфузионного модуля на основе роликового насоса со встроенным блоком управления (например, как указано в описании изобретения, модуля «Марс», разработки ЦНИИ робототехники и технической кибернетики, Санкт-Петербург), мембранного оксигенатора (например, производства фирмы Gish Vision Biomedical, Inc, США), лейкоцитарного фильтра (например, производства корпорации «Палл ГМБХ), экстракорпорального перфузионного аппарата (LifePort® Organ Recovery Systems), а также абсорбционного фильтра на основе композитного материала с наноуглеродом. Кроме того, из описания изобретений специалисту неочевидна возможность применения известных способов для рекондиционирования донорского сердца, поскольку указано выполнение окклюзии брюшного отдела аорты выше отхождения почечных артерий с последующей перфузией и эксплантацией только органов брюшной полости. К тому же, проведение первоначальной перфузии внутренних органов в нормотермических условиях может выступать дополнительным фактором реперфузионного повреждения для исходно ишемизированного донорского сердца за счет его высоких метаболических потребностей.
Известен способ и устройство для рекондиционирования органов [Pub. No. WO 2020/209788 2 441608 Int. Cl. A01N 1/02 “METHOD AND APPARATUS FOR RECONDITIONING ORGANS”/ Applicant: UGLX RESEARCH AB; Bjdrnstorp Gods, 247 98 Genarp; Priority Data: 12.04.2019], включающие изъятие органов не менее чем через 2 часа после остановки кровообращения у донора с последующей перфузией органов гиперонкотическим растворами, содержащими лиз-плазминоген, тканевой активатор плазминогена, альбумин, электролиты и эритроциты. С учетом сроков эксплантации донорских органов данное изобретение, как указано в описании, может быть использовано при трансплантации печени, почек, поджелудочной железы, матки, тонкой кишки и неприменимо при трансплантации сердца в связи с развитием необратимого повреждения миокарда при нормотермической ишемии продолжительностью более 30 минут.
Устройство и способ для поддержания и/или восстановления жизнеспособности органов [Pub. No.: US 2006/0063142 Int. Cl. A01N 1/02 “APPARATUS AND METHOD FOR MAINTAINING AND/OR RESTORING VIABILITY OF ORGANS”/ Donald R. Owen, David C. Kravitz; Assignee: ORGAN RECOVERY SYSTEMS, INC., Charleston, SC (US); Appl. No.: 11/257,066 Filed: Oct. 25, 2005] обеспечивают перфузию органа в гипотермических и/или нормотермических условиях предпочтительно после гипотермической промывки органа для транспортировки органа и/или консервации. Недостатком данного способа является то, что раствор для гипотермической перфузии органа не содержит кислород и является простым кристаллоидным раствором с добавлением антиоксидантов, что может приводить к дополнительному аноксическому повреждению и отеку кардиомиоцитов донорского сердца, перенесшего тепловую ишемию.
Известен способ, устройство и система для рекондиционирования внутренних органов [Pub. No.: US 2003/010985 Int. Cl. A61M 1/00 “METHOD, A DEVICE, AND A SYSTEM FOR ORGAN RECONDITIONING AND A DEVICE FOR PRESERVING AN INTERNAL BODY ORGAN”/ J. O. Solem, R. Gustafsson, R. Ingemansson; Appl. No.: 10/259,822 Filed: Sep. 30, 2002], основанные на удалении избытка интерстициальной жидкости из органа путем использования устройства в виде трубки, имеющей проксимальный конец, адаптированный для соединения с источником вакуума, и окруженную камерой дистальную часть со множеством отверстий. Рекондиционирование органа, проводимое по данному способу, является недостаточным, поскольку подразумевает лишь коррекцию вне- и внутриклеточного отека и не оказывает воздействия на метаболические пути и значимые звенья каскада патологических реакций при ишемическом и реперфузионном повреждении миокарда.
Известен раствор и способ для оживления и восстановления ишемически поврежденной ткани [Патент РФ 2199 310 МПК A61K 9/08; A61K 33/14, А61Р 41/00. “ Раствор и способ для оживления и восстановления ишемически поврежденной ткани” / БРЭСАЙЛ Лорен; патентный поверенный Егорова Г.Б. Заявка: № 99102851/14; заявл. 16.05.97; опубл. 27.02.03, Бюл. №6], недостатками которого являются применение буфера физиологического раствора для промывания органа, лишенного кровотока, что может вызвать внутриклеточный отек кардиомиоцитов в условиях ишемического повреждения мембран клеток, а также технически сложный в реализации данного способа многокомпонентный состав восстановительного раствора, который включает вазодилататоры (ацетилхолин и аргинин, простациклин и Мg+, аденозин и верапамил), химические энергетические субстраты (пируват, глюкозу, АТФ, АМФ, кофермент А, β-никотинамидадениндинуклеотид (НАД+), флавинадениндинуклеотид (ФАД), тиаминпирофосфат хлорида (кокарбоксилазу), УТФ, хлорид магния и их комбинацию), трофические факторы (аминокислоты, магний, производные нуклеиновых кислот, рибонуклеозиды, кислый фактор роста фибробластов (ФРФ), основной ФРФ, гепарин и хондроитинсульфата и их комбинацию), а также антиоксиданта, переносящего кислород агента и их комбинаций.
В связи с изложенным, поиск воспроизводимых способов эффективного рекондиционирования ишемически компрометированного донорского сердца для повышения потенциала его жизнеспособности и расширения пула донорских органов представляется актуальным. Известные способы рекондиционирования донорских органов не рассматривались нами в качестве прототипа.
Технической задачей, на решение которой направлено заявляемое изобретение, является разработка в эксперименте способа рекондиционирования донорского сердца, лишенного перечисленных недостатков.
Данная задача решается тем, что производят газовую перфузию донорского сердца, перенесшего тепловую ишемию, помещая орган в охлажденный консервирующий раствор.
Способ осуществляется следующим образом. После изъятия сердца, перенесшего тепловую ишемию и промывания его охлажденным до +12°С консервирующим раствором, канюлируют аорту, канюлю при помощи магистрали соединяют с увлажнителем и через редуктор с газовым баллоном. Далее сердце помещают в контейнер-термостат, заполненный охлажденным до +12°С консервирующим раствором. Осуществляют перфузию коронарного русла донорского сердца увлажненным кислородом под постоянным давлением 35 мм рт. ст. с объемной скоростью 5 мл/мин в течение 1 часа.
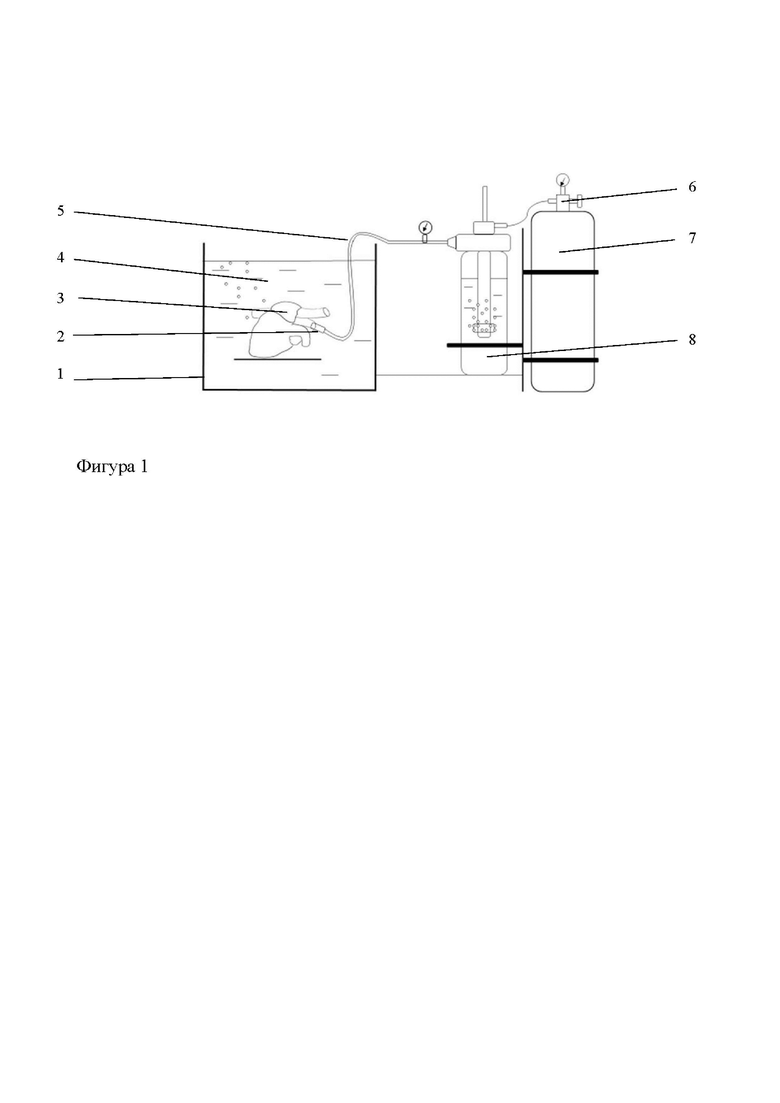
Общий вид рекондиционирования донорского сердца предлагаемым способом представлен на Фигуре 1 - “Схема проведения рекондиционирования донорского сердца”, где: 1 - контейнер-термостат, 2 - аортальная канюля, 3 - донорское сердце, 4 - консервирующий раствор, 5 - соединительные магистрали, 6 - редуктор, 7 - газовый баллон, 8 - увлажнитель.
Технический результат, обеспечиваемый приведенной совокупностью признаков, заключается в обеспечении достаточного уровня аэробного метаболизма изолированного донорского сердца в условиях умеренного снижения его метаболических потребностей и отсутствия дополнительного повреждения, возникающего при более глубокой гипотермии, обычно используемой в трансплантологии, что способствует восстановлению обратимых функционально-метаболических нарушений, развившихся в миокарде на донекротической стадии перенесенной тотальной тепловой ишемии. Оценка жизнеспособности донорского сердца при рекондиционировании предлагаемым способом может быть проведена после его трансплантации или при экстракорпоральной аппаратной реперфузии.
Экспериментальные примеры конкретного выполнения
Эксперименты были проведены на 24 половозрелых беспородных крысах-самцах. Под эфирным наркозом проводили билатеральную торакотомию, пересекали магистральные сосуды, извлекали сердце, помещали его в установку для экстракорпоральной перфузии. Перфузию сердца проводили через аорту раствором Кребса-Хензелайта, насыщенным карбогеном (95% О2 + 5% СО2), в режиме постоянного давления 70 мм рт. ст. при температуре 37°С, поддерживаемой ультратермостатом VT-8 (ООО “Термекс-2”, Россия), и рН=7,33-7,36. Через ушко левого предсердия в полость левого желудочка помещали латексный баллончик постоянного объема, соединенный с портативным монитором РМ-8000 (Mindray, Китай) и фиксировали его лигатурой. После стабилизации работы изолированного сердца, записывали кривую давления в левом желудочке. На основании анализа кривой давления рассчитывали систолическое, диастолическое и развиваемое давление.
Сердца экспериментальных животных были разделены на следующие группы: контроль - интактные сердца (n=8); группа сердец, перенесших тепловую ишемию и последующую реперфузию (n=8); группа сердец, перенесших тепловую ишемию, рекондиционирование предлагаемым способом и последующую реперфузию (n=8).
Тепловую ишемию донорского сердца моделировали путем остановки перфузии раствором Кребса-Хензелайта в течение 10 мин в условиях нормотермии. Для рекондиционирования донорские сердца, перенесшие тепловую ишемию, промывали охлажденным до +12°С консервирующим раствором, канюлировали аорту, канюлю при помощи магистрали соединяли с увлажнителем и через редуктор с газовым баллоном, сердца помещали в контейнер-термостат, заполненный охлажденным до +12°С консервирующим раствором. Коронарное русло донорского сердца перфузировали увлажненным кислородом под постоянным давлением 35 мм рт. ст. с объемной скоростью 5 мл/мин в течение 1 часа. По окончании эксперимента все донорские сердца были реперфузированы в установке для экстракорпоральной перфузии при первоначальных условиях.
Исходные показатели, характеризующие сократительную функцию изолированного сердца, в группах не отличались. Сердца, перенесшие тепловую ишемию, демонстрировали развитие ишемической контрактуры миокарда без восстановления сократительной функции в период реперфузии по сравнению с контролем и группой рекондиционирования. Показатели постишемической сократительной дисфункции сердец этой группы не позволяли рассматривать их в качестве жизнеспособных органов, пригодных к трансплантации. В группе сердец, подвергнутых рекондиционированию предлагаемым способом, отмечался постепенный регресс явлений постишемической сократительной дисфункции в ходе реперфузии до уровня приемлемого к трансплантации, что свидетельствует об эффективности предлагаемого способа и возможности восстановления функционально-метаболических нарушений, развившихся в изолированном сердце после 10-минутной тепловой ишемии в эксперименте.
Таким образом, полученные данные свидетельствуют, что предлагаемый в качестве изобретения способ рекондиционирования донорского сердца может быть использован в экспериментальной медицине для восстановления и поддержания жизнеспособности сердечного трансплантата, перенесшего тотальную тепловую ишемию.
| название | год | авторы | номер документа |
|---|---|---|---|
| Устройство для перфузионной консервации и рекондиционирования донорского сердца | 2020 |
|
RU2754592C1 |
| СПОСОБ КОНСЕРВАЦИИ ДОНОРСКОГО СЕРДЦА | 2020 |
|
RU2743235C1 |
| УСТРОЙСТВО ДЛЯ КОНСЕРВАЦИИ ДОНОРСКИХ ОРГАНОВ | 2020 |
|
RU2741219C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ И ПОДДЕРЖАНИЯ ЖИЗНЕСПОСОБНОСТИ ИШЕМИЧЕСКИ ПОВРЕЖДЕННОГО ДОНОРСКОГО ОРГАНА | 2010 |
|
RU2441608C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЧЕЧНЫХ ТРАНСПЛАНТАТОВ ОТ ДОНОРОВ С ВНЕГОСПИТАЛЬНОЙ ОСТАНОВКОЙ КРОВООБРАЩЕНИЯ | 2023 |
|
RU2821024C1 |
| СПОСОБ ПРЕЗЕРВИРОВАНИЯ МИОКАРДА ПРИ ТРАНСПЛАНТАЦИИ | 2013 |
|
RU2535036C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ ЖИЗНЕСПОСОБНОСТИ ИШЕМИЧЕСКИ ПОВРЕЖДЕННЫХ ДОНОРСКИХ ОРГАНОВ | 2009 |
|
RU2423931C2 |
| СПОСОБ ЭКСТРАКОРПОРАЛЬНОГО ВОССТАНОВЛЕНИЯ ПЕРФУЗИИ И ОКСИГЕНАЦИИ ВНУТРИ ТЕЛА ДОНОРА | 2017 |
|
RU2666515C2 |
| УСТРОЙСТВО ЭКСТРАКОРПОРАЛЬНОЙ АППАРАТНОЙ ПЕРФУЗИИ ДОНОРСКИХ ОРГАНОВ ВНУТРИ ТЕЛА ДОНОРА | 2014 |
|
RU2570391C1 |
| Раствор для предтрансплантационной подготовки донорских легких | 2023 |
|
RU2815501C1 |
Изобретение относится к биотехнологии и медицине, в частности к способу рекондиционирования донорского сердца, перенёсшего тепловую ишемию. Для осуществления способа изолированное сердце промывают охлажденным до +12°С консервирующим раствором, далее канюлируют аорту, канюлю соединяют с увлажнителем и через редуктор с газовым баллоном. После чего сердце помещают в контейнер-термостат и проводят его газовую перфузию увлажненным кислородом под постоянным давлением 35 мм рт.ст. в течение 1 часа. Настоящее изобретение позволяет повысить эффективность рекондиционирования ишемически компрометированного донорского сердца для повышения потенциала его жизнеспособности, что способствует расширению пула донорских органов. 1 ил., 1 пр.
Способ рекондиционирования донорского сердца, включающий изъятие и промывание сердца, перенесшего тепловую ишемию, охлажденным до +12°С консервирующим раствором с последующей канюляцией аорты и перфузией коронарного русла увлажненным кислородом под постоянным давлением 35 мм рт. ст. с объемной скоростью 5 мл/мин в течение 1 часа в контейнере-термостате, заполненном охлажденным до +12°С консервирующим раствором.
| US 2006063142 A1, 23.03.2006 | |||
| СПОСОБ ВОССТАНОВЛЕНИЯ И ПОДДЕРЖАНИЯ ЖИЗНЕСПОСОБНОСТИ ИШЕМИЧЕСКИ ПОВРЕЖДЕННОГО ДОНОРСКОГО ОРГАНА | 2010 |
|
RU2441608C1 |
| CHEW H.C | |||
| et al., The donor heart and organ perfusion technology, Journal of Thoracic Disease, 2019, 11(Suppl 6), S938-S945, doi: 10.21037/jtd.2019.02.59 | |||
| NIEDERBERGER P | |||
| et al., Heart transplantation with donation after circulatory death, Circulation: Heart Failure, Vol | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
2022-08-01—Публикация
2021-11-30—Подача