Изобретение относится к области медицины и может быть использовано для лечения и/или профилактики избыточной массы тела и/или ожирения и/или метаболических нарушений по генетическим полиморфизмам, ассоциированным с нарушениями углеводного, липидного, гормонального и энергетического обменов генов.
На сегодняшний день общепризнанным является мнение, что ожирение - это болезнь, причем самая распространенная в мире.
Ожирение (obesity) - хроническое рецидивирующее заболевание, проявляющееся избыточным развитием жировой ткани, прогрессирующее при естественном течении, имеющее определенный круг осложнений.
В последнее время во всем мире четко наметилась тенденция к росту заболеваемости ожирением и метаболическими нарушениями, даже в тех странах и популяциях, в которых ожирение было редким недугом, например в Китае, Японии. Так сегодня в мире 1,7 млрд. человек имеют лишний вес, из них 300 миллионов имеют ожирение. Известно, что среди взрослого населения планеты лишний вес имеют до 75% населения Самоа, 61% населения США (34% имеют избыточную массу тела, 27% - ожирение), 27,5% населения Китая. В России 30% населения имеет лишний вес.
Ожирение детства переходит в ожирение зрелого возраста, являясь мощным предиктором ожирения зрелого возраста, особенно когда им страдает один или оба родителя.
Актуальность и значимость проблемы обусловлены последствиями, к которым приводит ожирение.
Существующие способы лечения ожирения и метаболических нарушений включают стандартные диеты и физические упражнения, очень низкокалорийные диеты, поведенческую терапию, фармакотерапию, включающую средства, подавляющие аппетит, термогенные средства, ингибиторы всасывания пищи, механические устройства, такие как фиксация челюсти, стягивание талии и хирургическое вмешательство.
Из уровня техники известен способ лечения ожирения у человека, включающий введение указанному субъекту количества композиции, включающей агонист амилина, эффективного для лечения ожирения при условии, что композиция не включает холецистокинин или агонист холецистокинина, при этом агонист амилина представляет собой 25,28,29Pro-h-амилин (RU 2314121, 20.05.2004).
Известен способ профилактики и лечения заболеваний, связанных с нарушением липидного обмена путем диетотерапии на основе лакто-ово-вегетарианского рациона. С продуктами питания обеспечивают введение белков 65-76 г в сутки, из них животных - 40-49%, жиров 28-50 г в сутки, из них животных - 17-55%, углеводов
233-300 г в сутки, холестерина 40-311 мг в сутки, клетчатки 18-20 г в сутки, аргинина 3,5-4,3 г в сутки, калия (К) 4235-5461 мг в сутки, магния (Mg) 496-655 мг в сутки, витамина С 294-528 мг в сутки, витамина Е 16-30 мг в сутки (RU 2060012, 20.05.1996).
Известен способ лечения ожирения, заключающийся в регулировании аппетита и веса тела, а также липидного обмена при помощи ионов хрома, отличающийся тем, что применяют раствор в каплях оксида хрома (VI) в дозировке 0,35 мг/кг/сутки, соответствующей максимальному лечебному действию данного микроэлемента (RU 2277918, 20.06.2006).
При данных способах лечения ожирения не учитываются индивидуальные причины развития этого заболевания, и лечение направлено на коррекцию одного фактора.
Задача, на решение которой направлено предложенное изобретение, заключается в создании такого способа лечения и/или профилактики ожирения и метаболических нарушений, который исключал бы указанные выше недостатки.
Технический результат, достигаемый при реализации данного изобретения, заключается в повышении эффективности лечения избыточной массы тела или ожирения и метаболических нарушений по генетическим полиморфизмам за счет детального выяснения причин набора веса и метаболических нарушений.
Указанный технический результат достигается в способе лечения и/или профилактики ожирения и метаболических нарушений, включающем дифференциальную диагностику причин избыточной массы тела и/или ожирения по генетическим полиморфизмам и, в зависимости от полиморфных вариантов генов, назначение диеты, состоящей из продуктов, которым присвоен 2-цветный код по гликемическому индексу и жирности.
Если причина избыточной массы тела или ожирения связана с полиморфизмом в гене LPL, то для лечения ожирения назначают низкожировую диету.
Дополнительно к низкожировой диете назначают препарат Орлистат, блокирующий фермент LPL (липопротеинлипазы).
Если причина избыточной массы тела или ожирения связана с полиморфизмом в гене GREL (грелина), то для коррекции и профилактики нарушения пищевого поведения назначают диету из продуктов, богатых клетчаткой.
Дополнительно к диете из продуктов, богатых клетчаткой, назначают биологически активные добавки, богатые клетчаткой.
Если причина ожирения связана с полиморфизмом в гене INS (инсулина), то для коррекции нарушений углеводного обмена и снижения веса назначают низкогликемичную диету.
Дополнительно к низкогликемичной диете назначают препарат Акарбоза, снижающий всасывание углеводов в кишечнике.
Если причина ожирения и ассоциированной с ним дислипидемии связана с полиморфизмом в гене FABP2 (белка, способствующего всасыванию жирных кислоты в тонком кишечнике), то для коррекции нарушений липидного обмена назначают дополнительно препарат Эзетимиб, блокирующий всасывание жирных кислот в тонком кишечнике.
Если причина ожирения связана с полиморфизмом в гене ADRβ3 (адренорецептора типа β3), то для коррекции нарушения функции симпатической нервной системы на уровне регуляции энергетического обмена в жировой ткани, приводящего к абдоминальному ожирению, назначают препарат Сибутрамин, активирующий функцию адренорецептора типа β3.
Изобретение поясняется чертежами, где на фиг.1-23 изображена классификация продуктов по двухцветным кодам и категориям; на фиг.24 - карточка-ключ.
К заболеваниям, сопровождающим лишний вес (ожирение и метаболические нарушения), относятся СД 2 типа, артериальная гипертония (каждые 4,5 кг лишнего веса добавляют 4,5 мм рт.ст. артериального давления), дислипидемия, атеросклероз (на 1 килограмм лишнего веса общий холестерин возрастает на 20 мг), синдром ночного апноэ, нарушения дыхания, гиперурикемия, подагра, репродуктивная дисфункция, жировой гепатоз (стеатогепатоз или стеатогепатит), желчно-каменная болезнь, жировая инфильтрация поджелудочной железы, заболевания опорно-двигательной системы, онкологические заболевания (в целом на 33%), варикозная болезнь, геморрой, тромбофилии и т.д. Сочетание инсулинорезистентности с избыточной массой тела или ожирением, артериальной гипертонией, дислипидемией, нарушениями углеводного обмена - это основные проявления метаболического синдрома или «смертельного квартета».
Следует отметить, что артериальная гипертония при ожирении встречается в 3-6 раз чаще, чем при нормальной массе; атеросклероз при повышении веса у молодых людей встречается в 2 раза чаще, чем при нормальной массе; вероятность СД 2 типа при ожирении 1 степени возрастает в 2 раза, II степени - в 3-5 раз, при морбидном ожирении в 40 и более раз!
Совокупность артериальной гипертонии, дислипидемии, нарушений углеводного обмена на фоне лишнего веса с абдоминальным распределением жировой ткани принято называть метаболическим синдромом, синдромом инсулинорезистентности, «смертельным квартетом».
Существует несколько классификаций ожирения и метаболических нарушений: по этиологическому принципу, по характеру распределения жировой ткани, по индексу массы тела и т.д.
По этиологическому принципу ожирение и метаболические нарушения делят на: алиментарно-конституциональное, гипоталамическое (диэнцефальное), эндокринное (гипотиреоз, гиперкортицизм, инсулинома и др.), при редких генетических синдромах (Прадера-Вилли, Лоуренса-Муна и т.д.), церебральное (поражение ЦНС вследствие травмы, нейроинфекции и т.д.), ятрогенное.
По типу распределения жировой ткани: абдоминальное (андроидное, центральное, «тип яблока»), гиноидное (ягодично-бедренное, «тип груши»), смешанное.
По индексу массы тела (ВОЗ, 1997 г.): 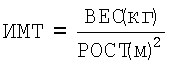 .
.
Кроме того, ожирение делят на первичное - экзогенно-конституциональное (95%) и вторичное - симптоматическое (5%) (по Г.А.Мельниченко).
К симптоматическому или вторичному ожирению чаще всего приводит дисбаланс некоторых гормонов (тиреоидных, гормонов надпочечников, половых гормонов).
За первичным (экзогенно-конституциональным) ожирением стоит наличие генетической предрасположенности к набору веса в сочетании с определенными особенностями образа жизни - внешними факторами развития ожирения.
Таким образом, к факторам, определяющим развитие ожирения и метаболических нарушений относятся: генетические, психологические и поведенческие (питание, физическая активность, алкоголь, курение, стрессы), демографические, социально-экономические. К системам, отвечающим за регуляцию веса, относятся: нейромедиаторная система головного мозга, гипоталамо-гипофизарная система, системы регуляции углеводного, липидного, энергетического обмена, симпато-адреналовая система, система регуляции чувства голода и насыщения. На конституциональном уровне функционирование этих систем регулируется генами.
В связи с полиэтиологичностью заболевания необходима «полидиагностичность» в установлении причин набора веса и метаболических нарушений. Только при таком детальном выяснении причин возможно максимально эффективное лечение и профилактика набора веса.
На наш взгляд целесообразным представляется следующий алгоритм обследования пациента с лишним весом.
- Антропометрия: рост, вес, ИМТ, ОТ, ОБ, ОТ/ОБ.
- Анализ состава тела: биоимпеданс, инфракрасная фотометрия.
- Психологическое тестирование.
- Клинический осмотр врача.
- Генетическое исследование.
- Гормональное исследование крови.
- Биохимическое исследование крови.
- ЭКГ.
- УЗИ щитовидной железы, органов брюшной полости, надпочечников.
- Клинический анализ крови.
- Определение маркеров жировой ткани.
При необходимости назначаются МРТ головного мозга, КТ надпочечников, поджелудочной железы, консультация окулиста, пробы с препаратами и т.д.
После такой тщательной диагностики подбирается индивидуальный алгоритм лечения пациента.
К методам лечения ожирения и метаболических нарушений относятся:
- немедикаментозные (психотерапия для коррекции психологических причин набора веса и изменения пищевого поведения, обучение больных рациональному питанию, повышение физической активности),
- медикаментозные,
- хирургические.
Как уже говорилось, лишний вес и метаболические нарушения - следствие дисбаланса многих систем. Роль многих факторов в формировании ожирения уже достаточно описана. Но изучению генетических причин набора лишнего веса уделялось мало внимания. В литературе периодически появляются работы о вкладе того или иного гена в развитие ожирения (в основном эти работы касались генов, кодирующих работу лептина), но работ, оценивающих ожирение как мультифакториальное заболевание практически нет.
Существующие на сегодняшний день подходы к лечению ожирения и метаболических нарушений не учитывают индивидуальных причин развития этих заболеваний и направлены на коррекцию одного фактора. Возможно поэтому эффективность лечения ожирения и метаболических нарушений традиционными методами не превышает 5-10%.
Лишь комплексный подход к ожирению и метаболическим нарушениям с выяснением всего спектра причин и нарушений, в том числе на молекулярно-генетическом уровне, способен эффективно решать и предупреждать эту проблему.
Коррекция лишнего веса и метаболических нарушений, ассоциированных с ним, невозможны без изменения (коррекции) питания. Огромное множество предлагаемых сегодня диет основаны на каком-либо одном факторе, например ограничении, а то и исключении углеводов или подсчете суточной калорийности. При этом подразумевается, что предлагаемый подход будет одинаково эффективным и безопасным у совершенно разных людей. Не учитываются особенности ферментных систем, участвующих в пищеварении, особенности метаболизма, например, липидов у конкретного человека, а также нередко игнорируются уже имеющиеся нарушения углеводного, липидного, белкового обменов.
В лучшем случае критерием индивидуального подбора продуктов, «нормализующих обмен веществ», являются аллергические реакции на продукты или группа крови. Такой подход, возможно, позволит избежать пищевой непереносимости (аллергии), но не улучшит параметров углеводного, липидного или белкового обменов.
Применяемая чаще всего система подсчета суточной калорийности безусловно важна, но она также не учитывает индивидуальных особенностей, связанных с пищеварением и метаболическими нарушениями (дислипидемией, гиперурикемией, нарушениями углеводного обмена).
Предлагаемая система питания учитывает те свойства продуктов, которые имеют значение для набора веса и нарушений липидного, углеводного обменов. При этом данная система питания удобна для применения пациентами, не требует сложных подсчетов и, самое главное, учитывает индивидуальные особенности пациентов.
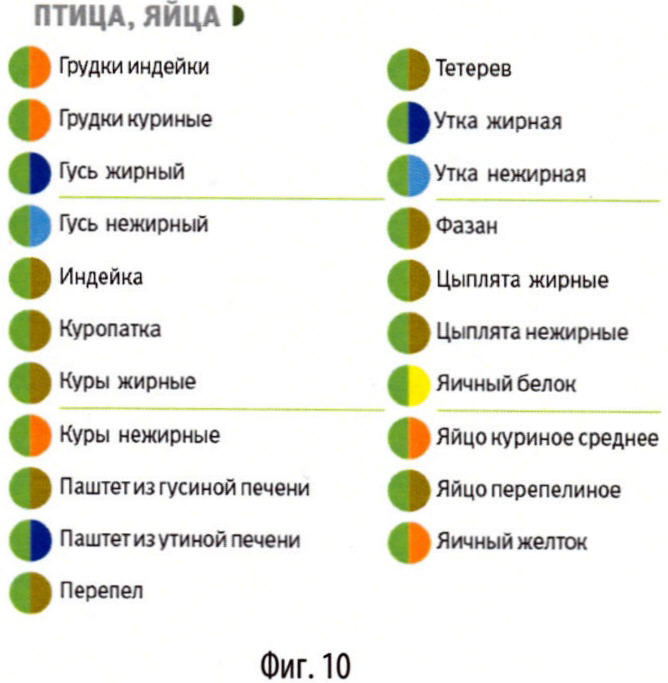
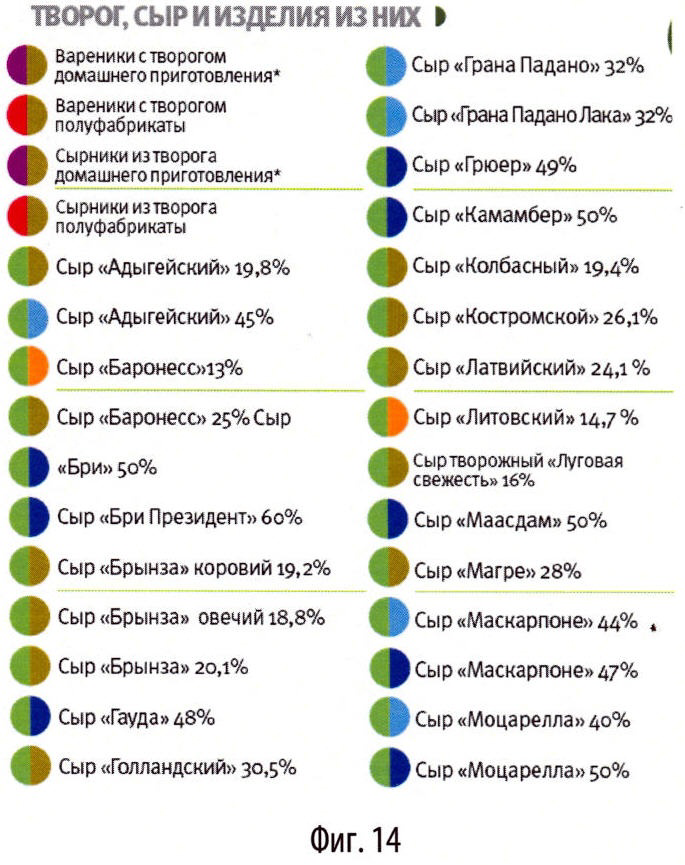
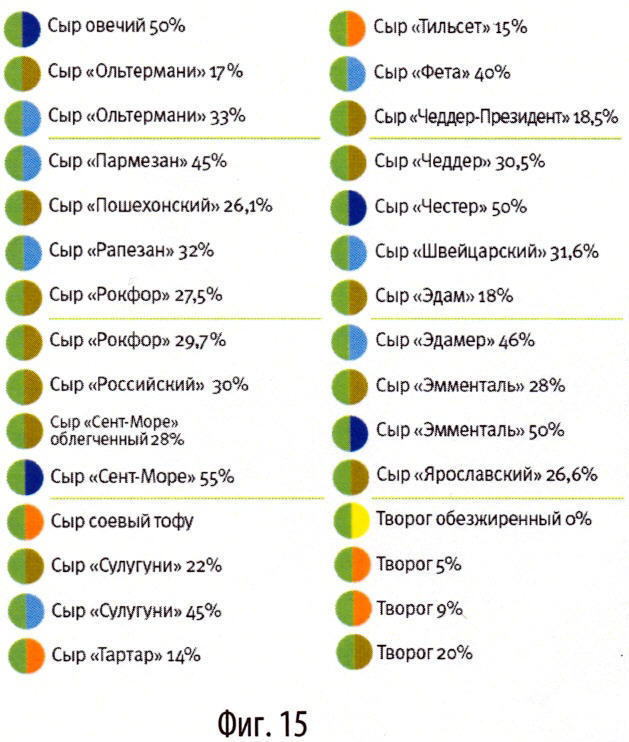
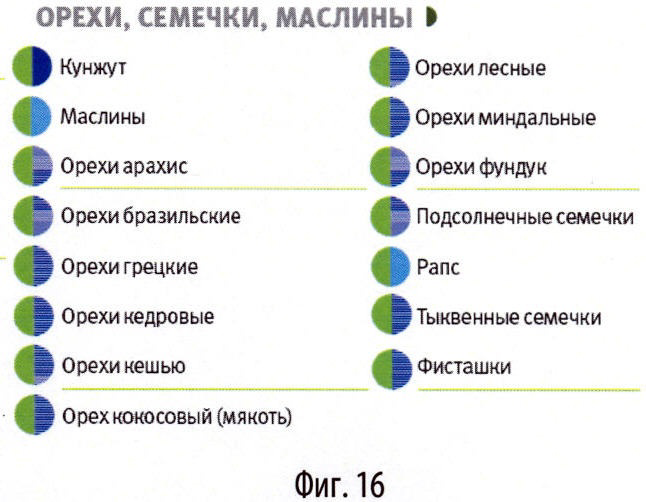
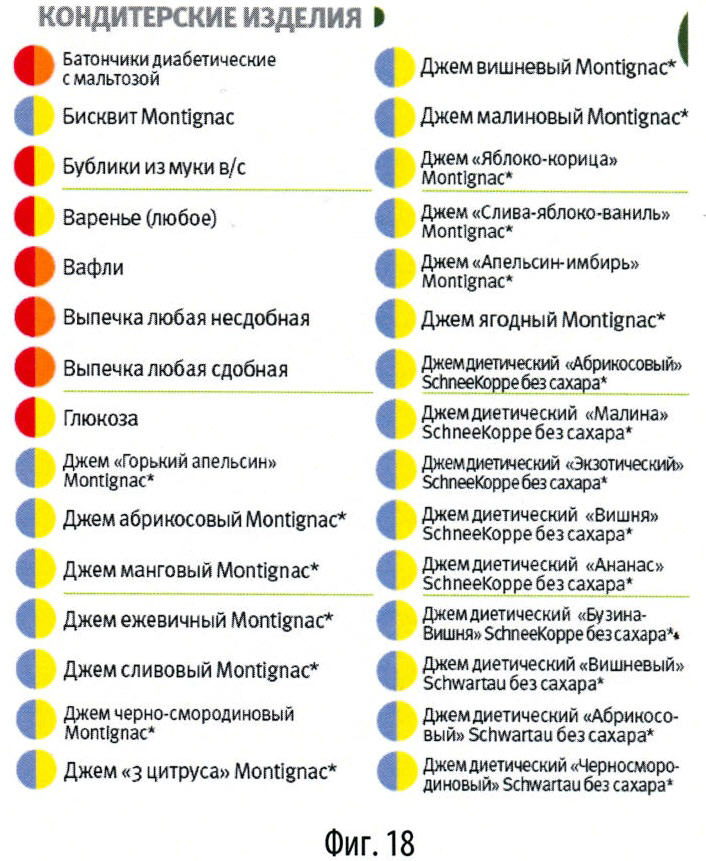
В данной системе в основу классификации продуктов положены такие параметры, как процентное содержание жира и гликемический индекс (или гликемичность) - это основные параметры продуктов, которые влияют на набор веса (суточная калорийность учитывается после составления рациона). Для простоты пользования данные параметры обозначены не цифрами, а цветами, соответствующими определенным значениям жирности и гликемичности. Таким образом, каждый продукт имеет 2 цвета: цвет слева обозначает определенный уровень гликемического индекса, цвет справа - процент жирности. Т.е. каждому продукту присвоен двухцветный код. В зависимо от выраженности признака (гликемического индекса или жирности) продукты разделены на несколько групп. По гликемическому индексу на 5 групп, соответственно на 5 цветов (цвета №1-5): №1 - гликемический индекс до 20, №2 - гликемический индекс от 20 до 35, №3 - гликемический индекс от 35 до 50, №4 - гликемический индекс от 50 до 65, №5 - гликемичекий индекс более 65.
По жирности продукты также разделены на 5 групп, 5 цветов (цвета №6-10): №6 - жирность до 2%, №7 - жирность от 2 до 10%, №8 - жирность от 10 до 20%, №9 - жирность от 20 до 30%, №10 - жирность более 30%.
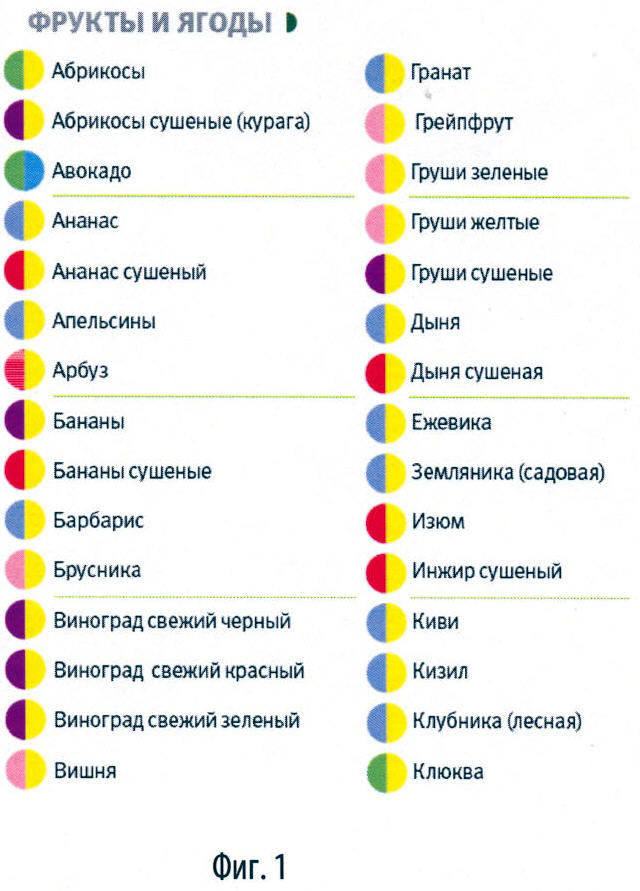
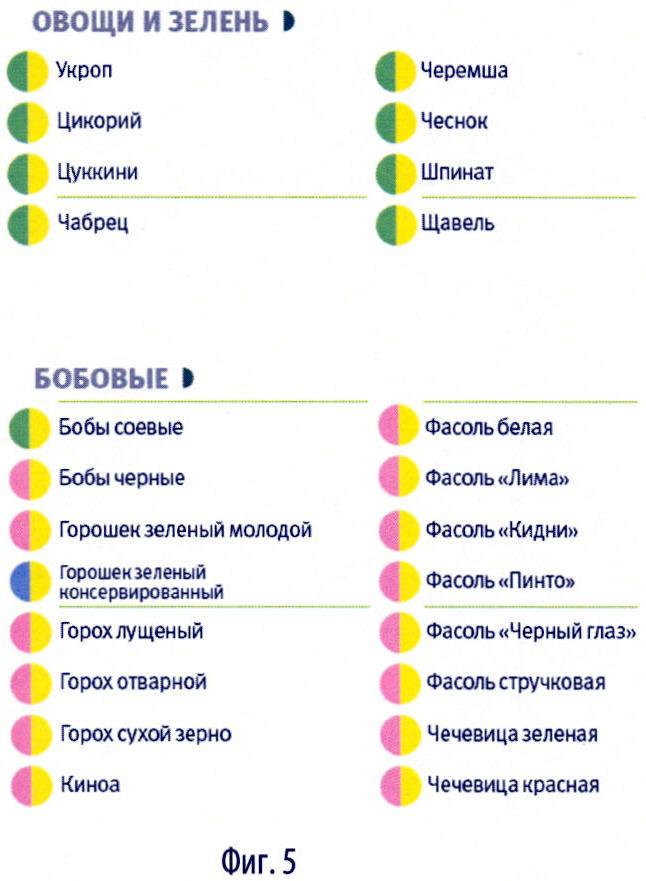
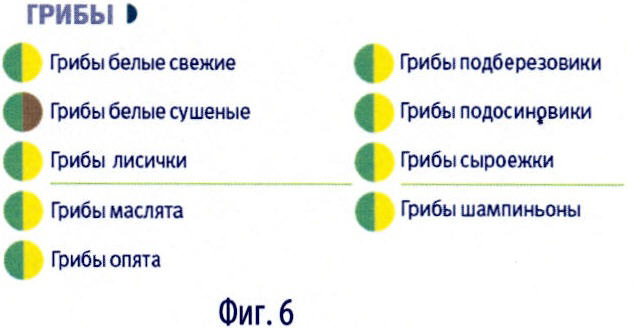
В итоге по сочетаниям параметров и соответственно по цветовым кодам около 700 продуктов, представленных на нашем рынке, распределились в 20 групп. Все проклассифицированные продукты с соответствующими их параметрам двухцветными кодами собраны в книге продуктов - классификаторе продуктов. Для удобства поиска все продукты разделены не только по цветовым кодам в группы, но и по категориям:
- фрукты и ягоды (фиг.1, 2),
- овощи и зелень (фиг.3-5),
- бобовые (фиг.5),
- грибы (фиг.6),
- рыба и морепродукты (фиг.7-9),
- птица и яйца (фиг.10),
- мясо и мясопродукты (фиг.11-13),
- творог, сыр и изделия из них (фиг.14, 15),
- орехи и семечки (фиг.16),
- крупы, каши (фиг.17),
- кондитерские изделия (фиг.18, 19),
- макаронные изделия (фиг.20),
- хлеб и хлебопродукты (фиг.21),
- суши и роллы (фиг.22),
- продукты Fast food (фиг.23).
Набор двухцветных кодов и их распределение по колонкам индивидуальны в зависимости от выявленных особенностей пациента.
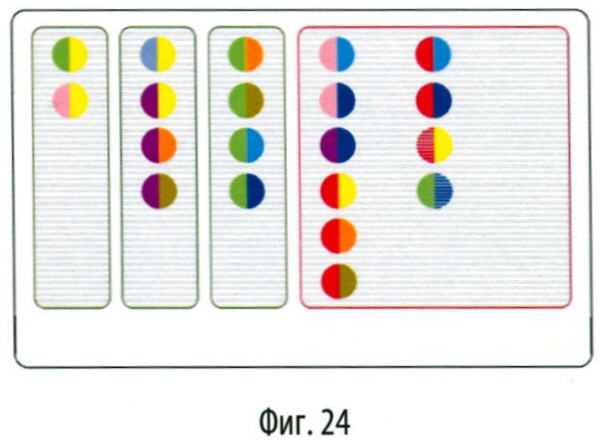
Выбор продуктов по карточке-ключу (фиг.24) и классификатору продуктов (фиг.1-23) осуществляется следующим образом:
1. по карточке-ключу пациент смотрит, какие двухцветные коды расположены в разрешенной зоне,
2. находит по классификатору продукты, относящиеся к этим кодам,
3. в зависимости от того, к какой колонке относится выбранный продукт, пациент определяет, с чем его можно сочетать.
Другой способ. Если пациент хочет узнать, можно ли ему есть какой-либо продукт, то он находит его по классификатору, например рыба дорадо:
1. он находит по классификатору раздел «рыба и морепродукты»,
2. находит в этом разделе рыбу дорадо и ее двухцветный код,
3. по своей карточке-ключу выясняет, к какой колонке относится двухцветный код, соответствующий рыбе дорадо, разрешен ли ему этот продукт и в каком сочетании.
Используя данную систему выбора продуктов, пациент постепенно учится формировать правильный пищевой рацион и изменяет пищевое поведение. При этом он ведет пищевой дневник, куда записывает все приемы пищи (что съел, сколько, в какое время и почему). В конце дня оценивается суточный калораж и сбалансированность по содержанию белков, жиров и углеводов, правильность распределения рациона в течение суток. После этого при необходимости вносятся коррективы. (В этот дневник также вносятся принимаемые препараты, если они назначены, самочувствие, уровень АД, гликемия, если есть нарушения углеводного обмена.) На основании записей в дневнике лечащий врач оценивает правильность соблюдения рекомендаций, вносит коррективы в лечение.
Принцип подбора продуктов по результатам комплексного обследования.
1. При выявлении по данным генетического анализа варианта гена LPL, предрасполагающего к усиленному всасыванию жиров, пациенту назначают продукты с низкой жирностью - цветовые коды №6, №7.
При отсутствии генетической предрасположенности к усиленному всасыванию жиров по гену LPL возможно назначение продуктов с цветовым кодом №8.
I.I. Липопротеинлипаза (ЛПЛ) - ключевой фермент метаболизма липидов. Липопротеинлипаза высвобождает жирные кислоты из состава липопротеинов очень низкой плотности (ЛПОНП) и хиломикронов. Жирные кислоты поступают в адипоциты и откладываются в жировой ткани.
Повышенная липолитическая активность приводит к увеличению количества свободных жирных кислот (ОКК) в системе воротной вены. Увеличивающееся количество жирных кислот в кровообращении, в свою очередь, способствует резистентности к инсулину скелетной мускулатуры из-за конкуренции между глюкозой и СЖК в цикле глюкоза - жирные кислоты. Повышенное содержание СЖК симулирует глюконеогенез в печени. Кроме того, повышенное воздействие СЖК на печень стимулирует синтез и высвобождение богатых триглициридами липопротеидов очень низкой плотности (ЛОНП). Из-за периферической резистентности к инсулину понижается активность связанной с эндотелием липопротеинлипазы скелетных мышц и клеток жировой ткани. Таким образом, уровни триглицеридов повышаются в результате усиленного образования их в печени в сочетании с уменьшенным периферическим метаболизмом, при этом уровни липопротеидов высокой плотности уменьшаются вследствие понижения активности периферического метаболизма ЛОНП.
I.II. Мутации в гене липопротеинлипазы (LPL), обуславливающие изменения в структуре ЛПЛ, приводят к увеличению концентрации триглицеридов и холестерина, гипертриглицеридемии и гиперхолестеронемии, что, в свою очередь, определяет развитие атеросклеротических изменений в сосудах.
Впервые в работе Jemaa R. и соавт. (1995) была показана связь полиморфизма HindIII с показателями уровня липидов и аполипопротеинов у лиц с абдоминальным ожирением (162 женщины и 74 мужчины). Генотип (+/+) LPL оказался ассоциированным при высоком уровне значимости с высоким уровнем триглицеридов и липопротеинов очень низкой плотности (ЛПОНП). Наиболее выраженной эта связь была у женщин при отсутствии корреляции с возрастом и индексом массы тела.
В исследовании Nicklas и соавт. (2000), проведенном в группе 75 американок в возрасте 51-69 лет с индексом массы тела более 25 кг/м2, была показана связь высокого уровня как общего холестерина, так и холестерина в составе липопротеинов низкой плотности с генотипом LPL H+/H+.
В Испании Senti и соавт. (2000) генотипирование мутации HindIII проводилось у женщин с абдоминальным типом ожирения в возрасте до 50 лет. Так же, как в предыдущих и последующих работах по изучению этой мутации у лиц, страдающих ожирением, была показана связь генотипа (+/+) LPL с высоким уровнем холестерина в составе липопротеинов низкой и очень низкой плотности. Кроме того, впервые была показана протективная (защитная) роль генотипа с отсутствием мутации (-/-) LPL для развития нарушений липидного профиля даже при наличии у пациенток абдоминального ожирения. Кроме того, было показано, что генотип (-/-) LPL определяется у 70% долгожителей (старше 90 лет), что свидетельствует о его вкладе в прогноз долголетия. Наиболее сильная связь показана для дефектной ЛПЛ (генотип +/+) и высоких уровней триглицеридов и холестерина общего и в составе ЛПНП улиц, страдающих диабетом типа 2 (Perez и соавт., 2006).
I.III. Выявление неблагоприятного (+/+) LPL генотипа подразумевает проведение ряда профилактических мероприятий, направленных на стабилизацию липидного обмена. Персонализированная медицина определяет значимость индивидуального подхода (определение генотипа) в коррекции как веса, так и уровня липидов (триглицеридов и холестерина) плазмы крови.
Проведено исследование терапевтического эффекта статинов в связи с мутацией HindIII в гене LPL (Taylor и соавт., 2001). Действие статинов направлено на снижение уровня липидов плазмы. Все статины, включая ловастатин, правастатин, симвастатин, флувастатин и др. ингибируют редуктазу коэнзима A (HMG-CoA). Полиморфизм HindIII в гене LPL оказался связанным с резистентностью к лечению статинами. Для носителей гомозиготного генотипа (+/+) LPL лечение статинами неэффективно.
Клинический пример.
Пациент В., 23 лет, обратился в клинику с жалобами на лишний вес, одышку при физической нагрузке, повышение артериального давления до 180 и 120 мм рт.ст.
Из анамнеза: резкая прибавка веса в 14 лет, повышение АД последние 2 года, лечения не проводилось. Наследственность отягощена - у отца ожирение. Питание 2 раза в день, основной прием пищи вечером, более 45% рациона составляют жиры (предпочитает сосиски, мясо, яйца).
При объективном осмотре: рост 184 см, вес 144 кг, индекс массы тела составил 42,6 кг/м2, что соответствует ожирению 3 степени, т.е. морбидному. Окружность талии - 124 см, окружность бедер - 132 см, соотношение ОТ/ОБ - 0,94, что свидетельствует об абдоминальном типе распределения жировой ткани и является косвенным признаком инсулинорезистентности, артериальное давление - 160 и 100 мм рт.ст. При анализе состава тела содержание жировой ткани составило 38,7% (при норме до 15,9%) или 55,7 кг, содержание воды составило 47,8% (при норме 60-65%) или 68,8 литров.
При биохимическом исследовании крови было выявлено незначительное повышение уровня общего холестерина до 5,41 ммоль/л (при норме до 5,2 ммоль/л), повышение уровня мочевой кислоты до 448 ммоль/л (при норме до 420 ммоль/л). Уровень инсулина составил 20,9 мкМЕ/мл (норма 2,1-27,0 мкМЕ/мл), индекс инсулинорезистентности НОМА составил 4,72 при норме до 2,77. Остальные биохимические и гормональные показатели соответствовали значениям нормы.
Генетический анализ выявил генотип, соответствующий повышенной активности липопротеинлипазы.
Диагноз: ожирение 3 ст. (морбидное) с распределением жировой ткани по абдоминальному типу, синдром инсулинорезистентности, дислипидемия, гиперурикемия, артериальная гипертензия 2 степени, недостаточность кровообращения 0-1.
Учитывая данные клинического, биохимического и генетического исследований, пациенту был изменен режим и характер питания: 5-разовый прием пищи с перераспределением 2/3 суточного рациона на первую половину дня, а также выбор продуктов с низким содержанием жира - продукты с цветовым кодами №6 и №7. Кроме того, учитывая уровень АД, был рекомендован регулярный контроль артериального давления, ограничение употребления поваренной соли до 5 г в сутки, ренитек в начальной дозе 5 мг в сутки.
В течение первого месяца наблюдения по данным пищевого дневника было отмечено неоднократное отклонение от рекомендаций по выбору продуктов и режима питания. Пациенту был назначен препарат Орлистат (Ксеникал), блокирующий липопротеинлипазу, по 120 мг перед приемом пищи.
Правильность выбора продуктов оценивалась по характеру стула на фоне приема Орлистата - при несоблюдении рекомендаций и употреблении продуктов, богатых жиром, у пациента отмечался жидкий стул.
При контрольном биохимическом исследовании через 6 недель отмечена положительная динамика: нормализовался уровень общего холестерина, уровень инсулина снизился до 11,3 мкМЕ/мл, а индекс инсулинорезистентности - с 4,72 до 2,6 (норма до 2,77). Артериальное давление составило 140 и 90 мм рт.ст.
Вес -134 кг (уменьшился на 10 кг за 6 недель), индекс массы тела составил 39,6 кг/м2, окружность талии уменьшилась на 4 см и соотношение ОТ/ОБ составило 0,9.
В результате проводимого лечения, назначенного с учетом данных генетического анализа, у пациента снизился вес (перешел из категории «морбидное ожирение» в категорию «ожирение 2 степени»), уменьшилась окружность талии, нормализовались соотношение ОТ/ОБ и артериальное давление. За время наблюдения удалось сформировать правильные навыки по режиму питания и выбору продуктов.
II.I. Гормон грелин выделяют клетки желудка и поджелудочной железы в состоянии голода.
Грелин был открыт японским ученым (Masayasu Kojima) в 1999 г.Этот гормон регулирует процессы, связанны с пищеварением. В течение десятилетий существовала теория о единственном способе регуляции чувства голода или насыщения путем снижения уровня глюкозы в крови. Открытие нейропептидов - холецистокинина, глюкагоноподобного пептида-1, нейропептида YY и грелина, регулирующих биохимические процессы в гипоталамических центрах голода и насыщения, позволило определить роль центральной нервной системы в регуляции пищевого поведения.
До установления функции грелина в 70-х годах прошлого века в Японии был синтезирован синтетический аналог грелина, который стимулировал выработку гормона роста и был назван «секретагогом гормона роста». Позднее в гипоталамической области головного мозга, регулирующей энергообмен, был выделен рецептор «секретагога гормона роста». Поиск эндогенного субстрата для этого рецептора привел к открытию грелина. Колебание уровня грелина в организме человека зависит от состояний голода или насыщения. В состоянии голода уровень грелина возрастает (до четырех раз), а в состоянии насыщения снижается.
Недавно было показано, что больные с синдромом Прадера-Вили, страдающие ожирением, имеют высокие уровни грелина. Известно, что в структуре симптоматики синдрома Прадера-Вили часто выявляются приступы булимии. Предполагается, что именно высокий уровень грелина приводит к неконтролируемому перееданию у больных с синдромом Прадера-Вили.
В опытах на крысах Karvonen и соавт. (2001) было показано, что инъекции грелина на протяжении двух месяцев вызывают увеличение веса животных.
Механизм орексигенных свойств грелина был изучен Asakawa и соавт. (2001) на мышах, получавших перитонеальные инъекции гормона. С помощью молекулярно-генетических методов было показано, что введение грелина вызывает экспрессию нейропептида YY в аркуатных ядрах гипоталамуса. Известно, что нейропептид YY является регулятором чувства голода в проопиомеланокортиновой системе.
В настоящее время Broglio и соавт. (2004) доказано, что грелин не только стимулирует секрецию гормона роста и повышает аппетит, но и стимулирует секрецию пролактина и адренокортикотропного гормона (АКТГ) и увеличивает уровень глюкозы в крови.
II.II. В гене грелина выявлена мутация (Leu7Pro), приводящая к замене аминокислоты в структуре белка.
В опытах на дефициентных по гену грелина мышах Wortley и соавт.(2004) установили роль грелина в энергообмене. В эксперименте мыши (GREL-), получавшие высококалорийный с преобладанием жиров корм, имели незначительную прибавку в весе, но значимо сниженный процент жира в тканях.
Мутация (Leu7Pro) была изучена в связи с морбидным ожирением у детей в возрасте 8-11 лет (Korbonits и соавт. 2002). В результате проведенного исследования оказалось, что у детей - носителей мутации в гене грелина значимо снижен уровень инсулина в глюкозотолерантном тесте.
II.III. Так как в механизмах развития ожирения важным является орексигенный эффект грелина, одним из методов лечения ожирения может быть блокирование грелиновой передачи в гипоталамусе. Однако с учетом множественных эффектов грелина такой метод может иметь серьезные побочные эффекты.
В настоящее время в литературе есть единственное сообщение Kallio и соавт. (2001) о связи мутации (Leu7Pro) с возрастанием на 54% уровня гормона роста во время велоэргометрической нагрузки. Клиническое значение выявленного факта не известно.
Клинический пример.
Пациент Б., 40 лет, обратился с жалобами на лишний вес, частые головные боли, одышку.
Лишний вес с 30 лет, связывает с изменением образа жизни - стал питаться обильнее на фоне низкой физической активности. Максимальный вес 132 кг. С 32 лет выявлена гипергликемия (цифр указать не может), у эндокринолога не наблюдался, лечения не получал. Курит 20-40 сигарет в день. Основные приемы пищи 2 раза в день - обед и ужин, между ними - многочисленные перекусы. Суточная калорийность составила 3520 ккал (потребность 2650 ккал). У матери ожирение и артериальная гипертония.
Объективно: рост 174 см, вес 128,3 кг, индекс массы тела (ИМТ) 42,4 кг/м2 (при норме до 25 кг/м2), окружность талии (ОТ) 133 см, окружность бедер (ОБ) 123 см, соотношение ОТ/ОБ 1,08 (при норме до 0,9, повышение ОТ/ОБ свидетельствует о распределении жировой ткани по абдоминальному типу). Артериальное давление 139/100 мм рт.ст.(норма до 140/90 мм рт.ст.).
Пастозность стоп, голеней.
По данным анализа состава тела методом фотометрии содержание жировой массы составило 39,9% при норме до 22,3%.
При биохимическом исследовании крови выявлено: глюкоза натощак 9,56 ммоль/л (при норме до 6,1 ммоль/л), общий холестерин 7,8 ммоль/л (норма 3,4-5,2 ммоль/л), триглицериды 3,34 ммоль/л (норма 0,5-2,0 ммоль/л), липопротеиды высокой плотности 1,65 ммоль/л (норма 0,9-1,8), липопротеиды низкой плотности 4,64 ммоль/л (норма 1,5-3,5 ммоль/л).
При гормональном исследовании выявлен: инсулин натощак 30,4 мкМе/мл (норма 2,1-27,0 мкМе/мл), С-пептид 1430 пмоль/л (норма 360-1650 пмоль/л). Индекс инсулинорезистентности НОМА составил 12,9 при норме до 2,77.
По данным генетического анализа выявлен генотип, предрасполагающий к высокому уровню грелина, повышающего чувство голода.
Диагноз: ожирение 3 степени (морбидное) с распределением жировой ткани по абдоминальному типу, сахарный диабет тип 2, стадия декомпенсации (осложнения требуют уточнения), дислипидемия IIб типа, артериальная гипертония 1 степени, степень сосудистого риска 4, миокардиодистрофия, недостаточность кровообращения 1.
Учитывая суточную калорийность, стиль питания с многочисленными перекусами на фоне генетической предрасположенности к повышенному уровню грелина, пациенту, помимо лечения сахарного диабета, артериальной гипертонии и дислипидемии, рекомендовано:
1. 5-разовое питание с перераспределением 2/3 суточного рациона на первую половину дня,
2. для заполнения объема желудка без увеличения калорийности за 20-30 минут до еды прием растительной клетчатки, например Цитрусового пектина 750 мг, по 1 таблетке, запивая водой.
Лечение сахарного диабета, артериальной гипертонии, дислипидемии:
1. диета с исключением высокогликемичных углеводов (разрешены продукты с гликемическим индексом до 20 - продукты с цветовым кодом №1), в рационе 15% должны составлять белки, 25% жиры, преимущественно растительные, 60% углеводы;
2. контроль глюкозы крови натощак и через 2 часа после еды, от приема сахароснижающих препаратов категорически отказался; контроль артериального давления 2 раза в день, ограничение употребления поваренной соли до 5 г в сутки, постоянный прием гипотензивных препаратов из группы ингибиторов АПФ (учитывая наличие сахарного диабета);
3. для коррекции дислипидемии назначен Эзетрол 10 мг по 1 таблетке 1 раз в день.
За 7 месяцев наблюдения пациент снизил вес на 42,5 кг (с 128,3 до 85,8 кг), окружность талии уменьшилась на 33 см (со 133 до 100 см), индекс массы тела снизился с 42,4 до 28,33 кг/м2 (при норме до 25 кг/м2). В результате пациент из категории морбидного ожирения перешел в категорию избыточной массы тела. Окружность бедер уменьшилась на 21 см (с 123 до 102 см), ОТ/ОБ уменьшилось с 1,08 до 0,98, содержание жировой ткани уменьшилось с 39,9 до 23,7% (при норме до 22,3%).
Артериальное давление стабильно на уровне 130/80 мм рт.ст. От приема гипотензивных препаратов оказался. Одышки, пастозности стоп и голеней нет.
При контрольном исследовании биохимических и гормональных параметров выявлено:
- глюкоза натощак 4,5 ммоль/л (без сахароснижающих препаратов), через 2 часа после еды не более 7,5 ммоль/л, что соответствует значениям нормы;
- уровень инсулина снизился с 30,4 до 12 мкМе/мл (что соответствует значениям нормы), индекс инсулинорезистентности нормализовался и составил 2,4 (при норме до 2,77);
- уровень холестерина снизился с 7,8 до 6,3 ммоль/л (норма 3,4-5,2 ммоль/л), триглицеридов - с 3/34 ммоль/л до 2,5 ммоль/л (норма 0,5-2,0 ммоль/л), липопротеидов низкой плотности - с 4,64 до 4,1 ммоль/л (норма 1,5-3,5 ммоль/л).
Пациент отмечает значительное снижение чувства голода, улучшение общего самочувствия, повышение работоспособности.
Наблюдение и лечение продолжаются.
III.I. Инсулин - низкомолекулярный белок, секретируемый β-клетками островков Лангерганса поджелудочной железы. Эффекты инсулина опосредуются путем связывания с рецепторами инсулина. Биологические эффекты инсулина включают не только его влияние на обмен глюкозы, но и обмен липидов и белков, функцию эндотелия сосудов. Индивидуальная способность к усвоению глюкозы определяется не только количеством инсулина, но и чувствительностью рецепторов, активным транспортом глюкозы, а также регулируется факторами, прямо не связанными с регуляцией углеводного обмена. При хронической первичной гиперинсулинемии, обусловленной генетическими факторами, плотность инсулиновых рецепторов компенсаторно снижается, приводя к состоянию инсулинорезистентности. Предположение о важной роли инсулина в атерогенезе к настоящему времени неоднократно подтвердилось. При ожирении так же, как и при атеросклерозе, сахарном диабете 2-го типа и артериальной гипертензии часто выявляется гиперинсулинемия. Высокие уровни как натощакового, так и постпрандиального инсулина выявляются у практически здоровых молодых родственников больных, страдающих перечисленными заболеваниями.
III.II. Ген инсулина (INS) с применением молекулярно-генетических методов был открыт и изучен одним из первых. Известны три спорадические мутации гена, возникшие и передаваемые потомкам в трех разных семьях de novo. Эти мутации находятся в кодирующих областях гена и меняют структуру и активность инсулина. У всех носителей мутаций имеется натощаковая гиперинсулинемия, снижена активность циркулирующего инсулина, отмечается адекватная реакция на введение экзогенного инсулина.
При генотипировании гена инсулина в связи с первичной гиперинсулинемией используют VNTR полиморфизм в промоторной области, а именно участок с вариабельным количеством повторов небольшого участка ДНК (14-15 пар оснований). У разных людей число повторов может значительно варьировать - от 30 до 160. В гене инсулина выделяют три типа аллелей: аллели класса I (28-44 повторов, распространенность у европейцев приблизительно 50-70%,), класса II (практически не встречаемые у европейцев) и класса III (138-160 повторов, частота встречаемости в разных европейских популяциях приблизительно 5-30%). Число повторов в гене прямо пропорционально влияет на его активность. Аллели с большим числом повторов, то есть III класса, ответственны за выработку значительно большего количества инсулина, чем аллели I и II класса.
В настоящее время роль гена инсулина при ожирении практически не оставляет сомнений - аллель III класса считается связанной с развитием гиперинсулинемии, инсулинорезистентности и сахарного диабета 2 типа.
В работах по исследованию ожирения, синдрома поликистозных яичников и сахарного диабета типа 2 в связи с полиморфизмом гена INS показано, что гомозиготные носители аллелей III класса имеют гиперинсулинемию натощак и с течением времени развивающуюся компенсаторно инсулинорезистентность.
Изучение VNTR полиморфизма в связи с гестационным диабетом было проведено в группах 161 беременных женщин с гестационным диабетом и 111 здоровых беременных женщин (Litou и соавт. 2003). Целью исследования являлось определение частот аллелей гена INS в обследованных группах. Генотип III/III гена инсулина значимо чаще встречался в группе беременных женщин с гестационным диабетом, чем в контрольной группе. Рассчитанный относительный риск (3,97) для носительниц генотипа III/III был достаточно высоким для прогнозирования развития диабета во время беременности.
Более детальное изучение наследуемость аллелей гена инсулина было проведено Bennett и соавт. (2006). Авторами было показано, что аллели класса III передаются преимущественно от отцов, и, кроме того, носители генотипа III/III имеют высокий уровень инсулина натощак, а носители гетерозиготного генотипа I/III, то есть носители аллеля III, полученного от отца имеют постпрандиальную гиперинсулинемию.
III.III. В настоящее время имеется единственное сообщение о лечении диабета типа 2 в связи с полиморфизмом гена инсулина (Knowler и соавт., 2003). В популяции индейцев Пима оценивалась эффективность пероральных сахароснижающих препаратов и инъекций инсулина у носителей различных генотипов гена INS. Для носителей «предрасполагающих» к развитию диабета типа 2 генотиов III/III эффективность лечения была достоверно более высокой.
Клинический пример.
Пациентка П., 35 лет, обратилась с жалобами на лишний вес.
Из анамнеза известно, что набрала вес в 29 лет, после рождения двойни. В дальнейшем вес постепенно нарастал, и в общей сложности прибавка за 5 лет составила 30 кг.
Физические нагрузки регулярные в течение всей жизни: в детстве занималась большим теннисом, в настоящее время 3 раза в неделю занимается йогой и 2 раза в неделю большим теннисом. Не курит. У ближайших родственников лишнего веса нет.
Питание 3-4 раза в день, 90% суточного рациона приходится на вторую половину дня, при этом 50% суточного рациона - на ужин. Суточная калорийность составила 3280 ккал. При потребности в 2070 ккал.
При осмотре: рост 170 см, вес 91,3 кг, индекс массы тела (ИМТ) 31,6 кг/м2 (при норме до 25 кг/м2), окружность талии (ОТ) составила 105 см (при норме до 82 см), окружность бедер (ОБ) - 122 см, соотношение ОТ/ОБ - 0,86 (при норме до 0,8, увеличение индекса ОТ/ОБ свидетельствует об абдоминальном характере распределения жировой ткани). Артериальное давление составило 132/78 мм рт.ст.
При анализе состава тела содержание жировой массы составило 37% при норме до 26%.
При биохимическом исследовании крови выявлено: глюкоза 5,0 ммоль/л (норма до 6,1 ммоль/л), инсулин 14 мкМе/мл (норма 2,1-27,0 мкМе/мл), индекс инсулинорезистентности НОМА составил 3,13 (при норме до 2,77).
При проведении генетического анализа был выявлен генотип по гену INS III/III, предрасполагающий к натощаковой и постпрандиальной гиперинсулинемии, инсулинорезистентности и к набору веса. Причем периоды набора веса могут приходиться на периоды физиологической инсулинорезистентности (например, беременность, как и произошло у нашей пациентки, тем более что ее беременность была многоплодной) или при употреблении большого количества легкоусваиваемых углеводов.
Диагноз: ожирение 1 степени с распределением жировой ткани по абдоминальному типу, инсулинорезистентность, дислипидемия.
Учитывая данные анамнеза (резкий набор веса за беременность двойней), наличие инсулинорезистентности натощак, выявленный генотип, предрасполагающий к гиперинсулинемии, инсулинорезистентности, пациентке было рекомендовано:
1. выбор углеводов с низким гликемическим индексом - не более 35 (продукты с цветовыми кодами №1 и №2), 60% рациона должны составлять овощи, сырые или подвергшиеся минимальной термической обработке, несладкие фрукты,
2. 5-разовое питание с перераспределением 2/3 суточного рациона на первую половину дня,
3. перед основными приемами пищи прием препарата Акарбоза (Глюкобай) 50 мг, блокирующего альфа-глюкозидазу и снижающего всасывание углеводов.
Через 3 месяца наблюдения пациентка снизила вес с 91,3 до 75 кг - на 16,3 кг, ИМТ с 31,6 до 26,5 кг/м2 (норма до 25 кг/м2), окружность талии (ОТ) со 105 до 88 см (норма до 82 см) - на 17 см, окружность бедер (ОБ) с 122 до 109 см - на 13 см, соотношение ОТ/ОБ с 0,86 до 0,8, т.е. до нормы. Содержание жировой массы снизилось с 37% до 30% при норме до 26%. Индекс инсулинорезистентности снизился с 3,13 до 2,2, что соответствует значениям нормы.
В дальнейшем прием препарата Акарбоза был отменен и пациентка осталась на питании низкогликемичной пищей.
Таким образом, назначение с учетом данных генетического анализа питания и препаратов, снижающих поступление легкоусваиваемых углеводов, привело к снижению веса, нормализации показателя ОТ/ОБ, свидетельствующего об уменьшении абдоминального жира, к устранению инсулинорезистентности.
IV.I. Белки, связывающие жирные кислоты, представляют семейство схожих по структуре протеинов, но функционирующих в разных органах и тканях. Кроме непосредственного участия в липидном обмене белки, связывающие полиненасыщенные жирные кислоты, доставляют их в ядра клеток, влияя на скорость транскрипции многих генов. Для диагностики острого коронарного синдрома в настоящее время используются иммуноферментные методы выявления миокардиального белка, связывающего жирные кислоты (H-FABP). Для оценки химически индуцированного апоптоза клеток печени используют метод выявления печеночного белка, связывающего жирные кислоты (L-FABP). Белок, связывающий жирные кислоты 2 (FABP2), обеспечивает транспорт длинноцепочечный жирных кислот в клетках кишечника.
IV.II. Среди всех известных полиморфизмов гена FABP2 только точечная замена 163 G>A (Ala54Thr) во втором экзоне связана с изменением первичной структуры белка, изменяя его активность. Частота мутации (аллеля Thr54) значительно варьирует в разных популяциях - от 0,14 у американских индейцев (Oji-Cree) до 0,43 у японцев. В азиатских популяциях частота находится в пределах от 0,30 до 0,40; в европейских - от 0,27 до 0,35.
При изучении постпрандиальной липемии в связи с разными вариантами преимущественно потребляемых жирных кислот было показано, что носители аллеля Thr54 имеют повышенный постпрандиальный уровень холестерина в хиломикронах при преобладании насыщенных жирных кислот в структуре питания (Dworatzek, 2004). Кроме того, по результатам исследований Baier и соавт., (1995) постпрандиальная аффинность к длинноцепочечным жирным кислотам белка FABP2 с заменой Thr54 оказалась выше in vivo, а также in vitro, что указывает на роль этого полиморфизма в этиологии нарушений липидного обмена. Носители аллеля Thr54 имеют статистически достоверно повышенный уровень триглицеридов натощак в составе липопротеинов высокой плотности (Berthier, 2006), а также повышенный постпрандиальный уровень триглицеридов в составе хиломикронов и липопротеидов низкой и очень низкой плотности. В ряде публикаций существуют согласованные данные о наличии связи между генотипом FABP2 Thr/Thr и повышенным уровнем инсулина, определяемого натощак (Albala, 2004). Для японской популяции показано, что генотип Thr/Thr ассоциирован с повышенным уровнем инсулина как натощак, так и после нагрузки глюкозой (Weiss, 2007). Многие исследования в различных популяциях подтверждают данные о наличии связи между полиморфизмом Ala54Thr и наличием инсулинорезистентности. У мексиканцев, больных диабетом типа 2, Mitchell и соавт.(2006) установили множественные связи между генотипом Thr/Thr и индексом массы тела, уровнем С-пептида, уровнем инсулина натощак и через 2 ч после приема пищи.
IV.III. Французские ученые Gastaldi и соавт., 2007, изучали связь полиморфизма FABP2 с показателями липидов плазмы крови у лиц с высокой предрасположенностью к сердечно-сосудистой патологии при изменении характера питания. План диетических рекомендаций включал значительное снижение в рационе питания насыщенных жирных кислот и увеличение мононенасыщенных и полиненасыщенных жирных кислот. Базальные уровни олеиновой кислоты и холестерина значительно варьировали у носителей различных генотипов FABP2. Однако изменение тех же показателей оказалось не связанным с полиморфизмом FABP2 после 12 месяцев применения диетотерапии.
Клинический пример.
Пациент Ж., 33 лет, обратился с жалобами на прогрессирующий набор веса. Из анамнеза: с детства пациент интенсивно занимался плаванием и не имел лишнего веса, после прекращения занятий спортом в 14 лет за год набрал 45 кг. В дальнейшем вес постепенно продолжал нарастать. Предпринимал неоднократные попытки снизить вес: различные виды диет, прием Гербалайфа - без существенных результатов. В 1996 г. с целью уменьшить потребление пищи проведено формирование малого желудка (объемом 50 мл). В результате указанного оперативного вмешательства достигнута относительная стабилизация веса, но снижения веса не произошло.
Мать пациента страдает ожирением, у сына пациента (11 лет) имеется избыточная масса тела.
Питание 2-3 раза в день, предпочитает колбасы, копчености, сыр, шоколад, мучное. Суточная калорийность составила 2200 ккал, основные приемы пищи приходятся на вторую половину дня.
Объективно: рост 177 см, вес 187,6 кг, индекс массы тела (ИМТ) - 59,9 кг/м2 (при норме до 25 кг/м2), окружность талии (ОТ) - 174 см, окружность бедер (ОБ) - 161 см, соотношение ОТ/ОБ -1,08 (при норме до 0,9), живот резко увеличен в объеме, свисает в виде «фартука». На коже живота, поясничной, подмышечной областей широкие розовые полосы растяжения («стрии»).
Артериальное давление составило 158/109 мм рт.ст.
При анализе состава тела выявлено значительное увеличение содержания жировой ткани - до 45,8% (при норме для мужчины 33 лет - до 22,3%).
При биохимическом исследовании крови выявлено: общий холестерин - 8,09 ммоль/л (норма 3,4-5,2 ммоль/л), триглицериды - 1,43 ммоль/л (норма 0,5-2,0 ммоль/л), липопротеиды высокой плоскости (ЛПВП) -1,9 ммоль/л (норма 0,9-1,8 ммоль/л), липопротеиды низкой плотности (ЛПНП) - 5,54 ммоль/л (норма 1,5-3,5 ммоль/л).
Данные гормонального исследования в пределах нормы.
Генетический анализ выявил генотип, соответствующий повышенной активности ферментов, отвечающих за всасывание холестерина в эпителии тонкого кишечника.
Диагноз: ожирение 3 степени (морбидное) с распределением жировой ткани по абдоминальному типу, дислипидемия тип IIа, артериальная гипертензия 2 степени, риск сосудистых осложнений 2-3.
Учитывая данные биохимического и генетического исследований, для коррекции дислипидемии на фоне морбидного ожирения пациенту была назначена низкожировая диета - продукты с цветовыми кодами №6 и №7, даны рекомендации по изменению режима питания (5-разовый прием пищи с обязательным завтраком, составляющим 20-25% суточного рациона). Кроме того, регулярно проводился контроль артериального давления, было ограничено употребления поваренной соли до 5 г в сутки, назначен прием гипотензивных препаратов (эналаприл 5 мг).
Через 2 месяца после контрольного определения параметров липидного обмена не было отмечено их снижения. В связи с этим к лечению был добавлен препарат Эзетимиб (Эзетрол), блокирующий ферменты, отвечающие за всасывание холестерина в эпителии тонкого кишечника, по 10 мг 1 раз в сутки.
Пациент находился под наблюдением более 2-х лет. За это время вес снизился со 187,6 кг до 146,1 кг (на 41,5 кг), индекс массы тела снизился с 59,9 кг/м2 до 46,6 кг/м2, окружность талии уменьшилась со 174 до 144 см (на 30 см), соотношение ОТ/ОБ с 1,08 до 0,9. При анализе состава тела содержание жировой массы уменьшилось с 45,6% до 36,4%.
При контрольном биохимическом исследовании уровень холестерина снизился до 6,4 ммоль/л, триглицеридов до 1,9 ммоль/л, ЛПНП до 3,1 ммоль/л.
Артериальное давление на фоне уменьшения веса и приема гипотензивных препаратов снизилось до 120-130/95 мм рт.ст.(У пациента при приеме гипотензивных препаратов из группы ингибиторов АПФ возник упорный кашель, из-за чего пациент был переведен на физиотенз.)
Таким образом, лечение ожирения и ассоциированных с ним нарушений липидного обмена с генотипированием FABP позволяет добиваться эффективных результатов.
V.I. Жировая ткань человеческого организма представлена белой и бурой жировой тканью. Бурая жировая ткань регулирует теплопродукцию - «дрожательный термогенез» у младенцев. У взрослых людей ее функция точно не установлена. В адипоцитах белой жировой ткани происходят биохимические процессы липолиза и липогенеза, поэтому этот вид жировой ткани играет основную роль в энергетическом обмене. Кроме того, белая жировая ткань посредством сложных рецепторных взаимодействий регулирует работу эндокринной и половой систем. В жировой ткани широко распространены β3-адренорецепторы. β3-адренорецепторы стимулируются симпатической нервной системой, их функцией в целом является ускорение процесса высвобождения энергии. Стимуляция этих рецепторов норадреналином приводит к усилению липолиза в жировой ткани, повышению энергообмена и теплопродукции
V.II. По результатам исследований, проведенных в разных странах, нарушение функции β3-адренорецепторов, связанное с мутацией гена Adrβ3, приводит к ожирению, инсулинорезистентности и раннему развитию сахарного диабета 2 типа. Предрасполагающий к ожирению генотип Trp64Arg встречается у европейцев с частотой от 0,08 до 0,13. Во всех работах по изучению мутации гена Adrβ3 установлен внешний фактор, необходимый для проявления рецепторной недостаточности β3-рецепторов - хроническое перенапряжение симпатической нервной системы.
V.III. Известны результаты разработок синтетических агонистов β3-рецепторов с целью их применения для лечения ожирения с повышением интенсивности энергообмена.
Впервые в сентябре 2006 г. на 10-м Всемирном конгрессе по ожирению в Сиднее было доложено о новом препарате ТАК-677, являющимся селективным агонистом β3-адренорецепторов. Этот препарат не вызывает таких побочных эффектов, как тахикардия, повышение артериального давления и тремор, и повышает базальный уровень энергообмена в жировой ткани. Однако введение ТАК-677 в практику лечения ожирения в ближайшее время маловероятно, так как он еще не прошел III фазу клинических испытаний.
В настоящее время при отсутствии противопоказаний для лечения ожирения и метаболических нарушений используют препарат центрального действия Сибутрамин. Механизм действия обусловлен селективным ингибированием обратного захвата моноаминов - серотонина, норадреналина и дофамина. Нормализация моноаминового обмена в гипоталамусе приводит к снижению чувства голода и соответственно к снижению потребления пищи, а через усиление норадреналинового обмена в симпатической нервной системе активирует β3-адренорецепторы.
Клинический пример.
Пациентка Я., 32 лет, обратилась с жалобами на выраженный лишний вес, ограничивающий физическую активность.
Сильный набор веса отмечает после 17 лет, когда после окончания школы прекратила занятия спортом (активно занималась баскетболом). Наследственность по ожирению не отягощена. Не курит. Физическая активность в настоящее время низкая.
Суточная калорийность рациона - 2105 ккал при потребности в 2214 ккал. Питание 4 раза в день, при этом 90% суточного рациона приходится на вторую половину дня.
Объективно: рост 174 см, вес 142,5 кг, индекс массы тела (ИМТ) 47,07 кг/м2, что ответствует 3 степени ожирения - морбидному (норма до 25 кг/м2), окружность талии (ОТ) - 111 см (норма до 82 см), окружность бедер (ОБ) - 143 см, соотношение ОТ/ОБ составило 0,78 (норма до 0,8), что говорит о равномерном распределении жировой клетчатки. Артериальное давление составило 125/86 мм рт.ст.
По данным анализа состава тела содержание жировой массы составило 45,5% при норме до 23,1%.
При биохимическом и гормональном исследовании крови выявлено: инсулин - 17,2 мкМе/мл (норма 2,1-27,0), глюкоза 4,82 ммоль/л (норма до 6,1 ммоль/л), индекс инсулинорезистентности НОМА составил 3,684 (норма до 2,77). Остальные параметры были в пределах нормы.
По данным генетического исследования выявлен генотип, предрасполагающий к низкой активности β3-адренорецепторов, расположенных в жировой ткани и отвечающих за активность высвобождения энергии путем теплообразования и липолиза.
Диагноз: ожирение 3 степени (морбидное) с равномерным распределением жировой ткани.
Представляет интерес тот факт, что пациентка с морбидным ожирением имеет суточную калорийность ниже требуемой. Первоначальный набор веса был связан с прекращением активных занятий спортом. Это подтверждает роль низкого уровня энергообмена в формировании у нее ожирения.
Учитывая выраженность ожирения и генетически обусловленную низкую активность метаболических процессов, пациентке рекомендовано:
1. перераспределить 2/3 суточного рациона на первую половину дня, последний прием пищи должен быть за 3 часа до сна,
2. учитывая инсулинорезистентность (вторичную), при выборе продуктов исключить углеводы с гликемическим индексом более 35 (разрешены продукты с цветовыми кодами №1 и №2),
3. прием препарата Сибутрамин (Меридиа), одним из эффектов которого является активация β3-адренорецепторов с усилением термогенеза; препарат был назначен в дозе 10 мг 1 раз в сутки утром.
Пациентка находилась под нашим наблюдением 9 месяцев. За это время она снизила вес на 58,6 кг (со 142,5 до 83,9 кг). Индекс массы тела снизился с 47,07 до 27,71 кг/м2. Таким образом, пациентка перешла из категории морбидного ожирения в категорию избыточной массы тела. Содержание жировой ткани снизилось с 45,5 до 32,06% (норма до 23,1%). Окружность талии уменьшилась со 111 до 84 см (на 27 см), окружность бедер - с 143 до 115 см (на 28 см), соотношение ОТ/ОБ составило 0,73. Уровень инсулина снизился с 17,2 до 11 мкМе/мл, индекс инсулинорезистентности так же снизился с 3,684 до 2,2 (норма до 2,77).
Сибутрамин отменен, пациентка продолжает придерживаться диетических рекомендаций.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ формирования индивидуальных диетических рекомендаций на основе ДНК анализа | 2017 |
|
RU2691145C2 |
| Панель для определения предрасположенности к увеличению индекса массы тела, метаболическому синдрому и сахарному диабету 2-го типа и ее использование | 2024 |
|
RU2822360C1 |
| СПОСОБ ЛЕЧЕНИЯ МЕТАБОЛИЧЕСКОГО СИНДРОМА | 2010 |
|
RU2452523C1 |
| Способ оценки индивидуального риска формирования избыточной массы тела и ожирения у детей, потребляющих питьевую воду с повышенным содержанием хлороформа и тетрахлорметана | 2016 |
|
RU2619872C1 |
| Способ лечения пациентов с метаболическим синдромом | 2017 |
|
RU2666288C1 |
| СПОСОБ ЛЕЧЕНИЯ АБДОМИНАЛЬНОГО ОЖИРЕНИЯ ПРИ МЕТАБОЛИЧЕСКОМ СИНДРОМЕ | 2013 |
|
RU2548709C1 |
| СПОСОБ ЛЕЧЕНИЯ МЕТАБОЛИЧЕСКОГО СИНДРОМА ПРИ ЭМОЦИОГЕННОМ ТИПЕ ПИЩЕВОГО ПОВЕДЕНИЯ | 2015 |
|
RU2591811C1 |
| СПОСОБ ЛЕЧЕНИЯ МЕТАБОЛИЧЕСКОГО СИНДРОМА | 2015 |
|
RU2583944C1 |
| СПОСОБ ЛЕЧЕНИЯ НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНИ ПЕЧЕНИ У ПАЦИЕНТОВ С МЕТАБОЛИЧЕСКИМ СИНДРОМОМ ПРИ НЕДОСТАТОЧНОСТИ ВИТАМИНА D | 2018 |
|
RU2694842C1 |
| СПОСОБ ОЦЕНКИ РИСКА РАЗВИТИЯ МЕТАБОЛИЧЕСКОГО СИНДРОМА У ДЕТЕЙ НА ОСНОВЕ ГЕНЕТИЧЕСКИХ И БИОХИМИЧЕСКИХ МАРКЕРОВ | 2012 |
|
RU2492485C1 |















Изобретение относится к медицине, а именно к эндокринологии, и касается лечения и/или профилактики ожирения или избыточной массы тела. Для этого конкретизируют причины избыточного веса путем исследования полиморфизма генов, выбранных из ряда: LPL, GREL, INS, FABP2, ADRb3. При этом выбор диеты и фармакотерапии осуществляют в зависимости от вариантов выявленного полиморфизма. Способ обеспечивает эффективное лечение избыточной массы тела за счет выбора адекватной фармако- и диетотерапии для каждого конкретного больного. 8 з.п. ф-лы, 1 табл., 24 ил.
1. Способ лечения и/или профилактики ожирения или избыточной массы тела, включающий конкретизацию причин избыточного веса путем исследования полиморфизма генов, выбранных из ряда: LPL, GREL, INS, FABP2, ADRb3, при этом выбор диеты и фармакотерапии осуществляют в зависимости от вариантов выявленного полиморфизма.
2. Способ по п.1, характеризующийся тем, что, если причина избыточной массы тела или ожирения связана с полиморфизмом в гене LPL, для лечения ожирения назначают низкожировую диету.
3. Способ по п.2, характеризующийся тем, что для лечения ожирения дополнительно к низкожировой диете вводят препарат Орлистат, блокирующий фермент LPL.
4. Способ по п.1, характеризующийся тем, что если причина избыточной массы тела и ожирения связана с полиморфизмом в гене GREL, то для коррекции и профилактики нарушения пищевого поведения назначают диету из продуктов, богатых клетчаткой.
5. Способ по п.4, характеризующийся тем, что дополнительно к диете из продуктов, богатых клетчаткой, вводят биологически активные добавки, богатые клетчаткой.
6. Способ по п.1, характеризующийся тем, что, если причина ожирения и нарушений углеводного обмена связана с полиморфизмом в гене INS, то для коррекции нарушений углеводного обмена и снижения веса назначают низкогликемичную диету.
7. Способ по п.6, характеризующийся тем, что дополнительно к низкогликемичной диете вводят препарат Акарбоза, снижающий всасывание углеводов в кишечнике.
8. Способ по п.1, характеризующийся тем, что, если причина ожирения и ассоциированной с ним дислипидемии связана с полиморфизмом в гене FABP2, то для коррекции нарушений липидного обмена вводят дополнительно препарат Эзетимиб, блокирующий всасывание жирных кислот в тонком кишечнике.
9. Способ по п.1, характеризующийся тем, что, если причина ожирения связана с полиморфизмом в гене ADRb3, то для коррекции нарушения функции симпатической нервной системы на уровне регуляции энергетического обмена в жировой ткани, приводящего к абдоминальному ожирению, вводят препарат Сибутрамин, активирующий функцию адренорецептора типа b3.
| СПОСОБ ЛЕЧЕНИЯ ИЛИ ПРЕДУПРЕЖДЕНИЯ ОЖИРЕНИЯ | 2002 |
|
RU2314121C9 |
| ПОЛИПЕПТИД ОЖИРЕНИЯ (ОВ)(ВАРИАНТЫ), ЕГО АНАЛОГ (ВАРИАНТЫ) И СЛИТЫЙ БЕЛОК (ВАРИАНТЫ), ИЗОЛИРОВАННАЯ МОЛЕКУЛА НУКЛЕИНОВОЙ КИСЛОТЫ, МОЛЕКУЛА ДНК, РЕКОМБИНАНТНЫЙ ВЕКТОР КЛОНИРОВАНИЯ, РЕКОМБИНАНТНЫЙ ВЕКТОР ЭКСПРЕССИИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, МОНОКЛОНАЛЬНОЕ И ПОЛИКЛОНАЛЬНОЕ АНТИТЕЛО | 1995 |
|
RU2273645C9 |
| MX 2008002028 А, 27.03.2008 | |||
| Диета и физические упражнения достаточно быстро нормализуют обмен веществ у мужчин с ожирением | |||
| Солесос | 1922 |
|
SU29A1 |
| ТРЕТЬЯКОВ В.Е | |||
| и др | |||
| Генетическая паспортизация населения - новая | |||
Авторы
Даты
2010-11-10—Публикация
2008-09-18—Подача