Область техники, к которой относится изобретение
Группа изобретений относится к области медицины, а именно к эндокринологии и генетике, и может быть использована для определения вероятности развития функциональных нарушений метаболизма и утилизации глюкозы, этиологически вызванных различными полиморфными вариантами в генах, отвечающих за синтез инсулина, восприимчивость клеток к инсулину, функцию бета-клеток поджелудочной железы, утилизацию глюкозы.
Изучение наследственной предрасположенности к многофакторным заболеваниям крайне важно для их диагностики и терапии. Сахарный диабет (СД) – это группа метаболических (обменных) заболеваний, характеризующихся хронической гипергликемией, которая является результатом нарушения секреции инсулина, действия инсулина или обоих этих факторов. В 1999 г. Всемирной Организацией здравоохранения была введена классификация СД основанная на различиях в механизмах развития данного заболевания:
СД 1-го типа. Развивается из-за аутоиммунной или идиопатической деструкции β-клеток поджелудочной железы, обычно приводящей к абсолютной инсулиновой недостаточности.
СД 2-го типа может развиваться двумя путями:
• с преимущественной инсулинорезистентностью и относительной инсулиновой недостаточностью;
• с преимущественным дефектом секреции инсулина с инсулинорезистентностью или без нее.
Другие специфические типы СД (генетические дефекты функции β-клеток, генетические дефекты действия инсулина, болезни экзокринной части поджелудочной железы, эндокринопатии, инфекции, др.генетические синдромы сочетающиеся с СД) и гестационный СД, возникающий при беременности.
Для СД типа 2, так же, как и для других многофакторных заболеваний характерна полигения, то есть клинический фенотип является результатом действия нескольких генетических локусов.
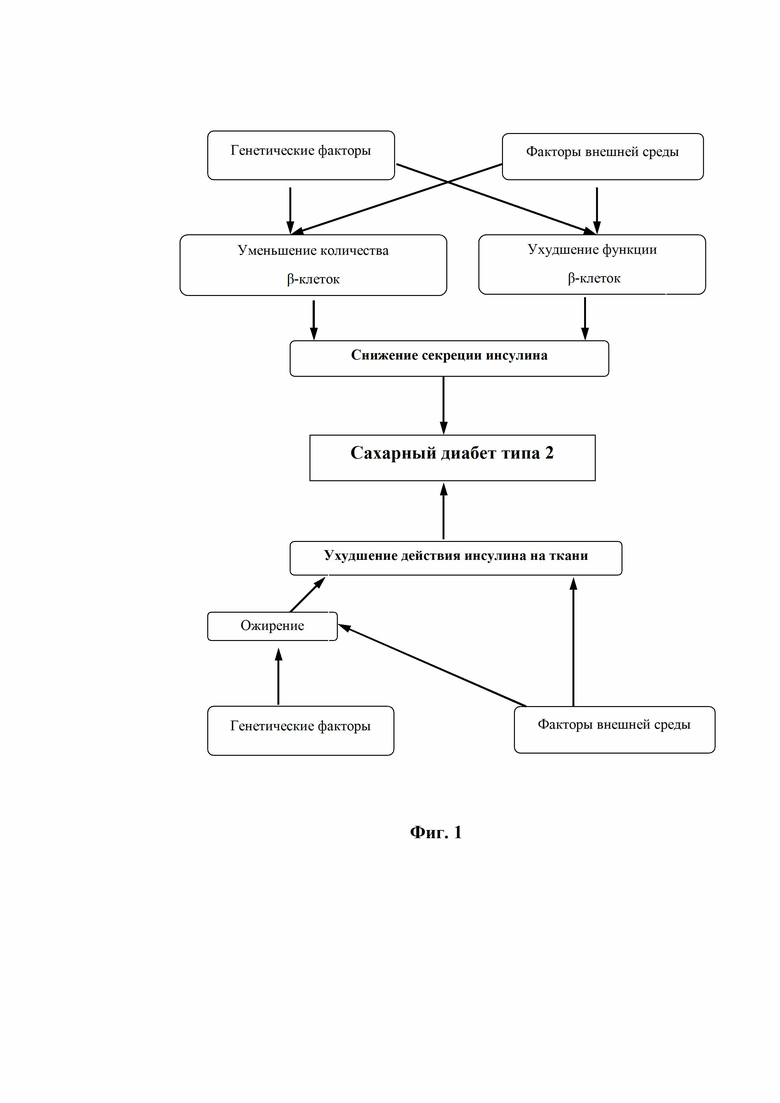
В настоящее время ключевыми звеньями патогенеза СД типа 2 считают инсулинорезистентность (ИР), нарушение секреции инсулина, повышение продукции глюкозы печенью, а также наследственную предрасположенность и особенности образа жизни и питания, ведущие к ожирению. Генетический вклад можно разделить на два типа: гены, влияющие на развитие инсулинорезистентности в периферических тканях (мышцы, печень) и гены, связанные с нарушением развития, роста, пролиферации и функции β-клеток поджелудочной железы (фиг.1. Факторы развития сахарного диабета 2 типа).
По мере углубления нашего понимания патогенеза сахарного диабета расширяются возможности применения этих знаний в клинической практике. Это позволит подбирать терапию для лечения при нарушениях метаболизма глюкозы на основе генетических данных, по всем принципам превентивной и предиктивной медицины.
Уровень техники
В настоящее время оценку метаболизма глюкозы проводят по результатам лабораторного определения уровня глюкозы, инсулина, индекса инсулинорезистентности, гликированного гемоглобина, которые в комплексе с другими клинико-лабораторными показателями определяют дальнейшую тактику ведения пациента. По результатам данного обследования делается вывод о нарушениях в обмене глюкозы и назначается определенная терапия, диета и прочие лечебные мероприятия. В ряде случаев нарушения метаболизма глюкозы обусловлены генетическими нарушениями в генах: функции бета-клеток поджелудочной железы (TCF7L, KCNJ11, PPARG), секреции инсулина (TCF7L, CDKAL), ассоциированных с индексом массы тела и ожирения (ADIPOQ, FTO, HHEX, MC4R, KCNQ1), повышенного уровня глюкозы (SLC30A8, TCF7L, CDKAL), инсулинорезистентности (TCF7L), гестационного диабета (MTNR1B, CDKAL1, HHEX), ассоциированных с СД 2-го типа (TCF7L, KCNJ11, PPARG, CDKAL, ADIPOQ, FTO, HHEX, SLC30A8, MC4R, KCNQ1, MTNR1B).
Некоторые полиморфные варианты генов хорошо известны своей ассоциацией с СД2, например, как PPARA, другие являются новыми и потенциально открывают новые возможности для дальнейших исследований. В работе [Liuetal. BMC SystemsBiology 2012, 6(Suppl 3):S15] были исследованы массивы данных, полученных от практически здоровых лиц (3004человек), в сравнении массивом данных, полученных от 1999 больных сахарным диабетом 2 типа. В результате было показано более 10 значимых полиморфизмов, ассоциированных в СД 2 типа. Найденные ассоциации могут использоваться для лучшего понимания патогенеза сахарного диабета 2 типа.
В научной литературе описаны различные полиморфизмы, связанные с гестационным сахарным диабетом (ГСД), который может поражать один или несколько функции, в статье [Ortega-Contreras B, Armella A, Appel J, et al (2022) Pathophysiological Role of Genetic Factors Associated With Gestational Diabetes Mellitus. Front. Physiol. 13:769924.doi: 10.3389/fphys.2022.769924] суммированы основные ткани и органы, которые могут подвержены влиянию полиморфизмов, ассоциированных с ГСД во время беременности.
Комплексное фенотипирование и генотипирование больных диабетом на преддиабетической стадии помогает в точной диагностике, профилактике, прогнозировании и терапии. Усовершенствование геномных технологий привело к идентификации нескольких генетических локусов, связанный с СД2. Однако полный набор вариантов генов предрасположенности к СД2 остается неадекватным, что требует дополнительных генетических исследований среди представителей различных этнических групп [Venkatachalapathy et al, Pharmacogenomics and Personalized Medicinein Type 2 Diabetes Mellitus: Potential Implications for Clinical Practice Pharmacogenomics and Personalized Medicine 2021:14 https://doi.org/10.2147/PGPM.S329787; https://www.snpedia.com/index.php/Rs2241766].
Наиболее близким аналогом разработанной нами диагностической панели является диагностическая панель по исследованию рисков развития СД 2 типа, которая уже существует на рынке медицинских лабораторных услуг [https://genomed.ru, https://web.archive.org/web/20221129171801/https:/price.genomed.ru/analysis/view?id=618]. Известная панель содержит средства для определения следующих полиморфизмов:TCF7L2 - rs7903146, rs12255372, MTNR1B - rs10830963, CDKAL1 - rs7754840, rs7756992, KCNJ11- rs5219. В известной панели предложено использование сочетания генотипов полиморфизмов в генах: функции бета-клеток поджелудочной железы (TCF7L, KCNJ11), секреции инсулина (TCF7L, CDKAL), ассоциированных с индексом массы тела и ожирении (FTO), повышенного уровня глюкозы (TCF7L, CDKAL), инсулинорезистентности (TCF7L), гестационного диабета (MTNR1B, CDKAL1), ассоциированных с СД 2-го типа (TCF7L, KCNJ11, CDKAL, FTO, MTNR1B).
Однако применение данной известной панели для полноценной диагностики ограничивается тем, что исследуются не все участки генов, ассоциированных с развитием метаболического синдрома, СД и ожирением, что не позволяет сделать полноценный диагностический охват возможных предрасположенностей к данным нарушениям.
Технической проблемой решаемой в настоящем изобретении являлся оригинальный выбор сочетания генов/полиморфизмов/генотипов, подходящий для точного выявления предрасположенности к развитию сахарного диабета, о чем свидетельствует практическое отсутствие на рынке диагностических панелей полиморфизмов (SNP), подходящих для диагностики нарушений обмена глюкозы, развития ожирения, метаболического синдрома и СД 2-го типа.
Раскрытие сущности изобретения
Достигаемым техническим результатом настоящего изобретения является повышение точности определения предрасположенности к развитию нарушений обмена глюкозы, развития ожирения, метаболического синдрома и СД 2-го типа, на основе уникального сочетания полиморфизмов, что позволяет одномоментно выявлять наиболее часто встречающиеся полиморфизмы, дает возможность провести более полный диагностический охват и не пропустить возможные изменения в генотипе. Данная панель также позволит превентивно скорректировать тип питания, образ жизни пациента, подобрать эффективную дозировку лекарственных препаратов.
Достижение указанного технического результата обеспечивается предложенной панелью для определения предрасположенности к развитию нарушений метаболизма на основе использования уникального сочетания генотипов полиморфизмов в генах: функции бета-клеток поджелудочной железы (TCF7L, KCNJ11, PPARG), секреции инсулина (TCF7L, CDKAL), ассоциированных с индексом массы тела и ожирения (ADIPOQ, FTO, HHEX, MC4R, KCNQ1), повышенного уровня глюкозы(SLC30A8, TCF7L, CDKAL), инсулинорезистентности (TCF7L), гестационного диабета (MTNR1B, CDKAL1, HHEX), ассоциированных с СД 2-го типа (TCF7L, KCNJ11, PPARG, CDKAL, ADIPOQ, FTO, HHEX, SLC30A8, MC4R, KCNQ1, MTNR1B).
Созданная панель включает средства для обнаружения в образце от пациента следующих полиморфизмов:
PPARG - rs1801282
TCF7L2 - rs7903146, rs12255372, rs7901695
MC4R - rs2229616
ADIPOQ - rs1501299, rs182052, rs2241766
KCNQ1 - rs2237892
FTO - rs17817449, rs1121980, rs1421085
MTNR1B - rs10830963
CDKAL1 - rs7754840, rs7756992, rs9465871,
SLC30A8 - rs13266634
HHEX - rs5015480
KCNJ11- rs5219, rs5215
Достижение указанного технического результата обеспечивается также предложенным способом определения предрасположенности к развитию нарушений метаболизма на основе использования уникального сочетания генотипов полиморфизмов в генах: функциибета-клетокподжелудочнойжелезы (TCF7L, KCNJ11, PPARG), секрецииинсулина (TCF7L, CDKAL), ассоциированных с индексом массы тела и ожирения (ADIPOQ, FTO, HHEX, MC4R, KCNQ1), повышенного уровня глюкозы (SLC30A8, TCF7L, CDKAL), инсулинорезистентности (TCF7L), гестационного диабета (MTNR1B, CDKAL1, HHEX), ассоциированных с СД 2-готипа (TCF7L, KCNJ11, PPARG, CDKAL, ADIPOQ, FTO, HHEX, SLC30A8, MC4R, KCNQ1, MTNR1B).
Предложенный способ характеризуется использованием средств для обнаружения в образце от пациента полиморфизмов генов, ассоциированных с нарушениями метаболизма глюкозы, и выявлением по результатам обнаружения полиморфизмов возможной предрасположенности пациента к развитию ожирения, метаболического синдрома и СД 2-го типа.
При этом предложенный способ предусматривает использование указанной панели полиморфизмов, а именно способ включает выявление в образце от пациента следующих полиморфизмов:
1. PPARG - rs1801282
2. TCF7L2 - rs7903146, rs12255372, rs7901695
3. MC4R - rs2229616
4. ADIPOQ - rs1501299, rs182052, rs2241766
5. KCNQ1 - rs2237892
6. FTO - rs17817449, rs1121980, rs1421085
7. MTNR1B - rs10830963
8. CDKAL1 - rs7754840, rs7756992, rs9465871,
9. SLC30A8 - rs13266634
10. HHEX - rs5015480
11. KCNJ11- rs5219, rs5215,
где наличие у пациента хотя бы одного из указанных полиморфизмов свидетельствует о возможной предрасположенности к развитию нарушений метаболизма.
По полученным нами данным, при использовании альтернативной диагностической панели для диагностики предрасположенностей к риску развития СД2, ожирения и инсулинорезистентности, из-за недостаточного охвата рисковых аллелей в генах, ассоциированных с развитием нарушений метаболизма, возможно установление ошибочного вывода, например, об отсутствии риска СД. При сравнении результатов исследования Пациента №3 с помощью альтернативной диагностической панели, было выявлено, что отсутствуют риски развития нарушения метаболизма глюкозы, низкий риск развития СД, инсулинорезистенстности и ожирения, при этом при анализе полиморфизмов с помощью предложенной панели были обнаружены полиморфизмы в генах рецептора мелатонина 1B (MTNR1B), рецептора активируемый пролифераторомперексиса типа 2 (PPARG2), в гене трансмембранного переносчика цинка типа 8 (SLC30A8), и данный генотип ассоциирован с увеличением риска СД2, метаболического синдрома более чем в 2 раза, о чем и свидетельствовали данные дополнительных лабораторных исследований (табл.8). Для поиска подходящего для создания панели сочетания полиморфизмов, позволяющих составить однозначное предположение о риске нарушений метаболизма было проведено исследование с учетом следующих факторов, указанных в таблице 1.
Таблица 1
С/Т - увеличение риска СД2 в 1,7
CYP2C9
С/Т – увеличение риска СД2 в 2,1 раза. Снижение выработки инсулина натощак и при увеличении уровня глюкозы.
T/T - увеличение риска СД2 в 1.5 раза, более высокий уровень при нагрузке глюкозой.
С/Т - увеличение риска СД2 в 2,5 раза
G/G - увеличение риска СД2 в 1,3 раза, фактор риска гестационного диабета, повышения уровня глюкозы, ухудшение секреции инсулина
С/Т - увеличение риска СД2 в 1,2 раза
С/Т - увеличивает риск ожирения в 1,3 раза
G/Т - увеличивает риск ожирения в 1,3 раза
G/A - увеличивает риск ожирения в 1,6 раз
С/G – увеличение риска развития СД2 типа в 1,3 раза
Согласно результатам проведенных исследований, на статистически значимой когорте пациентов были отобраны одиннадцать генов, а именно PPARG,TCF7L2, MC4R, ADIPOQ, KCNQ1,FTO, MTNR1B, CDKAL1, SLC30A8,HHEX, KCNJ11,выявлены определенные полиморфизмы этих генов и установлены наиболее ассоциированные с нарушениями метаболизма генотипы указанных полиморфизмов, где наличие у пациента хотя бы одного из следующих полиморфизмов:
1. PPARG - rs1801282
2. TCF7L2 - rs7903146, rs12255372, rs7901695
3. MC4R - rs2229616
4. ADIPOQ - rs1501299, rs182052, rs2241766
5. KCNQ1 - rs2237892
6. FTO - rs17817449, rs1121980, rs1421085
7. MTNR1B - rs10830963
8. CDKAL1 - rs7754840, rs7756992, rs9465871,
9. SLC30A8 - rs13266634
10. HHEX - rs5015480
11. KCNJ11- rs5219, rs5215
где наличие у пациента хотя бы одного из указанных полиморфизмов свидетельствует о возможной предрасположенности к развитию нарушений метаболизма.
Определение именно такого сочетания генотипов полиморфизмов указанных генов является диагностически значимым, так как охватывает достаточное количество генов, участвующих в функции бета-клеток поджелудочной железы, секреции инсулина, ассоциированных с индексом массы тела и ожирении, ассоциированных с повышенным уровнем глюкозы, развитием инсулинорезистентности, гестационного диабета , и СД 2-го типа.
Осуществление изобретения.
В основе предложенного изобретения лежит молекулярно-генетическое исследование образцов клеток, тканей или физиологических жидкостей от пациентов. В качестве неограничивающего примера приведено исследование образца периферической крови пациентов, в возрасте от 18 лет, на следующие группы мутаций в генах PPARG, TCF7L2, MC4R, ADIPOQ, KCNQ1, FTO, MTNR1B, CDKAL1, SLC30A8, HHEX, KCNJ11.
Процедура молекулярно-генетического исследования осуществляется следующим образом:
Для проведения генотипирования используется ДНК, выделенная из клеток крови человека. Для выделения используется, например, набор "ПРОБА-ГС-ГЕНЕТИКА" (ДНК-технология, Россия) или другой набор реагентов, позволяющий выделить ДНК из периферической крови с концентрацией выше 5 нг/мкл. Процедура выделения происходит по протоколу производителя.
В качестве реактивов для постановки полимеразной цепной реакции в реальном времени (ПЦР-РВ) используется, например, набор "5X ScreenMix-HS" (Евроген, Россия). В полимеразной цепной реакции используются, например, зонды типа TaqMan. Подбор олигонуклеотидов (праймеров и зондов) осуществлялся с помощью, например, ПО PrimerExpress v3 (Thermo, США). Синтез олигонуклеотидов производится, например, на приборе AppliedBiosistems 3900 (Thermo, США) по заказу в ООО"Люмипроб Рус"(Россия).
Для проведения ПЦР используется, например, амплификатор CFX96 c1000 Touch (BioRad) с детекцией продуктов амплификации в режиме реального времени.
Диагностика осуществляется по данным, полученным по результатам молекулярно-генетического анализа участков генов на наличие аллелей риска – патологических генотипов (Таблица 2).
Таблица 2.
CYP2C9
Ниже приведены примеры, демонстрирующие возможность достижения указанного технического результата, в которых показаны результаты исследований образцов от пациентов и подтверждение возможности реализации прогнозирования различий в функции бета-клеток поджелудочной железы, секреции инсулина, метаболизме глюкозы, которые были подтверждены дополнительными клинико-лабораторными исследованиями.
Примеры осуществления изобретения
ПРИМЕР 1: Пациент, 1974 г.р., пол женский, рост 165 см, вес 84 кг, ИМТ = 30,1.
Результаты анализа на генетические факторы риска к увеличению индекса массы тела, метаболическому синдрому и сахарному диабету 2-го типа, представлены в таблице 3.
Таблица 3
Таким образом, можно предположить, что возможно развитие нарушений метаболизма у данного пациента, т.к. выявлены полиморфизмы в гене белка, ассоциированного с регуляторной субъединицей-1 циклинзависимойкинназы типа 5 (CDKAL1), гене, ассоциированным с ожирением и увеличением жировой ткани (FTO), гене белка канала для ионов калия Kir6.2 (KCNJ11), гене рецептора мелатонина 1B (MTNR1B), гене транскрипционного фактора 7 (TCF7L2), в генотипах, ассоциированных с увеличением риска ожирения, развития СД2, инсулинорезистентности в 1,3-2,1 раза.
Выявленные изменения в генотипе были подтверждены данными лабораторных исследований (таблица 4).
Таблица 4.
Полученные данные свидетельствуют о том, что нарушены механизмы метаболизма и утилизации глюкозы, индекс инсулинорезистентности значительно превышает верхнюю границу нормы, значение глюкозы значительно выше нормы, значение гликированного гемоглобина стремиться к верхней границе нормы, т.е. лабораторные показатели свидетельствуют о гипергликемии, клинические показатели свидетельствуют о метаболическом синдроме.
ПРИМЕР 2: Пациент, 2010 г.р., пол мужской, ИМТ> 25.
Результаты анализа на генетические факторы риска к увеличению индекса массы тела, метаболическому синдрому и сахарному диабету 2-го типа (таблица 5).
Таблица 5.
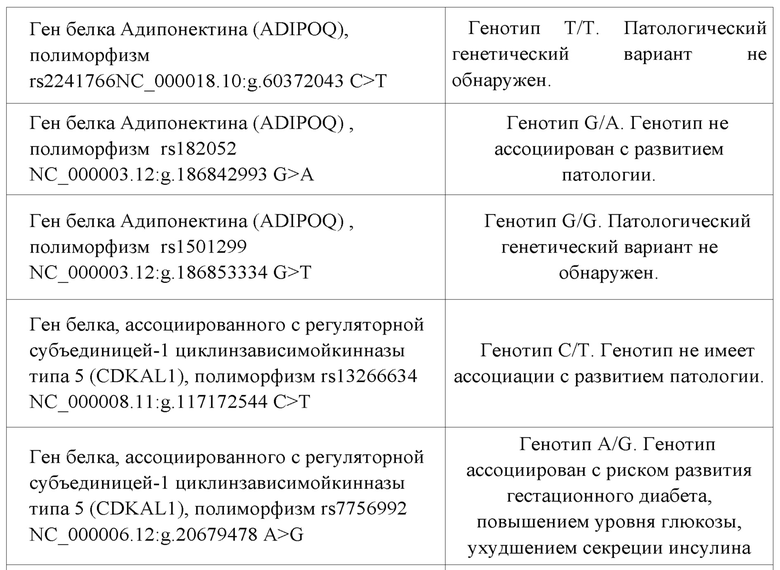
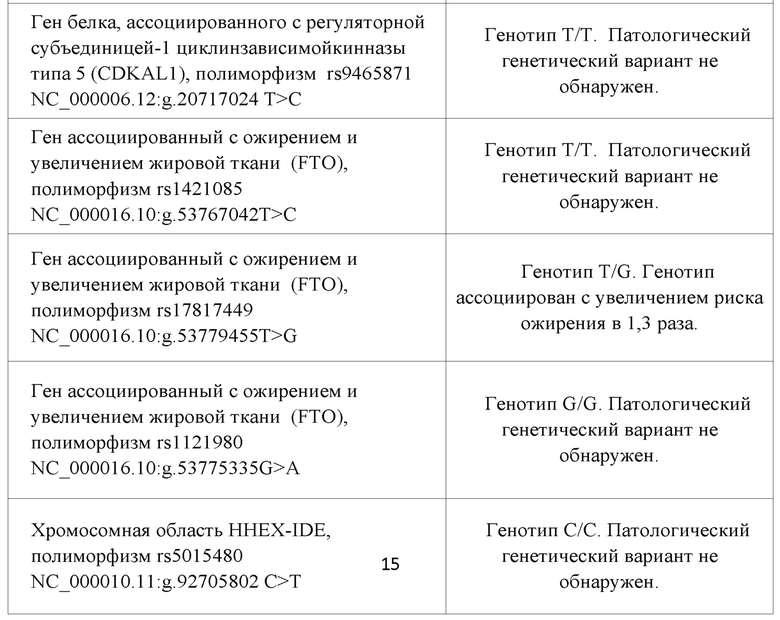
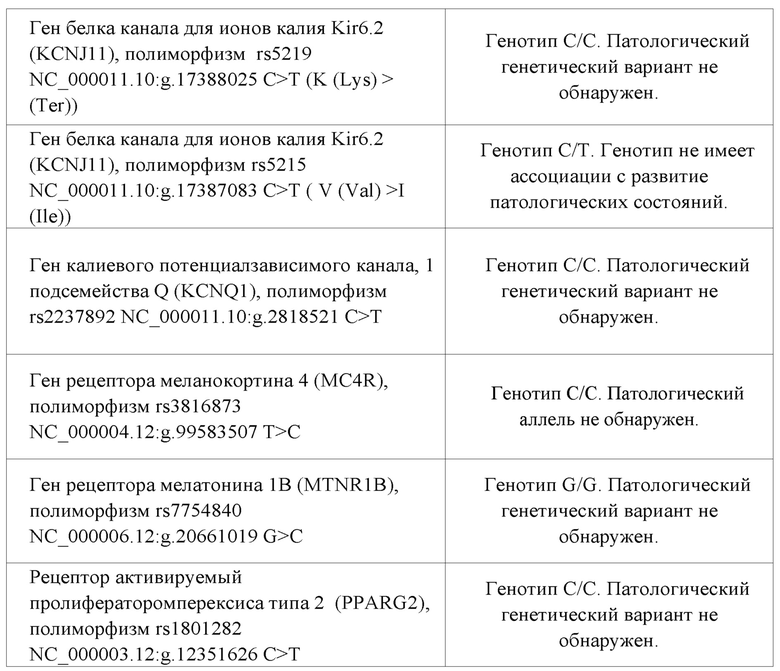
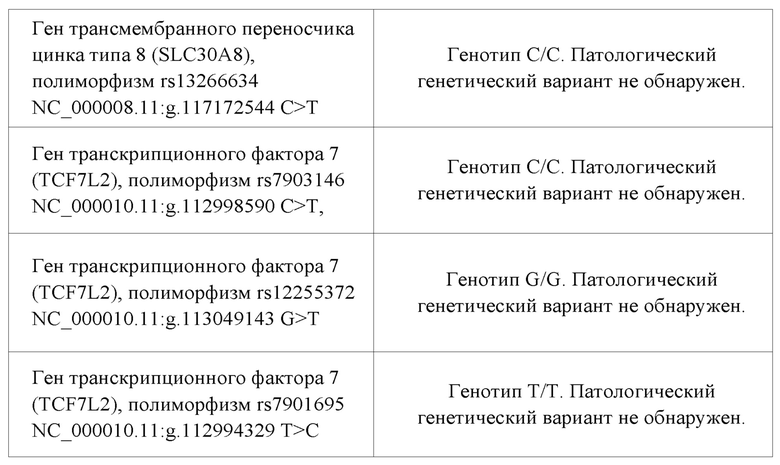
Таким образом, можно предположить, что возможно развитие нарушений метаболизма у данного пациента, т.к. выявлены полиморфизмы в гене белка, ассоциированного с регуляторной субъединицей-1 циклинзависимойкинназы типа 5 (CDKAL1), гене, ассоциированным с ожирением и увеличением жировой ткани (FTO), в генотипах, ассоциированных с риском повышения уровня глюкозы, ухудшения секреции инсулина,увеличением риска ожирения, в 1,3 раза.
Выявленные изменения в генотипе были подтверждены данными лабораторных исследований, представленными в таблице 6.
Таблица 6.
Полученные данные свидетельствуют о том, что нарушены механизмы метаболизма и утилизации глюкозы, инсулин и индекс инсулинорезистентности значительно превышает верхнюю границу нормы, но значение глюкозы в пределах нормы, т.е. лабораторные показатели свидетельствуют о гиперинсулинемии, клинические показатели свидетельствуют о метаболическом синдроме.
ПРИМЕР 3: Пациентка, 1951 г.р., пол женский, ИМТ=30. Результаты анализа на генетические факторы риска к увеличению индекса массы тела, метаболическому синдрому и сахарному диабету 2-го типа (таблица 7).
Таблица 7.
Таким образом, можно предположить, что возможно развитие нарушений метаболизма у данного пациента, т.к. выявлены полиморфизмы в гене рецептора активируемого пролифераторомперексиса типа 2 (PPARG2), гене трансмембранного переносчика цинка типа 8 (SLC30A8), в генотипах, ассоциированных с увеличением риска СД2 (в 2.5 раза), метаболического синдрома, инсулинорезистентности, повышение ИМТ.
Выявленные изменения в генотипе, подтверждены данными лабораторных исследований, представленными в таблице 8:
Таблица 8.
более 1.68 риск отсутствует,
менее 1.15 высокий риск
Полученные данные свидетельствуют о том, что нарушены механизмы метаболизма и утилизации глюкозы, индекс инсулинорезистентности значительно превышает верхнюю границу нормы, значение гликированного гемоглобина стремиться к верхней границе нормы, а также нарушен обмен липидов, и показатель холестерина ЛПВП, соответствует высокому риску развития атеросклероза, т.е. лабораторные показатели свидетельствуют о гипергликемии, клинические показатели свидетельствуют о метаболическом синдроме.
ПРИМЕР 4: Пациент, 1948 г.р., пол женский, ИМТ=29. Результаты анализа на генетические факторы риска к увеличению индекса массы тела, метаболическому синдрому и сахарному диабету 2-го типа (таблица 9):
Таблица 9.
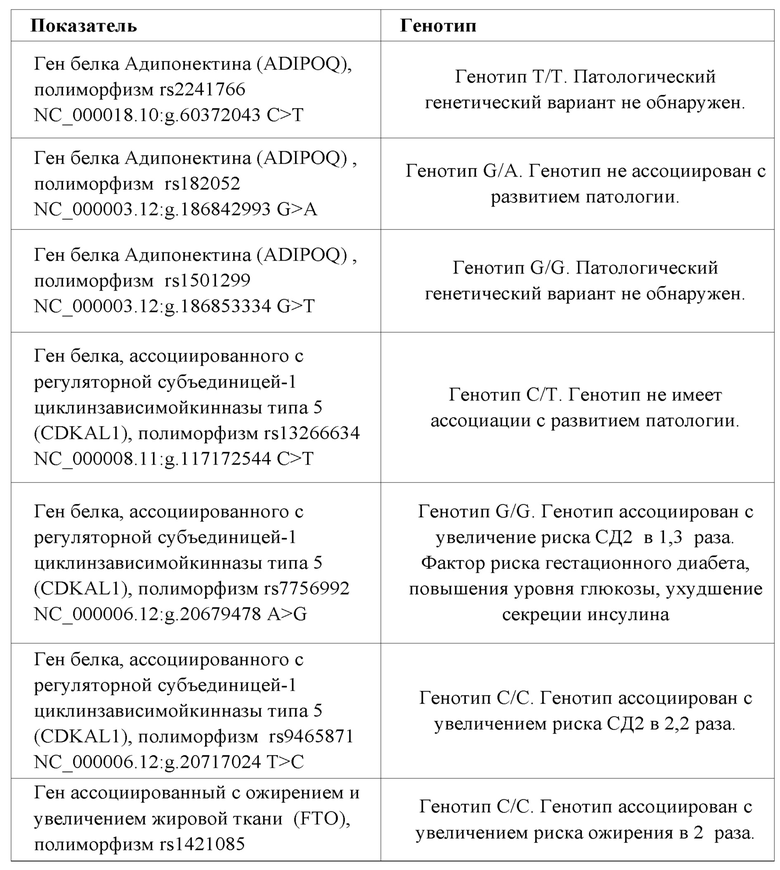
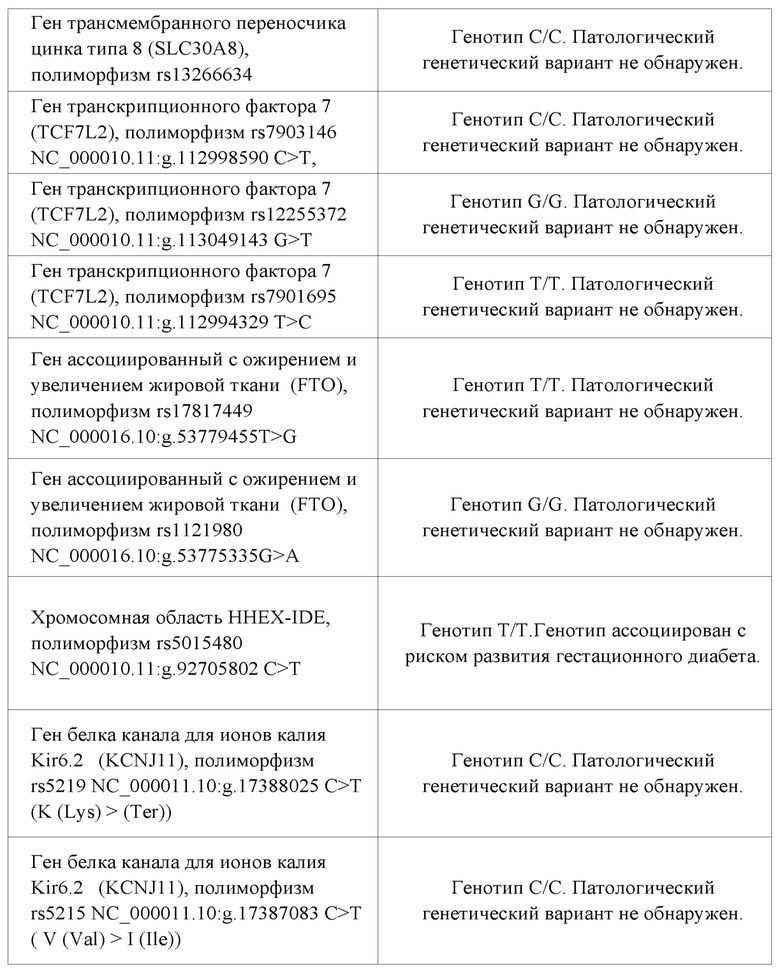

Таким образом, можно предположить, что возможно развитие нарушений метаболизма у данного пациента, т.к. выявлены полиморфизмы в генах белка, ассоциированного с регуляторной субъединицей-1 циклинзависимойкинназы типа 5 (CDKAL1), гене, ассоциированном с ожирением и увеличением жировой ткани (FTO), в хромосомной области HHEX-IDE, гене рецептора мелатонина 1B (MTNR1B), в генотипах, ассоциированных с увеличением риска СД2 (в 1.3-2.2 раза), и ожирения в 2 раза.
Выявленные изменения в генотипе, подтверждены данными лабораторных исследований, представленными в таблице 10:
Таблица 10.
Полученные данные свидетельствуют о том, что нарушены механизмы метаболизма и утилизации глюкозы, индекс инсулинорезистентности значительно превышает верхнюю границу нормы, значение глюкозы значительно выше нормы, значение гликированного гемоглобина стремиться к верхней границе нормы, т.е. лабораторные показатели свидетельствуют о гипергликемии, клинические показатели свидетельствуют о метаболическом синдроме.
ПРИМЕР 5: Пациент, 1992 г.р., пол мужской, ИМТ=25. Результаты анализа на генетические факторы риска к увеличению индекса массы тела, метаболическому синдрому и сахарному диабету 2-го типа (таблица 11):
Таблица 11.
Таким образом, можно предположить, что возможно развитие нарушений метаболизма у данного пациента, т.к. выявлены полиморфизмы в гене, ассоциированном с ожирением и увеличением жировой ткани (FTO) – в 1,6-2 раза, в гене транскрипционного фактора 7 (TCF7L2, в генотипах, ассоциированных с увеличением риска СД2 в 2,1 раза.
Выявленные изменения в генотипе, подтверждены данными лабораторных исследований, представленными в таблице 12:
Таблица 12.
3,34-4,12 пограничный уровень;
4,12-4,89 высокий риск; более 4.89 очень высокий риск
Полученные данные свидетельствуют о том, что нарушен обмен липидов, высокий индекс атерогенности свидетельствует о риске атеросклероза, но значение глюкозы находится в пределах нормы, т.е. лабораторные показатели свидетельствуют о гиперлипидемии, клинические показатели свидетельствуют о метаболическом синдроме.
РИМЕР 6: Пациент, 1993 г.р., пол женский, ИМТ=26. Результаты анализана генетические факторы риска к увеличению индекса массы тела, метаболическому синдрому и сахарному диабету 2-го типа (таблица 13):
Таблица 13.
Таким образом, можно предположить, что возможно развитие нарушений метаболизма у данного пациента, т.к. выявлены полиморфизмы в гене, ассоциированном с ожирением и увеличением жировой ткани (FTO) – в 1,6-1,7 раза, в гене белка канала для ионов калия Kir6.2 (KCNJ11), Рецептор активируемый пролифераторомперексиса типа 2 (PPARG2), Ген трансмембранного переносчика цинка типа 8 (SLC30A8), Ген транскрипционного фактора 7 (TCF7L2), в генотипах, ассоциированных с увеличением риска СД2 в 1,7-3,5 раза, развитием метаболического синдрома, инсулинорезистентности, повышением ИМТ.
Выявленные изменения в генотипе, подтверждены данными лабораторных исследований, представленными в таблице 14:
Таблица 14.
менее 5.2 желательный уровень,
более 6.2 высокий уровень
4,12-4,89 высокий риск; менее 4.89 очень высокий риск
Полученные данные свидетельствуют о том, что нарушен обмен липидов, но значение глюкозы находится в пределах нормы, т.е. лабораторные показатели свидетельствуют о гиперлипидемии, клинические показатели свидетельствуют о метаболическом синдроме.
ПРИМЕР 7: Пациент, 1964 г.р., пол женский, ИМТ=28. Результаты анализана генетические факторы риска к увеличению индекса массы тела, метаболическому синдрому и сахарному диабету 2-го типа (таблица 15):
Таблица 15.
Таким образом, можно предположить, что возможно развитие нарушений метаболизма у данного пациента, т.к. выявлены полиморфизмы в гене рецептора мелатонина 1B (MTNR1B), гене рецептора, активируемогопролифераторомперексиса типа 2 (PPARG2), гене трансмембранного переносчика цинка типа 8 (SLC30A8), гене транскрипционного фактора 7 (TCF7L2), в генотипах, ассоциированных с увеличением риска СД2 в 1,3-3,5 раза, развитием метаболического синдрома, инсулинорезистентности, повышением ИМТ.
Выявленные изменения в генотипе, подтверждены данными лабораторных исследований, представленными в таблице 16:
Таблица 16.
Полученные данные свидетельствуют о том, что нарушены механизмы метаболизма и утилизации глюкозы, индекс инсулинорезистентности значительно превышает верхнюю границу нормы, значение глюкозы значительно выше нормы, т.е. лабораторные показатели свидетельствуют о гипергликемии, клинические показатели свидетельствуют о метаболическом синдроме.
ПРИМЕР 8: Пациент, 1961 г.р., пол женский, ИМТ=23. Результаты анализана генетические факторы риска к увеличению индекса массы тела, метаболическому синдрому и сахарному диабету 2-го типа (таблица 17):
Таблица 17.
Таким образом, можно предположить, что возможно развитие нарушений метаболизма у данного пациента, т.к. выявлены полиморфизмы в гене белка, ассоциированного с регуляторной субъединицей-1 циклинзависимойкинназы типа 5 (CDKAL1), гене, ассоциированном с ожирением и увеличением жировой ткани (FTO), гене белка канала для ионов калия Kir6.2 (KCNJ11), в генотипах, ассоциированных с увеличением риска СД2 в 1,2-3,5 раза, ожирения в 1,3-1,5раза.
При этом, также были выявлены полиморфизмы в генах белка Адипонектина (ADIPOQ) и гене рецептора меланокортина 4 (MC4R), которые наоборот, ассоциированы с уменьшением риска развития СД2 в 2 раза,и метаболического синдрома.
Данные свидетельствуют о том, что применение предложенной панели позволило более точно определить генотип пациента, т.к. в расчет рисков были взяты гены, которые ассоциированы с прогнозом к уменьшению риска.
Выявленные изменения в генотипе, подтверждены данными лабораторных исследований, представленными в таблице 18:
Таблица 18.
3,34-4,12 пограничный уровень;
4,12-4,89 высокий риск; >4.89 очень высокий риск
<1.15 высокий риск
Полученные данные свидетельствуют о том, что механизмы метаболизма и утилизации глюкозы и липидного обмена осуществляются адекватно. Клинических признаков на момент исследования метаболического синдрома и/или СД не наблюдается. ИМТ находится в пределах нормы. В результатах анализа на генетические факторы обнаружены два генетических варианта, ассоциированных со снижением риска МС и СД, а также выявлен всего один генетический вариант, ассоциированный с повышенным риском гестационного диабета.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ ранней диагностики и прогнозирования диабетической фетопатии при гестационном сахарном диабете | 2024 |
|
RU2823332C1 |
| Панель для определения предрасположенности к развитию нарушений метаболизма стероидных гормонов и ее использование | 2024 |
|
RU2816705C1 |
| Панель для определения генетической предрасположенности к нарушению остеогенеза | 2024 |
|
RU2837396C1 |
| Способ определения предрасположенности к развитию ожирения у детей в условиях избыточной контаминации алюминием | 2019 |
|
RU2700565C1 |
| СПОСОБ ДИАГНОСТИКИ ПРЕДРАСПОЛОЖЕННОСТИ К МЕТАБОЛИЧЕСКОМУ СИНДРОМУ | 2009 |
|
RU2480154C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ МЕТАБОЛИТИЧЕСКОГО СИНДРОМА У ПАЦИЕНТА С АБДОМИНАЛЬНЫМ ОЖИРЕНИЕМ | 2010 |
|
RU2471193C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ САХАРНОГО ДИАБЕТА 2 ТИПА У НАСЕЛЕНИЯ БАШКОРТОСТАНА | 2018 |
|
RU2688208C1 |
| Способ прогнозирования риска развития избыточной массы тела и ожирения на основе анализа полиморфизмов генов циркадных ритмов. | 2024 |
|
RU2835187C1 |
| Способ прогнозирования риска развития гестационного сахарного диабета у беременных женщин | 2019 |
|
RU2716268C1 |
| Способ выявления предрасположенности к развитию метаболического синдрома в виде ожирения у школьников 7-10 лет | 2022 |
|
RU2779085C1 |
Изобретение относится к области биотехнологии и медицины. Описана панель, которая включает оригинальный набор средств для обнаружения в образце от пациента ряда полиморфизмов. Разработан способ определения предрасположенности к развитию нарушений метаболизма на основе использования уникального сочетания генотипов полиморфизмов в генах: функции бета-клеток поджелудочной железы (TCF7L, KCNJ11, PPARG), секреции инсулина (TCF7L, CDKAL), ассоциированных с индексом массы тела и ожирения (ADIPOQ, FTO, HHEX, MC4R, KCNQ1), повышенного уровня глюкозы (SLC30A8, TCF7L, CDKAL), инсулинорезистентности (TCF7L), гестационного диабета (MTNR1B, CDKAL1, HHEX), ассоциированных с СД 2-го типа (TCF7L, KCNJ11, PPARG, CDKAL, ADIPOQ, FTO, HHEX, SLC30A8, MC4R, KCNQ1, MTNR1B). Группа может быть использована для определения вероятности развития функциональных нарушений метаболизма и утилизации глюкозы, этиологически вызванных различными полиморфными вариантами в генах, отвечающих за синтез инсулина, восприимчивость клеток к инсулину, функцию бета-клеток поджелудочной железы, утилизацию глюкозы. Достигаемым техническим результатом настоящего изобретения является повышение точности определения предрасположенности к развитию нарушений обмена глюкозы, развития ожирения, метаболического синдрома и СД 2-го типа на основе уникального сочетания полиморфизмов, что позволяет одномоментно выявлять наиболее часто встречающиеся полиморфизмы, дает возможность провести более полный диагностический охват и не пропустить возможные изменения в генотипе. Разработанная панель также позволит превентивно скорректировать тип питания, образ жизни пациента, подобрать эффективную дозировку лекарственных препаратов. 2 н.п. ф-лы, 1 ил., 18 табл., 5 пр.
1. Панель для определения предрасположенности к увеличению индекса массы тела, метаболическому синдрому и сахарному диабету 2-го типа, включающая средства для обнаружения в образце от пациента следующих полиморфизмов:
1) PPARG - rs1801282;
2) TCF7L2 - rs7903146, rs12255372, rs7901695;
3) MC4R - rs2229616;
4) ADIPOQ - rs1501299, rs182052, rs2241766;
5) KCNQ1 - rs2237892;
6) FTO - rs17817449, rs1121980, rs1421085;
7) MTNR1B - rs10830963;
8) CDKAL1 - rs7754840, rs7756992, rs9465871;
9) SLC30A8 - rs13266634;
10) HHEX - rs5015480;
11) KCNJ11 - rs5219, rs5215.
2. Способ определения предрасположенности к увеличению индекса массы тела, метаболическому синдрому и сахарному диабету 2-го типа, включающий использование панели по п. 1, где наличие у пациента хотя бы одного из полиморфизмов, определяемых с помощью указанной панели, свидетельствует о предрасположенности к увеличению индекса массы тела, метаболическому синдрому и сахарному диабету 2-го типа.
| Способ прогнозирования риска развития сахарного диабета 2 типа у лиц с ожирением и/или предиабетом | 2022 |
|
RU2801174C1 |
| Способ определения предрасположенности к развитию ожирения у детей в условиях избыточной контаминации алюминием | 2019 |
|
RU2700565C1 |
| Способ формирования индивидуальных диетических рекомендаций на основе ДНК анализа | 2017 |
|
RU2691145C2 |
| WO 2011064352 A1, 03.06.2011 | |||
| А.Н | |||
| ДМИТРИЕВ, Метаболический синдром: маркеры индивидуальной предрасположенности, диагностика доклинической стадии, обоснование тактики ведения пациентов, Лекця для врачей, 2011, том 34, номер 2, стр.93-101. | |||
Авторы
Даты
2024-07-04—Публикация
2024-05-26—Подача