Область техники, к которой относится изобретение.
Изобретение относится к микробиологической промышленности и может быть использовано в фармацевтической и медицинской промышленности для получения ферментных средств бактериолитического спектра действия, используемых в медицине и ветеринарии для лечения заболеваний, вызванных патогенными стафилококками, а также в научных исследованиях (генетике, молекулярной биологии, биохимии) и в лабораторной практике.
Уровень техники.
Предложен штамм Staphylococcus epidermidis BVM-1987 - продуцент стафилолитического ферментного комплекса (СЛФК), способного лизировать клетки патогенных стафилококков Staphylococcus aureus, вызывающих широкий спектр заболеваний человека и животных, в том числе клетки штаммов патогенных стафилококков Staphylococcus aureus с множественной антибиотикоустойчивостью, и способного сохранять бактериолитическую активность в течение 5 лет при комнатной температуре.
Общепринятый метод лечения заболеваний, вызванных патогенными стафилококками Staphylococcus aureus, основан на применении антибиотиков. Однако у штаммов стафилококков Staphylococcus aureus быстро возникает высокая устойчивость к 10 и более антибиотикам.
Известен ферментный комплекс на основе бактериолитических ферментов, лизирующий клетки патогенных стафилококков - лизоцим яичного белка [1]. Лизоцим яичного белка используется в медицине для лечения наружных заболеваний, однако, имеет ограниченное применение из-за нестабильности своих свойств и дороговизны.
Известны штаммы микроорганизмов, при культивировании которых получают ферментные комплексы на основе бактериолитических ферментов, лизирующие клетки патогенных стафилококков: Streptomyces recifensis var. lyticus 2435 [2], Lysobacter sp. [3], Staphylococcus simulans biovar staphylolyticus [4].
Streptomyces recifensis var. lyticus 2435 - продуцент ферментного комплекса лизорецифин. Лизорецифин содержит в своем составе литические гликозидазы и эндопептидазы, а также ряд сопутствующих энзимов: нелитические протеазы, амилазы, ДНК-азы и др. Спектр литического антимикробного действия - стафилококки, некоторые виды псевдомонад, сальмонелл и микобактерий. Недостатками лизорецифина являются низкий выход целевого продукта и большая продолжительность процесса культивирования.
Lysobacter sp. - продуцент ферментного комплекса лизоамидаза. Лизоамидаза представляет собой ферментный комплекс, в состав которого входят не менее 5 белков-ферментов, обладающих бактериолитическими и протеолитическими свойствами, и липополисахарид. Спектр литического антимикробного действия лизоамидазы распространяется на стафилококки, стрептококки, коринебактерии, менингококки, гонококки. Однако содержание белка в препаратах лизоамидазы составляют 10-20%, причем на долю протеолитических и бактериолитических активных компонентов приходится около 25% от всего белка в препарате. Недостатком комплекса лизоамидазы является то, что способ выделения целевого продукта - осаждение ацетоном приводит к тому, что вместе с активным началом в состав препарата попадают балластные белки, что может быть причиной повышенной аллергенности продукта. Вторым недостатком лизоамидазы является узкий диапазон pH, в котором проявляет активность препарат, что требует добавления в упаковку с препаратом специального буфера.
Наиболее близким к предлагаемому объекту изобретения является Staphylococcus simulans biovar staphylolyticus. Staphylococcus simulans biovar staphylolyticus - продуцент ферментного комплекса лизостафин. Лизостафин содержит 3 фермента с глюкозамидазной (эндо-β-N-ацетилглюкозаминидазной), эндопептидазной (глициназной) и амидазной N-ацетилмурамил-L-аланинамидазной активностями. Оптимум бактериолитической активности проявляется при pH 7,0-7,5 и при температуре 45-50°C. Спектр действия лизостафина ограничен стафилококками. Анализ бактериолититической активности лизостафина показывает, что он проявлет литическую активность к коагулазоположительным антибиотикочувствительным и антибиотикоустойчивым штаммам St.aureus [5]. Большим недостатком лизостафина является необходимость его хранения при -20°C. Высокая стоимость и условия его хранения ограничивают его применение лабораторной практикой и научными исследованиями.
Сущность изобретения.
Задачей заявляемого изобретения является определение штамма микроорганизма, при культивировании которого получают ферментный комплекс, который обладает стафилолитической активностью, в том числе против клеток штаммов патогенных стафилококков Staphylococcus aureus с множественной антибиотикоустойчивостью, и который способен долговременно сохранять бактериолитическую активность при комнатной температуре.
Поставленная задача решается тем, что предложен неописанный ранее штамм Staphylococcus epidermidis BVM-1987, при культивировании которого получают стафилолитический ферментный комплекс, который обладает высокой стафилолитической активностью, в том числе против клеток штаммов патогенных стафилококков Staphylococcus aureus с множественной антибиотикоустойчивостью, который способен сохранять бактериолитическую активность в течение 5 лет при комнатной температуре.
Штамм Staphylococcus epidermidis BVM-1987 получен при смыве эпидермальных стафилококков с кожи здорового человека путем высевов на кровяном МПА (с 5% человеческой или бараньей крови).
Штамм депонирован в Федеральном государственном учреждении "Всероссийский государственный научно-исследовательский институт контроля, стандартизации и сертификации ветеринарных препаратов" (ВГНКИ ветпрепаратов) под номером BVM-1987-ДЕП.
Штамм Staphylococcus epidermidis BVM-1987 характеризуется следующими культурально-морфологическими и физиолого-биохимическими признаками.
Культурально-морфологические признаки.
Клетки Staphylococcus epidermidis BVM-1987 представляют собой правильной шаровидной формы клетки диаметром 0,5-1,0 мкм. Клетки группируются в скопления, напоминающие грозди винограда, окрашиваются по Граму положительно, неподвижны, не образуют спор или капсул. При росте на мясопептонном или молочно-солевом агаре клетки образуют колонии белого цвета, равномерно-выпуклые с гладкой матовой поверхностью, диаметром 0,5-1,0 мм. Колонии легко снимаются с поверхности агара бактериальной петлей. При росте на твердых средах, содержащих стафилококки, образуют крупные зоны лизиса вокруг своих колоний.
Физиолого-биохимические признаки.
Факультативный анаэроб. Температурный диапазон роста 29-41°C, но могут расти в диапазоне 7-46°C. Оптимум pH для роста 6,8-7,5, возможен рост при 4,2-9,3. Оптимальная температура для биосинтеза стафилолитического ферментного комплекса 32-37°C. Глюкоза, мальтоза, галактоза, сахароза, глицерин сбраживаются до образования кислоты без выделения газа. Ферментация маннита в анаэробных условиях не происходит. Рибозу, трегелозу не расщепляет. Нитраты восстанавливаются до нитритов. Образуют H2S, NH3.
Коагулаза отсутствует.
Лецитиназу, ДНК-азу, фибринолозин, гиалоуронидазу не образует [6]. α-токсин [7], α-гемолизин, β-гемолизин [8] не продуцирует.
Клетки устойчивы к лизоциму (100 мкг/мл), устойчивы к лизостафину (1 ед/мл).
Клетки Staphylococcus epidermidis BVM-1987 чувствительны к новобиоцину.
Литический спектр штамма:
Штамм Staphylococcus epidermidis BVM-1987 не патогенен для мышей при подкожном введении в дозе 109 клеток/мл.
СЛФК лизирует абсолютное большинство штаммов золотистого стафилококка (Staphylococcus aureus), в том числе и штаммы Staphylococcus aureus с множественной антибиотикоустойчивостью, и штаммы микрококка (Micrococcus lysodeikticus). Оптимум бактериолитической активности СЛФК наблюдается при pH 6,5-7,5 и при температуре 36-41°C.
По результатам определения острого токсического действия при однократном подкожном или внутрибрюшинном введении мышам и крысам СЛФК относится к V классу токсичности, то есть к практически нетоксичным веществам [9].
ЛД50 СЛФК, рассчитанное при бактериолитической активности 1 ЛЕ на 0,05 мг белка, составляет для мышей 1370±120 мг/кг, для крыс 1490±97 мг/кг. (За одну единицу бактериолитической активности ЛЕ принимают такое количество СЛФК, которое при температуре 37°C в течение 10 минут уменьшает в два раза оптическую плотность суспензии клеток Staphylococcus aureus Cowan 1 с концентрацией 5×108 клеток/мл в общем объеме реакционной смеси 6,0 мл при исходной оптической плотности 0,250 при длине волны 620 нм в кюветах с толщиной слоя 10 мм).
СЛФК не ингибируется сывороткой крови в физиологических концентрациях, это сохраняет активность препарата при использовании не только in vitro, но и in vivo.
Стафилолитический ферментный комплекс не обладает протеолитической активностью. Определение было проведено по методике Мура, Штейна [10]. В СЛФК не обнаружены активности щелочной и кислой фосфатаз, не обнаружена ДНК-азная активность.
СЛФК сухой легко растворим в воде, в изотоническом растворе хлорида натрия (0,85%), в новокаине, глицерине, диэтилсульфоксиде, в 1% растворе диоксидина без потери бактериолитической активности.
Оптимальные условия размножения:
Условия культивирования. Штамм Staphylococcus epidermidis BVM-1987 поддерживают пересевами на косяках мясопептонного агара (МПА) путем пересевов 1 раз в месяц.
Штамм Staphylococcus epidermidis BVM-1987 размножают на жидких питательных средах на основе пептона ферментативного или гидролизата рыбной муки с добавлением солей и ростовых добавок. При культивировании Staphylococcus epidermidis BVM-1987 для достижения оптимального выхода СЛФК используют те же питательные среды, что и для размножения клеток. В условиях ферментации при температуре 37°C в течение 22-26 часов накопление СЛФК в культуральной жидкости составляет 3-5 ЛЕ/мл среды. Для индукции биосинтеза литического комплекса в питательную среду добавляют автоклавированные клетки S.aureus Cowan 1 в количестве 0,5 г сухих клеток/литр питательной среды, что повышает выход СЛФК до 5-7 ЛЕ/мл.
Условия хранения:
Штамм сохраняют при температуре 20°C на косяках МПА, залитых стерильным вазелиновым маслом, пересевая 1 раз в 3-4 месяца. Штамм сохраняют также в лиофильно-высушенном состоянии при температуре 4°C, применяя в качестве стабилизатора для сушки смесь полиглюкина (0,15%) и сахарозы (0,1%).
Сведения, подтверждающие возможность использования данного изобретения.
Пример 1. Культивирование штамма Staphylococcus epidermidis BVM-1987 с целью получения стафилолитического ферментного комплекса
Готовят питательные среды следующего состава:
Среда А. Мясопептонный агар (МПА) готовят на основе мясопептонного бульона с содержанием аминного азота не менее 120 мг %; к 100 мл бульона добавляют 2 г агар-агара, далее агар расплавляют на водяной бане, разливают по 10 мл в стерильные пробирки, стерилизуют при 121°C в течение 30 минут. Пробирки оставляют застывать в горизонтальном положении для образования скошенной поверхности.
Вскрывают ампулу с лиофилизированной культурой Staphylococcus epidermidis BVM-1987. В ампулу вносят 3 мл 0,15 М стерильного раствора NaCl и перемешивают бактериологической петлей до получения однородной суспензии, полученной суспензией клеток засевают пробирки со скошенной плотной питательной средой (МПА) по 0,1 мл суспензии на пробирку. Выращивание культуры Staphylococcus epidermidis BVM-1987 проводят при температуре 37°C, в течение 20-24 часов, полученные клетки можно пассировать на МПА 3-4 раза. Чистоту культуры контролируют микроскопически с окраской по Граму.
Клетки Staphylococcus epidermidis BVM-1987, выращенные в пробирках на МПА, смывают с поверхности агара 8 мл 0,15 М стерильного раствора NaCl и высевают в качалочные колбы (колбы Эрленмейера) объемом 750 мл, содержащие 250 мл среды Б. Засев производят 2,0 мл суспензии клеток с концентрацией 109 клеток/мл по оптическому стандарту мутности ГИСК на 250 мл среды Б. Ферментацию осуществляют на качалке при температуре 37°C, 150 оборотов/минута в течение 20-22 часов. Значения pH по окончанию культивирования 7,8-8,2. По завершении ферментации клетки осаждают центрифугированием при 10000 g при 4°C в течение 20 минут. Прозрачная надосадочная жидкость исследуется на бактериолитическую активность.
Предварительно в стерильных условиях вскрывают ампулу с лиофильно высушенной маточной культурой Staphylococcus aureus Cowan 1. В ампулу вносят 3 мл 0,15 М стерильного раствора NaCl и перемешивают бактериологической петлей до получения однородной суспензии, полученной суспензией клеток засевают пробирки со скошенной плотной питательной средой (МПА) по 0,1 мл. Выращивают культуру Staphylococcus aureus Cowan 1 при 37°C. Чистоту контролируют по Граму и просмотром мазков под микроскопом. Клетки золотистого стафилококка осторожно снимают микробиологической петлей с поверхности скошенного агара и тщательно суспендируют на магнитной мешалке в забуференном физиологическом растворе (0,02 М KH2PO4 + 0,15 M NaCl, pH 7,5).
Далее определение бактериолитической активности рекомендовано проводить следующим образом. В две пробирки вместимостьью 15-20 мл вносят пипеткой по 5 мл суспензии клеток Staphylococcus aureus Cowan 1 с оптической плотностью 0,300 мл при 620 нм (концентрация 5×108 клеток/мл) и помещают в термостат при температуре 37°C на 10 минут. В пробирку 1 (испытуемая) прибавляют 100 мкл раствора СЛФК плюс 900 мл забуференного физиологического раствора (ЗФР) pH 7,5. В пробирку 2 (контроль) вносится 1,0 мл ЗФР pH 7,5. Пробирки выдерживают при 37°C в течение 10 минут, затем в обе пробирки добавляют по 100 мкл 4 М NaCl, встряхивают и определяют значения оптических плотностей содержимого пробирок на спектрофотометре при 620 нм в кювете с толщиной слоя 10 мм. В качестве раствора сравнения используют ЗФР, pH 7,5. Исследуемый таким образом фильтрат должен обладать бактериолитической активностью не менее 3,0±1,0 ЛЕ/мл.
Затем один литр посевного материала Staphylococcus epidermidis BVM-1987, полученный после культивирования в колбах на жидкой питательной среде Б, вносят в ферментер объемом 12 л, содержащий 10 л среды Б и далее выполняют ферментацию при температуре 37±0,3°C и при оборотах мешалки 350±50 об/мин, pH среды 7,2, расходе воздуха на аэрацию в первые 4 часа от начала ферментации 10 л/мин, следующие 4 часа 15 л/мин, далее - 20 л/мин. Продолжительность культивирования составляет 15±2 часа. Клетки отделяются центрифугированием, как описано выше. Бактериолитическая активность в данном примере должна быть не менее 3,0±1,0 ЛЕ/мл. Культуральную жидкость смешивают с ионообменным сорбентом типа «БИОКАРБ», доводят pH смеси до 5,5 с помощью концентрированной HCl и перемешивают в течение ночи при 4°C. Сорбент «БИОКАРБ» перед употреблением помещают на 2 часа в 0,5 1 н. раствор NaOH, далее промывают дистиллированной водой до pH 8,0, потом помещают в 0,5 1н HCl на 2 часа, затем отмывают дистиллированной водой до pH 4,0. После окончания перемешивания сорбенту дают осесть и через 15-20 минут декантируют.
Сорбент, сорбировавший стафилолитический ферментный комплекс, промывают 0,02 М раствором KH2PO4 и переносят в хроматографическую колонку. Элюцию проводят 0,7 М NaCl, pH 9,0, контролируя элюат на содержание белка спектрофотометрически при длине 280 нм. Элюцию заканчивают при показателе оптической плотности менее 0,08, далее элюат диализуют против фосфатного буфера (0,02 М KH2PO4 + 0,15 М NaCl, pH-7,5) и стерилизуют фильтрацией через мембраны с диаметром пор 0,22 мкм, контролируя поэтапно бактериолитическую активность. Полученный препарат стафилолитического ферментного комплекса представляет собой желтоватую слегка опалесцирующую жидкость без осадка и посторонних включений.
Пример 2. Определение состава стафилолитического ферментного комплекса
Содержание белка в полученном в примере 1 препарате стафилолитического ферментного комплекса от 0,2 до 1,0 мг/мл определяют по методу [11].
Состав белков в СЛФК определяют по данным электрофореза в полиакриламидном геле с додецилсульфатом натрия. Определение проводят по [12].
СЛФК, полученный в примере 1, представлен смесью трех белков (97-98% от общего количества белков) с молекулярными массами 18, 29, 42 кД.
Пример 3. Приготовление лиофильно высушенного стафилолитического ферментного комплекса
Препарат стафилолитического ферментного комплекса, полученный в примере 1, сублимационно высушивают.
Лиофильно высушенный препарат стафилолитического ферментного комплекса представляет собой порошок или пористую массу белого цвета, иногда с слабым желтоватым оттенком без запаха, гигроскопичен.
Пример 4 Определение бактериолитической активности стафилолитического ферментного комплекса
Определение бактериолитической активности рекомендовано проводить следующим образом. В две пробирки вместимостьью 15-20 мл вносят пипеткой по 5 мл суспензии клеток Staphylococcus aureus Cowan 1 с оптической плотностью 0,300 мл при 620 нм (концентрация 5×108 клеток/мл) и помещают в термостат при температуре 37°C на 10 минут. В пробирку 1 (испытуемая) прибавляют 100 мкл раствора СЛФК, полученного в примере 1, и 900 мл забуференного физиологического раствора (ЗФР), pH 7,5. В пробирку 2 (контроль) вносится 1,0 мл ЗФР pH 7,5. Пробирки выдерживают при 37°C в течение 10 минут, затем в обе пробирки добавляют по 100 мкл 4М NaCl, встряхивают и определяют значения оптических плотностей содержимого пробирок на спектрофотометре при 620 нм в кювете с толщиной слоя 10 мм. В качестве раствора сравнения используют ЗФР, pH 7,5. Исследуемый таким образом фильтрат должен обладать бактериолитической активностью не менее 3,0±1,0 ЛЕ/мл.
Пример 5. Определение бактериолитической активности лиофильно высушенного стафилолитического ферментного комплекса
Определение бактериолитической активности сухого препарата СЛФК выполняют следующим образом: готовят два раствора: 40 мг (точная навеска) препарата растворяют в 4,0 мл ЗФР, pH 7,5 и 40 мг рабочего стандартного образца (РСО) растворяют в 4,0 мл ЗФР.
(РСО может являться любая предыдущая серия препарата, активность которого выражена в бактериолитических единицах на 1 мг). Пробирки выдерживают при 37°C в течение 10 минут, затем в пробирки вносится по 0,1 мл 4 М раствора NaCl, пробирки встряхивают и определяют значения оптических плотностей содержимого пробирки при 620 нм в кювете с толщиной слоя 10 мм.
Для определения бактериолитической активности в три пробирки (вместимостью 15-20 мл) вносят пипеткой по 5,0 мл суспензии клеток Staphylococcus aureus Cowan 1, приготовленной, как описано в примере 1 с оптической плотностью 0,300 при длине волны 620 нм (концентрация 5×108 клеток/мл) и помещают в термостат при температуре 37°С на 5 минут. В пробирки 1 и 2 (испытуемые) микропипеткой прибавляют по 100 мкл раствора препарата СЛФК и рабочего стандартного образца (РСО) и 900 мкл ЗФР, рН-7.5, в пробирку 3 вносится 1000,0 мкл ЗФР, соответственно. Пробирки выдерживают при 37°C в течение 10 минут, затем в пробирки вносится по 0,1 мл 4 М раствора NaCl, пробирки встряхивают и определяют значения оптических плотностей содержимого пробирки при 620 нм в кювете с толщиной слоя 10 мм.
В качестве раствора сравнения используют забуференный физиологический раствор
Бактериолитическую активность препарата (ЛА) в единицах ЛЕ вычисляют по формуле:
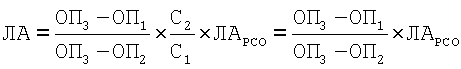
Здесь ОП1 ОП2, ОП3, - значения оптических плотностей растворов пробирок 1, 2, 3, соответственно.
С1, С2, - концентрации растворов препарата РСО, соответственно 1,0 и 1,0 мг/мл;
ЛАРСО - бактериолитическая активность РСО в ЛЕ.
Бактериолитическая активность 1 мг препарата должна быть не менее 0,8 ЛЕ.
Пример 6. Определение бактериостатической активности стафилолитического ферментного комплекса.
Препарат СЛФК, полученный в примере 3, растворяют в питательной среде, соответствующей ростовым потребностям соответствующих микроорганизмов для создания исходной концентрации бактериолитической активности СЛФК 40 ЛЕ/мл или 300 ЛЕ/мл. Из полученных растворов СЛФК готовят путем двухкратных серийных разведений в объеме 2 мл ряды убывающих концентраций препарата. Контролем служит пробирка с чистой питательной средой. После этого все пробирки (опытные и контрольные) засевают культурами микроорганизмов.
Бактериолитический эффект определяли по минимальной концентрации препарата СЛФК (ЛЕ/мл), при которой не наблюдали рост микроорганизмов.
В качестве тест-микроорганизмов использовали клинические полирезистентные штаммы Staphylococcus aureus, выделенные из больных.
Результаты исследования бактериостатической активности СЛФК в отношении клинических штаммов Staphylococcus aureus приведены в Таблице 1.
Тест-культуры стафилококков различных типов засевались на чашки МПА. На засеянные газоны накладывали бумажные диски, на которые наносилось 10 мкл препарата различной концентрации от 1,0 ЛЕ/мл до 0,031 ЛЕ/мл. Чашки переносились в термостат на 24 часа при 37°C, затем измеряли диаметр зоны лизиса вокруг бумажных дисков.
Результаты исследования бактериостатической активности СЛФК в отношении штаммов Staphylococcus aureus различных типов представлены в таблице 2.
Пример 7. Исследование бактериолитической активности СЛФК в отношении штаммов различных микроорганизмов.
Литическое действие препарата проверяли на живых клетках Staphylococcus, Streptococcus, Clostridium, Bacillus, Sarcina, Ervinia, Escherichia, Pseudomonas, Salmonella.
Определение активности СЛФК на клетках различных видов бактерий проводилось в тех же условиях, что и определение активности на стандартной культуре Staphylococcus aureus Cowan 1. На чашки с тест-культурами накладывались диски из фильтровальной бумаги, на которые наносили 10 мкл раствора СЛФК с концентрацией 0,5 ЛЕ/мл. Чашки оставляли в термостате на 24 часа при 37°C, в случае положительного результата вокруг диска образовывались зоны лизиса.
Результаты исследования бактериолитической активности СЛФК в отношении штаммов различных микроорганизмов представлены в таблице 3
Результаты показывают, что предлагаемый штамм, Staphylococcus epidermidis BVM-1987 продуцирует стафилолитический ферментный комплекс, способный лизировать абсолютное большинство патогенных штаммов золотистого стафилококка независимо от их устойчивости к широкому ряду антибиотиков.
Пример 8. Проверка сроков хранения СЛФК сухого при комнатной температуре.
СЛФК сухой при хранении при комнатной температуре не снижает бактериолитической активности в течение 5 лет. При исследовании активности контрольных образцов, заложенных на хранение при комнатной температуре, активность образцов определялась каждые 6 месяцев. Нами определено, что активность не менялась, что выгодно отличает его от лизостафина, который сохраняет свою активность при хранении при -20°C в течение 2 лет.
Библиографические данные
1. Бухарин О.В., Васильев Н.В. Лизоцим и его роль в биологии и медицине. Томск, 1974.
2. Жерносекова И.В., Килочек. Влияние глюкозы на биосинтез экстрацеллюлярных форм Streptomyces recifensis var. lyticus 2435 и его мутантами. Miкробioл. Ж. 62, 2 19-26 (2000).
3. Кулаев И.С. Бактериолитические ферменты микробного происхождения в биологии и медицине. Сб. "Бактериолитический препарат лизоамидаза. Физиологические, биохимические и клинические аспекты" 1989, Пущино, стр.3-9.
4. Schindler C.A., Schuhardt V.T. Lysostaphin: a new bacteriolytic agent for the Staphylococcus. Proc. Nation Acad. Sci. N.Y. 51, 3, 415-421 (1964).
5. Xin-yi Yang et al. "In vitro activity of recombinant lysostphin against Staphylococcus aureus isolated from hospitals in Beijing China" J. Med. Microbiol. 56, 71-76 (2007).
6. Приказ МЗ СССР №535 от 22.04.1985 "Об унификации микробиологических (бактериологических) методов исследования, применяемых в клинико-диагностическизх лабораториях лечебно-профилактических учреждений".
7. Указания по диагностике, лечению и профилактике в Вооруженных Силах РФ. "Дизентерии и другие острые кишечные диарейные инфекции" МО РФ ГВМУ.
8. Приложение №3 к приказу МЗ СССР №720 от 31.07.78. "Инструкция по бактериологическому обследованию на выявление носителей патогенного стафилококка и проведение санации".
9. Browder H.P., Zygmunt W.A., Young J.R., Tawormina P.A. Lysostaphin: enzymatic mode of action Biochem. Biophys. Res. Commun. 19,383-389 (1965).
10. Кочетов Г.А. Практическое руководство по энзимологии. М., 1989.
11. Lowry J.W. J. Biol. Chem. 191, 265-275 (1951).
12. Laemmli U.K. Nature, 227, p.680-685 (1970).
| название | год | авторы | номер документа |
|---|---|---|---|
| Фармацевтическая комбинированная композиция для местного и наружного применения на основе бактериолитического и протеолитического комплекса ферментов | 2016 |
|
RU2655808C2 |
| Фармацевтическая комбинированная композиция для местного и наружного применения на основе диоксидина | 2016 |
|
RU2667974C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИЗОСТАФИНА | 1994 |
|
RU2143489C1 |
| ШТАММ STAPHYLOCOCCUS HOMINIS KLP-1 - ПРОДУЦЕНТ НИЗКОМОЛЕКУЛЯРНЫХ ПЕПТИДНЫХ СОЕДИНЕНИЙ, ИНГИБИРУЮЩИХ РАЗВИТИЕ ГРАМПОЛОЖИТЕЛЬНЫХ БАКТЕРИЙ | 2010 |
|
RU2428470C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЧУВСТВИТЕЛЬНОСТИ БАКТЕРИЙ К ДЕЙСТВИЮ БАКТЕРИОЛИТИЧЕСКИХ ФЕРМЕНТОВ - ЛИЗОЦИМА ИЛИ ЛИЗОСТАФИНА | 2008 |
|
RU2410436C2 |
| СПОСОБ ПРЕОДОЛЕНИЯ УСТОЙЧИВОСТИ К ГЕНТАМИЦИНУ У МЕТИЦИЛЛИНОРЕЗИСТЕНТНЫХ ШТАММОВ СТАФИЛОКОККА | 2013 |
|
RU2553601C2 |
| ПРОТИВОМИКРОБНОЕ СРЕДСТВО | 2014 |
|
RU2556509C2 |
| Фармацевтическая комбинированная композиция для лечения гнойных ран на основе фторхинолонов (варианты) | 2016 |
|
RU2682171C2 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pDUALREP2 И ШТАММ, ТРАНСФОРМИРОВАННЫЙ ЕЮ ДЛЯ ВЫЯВЛЕНИЯ ВЕЩЕСТВ И СМЕСЕЙ, ИНГИБИРУЮЩИХ БИОСИНТЕЗ БЕЛКА И/ИЛИ ВЫЗЫВАЮЩИХ SOS-ОТВЕТ У БАКТЕРИЙ | 2016 |
|
RU2620074C1 |
| ШТАММ STAPHYLOCOCCUS WARNERI IEGM KL-1 - ПРОДУЦЕНТ НИЗКОМОЛЕКУЛЯРНОГО ПЕПТИДНОГО СОЕДИНЕНИЯ, ИНГИБИРУЮЩЕГО РОСТ КЛЕТОК ГРАМПОЗИТИВНЫХ БАКТЕРИЙ | 2001 |
|
RU2200195C2 |
Изобретение относится к области биотехнологии. Штамм бактерий Staphylococcus epidermidis депонирован в коллекции Всероссийского государственного научно-исследовательского института контроля, стандартизации и сертификации ветеринарных препаратов под регистрационным номером BVM-1987. Штамм является продуцентом стафилолитического ферментного комплекса, лизирующего антибиотикоустойчивые патогенные штаммы стафилококков и обладающего устойчивостью при хранении. Сухой стафилолитический ферментный комплекс при хранении при комнатной температуре сохраняет бактериолитическую активность в течение пяти лет. 3 табл.
Штамм бактерий Staphylococcus epidermidis - продуцент стафилолитического ферментного комплекса, лизирующего антибиотикоустойчивые патогенные штаммы стафилококков и обладающего устойчивостью при хранении, депонированный в коллекции Всероссийского государственного научно-исследовательского института контроля, стандартизации и сертификации ветеринарных препаратов под регистрационным номером BVM-1987.
| XIN-YI YANG et al., In vitro activity of recombinant lysostphin against Staphylococcus aureus isolated from hospitals in Beijing China, J | |||
| Med | |||
| Microbiol., 2007, 56, 71-76 | |||
| DE 3523478 A1, 08.01.1987 | |||
| KR 20030074926 A, 22.09.2003 | |||
| US 4197290 A, 08.04.1980. |
Авторы
Даты
2010-11-10—Публикация
2008-12-30—Подача