Изобретение относится к химии металлокомплексов тетрапиррольных соединений, в частности к иттербиевым комплексам природных порфиринов, которые могут быть использованы при решении задач люминесцентной диагностики злокачественных новообразований методом волоконно-лазерной спектрофлуориметрии.
Данный подход основан на способности соединений порфиринового ряда избирательно накапливаться в злокачественных тканях и люминесцировать при освещении светом определенной длины волны. При этом комплексы порфиринов с иттербием люминесцируют в ближней ИК-области (900-1050 нм), где практически отсутствует фоновая автолюминесценция биотканей. К тому же введение тяжелого металла в порфириновый макроцикл резко уменьшает выход триплетов и, следовательно, фототоксичность металлопорфиринов [Таубер А.Ю., Нижник А.Н., Миронов А.Ф., Гайдук М.И., Григорьянц В.В. / Фотофизическая активность порфириновых сенсибилизаторов в водных растворах // Биофизика. - 1989. - Т.34. - №3. - С.364-367].
В связи с тем, что в настоящее время смертность от злокачественных новообразований стоит на втором месте после сердечно-сосудистых заболеваний, очень остро стоит вопрос о ранней люминесцентной диагностике рака. Предлагаемое изобретение направлено на выявление наиболее распространенных визуально и эндоскопически доступных нозологических форм злокачественных новообразований.
В последние годы разрабатываются химические синтезы новых иттербиевых комплексов на основе природных порфиринов с аминокислотами [Wiglusz R., Legendziewicz J., Graczyk A., Radzki S., Gawryszewska P., Sokolnicki J. / Spectroscopic properties ofporphyrins and effect of lanthanide ions on their luminescence efficiency // J.Alloys Compounds. - 2004. - V.380. - P.396-404], а также синтетических порфиринов, содержащих в мезоположениях макроцикла изомерные радикалы пиридина, хинолина и хиноксалина, люминесцентные характеристики которых выше, чем в случае фенильных и нафтильных заместителей [Коровин Ю.В., Кузьмин В.Е., Русакова Н.В., Жилина З.И., Водзинский С. В., Юданова И.В. / Влияние природы мезозаместителей в порфиринах на излучательную способность ионов иттербия в комплексах с порфиринами // Ж. неорг. химии. - 2003. - Т.48. - №3. - С.489-493], а также асимметричные порфирины [Zhuravlyov S., Rusakova N., Korovin Yu. / 4f-luminescence of ytterbium ions in the complexes with asymmetric porphyrins // J. Alloys Compounds. - 2008. - V.45L - P.334-337] и димерные порфирины [Korovin Yu.V., Rusakova N.V., Zhilina Z.I., Ishkov Yu.V., Vodzinsky S.V., Dotsenko V.P. /Luminescence of ytterbium in binuclear bis(porphyrin)complexes // Mendeleev Commun. - 2002. - P.151-152].
При диагностике злокачественных новообразований важной задачей является исследование спектрально-люминесцентных характеристик Yb-порфиринов. Наиболее важными характеристиками являются времена жизни металлокомплексов и их квантовый выход флуоресценции. В работе [Rusakova N.V., Korovin Yu.V., Zhilina Z.I., Vodzinskii S.V., Ishkov Yu.V. / Influence of the nature of meso-substituents and extra-ligands on the luminescence of ytterbium in complexes with porphyrins // J. Applied Spectroscopy. - 2004. - V.71 - No.4. - P.506-511] изучено большое количество иттербиевых комплексов порфиринов с алкильными заместителями в мезоположениях макроцикла, а также их комбинации с изомерными пиридильными остатками. Показано, что наибольшие времена жизни (12.1 и 5.6 мкс) и квантовый выход флуоресценции (10.1 и 5.6×10-3) имеют синтетические порфирины, содержащие четыре пиридильных остатка в мезо-положениях и три пиридильных остатка и один алкильный н-C9H19, а в качестве экстралиганда наиболее оптимален остаток β-дикетона (ацетилацетон).
В случае лантаноидных комплексов порфиринов большое влияние на их спектральные свойства оказывает природа экстралигандов: монодентатные (хлориды, бромиды), бидентатные (ацетилацетон, бензоилацетон) и теноилтрифторацетат анионы.
Для диагностики рака возможно использование радиоактивного изотопа 169Yb как с природными, так и с синтетическими порфиринами [Schomaecker К., Gaidouk M.I., Rumyantseva V.D., Fischer Т., Loehr H., Salditt S. et al. / Synthese tumoraffiner Yb-169 und Y-90-Porphyrin-Komplexe und tiereexperimentelle Untersuchung verschiedener Yb-169-Pophyrins // Nuklearmedizin. - 1999. - Bd.38. - S.285-291]. Однако одним из недостатков является плохая растворимость некоторых порфиринов в воде при проведении эксперимента на животных. В этом случае возможно применение липосомальных форм, а также растворов в диметилсульфоксиде или в кремофоре. В работе [Zsvirko M., Korovin Yu., Rusakova N. / Ytterbium-porphyrins as a new class of the luminescent labels // J.Physics: Conference Series. - 2007. - V.79. 012025.] предлагаются комплексы иттербия с асимметричными порфиринами на основе производных тетрафенилпорфирина и гидрофобного мезо-(монофенил-п-оксипропил)трифенилпорфирина (ОТП) в виде водно-лецитиновой эмульсии. 4f-люминесценция Yb-комплекса проявляется в ближней ИК-области спектра (λмакс=980 нм). Также был приготовлен конъюгат Yb-комплекса с бычьим сывороточным альбумином (БСА). Время жизни Yb-комплекса составило 7.6-8.4 мкс, а квантовый выход 4f-люминесценции φ=4.2×10-3. Для ОТП была изучена токсичность как свободного основания (LD50=250 мг/кг), так и иттербиевого комплекса (LD50=160 мг/ кг). У металлокомплекса не обнаружена фототоксичность. Комплекс изучали на 36 мышах линии BALB/c с индуцированной метилхолантреном опухолью в дозе 75 мг/ кг веса. Недостатком этого метода является использование водно-лецитиновой дисперсии для солюбилизации Yb-комплекса порфирина, т.к. при применении липосом большая часть вещества задерживается в печени и селезенке.
Наиболее близким техническим решением, выбранным авторами за прототип, является патент РФ [Румянцева В.Д., Миронов А.Ф., Сапронова Е.В. и др. / Способ изучения малигнизации тканей у экспериментальных животных // Патент РФ №1621720, кл. G01N 33/52, приор, от 29.04.88 г.], где в качестве одного из контрастных веществ использована водно-липосомальная эмульсия Yb(асас)-2,4-диметоксигематопорфирина IX динатровой соли. Хотя в эксперименте на животных был достигнут высокий контраст между злокачественной опухолью и соседней здоровой мышцей, здесь имеются следующие недостатки: высокая концентрация вводимого металлокомплекса (50 мг/ кг), а также недостаточная растворимость в воде динатровой соли гематопорфирина IX, требующая применения липосомальных форм для солюбилизации препарата. Это существенно усложняет ввод препарата в организм, затрудняет количественное определение встроенного в липосомы соединения и требует его увеличенных доз, поскольку большая его часть при использовании липосомальных форм аккумулируется в печени, почках и селезенке.
Техническим результатом настоящего изобретения является создание нового малотоксичного соединения, используемого в ранней люминесцентной, а также радиологической диагностике злокачественных новообразований, которое имеет сравнительно высокий уровень времени жизни и интенсивности люминесценции в ближней ИК-области спектра, хорошую растворимость в воде, а также позволяет резко снизить дозу вводимого препарата, что обеспечивает существенное снижение цены на диагностические процедуры.
Для достижения указанного технического решения предполагается заменить динатровую соль 2,4-диметоксигематопорфирина IX на его более водорастворимую дикалиевую соль. Для этого на первом этапе получают Yb-комплекс 2,4-диметоксигематопорфирина IX по методу [Wong C.-P., Venteicher R.F., Horrocks W.DeW.Jr. / Lanthanide porphyrin complexes a potential new class of nuclear magnetic resonance dipolar probe // J.Am.Chem.Soc. - 1974. - V.96. - No 22. - P.7149-7150] кипячением свободного основания порфирина с 2÷3-х кратным избытком Yb(асас)3 в 1,2,4-трихлорбензоле в атмосфере аргона. На втором этапе дикислоту порфирина переводят в дикалиевую соль и подвергают очистке на акрилексе Р-2.
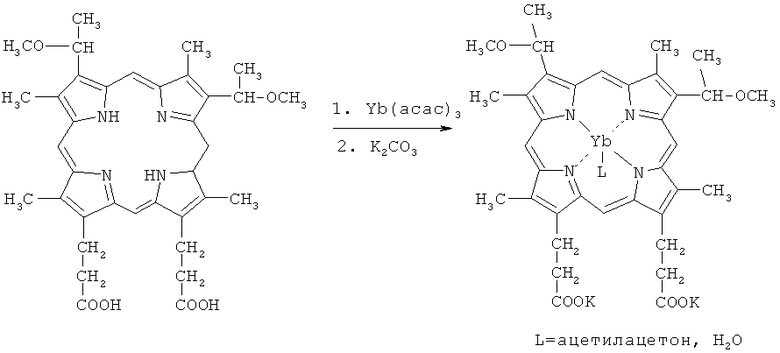
Реализация данного изобретения подтверждается следующим примером.
Пример 1. 100 мг (0.16 ммоль) 2,4-диметоксигематопорфирина IX растворяют в 20 мл 1,2,4-трихлорбензола, добавляют 150 мг (0.32 ммоль) ацетилацетоната иттербия и кипятят в токе аргона в течение 2.5 час. В электронном спектре поглощения исчезают пики свободного основания порфирина и появляются пики, характерные для металлокомплекса порфирина. Реакционную массу охлаждают, выливают на столбик оксида алюминия (5×3 см), вымывают 1,2,4-трихлобензол гептаном и затем ацетоном. Оставшийся наверху малиновый слой иттербиевого комплекса порфирина переносят в химический стакан, заливают 200 мл смеси горячего (50-60°С) изопропанола и 1% водного поташа (1:1). Фильтруют от оксида алюминия, малиновый раствор разбавляют водой, доводят рН до 7 действием разбавленной уксусной кислоты и трижды экстрагируют свежеперегнанным хлороформом. Хлороформный экстракт промывают водой три раза, сушат над безводным сульфатом натрия, фильтруют и упаривают в вакууме. Выход 68.4 мг (53.7%).
Для того чтобы перевести дикислоту порфирина в дикалиевую соль, вещество растворяют при перемешивании в минимальном количестве 5% водного поташа. Раствор наносят на колонку с акрилексом Р-2, в качестве элюента используют дистиллированную воду. В первых фракциях содержится исходное свободное основание порфирина, а далее движется малиновая зона иттербиевого комплекса. Водный раствор концентрируют и диализуют против дистиллированной воды в течение суток, затем раствор фильтруют и упаривают досуха. Получают 53 мг темно-фиолетового порошка, хорошо растворимого в воде. Электронный спектр в воде, λmax (ε×10-3), нм: 398 (196.0), 532 (9.15); 568.2 (10.6). Данные ВЭЖХ: время удерживания 7.95 мин. (Колонка Nova-Pack С 18, 3.9×150 мм). Элюент 0.1 М ацетат аммония в 70% метаноле, V 1 мл/мин, детектировали при 400 нм). ИК-спектр в KBr, ν, см-1: 3424 (ОН). Масс-спектр, m/z: 869.636 (30%), 870.638 (69%), 871.643 (100%), 872.660 (89%), 873.661 (49%). Рассчитано для С36Н38 N4O6K2 173Yb м.м. 873.96.
Были изучены спектры люминесценции иттербиевого комплекса дикалиевой соли 2,4-диметоксигематопорфирина IX в 20%-ном растворе диметилсульфоксида и по кинетике затухания определены времена жизни нового вещества и проведено сравнение их с веществом, описанным в прототипе.
Спектр интенсивности люминесценции заявляемого соединения приведен на чертеже. Иттербиевый комплекс порфирина имеет характерную люминесценцию при 975 нм, обусловленную переходами 2F5/2→2F7/2 4f электронов иона Yb3+ [Gaiduk M., Grigoryants V., Mironov A., Rumyantseva V./ Spectro-luminescent characteristics and kinetics of Yb3+ complexes of porphyrins// Proc. Estonian Acad. Sci. Phys. Math. - 1991 - V.40. - N3. - P.198-204]. Приведенный спектр по характеру интенсивности люминесценции близок к прототипу.
Время жизни иттербиевого комплекса дикалиевой соли 2,4-диметоксигематопорфирина IX в 20%-ном растворе диметилсульфоксида составляет около 10 мксек, что сопоставимо с временами жизни ИКП, выбранного в качестве прототипа (8-11 мксек для Yb-2,4-диметоксигематопорфирина IX динатровой соли).
Эффективность данного соединения как флуоресцентной метки подтверждается испытаниями на животных. Экспериментальным животным (мыши линии С57В 1/6) с химически индуцированной метилхолантреном саркомы вводят иттербиевый комплекс дикалиевой соли 2,4-диметоксигематопорфирина IX в хвостовую вену в дозе 0.5-2.5 мг/кг веса. Через 48 часов облучают лазером малигнизированные и нормальные ткани, проводят измерение сигнала люминесценции в области 975 нм, а затем рассчитывают коэффициент контрастности по отношению индекса люминесценции малигнизированных и нормальных тканей. Максимальный коэффициент контраста Ys составляет 51 через 48 часов после введения препарата.
Преимущество предлагаемого иттербиевого комплекса дикалиевой соли 2,4-диметоксигематопорфирина IX по сравнению с соединением, заявленным в прототипе, заключается в резком снижении дозы вводимого препарата, что позволит существенно снизить цены на диагностические процедуры, значительно упрощает ввод препарата в организм при сохранении высоких значений коэффициента контраста (табл.).
Проведены исследования токсичности дикалиевой соли Yb-комплекса 2,4-диметоксигематопорфирина IX. Поставлены эксперименты на 46 мышах Ваlb/С по определению тест-доз и поиску предельно переносимой дозы препарата. Использовали дозы 150 мг/кг веса, 250 мг/кг и 400 мг/кг веса животного. Было найдено, что LD100 соответствует доза 400 мг/кг, LD50 - 160-170 мг/кг, LD10 - доза составляет 130 мг/кг, а максимально переносимая доза (МПД) - 125 мг/кг. Приведенные результаты свидетельствуют о низкой токсичности заявляемого препарата.
На чертеже приведен спектр люминесценции иттербиевого комплекса дикалиевой соли 2,4-диметоксигематопорфирина IX в 20%-ном растворе диметилсульфоксида.
| название | год | авторы | номер документа |
|---|---|---|---|
| НАНОКОМПОЗИЦИЯ ДЛЯ ЛЮМИНЕСЦЕНТНОЙ ДИАГНОСТИКИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 2014 |
|
RU2578976C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЮМИНЕСЦЕНТНОЙ ДИАГНОСТИКИ ПАТОЛОГИЧЕСКИХ ИЗМЕНЕНИЙ КОЖИ И СЛИЗИСТЫХ ОБОЛОЧЕК | 2016 |
|
RU2617045C1 |
| ИТТЕРБИЕВЫЕ КОМПЛЕКСЫ ТЕТРАПИРАЗОЛИЛПОРФИРИНОВ КАК ФЛУОРЕСЦЕНТНЫЕ МЕТКИ ДЛЯ ДИАГНОСТИКИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2008 |
|
RU2372099C1 |
| Нанокомпозиты для магнитолюминесцентной тераностики новообразований | 2021 |
|
RU2766513C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИКАЛИЕВОЙ СОЛИ ИТТЕРБИЕВОГО КОМПЛЕКСА 2,4-ДИ(α-МЕТОКСИЭТИЛ)ДЕЙТЕРОПОРФИРИНА IX АЦЕТИЛАЦЕТОНАТА | 2019 |
|
RU2697418C1 |
| КОМПОЗИТНЫЕ НАНОЧАСТИЦЫ ДЛЯ ФОТОДИНАМИЧЕСКОЙ ДИАГНОСТИКИ | 2011 |
|
RU2463074C1 |
| СПОСОБ ПОЛУЧЕНИЯ БОРИРОВАННЫХ ПОРФИРИНОВ | 2013 |
|
RU2551539C2 |
| УСТРОЙСТВО ДЛЯ ЛЮМИНЕСЦЕНТНОЙ ДИАГНОСТИКИ НОВООБРАЗОВАНИЙ | 2012 |
|
RU2483678C1 |
| СПОСОБ ИССЛЕДОВАНИЯ МАЛИГНИЗАЦИИ ТКАНЕЙ У ЭКСПЕРИМЕНТАЛЬНЫХ ЖИВОТНЫХ | 1988 |
|
SU1621720A1 |
| ИТТЕРБИЕВЫЕ КОМПЛЕКСЫ ПОРФИРИНОВ В КАЧЕСТВЕ ЛЮМИНЕСЦЕНТНЫХ ВЕЩЕСТВ ДЛЯ ДИАГНОСТИКИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 1985 |
|
SU1340087A1 |

Изобретение относится к иттербиевому комплексу дикалиевой соли 2,4-диметоксигематопорфирина IX формулы:
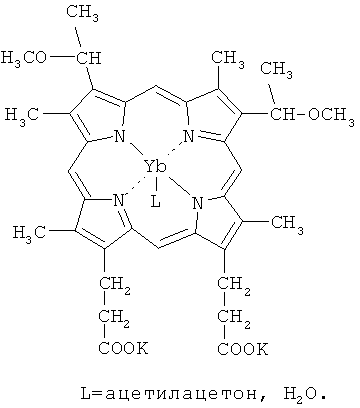
Технический результат заключается в получении малотоксичного соединения, используемого как флуоресцентная метка для ранней диагностики рака, имеющего сравнительно высокий уровень времени жизни и интенсивности люминесценции в ближней ИК-области спектра, а также хорошую растворимость в воде. 1 ил., 1 табл.
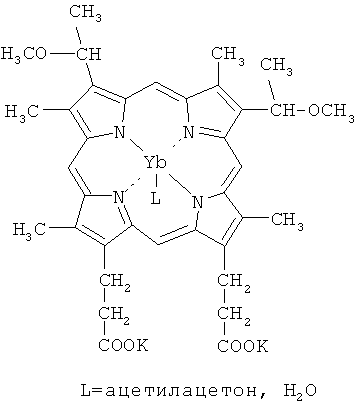
Иттербиевый комплекс дикалиевой соли 2,4-диметоксигематопорфирина IX как флуоресцентная метка для ранней диагностики рака
| СПОСОБ ИССЛЕДОВАНИЯ МАЛИГНИЗАЦИИ ТКАНЕЙ У ЭКСПЕРИМЕНТАЛЬНЫХ ЖИВОТНЫХ | 1988 |
|
SU1621720A1 |
| ИТТЕРБИЕВЫЕ КОМПЛЕКСЫ ПОРФИРИНОВ В КАЧЕСТВЕ ЛЮМИНЕСЦЕНТНЫХ ВЕЩЕСТВ ДЛЯ ДИАГНОСТИКИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 1985 |
|
SU1340087A1 |
| WO 2002096366 A2, 05.12.2002. | |||
Авторы
Даты
2011-02-10—Публикация
2009-07-09—Подача