Область техники, к которой относится изобретение
Раскрытое здесь изобретение представляет собой кристаллическую форму аналога γ-аминомасляной кислоты и способы получения его кристаллической формы. Эти аналоги могут применяться как терапевтические агенты при лечении определенных заболеваний и расстройств, включая, например, невропатическую боль и пост-герпетическую невралгию.
Уровень техники
В основном, кристаллические формы лекарственных средств предпочтительны по сравнению с аморфными, в частности, из-за их лучшей стабильности. Например, во многих ситуациях при хранении аморфное лекарственное средство превращается в кристаллическое. Поскольку аморфная и кристаллическая формы лекарственного средства обычно имеют различные физические/химические свойства, эффективность и/или биодоступность, при фармацевтическом введении такие взаимопревращения нежелательны по причинам безопасности. Ключевой характеристикой любого кристаллического лекарственного средства является полиморфное поведение такого материала. Полиморфами являются кристаллы одной и той же молекулы, которые имеют различные физические свойства, поскольку кристаллическая решетка включает в себя различную аранжировку молекул. Различные физические свойства, проявляемые полиморфами, влияют на важные фармацевтические параметры, такие как хранение, стабильность, спрессовываемость, плотность (имеющие значение при составлении рецептуры и производстве продукта) и скорости растворения (важные в определении биодоступности). Различия в стабильности могут быть вызваны изменениями в химической реакционноспособности (например, в различиях в гидролизе или окислении, таких, что дозированная форма окисляется быстрее, когда включает один полиморф, чем когда включает другой полиморф), механических изменениях (например, таблетки крошатся при хранении, при этом кинетически предпочтительная форма превращается в термодинамически более стабильную кристаллическую форму) или в изменении обоих параметров (например, таблетки одного полиморфа являются более чувствительными к распаду при высокой влажности). В экстремальных ситуациях различия в растворимости между полиморфами могут приводить к переходам к кристаллическим формам, для которых характерна минимальная эффективность или которые являются токсичными. Кроме того, физические свойства кристаллической формы могут быть важны в фармацевтическом производстве. Например, определенная кристаллическая форма может легче образовывать сольваты или ее труднее фильтровать и отмывать от загрязнений по сравнению с другими формами (то есть распределение конкретных форм и размеров у одной кристаллической формы может отличаться от других).
Ведомства, такие как Администрация по пищевым и лекарственным продуктам США (United States Food and Drug Administration), внимательно контролируют полиморфное содержание активного компонента лекарственного средства в твердой дозированной форме. В основном, регулирующие документы агентства требуют проведения мониторинга полиморфных лекарственных средств от партии к партии, если на рынок поступает любой другой, нежели чистый, термодинамически предпочтительный полиморф. В соответствии с этим медицинские и коммерческие причины приводят к заинтересованности в синтезе и маркетинге таких твердых лекарственных средств, как термодинамически стабильные полиморфы, в основном, свободные от кинетически предпочтительных полиморфов.
1-{[(α-Изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота (1), пролекарственное средство аналога гамма-аминомасляной кислоты (GABА) габапентина (2), имеет более высокую биодоступность, когда оно вводится орально или непосредственно в толстый кишечник млекопитающих (Gallop et al., международная публикация WO 02/100347). Высокая биодоступность делает соединение (1) ценным компонентом оральной дозированной формы (включая дозированную форму с пролонгированным высвобождением), полезным для лечения или профилактики эпилепсии, боли (особенно нейропатической боли и мышечной и скелетной боли), депрессии, тревоги, психозов, обмороков, гипокинезии, внутричерепных нарушений, нейродегенеративных заболеваний, паники, воспалительных заболеваний (например, артритов), бессонницы, желудочно-кишечных расстройств, приливов, синдрома усталых ног, недержания мочи или синдрома отмены алкоголя.
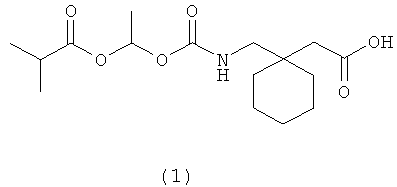
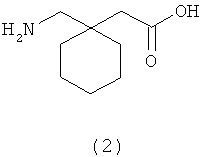
Соединение (1), полученное, как описано у Gallop et al., международная публикация No WO 02/100347, после лиофилизации выделяется из водного ацетонитрила в виде стекловидного твердого вещества. Материал, полученный благодаря этому процессу, частично или полностью аморфен, и определенные формы солей щелочных металлов являются гигроскопичными. Однако с аморфными твердыми, особенно гигроскопичными твердыми, веществами трудно работать при фармацевтическом производстве из-за низких плотностей и неудовлетворительных реологических свойств. Кроме того, манипуляции с гигроскопичными твердыми веществами требуют специальных методов и оборудования для получения, например, воспроизводимых количеств активного соединения или стабильности твердых рецептурных составов. К тому же гигроскопичные лекарственные соединения должны быть упакованы в специальные контейнеры, которые имеют барьеры для водяных паров, что, в основном, увеличивает цену таких продуктов.
В соответствии с этим существует потребность в кристаллических формах 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты с первоклассными физико-химическими свойствами, которые могут быть использованы преимущественно в процессе фармацевтического производства и в фармацевтических композициях.
Раскрытие изобретения
Обеспечена кристаллическая форма 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты, которая удовлетворяет этим и другим потребностям. Обеспечены также фармацевтические композиции кристаллической формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты, способы применения кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и ее фармацевтических композиций для лечения и профилактики различных заболеваний и способы получения кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты.
В первом аспекте обеспечивается кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота, которая на дифрактограмме рентгеновских лучей на порошке имеет характерные пики абсорбции (2θ) при 7,0°±0,3°, 8,2°±0,3°, 10,5°±0,3°, 12,8°±0,3°, 14,9°±0,3°, 16,4°±0,3°, 17,9°±0,3°, 18,1°±0,3°, 18,9°±0,3°, 20,9°±0,3°, 23,3°±0,3°, 25,3°±0,3° и 26,6°±0,3°.
Во втором аспекте обеспечиваются фармацевтические композиции кристаллической формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты. Фармацевтические композиции включают 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусную кислоту, которая имеет характерные пики абсорбции при 7,0°±0,3°, 8,2°±0,3°, 10,5°±0,3°, 12,8°±0,3°, 14,9°±0,3°, 16,4°±0,3°, 17,9°±0,3°, 18,1°±0,3°, 18,9°±0,3°, 20,9°±0,3°, 23,3°±0,3°, 25,3°±0,3° и 26,6°±0,3° на дифрактограмме рентгеновских лучей на порошке и фармацевтически приемлемый носитель.
В третьем аспекте обеспечиваются способы лечения или профилактики эпилепсии, боли (особенно нейропатической боли и мышечной и скелетной боли), депрессии, тревоги, психозов, обмороков, гипокинезии, внутричерепных нарушений, нейродегенеративных заболеваний, паники, воспалительных заболеваний (например, артритов), бессонницы, желудочно-кишечных расстройств, приливов, синдрома усталых ног, недержания мочи или синдрома отмены алкоголя. Эти способы, в основном, включают введение пациенту при необходимости такого лечения или профилактики терапевтически эффективного количества 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты, которая имеет характерные пики абсорбции (2θ) при 7,0°±0,3°, 8,2°±0,3°, 10,5°±0,3°, 12,8°±0,3°, 14,9°±0,3°, 16,4°±0,3°, 17,9°±0,3°, 18,1°±0,3°, 18,9°±0,3°, 20,9°±0,3°, 23,3°±0,3°, 25,3°±0,3° и 26,6°±0,3° на дифрактограмме рентгеновских лучей на порошке.
В четвертом аспекте обеспечиваются фармацевтические композиции для лечения или профилактики эпилепсии, боли (особенно нейропатической боли и мышечной и скелетной боли), депрессии, тревоги, психозов, обмороков, гипокинезии, внутричерепных нарушений, нейродегенеративных заболеваний, паники, воспалительных заболеваний (например, артритов), бессонницы, желудочно-кишечных расстройств, приливов, синдрома усталых ног, недержания мочи или синдрома отмены алкоголя у пациента нуждающегося в таком лечении или профилактике. Эти способы, в основном, включают введение пациенту при необходимости такого лечения или профилактики терапевтически эффективного количества 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексан уксусной кислоты, которая имеет характерные пики абсорбции (2θ) при 7,0°±0,3°, 8,2°±0,3°, 10,5°±0,3°, 12,8°±0,3°, 14,9°±0,3°, 16,4°±0,3°, 17,9°±0,3°, 18,1°±0,3°, 18,9°±0,3°, 20,9°±0,3°, 23,3°±0,3°, 25,3°±0,3° и 26,6°±0,3° на дифрактограмме рентгеновских лучей на порошке.
В пятом аспекте обеспечиваются способы получения кристаллической 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты, которая имеет характерные пики абсорбции при 7,0°±0,3°, 8,2°±0,3°, 10,5°±0,3°, 12,8°±0,3°, 14,9°±0,3°, 16,4°±0,3°, 17,9°±0,3°, 18,1°±0,3°, 18,9°±0,3°, 20,9°±0,3°, 23,3°±0,3°, 25,3°±0,3°, 26,6°±0,3° на дифрактограмме рентгеновских лучей на порошке.
Краткое описание чертежей
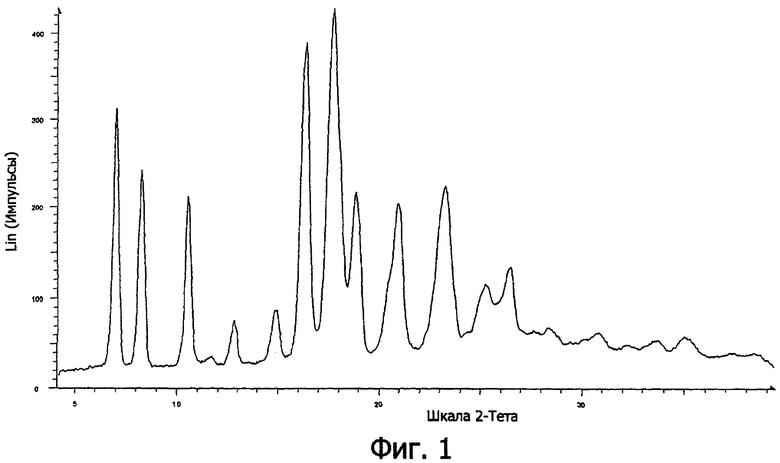
Фиг.1 иллюстрирует дифрактограмму рентгеновских лучей на порошке кристаллической 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и
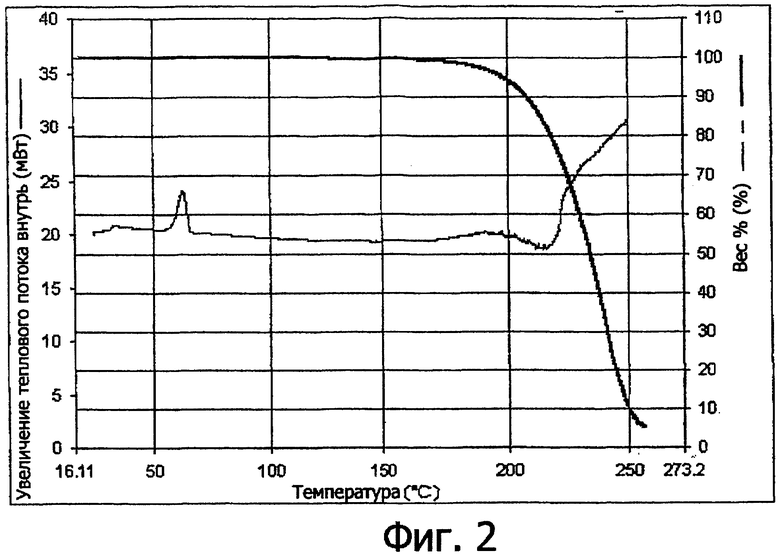
Фиг.2 иллюстрирует термограмму, полученную при дифференциальной сканирующей калориметрии кристаллической 1-{[(α-изобутаноилоксиэтокси)-карбонил]аминометил}-1-циклогексануксусной кислоты.
Осуществление изобретения
Определения
«Фармацевтически приемлемый носитель» относится к разбавителю, адъюванту, эксципиенту или носителю, с которым вводится 1-{[(α-изобутаноилоксиэтокси)-карбонил]аминометил}-1-циклогексануксусная кислота.
Термин «пациент» включает людей. Термин «человек» и «пациент» используются здесь как взаимозаменяемые.
«Профилактика» или «предотвращение» относится к снижению риска приобретения заболевания или расстройства (то есть индуцирования того, что у пациента, который может быть подвергнут воздействию или предрасположен к заболеванию, но не испытывает или не демонстрирует видимых симптомов заболевания).
«Прокомпонент» относится к форме защитной группы, которая, когда она используется для маскировки функциональной группы в пределах молекулы лекарственного соединения, превращает его в пролекарственное соединение. Типично прокомпонент будет прикрепляться к молекуле лекарственного соединения через связи, которые in vivo расщепляются ферментативным или неферментативным путем.
«Лечение» любого заболевания или расстройства относится, в одном воплощении, к облегчению заболевания или расстройства (то есть прекращению или спаду развития заболевания или, по меньшей мере, одного из их клинических симптомов). В другом воплощении «лечение» относится к облегчению, по меньшей мере, одного физического параметра, которое может быть неразличимо пациентом. В еще одном воплощении «лечение» относится к ингибированию заболевания или расстройства либо физически (например, путем стабилизация видимых симптомов), физиологически (например, путем стабилизации физических параметров) или обоих. Еще в одном воплощении «лечение» относится к задержке в начале заболевания или расстройства.
«Терапевтически эффективное количество» означает количество соединения, которое, когда оно вводится пациенту для лечения заболевания, достаточно для обеспечения эффекта лечения заболевания. «Терапевтически эффективное количество» будет варьировать в зависимости от соединения, заболевания и его тяжести, возраста, веса и тому подобного пациента, который будет подвергаться лечению.
Теперь должны быть сделаны ссылки для детализации предпочтительных воплощений. Хотя предпочтительные воплощения описаны, будет понятно, что изобретение не ограничивается этими предпочтительными воплощениями. Напротив, предполагается, что оно включает альтернативы, модификации и эквиваленты, которые могут быть включены в дух и рамки изобретения, как определено любыми пунктами формулы изобретения, приведенной здесь.
Кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и их получение
Кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил] аминометил}-1-циклогексануксусной кислоты и способы получения кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты раскрыты здесь в деталях.
Должно быть понятно, что ссылка на 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусную кислоту включает все, по существу, рацемические смеси, все возможные таутомерные формы традиционной химической структуры этого соединения и все изотопно меченые производные этого соединения (например, 2H, 3H, 13С, 14С, 15N, 17O, 18С и тому подобное).
Стартовый материал (то есть 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота) может быть получена в соответствии с процедурой, раскрытой в примере 13 Gallop et al., Международная публикация No WO 02/100347, или примере 12 Gallop et al., Международная публикация No WO 02/100347, заявке на предварительный патент США (United States Provisional Patent) серия No 60/6066 637, поданной 13 августа 2004 года, озаглавленной «Способы синтеза ациклоалкилкарбаматных пролекарственных средств».
В одном аспекте обеспечивается кристаллическая 1-{[(α-изобутаноилоксиэтокси)-карбонил]аминометил}-1-циклогексануксусная кислота. В определенных воплощениях кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерные пики абсорбции при 7,0°±0,3°, 8,2°±0,3°, 10,5°±0,3°, 12,8°±0,3°, 14,9°±0,3°, 16,4°±0,3°, 17,9°±0,3°, 18,1°±0,3°, 18,9°±0,3°, 20,9°±0,3°, 23,3°±0,3°, 25,3°±0,3°, 26,6°±0,3° на дифрактограмме рентгеновских лучей на порошке. В других воплощениях кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерные пики абсорбции при 7,0°±0,2°, 8,2°±0,2°, 10,5°±0,2°, 12,8°±0,2°, 14,9°±0,2°, 16,4°±0,2°, 17,9°±0,2°, 18,1°±0,2°, 18,9°±0,2°, 20,9°±0,2° 23,3°±0,2°, 25,3°±0,2° 26,6°±0,2° на дифрактограмме рентгеновских лучей на порошке.
В некоторых воплощениях кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота плавится между примерно 54°С и примерно 78°С. В других воплощениях кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота плавится между примерно 58°С и примерно 70°С. Еще в других воплощениях кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота плавится между примерно 62°С и примерно 68°С. Еще в других воплощениях кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота плавится между примерно 62°С и примерно 66°С. Еще в других воплощениях кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота плавится между примерно 62°С и примерно 66°С. Еще в других воплощениях кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота плавится между примерно 63°С и примерно 66°С. Еще в других воплощениях кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота плавится между примерно 64°С и примерно 66°С. Еще в других воплощениях кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота плавится между примерно 63°С и примерно 64°С.
В определенных воплощениях кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота может быть приготовлена путем добавления сначала 1-{[(α-изобутаноилоксиэтокси)-карбонил]аминометил}-1-циклогексануксусной кислоты к растворителю с образованием раствора или суспензии. Как это используется здесь, термины «раствор» и «суспензия» применяются взаимозаменяемо и предназначены для включения среды обстоятельств, при которых 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота помещается в растворитель или смесь растворителей независимо от растворимости. Растворитель, используемый при кристаллизации, может быть либо гомогенным растворителем, либо комбинацией растворителей, либо растворителем или комбинацией растворителей, в которых 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота проявляет зависимую от температуры растворимость. В основном, растворители или комбинация растворителей, в которых 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота является растворимой в пределах первого температурного интервала и плохо растворимой в пределах второго температурного интервала, могут быть предпочтительно использованы в способе, описанном здесь. Смеси «хорошего» растворителя и «антирастворителя» могут быть также использованы при температурно-зависимой солюбилизации, то есть растворении при повышенной температуре и кристаллизации при комнатной температуре. Примеры подходящих «хороших» растворителей включают метанол, этанол, 1,2-пропандиол, трет-бутанол, н-бутанол, изопропанол, уксусную кислоту, нитрометан, ацетонитрил, диметилсульфоксид, диметилформамид, N-метилпирролидон, ацетон, метилацетат, этилацетат, изопропилацетат, изобутилацетат, метилизобутилкетон, 1,2-диметоксиэтан, тетрагидрофуран, 2-метилтетрагидрофуран, толуол, метил-трет-бутиловый эфир, хлоробензол, 1,4-диоксан, диэтиловый эфир, кумен, о-ксилен, м-ксилен, п-ксилен, 2-этоксиэтанол, 1,2-этандиол, этилформиат, 2-метоксиэтанол, 1-пентанол, анизол, дихлорометан, цис- и транс- 1,2-дихлороэтилен, хлороформ, диметилацетамид, пропилацетат и их смеси. Примеры подходящих «антирастворителей» включают алканы, такие как пентан, гексан, гептан, октан, нонан, декан, индекан, додекан, цис- или транс-декалин, циклогексан, метилциклогексан и их смеси.
Предпочтительно процесс растворения проводится при повышенной температуре, до и включая точку кипения растворителя или комбинации растворителей. Соответственно, в определенных воплощениях 1-{[(α-изобутаноилоксиэтокси)-карбонил]аминометил}-1-циклогексануксусная кислота растворяется в растворителе или смеси растворителей с нагреванием и необязательно с перемешиванием или встряхиванием. Нагретый раствор может быть выдержан при повышенной температуре для гарантии полного растворения 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты. Нагретый раствор может быть также отфильтрован при повышенной температуре для удаления любых нерастворимых компонентов.
Предпочтительно раствор медленно охлаждается для обеспечения кристаллической 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты, которая может быть отделена от оставшегося растворителя путем фильтрации и/или путем сушки под пониженным давлением. В некоторых воплощениях раствор охлаждается до температуры между примерно 0°С и примерно 25°С. Другие способы, известные специалистам (например, выпаривание растворителя, обводнение, химическая реакция, кристаллизация желаемой формы с использованием малых количеств затравки и тому подобное) также могут быть применены для обеспечения кристаллической 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты.
В некоторых воплощениях 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота растворяется в гептане при температуре между примерно 70°С и температурой флегмы. Предпочтительно температура составляет примерно 70°С и концентрация 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты в гептане находится между примерно 0,07 г/мл и примерно 0,08 г/мл. Затем раствор охлаждается до комнатной температуры для обеспечения кристаллической формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты.
В другом воплощении 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота растворяется в смеси гептан/этилацетат (10:1 по объему) при температуре между примерно 50°С и примерно температурой флегмы, более предпочтительно при температуре примерно 70°С. Концентрация 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты в смеси гептан/этилацетат (10:1 по объему) находится между примерно 0,18 г/мл и примерно 0,22 г/мл. Затем раствор охлаждают до между примерно 0°С и примерно 25°С для обеспечения кристаллической 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты.
Еще в других воплощениях 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота растворяется в смеси метилциклогексан/метил-трет-бутилового эфира (объемное соотношение метилциклогексана/метил-трет-бутилового эфира между примерно 5:1 и примерно 20:1, предпочтительно около 10:1) при температуре между примерно 20°С и примерно 40°С и концентрации 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты в смеси метилциклогексана/метил-трет-бутилового эфира между примерно 0,1 г/мл и примерно 0,25 г/мл. Затем раствор охлаждают до температуры между примерно 0°С и примерно 25°С для обеспечения кристаллической 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты.
Терапевтическое применение
Кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции могут быть введены пациенту, преимущественно человеку, страдающему от эпилепсии, боли (особенно нейропатической боли и мышечной, и скелетной боли), постгерпетической невралгии, депрессии, тревоги, психозов, обмороков, гипокинезии, внутричерепных нарушений, нейродегенеративных заболеваний, паники, воспалительных заболеваний (например, артритов), бессонницы, желудочно-кишечных расстройств, приливов, синдрома усталых ног, недержания мочи или синдрома отмены алкоголя. Дополнительно в определенных воплощениях кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции вводятся пациенту, предпочтительно человеку, как профилактическая мера против различных заболеваний или расстройств. Кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции могут быть введены в качестве профилактической меры пациенту, имеющему предрасположенность к эпилепсии, боли (особенно нейропатической боли и мышечной и скелетной боли), постгерпетической невралгии, депрессии, тревоге, психозу, обморокам, гипокинезии, внутричерепным нарушениям, нейродегенеративным заболеваниям, панике, воспалительным заболеваниям (например, артритам), бессоннице, желудочно-кишечных расстройствам, приливам, синдрому усталых ног, недержанию мочи или синдрому отмены алкоголя. Соответственно, кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции могут применяться для профилактики одного заболевания и сопутствующего лечения другого (например, предотвращения психозов, в то время как лечатся желудочно-кишечные расстройства, предотвращение невропатической боли, в то время как лечат синдром отмены алкоголя).
Пригодность кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций для лечения эпилепсии, боли (особенно нейропатической боли и мышечной и скелетной боли), постгерпетической невралгии, депрессии, тревоги, психозов, обмороков, гипокинезии, внутричерепных нарушений, нейродегенеративных заболеваний, паники, воспалительных заболеваний (например, артритов), бессонницы, желудочно-кишечных расстройств, приливов, синдрома усталых ног, недержания мочи или синдрома отмены алкоголя может быть определено способами, известными специалистам (например, Satzinger et al., патент США No 4024175; Satzinger et al., патент США No 4087544; Woodruff et al., патент США No 5084169; Silverman et al., патент США No 5563175; Singh, патент США No 6001876; Horwell et al., патент США No 6020370; Silverman et al., патент США No 6028214; Horwell et al., патент США No 6103932; Silverman et al., патент США No 6117906; Silverman et al., международная публикация No WO 93/23383; Horwell et al., международная публикация No WO 97/29101; Horwell et al., международная публикация No WO 97/33858; Horwell et al., международная публикация No WO 97/33859; Bryans et al., международная публикация No WO 98/17627; Guglietta et al., международная публикация No WO 99/08671; Bryans et al., международная публикация No WO 99/21824; Bryans et al., международная публикация No WO 99/31057; Magnus-Miller et al., международная публикация No WO 99/37296; Bryans et al., международная публикация No WO 99/31075; Bryans et al., международная публикация No WO 99/61424; Pande, международная публикация No WO 00/23067; Bellioti, международная публикация No WO 00/31020; Bryans et al., международная публикация No WO 00/50027 и Bryans et al., международная публикация No WO 02/00209). Кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции могут применяться для лечения или предотвращения эпилепсии, боли (особенно нейропатической боли и мышечной и скелетной боли), пост-герпетической невралгии, депрессии, тревоги, психозов, обмороков, гипокинезии, внутричерепных нарушений, нейродегенеративных заболеваний, паники, воспалительных заболеваний (например, артритов), бессонницы, желудочно-кишечных расстройств, приливов, синдрома усталых ног, недержания мочи или синдрома отмены алкоголя с применением известных процедур, описанных в уровне техники (смотри ссылки выше).
Соединение, раскрытое здесь, может быть более эффективным, чем родительская молекула лекарственного средства (например, габапентин или другие аналоги GABA) в лечении или профилактике эпилепсии, боли (особенно нейропатической боли и мышечной и скелетной боли), постгерпетической невралгии, депрессии, тревоги, психозов, обмороков, гипокинезии, внутричерепных нарушений, нейродегенеративных заболеваний, паники, воспалительных заболеваний (например, артритов), бессонницы, желудочно-кишечных расстройств, приливов, синдрома усталых ног, недержания мочи или синдрома отмены алкоголя, поскольку для раскрытого соединения нужно меньше времени для достижения терапевтической концентрации в крови, то есть соединение, раскрытое здесь, имеет более короткое tmax, чем габапентин, когда он принимается орально. Не желая быть связанным теорией, полагают, что соединение, раскрытое здесь, абсорбируется из желудочно-кишечного тракта в кровь иными механизмами, чем те, с помощью которых абсорбируются габапентин и другие известные аналоги GABA. Например, полагают, что габапентин активно транспортируется через стенку кишечника с помощью транспортера-переносчика, локализованного в тонком кишечнике человека. Транспортер габапентина легко насыщается, это означает, что количество габапентина, абсорбированного в кровь, не пропорционально количеству габапентина, который вводится орально, поскольку, как только транспортный механизм насыщен, не происходит дополнительной абсорбции габапентина в сколь-либо существенной степени. По сравнению с габапентином соединение, раскрытое здесь, абсорбируется через стенку кишечника вдоль большей части желудочно-кишечного тракта, включая толстую кишку.
Поскольку соединение, раскрытое здесь, может быть включено в рецептуры с продленным высвобождением, которые обеспечивают высвобождение в желудочно-кишечном тракте непрерывно в течение часов и, в частности, высвобождение в толстом кишечнике, 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота также может быть более эффективной, чем габапентин при лечении или профилактике эпилепсии, боли (особенно нейропатической боли и мышечной и скелетной боли), постгерпетической невралгии, депрессии, тревоги, психозов, обмороков, гипокинезии, внутричерепных нарушений, нейродегенеративных заболеваний, паники, воспалительных заболеваний (например, артритов), бессонницы, желудочно-кишечных расстройств, приливов, синдрома усталых ног, недержания мочи или синдрома отмены алкоголя. Способность соединения, раскрытого здесь, применяться в оральной дозированной форме с пролонгированным высвобождением снижает частоту дозирования, необходимую для поддержания терапевтически эффективной концентрации лекарственного средства в крови.
Способы введения
Кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции могут быть с выгодой применены для лечения людей. Как описано ранее, кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции полезны для лечения или профилактики эпилепсии, боли (особенно нейропатической боли и мышечной и скелетной боли), постгерпетической невралгии, депрессии, тревоги, психозов, обмороков, гипокинезии, внутричерепных нарушений, нейродегенеративных заболеваний, паники, воспалительных заболеваний (например, артритов), бессонницы, желудочно-кишечных расстройств, приливов, синдрома усталых ног, недержания мочи или синдрома отмены алкоголя.
Когда они применяются для лечения или предотвращения перечисленных выше заболеваний или расстройств, кристаллические формы 1-{[(α-изобутаноилоксиэтокси)-карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции могут быть введены или применены отдельно или в комбинации с другими агентами. Кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции могут быть введены или применены отдельно или в комбинации с другими фармацевтически активными агентами, включая другие аналоги GABA.
Способы лечения и профилактики обеспечиваются путем введения пациенту терапевтически эффективного количества кристаллической формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций. Пациент может быть животным, более предпочтительно млекопитающим и наиболее предпочтительно - человеком.
Кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции предпочтительно вводятся орально. Кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции могут быть также введены любым подходящим путем, например путем инфузии или болюсной инъекции, путем абсорбции через эпителиальный или слизисто-кожный слои (например, слизистая оболочка рта, ректальная или желудочно-кишечная слизистая оболочка и тому подобное). Введение может быть системным или локальным. Известны различные системы доставки (например, инкапсуляция в липосомы, микрочастицы, микрокапсулы, капсулы и подобное), которые могут применяться для введения кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций. Способы введения включают, но не ограничиваются этим, внутрикожный, внутримышечный, внутрибрюшинный, внутривенный, подкожный, интраназальный, эпидуральный, оральный, сублингвальный, интраназальный, интрацеребральный, интравагинальный, трансдермальный, ректальный, путем ингаляции или локально, в частности через уши, нос, глаза или кожу.
В некоторых воплощениях кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции могут быть доставлены с применением систем пролонгированного высвобождения, предпочтительно оральных систем пролонгированного высвобождения. В одном воплощении может быть применен насос (Langer, supra; Sefton, 1987, CRC Crit Ref. Biomed. Eng. 14:201; Saudek et al., 1989, N. Engl. J. Med. 321-574).
В других воплощениях могут быть использованы полимерные материалы ("Medical Applications of Controlled Release," Langer and Wise (eds.) CRC Pres., Boca Raton, Florida (1974); "Controlled Drug Bioavailability", Drug Product Design and Performance, Smoled and Ball (ads.), Wiley, New York (1984); Langer et al., 1983, J. Macromol. Sci. Rev. Macromol. Chem. 23:61; см. также Levy et al., 1985, Science 228:190; During et al., 1989, Ann. Neurol. 25:351; Howard et al., 1989, J. Neurosurg. 71:105). Еще в других воплощениях полимерные материалы применяются для оральной доставки с пролонгированным высвобождением. Полимеры включают, например, натриевую карбоксиметилцеллюлозу, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу и гидроксиэтилцеллюлозу (предпочтительно гидроксипропилметилцеллюлозу). Были описаны и другие эфиры целлюлозы (Alderman, Int. J. Pharm. Tech. & Prod. Mfr. 1984, 5(3) 1-9). Факторы, влияющие на высвобождение лекарственного средства, были описаны и хорошо известны квалифицированным специалистам (Bamba et al., Int. J. Pharm. 1979, 2, 307).
В других воплощениях препараты, покрытые кишечно-растворимой оболочкой, могут быть применены для орального введения с пролонгированным высвобождением. Материалы оболочки включают, например, полимеры с зависимой от рН растворимостью (то есть рН-контролируемое высвобождение), полимеры с медленной или с рН-зависимой скоростью набухания, растворения или эрозии (то есть зависимое от времени высвобождение) и полимеры, которые деградируют при действии ферментов (то есть контролируемое ферментами высвобождение), и полимеры, которые формируют пленочные слои, которые разрушаются при увеличении давлении (то есть контролируемое давлением высвобождение).
В еще других воплощениях для орального введения с пролонгированным высвобождением применяются осмотические системы доставки (Verma et al., Drug Dev. Ind. Pharm. 2000, 26:695-708). В некоторых воплощениях в качестве устройств для орального пролонгированного освобождения применяются осмотические устройства OROS™ (Theeuwes et. al. патент США No 3845770; Theeuwes et al. патент США No 3916899).
Еще в других воплощениях система контролируемого высвобождения может быть размещена поблизости от мишени кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций, требуя, таким образом, только части системной дозы (например, Goodson в "Medical Applications of Controlled Release", supra, vol., 2, pp.115-138 (1984). Могут быть также применены другие системы контролируемого высвобождения, которые обсуждаются у Langer, 1990, Science 249:1527-1533.
Кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции при введении пациенту in vivo предпочтительно обеспечивают габапентин. Не желая быть связанным теорией, полагаем, что прокомпонент кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций может быть разрушен химически и/или ферментативно. Один или более ферментов, представленных в желудке, полости кишечника, тканях кишечника, крови, печени, мозге или любой другой подходящей ткани млекопитающего, могут расщеплять прокомпонент кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций. Механизм расщепления не имеет значения. Предпочтительно габапентин, образующийся при отщеплении прокомпонента из кристаллической формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций, не содержит значительных количеств примеси в виде γ-лактама (предпочтительно менее чем 0,5% по весу, более предпочтительно менее чем 0,2% по весу, более предпочтительно менее чем 0,1% по весу), которая образуется за счет внутримолекулярной циклизации γ-аминогруппы с карбоксильной группировкой. Степень образования лактама из кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций может быть определена in vitro с применением стандартных аналитических методов.
Не желая быть связанными теорией, полагаем, что прокомпонент кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций может расщепляться до абсорбции в желудочно-кишечном тракте (например, в желудке или полости кишечника) и/или после абсорбции в желудочно-кишечном тракте (например, в ткани кишечника, крови, печени или других подходящих тканях млекопитающего). Если прокомпонент кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций расщепляется до абсорбции в желудочно-кишечном тракте, габапентин может быть обычным путем абсорбирован в системное кровеносное русло (например, через транспортер больших нейтральных аминокислот, локализованный в тонком кишечнике). Если прокомпонент кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций отщепляется после абсорбции желудочно-кишечным трактом, этот предшественник аналога GABA может быть абсорбирован в системное кровеносное русло путем пассивной диффузии, активного транспорта или путем активного и пассивного процессов.
Если прокомпонент кристаллических форм 1-{[(α-изобутаноилоксиэтокси)-карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций отщепляется после абсорбции желудочно-кишечным трактом, это пролекарственное средство аналога GABA может иметь возможность абсорбироваться в системное кровеносное русло из толстого кишечника. В этой ситуации кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или их фармацевтические композиции предпочтительно вводятся как системы пролонгированного высвобождения. В определенных воплощениях кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции доставляются путем введения оральных форм пролонгированного высвобождения. Предпочтительно в этих воплощениях кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции вводятся дважды в день (более предпочтительно один раз в день).
Фармацевтические композиции
Настоящие фармацевтические композиции включают терапевтически эффективное количество кристаллической формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты с подходящим количеством фармацевтически приемлемого носителя, так что обеспечивается форма для должного введения пациенту. Когда они вводится пациенту, кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и фармацевтически приемлемые носители предпочтительно являются стерильными. Вода является предпочтительным носителем, когда кристаллическая форма 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты вводится внутривенно. Солевые растворы и водная декстроза и растворы глицерина также могут быть применены в качестве жидких носителей, особенно для инъецируемых растворов. Подходящие фармацевтические носители включают также такие эксципиенты как крахмал, глюкозу, лактозу, сахарозу, желатин, солод, рис, муку, уголь, силикагель, стеарат натрия, моностеарат глицерина, тальк, хлорид натрия, сухое обезжиренное молоко, глицерин, пропилен, гликоль, вода, этанол и тому подобное. По желанию настоящие композиции могут также содержать минорные количества увлажняющего или эмульсифицирующего агентов или рН-забуферивающих агентов. Дополнительно могут применяться вспомогательные, стабилизирующие, сгущающие, смазывающие и окрашивающие агенты.
В некоторых воплощениях фармацевтические композиции кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты являются свободными от лактамных побочных продуктов, образованных путем внутримолекулярной циклизации. В других воплощениях фармацевтические композиции кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты стабильны при длительном хранении (предпочтительно более чем один год) без значительного образования лактама (предпочтительно менее чем 0,5% лактама по весу, более предпочтительно менее чем 0,2% лактама по весу, еще более предпочтительно менее чем 0,1% лактама по весу).
Фармацевтические композиции, включающие кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты могут быть приготовлены путем традиционного смешивания, растворения, грануляции, приготовления драже, отмучивания, эмульсификации, инкапсулирования, включения или лиофилизации. Фармацевтические композиции могут быть сформулированы традиционным образом с применением одного или более физиологически приемлемых носителей, разбавляющих агентов, эксципиентов или вспомогательных агентов, которые облегчают обработку кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты в препаратах, которые могут быть применены фармацевтически. Подходящие рецептуры зависят от выбранного способа введения.
Настоящие фармацевтические композиции могут быть в форме растворов, суспензий, эмульсий, таблеток, пилюль, шариков, капсул, капсул, содержащих жидкости, порошков, композиций с пролонгированным высвобождением, суппозиториев, эмульсий, аэрозолей, спреев, суспензий или любых других форм, подходящих для применения. В некоторых воплощениях фармацевтически приемлемым носителем являются капсулы (например, Grosswald et al., патент США No 5698155). Другие примеры подходящих фармацевтических носителей были описаны в уровне техники (смотри Remington's Pharmaceutical Sciences, Philadelphia College of Pharmacy and Science, 19th Edition, 1995). Композиции кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты предпочтительно составляются для оральной доставки, особенно для орального введения с пролонгированным действием.
Фармацевтические композиции для оральной доставки могут быть, например, в форме таблеток, лепешек, водных или масляных суспензий, гранул, порошков, эмульсий, капсул, сиропов или эликсиров. Орально вводимые композиции могут включать один или более необязательных агентов, например подслащающие агенты, такие как фруктоза, аспартам или сахарин, вкусовые добавки, такие как перечная мята, масло грушанки или вишневый краситель, и консервирующие агенты для обеспечения фармацевтически приятных препаратов. Более того, в форме таблеток и пилюль фармацевтические композиции могут быть покрыты оболочкой для замедления дезинтеграции и абсорбции в желудочно-кишечном тракте, обеспечивая, таким образом, непрерывное действие в течение длительного периода времени. Селективно проницаемые мембраны, окружающие осмотически активное стимулирующее соединение, также являются подходящими для орального введения соединений и композиций, раскрытых здесь. В этих более поздних принципиальных решениях жидкость из среды, окружающей капсулу, входит благодаря стимулирующему соединению, которое набухает, вытесняя агент или агенты композиции через отверстие. Эти принципы доставки могут обеспечить, по существу, нулевой порядок профиля доставки в противоположность профилю с пиками, характерному для составов с немедленным освобождением. Могут быть также применены материалы, обеспечивающие задержку освобождения во времени, такие как моностеарат глицерина или стерата глицерина. Оральные композиции могут включать стандартные носители, такие как маннит, лактоза, крахмал, стеарат магния, сахарин натрия, целлюлоза, карбонат магния и тому подобное. Такие носители имеют предпочтительно фармацевтическую квалификацию.
Для оральных жидких препаратов, таких, например, как суспензии, эликсиры и растворы, подходящие переносчики, эксципиенты и разбавители включают воду, солевые растворы, алкиленгликоли (например, пропиленгликоль), полиалкиленгликоли (например, полиэтиленгликоль), масла, спирты, слабокислые буферные растворы с рН между 4 и 6 (например, ацетат, цитрат, аскорбат с концентрацией между примерно 5 мМ и примерно 50 мМ) и тому подобное. Дополнительно могут быть добавлены вкусовые добавки, консерванты, красящие агенты, соли желчных кислот, ацилкарнитины и подобное.
Могут быть также созданы фармацевтические композиции для введения другими путями. Для буккального введения композиции могут иметь форму таблеток, лепешек и тому подобного, сформулированных традиционным образом. Жидкие композиции лекарственного средства, подходящие для применения с распылителями и с устройствами для жидких спреев и аэрозольными устройствами EHD, типично будут включать кристаллическую форму 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты с фармацевтически приемлемым носителем. Предпочтительно фармацевтически приемлемый носитель является жидким, таким как спирт, вода, полиэтиленгликоль или перфторокарбон. Необязательно может быть добавлен другой материал для изменения аэрозольных свойств раствора или суспензии соединений, раскрытых здесь. Предпочтительно этот материал является жидким, таким как спирт, гликоль, полигликоль или жирная кислота. Другие способы для составления жидких растворов или суспензий лекарственного средства, подходящих для применения в аэрозольных устройствах, известны специалистам (смотри, например, Biesalski, патент США No 5112598; Biesalski, патент США No 5556611). Кристаллическая форма 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты также может быть сформулирована в виде ректальных или вагинальных суппозиториев или задерживающейся клизмы, содержащих, например, традиционную основу для суппозитория, такую как масло какао или другие глицериды. В дополнение к композициям, описанным ранее, кристаллическая форма 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты также может быть сформулирована как препарат в виде депо. Такие формулировки длительного действия могут быть введены путем имплантации (например, подкожно или внутримышечно) или путем внутримышечной инъекции. Таким образом, например, кристаллическая форма 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты может быть составлена с подходящими полимерными или гидрофобными материалами (например, как эмульсия в приемлемом масле) или ионообменными смолами, или как малорастворимые производные, например малорастворимая соль.
В некоторых воплощениях, кристаллическая форма 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты составляется как чистый активный агент. В других воплощениях кристаллическая форма 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты составляется как смесь с другими кристаллическими формами 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты.
Дозировки
Кристаллическая форма 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции, в основном, будут применяться в количестве, эффективном для достижения планируемых целей. В применении для лечения или профилактики заболеваний, таких как эпилепсия, боль (особенно нейропатическая боль и мышечная и скелетная боль), депрессия, тревога, психозы, обмороки, гипокинезия, внутричерепные нарушения, нейродегенеративные заболевания, паника, воспалительные заболевания (например, артриты), бессонница, желудочно-кишечные расстройства, приливы, синдром усталых ног, недержание мочи или синдром отмены алкоголя кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции вводятся или применяются в терапевтически эффективном количестве.
Количество кристаллической формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций, которые будут эффективны при лечении частных расстройств или состояний, раскрытых здесь, будет зависеть от природы расстройств или состояний, и может быть определено с применением стандартных клинических методов, известных в уровне техники, как описано ранее. Дополнительно анализы in vivo и in vitro могут необязательно помочь в идентификации оптимальных интервалов дозировок. Количество кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций будет среди других факторов, конечно, зависеть от субъекта, которого лечат, веса субъекта, тяжести болезни, способа введения и мнения лечащего врача.
Например, дозировка может быть доставлена в фармацевтической композиции путем единственного введения, множественных применений или контролируемого высвобождения. В некоторых воплощениях кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции доставляются путем орального введения с пролонгированным действием. Предпочтительно в этих воплощениях кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций вводятся дважды в день (более предпочтительно один раз в день). Дозировка может быть повторена периодически, может быть обеспечена поодиночке или в комбинации с другими лекарственными средствами и может продолжаться так долго, как требуется для эффективного лечения болезненного состояния или расстройства.
В некоторых воплощениях доза кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций может быть доведена для обеспечения дозы между примерно 500 мг/день и примерно 7000 мг/день пролекарства (эквивалент примерно 260 мг/день и примерно 3600 мг/день габапентина). Интервалы дозировок могут быть легко определены способами, известными специалистам.
Кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций предпочтительно анализируются in vivo и in vitro в отношении желательной терапевтической и профилактической активности перед применением на людях. Предпочтительно терапевтически эффективная доза кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций, описанных здесь, будет обеспечивать терапевтический эффект без обеспечения значительной токсичности. Токсичность кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций может быть определена с использованием стандартных фармацевтических процедур и может быть легко установлена квалифицированным средним исполнителем. Соотношение между дозами, обеспечивающими токсический и терапевтический эффект, представляет собой терапевтический индекс. Дозировка кристаллических форм 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтических композиций, описанных здесь, будет предпочтительно находиться в ряду концентраций в системном кровотоке, которые включают эффективную дозу с небольшой токсичностью или ее отсутствием.
Комбинированная терапия
В определенных воплощениях кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции могут применяться в комбинированной терапии с, по меньшей мере, одним другим терапевтическим агентом. Кристаллические формы 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и/или ее фармацевтические композиции и другой терапевтический агент могут действовать аддитивно или более предпочтительно синергически. В определенных воплощениях фармацевтическая композиция, включающая кристаллическую форму 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты, вводится одновременно с введением другого терапевтического агента, который может быть частью той же самой фармацевтической композиции, что и кристаллическая форма 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты или различной фармацевтической композиции. В других воплощениях фармацевтическая композиция, включающая кристаллическую форму 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты, вводится до или после введения другого терапевтического агента. Например, кристаллическая форма 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты может быть введена в комбинации с аморфной формой 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты, другой кристаллической формой 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты, габапентином или прегабалином.
Примеры
Следующие примеры в подробностях описывают приготовление 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и ее кристаллической формы. Для специалистов будет очевидно, что многие модификации как материалов, так и методов могут быть выполнены без отклонения от рамок изобретения.
В примерах, данных ниже, следующие сокращения имеют следующие значения. Если сокращение не определено, применяется общепринятое значение.
Атм = атмосфера
Вос = трет-бутилоксикарбонил
Cbz = карбобензилокси
DCC = дициклогексилкарбодиимид
DMAP = 4-N,N-диметиламинопиридин
DMF = N,N-диметилформамид
DMSO = диметилсульфоксид
Fmoc = 9-флуоренилметилоксикарбонил
г = грамм
ч = час
HPLC - высокоэффективная жидкостная хроматография
л = литр
LC/MS = жидкостная хроматография/масс-спектрометрия
М = молярный
мин = минута
мл = миллилитр
ммоль = миллимоли
NHS = N-гидроксисукцинимид
THF = тетрагидрофуран
TFA = трифторуксусная кислота
TLC = тонкослойная хроматография
TMS = триметилсилил
мкл = микролитры
мкМ = микромоли
v/v = объем/объем
Пример 1: 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота через интермедиат триметилсилилового эфира
Стадия А: 1-{[α-хлороэтокси)карбонил]аминометил}-1-циклогексануксусная кислота
В 5-литровую трехгорлую колбу с круглым дном, содержащую дихлорометан (1,6 л), был добавлен габапентин (120,4 г, 0,704 моль) с последующим добавлением триэтиламина (294 мл, 2,11 моль). Далее был медленно добавлен хлоротриметилсилан (178 мл, 1,40 моль), в то время как температуру реакции поддерживали менее 15°С, и полученную суспензию перемешивали в течение 30 мин. Затем медленно был добавлен 1-хлороэтилхлороформиат (100 г, 0,704 моль), в то время как температура поддерживалась ниже 15°С. После того, как процедура была закончена, был добавлен триэтиламин (88 мл, 0,63 моль) и полученную суспензию перемешивали при комнатной температуре в течение 30 мин. Полученный силиловый эфир был превращен через кислотную перегруппировку в соответствующую кислоту путем промывания реакционной смеси водой (2×1 л) с последующим промыванием 1 н. НСl (2×2 л) и затем рассолом (2×500 мл). После сушки над безводным сульфатом натрия и удаления растворителя под вакуумом был получен неочищенный продукт (190 г) в виде оранжевого масла и использован на стадии В без дальнейшей очистки. 1Н-ЯМР (СDСl3, 400 МГц): δ 1,41-1,57 (m, 10Н), 1,78 (d, 3H), 2,33 (s, 2H), 3,27 (d, 2H), 5,42 (br.s, 1H), 6,55 (q, 1H).
Стадия В: 1-{[α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота
В 3-литровую трехгорлую колбу с круглым дном была добавлена изомасляная кислота (254 г, 2,9 моль) с последующим добавлением триэтиламина (395 мл, 2,84 моль). Реакционная смесь была охлаждена до комнатной температуры и раствор неочищенной кислоты из проведенной выше реакционной стадии (190 г, 0,69 моль) в дихлорометане (80 мл) был добавлен в контролируемых условиях с поддержанием температуры ниже 30°С. Полученный бледно-желтый раствор перемешивали в течение ночи. Затем реакционная смесь была разведена одним объемом дихлорометана и промыта водой (6×500 мл), водным раствором бикарбоната калия (3×500 мл) и рассолом (2×500 мл). Сушка над безводным сульфатом натрия и удаление растворителя под вакуумом приводили к получению неочищенного продукта в виде темно-красного масла (87 г). Часть этого продукта (35 г) наносили на 800-г быструю колонку Biotage™ с нормальной силикагельной фазой и элюировали 40% диэтиловым эфиром в гексане (6 л), который после удаления растворителя под вакуумом давал бесцветное масло (13,5 г). Эту процедуру повторяли со второй 35 г порцией неочищенного продукта, получая дополнительно 13,5 г 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты. Образец продукта (25 г) был повторно кристаллизован путем растворения в гептане (325 мл) при 70°С с последующим медленным охлаждением до комнатной температуры. Белый кристаллический продукт (23 г) был получен путем фильтрации. Точка плавления 63-64°С.
Пример 2: 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексан-уксусная кислота через аллилэфирный интермедиат
Стадия А: гидрохлорид аллил-1-аминометил-1-циклогексанацетата
Через сухую 3-литровую трехгорлую колбу с круглым дном, оснащенную магнитной мешалкой и 500 мл воронкой с выравниванием давления, пропускали газообразный азот. В колбу помещали габапентин (171 г, 1,0 моль) и аллиловый спирт (1 л, 852 г, 14,6 моль) и полную смесь охлаждали до 0°С на ледяной бане. По каплям в течение 1 ч в перемешиваемый раствор добавляли тионилхлорид (225 мл, 360 г, 3,0 моль). Реакционной смеси позволяли находиться при комнатной температуре и перемешивании в течение 16 ч, затем ее разводили этиловым эфиром (2 л) и охлаждали до 0°С с перемешиванием. Через несколько минут формировались белые кристаллы, которые собирали путем фильтрования. Неочищенный продукт перекристаллизовывали из смеси этанола и этилового эфира 1/3 (v/v) (2 л) для получения твердого белого продукта (220 г, 80%). Точка плавления 138-142°С. 1H-ЯМР (CD3OD, 400 МГц): δ 1,36-1,54 (m, 10Н), 2,57 (s, 2H), 3,05 (s, 2H), 4,61 (d, J=6 Гц, 2H), 5,22 (dd, J1=10,4 Гц, J2=1,2 Гц, 1Н), 5,33 (dd, J1=17,2 Гц, J2=1,4 Гц, 1Н), 5,90-6,00 (m, 1Н). MS (ESI) m/z 212,0 (M-Cl)+.
Стадия В: аллил-1-{[(α-хлороэтокси)карбонил]аминометил}-1-циклогексанацетат
К раствору полученной выше гидрохлоридной соли (220 г, 0,89 моль) в дихлорометане (1 л) был медленно добавлен 1-хлороэтилхлорформиат (101,7 мл, 132,3 г, 0,92 моль). Реакционная смесь была охлаждена до 0°С и к ней был медленно добавлен 4-метилморфолин (205 мл, 188,9 г, 1,87 моль) в течение 1 ч, в то время как температура поддерживалась ниже 10°С. Полученный мутный раствор перемешивали при комнатной температуре в течение 1 ч. Затем был добавлен этанол (150 мл) и реакционную смесь перемешивали в течение 1 ч при комнатной температуре. Затем реакционная смесь была разведена эфиром (2,5 л), промыта водой (1 л) и рассолом (1 л). Органическая фаза была осушена под сульфатом натрия и сконцентрирована с получением указанного в заголовке соединения в виде светло-желтой вязкой жидкости (282 г, 100%). 1Н-ЯМР (CDCl3, 400 МГц): δ 1,35-1,58 (m, 10Н), 1,78 (d, J=5,6 Гц, 3Н), 2,32 (s, 2H), 3,22 (d, J=6,8 Гц, 2Н), 4,57 (d, J=5,6 Гц, 2H), 5,25 (dd, J1=10,4 Гц, 1H), 5,32 (dd, J1=17,2 Гц, J2=1,6 Гц 1H), 5,52 (br, 1H, NH), 5,90-5,94 (m, 1H), 6,54 (q, J=5,6 Гц, 1Н).
Стадия С: аллил 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексанацетат
К смеси изомасляной кислоты (432 мл, 391,5 г, 4,4 моль) и 4-метилморфолина (488 мл, 449 г, 4,4 моль) был добавлен раствор хлорокарбамата с предыдущей стадии (282 г, 0,88 мл) в изомасляной кислоте (432 мл, 391,5 г, 4,4 моля). Добавление происходило при температуре 0°С в течение 30 мин. Полученный мутный раствор перемешивали при комнатной температуре в течение 16 ч. Реакционную смесь разводили эфиром (2,5 л) и промывали водой (3×500 мл), затем 10% водным бикарбонатом калия (6×500 мл), а затем рассолом (500 мл). Органическая фаза была осушена под сульфатом натрия и сконцентрирована с получением указанного в заголовке соединения в виде вязкой жидкости (328 г, 100%). 1Н-ЯМР (CDCl3, 400 МГц): δ 1,1 5 (d, J=7,2 Гц, 6Н), 1,35-1,58 (m, 10Н), 2,31 (s, 2H), 2,51 (m, 1H), 3,19 (d, J=5,6 Гц, 2H), 4,56 (d, J=5,6 Гц, 2H), 5,24 (dd, J1=10 Гц, J2=1 Гц, 1H), 5,32 (dd, J1=17 Гц, 1H, J2=1,2 Гц, 1H), 5,35 (br, 1H), 5,84-5,94 (m, 1H), 6,78 (q, J=5,6 Гц, 1H). MS (ESI) m/z 392,24 (M+H)+.
Стадия D: снятие защиты с аллил-1-{[(α-изобутаноилоксиэтокси)карбонил]-аминометил}-1-1-циклогексанацетата
К перемешиваемой суспензии формиата аммония (112 г, 1,7 моль) в этаноле (500 мл) был добавлен полученный выше аллиловый эфир (328 г, 0,88 моль) вместе с 10% Pd/C (15 г) под атмосферой азота. Через 6 ч реакционную смесь отфильтровывали от катализатора. Катализатор был промыт с этанолом (2×250 мл), фильтраты соединяли и выпаривали. Грубый продукт был растворен в эфире (2 л) и органическая фаза была промыта 2 н. НСl(2×2 л) для превращения аммониевой соли в кислую форму с последующим промыванием водой (1 л) и рассолом (1 л). Эфирный слой был осушен под сульфатом натрия и сконцентрирован с получением неочищенного продукта в виде вязкой жидкости (240 г, 82%).
Стадия Е: кристаллизация 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-1-циклогексануксусной кислоты
Круглодонная на 3 л колба была снабжена нагревающей масляной баней, азотным впусковым адаптером, внутренним термометром, верхней механической мешалкой и обратным холодильником. Через колбу пропускали азот и в нее помещали 1/10 (v/v) смесь этилацетата/гептана (1,2 л) и неочищенный продукт из предыдущей реакции (240 г). Колбу нагревали до тех пор, пока продукт не растворялся, затем охлаждали по следующему расписанию:
Затем колба была охлаждена до 4°С в течение ночи с перемешиванием (охлаждение улучшает выход). Продукт был отфильтрован и промыт гептаном (2×100 мл), затем осушен под пониженным давлением (25 мм рт. ст. (0,033 атм)) при 30°С в течение 18 ч для получения 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты (185 г) в виде твердых белых кристаллов.
Пример 3: дифракционный рентгеновский анализ на порошке 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-1-циклогексануксусной кислоты
Дифрактограммы рентгеновских лучей на порошке (XRPD) кристаллических образцов 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты, полученной в соответствии с примерами 1 и 2, данными выше, были определены с использованием ретгеновского дифрактометра Bruker D8 Discover на порошке с использованием Кα излучения Сu. Инструмент оборудован параллельной лучевой оптикой и двумерным HI-STAR детектором областей. Напряжение в трубке и сила тока были установлены на 40 кВ и 40 мА соответственно. Коллимированный рентгеновский луч был уменьшен до размера пятна 0,5 мм в диаметре. Детектор области был помещен на 15 см от центра гониометра, и угловое разрешение составляло приблизительно 0,033°/пиксель. Детектор покрывал диапазон в 35° в 2-тета (2θ) в пределах рамки. Угол между рентгеновским лучом и горизонтальной пластиной образца был выбран равным 4° и центр детектора области был выбран равным углу 18°. Эта геометрия позволяла определение 2-тета в диапазоне от 4,5° до 39,5° в пределах одной рамки. Типичное время усреднения было 3 мин для каждого собранного профиля XRPD. Корундовый образец (NIST 1976) был использован для калибровки XRPD инструмента. Оба образца давали эквивалентные профили дифрактограмм, как показано на фиг.1.
Пример 4: точка плавления и дифференциальный сканирующий калориметрический анализ кристаллической 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты
Точки плавления кристаллических образцов 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты, полученной в соответствии с примерами 1 и 2, данными выше, были определены с использованием устройства для определения точки плавления Electrothermal 9200 и составили 63-64°С.
Анализ с использованием дифференциальной сканирующей калориметрия (DSC) кристаллических образцов 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты, полученной в соответствии с примерами 1 и 2, данными выше, был проведен с использованием аппарата Perkin Elmer серия 7 путем сканирования от 25°С до 250°С со скоростью сканирования 5°С/мин. Тестируемая порция образца была помещена в алюминиевый сосуд и крышка была закручена для устранения любых видимых стыков между крышкой и сосудом. Пустой сосуд был приготовлен таким же образом как контроль. Сосуды были помещены в дифференциальный сканирующий калориметр. Материал был сканирован при подходящей температурной программе (уравновешивание при начальной температуре, изотермальный, скорость повышения, конечная температура) для получения термограммы, показанной на фиг.2. DSC анализ показал эндотермический переход с температурой начала 58,3°С и ΔН 72,39 Дж/г. В пике эндотермы 63-64°С образец визуально плавился.
Пример 5: 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-1-циклогексануксусная кислота
К раствору габапентина (6,8 г, 0,04 моль) в воде (40 мл) был добавлен раствор [(1-изобутаноилоксиэтокси)карбонилокси]сукцинимида (10 г, 0,036 моль) в ацетонитриле (40 мл) в течение 30 мин. Смесь перемешивали при температуре окружающей среды в течение 3 ч. Реакционную смесь разводили метил-трет-бутиловым эфиром (200 мл), промывали водой (2×100 мл) и рассолом (50 мл). Органическую фазу отделяли, осушали над безводным сульфатом натрия, фильтровали и концентрировали под вакуумом для указанного в заголовке соединения в виде твердого белого вещества (12 г, количественно).
Кристаллизация. Твердое соединение (12 г) было суспендировано в метилциклогексане : метил-трет-бутиловом эфире 10:1 (60 мл). Суспензию медленно нагревали до 50°С в течение 30 мин. Прозрачному раствору затем позволяли охлаждаться до комнатной температуры. В мутную смесь добавляли 5 мг кристаллов указанного в заголовке соединения. Затем смесь дополнительно охлаждали до 0-4°С в течение 2 ч. Твердый продукт фильтровали и промывали метилциклогексаном (2×10 мл) для получения титульного соединения в виде твердых белых кристаллов (10 г, выход 83%). Кристаллический твердый материал имел точку плавления примерно 64-66°С, как было измерено в открытой капиллярной системе определения точки плавления.
В конечном итоге нужно отметить, что имеются альтернативные пути осуществления настоящего изобретения. Соответственно, настоящие воплощения рассматриваются как иллюстративные и не как ограничивающие, и изобретение не ограничивается деталями, данными здесь, но может быть модифицировано в пределах рамок и эквивалентов любого пункта(ов) формулы изобретения. Все публикации и патенты, цитированные здесь, включены сюда полностью путем отсылки.
Изобретение относится к фармацевтической композиции для лечения или профилактики эпилепсии, боли, депрессии, тревоги, психозов, обмороков, гипокинезии, внутричерепных нарушений, нейродегенеративных заболеваний, паники, воспалительного заболевания, бессонницы, желудочно-кишечных расстройств, приливов, синдрома усталых ног, недержания мочи или синдрома отмены алкоголя у пациента, нуждающегося в таком лечении, включающей терапевтически эффективное количество кристаллической 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты и фармацевтически приемлемый носитель, в которой кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерные пики абсорбции при 7,0°±0,3°, 8,2°±0,3°, 10,5°±0,3°, 12,8°±0,3°, 14,9°±0,3° и 16,4°+0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα. Технический результат - кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота, обладающая хорошими физико-химическими свойствами для процессов фармацевтического производства. 2 н. и 36 з.п. ф-лы, 2 ил.
1. Фармацевтическая композиция для лечения или профилактики эпилепсии, боли, депрессии, тревоги, психозов, обмороков, гипокинезии, внутричерепных нарушений, нейродегенеративных заболеваний, паники, воспалительного заболевания, бессонницы, желудочно-кишечных расстройств, приливов, синдрома усталых ног, недержания мочи или синдрома отмены алкоголя у пациента, нуждающегося в таком лечении, включающая терапевтически эффективное количество кристаллической 1-{[(α-изобутаноилоксиэтокси)карбонил] аминометил}-1-циклогексануксусной кислоты, и фармацевтически приемлемый носитель, в которой кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерные пики абсорбции при 7,0°±0,3°, 8,2°±0,3°, 10,5°±0,3°, 12,8°±0,3°, 14,9°±0,3° и 16,4°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
2. Фармацевтическая композиция по п.1, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет дифрактограмму рентгеновских лучей на порошке при использовании излучения Сu Кα, показанную на Фиг.1.
3. Фармацевтическая композиция по п.1 или 2, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет точку плавления в интервале между приблизительно 63°С и приблизительно 64°С при определении методом дифференциальной сканирующей калориметрии при скорости сканирования 5°С/мин.
4. Фармацевтическая композиция по п.1, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерный пик абсорбции при 17,9°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
5. Фармацевтическая композиция по п.1 или 4, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерный пик абсорбции при 18,1°±0,3° на дифрактограмме рентгеновских лучей на порошке при использований излучения Сu Кα.
6. Фармацевтическая композиция по любому из пп.1, 4 и 5, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерный пик абсорбиии при 18,9°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
7. Фармацевтическая композиция по любому из пп.1 и 4-6, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерный пик абсорбции при 20,9°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
8. Фармацевтическая композиция по любому из пп.1 и 4-7, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерный пик абсорбции при 23,3°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
9. Фармацевтическая композиция по любому из пп.1 и 4-8, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерный пик абсорбции при 25,3°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
10. Фармацевтическая композиция по любому из пп.1 и 4-9, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерный пик абсорбции при 26,6°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
11. Фармацевтическая композиция по п.1, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерные пики абсорбции при 17,9°±0,3°, 18,9°±0,3°, 20,9°±0,3°, 23,3°±0,3°, 25,3°±0,3° и 26,6°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
12. Фармацевтическая композиция по п.1, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерные пики абсорбции при 18,1°±0,3°, 18,9°±0,3°, 20,9°±0,3°, 23,3°±0,3°, 25,3°±0,3° и 26,6°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
13. Фармацевтическая композиция по п.1, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерные пики абсорбции при 17,9°±0,3°, 18,1°±0,3°, 18,9°±0,3°, 20,9°±0,3°, 23,3°±0,3°, 25,3°±0,3° и 26,6°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
14. Фармацевтическая композиция по любому из пп.1-13, представляющая собой пероральную лекарственную форму с замедленным высвобождением.
15. Применение кристаллической 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусной кислоты для изготовления фармацевтической композиции для лечения или профилактики эпилепсии, боли, депрессии, тревоги, психозов, обмороков, гипокинезии, внутричерепных нарушений, нейродегенеративных заболеваний, паники, воспалительного заболевания, бессонницы, желудочно-кишечных расстройств, приливов, синдрома усталых ног, недержания мочи или синдрома отмены алкоголя, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерные пики абсорбции при 7,0°±0,3°, 8,2°±0,3°, 10,5°±0,3°, 12,8°±0,3°, 14,9°±0,3° и 16,4°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
16. Применение по п.15, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет дифрактограмму рентгеновских лучей на порошке при использовании излучения Сu Кα, показанную на Фиг.1.
17. Применение по п.15 или 16, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет точку плавления в интервале между приблизительно 63°С и приблизительно 64°С при определении методом дифференциальной сканирующей калориметрии при скорости сканирования 5°С/мин.
18. Применение по п.15, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерный пик абсорбции при 17,9°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
19. Применение по п.15 или 18, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерный пик абсорбции при 18,1°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
20. Применение по любому из пп.15, 18 и 19, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерный пик абсорбции при 18,9°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
21. Применение по любому из пп.15 и 18-20, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерный пик абсорбции при 20,9°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
22. Применение по любому из пп.15 и 18-21, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерный пик абсорбции при 23,3°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
23. Применение по любому из пп.15 и 18-22, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерный пик абсорбции при 25,3°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
24. Применение по любому из пп.15 и 18-23, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерный пик абсорбции при 26,6°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
25. Применение по п.15, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерные пики абсорбции при 17,9°±0,3°, 18,9°±0,3°, 20,9°±0,3°, 23,3°±0,3°, 25,3°±0,3° и 26,6°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
26. Применение по п.15, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерные пики абсорбции при 18,1°±0,3°, 18,9°±0,3°, 20,9°±0,30, 23,3°±0,3°, 25,3°±0,3° и 26,6°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
27. Применение по п.15, где кристаллическая 1-{[(α-изобутаноилоксиэтокси)карбонил]аминометил}-1-циклогексануксусная кислота имеет характерные пики абсорбции при 17,9°±0,3°, 18,1°±0,3°, 18,9°±0,3°, 20,9°±0,3°, 23,3°±0,3°, 25,3°±0,3° и 26,6°±0,3° на дифрактограмме рентгеновских лучей на порошке при использовании излучения Сu Кα.
28. Применение по любому из пп.15-27 для изготовления фармацевтической композиции для лечения или профилактики боли.
29. Применение по п.28, где указанная боль представляет собой нейропатическую боль.
30. Применение по п.28 для изготовления фармацевтической композиции для лечения боли, где указанная боль представляет собой постгерпетическую невралгию.
31. Применение по любому из пп.15-27 для изготовления фармацевтической композиции для лечения или профилактики тревоги.
32. Применение по любому из пп.15-27 для изготовления фармацевтической композиции для лечения или профилактики синдрома отмены алкоголя.
33. Применение по любому из пп.15-27 для изготовления фармацевтической композиции для лечения или профилактики эпилепсии.
34. Применение по любому из пп.15-27 для изготовления фармацевтической композиции для лечения или профилактики бессонницы.
35. Применение по любому из пп.15-27 для изготовления фармацевтической композиции для лечения или профилактики синдрома усталых ног.
36. Применение по любому из пп.15-27 для изготовления фармацевтической композиции для лечения или профилактики приливов.
37. Применение по любому из пп.15-27 для изготовления фармацевтической композиции для лечения или профилактики недержания мочи.
38. Применение по любому из пп.15-36, где фармацевтическая композиция представляет собой пероральную лекарственную форму с замедленным высвобождением.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| US 6818787 A, 16.11.2004 | |||
| ВЕЩЕСТВА, ПОДАВЛЯЮЩИЕ РЕФЛЮКС | 1997 |
|
RU2199316C2 |
| Угрюмов П.Г | |||
| Органический синтез в промышленности | |||
| /Под общей ред | |||
| проф | |||
| А.Л.Клебанского | |||
| - М.: Государственное учебно-педагогическое изд-во министерства просвещения РСФСР, 1955, с.21. | |||
Авторы
Даты
2011-02-20—Публикация
2004-10-14—Подача