Настоящее изобретение относится к солям моносульфату и гемисульфату 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина, к их кристаллическим и аморфным формам и к их применению в фармацевтических препаратах.
2-Хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридин описан ранее в опубликованной патентной заявке РСТ №WO 2004/108701.
2-Хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридин описан как активный при рецепторе mGluR5 для лечения заболеваний, связанных с этим рецептором, таких как острые и/или хронические неврологические расстройства, в частности тревога, или для лечения хронической и острой боли, защиты против повреждения печени, расстройства, вызванного либо лекарством, либо заболеванием, недержания мочи, ожирения, ломкой Х-хромосомы или аутизма.
В первом аспекте настоящее изобретение относится к соли моносульфат и к солям гемисульфатам приведенного ниже соединения:
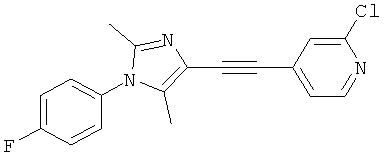
2-Хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридин.
В другом аспекте настоящее изобретение относится к двум различным кристаллическим формам А и В соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
Еще в одном другом аспекте настоящее изобретение относится к аморфной форме соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
Еще в одном другом аспекте настоящее изобретение относится к кристаллической форме А соли гемисульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
Вышеупомянутые соли и их кристаллические и аморфные формы могут отличаться по физическим и химическим свойствам, которые могут быть охарактеризованы инфракрасными спектрами, рентгеновскими порошковыми дифрактограммами, свойствами плавления или температурами стеклования.
В настоящем изобретении также предложены фармацевтические композиции, содержащие вышеупомянутые соли, кристаллические или аморфные формы, и фармацевтически приемлемый носитель. В частности, в настоящем изобретении также предложены фармацевтические композиции, содержащие вышеупомянутые соли, кристаллические или аморфные формы, и один или более чем один фармацевтически приемлемый носитель и/или адъювант.
В соответствии с изобретением вышеупомянутые соли, кристаллические или аморфные формы, можно применять для изготовления лекарственных средств, полезных при борьбе с заболеваниями, основанными на рецепторе mGluR5, или при их предупреждении. Такие заболевания включают острые и/или хронические неврологические расстройства, в частности тревогу, или лечение хронической и острой боли, защиту против повреждения печени, расстройство, вызванное либо лекарством, либо заболеванием, недержание мочи, ожирение, ломкую Х-хромосому или аутизм.
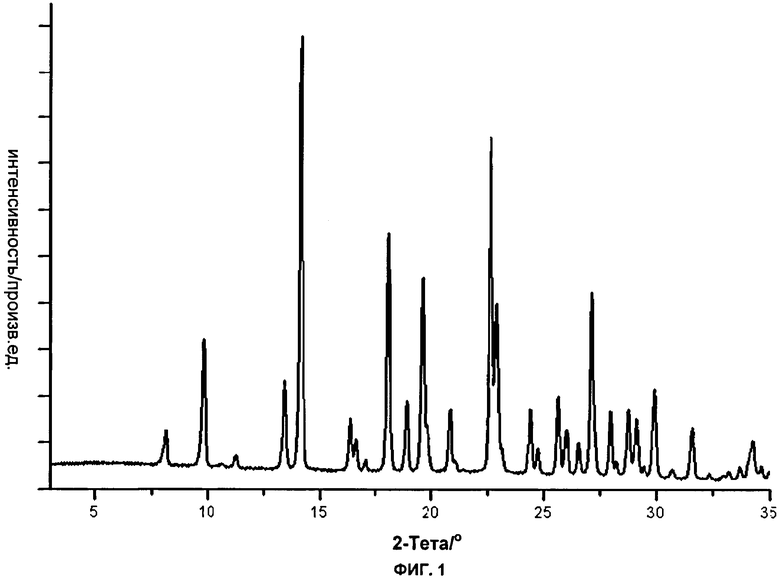
Фиг.1: показана рентгеновская порошковая дифрактограмма (порошковая рентгеновская дифракция, дифрактометр STOE) типичной партии формы А соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
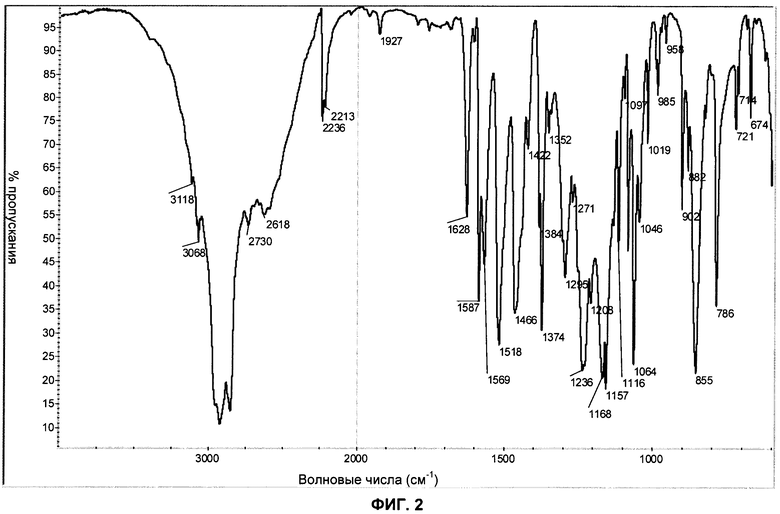
Фиг.2: показан ИК-спектр (инфракрасная спектроскопия, спектрометр Nicolet) типичной партии формы А соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
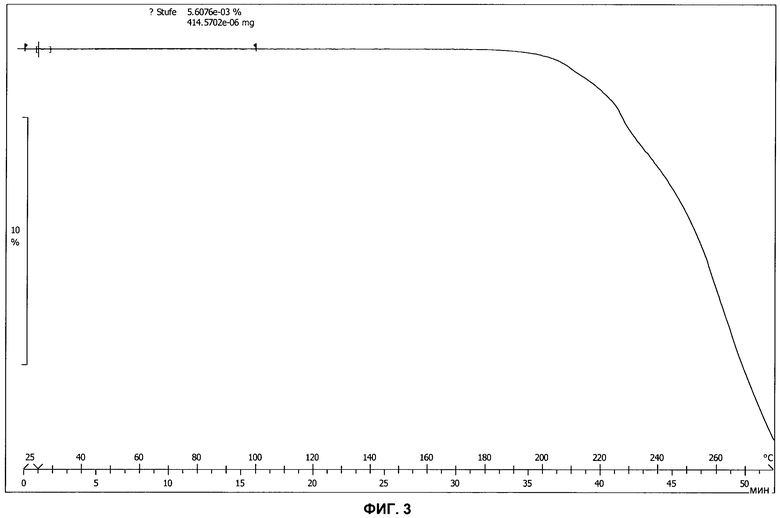
Фиг.3: показана кривая ТГА (термогравиметрический анализ, система Mettler-Toledo) типичной партии формы А соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
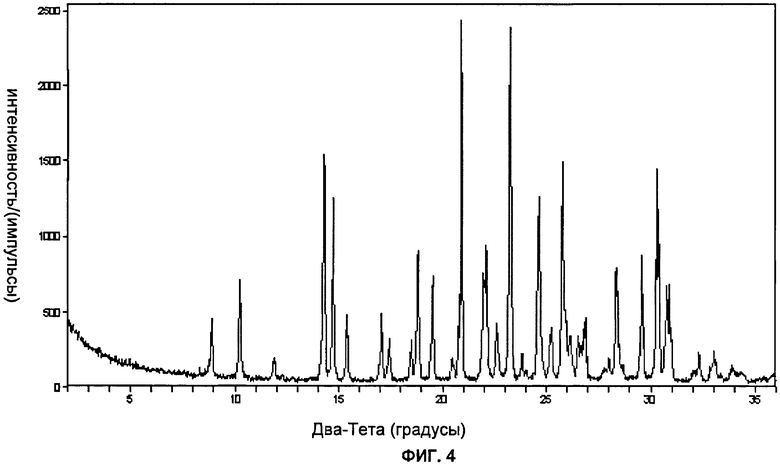
Фиг.4: показана рентгеновская порошковая дифрактограмма (дифрактометр Scintag) типичной партии формы В соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
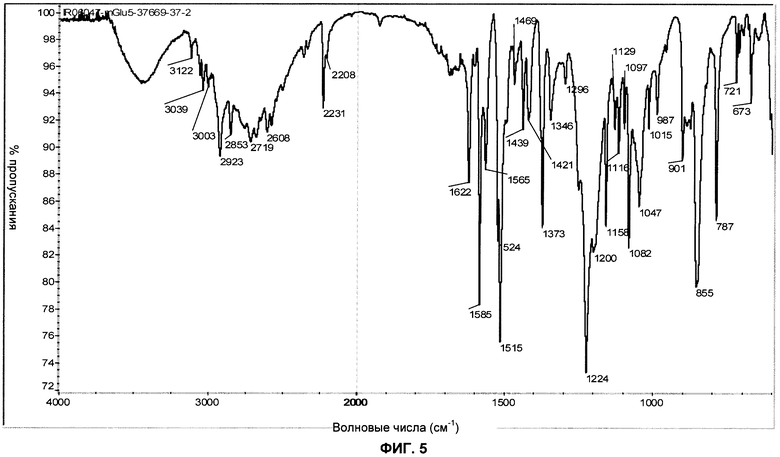
Фиг.5: показан ИК-спектр (инфракрасная спектроскопия, спектрометр Mattson) типичной партии формы В соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
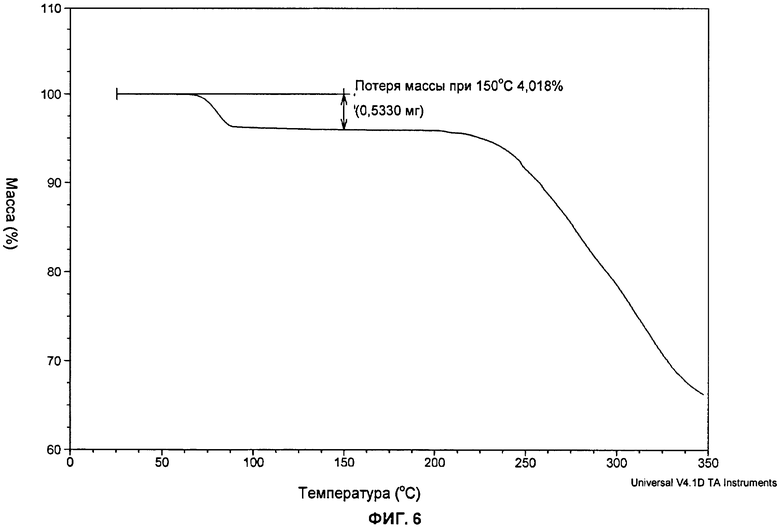
Фиг.6: показана кривая ТГА (термогравиметрический анализ, система ТА Instruments) типичной партии формы В соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
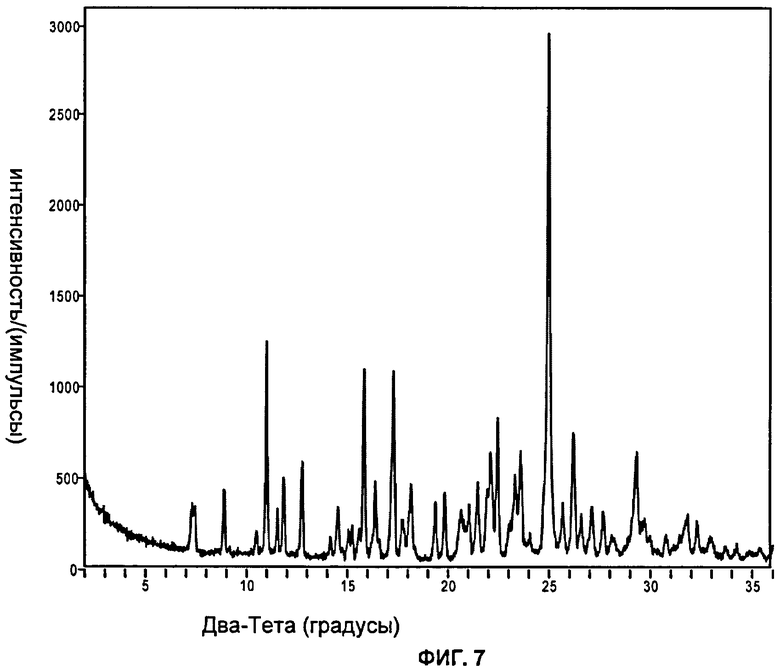
Фиг.7: показана рентгеновская порошковая дифрактограмма (дифрактометр Scintag) типичной партии формы А соли гемисульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
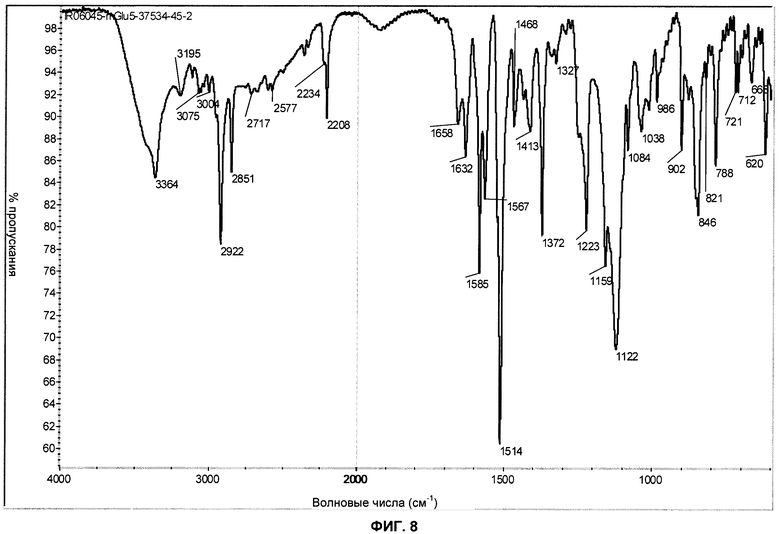
Фиг.8: показан ИК-спектр (инфракрасная спектроскопия, спектрометр Mattson) типичной партии формы А гемисульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
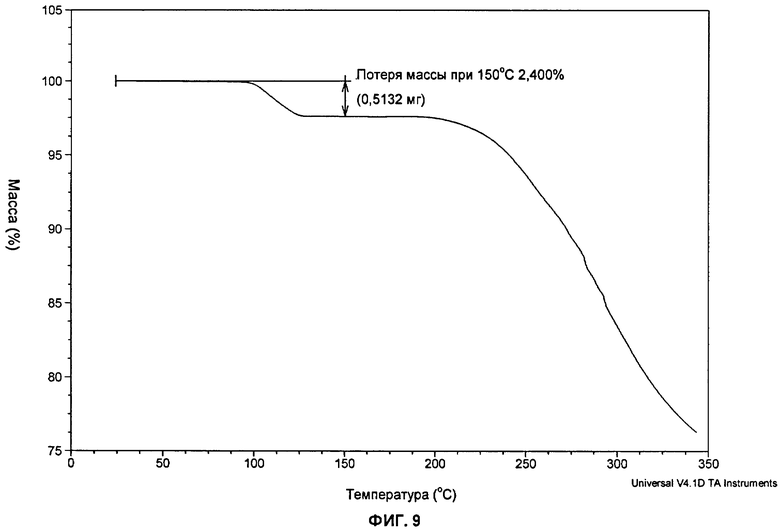
Фиг.9: показана кривая ТГА (термогравиметрический анализ, система ТА Instruments) типичной партии формы А соли гемисульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
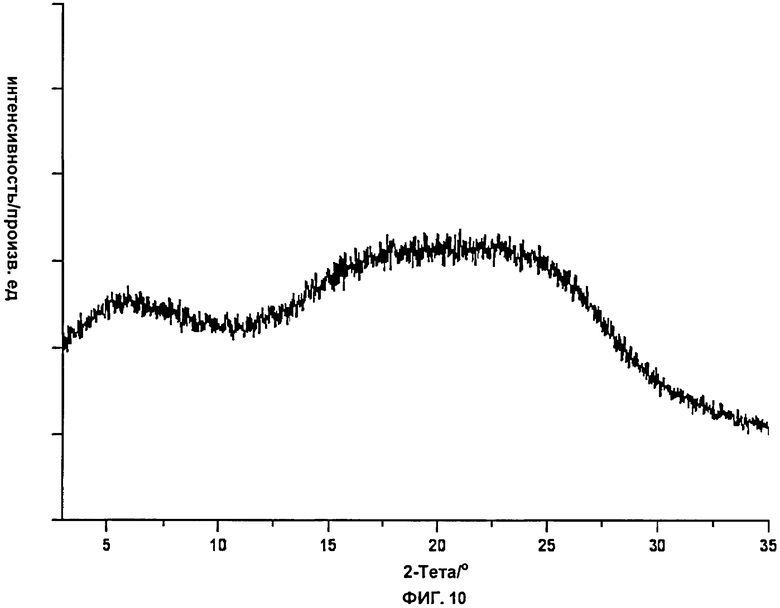
Фиг.10: показана рентгеновская порошковая дифрактограмма (дифрактометр STOE) типичной партии аморфной формы соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
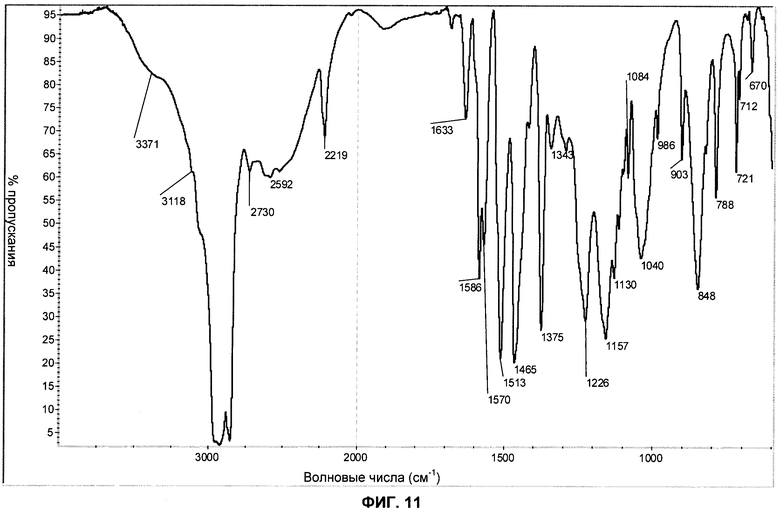
Фиг.11: показан ИК-спектр (инфракрасная спектроскопия, спектрометр Nicolet) типичной партии аморфной формы соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
Как используют здесь, "аморфные формы" или "аморфный" означает вещество, у которого отсутствует дальний порядок, и который не показывает острых пиков рентгеновской дифракции, то есть пика дифракции Брэгга. Рентгеновская порошковая дифрактограмма аморфного вещества характеризуется одним или более чем одним аморфным ореолом.
Закон Брэгга описывает дифракцию кристаллического вещества уравнением:
2d sin тета=n лямбда,
где d=расстояние между парами соседних плоскостей в кристалле по перпендикуляру (межплоскостное расстояние d), тета = угол Брэгга, лямбда = длина волны, и n = целое число.
Когда закон Брэгга выполняется, отраженные лучи находятся в фазе и конструктивно интерферируют таким образом, что пики дифракции Брэгга наблюдают на рентгеновской порошковой дифрактограмме. При углах падения, иных, чем угол Брэгга, отраженные лучи находятся не в фазе, и происходит деструктивная интерференция или аннулирование. Аморфное вещество не удовлетворяет закону Брэгга, и на рентгеновской порошковой дифрактограмме наблюдают отсутствие пиков дифракции Брэгга.
"Аморфный ореол" представляет собой максимум дифракции на рентгеновской порошковой дифрактограмме аморфного вещества примерно формы колокола. FWHM аморфного ореола составляет более чем два градуса в 2-тета.
"FWHM" означает полную ширину на половине максимума (от англ. full width at half maximum), которая представляет собой ширину пика, появляющегося на рентгеновской порошковой дифрактограмме при половине его высоты.
Термин "аморфная форма соли моносульфат" используют здесь как сокращение для обозначения аморфной формы соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
Термин "АФИ" используют здесь как акроним активного фармацевтического ингредиента.
Термин "форма А соли моносульфат" используют здесь как сокращение для обозначения кристаллической формы А соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
Термин "форма А соли гемисульфат" используют здесь как сокращение для обозначения кристаллической формы А соли гемисульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
Термин "форма В соли моносульфат" используют здесь как сокращение для обозначения кристаллической формы В соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
Термин "свободное основание" используют здесь как сокращение для обозначения свободного основания 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
"ИПА" используют здесь как акроним 2-пропанола.
'АЦН' используют здесь как акроним ацетонитрила.
"ИК" используют здесь как акроним Инфракрасный, следовательно, "ИК-спектр" означает Инфракрасный спектр. ИК-спектры записывали с пленки суспензии Nujol примерно 5 мг образца и небольшое количество Nujol между двумя пластинами хлорида натрия, где спектрометр FTIR (инфракрасный спектр с Фурье-преобразованием) находится в трансмиссии. Спектрометр представляет собой Nicolet™ 20SXB или эквивалентный (разрешение 2 см-1, 32 или более объединенные развертки, детектор МСТ).
Альтернативно ИК-спектры записывали с диска KBr примерно с 0,6 мг образца и 160 мг KBr. В этом случае спектрометр представляет собой систему Mattson Galaxy 5000 FTIR (разрешение 2 см-1, 32 или более объединенные развертки).
"Фармацевтически приемлемый", как, например, фармацевтически приемлемые носители, эксципиенты, адъюванты, консерванты, солюбилизаторы, стабилизаторы, увлажняющие агенты, эмульгаторы, подсластители, красители, корригенты, соли для варьирования осмотического давления, буферы, маскирующие агенты или антиоксиданты и т.д., означает фармакологически приемлемый и, по существу, нетоксичный для субъекта, которому вводят конкретное соединение.
"Фармацевтически приемлемый", следовательно, означает, по существу, нетоксичный для субъекта, которому вводят фармацевтически приемлемое вещество.
"ПРД" используют здесь как акроним порошковой рентгеновской дифракции. Рентгеновские порошковые дифрактограммы записывали в условиях окружающей среды в трансмиссионной геометрии на дифрактометре STOE STADI Р (излучение Cu Кα, первичный монохроматор, чувствительный элемент датчика положения, угловой диапазон от 3 до 42 2Тета (градусы), суммарное время измерения примерно 60 минут). Образцы готовили и анализировали без дополнительной обработки (например, измельчения или просеивания) вещества.
Альтернативно рентгеновские порошковые дифрактограммы получали на порошковом рентгеновском дифрактометре Scintag X1, оборудованном запаянным источником излучения меди Ка1. Образцы сканировали от 2° до 36° 2θ (от 2 до 36 2Тета (градусы)) со скоростью 1° в минуту с шириной щели падающего луча 2 и 4 мм и шириной щели дифракции луча 0,3 и 0,2 мм.
Для анализа монокристаллической структуры монокристалл закрепляли на петле на гониометре и измеряли в условиях окружающей среды. Альтернативно кристалл охлаждали в потоке азота во время измерения. Данные собирали на сигнальной пластине дифракционной системы (Imaging Plate Diffraction System, IPDS) STOE от STOE (Дармштадт). В данном случае для сбора данных использовали излучение Мо длины волны 0,71 А. Данные обрабатывали программным обеспечением STOE IPDS. Кристаллическую структуру разделяли и уточняли с помощью стандартного кристаллографического программного обеспечения. В этом случае использовали программу ShelXTL от Bruker AXS (Карлсруэ).
Альтернативно данные интенсивности дифракции монокристалла измеряли в условиях окружающей среды на дифрактометре Bruker SMART APEX™ (излучение Мо Кα, λ=0,71 Å). Интегрирование блока данных необработанных данных цифрового детектора проводили с помощью приведенных ниже программных обеспечений: SMART™, версия 5.630, SAINT™+, версия 6.45, и SADABS™, версия 2.10, Bruker Analytical X-ray Systems, Inc., Мэдисон, Висконсин, США, 2003. Прямые методы разрешения структуры, вычисления разности Фурье и уточнение полной матрицы наименьших квадратов против F2 проводили в соответствии с Sheldrick, G.M.SHELXTL™, версия 6,14; Bruker Analytical X-ray Systems, Inc., Мэдисон, Висконсин, США, 2000.
"ТГА" используют здесь как акроним термогравиметрического анализа. Кривые ТГА измеряли на термогравиметрическом анализаторе Mettler-Toledo™ (TGA850/SDTA). Тесты на пригодность системы и калибровки проводили в соответствии с рабочей методикой внутренних стандартов.
Для термогравиметрических анализов примерно 5-10 мг образца помещали в алюминиевые кюветы, точно взвешивали и герметично закрывали перфорированными крышками. Перед измерением крышки автоматически протыкались с получением в результате примерно 1,5 мм отверстий малого диаметра. Затем образцы нагревали в потоке азота примерно 50 мл/мин, используя скорость нагревания 5 К/мин вплоть до 280°С.
Альтернативно термогравиметрический анализ проводили, используя Hi-Res 2950 TGA от фирмы ТА Instruments. Скорость нагревания составляла 10°С/мин с продуванием азотом, поддерживаемым на протяжении всего измерения.
"Терапевтически эффективное количество" означает количество, которое является эффективным для предупреждения, облегчения или ослабления симптомов заболевания или для продления жизни субъекта, подлежащего лечению.
Фармацевтические композиции по изобретению, в дополнение к одной из солей, кристаллических или аморфных форм согласно изобретению, упомянутые здесь выше, могут содержать фармацевтически приемлемый носитель или более чем один фармацевтически приемлемый носитель. Пригодные фармацевтически приемлемые носители включают фармацевтически инертные, неорганические и органические носители. Лактозу, кукурузный крахмал или его производные, тальк, стеариновые кислоты или их соли и тому подобное можно использовать, например, в качестве таких носителей для таблеток, таблеток с покрытием, драже и твердых желатиновых капсул. Пригодными носителями для мягких желатиновых капсул являются, например, растительные масла, воски, жиры, полутвердые и жидкие полиолы и тому подобное. В зависимости от природы активного вещества никаких носителей, однако, обычно не требуется в случае мягких желатиновых капсул. Пригодные носители для растворов включают, например, воду, полиолы, сахарозу, инвертный сахар, глюкозу и тому подобное.
Получение свободного основания 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина ранее описано в опубликованной патентной заявке РСТ №WO 2004/108701, содержание которой включено здесь путем ссылки.
Как уже упомянуто здесь выше, настоящее изобретение относится к новым солям и к кристаллической и аморфной форме этих солей приведенного ниже соединения:
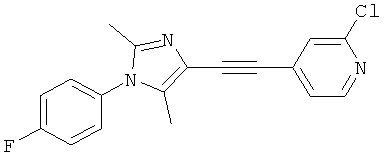
2-Хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридин.
Было обнаружено, что 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридин может быть выделен, в зависимости от способа получения, в виде соли моносульфат или в виде соли гемисульфат.
Форма А и форма В соли моносульфат, а также аморфная форма может быть выделена из соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
Форма А соли гемисульфат может быть получена из соли гемисульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
Соль моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина может быть получена путем образования соли 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина с серной кислотой в 2-пропаноле с последующим спонтанным осаждением.
Форма А соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина представляет собой свободную от растворителя кристаллическую форму.
Форма А соли моносульфат может быть получена путем образования соли 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина с серной кислотой в 2-пропаноле с последующим спонтанным осаждением или путем перекристаллизации формы А соли моносульфат в растворителях, включающих, но не ограниченных ими, АЦН, АЦН/вода, метанол, этанол, ИПА, уксусную кислоту, 1-октанол, ИПА/49% серная кислота (10:1, об./об.).
Форма А соли моносульфат может быть охарактеризована по меньшей мере тремя пиками, выбранными из приведенных ниже пиков рентгеновской дифракции, полученных с CuKα излучением при 2θ (2Тета (градусы)) = 9.8, 13.4, 14.2, 18.1, 18.9, 19.6, 22.6, 22.9, 25.7, 27.1 и 29.9 (±0,2° 2Тета).
Форма А соли моносульфат может быть охарактеризована по меньшей мере пятью пиками, выбранными из приведенных ниже пиков рентгеновской дифракции, полученных с CuKα излучение при 2θ (2Тета (градусы))=9.8, 13.4, 14.2, 18.1, 18.9, 19.6, 22.6, 22.9, 25.7, 27.1 и 29.9 (±0,2° 2Тета).
Форма А соли моносульфат может быть охарактеризована по меньшей мере семью пиками, выбранными из приведенных ниже пиков рентгеновской дифракции, полученных с CuKα излучение при 2θ (2Тета (градусы)) = 9.8, 13.4, 14.2, 18.1,18.9, 19.6, 22.6, 22.9, 25.7, 27.1 и 29,9 (±0,2° 2Тета).
Форма А соли моносульфат может быть также охарактеризована приведенными ниже пиками рентгеновской дифракции, полученных с CuKα излучение при 2θ (2Тета (градусы)) = 9.8, 13.4, 14.2, 18.1, 18.9, 19.6, 22.6, 22.9, 25.7, 27.1 и 29.9 (±0.2° 2Тета).
Форма А соли моносульфат может быть также охарактеризована рентгеновской порошковой дифрактограммой, показанной на фиг.1.
Форма А соли моносульфат может быть также охарактеризована инфракрасным спектром, имеющим отчетливые полосы при 3068, 2730, 2618, 2236, 2213, 1628, 1587, 1569, 1518, 1384, 1374, 1295, 1236, 1168, 1157, 1116, 1064, 1019, 902, 855, 786 и 674 см-1 (±3 см-1).
Форма А соли моносульфат может быть также охарактеризована инфракрасным спектром, показанным на 2.
Форма А соли моносульфат представляет собой свободную от растворителя форму, поскольку значимой потери массы не наблюдают на кривой ТГА перед распадом, как показано на фиг.3.
Как уже упомянуто выше, все эти характеристики представлены на фиг.1-3 здесь ниже.
Проводили рентгеновский анализ монокристалла формы А соли моносульфат. В Таблице 1 перечислены в качестве примера некоторые данные кристаллической структуры. Было обнаружено, что кристаллическая форма А соли моносульфат представляет собой ангидратную форму соли моносульфат, как определено путем анализа монокристалла. Экспериментальная рентгеновская порошковая дифрактограмма, снятая с полученной формы А соли моносульфат, находится в отличном соответствии с моделируемой дифрактограммой, вычисленной на основании атомных координат на основании анализа монокристаллической структуры, указывая на то, что форма А соли моносульфат представляет собой чистую кристаллическую фазу. В структуре формы А соли моносульфат фторбензольное кольцо почти перпендикулярно имидазольному кольцу, на что указывает двугранный угол 90,7°. Гидроксильная группа бисульфатного аниона образует межмолекулярную водородную связь с атомом кислорода соседнего бисульфатного аниона. Этот бисульфатный анион также служит в качестве акцептора водородной связи от протонированного атома азота имидазола.
Форма В соли моносульфат представляет собой моногидратную кристаллическую форму.
Форма В соли моносульфат может быть получена путем уравновешивания растворителем формы А соли моносульфат в ИПА/воде (например, 3:1 об./об.). Форма В соли моносульфат может быть также получена путем перекристаллизации формы А соли моносульфат в ИПА/воде (например, 3:1 об./об.). Форма В соли моносульфат может быть, кроме того, получена при гидролизе формы А соли моносульфат, например, в водной серной кислоте.
Форма В соли моносульфат может быть охарактеризована по меньшей мере тремя пиками, выбранными из приведенных ниже пиков рентгеновской дифракции, полученных с CuKα излучением при 2θ (2Тета (градусы)) = 8.9, 10.2, 14.3, 14.7, 15.4, 17.1, 18.8, 19.5, 20.9, 22.5 и 23.8 (±0,2° 2Тета).
Форма В соли моносульфат может быть охарактеризована по меньшей мере пятью пиками, выбранными из приведенных ниже пиков рентгеновской дифракции, полученных с CuKα излучением при 2θ (2Тета (градусы)) = 8.9, 10.2, 14.3, 14.7, 15.4, 17.1, 18.8, 19.5, 20.9, 22.5 и 23.8 (±0,2° 2Тета).
Форма В соли моносульфат может быть охарактеризована по меньшей мере семью пиками, выбранными из приведенных ниже пиков рентгеновской дифракции, полученных с CuKα излучением при 2θ (2Тета (градусы)) = 8.9, 10.2, 14.3, 14.7, 15.4, 17.1, 18.8, 19.5, 20.9, 22.5 и 23.8 (±0,2° 2Тета).
Форма В соли моносульфат может быть также охарактеризована приведенными ниже пиками, полученными с CuKα излучением при 2θ (2Тета (градусы)) = 8.9, 10.2, 14.3, 14.7, 15.4, 17.1, 18.8, 19.5, 20.9, 22.5 и 23.8 (±0,2° 2Тета).
Форма В соли моносульфат может быть также охарактеризована рентгеновской порошковой дифрактограммой, показанной на фиг.4.
Форма В соли моносульфат может быть также охарактеризована инфракрасным спектром, имеющим отчетливые полосы при 3122, 3039, 3003, 2923, 2853, 2719, 2608, 2231, 1622, 1585, 1565, 1515, 1439, 1373, 1346, 1224, 1158, 1116, 1082, 1047, 1015, 987, 901, 787 и 673 (±3 см-1).
Форма В соли моносульфат может быть также охарактеризована инфракрасным спектром, показанным на фиг.5.
Форма В соли моносульфат представляет собой моногидрат с соответствующей потерей массы на кривой ТГА, как показано на фиг.6.
Как упомянуто здесь выше, все три характеристики показаны на фиг.4-6 здесь ниже.
Проводили рентгеновский анализ монокристалла при комнатной температуре формы В соли моносульфат. В качестве примера в Таблице 2 перечислены некоторые данные кристаллической структуры.
Было обнаружено, что форма В соли моносульфат представляет собой моногидрат соли моносульфат, как определено путем анализа монокристалла. Экспериментальная рентгеновская порошковая дифрактограмма, снятая с полученной формы В соли моносульфат находится в отличном соответствии с моделируемой дифрактограммой, вычисленной на основании атомных координат на основании анализа монокристаллической структуры, указывая на то, что форма В соли моносульфат представляет собой чистую кристаллическую фазу. Было обнаружено, что в структуре формы В 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина двугранный угол между фторбензольным кольцом и имидазольным кольцом составляет примерно 77,3°. Протонированный атом азота имидазола образует межмолекулярную водородную связь с бисульфатным анионом. В то же время, бисульфатный анион также вовлечен в сети водородного связывания с атомом азота хлорпиридина и молекулой воды.
Аморфная форма соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина может быть получена из метанольного раствора при быстром выпаривании примерно при 65°С в вакууме.
Аморфная форма соли моносульфат может быть охарактеризована отсутствием отчетливых пиков рентгеновской дифракции на ее рентгеновской порошковой дифрактограмме; и/или инфракрасным спектром, имеющим отчетливые полосы при 2730, 2592, 2219, 1633, 1586, 1570, 1513, 1375, 1343, 1293, 1226, 1157, 1130, 1084, 1040, 986, 903, 848, 788, 712 и 670 см-1 (±3 см-1).
Аморфная форма соли моносульфат может быть также охарактеризована инфракрасным спектром, показанным на фиг.11.
Как упомянуто здесь выше, все эти характеристики показаны на фиг.10-11 здесь ниже.
Соль гемисульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина может быть получена путем уравновешивания растворителем формы А соли моносульфат в воде.
Форма А соли гемисульфат может быть получена путем уравновешивания растворителем формы А соли моносульфат в воде. Она также может быть получена путем перекристаллизации или гидролиза формы А соли моносульфат в системах растворителей, включающих, но не ограниченных ими, воду, воду/метанол (например, 4:1, об./об.), воду/этанол (например, 4:1, об./об.), воду/2-пропанол (например, 3:1, об./об.).
Форма А соли гемисульфат представляет собой кристаллическую полугидратную форму приведенной ниже соли 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина с серной кислотой (2:1) (соли гемисульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина свободного основания):
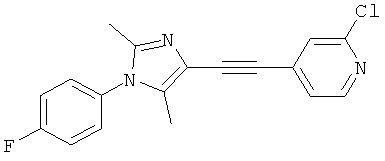
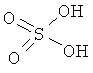
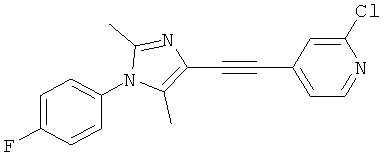
Форма А соли гемисульфат может быть охарактеризована по меньшей мере тремя пиками, выбранными из приведенных ниже пиков рентгеновской дифракции, полученных с излучением CuKα при 2θ (2Тета (градусы)) = 7.4, 8.9, 11.0, 11.8, 12.8, 15.8, 17.3, 18.1, 19.8, 25.0 и 26.2 (±0,2° 2Тета).
Форма А соли гемисульфат может быть охарактеризована по меньшей мере пятью пиками, выбранными из приведенных ниже пиков рентгеновской дифракции, полученных с излучением CuKα при 2θ (2Тета (градусы)) = 7.4, 8.9, 11.0, 11.8, 12.8, 15.8, 17.3, 18.1, 19.8, 25.0 и 26.2 (±0,2° 2Тета).
Форма А соли гемисульфат может быть охарактеризована по меньшей мере семью пиками, выбранными из приведенных ниже пиков рентгеновской дифракции, полученных с излучением CuKα при 2θ (2Тета (градусы)) = 7.4, 8.9, 11.0, 11.8, 12.8, 15.8, 17.3, 18.1,19.8, 25.0 и 26,2 (±0,2° 2Тета).
Форма А соли гемисульфат может быть также охарактеризована приведенными ниже пиками рентгеновской дифракции, полученных с излучением CuKα при 2θ (2Тета (градусы)) = 7.4, 8.9, 11.0, 11.8, 12.8, 15.8, 17.3, 18.1, 19.8, 25.0 и 26.2 (±0,2° 2Тета).
Форма А соли гемисульфат может быть также охарактеризована рентгеновской порошковой дифрактограммой, показанной на фиг.7.
Форма А соли гемисульфат может быть также охарактеризована инфракрасным спектром, имеющим отчетливые полосы при 3364, 3075, 3004, 2922, 2851, 2717, 2208, 1658, 1632, 1585, 1567, 1514, 1413, 1372, 1159, 1122, 1038, 986, 902, 846, 821, 788, 721, 712 и 668 (±3 см-1).
Форма А соли гемисульфат может быть также охарактеризована инфракрасным спектром, показанным на фиг.8.
Форма А соли гемисульфат представляет собой полугидрат с соответствующей потерей массы на кривой ТГА, как показано на фиг.9.
Как уже упомянуто выше, все эти характеристики показаны на фиг.7-9 здесь ниже.
Проводили рентгеновский анализ монокристалла при низкой и при комнатной температуре формы А соли гемисульфат. В Таблице 3 перечислены в качестве примера некоторые данные кристаллической структуры.
Было обнаружено, что форма А соли гемисульфат представляет собой полугидрат гемисульфата, как определено путем анализа монокристаллической структуры. В структуре формы А соли гемисульфат существует две молекулы АФИ в асимметрической ячейке. Снятая экспериментальная рентгеновская порошковая дифракгограмма соответствовала моделируемой дифрактограмме, вычисленной на основании атомных координат на основании анализа монокристаллической структуры, который указывает на чистую кристаллическую фазу. Конформации этих двух молекул АФИ несколько отличаются, на что указывают различия двугранных углов между фторбензольным кольцом и имидазольным кольцом (примерно 70° по сравнению с примерно 61°); однако, в обеих молекулах хлорпиридиновые кольца лежат почти в одной плоскости с имидазольным кольцом, что продемонстрировано очень малыми двугранными углами (примерно 5° по сравнению примерно с 6°). Протонированные атомы азота имидазола образуют межмолекулярные водородные связи с сульфатным анионом и молекулой воды. В то же время, молекула воды также вовлечена в водородное связывание с двумя сульфатными анионами.
Соль можно включать при низких или высоких концентрациях в композицию, дополнительно содержащую обычные фармацевтически приемлемые адъюванты, известные в данной области техники.
В настоящем изобретении также предложены фармацевтические композиции, содержащие один или более чем один из приведенных ниже препаратов:
- соль моно- или гемисульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина;
- форму А или В соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина;
- форму А соли гемисульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1H-имидазол-4-илэтинил]-пиридина;
- аморфную форму 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина;
и фармацевтически приемлемый носитель.
Кроме того, фармацевтические композиции могут содержать более чем один фармацевтически приемлемый носитель и/или один или более чем один адъювант.
Эти фармацевтические композиции могут находиться в форме таблеток, таблеток с покрытием, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий. В изобретении также предложен способ изготовления таких композиций, при котором приводят вышеупомянутые модификации и формы в форму введения галенова препарата вместе с одним или более чем одним терапевтически инертным носителем.
Кроме того, фармацевтические композиции могут содержать фармацевтически приемлемые консерванты, солюбилизаторы, стабилизаторы, увлажняющие агенты, эмульгаторы, подсластители, красители, корригенты, соли для варьирования осмотического давления, буферы, маскирующие агенты или антиоксиданты. Они также содержат еще другие терапевтически ценные вещества.
В одном воплощении изобретения соль моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина содержит по меньшей мере 70% кристаллического полиморфа формы А или В, как описано выше, предпочтительно по меньшей мере 90%, более предпочтительно по меньшей мере 95% и наиболее предпочтительно по меньшей мере 99%.
В одном воплощении изобретения соль моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина содержит по меньшей мере 70% аморфной формы, как описано выше, предпочтительно по меньшей мере 90%, более предпочтительно по меньшей мере 95% и наиболее предпочтительно по меньшей мере 99%.
В одном воплощении изобретения соль гемисульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина содержит по меньшей мере 70% кристаллического полиморфа формы А, как описано выше, предпочтительно по меньшей мере 90%, более предпочтительно по меньшей мере 95% и наиболее предпочтительно по меньшей мере 99%.
В соответствии с изобретением соли, кристаллические или аморфные формы согласно изобретению, упомянутые здесь выше, можно применять для изготовления лекарств, полезных при лечении или предупреждении заболеваний, при которых играет роль рецептор mGluR5. Такие заболевания включают острые и/или хронические неврологические расстройства, в частности тревогу, или для лечения хронической и острой боли, защиту против повреждения печени, расстройство, индуцированное либо лекарством, либо заболеванием, недержание мочи, ожирение, ломкую Х-хромосому или аутизм.
Соли и кристаллические или аморфные формы соединений по изобретению можно применять при способе лечения заболевания, выбранного из группы, состоящей из острых и/или хронических неврологических расстройств, в частности тревоги, или для лечения хронической и острой боли, защиты против повреждения печени, расстройства, индуцированного либо лекарством, либо заболеванием, недержания мочи, ожирения, ломкой Х-хромосомы или аутизма, при котором индивидууму вводят эффективное количество одного препарата, выбранного из группы, состоящей из солей, кристаллических или аморфных форм согласно изобретению, упомянутых выше.
Дозировка, при которой вводят соли, кристаллические или аморфные формы согласно изобретению, может варьировать в широких пределах и, конечно, должна быть отрегулирована по индивидуальным потребностям в каждом конкретном случае. В случае перорального введения дозировка для взрослых может варьировать от примерно 0,01 мг до примерно 1000 мг, предпочтительно от примерно 0,05 мг до примерно 20 мг, и еще более предпочтительно от примерно 0,5 мг до примерно 5 мг в сутки. Суточную дозировку можно вводить в виде единой дозы или в дробных дозах и, кроме того, верхний предел может быть также превышен, когда это считают показанным.
В следующем воплощении дозировка, при которой вводят соли, кристаллические или аморфные формы согласно изобретению, находится в диапазоне от примерно 0,001 мг до примерно 5 мг, предпочтительно от примерно 0,001 мг до примерно 3 мг, от примерно 0,001 до примерно 2 мг или от примерно 0,001 до примерно 1 мг.
Пример 1
Получение формы А соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина
Общее
Форма А соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина может быть образована при образовании соли с затравливанием или без затравливания формой А соли моносульфат в подходящей системе растворителей, как, например, 2-пропанол/вода, или путем перекристаллизации формы А соли моносульфат в растворителях, включающих, но не ограниченных ими, ацетонитрил, ацетонитрил/воду, метанол, этанол, 2-пропанол, уксусную кислоту, 1-октанол, 2-пропанол/49% серную кислоту (10:1, об./об.).
Методика получения
61,0 г 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина растворяли в 610 мл 2-пропанола. Раствор фильтровали, и фильтр ополаскивали 31 мл 2-пропанола. К объединенным растворам добавляли по каплям смесь 30 мл воды и 18,91 г серной кислоты (97%). Раствор охлаждали до 0-5°С. Затравливание проводили при 58°С по необходимости. Твердые остатки фильтровали, промывали 2-пропанолом (0-5°С) и высушивали при 50°С/<1 мбар в течение 18 ч. Выход: 69,1 г (87,1%).
Кристаллы для затравливания формы А могут быть получены при охлаждающей кристаллизации горячего раствора 250 мг соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина в 10 мл 2-пропанола. После охлаждения до 0°С твердые остатки можно фильтровать и высушивать при 50°С в вакууме.
Свойства твердого состояния формы А соли моносульфат
Рентгеновская порошковая дифрактограмма, ИК-спектр и кривая ТГА типичной партии формы А соли моносульфат приведены на фиг.1-3.
Пример 2
Получение формы В соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина
Общее
Форма В соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина может быть получена путем уравновешивания растворителем формы А соли моносульфат в системе растворителей, как, например, 2-пропанол/вода или 1 н. серная кислота, или при охлаждающей кристаллизации с затравливанием соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина в системе растворителей, как, например, 2-пропанол/вода.
Методика получения
300 мг формы А соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина растворяли в 3 мл 2-пропанола и 1 мл воды при 60°С с получением прозрачного раствора. Этот прозрачный раствор затравливали формой В соли моносульфат и герметично закрывали при комнатной температуре. Отдельные кристаллы образовались через 3 суток.
Кристаллы для затравливания могут быть получены путем образования насыщенной суспензии формы А соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина в 2-пропаноле и воде (3:1 об./об.) при комнатной температуре. Суспензию перемешивали при комнатной температуре в течение примерно 3 недель. Твердые вещества фильтровали через стеклянный фильтр с получением кристаллической формы В соли моносульфат в виде влажного кека.
Свойства твердого состояния формы В соли моносульфат
Рентгеновская порошковая дифрактограмма, ИК-спектр и кривая ТГА типичной партии формы В соли моносульфат приведены на фиг.4-6.
Пример 3
Получение формы А соли гемисульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина
Общее
Форма А соли гемисульфат 2-хлор-4-[1-(4-фтор-фенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина может быть получена путем уравновешивания растворителя формы А соли моносульфат в растворителях, таких как, например, вода. Она может быть также получена путем перекристаллизации или гидролиза формы А соли моносульфат в системе растворителей, включающей, но не ограниченной ими, воду, воду/метанол (например, 4:1, об./об.), воду/этанол (например, 4:1, об./об.), воду/2-пропанол (например, 3:1, об./об.).
Методика получения
41 г формы А моносульфата 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина смешивали со 128 г воды. Суспензию перемешивали при комнатной температуре в течение 2-16 ч. После того как вся форма А соли моносульфат была превращена в соль гемисульфат, кристаллы собирали фильтрованием и ополаскивали водой. Влажный кек высушивали при 40°С в вакуумной печи в течение 48 ч. Выход составлял ~93%.
Свойства твердого состояния формы А соли гемисульфат
Рентгеновская порошковая дифрактограмма, ИК-спектр и кривая ТГА типичной партии формы А соли гемисульфат приведены на фиг.7-9.
Пример 4
Получение аморфной формы соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина
Образование аморфной формы
Аморфная соль моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина может быть получена при быстром выпаривании раствора в подходящем растворителе, предпочтительно в метаноле.
Быстрое выпаривание
0,53 г 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина растворяли в 10 мл метанола примерно при 65°С. После полного выпаривания растворителя в вакууме твердое вещество (пену) дополнительно высушивали примерно при 50°С/5-20 мбар в течение 18 ч. Анализ выявил аморфный 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридин.
Свойства твердого состояния аморфной формы
Рентгеновская порошковая дифрактограмма и ИК-спектр аморфной формы приведены на фиг.10-11.
Препарат
Препарат в виде капсулы (влажная грануляция)
Методика изготовления
1. Смешивают п.п.1, 2, 3, 4, 5 и 6 в подходящем смесителе в течение 30 минут.
2. Добавляют п.п.7 и 8 и смешивают в течение 3 минут.
3. Заполняют в подходящую капсулу.
Настоящее изобретение относится к соли моносульфата 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина и к ее кристаллическим формам. Также настоящее изобретение относится к способу получения указанной соли, к фармацевтической композиции на основе указанной соли. Технический результат: получены новые кристаллические формы моносульфата 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина, обладающие активностью в отношении рецептора mGluR5. 8 н. и 12 з.п. ф-лы, 11 ил., 3 табл., 4 пр.
1. Соль моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина.
2. Кристаллическая форма соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина, характеризующаяся по меньшей мере тремя пиками, выбранными из приведенных ниже пиков рентгеновской дифракции, полученных с излучением СuKα при 2θ (2Тета (градусы))=9,8, 13,4, 14,2, 18,1, 18,9, 19,6, 22,6, 22,9, 25,7, 27,1 и 29,9 (±0,2° 2Тета).
3. Кристаллическая форма соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина по п.2, характеризующаяся приведенными ниже пиками рентгеновской дифракции, полученными с излучением СuKα при 2θ (2Тета (градусы))=9,8, 13,4, 14,2, 18,1, 18,9, 19,6, 22,6, 22,9, 25,7, 27,1 и 29,9 (±0,2° 2Тета).
4. Кристаллическая форма соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина по п.2, характеризующаяся рентгеновской порошковой дифрактограммой, показанной на фиг.1.
5. Кристаллическая форма соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина по любому из пп.2-4, характеризующаяся инфракрасным спектром, имеющим отчетливые полосы при 3068, 2730, 2618, 2236, 2213, 1628, 1587, 1569, 1518, 1384, 1374, 1295, 1236, 1168, 1157, 1116, 1064, 1019, 902, 855, 786 и 674 см-1 (±3 см-1).
6. Кристаллическая форма соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина по любому из пп.2-4, характеризующаяся инфракрасным спектром, показанным на фиг.2.
7. Кристаллическая форма соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина, характеризующаяся инфракрасным спектром, имеющим отчетливые полосы при 3068, 2730, 2618, 2236, 2213, 1628, 1587, 1569, 1518, 1384, 1374, 1295, 1236, 1168, 1157, 1116, 1064, 1019, 902, 855, 786 и 674 см-1 (±3 см-1).
8. Кристаллическая форма соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина по п.7, характеризующаяся инфракрасным спектром, показанным на фиг.2.
9. Кристаллическая форма соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина, характеризующаяся по меньшей мере тремя пиками, выбранными из приведенных ниже пиков рентгеновской дифракции, полученных с излучением СuKα при 2θ (2Тета (градусы))=8,9, 10,2, 14,3, 14,7, 15,4, 17,1, 18,8, 19,5, 20,9, 22,5 и 23,8 (±0,2° Тета).
10. Кристаллическая форма соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина по п.9, характеризующаяся приведенными ниже пиками рентгеновской дифракции, полученными с излучением СuKα при 2θ (2Тета (градусы))=8,9, 10,2, 14,3, 14,7, 15,4, 17,1, 18,8, 19,5, 20,9, 22,5 и 23,8 (±0,2° 2Тета).
11. Кристаллическая форма соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина по п.9, характеризующаяся рентгеновской порошковой дифрактограммой, показанной на фиг.4.
12. Кристаллическая форма соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил- 1Н-имидазол-4-илэтинил]-пиридина по любому из пп.9-11, характеризующаяся инфракрасным спектром, имеющим отчетливые полосы при 3122, 3039, 3003, 2923, 2853, 2719, 2608, 2231, 1622, 1585, 1565, 1515, 1439, 1373, 1346, 1224, 1158, 1116, 1082, 1047, 1015, 987, 901, 787 и 673 (±3 см-1).
13. Кристаллическая форма соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина по любому из пп.9-11, характеризующаяся инфракрасным спектром, показанным на фиг.5.
14. Кристаллическая форма соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина, характеризующаяся инфракрасным спектром, имеющим отчетливые полосы при 3122, 3039, 3003, 2923, 2853, 2719, 2608, 2231, 1622, 1585, 1565, 1515, 1439, 1373, 1346, 1224, 1158, 1116, 1082, 1047, 1015, 987, 901, 787 и 673 (±3 см-1).
15. Кристаллическая форма соли моносульфат 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина по п.14, характеризующаяся инфракрасным спектром, показанным на фиг.5.
16. Соединение по п.1, где по меньшей мере 70% составляет кристаллический полиморф по любому из пп.1-15.
17. Фармацевтическая композиция, обладающая активностью в отношении рецептора mGluR5, содержащая соль по п.1, либо кристаллическую форму по любому из пп.2-15 и один или более чем один фармацевтически приемлемый носитель.
18. Способ получения соединения по любому из пп.2-8, включающий стадии
(а) образования соли 2-хлор-4-[1-(4-фторфенил)-2,5-диметил-1Н-имидазол-4-илэтинил]-пиридина с серной кислотой в 2-пропаноле с последующим спонтанным осаждением или
(б) перекристаллизации продукта стадии (а) в АЦН, АЦН/воде, метаноле, этаноле, ИПА, уксусной кислоте, 1-октаноле или ИПА/49% серной кислоте (10:1, об./об.).
19. Способ получения соединения по любому из пп.9-15, включающий
(а) уравновешивание растворителем соединения по любому из пп.2-8 в ИПА/воде (3:1 об./об.) или
(б) перекристаллизацию соединения по любому из пп.2-8 в ИПА/воде (например, 3:1 об./об.) или
(в) гидролиз соединения по любому из пп.2-8 в водной серной кислоте.
20. Соединение по любому из пп.1-16 для применения в качестве терапевтически активного вещества, обладающего активностью в отношении рецептора mGluR5.
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| ПРОИЗВОДНЫЕ ПИРИДИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНТАГОНИСТИЧЕСКИМ ДЕЙСТВИЕМ НА MGLU R ЧЕЛОВЕКА | 1998 |
|
RU2203889C2 |
Авторы
Даты
2012-09-10—Публикация
2007-12-11—Подача