Изобретение относится к медицине, в частности к детской неврологии.
Детский церебральный паралич (ДЦП) - дизэмбриогенетическое полиэтиологическое заболевание, проявляющееся нарушением преимущественно двигательного и речевого развития [Christos P. Cerebral palsy. New York. - 2004. - P.267; Mauger U. Etiologies of cerebral palsy and classical treatment possibilities. - Wien. Med. Wochensch. - 2002. - V.152. - N.1-2. - P.14-18].
Большинство исследователей последних лет наиболее частой причиной развития спастических форм ДЦП как у родившихся доношенными и особенно у детей, родившихся недоношенными, считают перивентрикулярную лейкомаляцию (ПВЛ) [Белоусова Е.Д., Никанорова М.Ю., Кешишян Е.С., Малиновская О.Н. Роль перивентрикулярной лейкомаляции в развитии детского церебрального паралича // Рос. вест. перинат. и педиатр. - 2001. - №5. - С.26-32; Haynes R.L., Folkerth R.D., Keefe R.J., Sung I., Swzeda L.I., Rosenberg P.A., Voipe J.J., Kirnney H.C. Nitrosative and oxidative injury to premyelinating oligodendrocytes in periventricular leukomalacia // J. Neuropathol. Exp. Neurol. - 2003. - V.62. - N.5. - P.441-450; Resi В., Tomasovi M., Kuzmani-Samija R., Lozi M., Resi J., Solak M. Neurodevelopmental outcome in children with periventricular leukomalacia. // Coll. Antropol. - 2008. - V.32. - N.1. - P.143-147]. Многочисленные исследования показали, что генетические программы и средовая регуляция формообразования нервной системы контролируются, прежде всего, матричной перивентрикулярной областью. С ней связаны митоз, миграция нейронов к коре и подкорковым структурам, а также, что особенно важно в период онтогенеза, аксональный синаптогенез с клетками-мишенями и формирование функциональных систем [Rezaie P., Dean A. Periventricular leukomalacia, inflammation and white matter lesions within the developing nervous system. // Neuropathology - 2002. - V.22. - N.3. - P.106-132; Joseph J. Volpe. Neurology of the newborn. Elsevier Health Sciences. - 2008. - P.1094].
Как показывают исследования последних лет, не у каждого ребенка, развивающегося в неблагоприятных внутриутробных условиях, формируется ПВЛ [Скворцов И.А., Ермоленко Н.А. Развитие нервной системы у детей в норме и патологии // - M.: МЕДпресс-информ, 2003]. Очевидно, решающую роль в реализации потенциально патогенного воздействия играет генетически детерминированная индивидуальная реактивность организма ребенка, определяющая повышенную "восприимчивость" структур перивентрикулярной области и других отделов головного мозга плода и новорожденного к гипоксии. В литературе имеются доказательства того, что одним из провоцирующих моментов стойкости двигательного дефицита при ДЦП является нестабильность генома, проявляющаяся повышением уровня эритроцитов с микроядрами (ЭМ) и лимфоцитов с перестройками хромосом в периферической крови [Гайнетдинова Д.Д., Семенов В.В., Семенов А.В. и др. Хромосомная изменчивость при патологических состояниях ненаследственного генеза // Материалы III конгресса по патофизиологии с международным участием "Дизрегуляционная патология органов и систем". - М., 2004. - С.142-143; Гайнетдинова Д.Д. Состояние генетического аппарата у больных детским церебральным параличом // Казанский медицинский журнал. - 2005. - Т.86, приложение. - С.47-48]. Предполагается, что в основе этого явления лежит интенсификация в организме больных ДЦП процессов мутагенеза за счет усиленной генерации эндомутагенов и ослабления антимутагенных систем защиты генома. В то же время как сами механизмы дестабилизации генома, так и процессы их поддерживающие остаются неясными.
Существует мнение о том, что патологические изменения структур перивентрикулярной области могут быть инициированы во время внутриутробного развития, в период родов и продолжаться в течение всего детства [Семенова К.А. Восстановительное лечение детей с перинатальным поражением нервной системы и детским церебральным параличом. М.: Закон и порядок, серия "Великая Россия. Наследие", 2007. - С.616]. При этом происходит нарушение ауторегуляции и селективной уязвимости сосудов перивентрикулярной области, что ведет к хроническому ишемическому процессу в головном мозге биохимическим субстратом, который является усилением свободнорадикального окисления (СРО) [Sterk S., Schuller A., Sifringer M., Gerstner В., Brehmer F., Weber S., Altmann R., Obladen M., Buhrer C., Felderhoff-Mueser F. Suramin induces and enhances apoptosis in a model of hyperoxia-induced oligodendrocyte injury. // Neurotox. Res. - 2008. - V.13. - N.3-4. - P.197-207]. При избыточном образовании свободные радикалы воздействуют на клетку, приводят к различным цитогенетическим повреждениям и впоследствии к ее гибели. Чрезмерное образование активных форм кислорода (АФК) и продуктов перекисного окисления липидов может явиться причиной ряда хромосомных аббераций и мутацией некоторых генов в клетках человека [Гайнетдинова Д.Д., Семенов В.В., Семенов А.В. и др. Хромосомная изменчивость при патологических состояниях ненаследственного генеза // Материалы III конгресса по патофизиологии с международным участием "Дизрегуляционная патология органов и систем". - М., 2004. - С.142-143; Пескин А.В. Взаимодействие активного кислорода с ДНК // Биохимия. - 1997. - Т.62, Вып.12. - С.1571-1578; W.Kulak et al. Antioxidant enzymes and lipid peroxides in children with cerebral palsy // Life Sci. - 2005. - Vol.77, N24. - P.3031-3036]. Контроль над избыточной выработкой АФК осуществляет антиоксидантная система, регулирующая баланс свободнорадикальных реакций. К этой системе относятся: супероксиддисмутаза, каталаза, пероксидаза, церулоплазмин, глутатион-пероксидаза, глутатионтрансфераза и др. [Болдырев А.А. Окислительный стресс и мозг // Соросовский образовательный журнал. - 2001. - Т.7, N4. - С.21-28; Н.К.Зенков, В.З.Ланкин, Е.Б.Меньшикова. Окислительный стресс: Биохимический и патофизиологический аспекты /. - М.: МАИК "Наука / Интерпериодика", 2001. - С.343].
В последние годы в литературе описано исследование, доказывающее наличие у больных ДЦП высокого уровня цитогенетических нарушений в клетках периферической крови [Гайнетдинова Д.Д. Состояние генетического аппарата у больных детским церебральным параличом // Казанский медицинский журнал. - 2005. - Т.86, приложение. - С.47-48]. Но при этом механизмы формирования нестабильности генома при ДЦП остаются малоизученными. Известно, что нестабильность генома может поддерживать стойкость двигательного дефицита у детей со спастическими и дискинетическими формами заболевания, препятствуя успешной реабилитационной терапии. Таким образом, изучение некоторых патогенетических звеньев заболевания поможет уточнить механизмы, поддерживающие тяжесть заболевания и препятствующие эффективности лечебных мероприятий. Это позволит целенаправленно воздействовать на выявленные процессы, обоснованно назначать медикаментозную терапию и улучшать качество жизни пациента, больного ДЦП.
Известен способ определения нестабильности генома у детей с ДЦП, включающий выявление клинических признаков заболевания, определение в периферической крови ребенка уровня эритроцитов с микроядрами и уровень перестроек хромосом в лимфоцитах, и при значении сумм эритроцитов с микроядрами более 0,14% и лимфоцитов с абберациями хромосом более 3,33% у девочек и 3,38% у мальчиков устанавливают нестабильность генома у ребенка (пат. RU №2295130, МПК G01N 33/48, опуб. 10.03.07 г.).
В этом способе, наиболее близком к предлагаемому, нет четкой картины механизма формирования нестабильности генома при ДЦП, поскольку определяются только уровень эритроцитов с микроядрами и уровень перестроек хромосом в лимфоцитах в периферической крови без учета факторов, приводящих к мутагенезу и процессов его поддерживающих. В ходе сравнительной оценки методов исследования нестабильности генома определено, что метод регистрации микроядер в эритроцитах периферической крови более чувствителен при выявлении нестабильности генома, чем метод определения перестроек хромосом в лимфоцитах периферической крови. Это не распространяется на оценку степени повреждения генома.
Предполагается, что в основе явления нестабильности генома лежит интенсификация в организме больных ДЦП процессов мутагенеза за счет усиленной генерации эндомутагенов и (или) ослабления антимутагенных систем защиты генома.
При создании изобретения ставилась задача получения способа комплексной оценки нестабильности генома, основанного на взаимосвязи уровня эритроцитов с микроядрами, интенсивности процессов перекисного окисления липидов (ПОЛ) и активности ферментов антиоксидантной защиты у детей с ранней резидуальной стадией ДЦП, что позволит определять интенсивность процесса мутагенеза за счет усиленной генерации эндомутагенов (продуктов свободнорадикального окисления) и ослабления антимутагенной системы защиты генома (изменения активности ферментов антиоксидантной защиты) и включать в терапию специфические препараты с антиоксидантными свойствами.
Это достигается тем, что в способе определения нестабильности генома у детей, больных детским церебральным параличом с перивентрикулярной лейкомаляцией, включающем выявление клинических признаков заболевания, определение в периферической крови ребенка уровня эритроцитов с микроядрами, дополнительно исследуют кровь на содержание продукта перекисного окисления липидов - малонового диальдегида (МДА), и на определение активности антиоксидантного фермента супероксиддисмутазы (СОД) и при значении эритроцитов с микроядрами более 0,22%, повышении уровня МДА более 0,7 мкМ/л и СОД более 0,6 усл.ед. устанавливают нестабильность генома у ребенка, больного детским церебральным параличом с перивентрикулярной лейкомаляцией.
В результате дополнительного исследования крови на содержание продукта перекисного окисления липидов - МДА - и на определение активности антиоксидантного фермента - СОД - и при значении эритроцитов с микроядрами более 0,22%, повышении уровня МДА более 0,7 мкМ/л и СОД более 0,6 усл.ед. можно судить о выраженности окислительного стресса как фактора, дестабилизирующего геном. У детей, больных спастическими формами ДЦП с ПВЛ с активацией окислительного стресса, возрастает дестабилизация генома, при этом окислительный стресс утяжеляет клиническое течение спастических форм ДЦП. Следует отметить, что тяжесть клинических проявлений ДЦП взаимосвязана с уровнем цитогенетических нарушений в клетках периферической крови больных с ПВЛ: чем тяжелее степень ПВЛ, тем выше число эритроцитов с микроядрами и грубее клиническая картина ДЦП. Выраженный окислительный стресс и дестабилизация генома могут рассматриваться как постоянно действующие и взаимозависимые факторы, интегрированные в общую систему патогенеза при ДЦП. Выявление высокого уровня нестабильности клеточного генома, повышение активности показателей процесса свободнорадикального окисления у больных с ПВЛ являются основанием отнесения ребенка к группе риска формирования тяжелой степени ДЦП и разработке ранних индивидуальных терапевтических мероприятий.
Способ осуществляется следующим образом.
Цитогенетические нарушения исследовали в эритроцитах периферической крови микроядерным тестом [Schmid W. The micronucleus test / W.Schmid // Mutat. Res. - 1975. - Vol.31, N 1. - P.9-15]. Каплю крови наносили на чистое сухое предметное стекло и покровным стеклом готовили мазок. Препараты высушивали на воздухе в течение нескольких часов. Свежие высушенные мазки фиксировали 90-70% этиловым спиртом 3 мин. Сухие препараты окрашивали в растворе азур-эозинового красителя Романовского-Гимза 1:5 на дистиллированной воде (рН 6,8) 20 минут и хорошо промывали. Для исследования уровня эритроцитов с микроядрами осматривали по 1-2 препарата от каждого человека. В каждом случае анализировали 20000 эритроцитов. Число эритроцитов с микроядрами выражали в %.
Об интенсивности ПОЛ судят по уровню одного из конечных продуктов - МДА, который определяли с помощью стандартной методики [Гаврилов В.Б. Анализ методов определения продуктов перекисного окисления липидов в сыворотке крови по тесту с тиобарбитуровой кислотой /В.Б. Гаврилов, А.Р.Гаврилова, Л.М.Мажуль // Вопросы медицинской химии - 1987. - №8. - С.118-122]. К 0,3 мл сыворотки (плазмы) добавляли 2,4 мл 1/12N серной кислоты, встряхивали и оставляли на 10 минут при комнатной температуре. Затем добавляли 0,3 мл 10% раствора фосфорновольфрамовой кислоты, встряхивали и оставляли при комнатной температуре на 10 минут. Далее центрифугировали 15 минут при 3000 об/мин. Супернатант сливали, а к осадку добавляли 1 мл дистиллированной воды и вновь центрифугировали 10 мин при 3000 об/мин. Осадок промывали еще 2 раза при тех же условиях. Далее к полученному осадку добавляли 3 мл дистиллированной воды и 1 мл ТБК и нагревали в кипящей водяной бане в течение 1 часа. Затем охлаждали и центрифугировали 15 минут при 6000 об/мин. Оптическую плотность определяли на спектрофотометре при 532 нм против контроля на реактивы. Содержание малонового диальдегида в осадке липопротеидов плазмы крови рассчитывали, учитывая разведение и используя молярный коэффициент экстинкции (1,56×10 см-1×М-1), полученный результат выражали в мкМ/л.
Активность антиоксидантного фермента СОД определяли по стандартной методике [Е.Е.Дубинина. Активность и изоферментный спектр супероксиддисмутазы эритроцитов и плазмы крови человека / Е.Е.Дубинина, Л.А.Сальникова, Л.Ф.Ефимова // Лаб. дело. - 1983. - №10. - С.31-33]. Метод определения активности СОД основан на его способности конкурировать с нитросиним тетразолием (НСТ) за супероксидный анион, образующийся в результате аэробного взаимодействия с никотинамидадениндинуклеотидом восстановленным (НАДН) и феназинметасульфатом (ФМС). В присутствии СОД НСТ восстанавливается до гидрозинтетразолия, максимум поглощения которого регистрируется при 540 нм спектрофотометрически. К 0,1 мл крови добавляли 1,0 мл трис-HCl, 0,25 мл этилового спирта и 0,2 мл хлороформа. Затем хорошо перемешивали и насыпали 0,3 г порошка двухзамещенного фосфата натрия, помешивали стеклянной палочкой до обесцвечивания. Данную пробирку центрифугировали в течение 15 минут при 5000 об/мин, супернатант переливали в отдельную пробирку. В опытную пробирку вносили 1 мл ЭДТА, 1 мл фосфатного буфера (рН 7,4), 0,5 мл нитросиния тетразолия, 0,5 мл феназин метасульфата, 0,1 мл супернатанта и 0,1 мл НАДН. После добавления каждого реактива тщательно встряхивали пробирку. Затем пробы помещали в темное место на 10 минут. Активность супероксиддисмутазы определяли на спектрофотометре при 540 нм, против контрольной пробы со всеми составляющими, как и в опытной пробирке, но без НАДН. Контрольная проба - проба на реактивы. Активность СОД выражали в условных единицах. Расчет активности фермента проводился по формуле
Q=(Ек-Еоп)×К/Ек×10 у.е., где
К=20,
Ек - оптическая плотность контрольной пробы,
Еоп - оптическая плотность опытной пробы.
Статистический анализ полученных данных проводили с использованием непараметрического критерия - t-критерий Манна-Уитни - и корреляционного анализа по программе Origin 6,1. Оценку среднего уровня клеток с микроядрами и перестройками хромосом проводили с использованием медианы (Me). Нижний и верхний пороговые уровни клеток с цитогенетическими нарушениями определяли как 2,5-й и 97,5 перцентили соответственно.
Было обследовано 30 мальчиков и 32 девочки (62 чел., возраст от 1 до 5 лет) со спастическими формами ДЦП. Обследованные дети находились на стационарном лечении в неврологическом отделении Детской республиканской клинической больницы города Казани. Критерием отбора детей в исследование явилось обнаружение при нейровизуализации (нейросонография и рентгеновская компьютерная томография) только ПВЛ, без других находок. Для сравнения включили 20 практически здоровых детей. Обе группы были сопоставимы по полу и возрасту. Забор крови у всех детей осуществлялся до начала медицинского и реабилитационного лечения. У них не отмечалось острой инфекции и обострений хронической соматической патологии.
Для выявления цитогенетических аномалий в соматических клетках использовался метод учета микроядер в эритроцитах периферической крови согласно методике микроядерного теста. Биохимическим спектрофотометрическим методом исследовались: активность СОД в гемолизате крови и содержание МДА в плазме крови.
Цитогенетическое исследование выявило повышение числа ЭМ у каждого обследованного ребенка с ДЦП и составило 0,71%, что достоверно превышало показатель спонтанного мутагенеза 0,22% в группе контроля (уровень значимости (р)<0,001) (табл.1).
Выявленные цитогенетические нарушения свидетельствуют о дестабилизации генома обследованных больных. Нестабильность генома может возникнуть в условиях повышенной генерации эндомутагенов, приводящих к повреждению метаболических циклов анеугенеза и, как следствие, увеличению числа клеток с цитогенетическими перестройками.
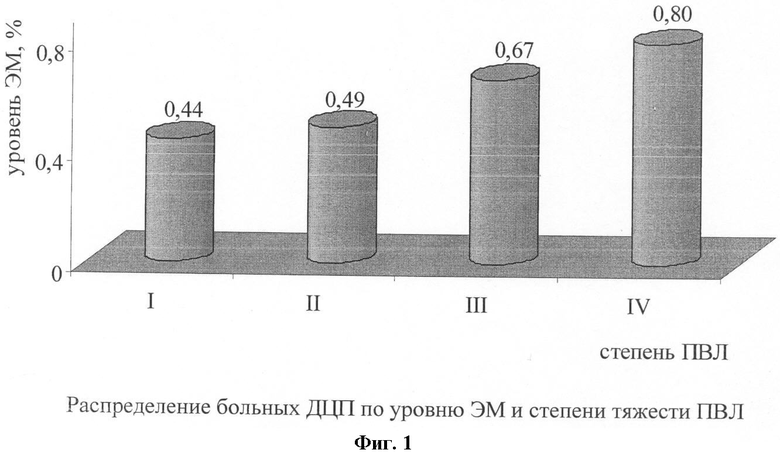
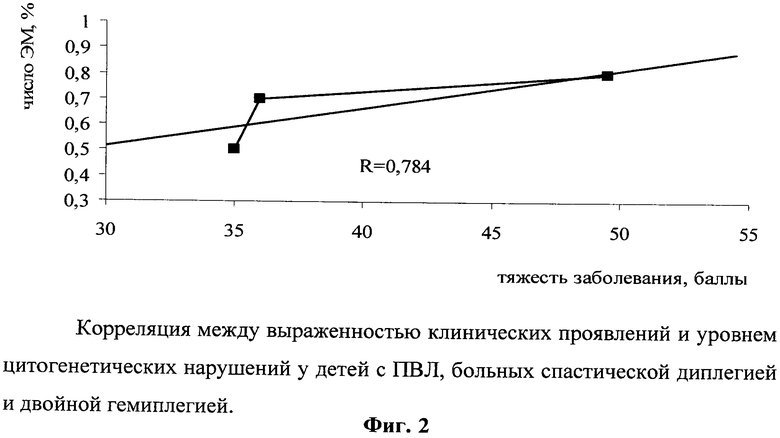
У обследованных детей нестабильность генома усугублялась с утяжелением степени ПВЛ: число ЭМ было максимальным при IV степени - 0,80%, минимальным - при I степени - 0,44% (р<0,05) (фиг.1). Обнаружена прямая корреляция числа ЭМ и тяжести клинической картины заболевания (коэффициент корреляции (R)=0,784): чем выше дестабилизация генома, тем тяжелее клинические проявления ДЦП (фиг.2). Таким образом, у детей с ПВЛ имеет место дестабилизации генома, коррелирующая с тяжестью клинических проявлений ДЦП. Наиболее вероятными генераторами эндомутагенеза у детей с ПВЛ больных ДЦП могут быть активные свободнорадикальные процессы. Для расшифровки механизмов, провоцирующих цитогенетические нарушения в клетках периферической крови и усиливающих спонтанный эндомутагенез у детей, больных ДЦП, определена активность фермента антиоксидантной защиты - СОД - и содержание продукта ПОЛ - МДА в крови.
Обнаружены достоверные различия показателей активности СОД у детей, больных ДЦП с ПВЛ, и здоровых лиц (1,0±0,3 и 0,6±0,2 усл.ед., р<0,002) (табл.1). Изучение содержания продуктов ПОЛ выявило у больных ДЦП достоверно высокое содержание конечного продукта - МДА - по сравнению с контролем (1,22±0,5 мкМ/л и 0,57±0,2 мкМ/л, р<0,001) (табл.1).
Анализ процессов окислительного стресса у детей со спастическими формами ДЦП выявил взаимосвязь содержания продуктов ПОЛ и ферментов антиоксидантной защиты от степени тяжести ПВЛ (табл.2).
По значениям уровня МДА выявлено, что содержание МДА увеличивается по мере утяжеления ПВЛ и, следовательно, тяжести ДЦП, что свидетельствует о высокой активации процессов ПОЛ у детей с грубым поражением перивентрикулярной области: максимальное значение показателя обнаружено у больных с IV степенью ПВЛ (2,1 мкМ/л), а минимальное - с I степенью (0,8 мкМ/л).
Анализ активности ферментативной системы антиоксидантной защиты у детей с различной степенью тяжести ПВЛ показал, что активность СОД увеличивается с утяжелением степени ПВЛ (табл.2). Однако при IV-й степени ПВЛ выявлено резкое снижение СОД по сравнению с показателями в группе детей с I, II и III степенью тяжести ПВЛ (р<0,05), что связано с дефицитом антиоксидантов и ослаблением антирадикальной защиты при усилении окислительного стресса.
На основании выявленного повышения фермента антирадикальной защиты и продукта ПОЛ (МДА) можно судить о течении выраженного окислительного стресса у детей, больных спастическими формами ДЦП с ПВЛ.
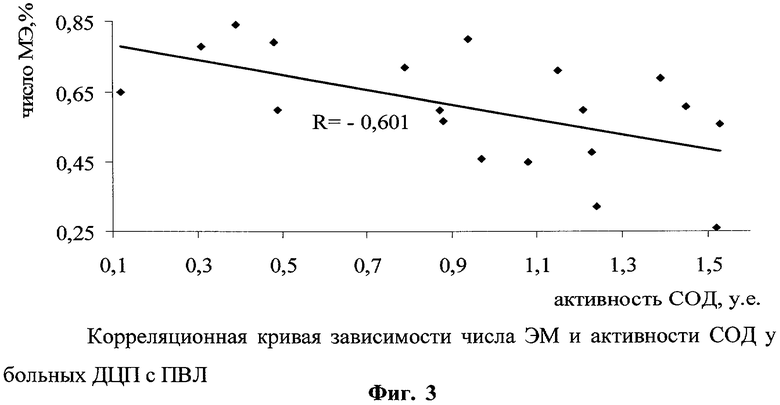
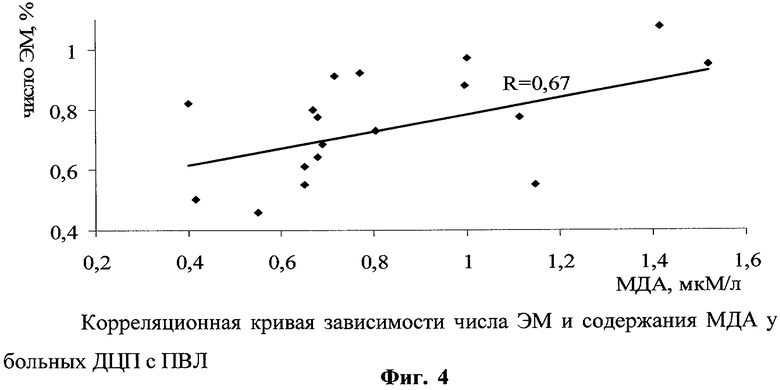
Полученные результаты биохимического и цитогенетического исследования свидетельствуют о наличии у детей с ПВЛ двух одновременно протекающих патологических процессов. С одной стороны, повышение интенсивности процессов свободнорадикального окисления, с другой, нестабильность генома с высоким числом цитогенетических перестроек. Оба эти процесса взаимосвязаны друг с другом: активность СОД обратно коррелируют с числом ЭМ (R=-0,601) (фиг.3), а по содержанию МДА выявлена прямая корреляция с числом эритроцитов с перестройками (R=0,67) (фиг.4). Следовательно, дестабилизация генома у детей с ПВЛ происходит на фоне активации свободнорадикальных процессов, и в условиях повышения уровня МДА более 0,7 мкМ/л и СОД более 0,6 усл.ед. значительно возрастает мутагенное действие свободных радикалов на геном, приводя к повышению показателя спонтанного мутагенеза - 0,22%. При одновременном отклонении этих показателей устанавливают нестабильность генома у ребенка, больного ДЦП с ПВЛ.
Таким образом, результаты анализа наших исследований позволяют сделать предположения, что у больных ДЦП нестабильность генома формируется на фоне активации свободнорадикальных процессов. Выраженные процессы свободнорадикального окисления провоцируют эндомутагенез, приводя к анеугенному эффекту в клетках организма больного ДЦП. Особенно отчетливо это прослеживается у больных ДЦП с IV степенью тяжести ПВЛ, при которой выявлен окислительный стресс высочайшей активности, проявляющийся высоким уровнем конечного продукта ПОЛ - МДА, обладающего доказанным цитотоксическим действием на фоне резкого дефицита ферментативной антиоксидантной защиты. В этих условиях повышенное содержание МДА проявляет свое выраженное цитотоксичное действие, вызывая дестабилизацию генома. У детей с ПВЛ, больных ДЦП, отмечается значительная активность СОД - ключевого фермента антиоксидантной защиты. СОД является первичным звеном защиты организма от цитотоксического действия супероксид анион-радикала. Отрицательная корреляция активности СОД с уровнем цитогенетических нарушений у детей с ПВЛ, больных ДЦП, может быть связана с недостаточной активностью антирадикальных ферментов для антимутагенной защиты на фоне усиления процессов эндомутагенеза. Поэтому можно предположить, что окислительный стресс дестабилизирует клеточный геном у детей с ДЦП и поддерживает процессы, протекающие (а может, и исходящие) в перивентрикулярной области, что способствует утяжелению имеющихся и появлению новых патологических процессов у больного. Это диктует необходимость дополнительных путей фармакологической коррекции окислительного стресса и цитогенетических нарушений у детей с ПВЛ.
Пример
Аниса Н.. (истории болезни 1365/61; 1542/40), 2,5 лет. Диагноз: ДЦП, двойная гемиплегия, тяжелая задержка психомоторного развития, частичная атрофия зрительных нервов. Девочка от 3 беременности (1 - м/а, 2 - выкидыш), протекавшей с токсикозом I половины, угрозой прерывания беременности на сроке 8-10 недель в виде повышения тонуса матки с 8 недель, во второй половине беременности отмечались подъемы АД до 160-180/100 мм рт.ст. От I преждевременных родов, стимулированных в связи с тяжестью гестоза, на сроке 33 недели. При рождении масса тела 1715 грамм, оценка по Апгар 4/7 баллов. Родилась в очень тяжелом состоянии, находилась на ИВЛ 16 часов. Тяжесть состояния обусловлена синдромом дыхательных расстройств незрелого типа, гипоксически - ишемическим поражением ЦНС. В неонатальном периоде отмечались синдром мышечной дистонии, синдром гипервозбудимости. Находилась на зондовом вскармливании 7 суток. Выписана под наблюдение невропатолога в возрасте 36 суток. Формула развития: к 6 месяцам фиксировала взгляд, голову удерживает с 11 месяцев, не переворачивается, слегка приподнимается на предплечьях, лежа на животе, не сидит, не стоит, не ползает, улыбается, произносит отдельные звуки, реагирует на близких, игрушками не интересуется. При осмотре состояние ребенка тяжелое по основному заболеванию. Зрение снижено, взгляд фиксирует кратковременно. Двигательная активность ограничена. Мышечный тонус высокий, сухожильные рефлексы высокие с расширенными зонами вызывания, патологические рефлексы положительные, клонусы стоп. Грубый спастический тетрапарез, более выраженный в руках. Эмоционально крайне лабильна. Самообслуживание затруднено.
Нейросонографическое исследование:
Исследование 1 (12 сутки жизни): на фоне повышенной эхогенности перивентрикулярных тканей в затылочно-теменной области выявляются множественные анэхогенные участки. Исследование 2 (2 месяца): боковые желудочки расширены. Перивентрикулярные ткани повышенной эхогенности, по всем отделам выявляются псевдокисты до 10-12 мм диаметром. Расширение межполушарной щели 7 мм. Заключение: ПВЛ 4 степени тяжести.
На РКТ головного мозга (16 месяцев) выявлено нарушение соотношения серого и белого вещества с уменьшением объема белого вокруг передних и задних рогов боковых желудочков. Вентрикуломегалия. Гипоплазия мозолистого тела.
Ребенок регулярно получает реабилитационную терапию, включающую медикаментозное и физиотерапевтическое лечение, повторные курсы массажа с минимальным положительным эффектом.
Исследование уровня эритроцитов с микроядрами выявило высокий уровень ЭМ (0,86%), превышающий спонтанный уровень цитогенетических нарушений в здоровой выборке (0,22%) более чем в 3 раза. Исследование оксидантного статуса выявило высокий уровень МДА (1,97 мкМ/л), в 3 раза превышающий уровень в контрольной группе (0,57 мкМ/л), и на этом фоне низкую активность СОД (0,62 усл.ед.).
Было проведено лечение с применением нейротрофического препарата с антиоксидантным действием - церебролизин в дозе 0,1 мл/кг/сут в/м 20 дней. Отмечалась положительная клиническая динамика: стала активнее следить за предметом, проявлять интерес к игрушкам, в положении на животе уверенно держится на предплечьях. Исследование оксидантного статуса показало снижение уровня МДА до 1,14 мкМ/л, также была обнаружена положительная динамика цитогенетических нарушений в виде снижения уровня ЭМ до 0,47%, но все же показатели оставались выше, чем у здоровых детей.
Высокую интенсивность кластогенеза и анеугенеза у данного больного ДЦП можно связать с повреждением метаболических циклов кластогенеза, сопровождающихся повышенной генерацией эндомутагенов и ослаблением антимутагенной системы защиты генома. Феномен нестабильности генома может служить косвенным доказательством стойкости этой патологии у данного больного ДЦП и, следовательно, рассматриваться как постоянно действующий фактор, интегрированный в общую систему патогенеза при этом заболевании, утяжеляющий клиническую картину ДЦП с ПВЛ. Полученная динамика процессов СРО на фоне терапии церебролизином свидетельствует о том, что церебролизин, обладая антиоксидантным действием, замедляет процессы оксидантного эндомутагенеза в организме детей с ПВЛ. Антирадикальные свойства церебролизина уменьшают цитотоксическое действие свободных радикалов на геном клетки, снижая нестабильность генома у больных ДЦП и соответственно препятствуя прогрессированию заболевания. Поскольку на фоне лечения не было достигнуто снижения продуктов ПОЛ и уровня нестабильности генома до показателей здоровых лиц, необходимы дальнейшие исследования в области фармакологической коррекции в целях оптимизации терапии ПВЛ и профилактики формирования ДЦП. В этих условиях на первый план выходит разработка подходов к фармакологической коррекции генома у больных ДЦП с ПВЛ, которая должна наметить более радикальные пути восстановительного лечения, включая препараты с антиоксидантным и антимутагенным действием детям со спастическими формами ДЦП.
Изобретение относится к области медицины, а именно к медицинской диагностике. Предложен способ определения нестабильности генома у детей, больных детским церебральным параличом с перивентрикулярной лейкомаляцией. Выявляют клинические признаки заболевания, определяют в периферической крови ребенка уровень эритроцитов с микроядрами, исследуют кровь на содержание продукта перекисного окисления липидов - малонового диальдегида - и на активность антиоксидантного фермента супероксиддисмутазы. При значении эритроцитов с микроядрами более 0,22%, повышении уровня малонового диальдегида более 0,7 мкМ/л и супероксиддисмутазы более 0,6 усл.ед. устанавливают нестабильность генома у ребенка, больного детским церебральным параличом с перивентрикулярной лейкомаляцией. 2 табл., 4 ил.
Способ определения нестабильности генома у детей, больных детским церебральным параличом с перивентрикулярной лейкомаляцией, включающий выявление клинических признаков заболевания, определение в периферической крови ребенка уровня эритроцитов с микроядрами, отличающийся тем, что дополнительно исследуют кровь на содержание продукта перекисного окисления липидов - малонового диальдегида - и на определение активности антиоксидантного фермента супероксиддисмутазы и при значении эритроцитов с микроядрами более 0,22%, повышении уровня малонового диальдегида более 0,7 мкМ/л и супероксиддисмутазы более 0,6 усл.ед. устанавливают нестабильность генома у ребенка, больного детским церебральным параличом с перивентрикулярной лейкомаляцией.
| СПОСОБ ОПРЕДЕЛЕНИЯ НЕСТАБИЛЬНОСТИ ГЕНОМА У ДЕТЕЙ С ДЕТСКИМ ЦЕРЕБРАЛЬНЫМ ПАРАЛИЧОМ | 2005 |
|
RU2295130C1 |
| МУТАГЕНЕЗ ДНК ЗА СЧЕТ НЕУПОРЯДОЧЕННОЙ ФРАГМЕНТАЦИИ И ВТОРИЧНОЙ СБОРКИ | 1995 |
|
RU2157851C2 |
| ГАЙНЕТДИНОВА Д.Д | |||
| и др | |||
| Клинико-цитогенетическое сопоставление выраженности клинических проявлений и уровня нестабильности генома у больных детским церебральным параличом, 2008, №3, с.29-32 | |||
| FENECH M | |||
| Micronutrients and genomic stability: a new paradigm for recommended dietary allowances (RDAs) | |||
| Food Chem Toxicol | |||
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| Review. | |||
Авторы
Даты
2011-02-27—Публикация
2009-11-20—Подача