ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к способам и композициям для лечения патологических состояний кишечника посредством применения технологии PHKi путем интраректального введения. Композиции согласно изобретению содержат молекулы коротких интерферирующих нуклеиновых кислот (siHK) и близких соединений, включая, но не ограничиваясь ими, короткие интерферирующие РНК (siPHK). В частности, композиции согласно изобретению можно использовать для лечения патологических состояний кишечника, включая гиперпролиферативные заболевания, в частности злокачественную опухоль ободочной и прямой кишки; аутоиммунные и воспалительные заболевания кишечника (IBD), в частности болезнь Крона; колит, в частности язвенный колит; синдром раздраженного кишечника; инфекционные заболевания кишечника, такие как псевдомембранозный колит, амебиаз или туберкулез кишечника; полипы ободочной кишки; дивертикулы; запор; непроходимость кишечника; синдромы нарушения всасывания; заболевания прямой кишки и диарею.
В некоторых вариантах осуществления заболевания кишечника, развитие которых вызвано повышенными концентрациями интерлейкина-12 (IL-12), цитокина, принимающего участие в иммунной ответной реакции Т-клеток-хелперов типа 1 (Th1), предназначаются для лечения с использованием данного подхода: например, это аутоиммунные заболевания и IBD. Обеспечиваются композиции и способы, включающие siPHK и близкие соединения с направленным действием на субъединицу IL12-р40 и/или субъединицу IL12-р35 для лечения заболеваний, связанных со сверхэкспрессией IL-12, в частности болезни Крона.
УРОВЕНЬ ТЕХНИКИ
PHKi в качестве инструмента для модуляции экспрессии гена
РНК-интерференция относится к процессу специфичного в отношении последовательности посттрансляционного «сайленсинга» генов, опосредуемого двухцепочечной РНК (dsPHK). После открытия этого феномена у растений в начале 1990 годов Andy Fire и Craig Mello показали, что dsPHK специфически и селективно подавляют экспрессию генов, причем очень эффективным образом у Caenorhabditis elegans (Fire et al., 1998). Последовательность первой цепи (смысловой РНК) совпадала с соответствующей областью матричной РНК-мишени (мРНК). Вторая цепь (антисмысловая РНК) была комплементарной мРНК. Полученные dsPHK оказались на несколько порядков более эффективными по сравнению с соответствующими молекулами одноцепочечной РНК (в частности, антисмысловой РНК).
Процесс PHKi начинается, когда фермент DICER сталкивается с dsPHK и «нарезает» ее на кусочки, называемые короткими интерферирующими РНК, или siPHK. Данный белок относится к семейству нуклеаз, РНК-азе III. Комплекс белков собирает данные siPHK и использует их код в качестве проводника для поиска и разрушения любой РНК в клетке с парной последовательностью, такой как мРНК-мишень (см. Boscher & Labouesse, 2000; и Akashi et al., 2001).
При попытке применить PHKi для «нокаута» гена было установлено, что клетки млекопитающих выработали различные защитные механизмы против вирусных инфекций, которые могут стать препятствием для применения данного подхода. Действительно, присутствие вирусной dsPHK в очень низких концентрациях «запускает» ответную выработку интерферона, приводя к общей неспецифической супрессии трансляции, что, в свою очередь, «запускает» апоптоз (Williams, 1997, Gil & Esteban, 2000).
В 2000 г. сообщалось, что dsPHK специфически ингибирует три гена в мышиных ооцитах и эмбрионах на ранних стадиях развития. Остановку трансляции и, таким образом, ответной реакции PKR не наблюдали, поскольку эмбрионы продолжали развиваться (Wianny & Zerniska-Goetz, 2000). В исследованиях, проведенных Ribopharma AG (Kulmbac, Германия), было показано функциональное значение PHKi в клетках млекопитающих с использованием коротких (из 20-24 пар нуклеотидов) dsPHK для «выключения» генов в человеческих клетках без инициации ответа в острой фазе. В аналогичных опытах, проведенных другими исследовательскими группами, эти результаты были подтверждены (Elbashir et al., 2001; Caplen et al., 2001). При тестировании в различных нормальных и опухолевых человеческих и мышиных клеточных линиях было показано, что короткие РНК-«шпильки» (shPHK) могут приводить к «сайленсингу» генов так же эффективно, как и их противоположности siPHK (Paddison et al., 2002). Недавно было показано, что другая группа коротких РНК (из 21-25 пар нуклеотидов) опосредует даун-регуляцию экспрессии гена. Данные РНК, короткие, временно регулируемые РНК (stPHK), регулируют время экспрессии гена в развитии в Caenorhabditis elegans (см. обзор Banerjee & Slack, 2002 и Grosshans & Slack, 2002).
Ученые использовали PHKi в различных системах, включая Caenorhabditis elegans, дрозофил, трипаносом и других беспозвоночных. Недавно несколько групп показали наличие специфической супрессии биосинтеза белка в различных клеточных линиях млекопитающих (в частности, в клетках HeLa), демонстрируя тем самым, что PHKi является широко применимым способом для «сайленсинга» генов в условиях in vitro. Основываясь на данных результатах, PHKi быстро превратилась в хорошо признанный инструмент для установления (идентификации и регистрации) функций генов. Использование в PHKi коротких олигонуклеотидов dsPHK будет способствовать пониманию функции генов, которые секвенированы только частично.
Недавно Krutzfeldt и коллеги показали, что группа специально созданных генно-инженерных соединений, названных «антагомирами», может эффективно подвергать «сайленсингу» действие микроРНК (miPHK), не кодирующих структуры РНК, которые регулируют экспрессию генов (Krutzfeldt et al., 2005).
Приведенное выше представляет обсуждение уровня техники, относящегося к PHKi. Обсуждение приводится только для понимания изобретения, описание которого следует, и не для признания того, что любая из описанных работ представляет предшествующий уровень техники по отношению к заявленному изобретению.
Интерлейкин-12 и болезнь Крона
Интерлейкин-12 (IL-12) представляет собой гетеродимерный гликопротеин массой 70 кДа (IL12-р70), состоящий из субъединицы с молекулярной массой 40 кДа (обозначаемой IL12-р40) и субъединицы с молекулярной массой 35 кДа (обозначаемой IL12-р35), связанных дисульфидными связями, которые имеют важное значение для проявления биологической активности IL-12.
IL-12 является ключевым цитокином, который регулирует опосредуемые клетками иммунные ответы и воспалительные реакции с участием Т-клеток-хелперов (Th1) (Gately et al., 1998; Trinchieri, 1998). Способность IL-12 эффективно стимулировать развитие Th1-клеток делает его идеальной мишенью при лечении опосредуемых Th1-клетками заболеваний, таких как аутоиммунные заболевания и воспалительные заболевания кишечника (IBD).
Одним конкретным IBD является болезнь Крона, патологическое состояние, характеризующееся повышенной продукцией IL-12 в антиген-представляющих клетках ткани кишечника и интерферона-γ и фактора-α некроза опухолей (TNF-α) лимфоцитами и макрофагами кишечника (Fais et al., 1994; Fuss et al., 1996; Monteleone et al., 1997; Parronchi et al., 1997; Plevy et al., 1997).
Болезнь Крона вызывает воспаление в тонком кишечнике. Воспаление может привести к возникновению боли и может вызвать частое освобождение кишечника, приводя к развитию диареи. Наиболее распространенными симптомами болезни Крона является боль в брюшной области и диарея, хотя также может иметь место кровотечение из прямой кишки, потеря массы тела и лихорадка. Кровотечение может быть сильным и длительным, приводя к анемии. У детей, страдающих болезнью Крона, может наблюдаться замедленное развитие и задержка роста.
Большинство людей вначале подвергается лечению лекарственными средствами, содержащими мезаламин, соединение, которое оказывает помощь в борьбе с воспалением. Сульфасалазин представляет собой наиболее часто применяемый препарат из данных лекарственных средств. Пациентов, которым он не помогает или которые его не переносят, можно перевести на другие, содержащие мезаламин лекарственные средства, обычно известные как средства 5-ASA, такие как азакол, дипентий или пентаза. Возможные побочные эффекты от препаратов на основе мезаламина включают тошноту, рвоту, диарею и головную боль. Некоторые пациенты для снятия воспаления принимают кортикостероиды. Данные лекарственные средства являются наиболее эффективными для лечения болезни Крона в активной стадии, но они могут вызывать серьезные побочные эффекты, включая развитие более высокой чувствительности к инфекции. Также для лечения болезни Крона применяют лекарственные средства, которые подавляют иммунную систему. Чаще всего назначают 6-меркаптопурин и близкое лекарственное средство, азатиоприн. Иммуносупрессоры функционируют посредством блокирования иммунной реакции, участвующей в развитии воспаления. Подобные лекарственные средства могут вызвать побочные эффекты, такие как тошнота, рвота и диарея, и могут привести к снижению устойчивости человека к инфекции. Оперативное вмешательство по поводу удаления части кишечника может привести к ослаблению болезни Крона, но не к его вылечиванию. В результате проявления побочных эффектов и отсутствия эффективности имеющихся средств лечения болезни Крона исследователи продолжают поиск более эффективных способов лечения.
Было показано, что при ингибировании IL-12 подавляется развитие и клиническое прогрессирование заболевания на многих экспериментальных моделях аутоиммунных и хронических воспалительных заболеваний (Caspi, 1998). Данные модели включают экспериментальный аутоиммунный энцефаломиелит (ЕАЕ), экспериментальный аутоиммунный увеит (EAU), индуцированный коллагеном артрит (CIA), аутоиммунный нефрит, инсулинзависимый сахарный диабет (IDDM) и различные модели IBD (Vandenbroeck et al., 2004). На данных моделях выясняли роль эндогенного IL-12 при использовании нокаутных мышей в отношении гена IL-12р40 или при введении антител против IL-12.
В частности, направленное действие антител против IL-12 представляет собой эффективный способ лечения воспаления кишечника на моделях болезни Крона на животных (Mannon et al., 2004). Так, у мышей с колитом, индуцированным тринитробензолом сульфонатом, имело место опосредуемое Th1-клетками воспаление кишечника, для которого характерна очень высокая продукция IL-12, интерферона-γ и фактора-α некроза опухолей (TNF-α). У мышей введение моноклональных антител против IL-12 приводило к вылечиванию развившегося колита, а при назначении во время индукции колита предупреждало развитие воспаления (Neurath et al., 1995).
С помощью антител против IL-12 можно также профилактировать или лечить спонтанный колит на моделях опосредуемого Th1-клетками воспаления, таких как мыши со сверхэкспрессией человеческого гена CD3ε и мыши с дефицитом интерлейкина-10 (Davidson et al., 1998; Simpson et al., 1998).
Результаты ранних испытаний фазы 2 обеспечивают некоторые доказательства того, что лечение моноклональными антителами против р40 IL-12 может стимулировать клиническую ответную реакцию и ремиссию у пациентов с активной формой болезни Крона (Mannon et al., 2004). Такое лечение связано со снижением уровня опосредуемых Th1-клетками цитокинов воспаления в месте заболевания.
Результаты, полученные ранее на животных моделях, а также данные клинических испытаний антител против IL-12 у пациентов с болезнью Крона (Mannon et al., 2004) подчеркивают важность IL-12 в качестве мишени для будущих способов лечения болезни Крона.
Модуляция концентраций IL-12 с помощью siPHK
Направленное действие siPHK на экспрессию IL-12 уже применяли для получения модифицированных дендритных клеток (DC), которые можно использовать в различных терапевтических способах в условиях in vitro, ex vivo и in vivo для модуляции активности Т-клеток, и, таким образом, их применяли в терапевтических подходах для лечения иммунных нарушений у млекопитающих (WO 2003/104456; Hill et al., 2003). При направленном действии siPHK на экспрессию IL-12 в зрелых DC была показана критическая роль IL-12 для секреции интерферона-γ (IFN-γ) в природных клетках-киллерах, стимулированной зрелыми DC (Borg et al., 2004). Кроме того, с удивлением было установлено, что ингибиторы IL-12 р35, включая siPHK, блокируют дифференциацию преадипоцитов в адипоциты и накопление триглицеридов в адипоцитах (WO 2003/104495).
Направленные на р40 IL-12 siPHK можно эффективно доставлять, при инкапсулировании в липосомы, в брюшную полость мышей для модуляции местной или системной воспалительной реакции после индукции эндотоксином (Flynn et al., 2004). Однако, для сведения, отсутствуют ранее полученные доказательства наличия интраректального введения siPHK для даун-регуляции гена IL-12 или любого другого гена, принимающего участие в развитии патологических состояний кишечника. Заявители разработали способы снижения экспрессии IL-12 в условиях in vivo для лечения заболеваний кишечника и разработали способы доставки siPHK в кишечник при интраректальном введении.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способам и композициям для лечения патологических состояний кишечника посредством применения технологии PHKi путем интраректального введения. Композиции согласно изобретению содержат молекулы коротких интерферирующих нуклеиновых кислот (siHK) и близкие соединения, включая, но не ограничиваясь ими, siPHK. В частности, композиции согласно изобретению можно использовать в получении лекарственного препарата для лечения патологических состояний кишечника, включающих: гиперпролиферативные заболевания, в частности злокачественную опухоль ободочной и прямой кишки; аутоиммунные и воспалительные заболевания кишечника (IBD), в частности болезнь Крона; колит, в частности язвенный колит; синдром раздраженного кишечника; инфекционные заболевания кишечника, такие как псевдомембранозный колит, амебиаз или туберкулез кишечника; полипы ободочной кишки; дивертикулы; запор; непроходимость кишечника; синдромы нарушения всасывания; заболевания прямой кишки и диарею. Настоящее изобретение включает композиции и способы применения siHK, в том числе, но не ограничиваясь ими, короткие интерферирующие РНК (siHK), двухцепочечные РНК (dsPHK), микро-РНК (miPHK), антагомиры и короткие РНК-«шпильки» (shPHK), способные опосредовать РНК-интерференцию.
Способы согласно изобретению включают введение пациенту, нуждающемуся в этом, эффективного количества одной или более siHK согласно изобретению для лечения заболевания кишечника. В предпочтительных вариантах осуществления способы согласно изобретению включают интраректальное введение терапевтической siHK.
В одном варианте осуществления настоящее изобретение относится к siHK или аналогичным, синтезированным химическим путем молекулам, действие которых направлено на интерференцию экспрессии мРНК субъединиц р35 или р40 цитокина IL-12, и что, в конечном итоге, модулирует количество продуцированного белка. Композиции и способы, включающие указанную выше siPHK и близкие соединения, предназначены для лечения заболеваний, связанных со сверхэкспрессией IL-12, таких как аутоиммунные заболевания и воспалительные заболевания кишечника (IBD), в частности болезнь Крона.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Фигура 1. Олигонуклеотидные последовательности молекул siPHK, действие которых направлено на субъединицы р35 и р40 IL-12, входящие в настоящее изобретение. Последовательности SEQ ID No, приведенные на фигуре, относятся к смысловой цепи (5'→3'); как правило, siPHK вводят в виде dsPHK так, что они будут включать смысловую цепь и комплементарную ей цепь.
Фигура 2. Влияние siPHK на экспрессию субъединицы р35 IL-12 в системе in vitro. В результате обработки siPHK снижается уровень транскриптов гена р35 IL-12. РНК получали из клеток SW480, обработанных siPHK в течение различных периодов времени. Пробы анализировали ОТ-ПЦР с использованием специфических праймеров. Значения показывают средние уровни экспрессии различных транскриптов, нормализованные к 18S, в качестве гена «домашнего хозяйства».
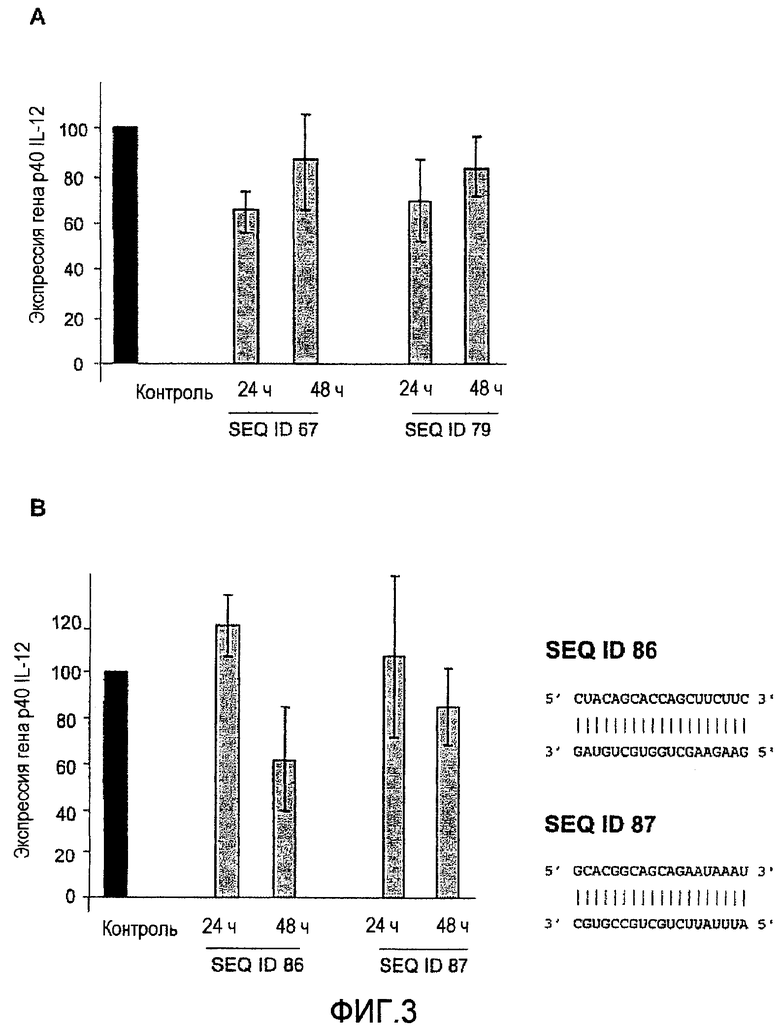
Фигура 3. Влияние siPHK на экспрессию субъединицы р40 IL-12 в системе in vitro. А: обработка siPHK приводит к снижению уровня транскриптов гена р40 IL-12 в человеческих клетках. РНК получали из клеток SW480, обработанных siPHK с последовательностями SEQ ID 67 и SEQ ID 79 в течение различного периода времени при дозе обработки, составляющей 200 нМ. Значения показывают средние уровни экспрессии различных транскриптов, нормализованные к 18S, в качестве гена «домашнего хозяйства». Значения представляют среднее значение процента нормализованных уровней мРНК при интерференции siPHK по сравнению с экспрессией контрольного гена и их средние значения стандартного отклонения среднего (SEM). В: обработка siPHK приводит к снижению уровня транскриптов гена р40 IL-12 в мышиных клетках. РНК получали из клеток С2С12, обработанных siPHK с последовательностями SEQ ID 86 и SEQ ID 87 в течение различного периода времени при дозе обработки, составляющей 100 нМ. Действие SEQ ID 86, которая является гомологичной к человеческой последовательности SEQ ID 67, направлено на субъединицу р40 мышиного IL-12. Кроме того, при наличии действия против субъединицы р40 мышиного IL-12 SEQ ID 87 представляет siPHK с наиболее высокими баллами у мышей и не имеет гомологичного siPHK-дуплекса у человека. Молекулы siPHK с последовательностями SEQ ID 86 и SEQ ID 87 представляют собой описанные ниже с 2 выступающими тимидиновыми нуклеотидными 3'-концами. Значения представляют среднее значение процента нормализованных уровней мРНК по сравнению с 18S при интереференции siPHK по сравнению с экспрессией контрольного гена и их средние значения стандартного отклонения среднего (SEM).
Фигура 4. Обработка siPHK приводит к снижению уровня транскриптов гена GFP в тонком кишечнике. Отобранную в среду ОСТ ткань исследовали микроскопией и оценивали фотопрограммой. Данные показывают обработку однократной дозой (мыши 2-3) и обработку двукратными дозами (мыши 4-5) siPHK. Значения показывают уровень экспрессии на 25 показательных снимках на мышь, относящихся к контрольным, не обработанным мышам. Представлены стандартные отклонения данных.
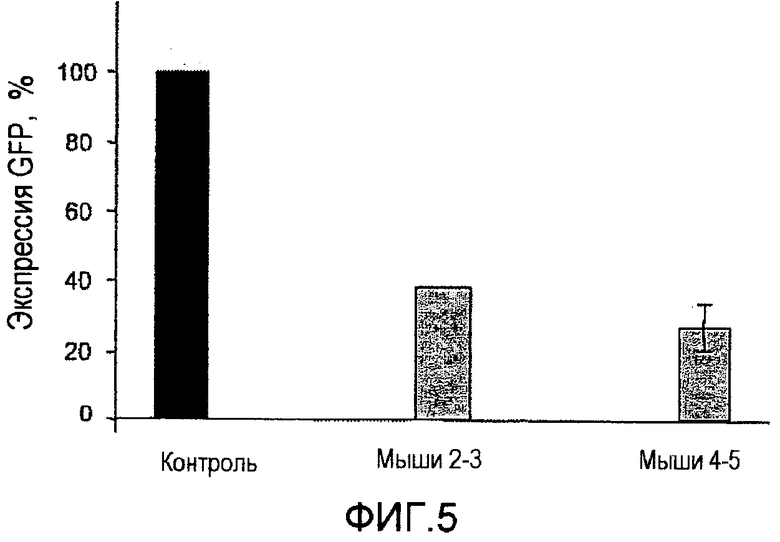
Фигура 5. Обработка siPHK приводит к снижению уровня транскриптов гена GFP в тонком кишечнике. Отобранную в РНК ткань затем исследовали, анализировали ОТ-ПЦР. Данные показывают обработку однократной дозой (мыши 2-3) и обработку двукратными дозами (мыши 4-5) siPHK. Представлены стандартные отклонения данных.
Фигура 6. Обработка siPHK приводит к снижению уровня транскриптов гена GFP в толстом кишечнике. Отобранную в среду ОСТ ткань исследовали микроскопией и оценивали фотопрограммой. Данные показывают обработку однократной дозой (мыши 2-3) и обработку двукратными дозами (мыши 4-5) siPHK. Значения показывают уровень экспрессии на 25 показательных снимках на мышь, относящихся к контрольным, не обработанным мышам. Представлены стандартные отклонения данных.
Фигура 7. Обработка siPHK приводит к снижению уровня транскриптов гена GFP в толстом кишечнике. Отобранную в РНК ткань затем исследовали, анализировали ОТ-ПЦР. Данные показывают обработку однократной дозой (мыши 2-3) и обработку двукратными дозами (мыши 4-5) siPHK. Представлены стандартные отклонения данных.
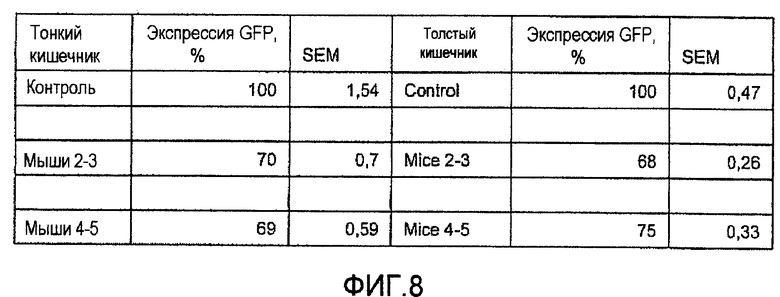
Фигура 8. Данные по пробам, отобранным в среду ОСТ.
Фигура 9. Данные по пробам, отобранным затем в РНК.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способам и композициям для лечения патологических состояний кишечника посредством применения технологии PHKi путем интраректального введения. Композиции согласно изобретению содержат молекулы короткой интерферирующей нуклеиновой кислоты (siHK), которая модулирует экспрессию генов-мишеней, связанных с развитием патологических состояний стенки кишечника.
Способы согласно изобретению включают введение пациенту, нуждающемуся в этом, эффективного количества одной или более siHK согласно изобретению.
Конструирование siPHK
Ген, на который направлено действие siHK согласно изобретению, означает ситуацию, когда, например, siHK избирательно снижает или подавляет экспрессию гена. Альтернативно, действие siHK направлено на ген, когда siHK гибридизуется в сильных условиях с транскриптом гена. siHK можно тестировать в условиях in vitro или in vivo на ее способность направленно воздействовать на ген.
В 1999 Tuschl et al. установили эффект «сайленсинга» siPHK, показав, что их эффективность является функцией длины дуплекса, длины выступающих 3'-концов и последовательности данных выступающих концов.
Выбор правильной гомологичной области в гене-мишени имеет большое значение для точного «сайленсинга». Короткий фрагмент последовательности гена-мишени (например, длиной 19-40 нуклеотидов) выбран в качестве последовательности siHK согласно изобретению. В одном варианте осуществления siHK представляет siHK. В таких вариантах осуществления короткий фрагмент последовательности гена-мишени представляет фрагмент мРНК гена-мишени. В предпочтительных вариантах осуществления критерии для выбора фрагмента последовательности из мРНК гена-мишени для возможной молекулы-кандидата siPHK включают: 1) последовательность из мРНК гена-мишени, длина которой составляет, по меньшей мере, 50-100 нуклеотидов от 5'- или 3'-конца нативной молекулы мРНК; 2) последовательность из мРНК гена-мишени, которая имеет соотношение G/C в пределах 30% до 70%, наиболее предпочтительно составляет примерно 50%; 3) последовательность из мРНК гена-мишени, которая не содержит повторяющихся последовательностей (например, ААА, ССС, GGG, ТТТ, АААА, СССС, GGGG, ТТТТ); 4) последовательность из мРНК гена-мишени, которая является доступной в мРНК, и 5) последовательность из мРНК гена-мишени, которая является уникальной для гена-мишени. Фрагмент последовательности из мРНК гена-мишени может соответствовать одному или более указанному выше критерию. В предпочтительных вариантах осуществления siPHK имеет соотношение G/C ниже 60% и/или в ней отсутствуют повторяющиеся последовательности.
На практике интересующий ген вводят в виде нуклеотидной последовательности в прогностическую программу, в которой предусмотрены все вариабельные величины, описанные выше, в целях конструирования оптимальных олигонуклеотидов. С помощью данной программы сканируется нуклеотидная последовательность любой мРНК в отношении областей, чувствительных к направленному воздействию siPHK. Результатом данного анализа является оценка в баллах олигонуклеотидов возможной siPHK. Молекулы с наиболее высокими баллами используют для конструирования олигоуклеотидов двухцепочечной РНК (как правило, длиной 21 пара нуклеотидов, хотя возможны также другие длины), которые обычно получают химическим синтезом. Заявители планируют подвергнуть тестированию несколько химических модификаций, которые хорошо известны в данной области. Данные модификации направлены на повышение стабильности или доступности олигонуклеотидов dsPHK.
Затем олигонуклеотиды-кандидаты можно «просеять» в отношении наличия межвидовой консервативности последовательности для облегчения перехода от испытаний на животных к клиническим испытаниям у людей.
В дополнение к siHK, которая является строго комплементарной к области-мишени, можно использовать вырожденные последовательности siHK для направленного воздействия на гомологичные области. В заявке WO 2005/045037 описывается конструирование молекул siHK с направленным действием на такие гомологичные последовательности, например, при включении необычных пар оснований, например ошибочно спаренных и/или неоднозначных пар оснований, которые могут обеспечить дополнительные последовательности-мишени. В тех случаях, когда ошибочно спаренные основания идентифицированы, можно использовать необычные пары оснований (например, ошибочно спаренные и/или неоднозначные пары оснований) для получения молекул siHK с направленным действием на последовательность более чем одного гена. В не ограничивающем примере необычные пары оснований, такие как пары оснований UU и СС, используют для получения молекул siHK, которые способны направленно воздействовать на последовательности различных мишеней, которые разделяют гомологию последовательностей. При этом одно преимущество применения siHK согласно изобретению заключается в том, что можно сконструировать одну siHK с включением последовательности нуклеиновой кислоты, которая является комплементарной нуклеотидной последовательности, которая консервативна для гомологичных генов. В данном подходе одну siHK можно использовать для подавления экспрессии более чем одного гена вместо применения более чем одной молекулы siHK с направленным действием на различные гены.
Идентичность последовательности можно рассчитать с помощью алгоритмов сравнения и сопоставления, известных в данной области (см. Gribskov and Devereux, Sequence Analysis Primer, Stockton Press, 1991 и цитированные там источники) и рассчитать различие в процентах между нуклеотидными последовательностями, например, при использовании алгоритма Smith-Waterman в качестве инструмента в программном обеспечении BESTFIT с использованием недостаточных параметров (например, University of Wisconsin Genetic Computing Group). Предпочтительной является идентичность последовательности, составляющая более чем 90%, 95% или 99% между siHK и участком гена-мишени. Альтернативно комплементарность между siHK и молекулой нативной РНК можно определить функционально гибридизацией, а также функционально по ее способности снижать или ингибировать экспрессию гена-мишени. Способность siHK воздействовать на экспрессию гена можно определить эмпирически в условиях in vivo и in vitro.
Предпочтительными молекулами siHK согласно изобретению являются двухцепочечные. В одном варианте осуществления двухцепочечные молекулы siHK содержат «тупые» концы. В другом варианте осуществления двухцепочечные молекулы siHK содержат выступающие нуклеотиды (например, «выступы» из 1-5 нуклеотидов, предпочтительно «выступы» из 2 нуклеотидов). В конкретном варианте осуществления выступающие нуклеотиды являются выступающими 3'-концами. В другом конкретном варианте осуществления выступающие нуклеотиды являются выступающими 5'-концами. Частью «выступа» может быть любой тип нуклеотидов. В одном варианте осуществления выступающие нуклеотид или нуклеотиды представляют рибонуклеиновые кислоты. В другом варианте осуществления выступающие нуклеотид или нуклеотиды представляют дезоксирибонуклеиновые кислоты. В предпочтительном варианте осуществления выступающие нуклеотид или нуклеотиды представляют тимидиновые нуклеотиды. В еще одном варианте осуществления выступающие нуклеотид или нуклеотиды являются модифицированными или неклассическими нуклеотидами. Выступающие нуклеотид или нуклеотиды могут представлять неклассические межнуклеотидные связи (например, иные, чем фосфодиэфирные связи).
Синтез siHK-дуплексов
siHK можно синтезировать любым методом, известным в данной области. Предпочтительно РНК синтезируют химическим путем с использованием соответствующим образом защищенных рибонуклеозидных фосфорамидитов и обычного ДНК/РНК синтезатора. Дополнительно siPHK можно получить от поставщиков промышленно доступных РНК олигосинтеза, включая, но не ограничиваясь ими, Proligo (Hamburg, Германия), Dharmacon Research (Lafayette, CO, США), Glen Research (Sterling, VA, США), ChemGenes (Ashland, MA, США) и Cruachem (Glasgow, Великобритания), Qiagen (Германия), Ambion (США) и Invitrogen (Шотландия). Альтернативно, молекулы siHK согласно изобретению можно экспрессировать в клетках при трансфекции клеток векторами, содержащими обратную комплементарную к siHK последовательность под контролем промотора. После экспрессии siHK можно выделить из клетки при использовании методов, известных в данной области.
При работе с одноцепочечными молекулами РНК необходима стадия отжига. Для отжига РНК по 30 мкл 50 мМ раствора каждого олигонуклеотида РНК объединяют в 100 мМ ацетате калия, 30 мМ HEPES-KOH рН 7,4, 2 мМ ацетате магния. Затем раствор инкубируют в течение 1 мин при 90°С, центрифугируют в течение 15 сек и инкубируют в течение 1 ч при 37°С.
В тех вариантах осуществления, в которых siPHK представляет короткую РНК-«шпильку» (shPHK), две молекулы siPHK можно соединить линкерным участком (например, нуклеотидным линкером или ненуклеотидным линкером).
Химическая модификация siHK
siHK согласно изобретению могут содержать один или более модифицированных нуклеотидов и/или нефосфодиэфирных связей. С помощью химических модификаций, известных в данной области, можно повысить стабильность, доступность и/или поглощение клетками siHK. Специалистам в данной области знакомы другие типы химических модификаций, которые можно включить в молекулы РНК (см. публикации международных заявок WO 2003/070744 и WO 2005/045037, в которых приводится обзор типов модификаций).
В одном варианте осуществления модификации можно использовать для обеспечения повышенной устойчивости к деградации или повышенного поглощения. Примеры таких модификаций включают фосфоротиоатные межнуклеотидные связи, 2'-О-метилрибонуклеотиды (особенно в смысловой цепи двухцепочечной siPHK), 2'-дезоксифторрибонуклеотиды, 2'-дезоксирибонуклеотиды, нуклеотиды с «универсальным основанием», 5-С-метилнуклеотиды и включение остатка инвертированного дезоксинуклеотида без основания (в основном см. GB 2406568).
В другом варианте осуществления модификации можно использовать для повышения стабильности siPHK или повышения эффективности направленного действия. Модификации включают химическое поперечное сшивание двух комплементарных цепей siPHK, химическую модификацию 3'- или 5'-конца цепи siPHK, модификации сахара, модификации азотистого основания и/или модификации остова, 2'-фторсодержащие модифицированные рибонуклеотиды и 2'-дезоксирибонуклеотиды (в основном см. публикацию международной заявки WO 2004/029212).
В другом варианте осуществления модификации можно использовать для повышения или снижения аффинности для комплементарных нуклеотидов в мРНК-мишени и/или в комплементарной цепи siHK (в основном см. публикацию международной заявки WO 2005/044976). Например, немодифицированный пиримидиновый нуклеотид можно заменить на 2-тио-, 5-алкинил-, 5-метил- или 5-пропинилпиримидин. Дополнительно немодифицированный пурин можно заменить на 7-деза-, 7-алкил- или 7-алкенилпурин.
В другом варианте осуществления в тех случаях, когда siHK представляет двухцепочечную siPHK, выступающие 3'-концевые нуклеотиды можно заменить на дезоксирибонуклеотиды (в основном см. Elbashir et al., 2001).
Тестирование siPHK-дуплексов в условиях in vitro
Для проверки специфичности интерференции siPHK использовали клеточные культуры, экспрессирующие гены-мишени.
В случае субъединиц р35 и р40 IL-12 использованные для опытов клетки представляли собой человеческие клетки SW480 и мышиные мышечные клетки С2С12. После инкубации клеток с соответствующими siPHK-дуплексами определяли уровни экспрессии р35 и р40. Для связывания «нокаута» под действием siPHK со специфическими фенотипами культивируемых клеток необходимо показать уменьшение концентрации белка-мишени или, по меньшей мере, показать снижение уровня мРНК-мишени.
Концентрации мРНК гена-мишени можно количественно определить ПЦР в режиме реального времени (ОТ-ПЦР). Кроме того, уровни белка можно определить различными методами, хорошо известными в данной области, такими как вестерн-блоттинг с использованием специфических антител против различных мишеней, что позволяет провести непосредственный мониторинг снижения уровня белка-мишени.
siPHK вводят в клетки методом трансфекции, хорошо известного в данной области. Единичную трансфекцию siPHK-дуплексом можно осуществить, например, при использовании катионного липида, такого как реагент липофектамин 2000 (Invitrogen), с последующим тестированием эффективности «сайленсинга» через 24, 48 и 72 ч после трансфекции.
Типичный протокол трансфекции можно осуществить следующим образом: в одной лунке 6-луночного планшета проводят трансфекцию с использованием 100 нМ siPHK для мышиных клеток С2С12 или 200 нМ siPHK для человеческих клеток SW480 в качестве конечной концентрации. Согласно протоколу с использованием реагента липофектамина 2000 за сутки до проведения трансфекции высевают 2-4×105 клеток на лунку в 3 мл соответствующей культуральной среды, содержащей DMEM, 10% сыворотки, антибиотики и глутамин, и инкубируют клетки в обычных условиях культивирования (при 37°С и 5% СО2). В день проведения трансфекции клетки должны иметь слияние, составляющее 30-50%. Разводят 12,5 мкл 20 мкМ siPHK-дуплекса (соответствует конечной концентрации 100 нМ) или 25 мкл 20 мкМ siPHK-дуплекса (соответствует конечной концентрации 200 нМ) в 250 мкл DMEM и перемешивают. Также 6 мкл липофектамина 2000 разводят в 250 мкл DMEM и перемешивают. Через 5 мин инкубации при комнатной температуре разведенный олигомер (siPHK-дуплекс) и разведенный липофектамин объединяют для образования комплекса во время инкубации в течение 20 мин при комнатной температуре. Затем комплекс наносят по каплям на клетки с 2 мл свежей культуральной среды с низким содержанием антибиотиков и осторожно перемешивают раскачиванием планшета назад и вперед для обеспечения равномерного распределения комплекса для трансфекции. Инкубируют клетки в обычных для них условиях культивирования и через сутки комплекс удаляют и вносят новую порцию полной культуральной среды. В целях мониторинга «сайленсинга» генов клетки собирают через 24, 48 и 72 ч после трансфекции.
Эффективность трансфекции может зависеть от типа клеток и также от номера пассажа и слияния клеток. Также критическими факторами являются время и характер образования комплекса siPHK-липосома (например, переворачивание по сравнению с обработкой на вортексе). Низкая эффективность трансфекции является наиболее частой причиной отсутствия успеха в «сайлесинге». Высокая степень трансфекции не является тривиальным вопросом, и для ее достижения необходимо тщательно проверить каждую новую клеточную линию, предназначенную для применения. Эффективность трансфекции можно тестировать при трансфекции генов-репортеров, например, с помощью экспрессирующей плазмиды EGFP под контролем CMV (например, от Clontech) или экспрессирующей плазмиды B-Gal и затем на следующие сутки оценить результаты фазово-контрастной и/или флуоресцентной микроскопией.
В зависимости от количества и периода полураспада (или оборота) белка-мишени наличие «нокаутного» фенотипа может стать очевидным через 1-3 суток или даже позже. В тех случаях, когда не наблюдают проявления фенотипа, можно фиксировать истощение белка иммунофлуоресценцией или вестерн-блоттингом.
После трансфекции общую фракцию РНК, экстрагированную из клеток, предварительно обрабатывают ДНК-азой I и используют для обратной транскрипции с применением произвольного праймера. Амплифицированную ПЦР с помощью пары специфических праймеров, включающих, по меньшей мере, одно экзон-экзонное сочленение используют в качестве контроля для амплификации пре-мРНК. Также в качестве контроля необходима постановка ОТ-ПЦР мРНК, не являющейся мишенью. Эффективное истощение мРНК при еще не детектируемом уменьшении концентрации белка-мишени может указывать на то, что в клетке может находиться большой запас стабильного белка. Альтернативно, амплификацию ОТ-ПЦР можно использовать для более точного тестирования снижения или исчезновения мРНК. С помощью ОТ-ПЦР количественно определяют первоначальное количество матрицы наиболее специфическим, чувствительным и воспроизводимым способом. При постановке ОТ-ПЦР определяют флуоресценцию, испускаемую во время реакции, в качестве показателя продукции ампликона во время каждого цикла ПЦР, в световом циклическом аппарате. Данный сигнал усиливается в прямой зависимости от количества продукта ПЦР в реакции. При регистрации количества эмиссии флуоресценции в каждом цикле является возможным прослеживать реакцию ПЦР во время экспоненциальной фазы, когда первое значительное увеличение количества продукта ПЦР коррелирует с первоначальным количеством матрицы-мишени.
Для подтверждения характера интерференции различным образом экспрессируемых генов IL-р35 и р40 к клеточных культурах проводят количественную ОТ-ПЦР. Для постановки количественной ОТ-ПЦР используют примерно 500 нг общей фракции РНК для обратной транскрипции с последующей амплификацией ПЦР со специфическими для каждого гена праймерами в реакции. Условия ПЦР представляют на первоначальной стадии следующее: 30 сек при 95°С, затем 40 циклов по 5 сек при 95°С, 10 сек при 62°С и 15 сек при 72°С. Количественное определение 18S мРНК используют в виде гена «домашнего хозяйства» в качестве контроля для нормализации данных. Сравнительный анализ относительной экспрессии гена является наилучшим, когда экспрессия выбранного эндогенного/внутреннего контроля является более избыточной в количественном отношении и остается постоянной, пропорционально общей РНК, среди проб. При использовании инвариантного эндогенного контроля в качестве активного стандарта количественное определение мРНК-мишени можно нормализовать в отношении различий в количестве общей РНК, внесенной в каждую реакцию. Полученные кривые амплификации со световым циклизатором анализировали в сочетании с контрольным набором ДНК, действие которого направлено на транскрибированную в условиях in vitro ДНК-матрицу бета-глобулина, с использованием протокола изготовителя. Для оценки специфичности амплифицированного продукта ПЦР строили кривую плавления. Полученные кривые плавления позволяют различить праймеры-димеры и специфический продукт ПЦР.
Интраректальное введение siHK
Опыты по интраректальному введению siHK проводили на мышах GFP C57BL/6-TG (ACTB-EGFP). Данную трансгенную линию мышей получали из питомника «The Jackson Laboratory». Трансгенных мышей использовали, поскольку гомозиготные мыши для данного трансгена погибают в течение 2 недель после рождения. Трансгенная линия мышей имеет кДНК «усиленного» GFP (EGFP) под контролем промотора куриного бета-актина и энхансера цитомегаловируса, что приводит к тому, что все ткани за исключением эритроцитов и волос становятся зелеными при возбуждении светом. Указанный штамм получали от мышей C57BL/6. кДНК, кодирующую «усиленный» зеленый флуоресцирующий белок (EGFP), присоединяли к промотору куриного бета-актина и энхансеру цитомегаловируса. Также в конструкцию включали сигнал полиаденилирования бычьего глобулина. Сайты EcoRI, включенные в праймеры ПЦР, также использовали для введения амплифицированной кДНК EGFP в экспрессирующий вектор pCAGGS, содержащий промотор птичьего бета-актина и энхансер цитомегаловируса, интрон бета-актина и сигнал полиаденилирования бычьего глобулина. Полную вставку с промотором и кодирующей последовательностью расщепляли Bam-HI и SaII и очищали в геле.
siPHK-дуплекс, использованный для интраректального введения мышам, получали от Dharmacon. Dharmacon Research Inc. (Lafayette, CO) разработали новое поколение модифицированной siPHK для применения в условиях in vivo в качестве терапевтического средства, названную siSTABLEv2. Было показано, что siPHK siSTABLEv2 производства Dharmacon обладает повышенной стабильностью в сыворотке крови по сравнению с немодифицированной siPHK. Как правило, обычные siPHK деградируют в течение нескольких минут в средах с сывороткой крови, что делает проблематичным применение siPHK в условиях in vivo. Модификация siSTABLEv2 существенно повышает стабильность siPHK в сыворотке крови, как представлено на сайте Dharmacon (http://www/dharmon.com/docs/siSTABLE%20v2%20Flier.pdf).
siPHK использовали для даун-регуляции экспрессии мРНК EGFP с направленным действием на следующую последовательность в мРНК EGFP: 5'-GGC UAC GUC CAG GAG CGC ACC-3' (SEQ ID No 88). Смысловая цепь siPHK-дуплекса представляла 5'-P GGC UAC GUC CAG CGC ACC-3' (SEQ ID No 89), и антисмысловая цепь представляла 5'-P U GCG CUC CUG GAC GUA GCC UU-3' (SEQ ID No 90). Указанную последовательность производства Dharmacon используют в качестве пресинтезированного контрольного siPHK-дуплекса зеленого флуоресцирующего белка.
Для проведения опытов по интраректальному введению использовали мышей C57BL/TG (ACTB-EGFP) (самцов в возрасте 8 недель). Животных содержали в клетках со свободным доступом к корму и воде до дня перед проведением обработки. Для терапевтического «сайленсинга» при интраректальном введении мышей выдерживали голодными в течение одного дня до проведения обработки. Лекарственные средства применяли, как правило, введением небольшого объема (120 мкл) в прямую кишку. Контрольным животных обрабатывали только наполнителем. Во всех случаях животных умерщвляли через 2 суток после первого введения дислокацией шейных позвонков. Протокол применения siPHK у мышей представлял собой следующее. Для каждого экспериментального введения 60 мкл siPHK-дуплекса предварительно смешивали с 60 мкл NaCl (1,8% мас./об.) до физиологических концентраций. Во всех случаях животных умерщвляли через 2 суток после первого введения.
Использованные экспериментальные условия приведены в таблице ниже. Каждый опыт проводили в двух параллелях. Мышей 2 и 3 обрабатывали интраректально одной дозой, составляющей 250 мкг (19 наномоль) siPHK с действием на GFP, в то время как мышей 4 и 5 обрабатывали двумя дозами по 125 мкг siPHK в течение двух суток.
Схематичное распределение экспериментальных условий для интраректального введения siPHK. Дозы siPHK указаны в таблице.
Отбирали образцы тканей и анализировали двумя методами: один в среде ОСТ и другой затем в РНК (Amblon). Блоки в ОСТ хранили при -80°С до обработки данных. Из блоков в ОСТ готовили срезы толщиной 12 мкм на криостате (Leica CM 1850) при -20°С. Отобранные срезы анализировали под флуоресцентным микроскопом (Olympus BX51), соединенным с цифровой камерой (DP70) при использовании фильтра 488 нм. Для всех проб были установлены чувствительные условия (ISO200), разрешение размера изображения (2040×1536) и время экспозиции (1 сек) в целях сравнения их между собой. Зеленое флуоресцентное свечение определяли в качестве показателя экспрессии GFP с помощью программы Adobe Photoshop (версия 8,0). С помощью данного метода собирали 25 различных снимков для каждой анализированной ткани. Ткани, отобранные затем в РНК, хранили при -20°С. Затем РНК удаляли перед экстракцией РНК. РНК выделяли с помощью тризолового реагента (Invitrogen) согласно протоколу изготовителя. Обработку ДНК-азой проводили перед определением экспрессии GFP с помощью ОТ-ПЦР, как описано выше.
Фармацевтические композиции и пути введения
Настоящее изобретение может включать введение одного или более видов молекул siHK одновременно. Данные виды молекул можно выбрать для обеспечения направленного действия в отношении одного или более генов-мишеней.
В одном варианте осуществления один тип siHK вводят в терапевтических способах согласно изобретению. В одном варианте осуществления siHK согласно изобретению вводят в комбинации с другой siHK согласно изобретению и/или с одним или более другим терапевтическим средством, не относящимся к siHK, пригодным для лечения, профилактики или контроля заболевания стенки кишечника. Термин «в комбинации с» не ограничивается введением терапевтических средств точно в одно и то же время, а в большей степени означает, что siHK согласно изобретению и другие средства вводят пациенту в последовательности и в течение периода времени, чтобы лечебный эффект комбинации был выше по сравнению с лечебным эффектом, когда их вводят иначе. Например, каждое терапевтическое средство можно вводить в одно время или последовательно в любом порядке в различные временные точки; однако, если их не вводят в одно и то же время, то их следует вводить достаточно близко во времени, чтобы обеспечить желаемое терапевтическое действие. Каждое терапевтическое средство можно вводить по отдельности, в любой соответствующей форме и любым подходящим путем.
siHK согласно изобретению можно формулировать в фармацевтические композиции любым обычным способом, известным в данной области (см., например, Alfonso G. et al., 1995; в The Science and Practice of Pharmacy, Mack Publishing, Easton PA, 19th ed.). Композиции, содержащие одну или более siHK для применения в способах согласно изобретению, могут находиться в многочисленных формах, и они могут зависеть от различных факторов, специфических для каждого пациента (например, в зависимости от типа и тяжести заболевания, типа вводимой siHK, возраста, массы тела, ответной реакции и анамнеза заболевания у пациента), числа и типа siHK в композиции, формы композиции (например, жидкой, полужидкой и твердой формы), схемы лечения (например, вводят терапевтическое средство в течение времени в виде медленной инфузии, однократного болюса, один раз в сутки, несколько раз в сутки или один раз в несколько суток) и/или пути введения (например, местным, пероральным, внутривенным, внутримышечным, внутриартериальным, интрамедуллярным, интратекальным, трансдермальным, подкожным, внутрибрюшинным, интраназальным, энтеральным или сублингвальным путями).
Молекулы siHK согласно изобретению и их лекарственные формы или композиции можно вводить непосредственно или местно, как это, в основном, известно в данной области. Например, молекула siHK может включать наполнитель для доставки, в том числе липосомы, для введения субъекту. В фармацевтически приемлемых композициях могут присутствовать носители и разбавители и их соли. Молекулы нуклеиновой кислоты можно вводить в клетки различными способами, известными специалистам в данной области, включая, но не ограничиваясь ими, инкапсулирование в липосомы, ионофорез или включение в другие наполнители, такие как биодеградируемые полимеры, гидрогели, циклодекстрины, микросферы из поли(молочной-со-гликолевой кислоты) (PLGA) и PLCA, биодеградируеме нанокапсулы и биоадгезивные микросферы, или с помощью белковых векторов. В другом варианте осуществления молекулы нуклеиновой кислоты согласно изобретению также можно формулировать или подвергнуть комплексообразованию с полиэтиленимином или его производными, такими как производные полиэтилениминполиэтиленгликоль-N-ацетилгалактозамина (PEI-PEG-GAL) или полиэтилениминполиэтиленгликоль-три-N-ацетилгалактозамина (PEI-PEG-триGAL).
Молекулу siHK согласно изобретению можно сочетать с разрушающими мембрану средствами и/или молекулой катионогенного липида или липида-хэлпера.
Системы для доставки, которые можно использовать в изобретении, включают, например, водные и неводные гели, кремы, сложные эмульсии, микроэмульсии, липосомы, мази, водные и неводные растворы, лосьоны, аэрозоли, углеводородные основы и порошки, и они могут содержать наполнители, такие как солюбилизаторы, усилители проникновения (например, жирные кислоты, сложные эфиры жирных кислот, жирные спирты и аминокислоты) и гидрофильные полимеры (например, поликарбофил и поливинилпиролидон). В одном варианте осуществления фармацевтически приемлемый носитель представляет липосому или вещество, усиливающее проникновение через кожу.
Фармацевтическая композиция согласно изобретению находится в форме, подходящей для введения, например системного или местного введения, в клетку или субъекту, включая, например, человека. Подходящие формы частично зависят от применения или пути введения, например перорального, трансдермального или с помощью инъекции. В данной области известны другие факторы, такие как токсичность и формы, которые предупреждают действие композиции или лекарственной формы.
Также настоящее изобретение включает композиции, приготовленные для хранения или введения, например которые содержат фармацевтически эффективное количество желаемых соединений в фармацевтически приемлемом носителе или разбавителе. Приемлемые носители или разбавители для терапевтического применения являются хорошо известными в данной области. Например, к ним относятся консерванты, стабилизаторы, красители и вкусовые вещества. Таковые включают бензоат натрия, сорбиновую кислоту и сложные эфиры п-оксибензойной кислоты. В дополнение можно использовать антиоксиданты и суспендирующие вещества.
Фармацевтически эффективной дозой является доза, необходимая для профилактики, подавления проявления или лечения (ослабления до некоторой степени симптома, предпочтительно всех симптомов) заболевания. Фармацевтически эффективная доза зависит от типа заболевания, используемой композиции, пути введения, типа млекопитающего, которое подвергается лечению, физического состояния конкретного млекопитающего, которое подвергается лечению, конкурентного лечения и других факторов, которые известны специалистам в данной области.
Композиции согласно изобретению можно вводить в разовых лекарственных формах, содержащих обычные, нетоксичные, фармацевтически приемлемые носители, адъюванты и/или наполнители. Композиции могут находиться в форме, подходящей для перорального приема, например в виде таблеток, пастилок, лозенджиз, водной или масляной суспензий, диспергируемых порошков или гранул, эмульсии, твердых или мягких капсул, или сиропов, или эликсиров. Композиции, предназначенные для приема внутрь, можно приготовить любым методом, известным в данной области для производства фармацевтических композиций, и такие композиции могут содержать одно или более из подсластителей, вкусовых веществ, красителей или консервантов для получения фармацевтических препаратов, удобных в употреблении и приятных на вкус. Таблетки содержат активный ингредиент в смеси с нетоксичными, фармацевтически приемлемыми наполнителями, которые подходят для производства таблеток.
Такие наполнители могут представлять собой, например, инертные разбавители, такие как карбонат кальция, карбонат натрия, лактозу, фосфат кальция или фосфат натрия; вещества для грануляции и разрыхлители, например кукурузный крахмал или альгиновая кислота; связующие вещества, например крахмал, желатин или аравийская камедь; и скользящие вещества, например стеарат магния, стеариновая кислота или тальк. Таблетки могут быть без оболочек, и также их можно покрыть оболочкой известными методами. В некоторых случаях такие оболочки можно приготовить известными методами для замедления разрыхления и всасывания в желудочно-кишечном тракте и, тем самым, обеспечить непрерывное действие в течение более длительного периода времени. Например, можно использовать вещество, которое замедляет всасывание, такое как глицерилмоностеарат и глицерилдистеарат.
Композиции для перорального применения также могут находиться в виде твердых желатиновых капсул, в которых активный ингредиент смешан с инертным твердым разбавителем, например карбонатом кальция, фосфатом кальция или каолином, или в виде мягких желатиновых капсул, в которых активный ингредиент смешан с водой или маслом, например кокосовым маслом, жидким парафином или оливковым маслом.
Водные суспензии содержат активные вещества в смеси с наполнителями, подходящими для получения водных суспензий. Такими наполнителями являются суспендирующие вещества, например натриевая соль карбоксиметилцеллюлозы, метилцеллюлоза, гидроксипропилметилцеллюлоза, альгинат натрия, поливинилпирролидон, трагакантовая камедь и аравийская камедь; диспергирующие или смачивающие вещества могут представлять собой природный фосфатид, например лецитин, или продукты конденсации алкиленоксида с жирными кислотами, например полиоксиэтиленстеарат, или продукты конденсации этиленоксида с алифатическими спиртами с длинной цепью, например гептадекаэтиленоксицетанол, или продукты конденсации этиленоксида с неполными сложными эфирами, полученными из жирных кислот и гексита, такие как полиоксиэтиленсорбит моноолеат, или продукты конденсации этиленоксида с неполными сложными эфирами, полученными из жирных кислот и ангидридов гексита, например полиэтиленсорбитан моноолеат. Водные суспензии могут также содержать один или более консервантов, например этил- или н-пропил-п-гидроксибензоат, один или более красителей, одно или более вкусовых веществ и один или более подсластителей, таких как сахароза или сахарин.
Масляные суспензии можно формулировать суспендированием активных ингредиентов в растительном масле, например арахисовом масле, оливковом масле, кунжутном масле, или кокосовом масле, или минеральном масле, таком как жидкий парафин. Масляные суспензии могут содержать загуститель, такой как пчелиный воск, твердый парафин или цетиловый спирт. Можно добавить подсластители и вкусовые вещества для обеспечения приятных на вкус препаратов для приема внутрь. Данные композиции можно длительно хранить при добавлении антиоксиданта, такого как аскорбиновая кислота.
Диспергируемые порошки и гранулы, подходящие для получения водной суспензии при добавлении воды, обеспечивают активный ингредиент в смеси с диспергирующим или смачивающим веществом, суспендирующим веществом и одним или более консервантами. Примерами подходящих диспергирующих или смачивающих веществ или суспендирующих веществ являются приведенные выше. Могут также присутствовать дополнительные наполнители, например подсластители, вкусовые вещества или красители.
Фармацевтические композиции согласно изобретению также могут находиться в форме эмульсий масло-в-воде. Масляная фаза может представлять собой растительное масло, или минеральное масло, или их смеси. Подходящими эмульгаторами могут быть природные камеди, например аравийская камедь или трагакантовая камедь, природные фосфатиды, например масло соевых бобов, лецитин и сложные эфиры или неполные сложные эфиры, полученные из жирных кислот и гексита, ангидриды, например сорбитан моноолеат, и продукты конденсации указанных неполных сложных эфиров с этиленоксидом, например полиоксиэтиленсорбитан моноолеат. Также эмульсии могут содержать подсластители и вкусовые вещества.
Сиропы и эликсиры можно приготовить с подсластителями, например глицерином, пропиленгликолем, сорбитом, глюкозой или сахарозой. Также такие композиции могут содержать снимающее раздражение средство, консервант и вкусовое вещество и краситель. Фармацевтические композиции могут находиться в форме стерильной инъекционной водной или масляной суспензии.
Суспензию можно приготовить способами, известными в данной области, с использованием подходящих диспергирующих или смачивающих веществ и суспендирующих веществ, которые уже указывались выше.
Стерильный инъекционный препарат также может представлять собой стерильный инъекционный раствор или суспензию в нетоксичном, приемлемом для парентерального введения разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. К приемлемым носителям или растворителям, которые можно использовать, относятся вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, в качестве растворителя или суспендирующей среды обычно применяют стерильные нежирные масла. Для данной цели можно использовать любое мягкое нежирное масло, включая синтетические моно- или диглицериды. Кроме того, при приготовлении инъекционных препаратов находят применение жирные кислоты, такие как олеиновая кислота.
Молекулы нуклеиновых кислот согласно изобретению можно также вводить в виде суппозиториев, например, для ректального введения лекарственного средства. Данные композиции можно приготовить смешением лекарственного средства с подходящим, не вызывающим раздражения наполнителем, который является твердым при обычной температуре, но становится жидким при температуре прямой кишки и, следовательно, будет плавиться в прямой кишке с высвобождением лекарственного средства. Такие вещества включают какао-масло и полиэтиленгликоли.
Молекулы нуклеиновых кислот согласно изобретению можно вводить парентерально в стерильной среде. Лекарственное средство в зависимости от используемого наполнителя и концентрации можно суспендировать или растворить в наполнителе. Преимущественно адъюванты, такие как местные анестетики, консерванты и забуферивающие вещества, можно растворить в наполнителе.
Для введения животным, не являющимся человеком, композицию можно также добавить в корм или питьевую воду для животного. Может быть удобно формулировать композиции в виде корма или питьевой воды для животного так, чтобы животное принимало их в терапевтически соответствующем количестве композиции вместе с рационом. Также может быть удобно приготовить композицию в виде премикса для добавления в корм или питьевую воду.
Молекулы нуклеиновых кислот согласно изобретению также можно вводить субъекту в комбинации с другими терапевтическими средствами для повышения общего терапевтического эффекта. Применение многих соединений для лечения заболевания может привести к повышению лечебного действия и одновременно к снижению проявления побочных эффектов.
Альтернативно, некоторые молекулы siHK согласно изобретению можно экспрессировать в клетках из эукариотических промоторов. Рекомбинантные векторы, способные экспрессировать молекулы siHK, можно доставить, и они будут сохраняться в клетках-мишенях. Альтернативно, можно использовать векторы, которые обеспечивают временную экспрессию молекул нуклеиновых кислот. Такие векторы можно вводить многократно, по необходимости. После экспрессии молекула siHK взаимодействует с мРНК-мишенью и индуцирует ответную PHKi. Доставка экспрессирующих молекулу siHK векторов может быть системной, такой как внутривенное или внутримышечное введение, может представлять собой введение в клетки-мишени, эксплантированные от субъекта, с последующим их введением субъекту или может быть обеспечена другими способами, позволяющими провести введение в желаемую клетку-мишень.
Результаты
Пример 1. Конструирование siHK
Номера в GenBank, соответствующие субъединицам IL-12 р35 (интерлейкин 12А, стимулирующий фактор 1 природных клеток-киллеров, фактор 1 созревания цитотоксических лимфоцитов, р35) и р40 (интерлейкин 12В, стимулирующий фактор 2 природных клеток-киллеров, фактор 2 созревания цитотоксических лимфоцитов, р40), представляют соответственно NM_000882 и NM_002187.
Соответствующие нуклеотидные последовательности мРНК вводили в патентованную прогностическую программу, описанную выше, и получали молекулы siHK с направленным действием на субъединицы-мишени р35 и р40 IL-12. Результатом данного анализа была оценка в баллах олигонуклеотидов возможных siHK, таковые с наиболее высокими баллами использовали для конструирования олигонуклеотидов двухцепочечной РНК (как правило, длиной 19 пар нуклеотидов), которые обычно получали химическим синтезом.
В предпочтительных вариантах осуществления композиции siHK согласно изобретению представляют любую из последовательностей SEQ ID No: 1-81 на фигуре 1; как правило, их вводят в виде дуплекса смысловой цепи и антисмысловой цепи. Изобретение также включает siHK, которые имеют длину 40 нуклеотидов или менее и которые представляют любую нуклеотидную последовательность из последовательностей SEQ ID No: 1-81. В конкретном варианте осуществления siHK имеет длину 21-30 нуклеотидов и представляет любую из последовательностей SEQ ID No: 1-81 на фигуре 1. Все молекулы siHK, использованные в представленных ниже опытах, были сконструированы таким образом, чтобы у них было 2 выступающих 3'-концевых тимидиновых нуклеотида.
Пример 2. Опыты в условиях in vitro для р35 IL-12
Для оценки подавления гена-мишени р35 IL-12 панель siPHK, представленную на фигуре 1, анализировали в клеточных культурах. Для тестирования отбирали siPHK с наилучшими характеристиками и вносили в соответствующую клеточную культуру, такую как SW480. Влияние siPHK на ген-мишень анализировали ОТ-ПЦР согласно протоколу изготовителя. Уровень транскриптов гена-мишени нормализовали с использованием 18S в качестве гена «домашнего хозяйства». Некоторые различные siPHK, которые тестировали, и их различные эффективности в отношении интерференции гена-мишени представлены на фигуре 2. Данные результаты соответствуют последовательностям SEQ ID No 8 и SEQ ID No 17 на фигуре 1 в клетках SW480, экспрессирующих р35. Значения представляют среднее значение процента нормализованных уровней мРНК при интерференции siPHK по сравнению с экспрессией контрольного гена и их средние стандартные отклонения (SEM). Концентрация транскриптов р35 после обработки siPHK существенно снижалась при обработке siPHK, соответствующим последовательностям SEQ ID No 8 и SEQ ID No 17, в клетках SW480 по сравнению с контрольными клетками. Снижение экспрессии гена зависит от эффективности «сайленсинга» siPHK. Фактически siPHK с последовательностью SEQ ID No 8 приводила к снижению экспрессии гена р35 на 56% на 24 ч по сравнению с контролем.
Пример 3. Опыты в условиях in vitro для р40 IL-12
Для оценки подавления гена-мишени р40 IL-12 анализировали панель siPHK, представленную на фигуре 1. siPHK с наилучшими характеристиками конструировали, как описано выше, и тестировали в человеческих и мышиных клетках. Уровень транскриптов гена-мишени анализировали ОТ-ПЦР и нормализовали с использованием 18S в качестве гена «домашнего хозяйства». Данные результаты соответствуют последовательностям SEQ ID No 67, SEQ ID No 79 в клетках SW480, экспрессирующих р40 (фигура 3А); и SEQ ID No 86 и SEQ ID No 87 в клетках С2С12, экспрессирующих р40 (фигура 3В). Молекулы siPHK с последовательностями SEQ ID No 86 и SEQ ID No 87 представлены на фигуре с 2 выступающими 3'-концевыми тимидиновыми нуклеотидами.
Концентрация транскрипта р40 после обработки siPHK существенно снижалась после обработки siPHK, соответствующей последовательности SEQ ID No 67, в клетках SW480, на 65% по сравнению с контрольными клетками. В клетках С2С12 siPHK с последовательностью SEQ ID No 86, приводила к снижению экспрессии гена на 61% на 48 ч по сравнению с контролем. Важно отметить, что последовательности SEQ ID No 67 и SEQ ID No 86 соответствуют гомологичным областям гена человеческой и мышиной р40 IL-12 соответственно.
Обобщение результатов опытов, приведенных на фигурах 2 и 3, представлено в последующей таблице:
Пример 4. Опыты в условиях in vivo. Анализ тонкого кишечника
siPHK применяли для определения должной доставки siPHK в кишечник. Для оценки влияния siPHK образцы тонкого кишечника отбирали в среду ОСТ и анализировали, как описано выше. Поскольку целью было установление даун-регуляции уровня транскриптов гена GFP, то определяли интенсивность флуоресценции после применения siPHK. У животных во время постановки опытов не наблюдали вторичных эффектов.
Животных первой группы (животные 2 и 3) обрабатывали однократной дозой, равной 250 мкг siPHK, и умерщвляли через 48 ч. Результаты показывают достоверное снижение флуоресценции при сравнении с контрольной мышью. Более того, при введении siPHK (250 мкг) в двух дозах по 125 мкг и анализе через 48 ч после первого введения уменьшение экспрессии GFP было аналогичным таковому после однократного применения. Результаты приведены на фигуре 4. Представлено среднее значение данных для каждого опыта.
В то же время затем отбирали образцы тонкого кишечника в РНК для подтверждения ранее полученных данных. Концентрацию мРНК определяли ОТ-ПЦР. Данные результаты, представленные на фигуре 5, подтверждают предыдущие данные, полученные при определении интенсивности флуоресценции.
Как представлено на фигуре 5, введенная в одном или двух применениях доза 250 мкг siPHK была адекватной и достаточной для снижения уровня мРНК GFP в тонком кишечнике, что, тем самым, подтверждает доставку siPHK в тонкий кишечника при интраректальном введении. Уровень снижения по сравнению с контролем был выше при анализе ОТ-ПЦР за счет более высокой чувствительности метода.
Пример 5. Опыты в условиях in vivo. Анализ толстого кишечника
Затем таким же образом анализу подвергали толстый кишечник. В целях оценки влияния siPHK образцы толстого кишечника, отобранные в среду ОСТ, анализировали для установления снижения концентрации GFP по определению интенсивности флуоресценции после применения siPHK. Результаты свидетельствуют о достоверном уменьшении флуоресценции при сравнении с контрольной мышью (фигура 6). Более того, при введении дозы в двух дозах по 125 мкг и анализе через 48 ч после первого введения уменьшение экспрессии было аналогичным таковому после однократного применения siPHK, что указывает на эффективность обработки.
Как и в случае тонкого кишечника, образцы толстого кишечника затем отбирали в РНК и данные по концентрациям мРНК представлены на фигуре 7. Данные, полученные при постановке ОТ-ПЦР, подтверждают ранее полученные при анализе интенсивности флуоресценции. Указанные результаты открывают новый путь для терапевтического применения siPHK при лечении заболеваний кишечника.
Данные по пробам, отобранным в среду ОСТ и затем в РНК, обобщены соответственно на фигурах 8 и 9.
Заявители также исследовали наличие возможного снижения экспрессии GFP других отобранных тканях мышей; уменьшение отсутствовало в тканях мочевого пузыря, почек, легких, яичников и печени, на основании чего можно предположить, что интраректальное введение siPHK можно использовать для специфически направленного воздействия на ткань-мишень.
ССЫЛКИ




| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕЧЕНИЕ ГЛАЗНЫХ БОЛЕЗНЕЙ, ОТЛИЧАЮЩИХСЯ ПОВЫШЕННЫМ ВНУТРИГЛАЗНЫМ ДАВЛЕНИЕМ, С ПОМОЩЬЮ siPHK | 2005 |
|
RU2407531C2 |
| ЛЕЧЕНИЕ НАРУШЕНИЙ ЦНС | 2007 |
|
RU2426544C2 |
| миРНК И ИХ ПРИМЕНЕНИЕ В СПОСОБАХ И КОМПОЗИЦИЯХ ДЛЯ ИНГИБИРОВАНИЯ ЭКСПРЕССИИ ГЕНА ORAI1 | 2014 |
|
RU2689607C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ИНГИБИРОВАНИЯ ЭКСПРЕССИИ РЕЦЕПТОРА P2Х7 | 2005 |
|
RU2410430C2 |
| ОЛИГОРИБОНУКЛЕОТИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ОСТРОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТИ И ДРУГИХ ЗАБОЛЕВАНИЙ | 2005 |
|
RU2434942C2 |
| ОЛИГОРИБОНУКЛЕОТИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ОСТРОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТИ | 2005 |
|
RU2584609C2 |
| МОДУЛИРОВАНИЕ ЭКСПРЕССИИ 11БЕТА-ГИДРОКСИСТЕРОИДНОЙ ДЕГИДРОГЕНАЗЫ 1 ДЛЯ ЛЕЧЕНИЯ ГЛАЗНЫХ БОЛЕЗНЕЙ | 2006 |
|
RU2420582C2 |
| ПОЛИКОНЪЮГАТЫ ДЛЯ ВВЕДЕНИЯ IN VIVO ПОЛИНУКЛЕОТИДОВ | 2007 |
|
RU2430740C2 |
| МИ-РНК И ИХ ПРИМЕНЕНИЕ В СПОСОБАХ И КОМПОЗИЦИЯХ ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ ГЛАЗНЫХ СОСТОЯНИЙ | 2013 |
|
RU2663100C2 |
| КиРНК И ИХ ИСПОЛЬЗОВАНИЕ В СПОСОБАХ И КОМПОЗИЦИЯХ ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ ГЛАЗНЫХ ЗАБОЛЕВАНИЙ | 2012 |
|
RU2653766C2 |










Группа изобретений относится к медицине, а именно к гастроэнтерологии, и может быть использована для лечения заболеваний кишечника. Для этого используют интраректальное введение соединений, вызывающих РНК-интеференцию. Кроме того, предложены соединения PHKi с определенной нуклеотидной последовательностью, вызывающие РНК-интерференцию и предназначенные для интраректального введения, мишенью которых является ген интерлейкина-12. Предложенные соединения также могут быть использованы для лечения заболеваний кишечника. Изобретения обеспечивают эффективное лечение заболеваний за счет эффективного достижения и воздействия на мишени действия. 7 н. и 36 з.п. ф-лы, 2 табл., 9 ил.
1. Способ лечения заболевания кишечника, включающий интраректальное введение пациенту соединения, вызывающего РНК-интерференцию.
2. Способ по п.1, где заболевание является заболеванием тонкого кишечника.
3. Способ по п.1, где заболевание является заболеванием толстого кишечника.
4. Способ по п.1, где заболевание является заболеванием прямой кишки.
5. Способ по п.1, где заболевание выбрано из группы, включающей гиперпролиферативные заболевания, в частности злокачественную опухоль ободочной и прямой кишки; аутоиммунные и воспалительные заболевания кишечника (IBD), в частности болезнь Крона; колит, в частности язвенный колит; синдром раздраженного кишечника; инфекционные заболевания кишечника, такие как псевдомембранозный колит, амебиаз или туберкулез кишечника; полипы ободочной кишки; дивертикулы; запор; непроходимость кишечника; синдромы нарушения всасывания; заболевания прямой кишки и диарею.
6. Способ по любому из пп.1-5, где соединение ингибирует экспрессию гена-мишени с измененными уровнями у нуждающегося в этом пациента.
7. Способ по п.6, где экспрессия гена-мишени ингибируется в клетке, отличной от дендритной клетки.
8. Способ по п.7, где экспрессия гена-мишени ингибируется в эпителиальной клетке кишечника.
9. Способ по п.1, где указанное соединение представляет собой siHK.
10. Способ по п.9, где siHK представляет собой siPHK.
11. Способ по п.9, где siHK представляет собой dsPHK.
12. Способ по п.9, где siHK представляет собой shPHK.
13. Способ по п.1, где указанное соединение ингибирует уровни мiPHK.
14. Способ по п.1 или 9, где указанное соединение содержит модифицированный олигонуклеотид.
15. Способ по п.9, где siHK имеет длину из 40 пар нуклеотидов или менее.
16. Способ по п.9 или 15, где siHK имеет выступающие 3′-концы.
17. Способ по п.16, где выступающие 3′-концы представляют собой динуклеотиды.
18. Способ по п.17, где динуклеотидные «выступы» состоят из тимидиновых нуклеотидов.
19. Способ по п.1 или 9, дополнительно включающий введение дополнительных видов соединений, которые вызывают РНК-интерференцию.
20. Способ по п.19, где указанные дополнительные виды соединений направлены на один и тот же вид мРНК.
21. Способ по п.19, где указанные дополнительные виды соединений направлены на различные виды мРНК.
22. Способ по п.1 или 9, где соединение ингибирует экспрессию гена-мишени, принимающего участие в развитии воспалительного заболевания кишечника (IBD).
23. Способ по п.22, где IBD представляет собой болезнь Крона.
24. Способ по п.22, где ген-мишень представляет собой ген интерлейкина-12.
25. Способ по п.22, где соединение представляет собой siHK.
26. Способ по п.25, где siHK выбрана из группы, состоящей из последовательностей SEQ ID No 1-SEQ ID No 85.
27. Способ по п.25, где siHK имеет длину из 40 пар нуклеотидов или менее и содержит нуклеотидную последовательность, выбранную из группы, состоящей из последовательностей SEQ ID No 1-SEQ ID No 85.
28. Способ по п.27, где siHK направлена на субъединицу интерлейкина-12 массой 35 кДа (IL12-p35) и содержит нуклеотидную последовательность, выбранную из группы, состоящей из последовательностей SEQ ID No 1-SEQ ID No 33.
29. Способ по п.27, где siHK направлена на субъединицу интерлейкина-12 массой 40 кДа (IL12-p40) и содержит нуклеотидную последовательность, выбранную из группы, состоящей из последовательностей SEQ ID No 34-SEQ ID No 85.
30. Применение соединения, которое вызывает РНК-интерференцию, в получении лекарственного средства для лечения заболевания кишечника, где указанное соединение вводят пациенту интраректально.
31. Применение siHK, направленной на IL-12, вызывающей РНК-интерференцию, в получении лекарственного средства для лечения заболевания кишечника, где siHK вводят пациенту интраректально.
32. Применение по п.31, где заболевание кишечника представляет собой воспалительное заболевание кишечника (IBD).
33. Применение по п.32, где IBD представляет собой болезнь Крона.
34. Применение по пп.31-33, где siHK выбрана из группы, состоящей из последовательностей SEQ ID No 1-SEQ ID No 85.
35. Соединение PHKi, направленное на интерлейкин-12, вызывающее РНК-интерференцию, имеющее нуклеотидную последовательность, выбранную из группы SEQ ID No 1-SEQ ID No 85, предназначенное для интраректального введения.
36. Соединение по п.35, где PHKi представляет собой dsPHK, siPHK или shPHK.
37. Соединение по п.35, направленное на субъединицу интерлейкина-12 массой 35 кДа (IL12-p35), содержащее нуклеотидную последовательность, выбранную из группы, состоящей из последовательностей SEQ ID No 1-SEQ ID No 33.
38. Соединение по п.35, направленное на субъединицу интерлейкина-12 массой 40 кДа (IL12-p40), содержащее нуклеотидную последовательность, выбранную из группы, состоящей из последовательностей SEQ ID No 34-SEQ ID No 85.
39. Фармацевтическая композиция, содержащая одну или множество siHK по п.35, вызывающих РНК-интерференцию, составленная для интраректального введения.
40. Способ подавления экспрессии IL12-p40 и/или IL12-p35 у пациента, включающий интраректального введения указанному пациенту соединения, вызывающего РНК-интерференцию по любому из пп.35-38, так, чтобы экспрессия IL12-p40 и/или IL12-p35 подавлялась.
41. Применение соединения, вызывающего РНК-интерференцию, по любому из пп.35-38, где указанное соединение вводят указанному пациенту интраректально, в производстве лекарственного средства для лечения заболевания или состояния, связанного с IL12-p40 и/или IL12-p35, при котором указанное лекарственное средство подавляет экспрессию IL12-р40 и/или IL12-p35.
42. Применение по п.41, где заболевание представляет собой аутоиммунное заболевание или воспалительное заболевание кишечника (IBD).
43. Применение по п.42, где заболевание представляет рассеянный склероз, диабет или болезнь Крона.
| NEURATH M.F | |||
| et al | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
| СПОСОБ ЛЕЧЕНИЯ ЯЗВЕННОГО КОЛИТА | 2000 |
|
RU2165758C1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| MARION F | |||
| et al | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
2011-05-20—Публикация
2006-03-14—Подача