Область техники
Настоящее изобретение относится к новым соединениям оксазола и фармацевтическим композициям.
Предпосылки изобретения
Различные соединения оксазола были разработаны и описаны в таких документах, как WO 03/072102, WO 98/15274 и т.д. Однако соединения оксазола по настоящему изобретению не раскрыты в литературе.
Сообщалось о некоторых соединениях, обладающих специфическим ингибирующим действием против фосфодиэстеразы 4 (PDE4). Тем не менее, известны ингибиторы PDE4, имеющие побочные эффекты, такие как вызывающие рвоту, тошноту и т.д., и/или такой минус, как недостаточная ингибирующая активность в отношении PDE4. Вследствие этого известные ингибиторы PDE4 не используются в клинических целях в качестве терапевтических средств.
Раскрытие изобретения
Целью настоящего изобретения является предоставление соединения, обладающего ингибирующим действием против PDE4 и не имеющего вышеупомянутых проблем предшествующего уровня техники.
Авторы настоящего изобретения провели всесторонние исследования для решения вышеописанных проблем и достигли цели в синтезе соединения оксазола с новой структурой, соединения, обладающего высокой специфичностью и сильным ингибирующим действием в отношении PDE4. Более того, авторы настоящего изобретения обнаружили, что соединения оксазола способны к проявлению профилактического и/или терапевтического действия в отношении PDE-опосредованных заболеваний, в частности, таких как атопический дерматит, основанного на их ингибирующем действии в отношении PDE4. Более того, авторы обнаружили, что соединение обладает низкой способностью протекать в кровь при чрескожном введении и, таким образом, имеет низкие системные побочные эффекты.
Авторы настоящего изобретения также обнаружили, что соединение оксазола способны к проявлению ингибирующего действия в отношении фактора некроза опухоли α (TNF-α).
Известно, что при хронических воспалительных заболеваниях, таких как аутоиммунные заболевания и аллергические заболевания, цитокины, продуцируемые иммунокомпетентными клетками, являются важными медиаторами воспаления, и среди таких цитокинов, TNF-α, как считается, играет особенно важную роль. Поэтому соединение оксазола по настоящему изобретению является чрезвычайно эффективным для лечения TNF-α-опосредованных заболеваний.
Настоящее изобретение было создано в результате последующих исследований, основанных на указанных выше открытиях.
Настоящее изобретение предоставляет соединение оксазола, фармацевтическую композицию, содержащую указанное соединение, применение указанного соединения, способ лечения или профилактики заболевания и способ для получения указанного соединения, как описано в пунктах 1-14 ниже.
Пункт 1. Соединение оксазола, представленное формулой (1)
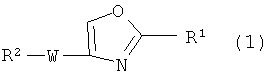
где R1 представляет собой арильную группу, которая может содержать один или несколько заместителей, выбранных из следующих групп (1-1)-(1-11):
(1-1) гидроксигруппы,
(1-2) незамещенные или галогензамещенные низшие алкоксигруппы,
(1-3) низшие алкенилоксигруппы,
(1-4) низшие алкинилоксигруппы,
(1-5) циклоC3-8алкил(низший)алкоксигруппы,
(1-6) циклоC3-8алкилоксигруппы,
(1-7) циклоC3-8алкенилоксигруппы,
(1-8) дигидроинденилоксигруппы,
(1-9) гидрокси(низший)алкоксигруппы,
(1-10) оксиранил(низший)алкоксигруппы,
(1-11) защищенные гидроксигруппы;
R2 представляет собой арильную группу или гетероциклическую группу, содержащую атом азота, каждая из которых может содержать один или несколько заместителей, выбранных из следующих групп (2-1)-(2-10):
(2-1) гидроксигруппы,
(2-2) незамещенные или галогезамещенные низшие алкоксигруппы,
(2-3) незамещенные или галогензамещенные низшие алкильные группы,
(2-4) низшие алкенилоксигруппы,
(2-5) атомы галогена,
(2-6) низшие алканоильные группы,
(2-7) низшие алкилтиогруппы,
(2-8) низшие алкилсульфонильные группы,
(2-9) оксогруппы и
(2-10) группы низший алкокси-низший алкокси; и
W представляет собой двухвалентную группу, представленную формулой (i) или (ii):
Формула (i) -Y1-A1-
Формула (ii) -Y2-C(=O)-
где A1 представляет собой низшую алкениленовую группу или низшую алкиленовую группу, которая может содержать один или несколько заместителей, выбранных из группы, состоящей из гидроксигруппы и низшей алкоксикарбонильной группы,
Y1 представляет собой простую связь, -C(=O)-, -C(=O)-N(R3)-, -N(R4)-C(=O)-, -S(O)m-NH- или -S(O)n-
где R3 и R4, каждый независимо, представляют собой атом водорода или низшую алкильную группу, и m и n, каждый независимо, представляют собой целое число, имеющее значение от 0 до 2, и
Y2 представляет собой пиперазиндиильную группу, или двухвалентную группу, представленную формулой (iii) или (iv):
Формула (iii) или (iv):
Формула (iii) -С(=О)-А2-N(R5)-
Формула (iv) А3-N(R6)-
где A2 и A3, каждый независимо, представляют собой низшую алкиленовую группу, и R5 и R6, каждый независимо, представляют собой атом водорода или низшую алкильную группу;
или его соль.
Пункт 2. Соединение по пункту 1,
в котором R1 представляет собой фенильную группу, которая имеет от 1 до 3 заместителей, выбранных из следующих групп (1-2), (1-3), (1-4) и (1-5):
(1-2) незамещенные или галогензамещенные низшие алкоксигруппы,
(1-3) низшие алкенилоксигруппы,
(1-4) низшие алкинилоксигруппы и
(1-5) циклоC3-8алкил(низший)алкоксигруппы;
R2 представляет собой фенильную группу или пиридильную группу, каждая из которых может содержать от 1 до 3 заместителей, выбранных из группы, состоящей из следующих (2-2), (2-3), (2-4) и (2-5):
(2-2) незамещенные или галогензамещенные низшие алкоксигруппы,
(2-3) незамещенные или галогензамещенные низшие алкильные группы,
(2-4) низшие алкенилоксигруппы и
(2-5) атомы галогена;
W представляет собой двухвалентную группу, представленную формулой (i):
Формула (i) -Y1-A1-
в которой A1 представляет собой низшую алкиленовую группу, и
Y1 представляет собой -C(=O)- или -C(=O)-N(R3)-
где R3 представляет собой атом водорода.
Пункт 3. Соединение по пункту 2,
в котором R1 представляет собой фенильную группу, содержащую два заместителя, выбранных из следующих групп (1-2), (1-3), (1-4) и (1-5):
(1-2) незамещенные или галогензамещенные низшие алкоксигруппы,
(1-3) низшие алкенилоксигруппы,
(1-4) низшие алкинилоксигруппы и
(1-5) циклоC3-8алкил(низший)алкоксигруппы;
R2 представляет собой фенильную группу или пиридильную группу, каждая из которых может содержать от 1 до 2 заместителей, выбранных из следующих групп (2-2), (2-3), (2-4) и (2-5):
(2-2) незамещенные или галогензамещенные низшие алкоксигруппы,
(2-3) незамещенные или галогензамещенные низшие алкильные группы,
(2-4) низшие алкенилоксигруппы и
(2-5) атомы галогена; и
W представляет собой двухвалентную группу, представленную формулой (i):
Формула (i) -Y1-A1-
в которой A1 представляет собой низшую алкиленовую группу, и Y1 представляет собой -C(=O)- или -C(=O)-N(R3)-, где R3 представляет собой атом водорода.
Пункт 4. Соединение по пункту 3,
в котором R1 представляет собой фенильную группу, замещенную в фенильном кольце двумя низшими алкоксигруппами, фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одной циклоC3-8алкил(низший)алкоксигруппой, фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одной галогензамещенной низшей алкоксигруппой, фенильную группу, замещенную в фенильной группе одной низшей алкоксигруппой и одной низшей алкенилоксигруппой, фенильную группу, замещенную в фенильном кольце одной галогензамещенной низшей алкоксигруппой и одной циклоC3-8алкил(низший)алкоксигруппой, фенильную группу, замещенную в фенильном кольце одной галогензамещенной низшей алкоксигруппой и одной низшей алкенилоксигруппой, или фенильную группу, замещенную в фенильном кольце двумя галогензамещенными низшими алкоксигруппами;
R2 представляет собой низшую алкоксифенильную группу, низшую алкенилоксифенильную группу, галогензамещенную низшую алкоксифенильную группу, низшую алкилпиридильную группу или фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одним атомом галогена; и
W представляет собой двухвалентную группу, представленную формулой (i):
Формула (i) -Y1-A1-
в которой A1 представляет собой C1-4алкиленовую группу, и
Y1 представляет собой -C(=O)- или -C(=O)-N(R3)-,
где R3 представляет собой атом водорода.
Пункт 5. Соединение по пункту 4,
в котором R1 представляет собой фенильную группу, замещенную в фенильном кольце двумя низшими алкоксигруппами, фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одной циклоC3-8алкил(низший)алкоксигруппой, фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одной галогензамещенной низшей алкоксигруппой, фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одной низшей алкенилоксигруппой, фенильную группу, замещенную в фенильном кольце одной галогензамещенной низшей алкоксигруппой и одной циклоC3-8алкил(низший)алкоксигруппой, фенильную группу, замещенную в фенильном кольце одной низшей галогензамещенной низшей алкоксигруппой и одной низшей алкенилоксигруппой, или фенильную группу, замещенную в фенильном кольце двумя галогензамещенными низшими алкоксигруппами;
R2 представляет собой низшую алкоксифенильную группу, низшую алкенилоксифенильную группу, галогензамещенную низшую алкоксифенильную группу, низшую алкилпиридильную группу или фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одним атомом галогена; и
W представляет собой двухвалентную группу, представленную формулой (i):
Формула (i) -Y1-A1-
в которой A1 представляет собой C1-4алкиленовую группу, и
Y1 представляет собой -C(=O)-.
Пункт 6. Соединение по пункту 4,
в котором R1 представляет собой фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одной галогензамещенной низшей алкоксигруппой, фенильную группу, замещенную в фенильном кольце одной галогензамещенной низшей алкоксигруппой и одной циклоC3-8алкил(низший)алкоксигруппой, или фенильную группу, замещенную в фенильном кольце одной галогензамещенной низшей алкоксигруппой и одной низшей алкенилоксигруппой;
R2 представляет собой низшую алкоксифенильную группу или низшую алкилпиридильную группу; и
W представляет собой двухвалентную группу, представленную формулой (i):
Формула (i) -Y1-A1-
в которой A1 представляет собой C1-4алкиленовую группу, и
Y1 представляет собой -C(=O)-N(R3)-,
где R3 представляет собой атом водорода.
Пункт 7. Фармацевтическая композиция, включающая соединение или соль по любому из пунктов 1-6 в качестве активного ингредиента и фармацевтически приемлемый носитель.
Пункт 8. Фармацевтическая композиция для лечения или профилактики заболеваний, опосредованных фосфодиэстеразой 4 и/или опосредованных фактором некроза опухоли α, где композиция включает соединение или соль по любому из пунктов 1-6.
Пункт 9. Фармацевтическая композиция для лечения или профилактики атопического дерматита, где композиция включает соединение или соль по любому из пунктов 1-6.
Пункт 10. Способ получения фармацевтической композиции, который включает смешивание соединения или соли по любому из пунктов 1-6 с фармацевтически приемлемым носителем.
Пункт 11. Применение соединения или соли по любому из пунктов 1-6 в качестве лекарственного средства.
Пункт 12. Применение соединения или соли по любому из пунктов 1-6 в качестве ингибитора фосфодиэстеразы 4 и/или ингибитора продукции фактора некроза опухоли α.
Пункт 13. Способ лечения или профилактики заболеваний, опосредованных фосфодиэстеразой 4 и/или опосредованных фактором некроза опухоли α, при этом способ включает введение соединения или соли по любому из пунктов 1-6 человеку или животному.
Пункт 14. Способ получения соединения оксазола, представленного формулой (1):

где R1, R2 и W имеют значения, определенные в пункте l, или его соли, при этом способ включает взаимодействие соединения, представленного формулой (2):
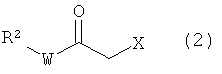
где R2 и W имеют значения, определенные выше, и X представляет собой атом галогена, или его соли с соединением, представленным формулой (3):
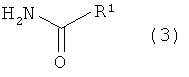
где R1 имеет значения, определенные выше, или его солью.
В формуле (1) R1 предпочтительно представляет собой фенильную группу. Фенильная группа, представленная R1, предпочтительно, содержит от 1 до 3 и, более предпочтительно, 2 заместителя, выбранных из группы, включающей (1-2) незамещенные или галогензамещенные низшие алкоксигруппы, (1-3) низшие алкенилоксигруппы, (1-4) низшие алкинилоксигруппы и (1-5) циклоC3-8алкил(низший)алкоксигруппы.
В формуле (1) R2, предпочтительно, представляет собой фенильную группу или пиридильную группу. Фенильная группа или пиридильная группа, представленная R2, предпочтительно, содержит от 1 до 3 заместителей и, более предпочтительно, 1 заместитель, выбранные из группы, включающей (2-2) незамещенные или галогензамещенные низшие алкоксигруппы, (2-3) незамещенные или галогензамещенные низшие алкилгруппы, (2-4) низшие алкенилоксигруппы и (2-5) атомы галогена.
В формуле (1) W, предпочтительно, представляет собой двухвалентную группу, представленную формулой (i) -Y1-A1-. A1, предпочтительно, представляет собой низшую алкиленовую группу; Y1, предпочтительно, представляет собой -C(=O)- или -C(=O)-N(R3)-; и R3, предпочтительно, представляет собой атом водорода.
Из соединений оксазола по настоящему изобретению предпочтительными являются те соединения, которые представлены формулой (1A), и их соли, и наиболее предпочтительными являются те соединения, которые представлены формулой (1B) и их соли.
Формула (1А):
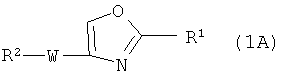
где R1 представляет собой фенильную группу, содержащую два заместителя, выбранных из следующих (1-2), (1-3), (1-4) и (1-5):
(1-2) незамещенные или галогензамещенные низшие алкоксигруппы,
(1-3) низшие алкенилоксигруппы,
(1-4) низшие алкинилоксигруппы и
(1-5) циклоC3-8алкил(низший)алкоксигруппы;
R2 представляет собой фенильную группу или пиридильную группу, каждая из которых может содержать один или несколько заместителей, выбранных из следующих групп (2-2), (2-3), (2-4) и (2-5):
(2-2) незамещенные или галогензамещенные низшие алкоксигруппы,
(2-3) незамещенные или галогензамещенные низшие алкилгруппы,
(2-4) низшие алкенилоксигруппы, и
(2-5) атомы галогена; и
W представляет собой двухвалентную группу, представленную формулой (i):
Формула (i) -Y1-A1-,
в которой A1 представляет собой низшую алкиленовую группу, и
Y1 представляет собой -C(=O)- или -C(=O)-N(R3)-
где R3 представляет собой атом водорода.
Формула (1В):
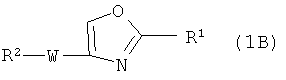
где R1 представляет собой фенильную группу, замещенную в фенильном кольце двумя низшими алкоксигруппами, фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одной циклоC3-8алкил(низший)алкоксигруппой, фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одной галогензамещенной низшей алкоксигруппой, фенильную группу, замещенную в фенильной группе одной низшей алкоксигруппой и одной низшей алкенилоксигруппой, фенильную группу, замещенную в фенильном кольце одной галогензамещенной низшей алкоксигруппой и одной цикло C3-8алкил(низший)алкоксигруппой, фенильную группу, замещенную в фенильном кольце одной галогензамещенной низшей алкоксигруппой и одной низшей алкенилоксигруппой, или фенильную группу, замещенную в фенильном кольце двумя галогензамещенными низшими алкоксигруппами;
R2 представляет собой низшую алкоксифенильную группу, низшую алкенилоксифенильную группу, галогензамещенную низшую алкоксифенильную группу, низшую алкилпиридильную группу или фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одним атомом галогена; и
W представляет собой двухвалентную группу, представленную формулой (i):
Формула (i) -Y1-A1-,
в которой A1 представляет собой C1-4алкиленовую группу и
Y1 представляет собой -C(=O)- или -C(=O)-N(R3)-,
где R3 представляет собой атом водорода.
Настоящее изобретение более подробно описано ниже.
Соединение, представленное формулой (1)
В формуле (1) R1 представляет собой арильную группу. Арильная группа может содержать от 1 до 3 и, предпочтительно, 2 заместителя, выбранных из группы, включающей (1-1) гидроксигруппы, (1-2) незамещенные или галогензамещенные низшие алкоксигруппы, (1-3) низшие алкенилоксигруппы, (1-4) низшие алкинилоксигруппы, (1-5) циклоC3-8алкил(низший)алкоксигруппы, (1-6) циклоC3-8алкилоксигруппы, (1-7) циклоC3-8алкенилоксигруппы, (1-8) дигидроинденилоксигруппы, (1-9) гидрокси(низший)алкоксигруппы, (1-10) оксиранил(низший)алкоксигруппы и (1-11) защищенные гидроксигруппы.
В формуле (1) R2 представляет собой арильную группу или гетероциклическую группу, содержащую атом азота. Арильная группа и гетероциклическая группа могут содержать от 1 до 3 заместителей и, предпочтительно, 1 заместитель, выбранные из группы включающей (2-1) гидроксигруппы, (2-2) незамещенные или галогензамещенные низшие алкоксигруппы, (2-3) незамещенные или галогензамещенные низшие алкильные группы, (2-4) низшие алкенилоксигруппы, (2-5) атомы галогена, (2-6) низшие алканоильные группы, (2-7) низшие алкилтиогруппы, (2-8) низшие алкилсульфонильные группы, (2-9) оксогруппы и (2-10) низший алкокси-низший алкоксигруппы.
В формуле (1) W представляет собой двухвалентную группу, представленную формулой (i) или (ii):
Формула (i) -Y1-A1-
Формула (ii) -Y2-С(=О)-
где A1 представляет собой низшую алкениленовую группу или низшую алкиленовую группу, которая может содержать от 1 до 3 и, предпочтительно, 1 заместитель, выбранные из группы, включающей гидроксигруппы и низшие алкоксикарбонильные группы;
Y1 представляет собой простую связь, -C(=O)-, -C(=O)-N(R3)-, -N(R4)-C(=O)-, -S(O)m-NH- или -S(O)n-,
где R3 и R4, каждый независимо, представляют собой атом водорода или низшую алкильную группу, и m и n, каждый независимо, представляют собой целое число, имеющее значение от 0 до 2; и
Y2 представляет собой пиперазиндиильную группу или двухвалентную группу, представленную формулой (iii) или (iv):
Формула (iii) -С(=О)-А2-N(R5)-
Формула (iv) А3-N(R6)-
где A2 и A3, каждый независимо, представляют собой низшую алкиленовую группу, и
R5 и R6, каждый независимо, представляют собой атом водорода или низшую алкильную группу.
Примеры арильных групп включают фенил, нафтил и т.д.
Примеры атомов галогена включают фтор, хлор, бром, йод и т.д.
Низшие алкильные группы представляют собой алкильные группы с прямой или разветвленной цепью, имеющие 1-6 атомов углерода, и их примеры включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил, втор-бутил, 1-этилпропил, н-пентил, неопентил, н-гексил, изогексил, 3-метилпентил и т.д.
Незамещенные или галогензамещенные низшие алкилгруппы представляют собой алкильные группы с прямой или разветвленной цепью, имеющие 1-6 атомов углерода, как определено выше, или такие алкильные группы, замещенные 1-7 атомами галогена. Примеры таких групп включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил, втор-бутил, 1-этилпропил, н-пентил, неопентил, н-гексил, изогексил, 3-метилпентил, фторметил, дифторметил, трифторметил, хлорметил, дихлорметил, трихлорметил, бромметил, дибромметил, дихлорфторметил, 2-фторэтил, 2,2-дифторэтил, 2,2,2-трифторэтил, пентафторэтил, 2-хлорэтил, 3,3,3-трифторпропил, гептафторпропил, гептафторизопропил, 3-хлорпропил, 2-хлорпропил, 3-бромпропил, 4,4,4-трифторбутил, 4,4,4,3,3-пентафторбутил, 4-хлорбутил, 4-бромбутил, 2-хлорбутил, 5,5,5-трифторпентил, 5-хлорпентил, 6,6,6-трифторгексил, 6-хлоргексил и т.д.
Низшие алкенилоксигруппы представляют собой группы, состоящие из атома кислорода и C2-6алкенильной группы с прямой или разветвленной цепью, содержащие 1-3 двойные связи. Низшие алкенилоксигруппы имеют цис- и трансформы. Более конкретные примеры таких групп включают винилокси, 1-пропенилокси, 2-пропенилокси, 1-метил-1-пропенилокси, 2-метил-1-пропенилокси, 2-метил-2-пропенилокси, 2-пропенилокси, 2-бутенилокси, 1-бутенилокси, 3-бутенилокси, 2-пентенилокси, 1-пентенилокси, 3-пентенилокси, 4-пентенилокси, 1,3-бутадиенилокси, 1,3-пентадиенилокси, 2-пентен-4-илокси, 3-метил-2-бутенилокси, 2-гексенилокси, 1-гексенилокси, 5-гексенилокси, 3-гексенилокси, 4-гексенилокси, 3,3-диметил-1-пропенилокси, 2-этил-1-пропенилокси, 1,3,5-гексатриенилокси, 1,3-гексадиенилокси, 1,4-гексадиенилокси и т.д.
Примеры низших алкинилоксигрупп включают группы, состоящие из атома кислорода и C2-6алкинильных групп с прямой или разветвленной цепью, содержащих от 1 до 3 тройных связей. Более конкретные примеры таких групп включают этинилокси, 2-пропинилокси, 2-бутинилокси, 3-бутинилокси, 1-метил-2-пропинилокси, 2-пентинилокси, 2-гексинилокси и т.д.
Примеры циклоC3-8алкильных групп включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил и т.д.
Предпочтительные примеры низших алкоксигрупп включают C1-6алкоксигруппы с прямой или разветвленной цепью. Конкретно, такие группы включают метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, трет-бутокси, втор-бутокси, 1-этилпропокси, н-пентокси, неопентокси, н-гексилокси, изогексилокси, 3-метилпентокси и т.д.
Примеры циклоC3-8алкил(низший)алкоксигрупп включают указанные выше низшие алкоксигруппы, которые содержат от 1 до 3 и, предпочтительно, 1 циклоC3-8алкильную группу, указанную выше. Более конкретные примеры таких групп включают циклопропилметокси, циклобутилметокси, циклогексилметокси, 2-циклопропилэтокси, 1-циклобутилэтокси, циклопентилметокси, 3-циклопентилпропокси, 4-циклогексилбутокси, 5-циклогептилпентокси, 6-циклооктилгексилокси, 1,1-диметил-2-циклогексилэтокси, 2-метил-3-циклопропилпропокси и т.д.
Примеры циклоC3-8алкилоксигрупп включают циклопропилокси, циклобутилокси, циклопентилокси, циклогексилокси, циклогептилокси, циклооктилокси и т.д.
Примеры циклоC3-8алкенилоксигрупп включают циклопропенилокси, циклобутенилокси, циклопентенилокси, циклогексенилокси, циклогептенилокси, циклооктенилокси и т.д.
Примеры дигидроинденилоксигрупп включают 2,3-дигидроинден-1-илокси, 2,3-дигидроинден-2-илокси и т.д.
Примеры гидрокси(низший)алкоксигрупп включают низшие алкоксигруппы (предпочтительно, C1-6алкоксигруппы с прямой или разветвленной цепью), содержащие от 1 до 5 и, предпочтительно, от 1 до 3 гидроксигрупп. Более конкретные примеры таких групп включают гидроксиметилокси, 2-гидроксиэтилокси, 1-гидроксиэтилокси, 3-гидроксипропилокси, 2,3-дигидроксипропилокси, 4-гидроксибутилокси, 3,4-дигидроксибутилокси, 1,1-диметил-2-гидроксиэтилокси, 5-гидроксипентилокси, 6-гидроксигексилокси, 3,3-диметил-3-гидроксипропилокси, 2-метил-3-гидроксипропилокси, 2,3,4-тригидроксибутилокси, пергидроксигексилокси и т.д.
Примеры оксиранил(низший)алкоксигрупп включают C1-6алкоксигруппы с прямой или разветвленной цепью, содержащие 1 или 2 оксиранилгруппы, такие как, например, оксиранилметокси, 2-оксиранилэтокси, 1-оксиранилэтокси, 3-оксиранилпропокси, 4-оксиранилбутокси, 5-оксиранилпентилокси, 6-оксиранилгексилокси, 1,1-диметил-2-оксиранилэтокси, 2-метил-3-оксиранилпропокси и т.д.
Примеры защитных групп для защиты гидроксигрупп включают низшие алканоильные и другие ацильные группы; группы фенил(низший)алкил, которые могут иметь один или несколько подходящих заместителей (например, бензил, фенэтил, 3-фенилпропил, 4-метоксибензил, тритил и т.д.); тризамещенные силильные группы [например, три(низший)алкилсилильные группы (например, триметилсилильные, трет-бутилдиметилсилильные и т.д.) и т.п.]; тетрагидропиранил и т.д.
Примеры гетероциклических групп, содержащих атом азота, включают пирролидинил, имидазолидинил, пиперидил, гексагидропиримидинил, пиперазинил, октагидроизоиндолил, азепанил, азоцанил, пирролил, дигидропирролил, имидазолил, дигидроимидазолил, триазолил, дигидротриазолил, пиразолил, пиридил и их N-оксиды, дигидропиридил, пиримидинил, дигидропиримидинил, пиразинил, дигидропиразинил, пиридазинил, тетразолил, индолил, изоиндолил, индолинил, изоиндолинил, гексагидроизоиндолинил, бензоимидазолил, хинолил, изохинолил, индазолил, хиназолинил, дигидрохиназолинил, бензотриазолил, карбазолил, оксазолил, изооксазолил, оксадиазолил, оксазолидинил, изооксазолидинил, морфолинилбензоксазолил, дигидробензоксазолил, бензоксазинил, дигидробензоксазинил, бензоксазолил, бензооксадиазолил, тиазолил, дигидротиазолил, изотиазолил, тиадиазолил, дигидротиазинил, тиазолизинил, бензотиазолил, бензотиадиазолил и т.д.
Незамещенные или галогензамещенные низшие алкоксигруппы представляют собой алкоксигруппы с прямой или разветвленной цепью, содержащие от 1 до 6 атомов углерода, или такие алкоксигруппы, замещенные 1-7 атомами галогена. Примеры таких групп включают метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, трет-бутокси, втор-бутокси, 1-этилпропокси, н-пентокси, неопентокси, н-гексилокси, изогексилокси, 3-метилпентокси, фторметокси, дифторметокси, трифторметокси, хлорметокси, дихлорметокси, трихлорметокси, бромметокси, дибромметокси, дихлорфторметокси, 2-фторэтокси, 2,2-дифторэтокси, 2,2,2-трифторэтокси, пентафторэтокси, 2-хлорэтокси, 3,3,3-трифторпропокси, гептафторпропокси, гептафторизопропокси, 3-хлорпропокси, 2-хлорпропокси, 3-бромпропокси, 4,4,4-трифторбутокси, 4,4,4,3,3-пентафторбутокси, 4-хлорбутокси, 4-бромбутокси, 2-хлорбутокси, 5,5,5-трифторпентокси, 5-хлорпентокси, 6,6,6-трифторгексилокси, 6-хлоргексилокси и т.д.
Примеры низших алканоильных групп включают формил, ацетил, пропионил, бутирил, изобутирил, пентаноил, трет-бутилкарбонил, гексаноил и другие C1-6алканоильные группы с прямой или разветвленной цепью.
Примеры низших алкилтиогрупп включают метилтио, этилтио, н-пропилтио, изопропилтио, н-бутилтио, трет-бутилтио, н-пентилтио, н-гексилтио и другие C1-6алкилтиогруппы с прямой или разветвленной цепью.
Предпочтительные примеры низших алкилсульфонильных групп включают C1-6алкилсульфонильные группы с прямой или разветвленной цепью. Более конкретные примеры таких групп включают метилсульфонил, этилсульфонил, н-пропилсульфонил, изопропилсульфонил, н-бутилсульфонил, изобутилсульфонил, трет-бутилсульфонил, втор-бутилсульфонил, н-пентилсульфонил, изопентилсульфонил, неопентилсульфонил, н-гексилсульфонил, изогексилсульфонил, 3-метилпентилсульфонил и т.д.
Низшие алкениленовые группы включают, например, винилиден, пропилен, бутенилен и другие C2-6алкениленгруппы с прямой или разветвленной цепью, содержащие от 1 до 3 двойных связей.
Предпочтительные примеры низших алкоксикарбонильных групп включают группы, состоящие из C1-6алкоксигрупп с прямой или разветвленной цепью и карбонильных групп. Конкретные примеры таких групп включают метоксикарбонил, этоксикарбонил, н-пропоксикарбонил, изопропоксикарбонил, н-бутоксикарбонил, изобутоксикарбонил, трет-бутоксикарбонил, втор-бутоксикарбонил, н-пентоксикарбонил, неопентоксикарбонил, н-гексилоксикарбонил, изогексилоксикарбонил, 3-метилпентоксикарбонил и т.д.
Низшие алкиленовые группы включают, например, этилен, триметилен, 2-метилтриметилен, 2,2-диметилтриметилен, 1-метилтриметилен, метилметилен, этилметилен, тетрaметилен, пентаметилен, гексаметилен и другие C1-6алкиленовые группы с прямой или разветвленной цепью.
Примеры групп низший алкокси-низший алкокси включают алкоксиалкоксигруппы, в которых каждый из двух алкоксифрагментов, независимо, представляет собой C1-6алкоксигруппу с прямой или разветвленной цепью. Конкретные примеры таких групп включают метоксиметокси, 2-метоксиэтокси, 3-метоксипропокси, 4-метоксибутокси, 5-метоксипентокси, 6-метоксигексилокси, этоксиметокси, 2-этоксиэтокси, н-пропоксиметокси, изопропоксиметокси, н-бутоксиметокси и т.д.
Примеры C1-4алкиленовых групп включают этилен, триметилен, 2-метилтриметилен, 2,2-диметилтриметилен, 1-метилтриметилен, метилметилен, этилметилен, тетрaметилен и другие C1-4алкиленовые группы с прямой или разветвленной цепью.
Способы получения соединения, представленного формулой (1)
Соединение оксазола, представленное формулой (1), может быть получено различными способами, один из примеров которых представлен на схеме реакций 1.
Схема реакций 1
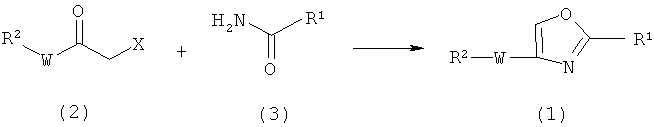
где R1, R2 и W имеют значения, определенные в формуле (1), и X представляет собой атом галогена.
Соединение (1) получают взаимодействием соединения (2) с соединением (3).
Взаимодействие соединения (2) с соединением (3) обычно осуществляют в подходящем растворителе. Можно использовать различные известные растворители, при условии, что они не ингибируют реакцию. Примеры таких растворителей включают диметилформамид, диметилсульфоксид, ацетонитрил и другие апротонные полярные растворители; ацетон, метилэтилкетон и другие кетоновые растворители; бензол, толуол, ксилол, тетралин, жидкий парафин и другие углеводородные растворители; метанол, этанол, изопропанол, н-бутанол, трет-бутанол и другие спиртовые растворители; тетрагидрофуран, диоксан, дипропиловый эфир, диэтиловый эфир, диметоксиэтан, диглим и другие эфирные растворители; этилацетат, метилацетат и другие сложноэфирные растворители; их смеси; и т.д. Такие растворители могут содержать воду.
Отношение соединения (3) к соединению (2) обычно составляет от 0,5 до 5 моль, и предпочтительно от 0,5 до 3 моль, на моль соединения (2).
Взаимодействие соединения (2) с соединением (3) обычно осуществляют при непрерывном перемешивании при температуре от -20 до 200°C и, предпочтительно, от 0 до 150°C, в течение времени от 30 минут до 60 часов и, предпочтительно, от 1 до 30 часов.
Соединение (3), используемое в качестве исходного вещества, представляет собой легкодоступное известное соединение. Соединение (2) охватывает новые соединения, и способ получения такого соединения описан ниже (схема реакций 9).
Из соединений оксазола, представленных формулой (1), соединения, в которых W представляет собой двухвалентную группу, представленную формулой -Y1-A1-, в которой Y1 представляет собой -C(=O)-N(R3)- (далее указано как “соединение (1a)”), могут быть получены, например, способом, представленным на схеме реакций 2.
Схема реакций 2
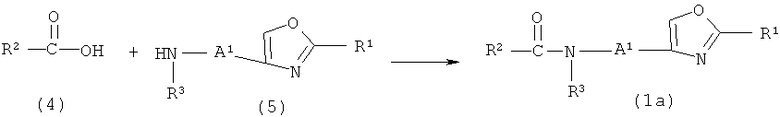
где R1, R2, R3 и A1 имеют значения, определенные в формуле (1).
Соединение (1a) получают взаимодействием соединения (4) или его реакционноспособного производного по карбоксигруппе с соединением (5) или его реакционноспособным производным по амино- или иминогруппе.
Предпочтительные примеры реакционноспособных производных соединения (4) включают галогенангидриды кислот, ангидриды кислот, активированные амиды, активированные сложные эфиры и т.д. Предпочтительные примеры реакционноспособных производных включают хлорангидриды кислот, азиды кислот; диалкилфосфорные кислоты, фенилфосфорную кислоту, дифенилфосфорную кислоту, дибензилфосфорную кислоту, галогенангидриды фосфорной кислоты и другие замещенные фосфорные кислоты, диалкилфосфористую кислоту, сернистую кислоту, тиосерную кислоту, серную кислоту, метансульфоновую кислоту и другие сульфоновые кислоты, уксусную кислоту, пропионовую кислоту, масляную кислоту, изомасляную кислоту, пивалиновую кислоту, пентановую кислоту, изопентановую кислоту, 2-этилмасляную кислоту, трихлоруксусную кислоту и другие алифатические карбоновые кислоты, и смешанные кислотные ангидриды с кислотами, такими как бензойная кислота или другие ароматические кислоты; симметричные кислотные ангидриды; активированные амиды с имидазолом, 4-замещенным имидазолом, диметилпиразолом, триазолом или тетразолом; цианометиловый эфир, метоксиметиловый эфир, диметилиминометиловый эфир, виниловый эфир, пропаргиловый эфир, пара-нитрофениловый эфир, 2,4-динитрофениловый эфир, трихлорфениловый эфир, пентахлорфениловый эфир, мезилфениловый эфир и другие активированные сложные эфиры, сложные эфиры с N,N-диметилгидроксиламином, 1-гидрокси-2-(1H)-пиридоном, N-гидроксисукцинимидом, N-гидроксифталимидом, 1-гидрокси-1H-бензотриазолом и другими N-гидроксисоединениями; и т.д. Такие реакционноспособные производные могут быть выбраны, если это желательно, в соответствии с типом используемого соединения (4).
При использовании соединения (4) в форме свободной кислоты или ее соли в вышеописанной реакции, предпочтительным является осуществление реакции в присутствии агента(ов) конденсации. Можно использовать широкий спектр агентов конденсации, известных в данной области, включая, например, N,N'-дициклогексилкарбoдиимид; N-циклогексил-N'-морфолинoэтилкарбoдиимид; N-циклогексил-N'-(4-диэтиламиноциклогексил)карбoдиимид; N,N'-диэтилкарбoдиимид; N,N'-диизопропилкарбoдиимид; N-этил-N'-(3-диметиламинопропил)карбoдиимид и их гидрохлориды; N,N'-карбонилбис(2-метилимидазол); пентаметиленкетен-N-циклогексилимин; дифенилкетен-N-циклогексилимин; этоксиацетилен, 1-алкокси-1-хлорэтилен; триалкилфосфит; этилполифосфат; изопропилполифосфат; фосфороксихлорид (фосфорилхлорид); трихлорид фосфора; фосфорилдифенилазид; тионилхлорид; оксалилхлорид; этилхлорформиат, изопропилхлорформиат, и другие низшие алкилгалоформиаты; трифенилфосфин; соль 2-этил-7-гидроксибензизооксазолия; внутренние соли 2-этил-5-(мета-сульфофенил)изооксазолийгидроксида; гексафторфосфорной кислоты бензотриазол-1-илокси-трис(диметиламино)фосфоний; 1-(пара-хлорбензолсульфонилокси)-6-хлор-1H-бензотриазол; так называемые реагенты Вильсмайера, полученные взаимодействием N,N-диметилформамида с тионилхлоридом, фосгеном, трихлорметилхлорформиатом, оксихлоридом фосфора и т.д.; и т.п. Наиболее предпочтительным является осуществление реакции в присутствии такого агента(ов) конденсации и активного агента(ов) этерификации, как N-гидроксисукцинимид, N-гидроксифталимид, 1-гидрокси-1H-бензотриазол, или т.п.
Предпочтительные примеры реакционноспособных производных соединения (5) включают таутомеры основания Шиффа имино- или енаминового типа, полученные взаимодействием соединения (5) с карбонильными соединениями, такими как альдегиды, кетоны и т.д.; силильные производные, полученные взаимодействием соединения (5) с силильными соединениями, такими как бис(триметилсилил)ацетамид, моно(триметилсилил)ацетамид, бис(триметилсилил)мочевина и т.д.; производные, полученные взаимодействием соединения (5) с трихлоридом фосфора, фосгеном и т.д.; и т.п.
Взаимодействие обычно осуществляют в известном растворителе, который не оказывает негативного влияния на реакцию. Такие растворители включают, например, воду; метанол, этанол, изопропанол, н-бутанол, трифторэтанол, этиленгликоль и другие спиртовые растворители; ацетон, метилэтилкетон и другие кетоновые растворители; тетрагидрофуран, диоксан, диэтиловый эфир, диизопропиловый эфир, диглим и другие эфирные растворители; метилацетат, этилацетат и другие сложноэфирные растворители; ацетонитрил, N,N-диметилформамид, диметилсульфоксид и другие апротонные полярные растворители; н-пентан, н-гексан, н-гептан, циклогексан и другие углеводородные растворители; метиленхлорид, этиленхлорид и другие галогенированные углеводородные растворители; другие органические растворители; и включающие их смешанные растворители.
Реакцию можно осуществлять в присутствии основания(ий). Можно использовать широкий спектр неорганических и органических оснований. Неорганические основания включают, например, щелочные металлы (например, натрий, калий, и т.д.), гидрокарбонаты щелочных металлов (например, гидрокарбонат лития, гидрокарбонат натрия, гидрокарбонат калия и т.д.), гидроксиды щелочных металлов (например, гидроксид лития, гидроксид натрия, гидроксид калия, гидроксид цезия и т.д.), карбонаты щелочных металлов (например, карбонат лития, карбонат натрия, карбонат калия, карбонат цезия и т.д.), низшие алкоксиды щелочных металлов (например, метоксид натрия, этоксид натрия и т.д.) и гидриды щелочных металлов (например, гидрид натрия, гидрид калия и т.д.). Органические основания включают, например, триалкиламины [например, триметиламин, триэтиламин, н-этилдиизопропиламин и т.д.], пиридин, хинолин, пиперидин, имидазол, пиколин, диметиламинопиридин, диметиланилин, н-метилморфолин, 1,5-диазабицикло[4.3.0]нон-5-ен (DBN), 1,4-диазабицикло[2.2.2]октан (DABCO), 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU) и т.д. Если такие основания представляют собой жидкости, то они также могут использоваться в качестве растворителей.
Такие основания могут использоваться отдельно или в сочетании.
Количество основания(ий) составляет обычно от 0,1 до 10 моль и, предпочтительно, от 0,1 до 3 моль, на моль соединения (4).
Отношение соединения (4) к соединению (5) в схеме реакций 1 составляет обычно по меньшей мере 1 и предпочтительно от около 1 до около 5 моль первого на моль последнего.
Температура реакции не ограничена, и реакцию обычно проводят при охлаждении, при комнатной температуре или при нагревании. Предпочтительным является осуществление реакции при температуре в пределах от комнатной температуры до 100°C в течение времени от 30 минут до 30 часов и, предпочтительно, в течение времени от 30 минут до 5 часов.
В вышеописанной реакции соединение (4), используемое в качестве исходного вещества, представляет собой легкодоступное известное соединение. Соединение (5) включает новые соединения. Способ получения соединения (5) описан ниже (схема реакций 10).
Из соединений оксазола, представленных формулой (1), соединения, в которых W представляет собой двухвалентную группу, представленную формулой -Y1-A1-, в которой Y1 представляет собой -C(=O)- и A1 представляет собой низшую алкиленовую группу, содержащую одну низшую алкоксикарбонильную группу (далее указано как “соединение (1b)”), можно получить, например, с помощью способа, представленного на схеме реакций 3.
Схема реакций 3
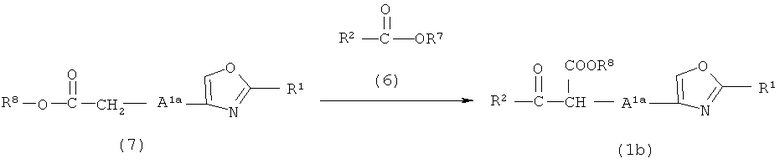
где R1 и R2 определены в формуле (1), R7 и R8, каждый независимо, представляют собой низшую алкильную группу и A1a представляет собой C1-5 алкиленовую группу.
-COOR8 группа в формуле (1b) имеет то же значение, что и низшая алкоксикарбонильная группа, определенная как заместитель A1 в формуле (1). Низшая алкильная группа, представленная R7, может иметь такое же значение, как низшая алкильная группа, определенная выше.
Примеры C1-5алкиленовой группы, представленной как A1a, включают этилен, триметилен, 2-метилтриметилен, 2,2-диметилтриметилен, 1-метилтриметилен, метилметилен, этилметилен, тетрaметилен, пентаметилен и другие C1-5алкиленовые группы с прямой или разветвленной цепью.
Соединение (1b) получают путем взаимодействия соединения (6) с соединением (7).
Реакцию обычно осуществляют в известном растворителе, который не оказывает негативного влияния на реакцию. Такие растворители включают, например, воду; метанол, этанол, изопропанол, н-бутанол, трифторэтанол, этиленгликоль и другие спиртовые растворители; ацетон, метилэтилкетон и другие кетоновые растворители; тетрагидрофуран, диоксан, диэтиловый эфир, диметоксиэтан, диглим и другие эфирные растворители; метилацетат, этилацетат и другие сложноэфирные растворители; ацетонитрил, N,N-диметилформамид, диметилсульфоксид, N-метилпирролидон и другие апротонные полярные растворители; метиленхлорид, этиленхлорид и другие галогенированные углеводородные растворители; другие органические растворители; и включающие их смешанные растворители.
Обычно реакцию можно осуществить в присутствии подходящего основания(ий). Можно использовать множество известных неорганических и органических оснований. Неорганические основания включают, например, щелочные металлы (например, литий, натрий, калий и т.д.), гидрокарбонаты щелочных металлов (например, гидрокарбонат лития, гидрокарбонат натрия, гидрокарбонат калия и т.д.), гидроксиды щелочных металлов (например, гидроксид лития, гидроксид натрия, гидроксид калия, гидроксид цезия и т.д.), карбонаты щелочных металлов (например, карбонат лития, карбонат натрия, карбонат калия, карбонат цезия и т.д.), низшие алкоксиды щелочных металлов (например, метоксид натрия, этоксид натрия, трет-бутоксид калия, трет-бутоксид натрия, трет-пентоксид натрия и т.д.), щелочнометаллгидриды (например, гидрид натрия, гидрид калия и т.д.) и т.п. Органические основания включают, например, триалкиламины (например, триметиламин, триэтиламин, N-этилдиизопропиламин и т.д.), пиридин, хинолин, пиперидин, имидазол, пиколин, диметиламинопиридин, диметиланилин, N-метилморфолин, 1,5-диазабицикло[4.3.0]нон-5-ен (DBN), 1,4-диазабицикло[2.2.2]октан (DABCO), 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU) и т.д. Когда такие основания представляют собой жидкость, их также можно использовать в качестве растворителей. Такие основания можно использовать отдельно или в сочетании.
Количество основания(ий) обычно составляет от 0,5 до 10 моль и предпочтительно от 0,5 до 6 моль, на моль соединения (6).
Отношение соединения (6) к соединению (7) обычно составляет, по меньшей мере, 1 моль и, предпочтительно, от около 1 до около 5 моль первого на моль последнего.
Температура реакции не ограничена, и обычно реакцию можно осуществить при охлаждении, при комнатной температуре или при нагревании. Подходящим является осуществление реакции при температуре в пределах от комнатной температуры до 150°C в течение времени от 30 минут до 60 часов, и предпочтительно от 1 до 30 минут.
Соединение (6), используемое в качестве исходного вещества в указанной выше реакции, является легкодоступным известным соединением. Соединение (7) охватывает новые соединения. Способ получения соединения (7) описан ниже (схема реакций 11).
Из соединений оксазола, представленных формулой (1), соединения, в которых W представляет собой двухвалентную группу, представленную -Y1-A1-, в которой A1 представляет собой низшую алкиленовую группу (далее указаны как “соединение (1d)”), получают из соответствующего соединения, в котором A1 представляет собой низшую алкиленовую группу, содержащую низшую алкоксикарбонильную группу(ы) (далее указано как “соединение (1c)”), способом, показанным на схеме реакций 4.
Схема реакций 4
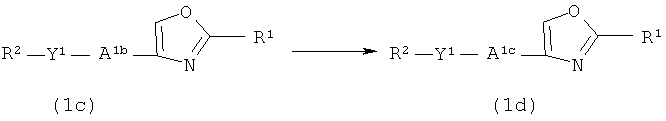
где R1, R2 и Y1 определены в формуле (1), A1b представляет собой низшую алкиленовую группу, содержащую низшую алкоксикарбонильную группу(ы), и A1c представляет собой низшую алкиленовую группу.
Соединение (1d) получают, подвергая соединение (1c) гидролизу-декарбоксилированию.
Реакцию обычно осуществляют в известном растворителе, который не оказывает негативного влияния на реакцию. Такие растворители включают, например, воду; метанол, этанол, изопропанол, н-бутанол, трифторэтанол, этиленгликоль и другие спиртовые растворители; ацетон, метилэтилкетон и другие кетоновые растворители; тетрагидрофуран, диоксан, диэтиловый эфир, диметоксиэтан, диглим и другие эфирные растворители; метилацетат, этилацетат и другие сложноэфирные растворители; ацетонитрил, N,N-диметилформамид, диметилсульфоксид, N-метилпирролидон, и другие апротонные полярные растворители; метиленхлорид, этиленхлорид и другие галогенированные углеводородные растворители; другие органические растворители; и включающие их смешанные растворители.
Гидролиз-декарбоксилирование соединения (1c) обычно осуществляют в кислотных условиях. Например, кислоту добавляют к суспензии или раствору соединения (1c) в подходящем растворителе, и полученную смесь перемешивают при температуре от 0 до 120°C для осуществления гидролиза-декарбоксилирования.
Примеры подходящих для использования кислот включают трифторуксусную кислоту, уксусную кислоту и другие органические кислоты, хлористоводородную кислоту, бромную кислоту, бромистоводородную кислоту, серную кислоту и другие неорганические кислоты и т.д. Из таких органических кислот органические кислоты также можно использовать в качестве растворителей для реакции.
Количество кислоты(кислот) обычно составляет от 0,5 до 30 моль, и предпочтительно от 0,5 до 10 моль, на моль соединения (1c).
Температура реакции обычно составляет от 0 до 120°C и предпочтительно от комнатной температуры до 110°C. Время реакции обычно составляет от 30 минут до 24 часов, предпочтительно от 30 минут до 12 часов и более предпочтительно от 1 до 8 часов.
Из соединений оксазола, представленных Формулой (1), соединения, в которых R1 представляет собой фенильную группу, замещенную в фенильном кольце гидроксигруппой(ами) (далее указано как “соединение (1f)”) получают из соответствующих соединений, где R1 представляет собой фенильную группу, замещенную в фенильном кольце защищенной гидроксигруппой(ами) (далее указано как “соединение (1е)”), способом, показанным на схеме реакций 5.
Схема реакций 5
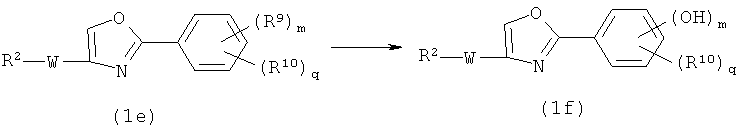
где R2 и W определены в формуле (1); R9 представляет собой защищенную гидроксигруппу; R10 представляет собой такую же группу, как заместитель (1-2), (1-3), (1-4), (1-5), (1-6), (1-7), (1-8), (1-9) или (1-10) арильной группы, представленной как R1 в формуле (1); m имеет значение от 1 до 5; q имеет значение от 0 до 4; m для групп R9 могут быть одинаковыми или отличными друг от друга; и q для групп R10 могут быть одинаковыми или отличными друг от друга; при условии, что m+q ≤5.
Соединение (1f) можно получить, подвергая соединение (1e) реакции элиминирования гидрокси-защитной группы(групп).
Реакцию элиминирования можно осуществить путем гидролиза, гидрогенолиза или другими традиционными способами.
Реакцию обычно осуществляют в известном растворителе, который не оказывает негативного влияния на реакцию. Такие растворители включают, например, воду; метанол, этанол, изопропанол, н-бутанол, трифторэтанол, этиленгликоль и другие спиртовые растворители; ацетон, метилэтилкетон и другие кетоновые растворители; тетрагидрофуран, диоксан, диэтиловый эфир, диметоксиэтан, диглим и другие эфирные растворители; метилацетат, этилацетат и другие сложноэфирные растворители; ацетонитрил, N,N-диметилформамид, диметилсульфоксид, N-метилпирролидон и другие апротонные полярные растворители; метиленхлорид, этиленхлорид и другие галогенированные углеводородные растворители; и другие органические растворители.
(i) Гидролиз:
Гидролиз, предпочтительно, осуществляют в присутствии основания(ий) или кислоты(кислот) (включая кислоты Льюиса).
Можно использовать множество известных неорганических и органических оснований. Предпочтительные примеры неорганических оснований включают щелочные металлы (например, натрий, калий и т.д.), щелочноземельные металлы (например, магний, кальций и т.д.), гидроксиды, карбонаты и гидрокарбонаты таких металлов и т.д. Предпочтительные примеры органических оснований включают триалкиламины (например, триметиламин, триэтиламин и т.д.), пиколин, 1,5-диазабицикло[4.3.0]нон-5-ен и т.д.
Можно использовать множество известных неорганических и органических кислот. Предпочтительные органические кислоты включают, например, муравьиную кислоту, уксусную кислоту, пропионовую кислоту и другие жирные кислоты; трихлоруксусную кислоту, трифторуксусную кислоту и другие тригалогенуксусные кислоты; и т.п. Предпочтительные неорганические кислоты включают, например, хлористоводородную кислоту, бромистоводородную кислоту, серную кислоту, хлористый водород, бромистый водород и т.д. Примеры кислот Льюиса включают эфирные комплексы трифторида бора, трибромид бора, хлорид алюминия, хлорид железа и т.д.
Когда используют тригалогенуксусную кислоту или кислоту Льюиса, предпочтительно осуществление гидролиза в присутствии акцептора катионов (например, анизол, фенол и т.д.).
Количество основания(ий) или кислоты(кислот) не ограничено. При условии, что оно представляет собой количество, необходимое для гидролиза.
Температура реакции обычно составляет от 0 до 120°C, предпочтительно от комнатной температуры до 100°C и более предпочтительно от комнатной температуры до 80°C. Время реакции обычно составляет от 30 минут до 24 часов, предпочтительно от 30 минут до 12 часов и более предпочтительно от 1 до 8 часов.
(ii) Гидрогенолиз:
Гидрогенолиз можно осуществить множеством известных способов, включая, например, химическое восстановление, каталитическое восстановление и т.д.
Примеры подходящих восстановителей для химического восстановления включают гидриды (например, иодистый водород, сульфид водорода, литийалюминийгидрид, боргидрид натрия, цианоборгидрид натрия и т.д.); и сочетания металлов (например, олова, цинка, железа и т.д.) или соединения металлов (например, хлорид хрома, ацетат хрома и т.д.) с органическими или неорганическими кислотами (например, муравьиной кислотой, уксусной кислотой, пропионовой кислотой, трифторуксусной кислотой, пара-толуолсульфоновой кислотой, хлористоводородной кислотой, бромоводородной кислотой и т.д.).
Примеры подходящих катализаторов для каталитического восстановления включают платиновые катализаторы (например, платиновые пластины, губчатая платина, платиновая чернь, коллоидная платина, оксид платины, платиновая проволока и т.д.), палладиевые катализаторы (например, губчатый палладий, палладиевая чернь, оксид палладия, палладий-на-углероде, палладий/барий сульфат, палладий/барий карбонат и т.д.), никелевые катализаторы (например, восстановленный никель, оксид никеля, никель Ренея и т.д.), кобальтовые катализаторы (например, восстановленный кобальт, кобальт Ренея и т.д.), катализаторы на основе железа (например, восстановленное железо и т.п.) и т.д.
Когда такие кислоты, используемые для химического восстановления, являются жидкими, их также можно использовать в качестве растворителей.
Количество восстановителя для химического восстановления и катализатора для каталитического восстановления не ограничено, и это может быть обычно используемое количество.
Температура реакции обычно составляет от 0 до 120°C, предпочтительно от комнатной температуры до 100°C и более предпочтительно от комнатной температуры до 80°C. Время реакции обычно составляет от 30 минут до 24 часов, предпочтительно от 30 минут до 10 часов и более предпочтительно 30 минут до 4 часов.
Из соединений оксазола, представленных формулой (1), соединения, в которых R1 представляет собой фенильную группу, замещенную в фенильном кольце R11O-группой(группами) (далее указаны как “соединение (1g)”), получают из соединения (1f), способом, показанным на схеме реакций 6.
Схема реакций 6
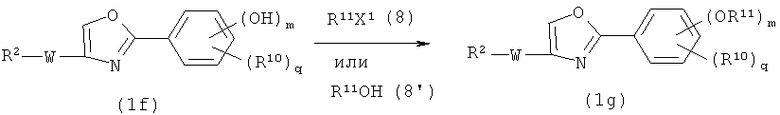
где R2 и W определены в формуле (1); R10, m и q определены выше; X1 представляет собой атом галогена или группу, которая подвергается такой же реакции замещения, как и атом галогена; R11O представляет собой такую же группу, как заместитель (1-2), (1-3), (1-4), (1-5), (1-6), (1-7), (1-8), (1-9) или (1-10) арильной группы, представленной R1 в формуле (1); и m для групп R11O могут иметь одинаковые или отличные друг от друга значения.
В соединении (8) атом галогена, представленный X1, представляет собой атом фтора, атом хлора, атом брома или атом йода.
Примеры группы, которая подвергается такой же реакции замещения, как и атом галогена, которая обозначена как X1, включают низшие алкансульфонилоксигруппы, арилсульфонилоксигруппы, аралкилсульфонилоксигруппы и т.д.
Конкретные примеры низших алкансульфонилоксигрупп включают метансульфонилокси, этансульфонилокси, изопропансульфонилокси, н-пропансульфонилокси, н-бутансульфонилокси, трет-бутансульфонилокси, н-пентансульфонилокси, н-гексансульфонилокси и другие C1-6алкансульфонилоксигруппы с прямой или разветвленной цепью и т.п.
Арилсульфонилоксигруппы включают, например, фенилсульфонилокси, нафтилсульфонилокси и т.д. Фенильное кольцо такой арилсульфонилоксигруппы может содержать, например, от 1 до 3 заместителей, выбранных из группы, включающей C1-6алкильные группы с прямой или разветвленной цепью, C1-6алкоксигруппы с прямой или разветвленной цепью, нитрогруппы и атомы галогена. Конкретные примеры таких арилсульфонилоксигрупп включают фенилсульфонилокси, 4-метилфенилсульфонилокси, 2-метилфенилсульфонилокси, 4-нитрофенилсульфонилокси, 4-метоксифенилсульфонилокси, 2-нитрофенилсульфонилокси, 3-хлорфенилсульфонилокси и т.д. Конкретные примеры нафтилсульфонилоксигрупп включают α-нафтилсульфонилокси, β-нафтилсульфонилокси и т.д.
Аралкилсульфонилоксигруппы включают, например, фенил-замещенные C1-6алкилсульфонилоксигруппы с прямой или разветвленной цепью, которые могут содержать, в фенильном кольце, от 1 до 3 заместителей, выбранных из группы, включающей C1-6алкильные группы с прямой или разветвленной цепью, C1-6алкоксигруппы с прямой или разветвленной цепью, нитрогруппы и атомы галогена; нафтил-замещенные C1-6алкилсульфонилоксигруппы с прямой или разветвленной цепью; и т.д. Конкретные примеры указанных выше фенил-замещенных алкилсульфонилоксигрупп включают бензилсульфонилокси, 2-фенилэтилсульфонилокси, 4-фенилбутилсульфонилокси, 2-метилбензилсульфонилокси, 4-метоксибензилсульфонилокси, 4-нитробензилсульфонилокси, 3-хлорбензилсульфонилокси и т.д. Конкретные примеры указанных выше нафтил-замещенных алкилсульфонилоксигрупп включают α-нафтилметилсульфонилокси, β-нафтилметилсульфонилокси и т.д.
Соединение (1g) получают путем взаимодействия соединения (1f) с соединением (8) или путем взаимодействия соединения (1f) с соединением (8').
Взаимодействие соединения (1f) с соединением (8) описано ниже.
Взаимодействие соединения (1f) с соединением (8) обычно осуществляют в известном растворителе, который не оказывает негативного влияния на реакцию. Такие растворители включают, например, воду; метанол, этанол, изопропанол, н-бутанол, трифторэтанол, этиленгликоль и другие спиртовые растворители; ацетон, метилэтилкетон и другие кетоновые растворители; тетрагидрофуран, диоксан, диэтиловый эфир, диглим и другие эфирные растворители; метилацетат, этилацетат и другие сложноэфирные растворители; ацетонитрил, N,N-диметилформамид, диметилсульфоксид и другие апротонные полярные растворители; метиленхлорид, этиленхлорид и другие галогенированные углеводородные растворители; другие органические растворители; включающие их смешанные растворители; и т.д.
Взаимодействие соединения (1f) с соединением (8) обычно осуществляют в присутствии основания(ий). Основания, которые можно использовать, включают известные неорганические и органические основания. Неорганические основания включают, например, щелочные металлы (например, натрий, калий и т.д.), гидрокарбонаты щелочных металлов (например, гидрокарбонат лития, гидрокарбонат натрия, гидрокарбонат калия и т.д.), гидроксиды щелочных металлов (например, гидроксид лития, гидроксид натрия, гидроксид калия, гидроксид цезия и т.д.), карбонаты щелочных металлов (например, карбонат лития, карбонат натрия, карбонат калия, карбонат цезия и т.д.), низшие алкоксиды щелочных металлов (например, метоксид натрия, этоксид натрия и т.д.), гидриды щелочных металлов (например, гидрид натрия, гидрид калия и т.д.) и т.п. Органические основания включают, например, триалкиламины (например, триметиламин, триэтиламин, N-этилдиизопропиламин и т.д.), пиридин, хинолин, пиперидин, имидазол, пиколин, диметиламинопиридин, диметиланилин, N-метилморфолин, 1,5-диазабицикло[4.3.0]нон-5-ен (DBN), 1,4-диазабицикло[2.2.2]октан (DABCO), 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU) и т.д. Когда такие основания представляют собой жидкость, их также можно использовать в качестве растворителей. Такие основания можно использовать отдельно или в сочетании.
Количество основания(ий) обычно составляет от 0,5 до 10 моль и предпочтительно от 0,5 до 6 моль, на моль соединения (1f).
При осуществлении указанной выше реакции в реакционную систему можно добавить иодиды щелочных металлов, такие как иодид калия, иодид натрия и т.д., в качестве ускорителей реакции, если это необходимо.
Отношение соединения (1f) к соединению (8) обычно составляет, по меньшей мере, 1 моль и предпочтительно от около 1 до около 5 моль последнего на моль первого.
Температура реакции не ограничена, и обычно реакцию можно осуществить при охлаждении, при комнатной температуре или при нагревании. Подходящим является осуществление реакции при температуре около комнатной, в течение времени от 1 до 30 часов.
Далее описано взаимодействие соединения (1f) с соединением (8').
Взаимодействие соединения (1f) с соединением (8') обычно осуществляют в известном растворителе, который не оказывает негативного влияния на реакцию. Такие растворители включают, например, воду; метанол, этанол, изопропанол, н-бутанол, трифторэтанол, этиленгликоль и другие спиртовые растворители; ацетон, метилэтилкетон и другие кетоновые растворители; тетрагидрофуран, диоксан, диэтиловый эфир, диглим и другие эфирные растворители; метилацетат, этилацетат и другие сложноэфирные растворители; ацетонитрил, N,N-диметилформамид, диметилсульфоксид и другие апротонные полярные растворители; бензол, толуол, ксилол, и другие ароматические углеводородные растворители; метиленхлорид, этиленхлорид и другие галогенированные углеводородные растворители; другие органические растворители; в том числе включающие их смешанные растворители; и т.д.
Реакцию обычно осуществляют в присутствии диалкилазодикарбоксилата(ов), такого как диизопропилазодикарбоксилат, диэтилазодикарбоксилат и т.д., и фосфинового лиганда(ов), такого как трифенилфосфин, три(н-бутил)фосфин и т.д. Количество диалкилазодикарбоксилата(ов) обычно составляет от 0,5 до 10 моль и предпочтительно от 0,5 до 6 моль, на моль соединения (1f). Количество фосфинового лиганда(ов) обычно составляет от 0,5 до 10 моль и предпочтительно от 0,5 до 6 моль, на моль соединения (1f).
Взаимодействие соединения (1f) с соединением (8') можно осуществить в присутствии подходящего основания(ий). Можно использовать множество известных неорганических и органических оснований. Неорганические основания включают, например, щелочные металлы (например, натрий, калий и т.д.), гидрокарбонаты щелочных металлов (например, гидрокарбонат лития, гидрокарбонат натрия, гидрокарбонат калия и т.д.), гидроксиды щелочных металлов (например, гидроксид лития, гидроксид натрия, гидроксид калия, гидроксид цезия и т.д.), карбонаты щелочных металлов (например, карбонат лития, карбонат натрия, карбонат калия, карбонат цезия и т.д.), низшие алкоксиды щелочных металлов (например, метоксид натрия, этоксид натрия и т.д.), гидриды щелочных металлов (например, гидрид натрия, гидрид калия и т.д.) и т.п. Органические основания включают, например, триалкиламины (например, триметиламин, триэтиламин, N-этилдиизопропиламин и т.д.), пиридин, хинолин, пиперидин, имидазол, пиколин, диметиламинопиридин, диметиланилин, N-метилморфолин, 1,5-диазабицикло[4.3.0]нон-5-ен (DBN), 1,4-диазабицикло[2.2.2]октан (DABCO), 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU) и т.д. Когда такие основания представляют собой жидкость, их также можно использовать в качестве растворителей. Такие основания можно использовать отдельно или в сочетании.
Количество основания(ий) обычно составляет от 0,5 до 10 моль и предпочтительно от 0,5 до 6 моль, на моль соединения (1f).
Отношение соединения (1f) к соединению (8') обычно составляет, по меньшей мере, 1 моль и предпочтительно от около 1 до около 5 моль последнего на моль первого.
Температура реакции не ограничена, и обычно реакцию можно осуществить при охлаждении, при комнатной температуре или при нагревании. Подходящим является осуществление реакции при температуре около комнатной, в течение времени от 1 до 30 часов.
Соединения (8) и (8'), используемые в качестве исходных веществ в указанной выше реакции, являются легкодоступными известными соединениями.
Из соединений оксазола, представленных формулой (1), соединения, в которых W представляет собой двухвалентную группу, представленную -Y1-A1-, где Y1 представляет собой -C(=O) и A1 представляет собой низшую алкениленовую группу (далее указаны как “соединение (1h)”), можно получить например, способом, показанным на схеме реакций 7.
Схема реакций 7
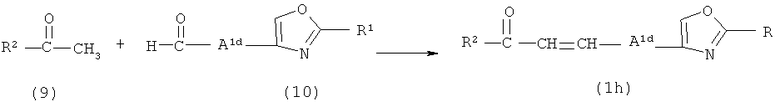
где R1 и R2 определены в формуле (1), и A1d представляет собой C2-4алкениленовую группу, C1-4алкиленовую группу или простую связь.
Каждая из C2-4алкенильных групп и C1-4алкиленовых групп может быть с прямой или разветвленной цепью. -CH=CH-A1d- соответствует низшей алкениленовой группе, представленной A1 в формуле (1).
Соединение (1h) получают путем взаимодействия соединения (9) с соединением (10).
Реакцию обычно осуществляют в известном растворителе, который не оказывает негативного влияния на реакцию. Такие растворители включают, например, воду; метанол, этанол, изопропанол, н-бутанол, трифторэтанол, этиленгликоль и другие спиртовые растворители; ацетон, метилэтилкетон и другие кетоновые растворители; тетрагидрофуран, диоксан, диэтиловый эфир, диметоксиэтан, диглим и другие эфирные растворители; метилацетат, этилацетат и другие сложноэфирные растворители; ацетонитрил, N,N-диметилформамид, диметилсульфоксид, N-метилпирролидон и другие апротонные полярные растворители; метиленхлорид, этиленхлорид и другие галогенированные углеводородные растворители; другие органические растворители; включающие их смешанные растворители; и т.д.
Реакцию можно осуществить в присутствии основания(ий). Можно использовать множество известных неорганических и органических оснований. Неорганические основания включают, например, щелочные металлы (например, литий, натрий, калий и т.д.), гидрокарбонаты щелочных металлов (например, гидрокарбонат лития, гидрокарбонат натрия, гидрокарбонат калия и т.д.), гидроксиды щелочных металлов (например, гидроксид лития, гидроксид натрия, гидроксид калия, гидроксид цезия и т.д.), карбонаты щелочных металлов (например, карбонат лития, карбонат натрия, карбонат калия, карбонат цезия и т.д.), низшие алкоксиды щелочных металлов (например, метоксид натрия, этоксид натрия, трет-бутоксид калия, трет-бутоксид натрия и т.д.), гидриды щелочных металлов (например, гидрид натрия, гидрид калия и т.д.) и т.п. Органические основания включают, например, триалкиламины (например, триметиламин, триэтиламин, N-этилдиизопропиламин и т.д.), пиридин, хинолин, пиперидин, имидазол, пиколин, диметиламинопиридин, диметиланилин, N-метилморфолин, 1,5-диазабицикло[4.3.0]нон-5-ен (DBN), 1,4-диазабицикло[2.2.2]октан (DABCO), 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU) и т.д. Когда такие основания представляют собой жидкость, их также можно использовать в качестве растворителей. Такие основания можно использовать отдельно или в сочетании.
Количество основания(ий) обычно составляет от 0,5 до 10 моль, и предпочтительно от 0,5 до 6 моль, на моль соединения (9).
Отношение соединения (9) к соединению (10) обычно составляет, по меньшей мере, 1 моль и, предпочтительно, от около 1 до около 5 моль последнего, на моль первого.
Температура реакции не ограничена, и обычно реакцию можно осуществить при охлаждении, при комнатной температуре или при нагревании. Подходящим является осуществление реакции при температуре в пределах от комнатной температуры до 150°C, в течение времени от 30 минут до 60 часов, и предпочтительно от 1 до 30 часов.
Соединение (9), используемое в качестве исходного вещества в указанной выше реакции, является легко доступным известным соединением. Соединение (10), используемое в качестве исходного вещества в указанной выше реакции, можно получить способом, показанным на схеме реакций 12.
Из соединений оксазола, представленных формулой (1), соединения, в которых W представляет собой двухвалентную группу, представленную -Y1-A1-, где A1 представляет собой низшую алкиленовую группу (далее указаны как “соединение (1j)”), можно получить из соединения, в котором A1 представляет собой низшую алкениленовую группу (далее указано как “cоединение (1i)”), способом, показанным на схеме реакций 8.
Схема реакций 8

где R1 и R2 определены в формуле (1), Y1 определен выше, A1e представляет собой низшую алкениленовую группу, и A1f представляет собой низшую алкиленовую группу.
Соединение (1j) получают, подвергая соединение (1i) гидрогенолизу.
Реакцию осуществляют в таких же реакционных условиях, как условия реакции, показанной на схеме реакций 5 для гидрогенолиза соединения (1e), с получением соединения (1f). Поэтому в указанной выше реакции можно использовать такие же реагент(ы) и реакционные условия (например, растворитель, температура реакции и т.д.), как используемые в гидрогенолизе, показанном на схеме реакций 5.
Схема реакций 9
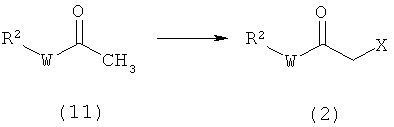
где R2 и W определены в формуле (1), и X определен выше.
Реакцию галогенирования соединения (11) осуществляют в подходящем растворителе в присутствии агента галогенирования. Агенты галогенирования, которые можно использовать, включают, например, Br2, Cl2, и другие молекулы галогенов; хлорид йода, сульфурилхлорид, бромид меди и другие соединения меди; N-бромсукцинимид, N-хлорсукцинимид и другие N-галогенсукцинимиды и т.д. Подходящие растворители включают, например, дихлорметан, дихлорэтан, хлороформ, тетрахлорид углерода и другие галогенированные углеводороды; уксусную кислоту, пропионовую кислоту и другие жирные кислоты; дисульфид углерода; и т.д. Количество агента галогенирования обычно составляет от 1 до 10 моль и предпочтительно от 1 до 5 моль, на моль соединения (11). Реакцию обычно осуществляют при температуре от 0°C до температуры кипения растворителя и предпочтительно от около 0 до около 100°C, в течение времени от около 5 минут до около 20 часов.
Из соединений (5) для использования в качестве исходных веществ, соединения, в которых R3 представляет собой атом водорода (далее указаны как “соединение (5a)”), получают способом, показанным на схеме реакций 10.
Схема реакций 10
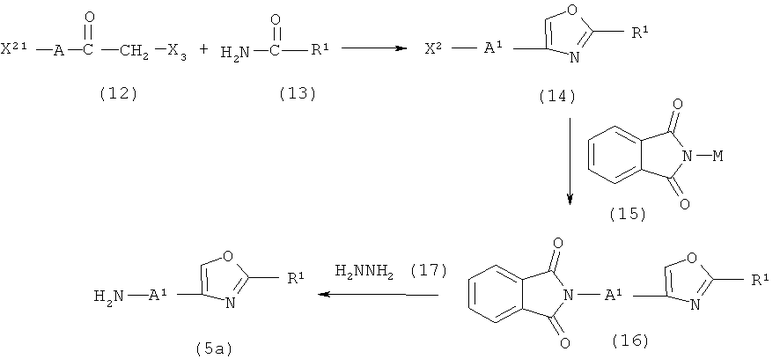
где R1 и A1 определены в формуле (1), X2 и X3, каждый независимо, представляют собой атом галогена или группу, которая подвергается такой же реакции замещения, как и атом галогена, как указано выше, и M представляет собой щелочной металл.
Примеры щелочного металла, представленного как M, включают натрий, калий и т.д.
Соединение (14) получают путем взаимодействия соединения (12) с соединением (13).
Взаимодействие соединения (12) с соединением (13) обычно осуществляют в известном растворителе, который не оказывает негативного влияния на реакцию. Такие растворители включают, например, воду; метанол, этанол, изопропанол, н-бутанол, трифторэтанол, этиленгликоль и другие спиртовые растворители; ацетон, метилэтилкетон и другие кетоновые растворители; тетрагидрофуран, диоксан, диэтиловый эфир, диметоксиэтан, диглим и другие эфирные растворители; метилацетат, этилацетат и другие сложноэфирные растворители; ацетонитрил, N,N-диметилформамид, диметилсульфоксид, N-метилпирролидон и другие апротонные полярные растворители; метиленхлорид, этиленхлорид и другие галогенированные углеводородные растворители; и другие органические растворители; и т.д.
Отношение соединения (12) к соединению (13) обычно составляет, по меньшей мере, 1 моль и, предпочтительно, от около 1 до около 5 моль последнего на моль первого. Взаимодействие соединения (12) с соединением (13) осуществляют при непрерывном перемешивании, обычно при температуре в пределах от комнатной температуры до 200°C и предпочтительно от комнатной температуры до 150°C, обычно в течение времени от 30 минут до 60 часов и предпочтительно от 1 до 30 часов.
Соединение (16) получают путем взаимодействия соединения (15) с соединением (14).
Взаимодействие соединения (15) с соединением (14) обычно осуществляют в известном растворителе, который не оказывает негативного влияния на реакцию. Такие растворители включают, например, воду; метанол, этанол, изопропанол, н-бутанол, трифторэтанол, этиленгликоль и другие спиртовые растворители; ацетон, метилэтилкетон и другие кетоновые растворители; тетрагидрофуран, диоксан, диэтиловый эфир, диглим и другие эфирные растворители; метилацетат, этилацетат и другие сложноэфирные растворители; ацетонитрил, N,N-диметилформамид, диметилсульфоксид и другие апротонные полярные растворители; метиленхлорид, этиленхлорид и другие галогенированные углеводородные растворители; другие органические растворители; их смеси; и т.д.
При осуществлении взаимодействия соединения (15) с соединением (14) в реакционную систему можно добавить иодиды щелочных металлов, такие как иодид калия, иодид натрия и т.д., в качестве ускорителей реакции, если это необходимо.
Отношение соединения (15) к соединению (14) обычно составляет, по меньшей мере, 1 моль и, предпочтительно, от около 1 до около 5 моль последнего на моль первого.
Температура реакции соединения (15) с соединением (14) не ограничена, и обычно реакцию можно осуществить при охлаждении, при комнатной температуре или при нагревании. Подходящим является осуществление реакции при температуре в пределах от комнатной температуры до 100°C, в течение времени от 1 до 60 часов и, предпочтительно, от 1 до 30 часов.
В реакции соединения (15) с соединением (14) фталимид можно использовать вместо соединения (15), и реакцию можно осуществлять в присутствии основания(ий). Можно использовать множество известных неорганических и органических оснований. Примеры неорганического основания включают щелочной металл (например, литий, натрий, калий и т.д.), гидрокарбонаты щелочных металлов (например, гидрокарбонат лития, гидрокарбонат натрия, гидрокарбонат калия и т.д.), гидроксиды щелочных металлов (например, гидроксид лития, гидроксид натрия, гидроксид калия, гидроксид цезия и т.д.), карбонаты щелочных металлов (например, карбонат лития, карбонат натрия, карбонат калия, карбонат цезия и т.д.), низшие алкоксиды щелочных металлов (например, метоксид натрия, этоксид натрия, трет-бутоксид калия, трет-бутоксид натрия и т.д.), гидриды щелочных металлов (например, гидрид натрия, гидрид калия и т.д.) и т.п. Органические основания включают, например, триалкиламины (например, триметиламин, триэтиламин, N-этилдиизопропиламин и т.д.), пиридин, хинолин, пиперидин, имидазол, пиколин, диметиламинопиридин, диметиланилин, N-метилморфолин, 1,5-диазабицикло[4.3.0]нон-5-ен (DBN), 1,4-диазабицикло[2.2.2]октан (DABCO), 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU) и т.д.
Количество основания(ий) обычно составляет от 0,5 до 10 моль и предпочтительно от 0,5 до 6 моль, на моль соединения (14).
Соединение (5a) получают путем взаимодействия соединения (16) с соединением (17).
Взаимодействие соединения (16) с соединением (17) обычно осуществляют в известном растворителе, который не оказывает негативного влияния на реакцию. Такие растворители включают, например, воду; метанол, этанол, изопропанол, н-бутанол, трифторэтанол, этиленгликоль и другие спиртовые растворители; ацетон, метилэтилкетон и другие кетоновые растворители; тетрагидрофуран, диоксан, диэтиловый эфир, диглим и другие эфирные растворители; метилацетат, этилацетат и другие сложноэфирные растворители; ацетонитрил, N,N-диметилформамид, диметилсульфоксид и другие апротонные полярные растворители; метиленхлорид, этиленхлорид и другие галогенированные углеводородные растворители; другие органические растворители; их смеси; и т.д.
Отношение соединения (16) к соединению (17) обычно составляет, по меньшей мере, 1 моль и, предпочтительно, от около 1 до около 5 моль последнего на моль первого.
Температура реакции соединения (16) с соединением (17) не ограничена, и обычно реакцию можно осуществить при охлаждении, при комнатной температуре или при нагревании.
Подходящим является осуществление реакции при температуре около комнатной, в течение времени от 1 до 30 часов.
Схема реакций 11
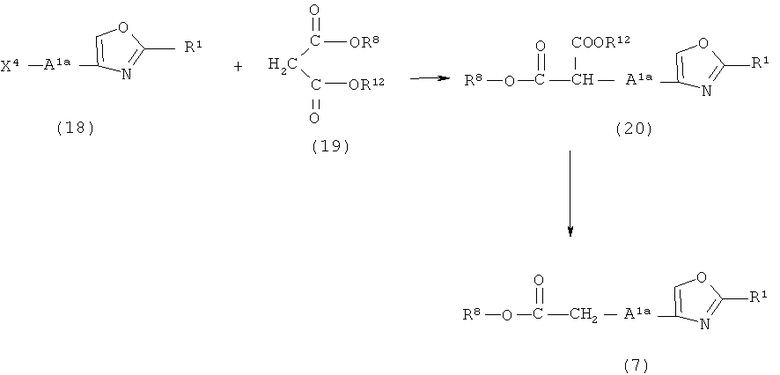
где R1 определен в формуле (1); R8 и A1a определены выше; X4 представляет собой атом галогена или группу, которая подвергается такой же реакции замещения, как и атом галогена, как указано выше; и R12 представляет собой низшую алкильную группу.
Соединение (20) получают путем взаимодействия соединения (18) с соединением (19).
Взаимодействие соединения (18) с соединением (19) обычно осуществляют в известном растворителе, который не оказывает негативного влияния на реакцию. Такие растворители включают, например, воду; метанол, этанол, изопропанол, н-бутанол, трифторэтанол, этиленгликоль и другие спиртовые растворители; ацетон, метилэтилкетон и другие кетоновые растворители; тетрагидрофуран, диоксан, диэтиловый эфир, диметоксиэтан, диглим и другие эфирные растворители; метилацетат, этилацетат и другие сложноэфирные растворители; ацетонитрил, N,N-диметилформамид, диметилсульфоксид, N-метилпирролидон и другие апротонные полярные растворители; метиленхлорид, этиленхлорид и другие галогенированные углеводородные растворители; другие органические растворители; их смеси; и т.д.
Взаимодействие соединения (18) с соединением (19) обычно осуществляют в присутствии подходящего основания(ий). Можно использовать множество известных неорганических и органических оснований. Неорганические основания включают, например, щелочные металлы (например, литий, натрий, калий и т.д.), гидрокарбонаты щелочных металлов (например, гидрокарбонат лития, гидрокарбонат натрия, гидрокарбонат калия и т.д.), гидроксиды щелочных металлов (например, гидроксид лития, гидроксид натрия, гидроксид калия, гидроксид цезия и т.д.), карбонаты щелочных металлов (например, карбонат лития, карбонат натрия, карбонат калия, карбонат цезия и т.д.), низшие алкоксиды щелочных металлов (например, метоксид натрия, этоксид натрия, трет-бутоксид калия, трет-бутоксид натрия и т.д.), гидриды щелочных металлов (например, гидрид натрия, гидрид калия и т.д.) и т.п. Органические основания включают, например, триалкиламины (например, триметиламин, триэтиламин, н-этилдиизопропиламин и т.д.), пиридин, хинолин, пиперидин, имидазол, пиколин, диметиламинопиридин, диметиланилин, N-метилморфолин, 1,5-диазабицикло[4.3.0]нон-5-ен (DBN), 1,4-диазабицикло[2.2.2]октан (DABCO), 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU) и т.д. Когда такие основания представляют собой жидкость, их также можно использовать в качестве растворителей.
Такие основания можно использовать отдельно или в сочетании.
Количество основания(ий) обычно составляет от 0,5 до 10 моль и предпочтительно от 0,5 до 6 моль, на моль соединения (18).
Отношение соединения (18) к соединению (19) в схеме реакций 11 обычно составляет, по меньшей мере, 1 моль и, предпочтительно, от около 1 до около 5 моль последнего на моль первого.
Температура реакции не ограничена, и обычно реакцию можно осуществить при охлаждении, при комнатной температуре или при нагревании. Подходящим является осуществление реакции при температуре в пределах от комнатной температуры до 100°C, в течение времени от 30 минут до 60 часов и, предпочтительно, от 1 до 30 часов.
Соединение (7) получают, подвергая соединение (20) гидролизу-декарбоксилированию. Гидролиз-декарбоксилирование соединения (20) можно осуществить способом, показанным в ссылочном примере 48 ниже, способом, аналогичным этому, способом показанным на схеме реакций 4 выше, или способом, аналогичным этому.
Схема реакций 12
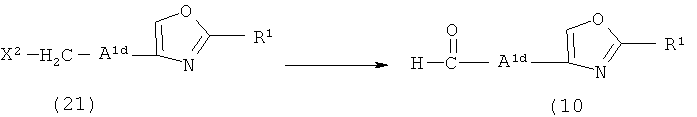
где R1 определен в формуле (1) и X2 и A1d определены выше.
Соединение (10) получают, подвергая соединение (21) реакции окисления. Эту реакцию можно осуществить способом, показанным в ссылочном примере 64 ниже, или способом, аналогичным этому, и ее осуществляют в присутствии известного растворителя, который не оказывает негативного влияния на реакцию. Такие растворители включают, например, воду; метанол, этанол, изопропанол, н-бутанол, трифторэтанол, этиленгликоль и другие спиртовые растворители; ацетон, метилэтилкетон и другие кетоновые растворители; тетрагидрофуран, диоксан, диэтиловый эфир, диглим и другие эфирные растворители; метилацетат, этилацетат и другие сложноэфирные растворители; ацетонитрил, N,N-диметилформамид, диметилсульфоксид и другие апротонные полярные растворители; метиленхлорид, этиленхлорид и другие галогенированные углеводородные растворители; другие органические растворители; их смеси; и т.д.
Реакцию обычно осуществляют с использованием окислителя(ей), такого как диметилсульфоксид, гексаметилентетрамин, триэтиламин-N-оксид и т.д.
Если это необходимо, реакцию можно осуществить в присутствии подходящего основания(ий). Можно использовать множество известных неорганических и органических оснований. Неорганические основания включают, например, щелочные металлы (например, натрий, калий и т.д.), гидрокарбонаты щелочных металлов (например, гидрокарбонат лития, гидрокарбонат натрия, гидрокарбонат калия и т.д.), гидроксиды щелочных металлов (например, гидроксид лития, гидроксид натрия, гидроксид калия, гидроксид цезия и т.д.), карбонаты щелочных металлов (например, карбонат лития, карбонат натрия, карбонат калия, карбонат цезия и т.д.), низшие алкоксиды щелочных металлов (например, метоксид натрия, этоксид натрия и т.д.), гидриды щелочных металлов (например, гидрид натрия, гидрид калия и т.д.) и т.п. Органические основания включают, например, триалкиламины (например, триметиламин, триэтиламин, N-этилдиизопропиламин и т.д.), пиридин, хинолин, пиперидин, имидазол, пиколин, диметиламинопиридин, диметиланилин, N-метилморфолин, 1,5-диазабицикло[4.3.0]нон-5-ен (DBN), 1,4-диазабицикло[2.2.2]октан (DABCO), 1,8-диазабицикло[5.4.0]ундец-7-ен (DBU) и т.д. Когда такие основания представляют собой жидкость, их также можно использовать в качестве растворителей. Такие основания можно использовать отдельно или в сочетании.
Количество окислителя обычно составляет от 0,5 до 10 моль и предпочтительно от 0,5 до 6 моль, на моль соединения (21).
Количество основания(ий) обычно составляет от 0,5 до 10 моль и предпочтительно от 0,5 до 6 моль, на моль соединения (21).
При осуществлении указанной выше реакции в реакционную систему можно добавить щелочные металлы, такие как иодид калия, иодид натрия и т.д., в качестве ускорителей реакции, если это необходимо.
Температура реакции не ограничена, и обычно реакцию можно осуществить при охлаждении, при комнатной температуре или при нагревании. Подходящим является осуществление реакции при температуре в пределах от комнатной температуры до 120°C в течение времени от 30 минут до 30 часов.
Соединения, используемые в качестве исходных веществ в представленных выше схемах реакций, могут представлять собой подходящие соли, и целевые соединения, получаемые при осуществлении указанных выше реакций, могут быть в форме подходящих солей.
Каждое из целевых соединений, полученных в соответствии с представленными выше схемами реакций, может быть выделено из реакционной смеси и очищено, например путем охлаждения реакционной смеси, выделения неочищенного продукта реакции из реакционной смеси с использованием процедуры выделения, такой как фильтрование, концентрирование, экстракция и/или другие процедуры выделения, с последующей очисткой неочищенного продукта реакции колоночной хроматографией, перекристаллизацией и/или с использованием других традиционных процедур очистки.
Подходящие соли соединения (1) представляют собой фармацевтически приемлемые соли, включая, например, соли металлов, такие как соли щелочных металлов (например, соли натрия, соли калия и т.д.), соли щелочноземельных металлов (например, соли кальция, соли магния и т.д.) и т.д., соли аммония, карбонаты щелочных металлов (например, карбонат лития, карбонат калия, карбонат натрия, карбонат цезия и т.д.), гидрокарбонаты щелочных металлов (например, гидрокарбонат лития, гидрокарбонат натрия, гидрокарбонат калия и т.д.), гидроксиды щелочных металлов (например, гидроксид лития, гидроксид натрия, гидроксид калия, гидроксид цезия и т.д.), и другие соли неорганических оснований; три(низший)алкиламины (например, триметиламин, триэтиламин, N-этилдиизопропиламин и т.д.), пиридин, хинолин, пиперидин, имидазол, пиколин, диметиламинопиридин, диметиланилин, N-(низший)алкилморфолины (например, N-метилморфолин и т.п.), DBN, DBU, DABCO и другие соли органических оснований; гидрохлориды, гидробромиды, гидроиодиды, сульфаты, нитраты, фосфаты и другие соли неорганических кислот; формиаты, ацетаты, пропионаты, оксалаты, малонаты, сукцинаты, фумараты, малеинаты, лактаты, малаты, тартраты, цитраты, карбонаты, пикраты, метансульфонаты, этансульфонаты, пара-толуолсульфонаты, глутаматы и другие соли органических кислот; и т.д.
Исходные соединения и целевые соединения, представленные формулами в схемах реакций выше, охватывают сольваты (например, гидраты, этаноляты и т.д.). Предпочтительные сольваты включают гидраты.
Соединения, представленные формулой (1) по настоящему изобретению, безусловно, охватывают изомеры, такие как геометрические изомеры, стереоизомеры, оптические изомеры и т.д.
Эффективность и применение лекарственного средства
Соединения, представленные формулой (1), их оптически активные изомеры и их соли (далее указаны как “соединения по настоящему изобретению”) обладают специфическим ингибирующим действием против PDE4 и, следовательно, являются полезными в качестве активных ингредиентов для ингибитора PDE4.
Кроме того, благодаря их PDE4-специфическому ингибирующему действию, соединения по настоящему изобретению могут быть полезными в качестве активных ингредиентов фармацевтических композиций, используемых в качестве профилактических и терапевтических средств от различных заболеваний. Более конкретно, заболевания, профилактику и лечение которых можно эффективно осуществлять посредством PED4-специфического ингибирующего действия, включают имеющие различное происхождение острые и хронические (в частности, воспалительные и индуцированные аллергенами) заболевания дыхательных путей (например бронхиальная астма, хроническое обструктивное легочное заболевание и т.д.); дерматозы (в частности, гиперпластические, воспалительные и аллергические заболевания) (например псориаз (обычный), токсическая и аллергическая контактная экзема, атопический дерматит, очаговая алопеция и другие гиперпластические, воспалительные и аллергические дерматозы); заболевания с нервными функциональными отклонениями, такие как расстройства способности к запоминанию, памяти и познавательной способности, связанные с болезнью Альцгеймера и болезнью Паркинсона; заболевания, связанные с психическими нарушениями (например маниакально-депрессивный психоз, шизофрения, тревога и т.д.); системный и местный артрит (например остеоартрит коленного сустава, ревматизм суставов и т.д.); желудочно-кишечное диффузное воспаление (например болезнь Крона и язвенный колит); аллергические и/или хронические иммуно-опосредованные воспалительные заболевания верхних дыхательных путей (глотки, носа) и смежных областей (носовых пазух, глаз) (например аллергический ринит/синусит, хронический ринит/синусит, аллергический конъюнктивит), и т.п. Из указанного выше соединения являются особенно эффективными для профилактики и лечения атопического дерматита, что делает это заболевание подходящей мишенью для профилактики и лечения.
При использовании в качестве ингибитора PDE4 или в качестве профилактического или терапевтического средства от указанных выше различных заболеваний соединения по настоящему изобретению можно использовать в качестве оральных средств, растворов для инъекций, наружных препаратов и т.п.
Для оральных средств, например, соединения могут быть получены в такой форме, как порошки, таблетки, гранулы, капсулы, сиропы, пленки, драже, жидкости и т.д. Такие оральные средства могут содержать фармацевтически приемлемые материалы основы и носители и, кроме того, могут, необязательно, содержать связующие, дезинтеграторы, лубриканты, увлажняющие вещества, буферы, консерванты, отдушки и т.п., если это необходимо.
Для растворов для инъекций соединения могут быть получены в форме растворов, растворенных в физиологическом растворе, растворах виноградного сахара и т.п., или в форме водных суспензий.
Для наружных препаратов соединения, например, могут быть получены в такой форме, как жидкие лекарственные препараты, масляные лекарственные препараты, лосьоны, линименты, эмульсии, суспензии, кремы, мази и т.д. Такие наружные препараты могут, необязательно, содержать различные носители, материалы основы и добавки, обычно используемые в наружных препаратах, и их примеры включают воду, масла, поверхностно-активные вещества, солюбилизированные компоненты, эмульгаторы, красящие вещества (красители и пигменты), отдушки, консерванты, дезинфицирующие вещества, загустители, антиоксиданты, хелатообразующие вещества, вещества для регулирования pH, дезодорирующие вещества и т.д.
При использовании в качестве ингибитора PDE4 или в качестве профилактического или терапевтического средства от указанных выше различных заболеваний эффективная доза и количество доз в день соединения варьируют в зависимости от цели использования, типа используемого соединения, возраста, массы тела, симптомов и т.д. субъекта, и не могут назначаться одинаково. Например, ингибитор или средство можно вводить в дозе от 0,1 до 1000 мг соединения(соединений) по настоящему изобретению в день в расчете на взрослого, и такую дозу можно вводить в один или несколько приемов в день.
Кроме того, с других точек зрения, настоящее изобретение обеспечивает способ лечения или профилактики указанных выше различных заболеваний, включающий стадию введения эффективной дозы соединения(соединений) по настоящему изобретению млекопитающему, такому как человек.
Более того, поскольку соединения по настоящему изобретению обладают ингибирующим действием против продукции TNF-α, они являются полезными в качестве активных ингредиентов для средств, подавляющих продукцию TNF-α. Заболевания, при которых полезно такое действие по ингибированию продукции TNF-α, включают заболевания, профилактику и лечение которых можно эффективно осуществлять посредством PED4-специфического ингибирующего действия. Лекарственные формы, пути введения и дозы средств, подавляющих продукцию TNF-α, содержащих соединения по настоящему изобретению, такие же, как указано выше для ингибитора PDE4 и профилактических и терапевтических средств.
Эффект настоящего изобретения
Соединения по настоящему изобретению обладают специфическим ингибирующим действием против PDE4 и, таким образом, являются полезными в качестве активных ингредиентов для ингибиторов PDE4.
Благодаря их ингибирующей активности, специфической в отношении PDE4, соединения по настоящему изобретению также являются полезными в качестве профилактических и терапевтических средств от различных заболеваний, включая атопический дерматит.
Лучший способ осуществления изобретения
Настоящее изобретение описано более подробно ниже со ссылкой на примеры; однако настоящее изобретение не ограничивается ими.
Ссылочный пример 1
25 г изованилиновой кислоты суспендировали в 250 мл метанола и добавляли 1,5 г моногидрата пара-толуолсульфоновой кислоты. Смесь нагревали и кипятили с обратным холодильником в течение ночи. После завершения реакции метанол отгоняли при пониженном давлении. Остаток нейтрализовали насыщенным водным раствором бикарбоната натрия и затем экстрагировали этилацетатом. После промывки насыщенным солевым раствором дважды, органический слой отделяли и концентрировали при пониженном давлении. Остаток очищали при помощи колоночной хроматографии на силикагеле (н-гексан:этилацетат = 1:1) с получением 24,5 г метил 3-гидрокси-4-метоксибензоата в виде белого кристаллического вещества.
1Н-ЯМР (CDCl3) δ: 7,63-7,58 (2H, м), 6,67 (1H, д, J=8,1 Гц), 5,63 (1H, с), 3,98 (3H, с), 3,90 (3H, с).
Ссылочный пример 2
20 г метил 3-гидрокси-4-метоксибензоата, полученного в ссылочном примере 1, растворяли в 200 мл метанола и добавляли 24,6 мл 1,8-диазабицикло[5.4.0]ундец-7-ена и 21 г бензилбромида. Смесь нагревали и кипятили с обратным холодильником в течение ночи. Затем реакционную смесь концентрировали, добавляли к остатку воду и осуществляли экстракцию этилацетатом. Экстракт дважды промывали насыщенным солевым раствором и органический слой отделяли и сушили над сульфатом магния. Затем нерастворимые вещества удаляли при помощи фильтрации, фильтрат концентрировали при пониженном давлении с получением 25,5 г метил 3-бензилокси-4-метоксибензоата в виде белого кристаллического вещества.
1Н-ЯМР (CDCl3) δ: 7,68 (1H, дд, J=8,4, 1,8 Гц), 7,61 (1H, д, J=1,8 Гц), 7,48-7,28 (5H, м), 6,91 (1H, д, J=8,4 Гц), 5,17 (2H, с), 3,93 (3H, с), 3,87 (3H, с).
Ссылочный пример 3
25 г метил 3-бензилокси-4-метоксибензоата, полученного в ссылочном примере 2, растворяли в 100 мл ацетонитрила и добавляли раствор 11 г гидроксида натрия в 100 мл воды. Смесь перемешивали при нагревании при 40°C в течение 5 часов. Реакционную смесь охлаждали льдом и добавляли концентрированную соляную кислоту, доводя уровень pH до приблизительно 3. Осажденные кристаллы собирали при помощи фильтрации и сушили при пониженном давлении с получением 22,1 г 3-бензилокси-4-метоксибензойной кислоты в виде белого кристаллического вещества.
1Н-ЯМР (CDCl3) δ: 7,77 (1H, дд, J=8,4, 1,8 Гц), 7,65 (1H, д, J=1,8 Гц), 7,48-7,29 (5H, м), 6,94 (1H, д, J=8,4 Гц), 5,19 (2H, с), 3,95 (3H, с).
Ссылочный пример 4
20 г 3-бензилокси-4-метоксибензойной кислоты, полученной в ссылочном примере 3, суспендировали в 200 мл дихлорметана и добавляли одну каплю диметилформамида. Добавляли по каплям 8,1 мл оксалилхлорида при охлаждении льдом и перемешивании. Через 2 часа реакционную смесь концентрировали при пониженном давлении. Остаток растворяли в 50 мл тетрагидрофурана и полученный раствор добавляли по каплям к 28%-ному водному раствору аммиака при охлаждении льдом и перемешивании. Полученную смесь перемешивали в течение 1 часа и осажденные кристаллы собирали при помощи фильтрации и сушили при пониженном давлении с получением 19,9 г белого порошкообразного 3-бензилокси-4-метоксибензамида.
1Н-ЯМР (CDCl3) δ: 7,85-7,28 (7H, м), 6,90 (1H, д, J=8,1 Гц), 5,67 (2H, ушир.с), 5,18 (2H, с), 3,93 (3H, с)
Ссылочный пример 5
15 г 3-бензилокси-4-метоксибензамида, полученного в ссылочном примере 4, суспендировали в 450 мл изопропанола, и добавляли 13,9 г 1,3-дихлор-2-пропанона. Смесь нагревали и кипятили с обратным холодильником в течение ночи. Затем реакционную смесь концентрировали до половины ее начального объема при пониженном давлении, к концентрату добавляли 200 мл н-гексана и смесь перемешивали. Осажденные кристаллы собирали при помощи фильтрации и сушили при пониженном давлении с получением 12,2 г белого порошкообразного 2-(3-бензилокси-4-метоксифенил)-4-хлорметилоксазола.
1Н-ЯМР (CDCl3) δ: 7,73-7,71 (3H, м), 7,50-7,29 (5H, м), 6,95 (1H, д, J=5,7 Гц), 5,20 (2H, с), 4,56 (2H, с), 3,93 (3H, с).
Ссылочный пример 6
11 г 2-(3-бензилокси-4-метоксифенил)-4-хлорметилоксазола, полученного в ссылочном примере 5, суспендировали в 220 мл этанола и добавляли 7,5 г иодида натрия и 9,3 г фталимида калия. Смесь нагревали и кипятили с обратным холодильником в течение ночи. Реакционную смесь охлаждали льдом и осажденные кристаллы собирали при помощи фильтрации. Полученные неочищенные кристаллы суспендировали и промывали 100 мл воды. Полученные кристаллы сушили при пониженном давлении с получением 9,4 г белого порошкообразного 2-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]изоиндoлин-1,3-диона.
1Н-ЯМР (CDCl3) δ: 7,91-7,85 (2H, м), 7,76-7,69 (2H, м), 7,61-7,58 (3H, м), 7,46 (2H, д, J=6,6 Гц), 7,39-7,26 (3H, м), 6,91 (1H, д, J=9 Гц), 5,18 (2H, с), 4,85 (2H, с), 3,90 (3H, с).
Ссылочный пример 7
9 г 2-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]изоиндoлин-1,3-диона, полученного в ссылочном примере 6, суспендировали в 200 мл этанола и добавляли 3,1 мл гидразинмоногидрата. Смесь нагревали и кипятили с обратным холодильником в течение 3 часов. После охлаждения реакционной смеси добавляли 200 мл дихлорметана и смесь перемешивали. Нерастворимые вещества удаляли при помощи фильтрации и фильтрат концентрировали при пониженном давлении. Остаток очищали при помощи колоночной хроматографии на силикагеле (NH диоксид кремния, продукт фирмы Fuji Sylisia Chemical Ltd., дихлорметан:метанол = 20:1) с получением 4,5 г бледно-желтого порошкообразного [2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]метиламина.
1Н-ЯМР (CDCl3) δ: 7,63-7,59 (2H, м), 7,53-7,46 (3H, м), 7,41-7,27 (3H, м) 6,94 (1H, д, J=9 Гц), 5,20 (2H, с), 3,89 (3H, с), 3,87 (2H, с), 2,14 (2H, ушир.с).
Ссылочный пример 8
15 г метил 3-гидрокси-4-метоксибензоата, полученного в ссылочном примере 1, растворяли в 150 мл диметилформамида и добавляли 34 г карбоната калия и 22,2 г (бромметил)циклопропана. Смесь нагревали при 90°C в течение ночи. К реакционной смеси добавляли ледяную воду и осажденные кристаллы собирали при помощи фильтрации и промывали большим количеством воды. Полученные кристаллы сушили при пониженном давлении при комнатной температуре с получением 18,3 г белого кристаллического метил 3-циклопропилметокси-4-метоксибензоата.
1Н-ЯМР (CDCl3) δ: 7,67 (1H, дд, J=8,4, 1,8 Гц), 7,52 (1H, д, J=2,1 Гц), 6,89 (1H, д, J=8,4 Гц), 3,94-3,86 (8H, м), 1,43-1,29 (1H, м), 0,70-0,58 (2H, м), 0,45-0,30 (2H, м).
Ссылочный пример 9
Используя 18 г метил 3-циклопропилметокси-4-метоксибензоата, полученного в ссылочном примере 8, и следуя процедуре ссылочного примера 3, получали 16,6 г белой кристаллической 3-циклопропилметокси-4-метоксибензойной кислоты.
1Н-ЯМР (CDCl3) δ: 7,76 (1H, дд, J=8,4, 1,8 Гц), 7,58 (1H, д, J=2,1 Гц), 6,92 (1H, д, J=8,4 Гц), 3,98-3,92 (8H, м), 1,43-1,29 (1H, м), 0,70-0,58 (2H, м), 0,46-0,35 (2H, м).
Ссылочный пример 10
Используя 16,5 г 3-циклопропилметокси-4-метоксибензойной кислоты, полученной в ссылочном примере 9, и следуя процедуре, описанной в ссылочном примере 4, получали 16,2 г бледно-желтого порошкообразного 3-циклопропилметокси-4-метоксибензамида.
1Н-ЯМР (CDCl3) δ: 7,43 (1H, д, J=2,1 Гц), 7,31 (1H, дд, J=8,4, 2,1 Гц), 6,88 (1H, д, J=8,1 Гц), 5,75 (2H, ушир.с), 3,97-3,89 (5H, м), 1,40-1,28 (1H, м), 0,69-0,62 (2H, м), 0,39-0,33 (2H, м).
Ссылочный пример 11
Используя 13 г 3-циклопропилметокси-4-метоксибензамида, полученного в ссылочном примере 10, и следуя процедуре, описанной в ссылочном примере 5, получали 10,5 г бледно-желтого порошкообразного 4-хлорметил-2-(3-циклопропилметокси-4-метоксифенил)оксазола.
1Н-ЯМР (CDCl3) δ: 7,65 (1H, д, J=0,9 Гц), 7,20 (1H, дд, J=8,7, 2,1 Гц), 7,53 (1H, д, J=2,1 Гц), 6,93 (1H, д, J=8,4 Гц), 4,57 (2H, с), 3,97-3,90 (5H, м), 1,43-1,32 (1H, м), 0,71-0,63 (2H, м), 0,41-0,35 (2H, м).
Ссылочный пример 12
Используя 8 г 4-хлорметил-2-(3-циклопропилметокси-4-метоксифенил)оксазола, полученного в ссылочном примере 11, и следуя процедуре, описанной в ссылочном примере 6, получали 10 г белого кристаллического 2-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]изоиндoлин-1,3-диона.
1Н-ЯМР (CDCl3) δ: 7,90-7,84 (2H, м), 7,76-7,69 (2H, м), 7,62 (1H, с), 7,57 (1H, дд, J=8,4, 2,1 Гц), 7,48 (1H, д, J=2,1 Гц), 6,89 (1H, д, J=8,4 Гц), 4,85 (2H, с), 3,95-3,90 (5H, м), 1,41-1,31 (1H, м), 0,69-0,62 (2H, м), 0,41-0,35 (2H, м).
Ссылочный пример 13
Используя 9,5 г 2-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]изоиндoлин-1,3-диона, полученного в ссылочном примере 12, и следуя процедуре, описанной в ссылочном примере 7, получали 5,1 г белого порошкообразного [2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]метиламина.
1Н-ЯМР (CDCl3) δ: 7,61-7,55 (1H, м), 7,53-7,50 (2H, м), 6,92 (1H, д, J=8,4 Гц), 3,96-3,87 (5H, м), 3,83 (2H, с), 1,41-1,33 (1H, м), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Ссылочный пример 14
5 г метил 3-гидрокси-4-метоксибензоата, полученного в ссылочном примере 1, растворяли в 100 мл диметилформамида и добавляли 11,3 г карбоната калия и 5,64 г изобутилбромида. Смесь нагревали при 80°C в течение 6 часов. К реакционной смеси добавляли ледяную воду и осажденные кристаллы собирали при помощи фильтрации и промывали большим количеством воды. Полученные кристаллы сушили при пониженном давлении при комнатной температуре с получением 5,85 г белого порошкообразного метил 3-изобутокси-4-метоксибензоата.
1Н-ЯМР (CDCl3) δ: 7,65 (1H, дд, J=8,4, 2,1 Гц), 7,53 (1H, д, J=1,8 Гц), 6,88 (1H, д, J=8,1 Гц), 3,96 (3H, с), 3,91 (3H, с), 3,82 (2H, д, J=6,9 Гц), 2,20-2,11 (1H, м), 1,05 (6H, д, J=6,6 Гц).
Ссылочный пример 15
Используя 5,85 г метил 3-изобутокси-4-метоксибензоата, полученного в ссылочном примере 14, и следуя процедуре, описанной в ссылочном примере 3, получали 5,6 г белой порошкообразной 3-изобутокси-4-метоксибензойной кислоты.
1Н-ЯМР (CDCl3) δ: 7,75 (1H, дд, J=8,4, 1,8 Гц), 7,58 (1H, д, J=2,1 Гц), 6,91 (1H, д, J=8,7 Гц), 3,94 (3H, с), 3,83 (2H, д, J=6,6 Гц), 2,26-2,12 (1H, м), 1,05 (6H, д, J=6,6 Гц).
Ссылочный пример 16
Используя 5,5 г 3-изобутокси-4-метоксибензойной кислоты, полученной в ссылочном примере 15, и следуя процедуре, описанной в ссылочном примере 4, получали 5,1 г бледно-желтого порошкообразного 3-изобутокси-4-метоксибензамида.
1Н-ЯМР (CDCl3) δ: 7,43 (1H, д, J=2,1 Гц), 7,31 (1H, дд, J=8,4, 2,1 Гц), 6,87 (1H, д, J=8,7 Гц), 5,78 (2H, ушир.с), 3,91 (3H, с), 3,83 (2H, д, J=6,6 Гц), 2,25-2,11 (1H, м), 1,04 (6H, д, J=6,6 Гц).
Ссылочный пример 17
Используя 5 г 3-изобутокси-4-метоксибензамида, полученного в ссылочном примере 16, и следуя процедуре, описанной в ссылочном примере 5, получали 3,4 г бледно-желтого порошкообразного 4-хлорметил-2-(3-изобутокси-4-метоксифенил)оксазола.
1Н-ЯМР (CDCl3) δ: 7,65 (1H, с), 7,60 (1H, дд, J=8,4, 2,1 Гц), 7,53 (1H, д, J=2,1 Гц), 6,92 (1H, д, J=8,4 Гц), 4,57 (2H, с), 3,91 (3H, с), 3,85 (2H, д, J=6,9 Гц), 2,27-2,13 (1H, м), 1,05 (6H, д, J=6,6 Гц).
Ссылочный пример 18
Используя 3,3 г 4-хлорметил-2-(3-изобутокси-4-метоксифенил)оксазола, полученного в ссылочном примере 17, и следуя процедуре, описанной в ссылочном примере 6, получали 4,4 г белого порошкообразного 2-[2-(3-изобутокси-4-метоксифенил)оксазол-4-илметил]изоиндoлин-1,3-диона.
1Н-ЯМР (CDCl3) δ: 7,91-7,84 (2H, м), 7,76-7,71 (2H, м), 7,62 (1H, с), 7,55 (1H, дд, J=8,4, 2,1 Гц), 7,49 (1H, д, J=2,1 Гц), 6,88 (1H, д, J=8,4 Гц), 4,85 (2H, с), 3,89 (3H, с), 3,83 (2H, д, J=6,6 Гц), 2,23-2,13 (1H, м), 1,05 (6H, д, J=6,6 Гц).
Ссылочный пример 19
Используя 4,4 г 2-[2-(3-изобутокси-4-метоксифенил)оксазол-4-илметил]изоиндoлин-1,3-диона, полученного в ссылочном примере 18, и следуя процедуре, описанной в ссылочном примере 7, получали 2 г белого твердого [2-(3-изобутокси-4-метоксифенил)оксазол-4-ил]метиламина.
1Н-ЯМР (CDCl3) δ: 7,60-7,51 (3H, м), 6,92 (1H, д, J=8,4 Гц), 3,91 (3H, с), 3,87-3,84 (4H, м), 2,27-2,13 (1H, м), 1,71 (2H, ушир.с), 1,06 (6H, д, J=6,6 Гц).
Ссылочный пример 20
Используя 10 г метил 3-гидрокси-4-метоксибензоата, полученного в ссылочном примере 1, и следуя процедуре, описанной в ссылочном примере 14, получали 12,5 г белого порошкообразного метил 4-метокси-3-(2,2,2-трифторэтокси)бензоата.
1Н-ЯМР (CDCl3) δ: 7,79 (1H, дд, J=8,7, 1,8 Гц), 7,63 (1H, с), 6,94 (1H, д, J=8,7 Гц), 4,42 (2H, кв, J=8,1 Гц), 3,94 (3H, с), 3,91 (3H, с).
Ссылочный пример 21
Используя 12 г метил 4-метокси-3-(2,2,2-трифторэтокси)бензоата, полученного в ссылочном примере 20, и следуя процедуре, описанной в ссылочном примере 3, получали 11,5 г белой порошкообразной 4-метокси-3-(2,2,2-трифторэтокси)бензойной кислоты.
1Н-ЯМР (CDCl3) δ: 7,86 (1H, дд, J=8,4, 1,8 Гц), 7,67 (1H, д, J=1,8 Гц), 6,97 (1H, д, J=8,4 Гц), 4,43 (2H, кв, J=8,4 Гц), 3,96 (3H, с).
Ссылочный пример 22
Используя 11,5 г 4-метокси-3-(2,2,2-трифторэтокси)бензойной кислоты, полученной в ссылочном примере 21, и следуя процедуре, описанной в ссылочном примере 4, получали 10,8 г белого порошкообразного 4-метокси-3-(2,2,2-трифторэтокси)бензамида.
1Н-ЯМР (CDCl3) δ: 7,50 (1H, ушир.с), 7,49 (1H, дд, J=8,4, 2,4 Гц), 6,94 (1H, д, J=8,4 Гц), 4,43 (2H, кв, J=8,4 Гц), 3,93 (3H, с).
Ссылочный пример 23
Используя 10,5 г 4-метокси-3-(2,2,2-трифторэтокси)бензамида, полученного в ссылочном примере 22, и следуя процедуре, описанной в ссылочном примере 5, получали 7,1 г бледно-желтого порошкообразного 4-хлорметил-2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазола.
1Н-ЯМР (CDCl3) δ: 7,75 (1H, дд, J=8,4, 2,1 Гц), 7,66 (1H, ушир.с), 7,64 (1H, д, J=2,1 Гц), 6,98 (1H, д, J=8,4 Гц), 4,56 (2H, с), 4,45 (2H, кв, J=8,4 Гц), 3,94 (3H, с).
Ссылочный пример 24
Используя 3 г 4-хлорметил-2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазола, полученного в ссылочном примере 23, и следуя процедуре, описанной в ссылочном примере 6, получали 3,6 г белого порошкообразного 2-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил] оксазол-4-илметил}изоиндoлин-1,3-диона.
1Н-ЯМР (CDCl3) δ: 7,91-7,85 (2H, м), 7,76-7,64 (3H, м), 7,60 (1H, с), 7,59 (1H, д, J=2,1 Гц), 6,94 (1H, д, J=8,7 Гц), 4,85 (2H, с), 4,43 (2H, кв, J=8,4 Гц), 3,91 (3H, с).
Ссылочный пример 25
Используя 3,6 г 2-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}изоиндoлин-1,3-диона, полученного в ссылочном примере 24, и следуя процедуре, описанной в ссылочном примере 7, получали 1,93 г белого порошкообразного {2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}метиламина.
1Н-ЯМР (CDCl3) δ: 7,73 (1H, дд, J=8,4, 2,1 Гц), 7,63 (1H, д, J=2,1 Гц), 7,52 (1H, с), 6,98 (1H, д, J=8,4 Гц), 4,46 (2H, кв, J=8,4 Гц), 3,93 (3H, с), 3,83 (2H, с), 1,55 (2H, ушир.с).
Ссылочный пример 26
Используя 9,5 г этилваннилата, и следуя процедуре, описанной в ссылочном примере 14, получали 11 г белого порошкообразного этил 3-метокси-4-(2,2,2-трифторэтокси)бензоата.
1Н-ЯМР (CDCl3) δ: 7,65 (1H, дд, J=8,4, 2,1 Гц), 7,60 (1H, д, J=2,1 Гц), 6,96 (1H, д, J=8,4 Гц), 4,49-4,33 (4H, м), 3,93 (3H, с), 1,39 (3H, т, J=6,9 Гц).
Ссылочный пример 27
12 г этил 3-метокси-4-(2,2,2-трифторэтокси)бензоата, полученного в ссылочном примере 26, суспендировали в 120 мл 47% бромистоводородной кислоты и суспензию нагревали и кипятили с обратным холодильником в течение ночи. Реакционную смесь выливали в ледяную воду и осажденные кристаллы собирали при помощи фильтрации, промывали большим количеством воды и затем сушили при пониженном давлении с получением 8,4 г бледно-красной кристаллической 3-гидрокси-4-(2,2,2-трифторэтокси)бензойной кислоты.
1Н-ЯМР (CDCl3) δ: 7,71-7,66 (2H, м), 6,91 (1H, д, J=5,1 Гц), 5,55 (1H, ушир.с), 4,50 (2H, кв, J=7,8 Гц).
Ссылочный пример 28
8,4 г 3-гидрокси-4-(2,2,2-трифторэтокси)бензойной кислоты, полученной в ссылочном примере 27, суспендировали в 150 мл этанола и добавляли 0,5 мл концентрированной серной кислоты. Смесь нагревали и кипятили с обратным холодильником в течение ночи. После завершения реакции этанол отгоняли при пониженном давлении. Остаток нейтрализовали насыщенным водным раствором бикарбоната натрия и затем экстрагировали этилацетатом. После двукратной промывки насыщенным солевым раствором органический слой отделяли и концентрировали при пониженном давлении. Остаток очищали при помощи колоночной хроматографии на силикагеле (н-гексан:этилацетат = 1:1) с получением 7,2 г белого кристаллического этил 3-гидрокси-4-(2,2,2-трифторэтокси)бензоата.
1Н-ЯМР (CDCl3) δ: 7,66-7,60 (2H, м), 6,87 (1H, д, J=8,1 Гц), 5,54 (1H, с), 4,48 (2H, кв, J=7,8 Гц), 4,35 (2H, кв, J=7,2 Гц), 1,38 (3H, т, J=7,2 Гц).
Ссылочный пример 29
Используя 7 г этил 3-гидрокси-4-(2,2,2-трифторэтокси)бензоата, полученного в ссылочном примере 28, и следуя процедуре, описанной в ссылочном примере 14, получали 8,5 г белого порошкообразного этил 3-циклопропилметокси-4-(2,2,2-трифторэтокси)бензоата.
1Н-ЯМР (CDCl3) δ: 7,63 (1H, дд, J=8,7, 2,1 Гц), 7,58 (1H, д, J=2,1 Гц), 7,00 (1H, д, J=8,7 Гц), 4,48 (2H, кв, J=8,1 Гц), 4,35 (2H, кв, J=6,9 Гц), 3,92 (2H, д, J=7,2 Гц), 1,41-1,25 (4H, м), 0,69-0,60 (2H, м), 0,40-0,32 (2H, м).
Ссылочный пример 30
Используя 8,5 г этил 3-циклопропилметокси-4-(2,2,2-трифторэтокси)бензоата, полученного в ссылочном примере 29, и следуя процедуре, описанной в ссылочном примере 3, получали 7,5 г белой порошкообразной 3-циклопропилметокси-4-(2,2,2-трифторэтокси)бензойной кислоты.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, дд, J=8,4, 1,8 Гц), 7,63 (1H, д, J=2,1 Гц), 7,02 (1H, д, J=8,1 Гц), 4,51 (2H, кв, J=8,1 Гц), 3,93 (2H, д, J=7,2 Гц), 1,37-1,25 (1H, м), 0,69-0,60 (2H, м), 0,41-0,35 (2H, м).
Ссылочный пример 31
Используя 7 г 3-циклопропилметокси-4-(2,2,2-трифторэтокси)бензойной кислоты, полученной в ссылочном примере 30, и следуя процедуре, описанной в ссылочном примере 4, получали 7,35 г белого твердого 3-циклопропилметокси-4-(2,2,2-трифторэтокси)бензамида.
1Н-ЯМР (CDCl3) δ: 7,48 (1H, д, J=2,1 Гц), 7,28-7,25 (1H, м), 7,01 (1H, д, J=8,4 Гц), 4,48 (2H, кв, J=8,4 Гц), 3,93 (2H, д, J=6,9 Гц), 1,37-1,25 (1H, м), 0,69-0,60 (2H, м), 0,41-0,35 (2H, м).
Ссылочный пример 32
Используя 5 г 3-циклопропилметокси-4-(2,2,2-трифторэтокси)бензамида, полученного в ссылочном примере 31, и следуя процедуре, описанной в ссылочном примере 5, получали 3,1 г белого порошкообразного 4-хлорметил-2-[3-циклопропилметокси-4-(2,2,2-трифторэтокси)фенил]оксазола.
1Н-ЯМР (CDCl3) δ: 7,67 (1H, с), 7,59-7,56 (2H, м), 7,05 (1H, д, J=9,0 Гц), 4,56 (2H, с), 4,48 (2H, кв, J=8,4 Гц), 1,35-1,26 (1H, м), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Ссылочный пример 33
Используя 0,85 г 4-хлорметил-2-[3-циклопропилметокси-4-(2,2,2-трифторэтокси)фенил]оксазола, полученного в ссылочном примере 32, и следуя процедуре, описанной в ссылочном примере 6, получали 0,6 г белого порошкообразного 2-{2-[3-циклопропилметокси-4-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}изоиндoлин-1,3-диона.
1Н-ЯМР (CDCl3) δ: 7,91-7,84 (2H, м), 7,76-7,69 (2H, м), 7,64 (1H, с), 7,60-7,51 (2H, м), 7,01 (1H, д, J=8,7 Гц), 4,85 (2H, с), 4,46 (2H, кв, J=8,4 Гц), 3,93 (2H, д, J=6,9 Гц), 1,35-1,24 (1H, м), 0,68-0,61 (2H, м), 0,40-0,34 (2H, м).
Ссылочный пример 34
Используя 0,55 г 2-{2-[3-циклопропилметокси-4-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}изоиндoлин-1,3-диона, полученного в ссылочном примере 33, и следуя процедуре, описанной в ссылочном примере 7, получали 0,32 г белого порошкообразного {2-[3-циклопропилметокси-4-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}метиламина.
1Н-ЯМР (CDCl3) δ: 7,61-7,52 (3H, м), 7,05 (1H, д, J=8,7 Гц), 4,48 (2H, кв, J=8,4 Гц), 3,95 (2H, д, J=7,2 Гц), 3,84 (2H, с), 1,56 (2H, ушир.с), 1,35-1,24 (1H, м), 0,70-0,61 (2H, м), 0,41-0,35 (2H, м).
Ссылочный пример 35
Используя 20 г 3,4-диэтоксибензамида, и следуя процедуре, описанной в ссылочном примере 5, получали 24,5 г белого порошкообразного 4-хлорметил-2-(3,4-диэтоксифенил)оксазола.
1Н-ЯМР (CDCl3) δ: 7,65 (1H, с), 7,58 (1H, дд, J=8,4, 1,8 Гц), 7,54 (1H, д, J=1,8 Гц), 6,92 (1H, д, J=8,4 Гц), 4,56 (2H, с), 4,18 (2H, кв, J=6,9 Гц), 4,15 (2H, кв, J=6,9 Гц), 1,48 (6H, т, J=6,9 Гц).
Ссылочный пример 36
Используя 8 г 4-хлорметил-2-(3,4-диэтоксифенил)оксазола, полученного в ссылочном примере 35, и следуя процедуре, описанной в ссылочном примере 6, получали 10 г белого порошкообразного 2-[2-(3,4-диэтоксифенил)оксазол-4-илметил]изоиндoлин-1,3-диона.
1Н-ЯМР (CDCl3) δ: 7,88 (2H, м), 7,72 (2H, м), 7,62 (1H, с), 7,54 (1H, д, J=8,4, 2,1 Гц), 7,50 (1H, д, J=2,1 Гц), 6,88 (1H, д, J=8,4 Гц), 4,85 (2H, с), 4,16 (2H, кв, J=6,9 Гц), 4,11 (2H, кв, J=6,9 Гц), 1,47 (6H, т, J=6,9 Гц).
Ссылочный пример 37
Используя 10 г 2-[2-(3,4-диэтоксифенил)оксазол-4-илметил]изоиндoлин-1,3-диона, полученного в ссылочном примере 36, и следуя процедуре, описанной в ссылочном примере 7, получали 5,7 г белого порошкообразного [2-(3,4-диэтоксифенил)оксазол-4-ил]метиламина.
1Н-ЯМР (CDCl3) δ: 7,56 (1H, д, J=8,4, 1,8 Гц), 7,54 (1H, д, J=1,8 Гц), 7,51 (1H, с), 6,91 (1H, д, J=8,4 Гц), 4,18 (2H, кв, J=6,9 Гц), 4,14 (2H, кв, J=6,9 Гц), 1,80 (1H, ушир.с), 3,84 (2H, с), 1,48 (3H, т, J=6,9 Гц), 1,48 (3H, т, J=6,9 Гц).
Ссылочный пример 38
Используя 2,0 г 3,4-диметоксибензамида, и следуя процедуре, описанной в ссылочном примере 5, получали 2,4 г белого порошкообразного 4-хлорметил-2-(3,4-диметоксифенил)оксазола.
1Н-ЯМР (CDCl3) δ: 7,66 (1H, с), 7,62 (1H, дд, J=8,4, 1,8 Гц), 7,55 (1H, д, J=1,8 Гц), 6,93 (1H, д, J=8,4 Гц), 4,52 (2H, с), 3,95 (3H, с), 3,91 (3H, с).
Ссылочный пример 39
Используя 2,4 г 4-хлорметил-2-(3,4-диметоксифенил)оксазола, полученного в ссылочном примере 38, и следуя процедуре, описанной в ссылочном примере 6, получали 2,3 г белого порошкообразного 2-[2-(3,4-диметоксифенил)оксазол-4-илметил]изоиндoлин-1,3-диона.
Ссылочный пример 40
Используя 2,3 г 2-[2-(3,4-диметоксифенил)оксазол-4-илметил]изоиндoлин-1,3-диона, полученного в ссылочном примере 39, и следуя процедуре, описанной в ссылочном примере 7, получали 1,3 г белого порошкообразного [2-(3,4-диметоксифенил)оксазол-4-ил]метиламина.
1Н-ЯМР (CDCl3) δ: 7,60 (1H, д, J=8,1, 2,1 Гц), 7,54 (1H, д, J=2,1 Гц), 6,92 (1H, д, J=8,1 Гц), 3,96 (3H, с), 3,93 (3H, с), 3,85 (2H, с), 1,81 (2H, ушир.с).
Ссылочный пример 41
9 г 4-дифторметокси-3-гидроксибензальдегида растворяли в 180 мл ацетонитрила и добавляли 13,1 г карбоната калия и 8,6 мл бензилбромида. Смесь перемешивали при комнатной температуре в течение 4 часов. Затем нерастворимые вещества удаляли при помощи фильтрации, фильтрат концентрировали и остаток очищали при помощи колоночной хроматографии на силикагеле (н-гексан:этилацетат = 1:1) с получением 11,9 г бесцветного маслянистого 3-бензилокси-4-дифторметоксибензальдегида.
1Н-ЯМР (CDCl3) δ: 10,21 (1H, с), 7,56 (1H, т, J=74,1 Гц), 7,53-7,28 (7H, м), 6,68 (1H, д, J=8,4 Гц), 5,20 (2H, с).
Ссылочный пример 42
6 г 3-бензилокси-4-дифторметоксибензальдегида, полученного в ссылочном примере 41, растворяли в 500 мл ацетона и добавляли 17 г перманганата калия. Смесь нагревали и кипятили с обратным холодильником в течение ночи. После отгонки ацетона из реакционной смеси к остатку добавляли 100 мл 5н. раствора гидроксида натрия и нерастворимые вещества удаляли при помощи фильтрации. К фильтрату добавляли концентрированную соляную кислоту, доводя уровень pH до приблизительно 3, и осажденные кристаллы собирали при помощи фильтрации. Полученные кристаллы сушили при пониженном давлении с получением 2,1 г коричневатой порошкообразной 3-бензилокси-4-дифторметоксибензойной кислоты.
1Н-ЯМР (CDCl3) δ: 7,78-7,72 (2H, м), 7,73-7,32 (5H, м), 7,33-7,24 (1H, м), 6,67 (1H, т, J=74,1 Гц), 5,20 (2H, с).
Ссылочный пример 43
2 г 3-бензилокси-4-дифторметоксибензойной кислоты, полученной в ссылочном примере 42, суспендировали в 40 мл дихлорметана и добавляли одну каплю диметилформамида. По каплям при охлаждении льдом и перемешивании добавляли 0,7 мл оксалилхлорида. Через 2 часа реакционную смесь концентрировали при пониженном давлении. Остаток растворяли в 5 мл ацетона и полученный раствор добавляли по каплям к 28%-ному водному раствору аммиака при охлаждении льдом и перемешивании. Полученную смесь перемешивали в течение 1 часа и осажденные кристаллы собирали при помощи фильтрации и сушили при пониженном давлении с получением 1,9 г белого порошкообразного 3-бензилокси-4-дифторметоксибензамида.
1Н-ЯМР (CDCl3) δ: 7,62 (1H, д, J=1,8 Гц), 7,45-7,20 (7H, м), 6,63 (1H, т, J=74,4 Гц), 5,19 (2H, с), 4,73 (2H, ушир.с).
Ссылочный пример 44
1,8 г 3-бензилокси-4-дифторметоксибензамида, полученного в ссылочном примере 43, суспендировали в 50 мл изопропанола и добавляли 1,17 г 1,3-дихлор-2-пропанона. Смесь нагревали и кипятили с обратным холодильником в течение ночи. Реакционную смесь концентрировали и полученный остаток очищали при помощи колоночной хроматографии на силикагеле (дихлорметан). Полученные неочищенные кристаллы перекристаллизовывали из изопропанола с получением 0,7 г белого порошкообразного 2-(3-бензилокси-4-дифторметоксифенил)-4-хлорметилоксазола.
1Н-ЯМР (CDCl3) δ: 7,44 (1H, д, J=1,8 Гц), 7,70 (1H, с), 7,48-7,32 (5H, м), 7,28-7,24 (1H, м), 6,63 (1H, т, J=74,7 Гц), 5,21 (2H, с), 4,57 (2H, с).
Ссылочный пример 45
0,37 г 2-(3-бензилокси-4-дифторметоксифенил)-4-хлорметилоксазола, полученного в ссылочном примере 44, растворяли в 20 мл этанола и добавляли 0,23 г иодида натрия и 0,27 г фталимида калия. Смесь нагревали и кипятили с обратным холодильником в течение 4 часов. Затем реакционную смесь концентрировали, к остатку добавляли воду и осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой и концентрировали с удалением растворителя и остаток очищали при помощи колоночной хроматографии на силикагеле (дихлорметан:метанол = 20:1) с получением 0,3 г белого порошкообразного 2-[2-(3-бензилокси-4-дифторметоксифенил)оксазол-4-илметил]изоиндoлин-1,3-диона.
1Н-ЯМР (CDCl3) δ: 7,90-7,84 (2H, м), 7,76-7,71 (4H, м), 7,59 (1H, дд, J=8,4, 2,1 Гц), 7,47-7,30 (5H, м), 7,22 (1H, д, J=2,4 Гц), 6,60 (1H, т, J=74,7 Гц), 5,20 (2H, с), 4,87 (2H, с).
Ссылочный пример 46
0,3 г 2-[2-(3-бензилокси-4-дифторметоксифенил)оксазол-4-илметил]изоиндoлин-1,3-диона, полученного в ссылочном примере 45, суспендировали в 10 мл этанола и добавляли 0,1 мл гидразинмоногидрата. Смесь нагревали и кипятили с обратным холодильником в течение 2 часов. После охлаждения реакционной смеси осажденные нерастворимые вещества удаляли при помощи фильтрации. Фильтрат концентрировали при пониженном давлении с получением 0,13 г бесцветного маслянистого [2-(3-бензилокси-4-дифторметоксифенил)оксазол-4-ил]метиламина.
1Н-ЯМР (CDCl3) δ: 7,74 (1H, д, J=1,8 Гц), 7,61 (1H, дд, J=7,8, 1,8 Гц), 7,47 (1H, д, J=1,8 Гц), 7,45-7,31 (5H, м), 7,26-7,20 (1H, м), 6,62 (1H, т, J=74,7 Гц), 5,21 (2H, с), 3,85 (2H, ушир.с).
Ссылочный пример 47
5,25 г гидрида натрия суспендировали в 150 мл тетрагидрофурана и добавляли по каплям при охлаждении льдом раствор 14,4 г диметилмалоната в 75 мл тетрагидрофурана в течение 15 минут. После перемешивания в течение 30 минут добавляли по каплям раствор 25 г 2-(3-бензилокси-4-метоксифенил)-4-хлорметилоксазола, полученного в ссылочном примере 5, в 150 мл диметилформамида в течение 15 минут. После добавления по каплям смесь перемешивали при температуре от 50 до 60°C в течение 4 часов и при охлаждении льдом добавляли водный насыщенный раствор хлорида аммония. После перемешивания смеси в течение 30 минут добавляли воду и осуществляли экстракцию этилацетатом. Экстракт сушили над безводным сульфатом магния и растворитель отгоняли при помощи дистилляции. Остаток перекристаллизовывали из смеси этилацетата и диизопропилового эфира с получением 26,5 г белого порошкообразного диметил 2-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]малоната.
1Н-ЯМР (ДМСО-d6) δ: 7,89 (1H, с), 7,59-7,31 (7H, м), 7,15 (1H, д, J=7,8 Гц), 5,16 (2H, с), 3,90-3,84 (4H, м), 3,71 (6H, с), 3,04 (2H, д, J=7,8 Гц).
Ссылочный пример 48
26,52 г диметил 2-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]малоната, полученного в ссылочном примере 47, суспендировали в 53 мл диметилсульфоксида и добавляли 2,62 г хлорида лития и 1,12 мл дистиллированной воды. Смесь перемешивали при 130°C в течение 4 часов. Затем реакционную смесь оставляли охлаждаться, добавляли воду и осуществляли экстракцию этилацетатом. Экстракт сушили над безводным сульфатом магния и растворитель отгоняли при помощи дистилляции. Остаток очищали при помощи колоночной хроматографии на силикагеле (н-гексан:этилацетат = 3:1) с получением 16 г белого порошкообразного метил 3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]пропионата.
1Н-ЯМР (CDCl3) δ: 7,62-7,59 (2H, м), 7,47 (2H, д, J=6,9 Гц), 7,40-7,31 (4H, м), 6,93 (1H, д, J=8,4 Гц), 5,20 (2H, с), 3,92 (3H, с), 3,69 (3H, с), 2,91 (2H, т, J=7,2 Гц), 2,72 (2H, т, J=7,2 Гц).
Ссылочный пример 49
0,48 г гидрида натрия суспендировали в 15 мл тетрагидрофурана и в течение 15 минут добавляли по каплям раствор 1,31 г диметилмалоната в 7,5 мл тетрагидрофурана. Затем смесь перемешивали в течение 30 минут, в течение 15 минут добавляли раствор 3,0 г 4-хлорметил-2-[3-циклопропилметокси-4-(2,2,2-трифторэтокси)фенил]оксазола, полученного в ссылочном примере 32, растворенного в 15 мл диметилформамида. После добавления по каплям смесь нагревали при температуре от 50 до 60°C при перемешивании в течение 4 часов. К реакционной смеси при охлаждении льдом добавляли насыщенный водный раствор хлорида аммония и перемешивание продолжали в течение 30 минут. Добавляли воду и осуществляли экстракцию этилацетатом. Экстракт сушили над безводным сульфатом магния и растворитель отгоняли при помощи дистилляции. К остатку добавляли 8,0 мл диметилсульфоксида, 0,35 г хлорида лития и 0,15 мл дистиллированной воды и смесь нагревали при перемешивании при 130°C в течение 4 часов. Затем реакционную смесь оставляли охлаждаться, добавляли воду и осуществляли экстракцию этилацетaтом. Экстракт сушили над безводным сульфатом магния и растворитель отгоняли при помощи дистилляции. Остаток очищали при помощи колоночной хроматографии на силикагеле (н-гексан:этилацетат = 4:1) с получением 1,63 г бесцветного маслянистого метил 3-{2-[3-циклопропилметокси-4-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}пропионата.
1Н-ЯМР (CDCl3) δ: 7,56-7,53 (2H, м), 7,43 (1H, с), 7,04 (1H, д, J=8,4 Гц), 4,47 (2H, кв, J=8,4 Гц), 3,94 (2H, д, J=6,6 Гц), 3,69 (3H, с), 2,91 (2H, т, J=7,2 Гц), 2,72 (2H, т, J=7,2 Гц), 0,88 (1H, т, J=6,6 Гц), 0,69-0,65 (2H, м), 0,40-0,35 (2H, м).
Ссылочный пример 50
0,5 г 2-циклопропилэтанола и 3,1 мл триэтиламина растворяли в 10 мл этилацетата и при охлаждении льдом и перемешивании добавляли 0,75 мл метансульфонилхлорида. После перемешивания в течение 30 минут к реакционной смеси добавляли воду и осуществляли экстракцию. Органический слой промывали двукратно водой и концентрировали с удалением растворителя при пониженном давлении с получением 1 г бледно-желтого маслянистого 2-циклопропилэтилметансульфоната.
1Н-ЯМР (CDCl3) δ: 4,29 (2H, т, J=6,6 Гц), 3,03 (3H, с), 1,66 (2H, кв, J=6,6 Гц), 0,84-0,70 (1H, м), 0,54-0,47 (2H, м), 0,20-0,10 (2H, м).
Ссылочный пример 51
Используя 2 г 2-циклопентилэтанола и следуя процедуре, описанной в ссылочном примере 50, получали 3,4 г бледно-желтого маслянистого 2-циклопентилэтилметансульфоната.
1Н-ЯМР (CDCl3) δ: 4,24 (2H, т, J=6,6 Гц), 3,03 (3H, с), 1,95-1,73 (5H, м), 1,70-1,48 (4H, м), 1,29-1,06 (2H, м).
Ссылочный пример 52
Используя 0,5 г циклопентилметанола и следуя процедуре, описанной в ссылочном примере 50, получали 0,7 г бледно-желтого маслянистого циклопентилметилметансульфоната.
1Н-ЯМР (CDCl3) δ: 4,11 (2H, д, J=6,9 Гц), 3,04 (3H, с), 2,38-2,23 (1H, м), 1,86-1,76 (2H, м), 1,74-1,53 (4H, м), 1,36-1,24 (2H, м).
Ссылочный пример 53
25 г 1-(2-гидроксифенил)этанона и 76 г карбоната калия суспендировали в 500 мл ацетонитрила и добавляли 31 мл аллилбромида. Смесь перемешивали при комнатной температуре в течение 48 часов. Реакционную смесь фильтровали для удаления нерастворившихся веществ и фильтрат концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 4:1) с получением 34 г бледно-желтого маслянистого 1-(2-аллилоксифенил)этанона.
1Н-ЯМР (CDCl3) δ: 7,73 (1H, дд, J=7,8, 1,8 Гц), 7,46-7,40 (1H, м), 7,02-6,93 (2H, м), 6,15-6,02 (1H, м), 5,47-5,30 (2H, м), 4,66-4,61 (2H, м), 2,64 (3H, с).
Ссылочный пример 54
40 г 3,4-диэтоксибензамида и 80 г метил 5-бром-4-оксопентаноата (содержащего около 35% метил 3-бром-4-оксопентаноата) добавляли к 400 мл диметилформамида и смесь перемешивали при 130°C в течение 16 часов. Реакционную смесь концентрировали при пониженном давлении и разбавляли этилацетатом. Постепенно добавляли этилацетат (500 мл) и насыщенный раствор бикарбоната натрия (500 мл) при перемешивании и продолжали перемешивание. Органический слой сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат:н-гексан = 1:8 до 1:4) с получением 18 г белого порошкообразного метил 3-[2-(3,4-диэтоксифенил)оксазол-4-ил]пропионата.
1Н-ЯМР (CDCl3) δ: 7,65-7,55 (2H, м), 7,51 (1H, с), 6,93 (1H, д, J=8,1 Гц), 4,19 (2H, кв, J=6,9 Гц), 4,15 (2H, кв, J=6,9 Гц), 3,80 (3H, с), 3,00-2,90 (2H, м), 2,70-2,60 (2H, м), 1,50 (3H, т, J=6,9 Гц), 1,49 (3H, т, J=6,9 Гц).
Ссылочный пример 55
37,9 г 3,4-дибензилоксибензамида и 28,8 г 1,3-дихлор-2-пропанона суспендировали в 500 мл пропанола и суспензию нагревали и кипятили с обратным холодильником в течение 3 дней. После охлаждения реакционную смесь концентрировали до половины ее исходного объема при пониженном давлении и добавляли 300 мл диизопропилового эфира. Осажденные кристаллы собирали при помощи фильтрации и перекристаллизовывали из смеси ацетон-метанол-диизопропиловый эфир. Полученные кристаллы сушили при пониженном давлении с получением 20,1 г бесцветного порошкообразного 2-(3,4-бис(бензилокси)фенил)-4-хлорметилоксазола.
1Н-ЯМР (CDCl3) δ: 7,66 (1H, д, J=2,1 Гц), 7,64 (1H, с), 7,59 (1H, дд, J=8,4, 2,1 Гц), 7,50-7,28 (10H, м), 6,99 (1H, д, J=8,4 Гц), 5,22 (2H, с), 5,21 (2H, с), 4,55 (2H, с).
Ссылочный пример 56
Используя 10 г 2-(3,4-бис(бензилокси)фенил)-4-хлорметилоксазола, полученного в ссылочном примере 55, и следуя процедуре, описанной в ссылочном примере 47, получали 12,3 г бесцветного маслянистого диметил 2-[2-(3,4-бис(бензилокси)фенил)оксазол-4-илметил]малоната.
1Н-ЯМР (CDCl3) δ: 7,61 (1H, д, J=2,1 Гц), 7,58-7,27 (12H, м), 6,97 (1H, д, J=8,4 Гц), 5,23-5,20 (4H, м), 3,89 (1H, т, J=7,5 Гц), 3,75 (3H, с), 3,73 (3H, с), 3,18 (2H, д, J=7,5 Гц).
Ссылочный пример 57
Используя 12,3 г диметил 2-[2-(3,4-бис(бензилокси)фенил)оксазол-4-илметил]малоната, полученного в ссылочном примере 56, и следуя процедуре, описанной в ссылочном примере 48, получали 4 г бледно-красного порошкообразного метил 3-[2-(3,4-бис(бензилокси)фенил)оксазол-4-ил]пропионата.
1Н-ЯМР (CDCl3) δ: 7,63 (1H, д, J=2,1 Гц), 7,57-7,27 (12H, м), 6,97 (1H, д, J=8,4 Гц), 5,21 (2H, д, J=7,2 Гц), 3,69 (3H, с), 2,90 (2H, т, J=7,2 Гц), 2,72 (2H, д, J=7,2 Гц).
Ссылочный пример 58
Используя 29,4 г 3-этокси-4-метоксибензамида и 57 г 1,3-дихлор-2-пропанона и следуя процедуре, описанной в ссылочном примере 55, получали 19,9 г белого порошкообразного 4-хлорметил-2-(3-этокси-4-метоксифенил)оксазола.
1Н-ЯМР (CDCl3) δ: 7,65 (1H, с), 7,61 (1H, дд, J=8,1, 2,1 Гц), 7,55 (1H, д, J=2,1 Гц), 6,92 (1H, д, J=8,1 Гц), 4,56 (2H, с), 4,18 (2H, кв, J=6,9 Гц), 3,93 (3H, с), 1,50 (3H, т, J=6,9 Гц).
Ссылочный пример 59
25 г этил 3,4-дигидроксибензоата растворяли в 250 мл диметилформамида и добавляли 5,5 г гидрида натрия при охлаждении льдом и перемешивании. Смесь перемешивали и добавляли по каплям раствор 16,3 мл бензилбромида в 10 мл диметилформамида. После добавления по каплям смесь перемешивали при комнатной температуре в течение ночи. К реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой два раза промывали водой и концентрировали путем удаления растворителя при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 2:1) с получением 15 г неочищенных кристаллов. Неочищенные кристаллы перекристаллизовывали из смеси 30 мл н-гексана и 15 мл этилацетата с получением 8,6 г бесцветного пластинчато-кристаллического этил 4-бензилокси-3-гидроксибензоната.
1Н-ЯМР (CDCl3) δ: 7,67-7,47 (2H, м), 7,41-7,30 (5H, м), 6,94 (1H, д, J=8,7 Гц), 5,67 (1H, с), 5,16 (2H, с), 4,34 (2H, кв, J=7,2 Гц), 1,37 (3H, т, J=7,2 Гц).
Ссылочный пример 60
Используя этил 4-бензилокси-3-гидроксибензонат, полученный в ссылочном примере 59, и следуя процедуре, описанной в ссылочном примере 2, получали этил 4-бензилокси-3-этоксибензоат.
1Н-ЯМР (CDCl3) δ: 7,61-7,55 (2H, м), 7,45-7,27 (5H, м), 6,90 (1H, д, J=8,1 Гц), 5,21 (2H, с), 4,34 (2H, кв, J=6,9 Гц), 4,17 (2H, кв, J=6,9 Гц), 1,48 (3H, т, J=6,9 Гц), 1,37 (3H, т, J=6,9 Гц).
Ссылочный пример 61
Используя этил 4-бензилокси-3-этоксибензоат, полученный в ссылочном примере 60, и следуя процедуре, описанной в ссылочном примере 3, получали 4-бензилокси-3-этоксибензойную кислоту.
1Н-ЯМР (CDCl3) δ: 7,68 (1H, дд, J=8,4, 1,2 Гц), 7,61 (1H, д, J=1,2 Гц), 7,45-7,28 (5H, м), 6,92 (1H, д, J=8,4 Гц), 5,23 (2H, с), 4,17 (2H, кв, J=6,9 Гц), 1,48 (3H, т, J=6,9 Гц).
Ссылочный пример 62
Используя 4-бензилокси-3-этоксибензойную кислоту, полученную в ссылочном примере 61, и следуя процедуре, описанной в ссылочном примере 4, получали 4-бензилокси-3-этоксибензамид в виде бесцветных игольчатых кристаллов.
1Н-ЯМР (CDCl3) δ: 7,47-7,21 (7H, м), 6,88 (1H, д, J=8,1 Гц), 5,21 (2H, с), 4,18 (2H, кв, J=7,2 Гц), 1,48 (3H, т, J=7,2 Гц).
Ссылочный пример 63
Используя 4-бензилокси-3-этоксибензамид, полученный в ссылочном примере 62, и следуя процедуре, описанной в ссылочном примере 5, получали бесцветный порошкообразный 4-хлорметил-2-(4-бензилокси-3-этоксифенил)оксазол.
1Н-ЯМР (CDCl3) δ: 7,64 (1H, с), 7,57-7,30 (7H, м), 6,94 (1H, д, J=8,4 Гц), 5,20 (2H, с), 4,56 (2H, с), 4,20 (2H, кв, J=7,2 Гц), 1,49 (3H, т, J=7,2 Гц).
Ссылочный пример 64
6,81 г иодида натрия и 5,09 г бикарбоната натрия добавляли к суспензии 10 г 2-(3-бензилокси-4-метоксифенил)-4-хлорметилоксазола, полученного в ссылочном примере 5, в 60 мл диметилсульфоксида. Смесь нагревали при 120°C при перемешивании в течение 30 минут. Затем реакционной смеси давали охладиться, добавляли насыщенный солевой раствор и осуществляли экстракцию этилацетатом. Органический слой промывали насыщенным солевым раствором и сушили над безводным сульфатом магния и растворитель затем отгоняли при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1) с получением 2,98 г желтого маслянистого 2-(3-бензилокси-4-метоксифенил)оксазол-4-карбальдегида.
1Н-ЯМР (CDCl3) δ: 9,98 (1H, с), 8,26 (1H, с), 7,71 (1H, дд, J=8,1, 2,1 Гц), 7,69 (1H, ушир.с), 7,48 (2H, ушир.д, J=8,4 Гц), 7,42-7,31 (3H, м), 6,98 (1H, д, J=8,1 Гц), 5,21 (2H, с), 3,95 (3H, с).
Ссылочный пример 65
Используя 4-хлорметил-2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол, полученный в ссылочном примере 23, и следуя процедуре, описанной в ссылочном примере 64, получали бесцветный порошкообразный 2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-карбальдегид.
1Н-ЯМР (CDCl3) δ: 9,99 (1H, с), 8,28 (1H, с), 7,82 (1H, дд, J=8,4, 2,1 Гц), 7,71 (1H, д, J=2,1 Гц), 7,01 (1H, д, J=8,4 Гц), 4,46 (2H, кв, J=8,4 Гц), 3,95 (3H, с).
Ссылочный пример 66
Используя 4-хлорметил-2-(3,4-диэтоксифенил)оксазол, полученный в ссылочном примере 35, и следуя процедуре, описанной в ссылочном примере 64, получали бледно-желтый порошкообразный 2-(3,4-диэтоксифенил)оксазол-4-карбальдегид.
1Н-ЯМР (CDCl3) δ: 9,99 (1H, с), 8,26 (1H, с), 7,65 (1H, дд, J=8,4, 2,1 Гц), 7,62 (1H, д, J=2,1 Гц), 6,94 (1H, д, J=8,4 Гц), 4,19 (2H, кв, J=7,2 Гц), 4,17 (2H, кв, J=7,2 Гц), 1,50 (6H, т, J=7,2 Гц).
Ссылочный пример 67
Используя 12,7 г 3-изопропокси-4-метоксибензойной кислоты и следуя процедуре, описанной в ссылочном примере 4, получали белый порошкообразный 3-изопропокси-4-метоксибензамид.
1Н-ЯМР (CDCl3) δ: 7,46 (1H, д, J=2,1 Гц), 7,34 (1H, дд, J=8,4, 2,1 Гц), 6,87 (1H, д, J=8,4 Гц), 5,93 (1H, ушир.с), 4,62 (1H, м), 3,90 (3H, с), 1,38 (6H, д, J=6,0 Гц).
Ссылочный пример 68
Используя 11,4 г 3-изопропокси-4-метоксибензамида, полученного в ссылочном примере 67, и 25 г 1,3-дихлор-2-пропанона и следуя процедуре, описанной в ссылочном примере 5, получали 12,2 г белого порошкообразного 4-хлорметил-2-(3-изопропокси-4-метоксифенил)оксазола.
1Н-ЯМР (CDCl3) δ: 7,65 (1H, с), 7,61 (1H, дд, J=8,4, 2,1 Гц), 7,57 (1H, д, J=2,1 Гц), 6,93 (1H, д, J=8,4 Гц), 4,64 (1H, м), 4,53 (2H, с), 3,90 (3H, с), 1,40 (6H, д, J=6,0 Гц).
Ссылочный пример 69
Используя 4-хлорметил-2-(3-изопропокси-4-метоксифенил)оксазол, полученный в ссылочном примере 68, и следуя процедуре, описанной в ссылочном примере 64, получали бледно-желтый порошкообразный 2-(3-изопропокси-4-метоксифенил)оксазол-4-карбальдегид.
1Н-ЯМР (CDCl3) δ: 9,99 (1H, с), 8,27 (1H, с), 7,68 (1H, дд, J=8,1, 2,1 Гц), 7,64 (1H, д, J=2,1 Гц), 6,95 (1H, д, J=8,1 Гц), 4,67 (1H, септ., J=6,3 Гц), 3,92 (3H, с), 1,41 (6H, д, J=6,3 Гц).
Ссылочный пример 70
10 г 1-(2-гидроксифенил)этанона растворяли в 100 мл диметилформамида и добавляли 11,2 мл хлорметилметилового эфира и 25,4 г карбоната калия. Смесь перемешивали при 50°C в течение 6 часов и затем при комнатной температуре в течение 4 дней. Затем нерастворимые вещества удаляли при помощи фильтрации из реакционной смеси, добавляли к фильтрату ледяную воду и осуществляли экстракцию этилацетатом. Органический слой промывали водой и сушили над безводным сульфатом магния. Органический слой концентрировали при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 5:1) с получением 6,26 г бесцветного маслянистого 1-(2-метоксиметоксифенил)этанона.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, дд, J=7,8, 1,8 Гц), 7,43 (1H, тд, J=7,8, 1,8 Гц), 7,18 (1H, д, J=7,8 Гц), 7,05 (1H, т, J=7,8 Гц), 5,28 (2H, с), 3,52 (3H, с), 2,64 (3H, с).
Ссылочный пример 71
3 г метил 3-[2-(3,4-диэтоксифенил)оксазол-4-ил]пропионата, полученного в ссылочном примере 54, суспендировали в 5 мл метанола и добавляли 5 мл 20%-ного водного раствора гидроксида натрия. Смесь нагревали и кипятили с обратным холодильником в течение 4 часов. После охлаждения реакционной смеси до комнатной температуры осуществляли экстракцию дихлорметаном. Дихлорметановый слой промывали водой и сушили над безводным сульфатом магния. Осуществляли отгонку растворителя и полученные кристаллы сушили с получением 2,8 г белой порошкообразной 3-[2-(3,4-диметоксифенил)оксазол-4-ил]пропионовой кислоты.
1Н-ЯМР (CDCl3) δ: 7,65-7,55 (3H, м), 7,51 (1H, д, J=2,1 Гц), 6,91 (1H, д, J=8,4 Гц), 4,17 (2H, кв, J=6,9 Гц), 4,15 (2H, кв, J=6,9 Гц), 3,00-2,90 (2H, м), 2,90-2,80 (2H, м), 1,48 (3H, т, J=6,9 Гц), 1,48 (3H, т, J=6,9 Гц).
Ссылочный пример 72
Используя 10 г 4-бензилокси-3-метоксибензамида и следуя процедуре, описанной в ссылочном примере 54, получали 2 г белого порошкообразного метил 3-[2-(4-бензилокси-3-метоксифенил)оксазол-4-ил]пропионата.
1Н-ЯМР (CDCl3) δ: 7,54-7,28 (8H, м) 6,93 (1H, д, J=8,1 Гц), 5,20 (2H, с), 3,97 (3H, с), 3,68 (3H, с), 2,91 (2H, т, J=7,5 Гц), 2,64 (2H, т, J=7,5 Гц).
Ссылочный пример 73
Используя 2 г метил 3-[2-(4-бензилокси-3-метоксифенил)оксазол-4-ил]пропионата, полученного в ссылочном примере 72, и следуя процедуре, описанной в ссылочном примере 71, получали 1,03 г белой порошкообразной 3-[2-(4-бензилокси-3-метоксифенил)оксазол-4-ил]пропионовой кислоты.
1Н-ЯМР (CDCl3) δ: 12,20 (1H, с), 7,86 (1H, с), 7,51-7,31 (7H, м) 7,17 (1H, д, J=8,4 Гц), 5,15 (2H, с), 3,85 (3H, с), 2,75 (2H, т, J=7,5 Гц), 2,59 (2H, т, J=7,5 Гц).
Ссылочный пример 74
0,4 г 4-хлорметил-2-(3,4-диэтоксифенил)оксазола, полученного в ссылочном примере 35, растворяли в 15 мл метиламина (40%-ный раствор в метаноле), нагревали и кипятили с обратным холодильником в течение 1 часа. Реакционную смесь концентрировали и полученный остаток сушили при пониженном давлении с получением 0,23 г желтого маслянистого [2-(3,4-диметоксифенил)оксазол-4-илметил]метиламина.
1Н-ЯМР (CDCl3) δ: 8,00 (1H, с), 7,58-7,50 (2H, м), 6,90 (1H, д, J=8,4 Гц), 4,21-4,10 (6H, м), 2,76 (3H, с), 1,51-1,45 (6H, м).
Ссылочный пример 75
Используя этил 2-хлорацетoацетат и 16 г 3,4-диэтоксибензамида и следуя процедуре, описанной в ссылочном примере 5, получали 3,8 г этил [2-(3,4-диметоксифенил)оксазол-4-ил]ацетата.
1Н-ЯМР (CDCl3) δ: 7,64 (1H, с), 7,60-7,50 (2H, м), 6,91 (1H, д, J=8,1 Гц), 4,25-4,10 (6H, м), 3,58 (2H, с), 1,50-1,40 (6H, м), 1,29 (3H, т, J=6,9 Гц).
Ссылочный пример 76
0,35 г литийалюминийгидрида добавляли к 30 мл тетрагидрофурана при охлаждении льдом и перемешивании и медленно добавляли этил [2-(3,4-диметоксифенил)оксазол-4-ил]ацетат, полученный в ссылочном примере 75, при перемешивании. После перемешивания при комнатной температуре в течение 3 часов смесь перемешивали при охлаждении льдом в течение 3 часов и добавляли 0,35 мл воды, 0,35 мл 15%-ного водного раствора гидроксида натрия и 1,05 мл воды, в указанном порядке. Реакционную смесь сушили над безводным сульфатом магния и нерастворимые вещества затем удаляли при помощи фильтрации. Фильтрат концентрировали при пониженном давлении с получением 2,5 г бесцветного кристаллического 2-[2-(3,4-диметоксифенил)оксазол-4-ил]этанола.
1Н-ЯМР (CDCl3) δ: 7,56 (1H, д, J=8,4, 2,1 Гц), 7,52 (1H, д, J=2,1 Гц), 7,46 (1H, с), 6,91 (1H, д, J=8,4 Гц), 4,17 (2H, кв, J=7,2 Гц), 4,15 (2H, кв, J=7,2 Гц), 3,94 (2H, кв, J=5,4 Гц), 2,94 (1H, т, J=5,4 Гц), 2,81 (2H, т, J=5,4 Гц), 1,48 (3H, т, J=7,2 Гц), 1,48 (3H, т, J=7,2 Гц).
Ссылочный пример 77
2,0 г 2-[2-(3,4-диметоксифенил)оксазол-4-ил]этанола, полученного в ссылочном примере 76, и 2,3 г трифенилфосфина добавляли к 20 мл дихлорметана и медленно добавляли 2,9 г тетрабромида углерода при охлаждении льдом и перемешивании. После того как температура смеси достигала комнатной температуры, перемешивание продолжали в течение 1,5 часов. Реакционную смесь концентрировали и остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 8:1) с получением 1,9 г бесцветного кристаллического 4-(2-бромэтил)-2-(3,4-диэтоксифенил)оксазола.
1Н-ЯМР (CDCl3) δ: 7,60-7,50 (3H, м), 6,91 (1H, д, J=8,4 Гц), 4,18 (2H, кв, J=7,2 Гц), 4,14 (2H, кв, J=7,2 Гц), 3,67 (2H, т, J=6,9 Гц), 3,14 (2H, т, J=6,9 Гц), 1,48 (3H, т, J=7,2 Гц), 1,48 (3H, т, J=7,2 Гц).
Ссылочный пример 78
Используя 1,5 г 4-(2-бромэтил)-2-(3,4-диэтоксифенил)оксазола, полученного в ссылочном примере 77, и следуя процедурам ссылочных примеров 6 и 7, получали 0,8 г желтого маслянистого 2-[2-(3,4-диэтоксифенил)оксазол-4-ил]этиламина.
1Н-ЯМР (CDCl3) δ: 7,60-7,50 (3H, м), 6,91 (1H, д, J=8,4 Гц), 4,17 (2H, кв, J=7,2 Гц), 4,15 (2H, кв, J=7,2 Гц), 3,90-3,80 (2H, м), 3,00-2,90 (2H, м), 1,85 (2H, ушир.с), 1,48 (3H, т, J=7,2 Гц), 1,48 (3H, т, J=7,2 Гц).
Ссылочный пример 79
Используя 10,4 г 3,4-диэтоксибензамида и 19,5 г этил 3-бром-2-оксопропионата и следуя процедуре, описанной в ссылочном примере 5, получали 12,9 г белого порошкообразного этил 2-(3,4-диэтоксифенил)оксазол-4-карбоксилата.
1Н-ЯМР (CDCl3) δ: 8,21 (1H, д, J=0,9 Гц), 7,64 (1H, дд, J=8,1, 0,9 Гц), 7,63 (1H, с), 6,92 (1H, д, J=8,1 Гц), 4,42 (2H, кв, J=7,2 Гц), 4,17 (2H, кв, J=6,9 Гц), 4,15 (2H, кв, J=6,9 Гц), 1,48 (3H, т, J=6,9 Гц), 1,41 (3H, т, J=7,2 Гц).
Ссылочный пример 80
Используя 10 г этил 2-(3,4-диэтоксифенил)оксазол-4-карбоксилата, полученного в ссылочном примере 79, и следуя процедуре, описанной в ссылочном примере 71, получали 8,6 г белой порошкообразной 2-(3,4-диэтоксифенил)оксазол-4-карбоновой кислоты.
1Н-ЯМР (CDCl3) δ: 8,24 (1H, с), 7,60-7,50 (3H, м), 6,02 (1H, ушир.с), 4,13 (4H, кв, J=6,9 Гц), 1,46 (3H, т, J=6,9 Гц), 1,39 (3H, т, J=6,9 Гц).
Ссылочный пример 81
Используя 0,4 г этил [2-(3,4-диэтоксифенил)оксазол-4-ил]ацетата, полученного в ссылочном примере 75, и следуя процедуре, описанной в ссылочном примере 71, получали 0,35 г белой порошкообразной [2-(3,4-диэтоксифенил)оксазол-4-ил]уксусной кислоты.
1Н-ЯМР (CDCl3) δ: 7,65-7,55 (3H, м), 7,51 (1H, д, J=2,1 Гц), 6,91 (1H, д, J=8,4 Гц), 4,17 (2H, кв, J=6,9 Гц), 4,15 (2H, кв, J=6,9 Гц), 3,73 (2H, с), 1,49 (6H, т, J=6,9 Гц).
Ссылочный пример 82
Используя 3 г 4-хлорметил-2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазола, полученного в ссылочном примере 23, и следуя процедуре, описанной в ссылочном примере 47, получали 1,91 г бесцветного маслянистого диметил 2-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}малоната.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=8,4, 2,1 Гц), 7,60 (1H, д, J=2,1 Гц), 7,42 (1H, с), 6,96 (1H, д, J=8,4 Гц), 4,44 (2H, кв, J=6,9 Гц), 3,93 (3H, с), 3,89 (1H, т, J=7,5 Гц), 3,18 (2H, д, J=7,5 Гц).
Ссылочный пример 83
Используя 1,9 г диметил 2-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}малоната, полученного в ссылочном примере 82, и следуя процедуре, описанной в ссылочном примере 48, получали 1,44 г бесцветного маслянистого метил 3-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}пропионата.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=8,4, 2,1 Гц), 7,60 (1H, д, J=2,1 Гц), 7,42 (1H, с), 6,96 (1H, д, J=8,4 Гц), 4,45 (2H, кв, J=6,9 Гц), 3,92 (3H, с), 3,75 (3H, с), 2,91 (2H, т, J=7,5 Гц), 2,72 (2H, т, J=7,5 Гц).
Пример 1
3,5 г [2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 7, суспендировали в 70 мл ацетона. К полученной суспензии добавляли 2,3 г 1-гидроксибензотриазола, 3,3 г гидрохлорида 1-этил-3-(3-диметиламинопропил)карбoдиимида и 3,8 г 2-этоксибензойной кислоты и смесь нагревали и кипятили с обратным холодильником в течение одного часа. Реакционную смесь охлаждали и ацетон отгоняли при пониженном давлении. К остатку добавляли воду и затем осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой и концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (дихлорметан:метанол = 20:1) с получением 4,6 г белого порошкообразного N-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-2-этоксибензамида.
1Н-ЯМР (CDCl3) δ: 8,55 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 1,8 Гц), 7,65-7,61 (3H, м), 7,49-7,29 (6H, м), 7,09 (1H, т, J=7,5 Гц), 7,04-6,92 (2H, м), 5,20 (2H, с), 4,61 (2H, д, J=5,4 Гц), 4,16 (2H, кв, J=6,9 Гц), 3,93 (3H, с), 1,26 (3H, т, J=6,9 Гц).
Пример 2
4,65 г N-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-2-этоксибензамида, полученного в примере 1, растворяли в 90 мл этанола и добавляли 0,45 г 10% палладия-на-углероде в виде порошка. Смесь перемешивали в атмосфере водорода при комнатной температуре в течение одного часа. Катализатор удаляли при помощи фильтрации и фильтрат затем концентрировали при пониженном давлении с получением 3,7 г белого кристаллического N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-2-этоксибензамида.
1Н-ЯМР (CDCl3) δ: 8,58 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 1,8 Гц), 7,62-7,55 (3H, м), 7,41 (1H, тд, J=7,5 Гц, 1,8 Гц), 7,06 (1H, т, J=7,2 Гц), 6,95-6,88 (2H, м), 5,74 (1H, с), 4,62 (2H, д, J=5,1 Гц), 4,17 (2H, кв, J=6,9 Гц), 3,95 (3H, с), 1,47 (3H, т, J=6,9 Гц).
Пример 3
0,2 г N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-2-этоксибензамида, полученного в примере 2, и 0,3 мл 1,8-диазабицикло[5.4.0]ундец-7-ена растворяли в 4 мл этанола и к смеси добавляли 0,14 г (бромметил)циклопропана. Смесь нагревали и кипятили с обратным холодильником в течение ночи. Реакционной смеси давали охладиться, затем к смеси добавляли воду и осуществляли экстракцию этилацетатом. Смесь два раза промывали водой и затем органический слой концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1) с получением 0,18 г белого порошкообразного N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-этоксибензамида.
1Н-ЯМР (CDCl3) δ: 8,55 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 2,1 Гц), 7,62-7,59 (2H, м), 7,53 (1H, д, J=2,1 Гц), 7,45-7,39 (1H, м), 7,07 (1H, тд, J=8,1 Гц, 1,2 Гц), 6,95-6,91 (2H, м), 4,62 (2H, д, J=5,4 Гц), 4,18 (2H, кв, J=6,9 Гц), 3,94-3,92 (5H, м), 1,49 (3H, т, J=6,9 Гц), 1,42-1,34 (1H, м), 0,71-0,64 (2H, м), 0,41-0,35 (2H, м).
Пример 4
0,3 г N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-2-этоксибензамида, полученного в примере 2, и 0,22 г карбоната калия растворяли в 10 мл диметилформамида и к смеси добавляли 0,34 г 1,1,1-трифтор-2-йодэтана. Смесь перемешивали при нагревании при 50°C в течение ночи. Реакционной смеси давали охладиться, затем к смеси добавляли воду и осуществляли экстракцию этилацетатом. Смесь два раза промывали водой и затем органический слой концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1) с получением 0,14 г белого порошкообразного N-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}-2-этоксибензамида.
1Н-ЯМР (CDCl3) δ: 8,56 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 2,1 Гц), 7,73 (1H, дд, J=8,4, 2,1 Гц), 7,65-7,63 (2H, м), 7,45-7,39 (1H, м), 7,09-7,01 (1H, м), 6,99-6,90 (2H, м), 4,62 (2H, д, J=5,4 Гц), 4,55 (2H, кв, J=8,4 Гц), 4,32 (2H, кв, J=6,9 Гц), 3,93 (3H, с), 1,49 (3H, т, J=6,9 Гц).
Используя 0,2 г N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-2-этоксибензамида, полученного в примере 2, соединения примеров 5 - 14 получали таким же способом, как в примере 3.
Пример 5
N-[2-(3-бутокси-4-метоксифенил)оксазол-4-илметил]-2-этоксибензамид
Выход 0,2 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,56 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 2,1 Гц), 7,62-7,54 (3H, м), 7,45-7,39 (1H, м), 7,07 (1H, т, J=8,1 Гц), 6,96-6,90 (2H, м), 4,62 (2H, д, J=5,4 Гц), 4,18 (2H, кв, J=6,9 Гц), 4,10 (2H, т, J=6,9 Гц), 3,92 (3H, с), 1,92-1,82 (2H, м), 1,59-1,47 (5H, м), 1,00 (3H, т, J=7,5 Гц).
Пример 6
N-[2-(3-циклопентилокси-4-метоксифенил)оксазол-4-илметил]-2-этоксибензамид
Выход 0,22 г
Бесцветное маслянистое вещество
1Н-ЯМР (CDCl3) δ: 8,57 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 2,1 Гц), 7,62-7,54 (3H, м), 7,45-7,39 (1H, м), 7,07 (1H, т, J=8,1 Гц), 6,96-6,90 (2H, м), 4,91-4,86 (1H, м), 4,62 (2H, д, J=5,4 Гц), 4,17 (2H, кв, J=6,9 Гц), 3,90 (3H, с), 2,02-1,60 (8H, м), 1,49 (3H, т, J=6,9 Гц).
Пример 7
N-{2-[3-(3-гидроксипропокси)-4-метоксифенил]оксазол-4-илметил}-2-этоксибензамид
Выход 0,12 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,56 (1H, ушир.с), 8,24 (1H, д, J=7,8 Гц), 7,62-7,54 (3H, м), 7,45-7,39 (1H, м), 7,09-7,06 (1H, м), 6,96-6,90 (2H, м), 4,62 (2H, д, J=5,4 Гц), 4,29-4,16 (4H, м), 3,92-3,79 (5H, м), 2,57 (1H, ушир.с), 2,12 (2H, т, J=5,4 Гц), 1,49 (3H, т, J=6,9 Гц).
Пример 8
N-[2-(4-метокси-3-(2-пропинилокси)фенил)оксазол-4-илметил]-2-этоксибензамид
Выход 0,19 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,58 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,8 Гц), 7,70-7,63 (3H, м), 7,45-7,39 (1H, м), 7,07 (1H, тд, J=8,4, 0,9 Гц), 6,98-6,93 (2H, м), 4,84 (2H, д, J=2,4 Гц), 4,63 (2H, дд, J=5,4, 0,9 Гц), 4,19 (2H, кв, J=7,2 Гц), 3,94 (3H, с), 2,54 (1H, т, J=2,4 Гц), 1,50 (3H, т, J=7,2 Гц).
Пример 9
N-[2-(3-этокси-4-метоксифенил)оксазол-4-илметил]-2-этоксибензамид
Выход 0,22 г
Белое порошкообразное вещество
1Н-ЯМР (CDCl3) δ: 8,55 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,8 Гц), 7,62-7,54 (3H, м), 7,44-7,39 (1H, м), 7,07 (1H, т, J=8,1 Гц), 6,96-6,91 (2H, м), 4,62 (2H, д, J=5,4 Гц), 4,23-4,14 (4H, м), 3,93 (3H, с), 1,53-1,46 (6H, м).
Пример 10
N-[2-(4-метокси-3-(2-оксиранилметокси)фенил)оксазол-4-илметил]-2-этоксибензамид
Выход 27 мг
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,54 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,8 Гц), 7,67-7,58 (3H, м), 7,45-7,38 (1H, м), 7,07 (1H, т, J=7,8 Гц), 6,95 (2H, д, J=8,4 Гц), 4,62 (2H, д, J=5,1 Гц), 4,36-4,07 (4H, м), 3,93 (3H, с), 3,46-3,41 (1H, м), 2,92 (1H, т, J=4,5 Гц), 2,80-2,76 (1H, м), 1,48 (3H, т, J=7,2 Гц).
Пример 11
N-[2-(4-метокси-3-пропоксифенил)оксазол-4-илметил]-2-этоксибензамид
Выход 0,19 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,56 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,8 Гц), 7,63-7,54 (3H, м), 7,45-7,39 (1H, м), 7,07 (1H, тд, J=8,4, 1,2 Гц), 6,96-6,91 (2H, м), 4,63 (2H, дд, J=5,1, 0,9 Гц), 4,18 (2H, кв, J=6,9 Гц), 4,06 (2H, т, J=6,9 Гц), 3,92 (3H, с), 1,97-1,85 (2H, м), 1,49 (3H, т, J=6,9 Гц), 1,07 (3H, т, J=7,2 Гц).
Пример 12
N-[2-(3-изопропокси-4-метоксифенил)оксазол-4-илметил]-2-этоксибензамид
Выход 0,17 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,57 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,8 Гц), 7,62-7,55 (3H, м), 7,45-7,38 (1H, м), 7,07 (1H, т, J=7,8 Гц), 6,96-6,91 (2H, м), 4,72-4,59 (3H, м), 4,18 (2H, кв, J=6,9 Гц), 3,91 (3H, с), 1,49 (3H, т, J=6,9 Гц), 1,41 (6H, д, J=6,3 Гц).
Пример 13
N-[2-(3-(3-бутенилокси)-4-метоксифенил)оксазол-4-илметил]-2-этоксибензамид
Выход 0,21 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,56 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 1,8 Гц), 7,63-7,55 (3H, м), 7,45-7,38 (1H, м), 7,07 (1H, т, J=7,8 Гц), 6,96-6,91 (2H, м), 5,97-5,88 (1H, м), 5,23-5,10 (2H, м), 4,62 (2H, дд, J=5,1, 0,9 Гц), 4,21-4,12 (4H, м), 3,92 (3H, с), 2,68-2,60 (2H, м), 1,49 (3H, т, J=6,9 Гц).
Пример 14
N-[2-(3-изобутокси-4-метоксифенил)оксазол-4-илметил]-2-этоксибензамид
Выход 84 мг
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,54 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 1,8 Гц), 7,62-7,53 (2H, м), 7,44 (1H, д, J=1,8 Гц), 7,41 (2H, тд, J=7,8, 1,8 Гц), 7,06 (1H, т, J=7,8 Гц), 6,95-6,90 (2H, м), 4,62 (2H, д, J=5,4 Гц), 4,18 (2H, кв, J=6,9 Гц), 3,91 (3H, с), 3,85 (2H, д, J=6,9 Гц), 2,20 (1H, кв.т, J=6,9, 6,6 Гц), 1,49 (3H, т, J=6,9 Гц), 1,06 (6H, д, J=6,6 Гц).
Пример 15
Используя 0,2 г N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-2-этоксибензамида, полученного в примере 2, N-{2-[4-метокси-3-(3,3,3-трифторпропокси)фенил]оксазол-4-илметил}-2-этоксибензамид получали таким же способом, как в примере 4.
Выход 60 мг
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,55 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 1,8 Гц), 7,68-7,63 (2H, м), 7,56 (1H, д, J=2,1 Гц), 7,45-7,39 (1H, м), 7,07 (1H, т, J=7,2 Гц), 6,97-6,93 (2H, м), 4,62 (2H, д, J=5,4 Гц), 4,32 (2H, т, J=6,9 Гц), 4,18 (2H, кв, J=6,9 Гц), 3,92 (3H, с), 2,78-2,67 (2H, м), 1,49 (3H, т, J=6,9 Гц).
Пример 16
1,5 г [2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 7, суспендировали в 30 мл ацетона. К полученной суспензии добавляли 1,0 г 1-гидроксибензотриазола, 1,4 г гидрохлорида 1-этил-3-(3-диметиламинопропил)карбoдиимида и 0,8 г 3-метилпиколиновой кислоты и смесь нагревали и кипятили с обратным холодильником в течение 30 минут. Реакционную смесь охлаждали и ацетон отгоняли при пониженном давлении. К остатку добавляли воду и затем осуществляли экстракцию этилацетатом. Органический слой два раза промывали водой и растворитель концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (дихлорметан:метанол = 20:1) с получением 1,5 г белого порошкообразного N-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-3-метилпиколинамида.
1Н-ЯМР (CDCl3) δ: 8,57 (1H, ушир.с), 8,39 (1H, д, J=7,5 Гц), 7,65-7,28 (10H, м), 6,94 (1H, д, J=9,0 Гц), 5,21 (2H, с), 4,58 (2H, дд, J=5,7, 0,9 Гц), 3,93 (3H, с), 2,76 (3H, с).
Пример 17
1,5 г N-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-3-метилпиколинамида, полученного в примере 16, растворяли в 50 мл этанола и к смеси добавляли 0,1 г 10% палладия-на-углероде в виде порошка. Смесь перемешивали в атмосфере водорода при 50°C в течение двух часов. Катализатор удаляли при помощи фильтрации и фильтрат затем концентрировали с получением 1,3 г белого кристаллического N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-3-метилпиколинамида.
1Н-ЯМР (CDCl3) δ: 8,58 (1H, ушир.с), 8,38 (1H, дд, J=4,5, 0,9 Гц), 7,63 (1H, с), 7,62-7,54 (3H, м), 7,32-7,27 (1H, м), 6,90 (1H, д, J=8,4 Гц), 5,75 (1H, ушир.с), 4,58 (2H, дд, J=6,0, 0,9 Гц), 3,94 (3H, с), 2,75 (3H, с).
Пример 18
0,15 г N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-3-метилпиколинамида, полученного в примере 17, и 0,5 мл 1,8-диазабицикло[5.4.0]ундец-7-ена растворяли в 4 мл этанола и к смеси добавляли 0,13 г бромциклопентана. Смесь нагревали и кипятили с обратным холодильником в течение 3 часов. Реакционной смеси давали охладиться, затем к смеси добавляли воду и осуществляли экстракцию этилацетатом. Экстракт два раза промывали водой и органический слой концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1) с получением 0,11 г белого порошкообразного N-[2-(3-циклопентилокси-4-метоксифенил)оксазол-4-илметил]-3-метилпиколинамида.
1Н-ЯМР (CDCl3) δ: 8,57 (1H, ушир.с), 8,39 (1H, дд, J=4,8, 0,9 Гц), 7,62-7,53 (4H, м), 7,32-7,27 (1H, м), 6,91 (1H, д, J=8,4 Гц), 4,88 (1H, тт, J=3,3 Гц), 4,59 (2H, дд, J=5,7, 0,9 Гц), 3,89 (3H, с), 2,76 (3H, с), 2,07-1,79 (6H, м), 1,70-1,60 (2H, м).
Пример 19
0,15 г N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-3-метилпиколинамида, полученного в примере 17, и 0,18 г карбоната калия растворяли в 4 мл диметилформамида и к смеси добавляли 0,19 г 1,1,1-трифтор-2-йодэтана. Смесь перемешивали при нагревании при 80°C в течение ночи. Реакционной смеси давали охладиться, затем к смеси добавляли воду и осуществляли экстракцию этилацетатом. Экстракт два раза промывали водой и органический слой концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1) с получением 0,11 г белого порошкообразного N-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}-3-метилпиколинамида.
1Н-ЯМР (CDCl3) δ: 8,58 (1H, ушир.с), 8,39 (1H, дд, J=4,5, 1,2 Гц), 7,73 (1H, дд, J=8,7, 2,1 Гц), 7,63-7,57 (3H, м), 7,32-7,27 (1H, м), 6,97 (1H, д, J=8,4 Гц), 4,59 (2H, дд, J=5,7, 0,9 Гц), 4,46 (2H, кв, J=8,4 Гц), 3,93 (3H, с), 2,76 (3H, с).
Пример 20
Используя 0,2 г N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-3-метилпиколинамида, полученного в примере 17, 0,11 г N-[2-(3-этокси-4-метоксифенил)оксазол-4-илметил]-3-метилпиколинамида получали таким же способом, как в примере 3.
Бесцветные кристаллы
1Н-ЯМР (CDCl3) δ: 8,57 (1H, ушир.с), 8,39 (1H, дд, J=4,8, 1,5 Гц), 7,65-7,50 (4H, м), 7,30 (1H, дд, J=7,8, 4,8 Гц), 6,92 (1H, д, J=8,1 Гц), 4,59 (1H, дд, J=6,0, 0,6 Гц), 4,19 (2H, кв, J=6,9 Гц), 4,17 (2H, кв, J=6,9 Гц), 3,92 (3H, с), 2,76 (3H, с), 1,50 (3H, т, J=6,9 Гц).
Пример 21
Используя 0,15 г N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-3-метилпиколинамида, полученного в примере 17, 45 мг N-[2-(3-аллилокси-4-метоксифенил)оксазол-4-илметил]-3-метилпиколинамида получали таким же способом, как в примере 3.
Бесцветные кристаллы
1Н-ЯМР (CDCl3) δ: 8,58 (1H, ушир.с), 8,39 (1H, дд, J=4,5, 1,5 Гц), 7,65-7,50 (4H, м), 7,30 (1H, дд, J=7,8, 4,5 Гц), 6,93 (1H, д, J=8,4 Гц), 6,12 (1H, м), 5,45 (1H, м), 5,32 (1H, дд, J=9,6, 1,5 Гц), 4,70 (2H, д, J=5,4 Гц), 4,59 (1H, д, J=6,0 Гц), 3,92 (3H, с), 2,76 (3H, с).
Пример 22
170 мг N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-3-метилпиколинамида, полученного в примере 17, растворяли в 10 мл тетрагидрофурана. К полученному раствору добавляли 134 мг 2-гидроксииндана, 0,5 мл диизопропилазодикарбоксилата (40%-ный раствор в толуоле) и 202 мг три(н-бутил)фосфина и смесь перемешивали при комнатной температуре в течение ночи и при 50°C в течение 2,5 часов. К реакционной смеси добавляли 100 мг 2-гидроксииндана, 0,5 мл диизопропилазодикарбоксилата (40%-ный раствор в толуоле) и 200 мг три(н-бутил)фосфина и смесь перемешивали при 50°C в течение 5 часов и при комнатной температуре в течение ночи. Реакционную смесь концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат:метиленхлорид = 1:1:1) с получением 92 мг N-{2-[3-(индaн-2-илокси)-4-метоксифенил]оксазол-4-илметил}-3-метилпиколинамида.
Бледно-желтое маслянистое вещество
1Н-ЯМР (CDCl3) δ: 8,59 (1H, ушир.с), 8,39 (1H, д, J=3,3 Гц), 7,65-7,16 (9H, м), 6,93 (1H, д, J=8,1 Гц), 5,30 (1H, тт, J=6,6, 3,9 Гц), 4,60 (2H, д, J=5,7 Гц), 3,86 (3H, с), 3,46 (2H, дд, J=16,8, 6,6 Гц), 3,27 (2H, дд, J=16,8, 3,9 Гц), 2,76 (3H, с).
Пример 23
Используя 0,88 г [2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 7, 1,03 г белого порошкообразного N-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-2-трифторметилбензамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 7,72-7,46 (9H, м), 7,40-7,27 (3H, м), 6,95 (1H, д, J=8,4 Гц), 6,34 (1H, ушир.с), 5,20 (2H, с), 4,59 (2H, д, J=5,4 Гц), 3,93 (3H, с).
Пример 24
Используя 1,0 г N-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-2-трифторметилбензамида, полученного в примере 23, 0,66 г белого порошкообразного N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-2-трифторметилбензамида получали таким же способом, как в примере 2.
1Н-ЯМР (CDCl3) δ: 7,71-7,50 (7H, м), 6,90 (1H, д, J=8,4 Гц), 6,39 (1H, ушир.с), 5,76 (1H, с), 4,59 (2H, д, J=5,4 Гц), 3,94 (3H, с).
Пример 25
Используя 0,2 г N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-2-трифторметилбензамида, полученного в примере 24, 0,18 г белого порошкообразного N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-трифторметилбензамида получали таким же способом, как в примере 3.
1Н-ЯМР (CDCl3) δ: 7,72-7,50 (7H, м), 6,93 (1H, д, J=8,4 Гц), 6,34 (1H, с), 4,60 (2H, д, J=5,4 Гц), 3,93 (3H, с), 1,42-1,32 (1H, м), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 26
Используя 0,2 г N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-2-трифторметилбензамида, полученного в примере 24, 40 мг белого порошкообразного N-{2-[3-(3-гидроксипропокси)-4-метоксифенил]оксазол-4-илметил}-2-трифторметилбензамида получали таким же способом, как в примере 3.
1Н-ЯМР (CDCl3) δ: 7,71-7,50 (7H, м), 6,92 (1H, д, J=8,4 Гц), 6,34 (1H, ушир.с), 4,60 (2H, д, J=5,4 Гц), 4,28 (2H, кв, J=5,7 Гц), 3,98-3,86 (5H, м), 2,47 (1H, т, J=5,7 Гц), 2,15-2,07 (3H, м).
Пример 27
Используя 0,5 г 2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 7, 0,62 г белого порошкообразного N-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-3-этоксипиколинамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 8,24-8,22 (2H, м), 7,64-7,60 (3H, м), 7,50-7,46 (2H, м), 7,41-7,28 (5H, м), 6,94 (1H, д, J=9,0 Гц), 5,20 (2H, с), 4,61 (2H, д, J=5,7 Гц), 4,17 (2H, кв, J=6,9 Гц), 3,93 (3H, с), 1,50 (3H, т, J=6,9 Гц).
Пример 28
Используя 0,6 г N-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-3-этоксипиколинамида, полученного в примере 27, 0,5 г белого аморфного N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-3-этоксипиколинамида получали таким же способом, как в примере 2.
1Н-ЯМР (CDCl3) δ: 8,25-8,22 (2H, м), 7,64 (1H, д, J=1,8 Гц), 7,60-7,54 (2H, м), 7,39-7,28 (2H, м), 6,91 (1H, д, J=8,1 Гц), 5,71 (1H, ушир.с), 4,61 (2H, дд, J=5,4, 0,9 Гц), 4,17 (2H, кв, J=6,9 Гц), 3,94 (3H, с), 1,52 (3H, т, J=6,9 Гц).
Пример 29
Используя 0,5 г N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-3-этоксипиколинамида, полученного в примере 28, 0,18 г белого аморфного N-[2-(3-циклопентилокси-4-метоксифенил)оксазол-4-илметил]-3-этоксипиколинамида получали таким же способом, как в примере 3.
1Н-ЯМР (CDCl3) δ: 8,25-8,22 (2H, м), 7,64 (1H, с), 7,58 (1H, дд, J=8,4, 2,1 Гц), 7,53 (1H, д, J=1,8 Гц), 7,39-7,32 (2H, м), 6,91 (1H, д, J=8,4 Гц), 4,91-4,86 (1H, м), 4,62 (2H, дд, J=5,4, 0,9 Гц), 4,17 (2H, кв, J=6,9 Гц), 3,89 (3H, с), 2,05-1,79 (6H, м), 1,66-1,60 (2H, м), 1,51 (3H, т, J=6,9 Гц).
Пример 30
Используя 0,31 г 2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 7, 0,16 г белого порошкообразного N-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-2-(2,2,2-трифторэтокси)бензамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 8,22 (1H, дд, J=7,8, 1,8 Гц), 7,82 (1H, ушир.с), 7,63-7,60 (3H, м), 7,49-7,27 (6H, м), 7,19 (1H, т, J=7,2 Гц), 6,96-6,88 (2H, м), 5,19 (2H, с), 4,62 (2H, д, J=5,4 Гц), 4,47 (2H, кв, J=7,8 Гц), 3,92 (3H, с).
Пример 31
Используя 0,16 г N-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-2-(2,2,2-трифторэтокси)бензамида, полученного в примере 30, 0,11 г белого порошкообразного N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-2-(2,2,2-трифторэтокси)бензамида получали таким же способом, как в примере 2.
1Н-ЯМР (CDCl3) δ: 8,21 (1H, дд, J=7,8, 1,8 Гц), 7,84 (1H, ушир.с), 7,62-7,54 (3H, м), 7,49-7,43 (1H, м), 7,19 (1H, тд, J=7,8, 0,9 Гц), 5,71 (1H, с), 4,62 (2H, дд, J=5,4, 0,9 Гц), 4,48 (2H, кв, J=7,8 Гц), 3,94 (3H, с).
Пример 32
Используя 0,11 г N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-2-(2,2,2-трифторэтокси)бензамида, полученного в примере 31, 78 мг белого аморфного N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-(2,2,2-трифторэтокси)бензамида получали таким же способом, как в примере 3.
1Н-ЯМР (CDCl3) δ: 8,22 (1H, дд, J=7,8, 2,1 Гц), 7,83 (1H, ушир.с), 7,61-7,57 (3H, м), 7,53 (1H, д, J=2,1 Гц), 7,50-7,43 (1H, м), 7,19 (1H, тд, J=7,8, 0,9 Гц), 6,94-6,88 (2H, м), 4,63 (2H, дд, J=5,4, 0,9 Гц), 4,48 (2H, кв, J=7,8 Гц), 1,42-1,32 (1H, м), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 33
Используя 0,5 г 2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]метиламина, полученного в с ссылочном примере 7, 0,68 г бледно-желтого порошкообразного N-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-2-метоксибензамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 8,39 (1H, ушир.с), 8,23 (1H, дд, J=4,8, 1,8 Гц), 7,65-7,60 (3H, м), 7,50-7,28 (6H, м), 7,08 (1H, т, J=7,2 Гц), 6,98-6,93 (2H, м), 5,21 (2H, с), 4,61 (2H, дд, J=5,4, 0,9 Гц), 3,95 (3H, с), 3,93 (3H, с).
Пример 34
Используя 0,67 г N-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-2-метоксибензамида, полученного в примере 33, 0,52 г белого аморфного N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-2-метоксибензамида получали таким же способом, как в примере 2.
1Н-ЯМР (CDCl3) δ: 8,43 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 2,1 Гц), 7,63 (1H, с), 7,60-7,54 (2H, м), 7,47-7,41 (1H, м), 7,10-7,05 (1H, м), 6,97 (1H, д, J=8,4 Гц), 6,91 (1H, д, J=8,1 Гц), 5,74 (1H, ушир.с), 4,62 (2H, дд, J=5,4, 0,9 Гц), 3,97 (3H, с), 3,95 (3H, с).
Пример 35
Используя 0,5 г N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]-2-метоксибензамида, полученного в примере 34, 0,39 г белого порошкообразного N-[2-(3-циклопентилокси-4-метоксифенил)оксазол-4-илметил]-2-метоксибензамида получали таким же способом, как в примере 3.
1Н-ЯМР (CDCl3) δ: 8,41 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 1,8 Гц), 7,63 (1H, с), 7,59 (1H, дд, J=8,4, 1,8 Гц), 7,54 (1H, д, J=1,8 Гц), 7,48-7,42 (1H, м), 7,08 (1H, т, J=7,8 Гц), 6,98 (1H, д, J=8,1 Гц), 6,92 (1H, д, J=8,4 Гц), 4,91-4,87 (1H, м), 4,62 (2H, дд, J=5,4, 0,9 Гц), 3,97 (3H, с), 3,90 (3H, с), 2,05-1,80 (6H, м), 1,66-1,59 (2H, м).
Пример 36
0,2 г [2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 13, суспендировали в 4 мл ацетона. К полученной суспензии добавляли 0,2 г 1-гидроксибензотриазола, 0,29 г гидрохлорида 1-этил-3-(3-диметиламинопропил)карбoдиимида и 0,14 г 3-метилпиколиновой кислоты и смесь нагревали и кипятили с обратным холодильником в течение 30 минут. Реакционную смесь охлаждали, затем к смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой два раза промывали водой и растворитель концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 1:1) с получением 0,16 г белого порошкообразного N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-3-метилпиколинамида.
1Н-ЯМР (CDCl3) δ: 8,58 (1H, ушир.с), 8,39 (1H, дд, J=4,5, 1,2 Гц), 7,63-7,57 (3H, м), 7,52 (1H, д, J=2,1 Гц), 7,33-7,28 (1H, м), 6,92 (1H, д, J=8,4 Гц), 4,59 (2H, дд, J=6,0, 0,9 Гц), 3,97-3,90 (5H, м), 2,76 (3H, с), 1,41-1,31 (1H, м), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Используя 0,2 г [2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 13, соединения примеров 37-43 получали таким же способом, как в примере 1.
Пример 37
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-изопропоксибензамид
Выход 0,17 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,62 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 1,8 Гц), 7,62-7,58 (2H, м), 7,54 (1H, д, J=2,1 Гц), 7,43-7,38 (1H, м), 7,05 (1H, тд, J=8,1, 0,9 Гц), 6,97-6,91 (2H, м), 4,76-4,67 (1H, м), 4,61 (2H, дд, J=5,4, 0,9 Гц), 3,94-3,90 (5H, м), 1,41-1,38 (7H, м), 0,69-0,64 (2H, м), 0,41-0,35 (2H, м).
Пример 38
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-метилбензамид
Выход 0,16 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 7,64 (1H, с), 7,59 (1H, дд, J=8,4, 2,1 Гц), 7,50 (1H, д, J=2,1 Гц), 7,41-7,16 (3H, м), 6,93 (1H, д, J=8,4 Гц), 6,31 (1H, ушир.с), 4,58 (2H, дд, J=5,4, 0,9 Гц), 3,95-3,92 (5H, м), 2,46 (3H, с), 1,42-1,32 (1H, м), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 39
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-этилбензамид
Выход 0,15 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 7,64 (1H, с), 7,59 (1H, дд, J=8,4, 2,1 Гц), 7,50 (1H, д, J=1,8 Гц), 7,41-7,16 (3H, м), 6,93 (1H, д, J=8,1 Гц), 6,31 (1H, ушир.с), 4,57 (2H, д, J=5,4 Гц), 3,95-3,92 (5H, м), 2,81 (2H, кв, J=7,5 Гц), 1,42-1,32 (1H, м), 1,23 (3H, т, J=7,5 Гц), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 40
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-хлорбензамид
Выход 0,17 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 7,71-7,66 (2H, м), 7,59 (1H, дд, J=8,4, 1,8 Гц), 7,50 (1H, д, J=2,1 Гц), 7,42-7,29 (3H, м), 6,93 (1H, д, J=8,4 Гц), 6,75 (1H, ушир.с), 4,62 (2H, дд, J=5,4, 0,9 Гц), 3,95-3,92 (5H, м), 1,41-1,32 (1H, м), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 41
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-5-фтор-2-метоксибензамид
Выход 0,19 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,45 (1H, ушир.с), 7,94 (1H, дд, J=9,6, 3,3 Гц), 7,63 (1H, с), 7,61 (1H, дд, J=8,1, 1,8 Гц), 7,51 (1H, д, J=1,8 Гц), 7,17-7,10 (1H, м), 6,95-6,90 (2H, м), 4,61 (2H, д, J=5,4 Гц), 3,96-3,92 (8H, м), 1,40-1,30 (1H, м), 0,70-0,64 (2H, м), 0,41-0,35 (2H, м).
Пример 42
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-4-фтор-2-метоксибензамид
Выход 0,19 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,27-8,21 (2H, м), 7,63-7,58 (2H, м), 7,52 (1H, д, J=2,1 Гц), 6,93 (1H, д, J=8,4 Гц), 6,81-6,74 (1H, м), 6,69 (1H, дд, J=10,2, 2,1 Гц), 4,60 (2H, дд, J=5,4, 0,9 Гц), 3,97-3,90 (8H, м), 1,40-1,30 (1H, м), 0,70-0,64 (2H, м), 0,41-0,35 (2H, м).
Пример 43
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-фтор-6-метоксибензамид
Выход 0,17 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 7,65 (1H, с), 7,59 (1H, дд, J=8,4, 2,1 Гц), 7,50 (1H, д, J=2,1 Гц), 7,34-7,27 (1H, м), 6,92 (1H, д, J=8,4 Гц), 6,76-6,70 (2H, м), 6,51 (1H, ушир.с), 4,61 (2H, д, J=5,7 Гц), 3,94-3,91 (5H, м), 3,85 (3H, с), 1,42-1,31 (1H, м), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 44
Используя 0,4 г [2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 13, N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-метилсульфанилбензамид получали таким же способом, как в примере 1.
Выход 0,4 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 7,68 (1H, с), 7,61-7,56 (2H, м), 7,50 (1H, д, J=1,8 Гц), 7,34-7,17 (3H, м), 6,95-6,90 (2H, м), 4,61 (2H, дд, J=5,4, 0,9 Гц), 3,95-3,92 (5H, м), 2,46 (3H, с), 1,42-1,31 (1H, м), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 45
Используя 0,7 г [2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 13, N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-3-гидроксипиколинамид получали таким же способом, как в примере 1.
Выход 0,6 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 12,02 (1H, с), 8,45 (1H, ушир.с), 8,06 (1H, дд, J=4,2, 1,8 Гц), 7,63-7,59 (2H, м), 7,52 (1H, с), 7,37-7,29 (3H, м), 6,93 (1H, д, J=8,4 Гц), 4,60 (2H, д, J=6,0 Гц), 3,96-3,93 (5H, м), 1,56-1,33 (1H, м), 0,70-0,64 (2H, м), 0,42-0,36 (2H, м).
Используя 0,1 г [2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 13, соединения примеров 46-56 получали таким же способом, как в примере 1.
Пример 46
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-метоксибензамид
Выход 0,1 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,40 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 2,1 Гц), 7,64-7,58 (2H, м), 7,52 (1H, д, J=2,1 Гц), 7,48-7,42 (1H, м), 7,08 (1H, тд, J=7,8, 0,9 Гц), 6,99-6,91 (2H, м), 4,62 (2H, дд, J=5,4, 0,9 Гц), 3,97-3,91 (8H, м), 1,40-1,32 (1H, м), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 47
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-трифторметоксибензамид
Выход 43 мг
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,02 (1H, дд, J=7,8, 1,8 Гц), 7,64-7,27 (6H, м), 7,10 (1H, ушир.с), 6,93 (1H, д, J=8,4 Гц), 4,62 (2H, дд, J=5,4, 0,9 Гц), 3,95-3,92 (5H, м), 1,43-1,28 (1H, м), 0,69-0,63 (2H, м), 0,41-0,36 (2H, м).
Пример 48
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-пропоксибензамид
Выход 0,1 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,50 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,8 Гц) 7,61-7,58 (2H, м), 7,53 (1H, д, J=1,8 Гц), 7,44-7,38 (1H, м), 7,06 (1H, т, J=7,8 Гц), 6,95-6,91 (2H, м), 4,62 (2H, д, J=5,1 Гц), 4,06 (2H, т, J=6,6 Гц), 3,95-3,68 (5H, м), 1,86 (2H, тд, J=7,5, 6,6 Гц), 1,41-1,31 (1H, м), 0,96 (3H, т, J=7,5 Гц), 0,70-0,61 (2H, м), 0,41-0,35 (2H, м).
Пример 49
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]пиразин-2-карбоксамид
Выход 90 мг
Белый порошок
1Н-ЯМР (CDCl3) δ: 9,42 (1H, с), 8,75 (1H, д, J=2,4 Гц), 8,52 (1H, дд, J=2,7, 1,5 Гц), 8,25 (1H, ушир.с), 7,64 (1H, с), 7,60 (1H, дд, J=8,4, 1,8 Гц), 7,52 (1H, д, J=1,8 Гц), 6,92 (1H, д, J=8,4 Гц), 4,63 (2H, дд, J=5,4, 0,9 Гц), 4,11-3,92 (5H, м), 1,40-1,32 (1H, м), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 50
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-3-этоксипиколинамид
Выход 85 мг
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,24-8,22 (2H, м), 7,64 (1H, с), 7,60 (1H, дд, J=8,4, 1,8 Гц), 7,51 (1H, д, J=2,1 Гц), 7,39-7,32 (2H, м), 6,92 (1H, д, J=8,4 Гц), 4,62 (2H, дд, J=5,4, 0,9 Гц), 4,17 (2H, кв, J=6,9 Гц), 3,98-3,92 (5H, м), 1,52 (3H, т, J=6,9 Гц), 1,43-1,32 (1H, м), 0,71-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 51
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-бутоксибензамид
Выход 70 мг
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,48 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 1,8 Гц), 7,63-7,59 (2H, м), 7,53 (1H, д, J=2,1 Гц), 7,45-7,38 (1H, м), 7,06 (1H, тд, J=8,4, 0,9 Гц), 6,96-6,91 (2H, м), 4,61 (2H, д, J=5,1 Гц), 4,09 (2H, т, J=6,6 Гц), 3,94-3,91 (5H, м), 1,84-1,75 (2H, м), 1,46-1,33 (3H, м), 0,84 (3H, т, J=7,2 Гц), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 52
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-изобутоксибензамид
Выход 0,12 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,46 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,8 Гц), 7,62-7,58 (2H, м), 7,52 (1H, д, J=1,8 Гц), 7,41 (1H, т, J=7,2 Гц), 7,06 (1H, т, J=7,2 Гц), 6,95-6,91 (2H, м), 4,62 (2H, д, J=5,1 Гц), 3,95-3,92 (5H, м), 3,86 (2H, д, J=6,3 Гц), 2,20-2,10 (1H, м), 1,40-1,31 (1H, м), 0,95 (6H, д, J=6,6 Гц), 0,70-0,63 (2H, м), 0,41-0,37 (2H, м).
Пример 53
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-3-изопропоксипиколинамид
Выход 0,1 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,28-8,25 (2H, м), 7,63 (1H, с), 7,60 (1H, дд, J=8,4, 2,1 Гц), 7,52 (1H, д, J=2,1 Гц), 7,38-7,31 (2H, м), 6,93 (1H, д, J=8,4 Гц), 4,70-4,61 (3H, м), 3,98-3,90 (5H, м), 1,42-1,31 (7H, м), 0,70-0,61 (2H, м), 0,41-0,35 (2H, м).
Пример 54
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-этилсульфанилбензамид
Выход 85 мг
Белый порошок
1Н-ЯМР (CDCl3) δ: 7,70-7,66 (2H, м), 7,59 (1H, дд, J=8,4, 1,8 Гц), 7,51 (1H, д, J=2,1 Гц), 7,43-7,32 (2H, м), 7,27-7,22 (2H, м), 6,92 (1H, д, J=8,7 Гц), 4,61 (2H, дд, J=5,4, 0,6 Гц), 3,95-3,92 (5H, м), 2,90 (2H, кв, J=7,5 Гц), 1,40-1,34 (1H, м), 1,26 (3H, т, J=7,2 Гц), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 55
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-1-оксидпиколинамид
Выход 53 мг
Бледно-желтый порошок
1Н-ЯМР (CDCl3) δ: 11,64 (1H, ушир.с), 8,44 (1H, дд, J=7,8, 2,1 Гц), 8,25 (1H, д, J=6,3 Гц), 7,63-7,35 (5H, м), 6,91 (1H, д, J=8,7 Гц), 4,65 (2H, д, J=5,7 Гц), 3,97-3,88 (5H, м), 1,43-1,32 (1H, м), 0,70-0,63 (2H, м), 0,41-0,36 (2H, м).
Пример 56
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2,6-диметоксибензамид
Выход 46 мг
Белый порошок
1Н-ЯМР (CDCl3) δ: 7,67 (1H, с), 7,59 (1H, дд, J=8,4, 1,8 Гц), 7,50 (1H, д, J=2,1 Гц), 7,30-7,24 (1H, м), 6,92 (1H, д, J=8,4 Гц), 6,56 (2H, д, J=8,4 Гц), 6,24 (1H, ушир.с), 4,62 (2H, дд, J=5,7, 0,9 Гц), 3,95-3,92 (5H, м), 3,81 (6H, с), 1,41-1,32 (1H, м), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Используя 0,13 г [2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]метиламина, соединения примеров 57-59 получали таким же способом, как в примере 1.
Пример 57
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-3-метоксипиколинамид
Выход 24 мг
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,23-8,19 (2H, м), 7,65 (1H, с), 7,59 (1H, дд, J=8,4, 2,1 Гц), 7,51 (1H, д, J=1,8 Гц), 7,43-7,34 (2H, м), 6,92 (1H, д, J=8,7 Гц), 4,60 (2H, д, J=5,4 Гц), 3,96-3,93 (8H, м), 1,43-1,30 (1H, м), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 58
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-3-изобутоксипиколинамид
Выход 0,11 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,24 (1H, дд, J=3,9, 1,8 Гц), 8,17 (1H, ушир.с), 7,63 (1H, с), 7,59 (1H, дд, J=8,4, 1,8 Гц), 7,38-7,31 (2H, м), 6,92 (1H, д, J=8,4 Гц), 4,62 (2H, дд, J=5,4, 0,9 Гц), 3,95-3,92 (5H, м), 3,84 (2H, д, J=6,3 Гц), 2,20 (1H, кв.т, J=6,6 Гц), 1,40-1,34 (1H, м), 1,03 (6H, д, J=6,6 Гц), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 59
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-метилникотинамид
Выход 71 мг
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,55 (1H, дд, J=7,8, 1,8 Гц), 7,71 (1H, дд, J=7,5, 1,8 Гц), 7,65 (1H, с), 7,59 (1H, дд, J=8,4, 2,1 Гц), 7,17-7,13 (1H, м), 6,93 (2H, д, J=8,4 Гц), 6,35 (1H, ушир.с), 4,58 (2H, дд, J=5,4, 0,9 Гц), 3,96-3,91 (5H, м), 2,69 (3H, с), 1,41-1,31 (1H, м), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 60
0,4 г N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-метилсульфанилбензамида, полученного в примере 44, растворяли в 20 мл дихлорметана и к смеси добавляли 0,67 г метахлорпербензойной кислоты при охлаждении раствора льдом при перемешивании. Смесь затем перемешивали в течение часа. Реакционную смесь концентрировали при пониженном давлении, остаток очищали колоночной хроматографией на силикагеле (NH диоксид кремния, н-гексан:этилацетат = 1:1) и получали 50 мг белого порошкообразного N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-метансульфонилбензамида.
1Н-ЯМР (CDCl3) δ: 8,11 (1H, дд, J=7,8, 0,9 Гц), 7,76 (1H, с), 7,69-7,55 (4H, м), 7,50 (1H, д, J=2,1 Гц), 6,93 (1H, д, J=8,4 Гц), 6,50 (1H, ушир.с), 4,62 (2H, д, J=5,4 Гц), 3,95-3,90 (5H, м), 3,93-3,67 (1H, м), 3,37 (3H, с), 1,40-1,32 (1H, м), 1,27-1,18 (3H, м), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 61
0,1 г N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-3-гидроксипиколинамида, полученного в примере 45, и 0,16 г карбоната цезия растворяли в 4 мл ацетoнитрила и к смеси добавляли 0,2 г 1-бромпропана и перемешивали в течение ночи при комнатной температуре. К реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Экстракт промывали один раз водой и затем промывали один раз насыщенным водным раствором лимонной кислоты. Органический слой концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле с получением 72 мг белого порошкообразного N-2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-3-пропоксипиколинамида.
1Н-ЯМР (CDCl3) δ: 8,25-8,20 (2H, м) 7,64 (1H, с), 7,60 (1H, дд, J=8,4, 1,8 Гц), 7,52 (1H, д, J=1,8 Гц), 7,39-7,32 (2H, м), 6,92 (1H, д, J=8,4 Гц), 4,62 (2H, дд, J=5,7, 0,9 Гц), 4,05 (2H, т, J=6,6 Гц), 3,94-3,92 (5H, м), 1,90 (2H, т, J=7,5, 6,6 Гц), 1,40-1,33 (1H, м), 1,04 (3H, т, J=7,5 Гц), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 62
Используя 0,18 г [2-(3-изобутокси-4-метоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 19, 0,16 г белого порошкообразного N-[2-(3-изобутокси-4-метоксифенил)оксазол-4-илметил]-3-метилпиколинамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 8,58 (1H, ушир.с), 8,39 (1H, дд, J=4,5, 1,8 Гц), 7,63 (1H, с), 7,62-7,59 (2H, м), 7,57 (1H, д, J=0,9 Гц), 7,32-7,27 (1H, м), 6,92 (1H, д, J=8,4 Гц), 4,59 (2H, дд, J=6,0, 0,9 Гц), 3,91 (3H, с), 3,86 (2H, д, J=6,9 Гц), 2,76 (3H, с), 2,20 (1H, кв.т, J=6,9, 6,6 Гц), 1,06 (6H, д, J=6,6 Гц).
Используя 0,15 г [2-(3-изобутокси-4-метоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 19, соединения примеров 63-75 получали таким же способом, как в примере 1.
Пример 63
N-[2-(3-изобутокси-4-метоксифенил)оксазол-4-илметил]-2-метоксибензамид
Выход 0,12 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,41 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 1,8 Гц), 7,64 (1H, с), 7,59 (1H, дд, J=8,4, 2,1 Гц), 7,53 (1H, д, J=2,1 Гц), 7,48-7,42 (1H, м), 7,11-6,90 (3H, м), 4,63 (2H, дд, J=5,4, 0,9 Гц), 3,97 (3H, с), 3,91 (3H, с), 3,86 (2H, д, J=6,9 Гц), 2,21 (1H, кв.т, J=6,6 Гц), 1,06 (6H, д, J=6,6 Гц).
Пример 64
N-[2-(3-изобутокси-4-метоксифенил)оксазол-4-илметил]-2-метилсульфанилбензамид
Выход 0,15 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 7,69 (1H, с), 7,61-7,56 (2H, м), 7,51 (1H, д, J=1,8 Гц), 7,45-7,15 (3H, м), 6,94-6,90 (2H, м), 4,61 (2H, д, J=5,7 Гц), 3,91 (3H, с), 3,85 (2H, д, J=6,9 Гц), 2,46 (3H, с), 2,20 (1H, кв.т, J=6,9 Гц), 1,06 (6H, д, J=6,9 Гц).
Пример 65
N-[2-(3-изобутокси-4-метоксифенил)оксазол-4-илметил]-3-этоксипиколинамид
Выход 80 мг
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,25-8,22 (2H, м), 7,65 (1H, с), 7,58 (1H, дд, J=8,4, 1,8 Гц), 7,52 (1H, д, J=1,8 Гц), 7,40-7,32 (2H, м), 6,92 (1H, д, J=8,4 Гц), 4,62 (2H, дд, J=5,4, 0,9 Гц), 4,18 (2H, кв, J=6,9 Гц), 3,91 (3H, с), 3,86 (2H, д, J=6,9 Гц), 2,20 (1H, кв.т, J=6,9 Гц), 1,52 (3H, т, J=6,9 Гц), 1,06 (6H, д, J=6,6 Гц).
Пример 66
N-[2-(3-изобутокси-4-метоксифенил)оксазол-4-илметил]-2-метокси-4-фторбензамид
Выход 0,11 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,27-8,21 (2H, м), 7,63 (1H, с), 7,59 (1H, дд, J=8,4, 2,1 Гц), 7,52 (1H, д, J=2,1 Гц), 6,93 (1H, д, J=8,4 Гц), 6,81-6,74 (1H, м), 6,69 (1H, дд, J=10,5, 2,4 Гц), 4,61 (2H, дд, J=5,4, 0,9 Гц), 3,96 (3H, с), 3,91 (3H, с), 3,85 (2H, д, J=6,6 Гц), 2,20 (1H, кв.т, J=6,9, 6,6 Гц), 1,06 (6H, д, J=6,6 Гц).
Пример 67
N-[2-(3-изобутокси-4-метоксифенил)оксазол-4-илметил]-2-изопропоксибензамид
Выход 0,15 г
Бесцветное маслянистое вещество
1Н-ЯМР (CDCl3) δ: 8,64 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,8 Гц), 7,62-7,57 (2H, м), 7,54 (1H, д, J=1,8 Гц), 7,44-7,37 (1H, м), 7,08-7,02 (1H, м), 6,98-6,91 (2H, м), 4,72 (1H, кв, J=6,0 Гц), 4,62 (2H, дд, J=5,1, 0,9 Гц), 3,92 (3H, с), 3,85 (2H, д, J=6,6 Гц), 2,20 (1H, кв.т, J=6,6 Гц), 1,40 (6H, д, J=6,0 Гц), 1,06 (6H, д, J=6,6 Гц).
Пример 68
N-[2-(3-изобутокси-4-метоксифенил)оксазол-4-илметил]-2-фтор-6-метоксибензамид
Выход 0,13 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 7,65 (1H, д, J=0,9 Гц), 7,58 (1H, дд, J=8,4, 2,1 Гц), 7,51 (1H, д, J=2,1 Гц), 7,34-7,24 (1H, м), 6,92 (1H, д, J=8,4 Гц), 6,77-6,70 (2H, м), 6,52 (1H, ушир.с), 4,62 (2H, дд, J=5,7, 0,9 Гц), 3,91 (3H, с), 3,90-3,82 (5H, м), 2,20 (1H, кв.т, J=6,9 Гц), 1,06 (6H, д, J=6,9 Гц).
Пример 69
N-[2-(3-изобутокси-4-метоксифенил)оксазол-4-илметил]-3-метоксипиколинамид
Выход 0,14 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,19-8,22 (2H, м), 7,65 (1H, с), 7,58 (1H, дд, J=8,4, 1,8 Гц), 7,52 (1H, д, J=2,1 Гц), 7,43-7,34 (1H, м), 6,92 (1H, д, J=8,4 Гц), 4,61 (2H, дд, J=5,7, 0,9 Гц), 3,96 (3H, с), 3,91 (3H, с), 3,86 (2H, д, J=6,6 Гц), 2,20 (1H, кв.т, J=6,9, 6,6 Гц), 1,06 (6H, д, J=6,9 Гц).
Пример 70
N-[2-(3-изобутокси-4-метоксифенил)оксазол-4-илметил]-3-изобутоксипиколинамид
Выход 68 мг
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,24 (1H, дд, J=3,9, 2,1 Гц), 8,17 (1H, ушир.с), 7,64 (1H, с), 7,58 (1H, дд, J=8,4, 2,1 Гц), 7,52 (1H, д, J=1,8 Гц), 7,38-7,28 (2H, м), 6,92 (2H, д, J=8,4 Гц), 4,63 (2H, дд, J=5,4, 0,9 Гц), 3,91 (3H, с), 3,87-3,82 (4H, м), 2,27-2,13 (2H, м), 1,07-1,02 (2H, м).
Пример 71
N-[2-(3-изобутокси-4-метоксифенил)оксазол-4-илметил]-2-пропоксибензамид
Выход 75 мг
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,52 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 1,8 Гц), 7,62-7,58 (2H, м), 7,53 (1H, с), 7,42 (1H, тд, J=7,2, 1,8 Гц), 7,06 (1H, т, J=7,8 Гц), 6,95-6,91 (2H, м), 4,62 (2H, д, J=5,1 Гц), 4,06 (2H, т, J=6,6 Гц), 3,94 (3H, с), 3,85 (2H, д, J=6,6 Гц), 2,24-2,16 (1H, м), 1,93-1,81 (2H, м), 1,06 (6H, д, J=6,6 Гц), 0,97 (3H, т, J=7,2 Гц).
Пример 72
N-[2-(3-изобутокси-4-метоксифенил)оксазол-4-илметил]-2-бутоксибензамид
Выход 47 мг
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,48 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 1,8 Гц), 7,62-7,58 (2H, м), 7,53 (1H, с), 7,42 (1H, тд, J=7,2, 1,8 Гц), 7,06 (1H, т, J=7,8 Гц), 6,95-6,91 (2H, м), 4,61 (2H, д, J=5,1 Гц), 4,10 (2H, т, J=6,6 Гц), 3,91 (3H, с), 3,85 (2H, д, J=6,6 Гц), 2,24-2,16 (1H, м), 1,85-1,75 (2H, м), 1,43-1,36 (2H, м), 1,05 (6H, д, J=6,6 Гц), 0,84 (3H, т, J=7,2 Гц).
Пример 73
N-[2-(3-изобутокси-4-метоксифенил)оксазол-4-илметил]-2-изобутоксибензамид
Выход 90 мг
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,52 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 1,8 Гц), 7,62-7,58 (2H, м), 7,53 (1H, с), 7,42 (1H, тд, J=7,2, 1,8 Гц), 7,06 (1H, т, J=7,8 Гц), 6,93-6,90 (2H, м), 4,62 (2H, д, J=5,1 Гц), 3,91 (3H, с), 3,87-3,83 (4H, м), 2,24-2,16 (2H, м), 1,06 (6H, д, J=6,6 Гц), 0,95 (6H, д, J=6,6 Гц).
Пример 74
N-[2-(3-изобутокси-4-метоксифенил)оксазол-4-илметил]-3-изопропоксипиколинамид
Выход 0,11 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,52 (1H, ушир.с), 8,27 (1H, ушир.с), 7,63 (1H, с), 7,58 (1H, дд, J=7,8, 1,8 Гц), 7,53 (1H, с), 7,35-7,34 (2H, м), 6,92 (1H, д, J=8,4 Гц), 4,67-4,61 (3H, м), 3,91 (3H, с), 3,85 (2H, д, J=6,6 Гц), 2,22-2,17 (1H, м), 1,42 (6H, д, J=6,6 Гц), 1,06 (6H, д, J=6,6 Гц).
Пример 75
N-[2-(3-изобутокси-4-метоксифенил)оксазол-4-илметил]-2-метилникотинамид
Выход 0,13 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,52 (1H, ушир.с), 7,86 (1H, д, J=7,5 Гц), 7,76 (1H, д, J=7,5 Гц), 7,69 (1H, с), 7,59 (1H, д, J=4,2 Гц), 7,56 (1H, с), 6,92 (1H, д, J=8,7 Гц), 4,58 (2H, д, J=5,1 Гц), 3,91 (3H, с), 3,84 (2H, д, J=6,9 Гц), 2,69 (3H, с), 2,23-2,15 (1H, м), 1,05 (6H, д, J=5,1 Гц).
Пример 76
Используя 0,2 г {2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}метиламина, полученного в ссылочном примере 25, 0,24 г белого порошкообразного N-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}-3-метоксипиколинамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 8,24-8,19 (2H, м), 7,72 (1H, дд, J=8,4, 1,8 Гц), 7,65 (1H, д, J=0,9 Гц), 7,62 (1H, д, J=1,8 Гц), 7,43-7,35 (2H, м), 6,98 (1H, д, J=8,4 Гц), 4,60 (2H, дд, J=5,7, 0,9 Гц), 4,46 (2H, кв, J=5,4 Гц), 3,95 (3H, с), 3,93 (3H, с).
Используя 0,2 г {2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}метиламина, полученного в ссылочном примере 25, соединения примеров 77-79 получали таким же способом, как в примере 1.
Пример 77
N-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}-3-этоксипиколинамид
Выход 0,24 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,26-8,22 (2H, м), 7,72 (1H, дд, J=8,4, 2,1 Гц), 7,65 (1H, с), 7,63 (1H, д, J=1,8 Гц), 7,40-7,32 (2H, м), 6,98 (1H, д, J=8,1 Гц), 4,62 (2H, дд, J=5,7, 0,9 Гц), 4,46 (2H, кв, J=8,4 Гц), 4,18 (2H, кв, J=6,9 Гц), 1,52 (3H, т, J=6,9 Гц).
Пример 78
N-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}-2-метоксибензамид
Выход 0,18 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,42 (1H, ушир.с), 8,23 (1H, дд, J=7,5, 1,8 Гц), 7,73 (1H, дд, J=8,4, 2,1 Гц), 7,65-7,60 (2H, м), 7,48-7,42 (1H, м), 7,08 (1H, тд, J=8,4, 0,9 Гц), 6,98 (1H, д, J=8,4 Гц), 4,62 (2H, дд, J=5,4, 0,9 Гц), 4,46 (2H, кв, J=8,4 Гц), 3,98 (3H, с), 3,93 (3H, с).
Пример 79
N-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}-2-метилбензамид
Выход 0,15 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 7,72 (1H, дд, J=8,4, 2,1 Гц), 7,66 (1H, с), 7,61 (1H, д, J=2,1 Гц), 7,41-7,14 (4H, м), 6,98 (1H, д, J=8,4 Гц), 6,31 (1H, ушир.с), 4,58 (2H, дд, J=5,4, 0,9 Гц), 4,45 (2H, кв, J=8,4 Гц), 3,93 (3H, с), 2,46 (3H, с).
Используя 0,15 г {2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}метиламина, полученного ссылочный пример 25, соединения примеров 80-82 получали таким же способом, как в примере 1.
Пример 80
N-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}-2-пропоксибензамид
Выход 0,15 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,53 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,8 Гц), 7,73 (1H, дд, J=8,4, 2,1 Гц), 7,65-7,60 (2H, м), 7,45-7,38 (1H, м), 7,09-6,93 (3H, м), 4,62 (2H, д, J=5,1 Гц), 4,45 (2H, кв, J=8,1 Гц), 4,07 (2H, т, J=6,6 Гц), 3,94 (3H, с), 1,88 (2H, кв.т, J=7,5, 6,6 Гц), 0,98 (3H, т, J=7,5 Гц).
Пример 81
N-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}-2-изопропоксибензамид
Выход 0,18 г
Белый порошок
1Н-ЯМР (CDCl3) δ: ,64 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 1,8 Гц), 7,74 (1H, дд, J=8,4, 2,1 Гц), 7,65 (1H, д, J=2,1 Гц), 7,63 (1H, с), 7,44-7,37 (1H, м), 7,08-6,94 (3H, м), 4,73 (1H, тт, J=6,0 Гц), 4,62 (2H, дд, J=5,1, 0,9 Гц), 4,46 (2H, кв, J=8,4 Гц), 3,94 (3H, с), 1,41 (6H, д, J=6,0 Гц).
Пример 82
N-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}-4-хлор-2-метоксибензамид
Выход 0,21 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,29 (1H, ушир.с), 8,17 (1H, д, J=8,4 Гц), 7,73 (1H, дд, J=8,4, 1,8 Гц), 7,64 (1H, д, J=1,5 Гц), 7,07 (1H, дд, J=8,4, 1,8 Гц), 7,00-6,96 (2H, м), 4,60 (2H, дд, J=5,4, 0,9 Гц), 4,46 (2H, кв, J=8,4 Гц), 3,98 (3H, с), 3,93 (3H, с).
Пример 83
Используя 0,1 г {2-[3-циклопропилметокси-4-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}метиламина, полученного в ссылочном примере 34, 0,11 г белого порошкообразного N-{2-[3-циклопропилметокси-4-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}-2-этоксибензамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 8,54 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 1,8 Гц) 7,64 (1H, с), 7,60-7,55 (2H, м), 7,45-7,38 (1H, м), 7,10-7,04 (2H, м), 6,94 (1H, д, J=8,1 Гц), 4,62 (2H, дд, J=5,4, 0,9 Гц), 4,48 (2H, кв, J=8,4 Гц), 4,18 (2H, кв, J=6,9 Гц), 3,95 (2H, д, J=7,2 Гц), 1,48 (3H, т, J=7,2 Гц), 1,35-1,29 (1H, м), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 84
Используя 0,18 г {2-[3-циклопропилметокси-4-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}метиламина, полученного в ссылочном примере 34, 0,2 г белого порошкообразного N-{2-[3-циклопропилметокси-4-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}-3-метилпиколинамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 8,57 (1H, ушир.с), 8,39 (1H, дд, J=4,5, 1,2 Гц), 7,64 (1H, с), 7,60-7,55 (3H, м), 7,32-7,26 (1H, м), 7,06-7,03 (1H, м), 4,59 (2H, дд, J=5,7, 0,9 Гц), 4,48 (2H, кв, J=8,4 Гц), 3,95 (2H, д, J=6,9 Гц), 2,76 (3H, с), 1,38-1,28 (1H, м), 0,69-0,62 (2H, м), 0,40-0,35 (2H, м).
Пример 85
Используя 0,3 г [2-(3,4-диэтоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 37, 0,11 г белого порошкообразного N-[2-(3,4-диэтоксифенил)оксазол-4-илметил]-2-пропоксибензамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 8,51 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,8 Гц), 7,60-7,50 (3H, м), 7,41 (1H, м), 7,06 (1H, м), 7,00-6,90 (2H, м), 4,61 (2H, д, J=5,1 Гц), 4,06 (2H, т, J=6,6 Гц), 1,87 (2H, ткв., J=7,2, 6,6 Гц), 1,49 (6H, т, J=6,9 Гц), 0,96 (3H, т, J=7,2 Гц).
Используя 0,3 г [2-(3,4-диэтоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 37, соединения примеров 86-91 получали таким же способом, как в примере 1.
Пример 86
N-[2-(3,4-диэтоксифенил)оксазол-4-илметил]-2-трифторметилбензамид
Выход 0,11 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 7,75-7,50 (7H, м), 6,91 (1H, д, J=8,4 Гц), 6,32 (1H, ушир.с), 4,59 (2H, д, J=5,4 Гц), 4,17 (2H, кв, J=6,9 Гц), 4,14 (2H, кв, J=6,9 Гц), 1,48 (6H, т, J=6,9 Гц).
Пример 87
N-[2-(3,4-диэтоксифенил)оксазол-4-илметил]пиколинамид
Выход 0,34 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,55 (1H, м), 8,47 (1H, ушир.с), 8,21 (1H, д, J=7,8 Гц), 7,85 (1H, м), 7,57 (1H, дд, J=8,4, 1,8 Гц), 7,55 (1H, д, J=1,8 Гц), 7,42 (1H, м), 6,91 (1H, д, J=8,4 Гц), 6,32 (1H, ушир.с), 4,63 (2H, д, J=6,0 Гц), 4,18 (2H, кв, J=6,9 Гц), 4,15 (2H, кв, J=6,9 Гц), 1,48 (3H, т, J=6,9 Гц), 1,48 (3H, т, J=6,9 Гц).
Пример 88
N-[2-(3,4-диэтоксифенил)оксазол-4-илметил]-2-этоксибензамид
Выход 0,23 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 8,55 (1H, м), 8,47 (1H, ушир.с), 8,21 (1H, д, J=7,8 Гц), 7,85 (1H, м), 7,57 (1H, дд, J=8,4, 1,8 Гц), 7,55 (1H, д, J=1,8 Гц), 7,42 (1H, м), 6,91 (1H, д, J=8,4 Гц), 6,32 (1H, ушир.с), 4,63 (2H, д, J=6,0 Гц), 4,18 (2H, кв, J=6,9 Гц), 4,15 (2H, кв, J=6,9 Гц), 1,48 (3H, т, J=6,9 Гц), 1,48 (3H, т, J=6,9 Гц).
Пример 89
N-[2-(3,4-диэтоксифенил)оксазол-4-илметил]-4-этоксибензамид
Выход 0,32 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 7,80-7,70 (2H, м), 7,63 (1H, с), 7,60-7,50 (2H, м), 6,95-6,85 (3H, м), 6,66 (1H, ушир.с), 4,57 (2H, кв, J=6,0 Гц), 4,17 (2H, кв, J=6,9 Гц), 4,15 (2H, кв, J=6,9 Гц), 4,06 (2H, кв, J=6,9 Гц), 1,48 (3H, т, J=6,9 Гц), 1,48 (3H, т, J=6,9 Гц), 1,42 (3H, т, J=6,9 Гц).
Пример 90
N-[2-(3,4-диэтоксифенил)оксазол-4-илметил]-5-метокси-2-трифторметоксибензамид
Выход 0,34 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 7,95 (1H, ушир.с), 7,73 (1H, д, J=3,0 Гц), 7,70-7,50 (3H, м), 6,99 (1H, дд, J=9,0, 3,0 Гц), 6,90-6,80 (2H, м), 4,61 (2H, д, J=6,0 Гц), 4,18 (2H, кв, J=6,9 Гц), 4,15 (2H, кв, J=6,9 Гц), 3,82 (3H, с), 1,48 (3H, т, J=6,9 Гц), 1,46 (3H, т, J=6,9 Гц).
Пример 91
N-[2-(3,4-диэтоксифенил)оксазол-4-илметил]-3-этоксибензамид
Выход 0,12 г
Белый порошок
1Н-ЯМР (CDCl3) δ: 7,57 (1H, дд, J=8,1, 2,1 Гц), 7,53 (1H, д, J=2,1 Гц), 7,35-7,25 (3H, м), 7,01 (1H, м), 6,92 (1H, д, J=8,1 Гц), 6,68 (1H, ушир.с), 4,58 (2H, д, J=5,4 Гц), 4,18 (2H, кв, J=6,9 Гц), 4,15 (2H, кв, J=6,9 Гц), 4,07 (2H, кв, J=6,9 Гц), 1,49 (3H, т, J=6,9 Гц), 1,48 (3H, т, J=6,9 Гц), 1,42 (3H, т, J=6,9 Гц).
Пример 92
Используя 0,3 г [2-(3,4-диметоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 40, 0,27 г белого порошкообразного N-[2-(3,4-диметоксифенил)оксазол-4-илметил]-2-этоксибензамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 8,56 (1H, ушир.с), 8,24 (1H, дд, J=8,1, 1,8 Гц), 7,65-7,60 (2H, м), 7,55 (1H, д, J=1,5 Гц), 7,42 (1H, м), 7,07 (1H, м), 6,95-6,90 (2H, м), 4,63 (2H, д, J=5,1 Гц), 4,18 (2H, кв, J=6,9 Гц), 3,98 (3H, с), 3,97 (3H, с), 1,26 (3H, т, J=6,9 Гц).
Пример 93
Используя 0,25 г [2-(3,4-диметоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 40, 0,23 г белого порошкообразного N-[2-(3,4-диметоксифенил)оксазол-4-илметил]-2-этилбензамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 7,66 (1H, с), 7,60 (1H, дд, J=8,4, 1,8 Гц), 7,52 (1H, д, J=1,8 Гц), 7,40-7,20 (4H, м), 6,93 (1H, д, J=8,4 Гц), 6,34 (1H, ушир.с), 4,58 (2H, д, J=5,4 Гц), 3,96 (3H, с), 3,94 (3H, с), 2,82 (2H, кв, J=7,5 Гц), 1,20 (3H, т, J=7,5 Гц).
Пример 94
Используя 0,2 г [2-(3,4-диметоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 40, 0,16 г белого порошкообразного N-[2-(3,4-диметоксифенил)оксазол-4-илметил]-3-метилпиколинамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 8,58 (1H, ушир.с), 8,39 (1H, м), 7,65-7,55 (4H, м), 7,30 (1H, м), 6,92 (1H, д, J=8,4 Гц), 4,59 (2H, д, J=6,0 Гц), 3,97 (3H, с), 3,93 (3H, с), 2,76 (3H, с), 1,58 (3H, с).
Пример 95
Используя 0,2 г [2-(3,4-диметоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 40, 0,12 г белого порошкообразного N-[2-(3,4-диметоксифенил)оксазол-4-илметил]-3-метоксипиколинамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 8,21 (1H, ушир.с), 8,20 (1H, дд, J=3,9, 1,8 Гц), 7,65 (1H, с), 7,61 (1H, дд, J=8,4, 1,8 Гц), 7,54 (1H, д, J=1,8 Гц), 7,45-7,30 (2H, м), 6,92 (1H, д, J=8,4 Гц), 4,61 (2H, д, J=6,0 Гц), 3,97 (3H, с), 3,96 (3H, с), 3,93 (3H, с).
Пример 96
0,13 г [2-(3-бензилокси-4-дифторметоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 46, суспендировали в 10 мл ацетона. Затем к полученной суспензии добавляли 0,14 г 1-гидроксибензотриазола, 0,19 г гидрохлорида 1-этил-3-(3-диметиламинопропил)карбoдиимида и 0,14 г 3-метилпиколината и смесь кипятили с обратным холодильником в течение 30 минут. Реакционную смесь концентрировали при пониженном давлении и к остатку добавляли воду. Осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой и концентрировали. Остаток очищали колоночной хроматографией на силикагеле(н-гексан:этилацетат = 1:1) с получением 0,16 г белого порошкообразного N-[2-(3-бензилокси-4-дифторметоксифенил)оксазол-4-илметил]-3-метилпиколинамида.
1Н-ЯМР (CDCl3) δ: 8,56 (1H, ушир.с), 8,40 (1H, д, J=3,9 Гц), 7,74-7,58 (4H, м), 7,47-7,23 (7H, м), 6,62 (1H, т, J=74,7 Гц), 5,21 (2H, с), 4,60 (2H, д, J=5,7 Гц), 2,76 (3H, с).
Пример 97
0,16 г N-[2-(3-бензилокси-4-дифторметоксифенил)оксазол-4-илметил]-3-метилпиколинамида, полученного в примере 96, растворяли в 5 мл этанола, к смеси добавляли 20 мг 10% палладия-на-углероде в виде порошка и смесь перемешивали при комнатной температуре в течение 30 минут в атмосфере водорода. Катализатор отфильтровывали и фильтрат концентрировали с получением 0,12 г белого порошкообразного N-[2-(4-дифторметокси-3-гидроксифенил)оксазол-4-илметил]-3-метилпиколинамида.
1Н-ЯМР (CDCl3) δ: 8,60-8,54 (1H, м), 8,39 (1H, д, J=3,3 Гц), 7,69-7,55 (4H, м), 7,37-7,28 (1H, м), 7,18 (1H, д, J=8,4 Гц), 6,59 (1H, т, J=73,2 Гц), 5,79 (1H, ушир.с), 4,59 (2H, дд, J=6,0, 0,9 Гц), 2,76 (3H, с).
Пример 98
0,12 г N-[2-(4-дифторметокси-3-гидроксифенил)оксазол-4-илметил]-3-метилпиколинамида, полученного в примере 97, и 0,15 мл 1,8-диазабицикло[5.4.0]ундец-7-ена растворяли в 4 мл этанола. К смеси добавляли 0,15 мл (бромметил)циклопропана и нагревали при кипячении с обратным холодильником в течение 3 часов. Растворитель отгоняли при помощи дистилляции и к остатку добавляли воду. Осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой и концентрировали. Остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 1:1). Полученные неочищенные кристаллы перекристаллизовывали с использованием смеси этанол-н-гексан и получали 60 мг белого порошкообразного N-[2-(3-циклопропилметокси-4-дифторметоксифенил)оксазол-4-илметил]-3-метилпиколинамида.
1Н-ЯМР (CDCl3) δ: 8,59-8,54 (1H, м), 8,39 (1H, дд, J=4,5, 1,2 Гц), 7,67 (1H, с), 7,63-7,56 (3H, м), 7,37-7,28 (1H, м), 7,22 (1H, д, J=8,1 Гц), 6,69 (1H, т, J=75,0 Гц), 4,59 (2H, дд, J=5,7, 0,9 Гц), 3,98 (2H, д, J=6,9 Гц), 2,76 (3H, с), 1,35-1,20 (1H, м), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 99
Используя 0,2 г [2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 13, 0,11 г белого порошкообразного N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]изохинолин-1-карбоксамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 9,60 (1H, м), 8,67 (1H, ушир.с), 8,47 (1H, д, J=2,4 Гц), 7,90-7,80 (2H, м), 7,75-7,65 (3H, м), 7,61 (1H, дд, J =8,4, 1,8 Гц), 7,53 (1H, д, J=1,8 Гц), 6,92 (1H, д, J=8,4 Гц), 4,68 (2H, д, J=6,0 Гц), 3,94 (2H, д, J=7,5 Гц), 3,92 (3H, с), 1,39 (1H, м), 0,70-0,60 (2H, м), 0,40-0,35 (2H, м).
Пример 100
4,42 г гидроксида натрия суспендировали в 160 мл диметоксиэтана. Суспензию перемешивали при охлаждении льдом при одновременном отдельном добавлении 16 г 3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]метилпропионата, полученного в ссылочном примере 48, и 39,23 г 2-этоксипербензойной кислоты и затем осуществляли нагревание и кипячение с обратным холодильником в течение 7 часов. После охлаждения льдом к смеси добавляли насыщенный раствор хлорида аммония и перемешивали в течение 30 минут. Затем к смеси добавляли воду и осуществляли экстракцию этилацетатом, а затем сушили над безводным сульфатом магния и растворитель затем отгоняли. Остаток подвергали очистке на колонке с силикагелем (н-гексан:этилацетат = 3:1) и получали 13,4 г желтого маслянистого вещества, метил 2-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-3-(2-этоксифенил)-3-оксопропионата.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, д, J=7,8 Гц), 7,57-7,54 (3H, м), 7,48-7,28 (6H, м), 6,99-6,90 (3H, м), 5,16 (2H, с), 4,98 (1H, т, J=6,9 Гц), 4,14 (2H, кв, J=6,9 Гц), 3,91 (3H, с), 3,70 (3H, с), 3,27-3,19 (2H, м), 1,45 (3H, т, J=6,9 Гц).
Пример 101
13,4 г метил 2-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-3-(2-этоксифенил)-3-оксопропионат, полученного в примере 100, суспендировали в 67 мл этанола, к смеси добавляли 67 мл 47%-ной бромистоводородной кислоты и суспензию нагревали и кипятили с обратным холодильником в течение ночи. Смесь оставляли для охлаждения и затем образовавшиеся кристаллы собирали при помощи фильтрации, промывали водой и диизопропиловым эфиром и сушили с получением, таким образом, 8,1 г белого порошкообразного 1-(2-этоксифенил)-3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,30 (1H, д, J=8,7 Гц), 7,84 (1H, д, J=1,8 Гц), 7,83-7,71 (2H, м), 7,45 (1H, т, J=8,4 Гц), 7,06 (1H, д, J=8,7 Гц), 6,99-6,93 (2H, м), 4,17 (2H, кв, J=6,9 Гц), 4,00 (3H, с), 3,67 (2H, т, J=6,6 Гц), 3,35 (2H, т, J=6,6 Гц), 1,55 (3H, т, J=6,9 Гц).
Пример 102
8,1 г 1-(2-этоксифенил)-3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]пропан-1-она, полученного в примере 101, суспендировали в 220 мл этанола, к смеси добавляли 10 г 1,8-диазабицикло[5.4.0]ундец-7-ен и 5,96 г (бромметил)циклопропана и осуществляли перемешивание в течение 5 часов при одновременном нагревании и кипячении с обратным холодильником. После отгонки этанола при пониженном давлении добавляли воду, осуществляли экстракцию этилацетатом, а затем сушили над безводным сульфатом магния и отгоняли растворитель. Остаток подвергали очистке на колонке с силикагелем (н-гексан:этилацетат = 4:1) и полученные неочищенные кристаллы перекристаллизовывали с использованием этанола с получением, таким образом, 4,4 г белого порошкообразного 3-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,56 (1H, дд, J=8,4, 2,1 Гц), 7,50 (1H, с), 7,45-7,39 (2H, м), 7,00-6,89 (3H, м), 4,13 (2H, кв, J=7,2 Гц), 3,93-3,91 (5H, м), 3,41 (2H, т, J=6,6 Гц), 2,99 (2H, т, J=6,6 Гц), 1,51 (3H, т, J=7,2 Гц), 1,47 (1H, м), 0,67-0,64 (2H, м), 0,40-0,36 (2H, м).
Пример 103
0,3 г 1-(2-этоксифенил)-3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]пропан-1-она, полученного в примере 101, суспендировали в 10 мл этанола, к смеси добавляли 0,37 г 1,8-диазабицикло[5.4.0]ундец-7-ена и 0,26 г этилиодида и суспензию перемешивали в течение 4 часов при одновременном нагревании и кипячении с обратным холодильником. После отгонки этанола при пониженном давлении добавляли воду, осуществляли экстракцию этилацетатом, а затем сушили над безводным сульфатом магния и отгоняли растворитель. Остаток подвергали очистке на колонке с силикагелем (н-гексан:этилацетат = 3:1) с получением, таким образом, 0,15 г белого порошкообразного 3-[2-(3-этокси-4-метоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,56 (1H, дд, J=8,4, 1,8 Гц), 7,52-7,40 (2H, м), 6,99-6,89 (3H, м), 4,21-4,09 (4H, м), 3,91 (3H, с), 3,42 (2H, т, J=6,9 Гц), 2,99 (2H, т, J=6,9 Гц), 1,51-1,45 (6H, м).
Пример 104
0,3 г 1-(2-этоксифенил)-3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]пропан-1-она, полученного в примере 101, суспендировали в 10 мл этанола, к смеси добавляли 0,37 г 1,8-диазабицикло[5.4.0]ундец-7-ена и 0,14 мл аллилбромида и осуществляли перемешивание в течение 3 часов при одновременном нагревании и кипячении с обратным холодильником. После отгонки этанола при пониженном давлении добавляли воду, осуществляли экстракцию этилацетатом, а затем сушили над безводным сульфатом магния и отгоняли растворитель. Остаток подвергали очистке на колонке с силикагелем (н-гексан:этилацетат = 3:1) с получением, таким образом, 0,2 г белого порошкообразного 3-[2-(3-аллилокси-4-метоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,8, 1,8 Гц), 7,58 (1H, дд, J=8,4, 1,8 Гц), 7,52 (1H, д, J=1,8 Гц), 7,45-7,40 (2H, м), 7,00-6,90 (3H, м), 6,18-6,05 (1H, м), 5,47-5,29 (2H, м), 4,67 (2H, д, J=5,1 Гц), 4,13 (2H, кв, J=6,9 Гц), 3,92 (3H, с), 3,42 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 1,47 (3H, т, J=6,9 Гц).
Используя 1-(2-этоксифенил)-3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]пропан-1-он, полученный в примере 101, соединения примеров 105-110 получали таким же способом, как в примере 102.
Пример 105
3-[2-(3-циклопентилокси-4-метоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,57-7,51 (2H, м), 7,45-7,39 (2H, м), 6,99-6,88 (3H, м), 4,88 (1H, ушир.с), 4,12 (2H, кв, J=6,9 Гц), 3,88 (3H, с), 3,42 (2H, т, J=6,9 Гц), 2,99 (2H, т, J=6,9 Гц), 2,04-1,87 (6H, м), 1,65-1,60 (2H, м), 1,47 (3H, т, J=6,9 Гц).
Пример 106
3-[2-(3-изобутокси-4-метоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,55 (1H, дд, J=8,4, 1,8 Гц), 7,50 (1H, д, J=2,1 Гц), 7,45-7,40 (2H, м), 4,13 (2H, кв, J=6,9 Гц), 3,90 (3H, с), 3,84 (2H, д, J=6,9 Гц), 3,42 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 2,23-2,14 (1H, м), 1,48 (3H, т, J=6,9 Гц), 1,05 (6H, д, J=6,9 Гц).
Пример 107
1-(2-этоксифенил)-3-[2-(4-метокси-3-пропоксифенил)оксазол-4-ил]пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,56 (1H, дд, J=8,1, 1,8 Гц), 7,52 (1H, с), 7,45-7,40 (2H, м), 7,00-6,89 (3H, м), 4,13 (2H, кв, J=6,9 Гц), 4,05 (2H, т, J=6,9 Гц), 3,90 (3H, с), 3,42 (2H, т, J=7,5 Гц), 3,00 (2H, т, J=7,5 Гц), 1,95-1,84 (2H, м), 1,47 (3H, т, J=6,9 Гц), 1,05 (3H, т, J=6,9 Гц).
Пример 108
3-[2-(3-(3-бутенилокси)-4-метоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,57 (1H, дд, J=8,4, 1,8 Гц), 7,52 (1H, с), 7,45-7,40 (2H, м), 6,97-6,89 (3H, м), 6,00-5,90 (1H, м), 5,22-5,10 (2H, м), 4,17-4,11 (4H, м), 3,90 (3H, с), 3,42 (2H, т, J=7,5 Гц), 3,00 (2H, т, J=7,5 Гц), 2,67-2,62 (2H, м), 1,47 (3H, т, J=6,9 Гц).
Пример 109
3-[2-(3-бутокси-4-метоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,57 (1H, дд, J=8,4, 1,8 Гц), 7,53 (1H, д, J=2,1 Гц), 7,45-7,39 (2H, м), 7,00-6,89 (3H, м), 4,16-4,07 (4H, м), 3,98 (3H, с), 3,42 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,90-1,86 (2H, м), 1,57-1,42 (5H, м), 0,99 (3H, т, J=7,2 Гц).
Пример 110
1-(2-этоксифенил)-3-[2-(4-метокси-3-(2-пропенилокси)фенил)оксазол-4-ил]пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,8, 1,8 Гц), 7,66-7,63 (2H, м), 7,46-7,39 (2H, м), 7,00-6,92 (3H, м), 4,83 (2H, д, J=2,1 Гц), 4,13 (2H, кв, J=6,9 Гц), 3,92 (3H, с), 3,42 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 2,52 (1H, т, J=2,1 Гц), 1,47 (3H, т, J=6,9 Гц).
Пример 111
5,0 г 1-(2-этоксифенил)-3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]пропан-1-она, полученного в примере 101, растворяли в 50 мл диметилформамида, к смеси добавляли 3,35 г 2-бромпропана и 5,63 г карбоната калия и осуществляли перемешивание в течение ночи при комнатной температуре. К полученной смеси добавляли воду, осуществляли экстракцию этилацетатом, а затем сушили над безводным сульфатом магния и отгоняли растворитель. Остаток подвергали очистке на колонке с силикагелем (н-гексан:этилацетат = 4:1) и полученные неочищенные кристаллы перекристаллизовывали с использованием этанола с получением, таким образом, 2,99 г белого порошкообразного 1-(2-этоксифенил)-3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,59-7,54 (2H, м), 7,45-7,39 (2H, м), 7,00-6,89 (3H, м), 4,68-4,60 (1H, м), 4,13 (2H, кв, J=6,9 Гц), 3,89 (3H, с), 3,42 (2H, т, J=7,5 Гц), 2,99 (2H, т, J=7,5 Гц), 1,47 (3H, т, J=6,9 Гц), 1,39 (6H, д, J=6,3 Гц).
Используя 1-(2-этоксифенил)-3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]пропан-1-он, полученный в примере 101, соединения примеров 112-122 получали таким же способом, как в примере 111.
Пример 112
1-(2-этоксифенил)-3-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,72-7,68 (2H, м), 7,60 (1H, д, J=1,8 Гц), 7,45-7,39 (2H, м), 7,00-6,92 (3H, м), 4,44 (2H, кв, J=8,4 Гц), 4,13 (2H, кв, J=6,6 Гц), 3,90 (3H, с), 3,42 (2H, т, J=6,9 Гц), 2,99 (2H, т, J=6,9 Гц), 1,48 (3H, т, J=6,6 Гц).
Пример 113
3-[2-(3-циклогексилметокси-4-метоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,55 (1H, дд, J=8,4, 1,8 Гц), 7,50 (1H, д, J=1,8 Гц), 7,45-7,40 (2H, м), 7,00-6,88 (3H, м), 4,14 (2H, кв, J=6,9 Гц), 3,90 (3H, с), 3,86 (2H, д, J=6,0 Гц), 3,42 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 2,00-1,86 (3H, м), 1,79-1,63 (3H, м), 1,45 (3H, т, J=6,9 Гц), 1,40-1,22 (2H, м), 1,10-1,02 (2H, м).
Пример 114
3-[2-(3-циклопентилметокси-4-метоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,55 (1H, дд, J=8,4, 1,8 Гц), 7,50 (1H, д, J=1,8 Гц), 7,45-7,40 (2H, м), 7,00-6,88 (3H, м), 4,14 (2H, кв, J=6,9 Гц), 3,95 (2H, д, J=7,2 Гц), 3,90 (3H, с), 3,42 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 2,48-2,44 (1H, м), 2,04-1,86 (2H, м), 1,63-1,50 (4H, м), 1,45 (3H, с), 1,39-1,35 (2H, м).
Пример 115
1-(2-этоксифенил)-3-[2-(4-метокси-3-(4-пентенилокси)фенил)оксазол-4-ил]пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 2,1 Гц), 7,56 (1H, дд, J=8,1, 2,1 Гц), 7,51 (1H, д, J=2,1 Гц), 7,45-7,39 (2H, м), 7,00-6,89 (3H, м), 5,87-5,81 (1H, м), 5,10-4,99 (2H, м), 4,17-4,08 (4H, м), 3,91 (3H, с), 3,42 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 2,27-2,22 (2H, м), 2,04-1,95 (2H, м), 1,47 (3H, т, J=7,2 Гц).
Пример 116
3-[2-(3-циклобутилметокси-4-метоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 2,1 Гц), 7,56 (1H, дд, J=8,1, 2,1 Гц), 7,51 (1H, д, J=2,1 Гц), 7,45-7,39 (2H, м), 7,00-6,80 (3H, м), 4,13 (2H, кв, J=7,2 Гц), 4,07 (2H, д, J=7,2 Гц), 3,90 (3H, с), 3,42 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 2,96-2,85 (1H, м), 2,20-2,14 (2H, м), 1,91-1,80 (2H, м), 1,45 (3H, т, J=7,2 Гц).
Пример 117
1-(2-этоксифенил)-3-{2-[4-метокси-3-(3-метил-2-бутенилокси)фенил]оксазол-4-ил}пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,57 (1H, дд, J=8,1, 1,8 Гц), 7,51 (1H, д, J=1,8 Гц), 7,00-6,89 (3H, м), 5,55 (1H, т, J=6,6 Гц), 4,64 (2H, д, J=6,6 Гц), 4,13 (2H, кв, J=6,9 Гц), 3,91 (3H, с), 3,42 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,77 (6H, д, J=6,6 Гц), 1,45 (3H, т, J=6,9 Гц).
Пример 118
3-{2-[3-(2-циклогексенилокси)-4-метоксифенил]оксазол-4-ил}-1-(2-этоксифенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,60-7,57 (2H, м), 7,42-7,39 (2H, м), 7,00-6,89 (3H, м), 6,00-5,92 (2H, м), 4,88 (1H, ушир.с), 4,15 (2H, кв, J=7,2 Гц), 3,89 (3H, с), 3,42 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 2,04-1,80 (4H, м), 1,72-1,53 (2H, м), 1,45 (3H, т, J=7,2 Гц).
Пример 119
1-(2-этоксифенил)-3-[2-(4-метокси-3-фенэтилоксифенил)оксазол-4-ил]пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,69 (1H, дд, J=7,8, 1,8 Гц), 7,59 (1H, дд, J=8,4, 1,8 Гц), 7,56 (1H, д, J=1,8 Гц), 7,51-6,98 (7H, м), 6,95-6,90 (3H, м), 4,27 (2H, т, J=7,2 Гц), 4,11 (2H, кв, J=6,9 Гц), 3,91 (3H, с), 3,41 (2H, т, J=7,2 Гц), 3,20 (2H, т, J=7,2 Гц), 2,98 (2H, т, J=7,2 Гц), 1,54 (3H, т, J=6,9 Гц).
Пример 120
1-(2-этоксифенил)-3-{2-[4-метокси-3-(3-фенилпропокси)фенил]оксазол-4-ил}пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,58 (1H, дд, J=8,4, 1,8 Гц), 7,56 (1H, д, J=1,8 Гц), 7,49-7,39 (2H, м), 7,30-7,15 (5H, м), 6,99-6,90 (3H, м), 4,16-4,08 (4H, м), 3,92 (3H, с), 3,42 (2H, т, J=7,2 Гц), 2,98 (2H, т, J=7,2 Гц), 2,84 (2H, т, J=8,1 Гц), 2,24-2,15 (2H, м), 1,46 (3H, т, J=6,9 Гц).
Пример 121
3-{2-[3-(2-циклопропилэтокси)-4-метоксифенил]оксазол-4-ил}-1-(2-этоксифенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,8, 1,8 Гц), 7,57-7,55 (2H, м), 7,43-7,39 (2H, м), 7,00-6,89 (3H, м), 4,19-4,10 (4H, м), 3,91 (3H, с), 3,42 (2H, т, J=6,9 Гц), 3,01 (2H, т, J=6,9 Гц), 1,81-1,74 (2H, м), 1,48 (3H, т, J=6,9 Гц), 0,88-0,83 (1H, м), 0,52-0,47 (2H, м), 0,16-0,12 (2H, м).
Пример 122
3-{2-[3-(2-циклопентилэтокси)-4-метоксифенил]оксазол-4-ил}-1-(2-этоксифенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,8, 1,8 Гц), 7,56 (1H, дд, J=8,4, 1,8 Гц), 7,51 (1H, д, J=2,1 Гц), 7,45-7,39 (2H, м), 7,00-6,89 (3H, м), 4,17-4,07 (4H, м), 3,90 (3H, с), 3,42 (2H, т, J=6,9 Гц), 3,00 (2H, т, J=6,9 Гц), 2,00-1,81 (5H, м), 1,66-1,62 (4H, м), 1,45 (3H, т, J=6,9 Гц), 1,28-1,15 (2H, м).
Пример 123
1,0 г метил 3-{2-[3-циклопропилметокси-4-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}пропионата, полученного в ссылочном примере 49, и 0,54 г метил 3-метоксипиколината добавляли к 5 мл диметилформамида и смесь перемешивали при охлаждении льдом в течение 10 минут. К полученной смеси добавляли 0,83 г трет-пентоксида натрия и затем перемешивали при охлаждении льдом в течение часа с последующим перемешиванием при комнатной температуре в течение 1 часа. Реакционную смесь перемешивали при охлаждении льдом, к смеси добавляли насыщенный раствор хлорида аммония и снова перемешивали в течение 30 минут. К смеси добавляли воду, осуществляли экстракцию этилацетатом, а затем сушили над безводным сульфатом магния и отгоняли растворитель. К остатку добавляли 5,0 мл диметилсульфоксида, 84 мг хлорида лития и 41 мкл дистиллированной воды и смесь перемешивали при нагревании при 110°C в течение ночи. Смесь оставляли для охлаждения и затем к полученной смеси добавляли воду, осуществляли экстракцию этилацетатом, а затем сушили над безводным сульфатом магния и отгоняли растворитель. Полученный остаток подвергали очистке на колонке с силикагелем (н-гексан:этилацетат = 4:1) и полученные неочищенные кристаллы перекристаллизовывали из смеси этилацетата и диизопропилового эфира с получением, таким образом, 0,11 г белого порошкообразного 3-{2-[3-циклопропилметокси-4-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}-1-(3-метоксипиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,24 (1H, д, J=4,2 Гц), 7,55-7,47 (2H, м), 7,43 (1H, с), 7,40-7,35 (2H, м), 7,03 (1H, д, J=8,4 Гц), 4,46 (2H, кв, J=7,2 Гц), 3,94 (2H, д, J=6,6 Гц), 3,90 (3H, с), 3,51 (2H, д, J=7,2 Гц), 3,01 (2H, д, J=7,2 Гц), 1,31-1,26 (1H, м), 0,68-0,62 (2H, м), 0,39-0,34 (2H, м).
Пример 124
2 г метил 3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]пропионата, полученного в ссылочном примере 48, и 1,1 г метил 3-метоксипиколината растворяли в 10 мл диметилформамида и при одновременном перемешивании при охлаждении льдом к смеси добавляли 1,81 г раствора трет-пентоксида натрия и перемешивали в течение 30 минут. Смесь снова перемешивали в течение 5 часов при комнатной температуре, к реакционной смеси добавляли лед с последующим добавлением насыщенного водного раствора хлорида аммония и продолжали перемешивание смеси. После перемешивания реакционной смеси в течение 30 минут к смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой и концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 1:1) с получением, таким образом, 1,55 г белого аморфного метил 2-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-3-(3-метоксипиридин-2-ил)-3-оксопропионата.
1Н-ЯМР (CDCl3) δ: 8,24 (1H, дд, J=4,5, 1,8 Гц), 7,57-7,28 (10H, м), 6,91 (1H, д, J=9,0 Гц), 5,18-5,13 (3H, м), 3,91-3,90 (6H, м), 3,64 (3H, с), 3,36-3,18 (2H, м).
Пример 125
1,5 г метил 2-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-3-(3-метоксипиридин-2-ил)-3-оксопропионата, полученного в примере 124, растворяли в 22,5 мл этанола, к смеси добавляли 7,5 мл 47%-ной бромистоводородной кислоты и смесь перемешивали при нагревании при 80°C в течение 7,5 часов. При одновременном перемешивании при охлаждении льдом реакционную смесь нейтрализовали с использованием 5н. раствора гидроксида натрия и осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой и концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (дихлорметан:метанол = 20:1) с получением, таким образом, 0,65 г бледно-желтого маслянистого вещества, 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-3-(3-метоксипиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,24 (1H, дд, J=7,2, 1,5 Гц), 7,55-7,27 (5H, м), 6,88 (1H, д, J=8,7 Гц), 5,72 (1H, с), 3,92-3,89 (6H, м), 3,51 (2H, т, J=7,5 Гц), 3,03 (2H, т, J=7,5 Гц).
Пример 126
Используя 0,24 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-3-(3-метоксипиридин-2-ил)пропан-1-она, полученного в примере 125, 0,11 г белого порошкообразного 3-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]-3-(3-метоксипиридин-2-ил)пропан-1-она получали таким же способом, как в примере 102.
1Н-ЯМР (CDCl3) δ: 8,24 (1H, дд, J=4,2, 1,2 Гц), 7,59-7,32 (5H, м), 6,91 (1H, д, J=8,4 Гц), 3,94-3,90 (8H, м), 3,51 (2H, т, J=7,2 Гц), 3,01 (2H, т, J=7,2 Гц), 1,40-1,30 (1H, м), 0,69-0,62 (2H, м), 0,41-0,35 (2H, м).
Используя 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-3-(3-метоксипиридин-2-ил)пропан-1-он, полученный в примере 125, соединения примеров 127 и 128 получали таким же способом, как в примере 102.
Пример 127
3-[2-(3-изобутокси-4-метоксифенил)оксазол-4-ил]-3-(3-метоксипиридин-2-ил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 8,24 (1H, дд, J=4,2, 1,5 Гц), 7,58-7,30 (5H, м), 6,91 (1H, д, J=8,4 Гц), 3,92-3,90 (6H, м), 3,84 (2H, д, J=6,9 Гц), 3,52 (2H, т, J=7,2 Гц), 3,01 (2H, т, J=7,2 Гц), 2,20 (1H, кв, J=6,9 Гц), 1,06 (6H, д, J=6,9 Гц).
Пример 128
3-[2-(3-циклопентилокси-4-метоксифенил)оксазол-4-ил]-1-(3-метоксипиридин-2-ил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 8,24 (1H, дд, J=4,5, 1,5 Гц), 7,60-7,30 (5H, м), 6,90 (1H, д, J=8,7 Гц), 4,90-4,85 (1H, м), 3,90-3,88 (6H, м), 3,51 (2H, д, J=6,9 Гц), 3,01 (2H, т, J=6,9 Гц), 2,00-1,81 (6H, м), 1,64-1,60 (2H, м).
Пример 129
Используя 0,15 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-3-(3-метоксипиридин-2-ил)пропан-1-она, полученного в примере 125, 44 мг белого порошкообразного 1-(3-метоксипиридин-2-ил)-3-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}пропан-1-она получали таким же способом, как в примере 111.
1Н-ЯМР (CDCl3) δ: 8,24 (1H, дд, J=4,2, 1,2 Гц), 7,70 (1H, дд, J=8,4, 1,8 Гц), 7,60 (1H, д, J=1,8 Гц), 7,51 (1H, д, J=1,8 Гц), 7,47-7,32 (2H, м), 6,96 (1H, д, J=8,4 Гц), 4,45 (2H, кв, J=8,4 Гц), 3,95-3,88 (6H, м), 3,52 (2H, т, J=7,2 Гц), 3,01 (2H, т, J=7,2 Гц).
Пример 130
2 г метил 3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]пропионата, полученного в ссылочном примере 48, и 1 г метил 3-этоксипиколината растворяли в 10 мл диметилформамида и при одновременном перемешивании к смеси добавляли раствор 1,81 г трет-пентоксида натрия при охлаждении льдом и перемешивали в течение 30 минут. Смесь снова перемешивали в течение 4 часов при комнатной температуре и к реакционной смеси добавляли лед с последующим добавлением насыщенного водного раствора хлорида аммония для дальнейшего перемешивания. После перемешивания реакционной смеси в течение 30 минут к смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой и концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 1:1) с получением, таким образом, 1,5 г бесцветного маслянистого вещества метил 2-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-3-(3-этоксипиридин-2-ил)-3-оксопропионата.
1Н-ЯМР (CDCl3) δ: 8,22 (1H, дд, J=4,2, 1,2 Гц), 7,57-7,27 (10H, м), 6,91 (1H, д, J=9,0 Гц), 5,18-5,12 (3H, м), 4,12 (2H, кв, J=6,9 Гц), 3,92 (3H, с), 3,65 (3H, с), 3,30-3,23 (2H, м), 1,46 (3H, т, J=6,9 Гц).
Пример 131
Используя 1,5 г метил 2-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-3-(3-этоксипиридин-2-ил)-3-оксопропионата, полученного в примере 130, 0,7 г бледно-желтого маслянистого вещества, 1-(3-этоксипиридин-2-ил)-3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]пропан-1-она получали таким же способом, как в примере 125.
1Н-ЯМР (CDCl3) δ: 8,23 (1H, дд, J=4,2, 1,2 Гц), 7,55-7,49 (2H, м), 7,45 (1H, с), 7,42-7,28 (2H, м), 6,88 (1H, д, J=8,7 Гц), 5,70 (1H, с), 4,11 (2H, кв, J=6,9 Гц), 3,49 (2H, т, J=7,2 Гц), 3,01 (2H, т, J=6,9 Гц), 1,46 (3H, т, J=6,9 Гц).
Пример 132
Используя 0,2 г 1-(3-этоксипиридин-2-ил)-3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]пропан-1-она, полученного в примере 131, 0,2 г бледно-желтого маслянистого вещества, 3-[2-(3-циклопентилокси-4-метоксифенил)оксазол-4-ил]-1-(3-этоксипиридин-2-ил)пропан-1-он получали таким же способом, как в примере 102.
1Н-ЯМР (CDCl3) δ: 8,23 (1H, дд, J=4,5, 1,5 Гц), 7,57-7,45 (2H, м), 7,44 (1H, д, J=0,9 Гц), 7,38-7,28 (2H, м), 6,89 (1H, д, J=8,7 Гц), 4,89-4,87 (1H, м), 4,12 (2H, кв, J=6,9 Гц), 3,94-3,91 (5H, м), 3,88 (3H, с), 3,49 (2H, т, J=7,2 Гц), 3,01 (2H, т, J=7,2 Гц), 2,01-1,81 (6H, м), 1,65-1,58 (2H, м), 1,47 (3H, т, J=6,9 Гц).
Используя 1-(3-этоксипиридин-2-ил)-3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]пропан-1-он, полученный в примере 131, соединения примеров 133 и 134 получали таким же способом, как в примере 102.
Пример 133
3-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]-1-(3-этоксипиридин-2-ил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 8,23 (1H, дд, J=4,2, 1,5 Гц), 7,57 (1H, дд, J=8,4, 1,8 Гц), 7,50 (1H, д, J=1,8 Гц), 7,45 (1H, д, J=1,8 Гц), 7,38-7,28 (2H, м), 6,91 (1H, д, J=8,4 Гц), 4,12 (2H, кв, J=6,9 Гц), 3,94-3,91 (5H, м), 3,49 (2H, т, J=7,2 Гц), 3,02 (2H, т, J=7,2 Гц), 1,46 (3H, т, J=6,9 Гц), 1,42-1,32 (1H, м), 0,69-0,62 (2H, м), 0,40-0,35 (2H, м).
Пример 134
1-(3-этоксипиридин-2-ил)-3-[2-(3-изобутокси-4-метоксифенил)оксазол-4-ил]пропан-1-он
1Н-ЯМР (CDCl3) δ: 8,23 (1H, дд, J=4,5, 1,5 Гц), 7,56 (1H, дд, J=8,4, 2,1 Гц), 7,50 (1H, д, J=2,1 Гц), 7,45 (1H, с), 7,38-7,28 (2H, м), 6,90 (1H, д, J=8,4 Гц), 4,12 (2H, кв, J=6,9 Гц), 3,90 (3H, с), 3,85 (2H, д, J=6,6 Гц), 3,50 (2H, т, J=6,9 Гц), 3,02 (2H, т, J=6,9 Гц), 2,19 (2H, кв.т, J=6,6 Гц), 1,47 (3H, т, J=6,9 Гц), 1,05 (6H, д, J=6,6 Гц).
Пример 135
5 г метил 3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]пропионата, полученного в ссылочном примере 48, и 3,2 г метил 3-метилпиколината растворяли в 150 мл диметоксиэтана. При одновременном перемешивании раствора при охлаждении льдом к смеси добавляли 1,2 г гидрида натрия и продолжали перемешивание. Реакционную смесь нагревали и кипятили с обратным холодильником в течение 4 часов. По завершении реакции к смеси добавляли насыщенный водный раствор хлорида аммония при одновременном перемешивании при охлаждении льдом и продолжали перемешивание смеси. После перемешивания реакционной смеси в течение 30 минут к смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой и концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 2:1) с получением, таким образом, 5,5 г бесцветного маслянистого вещества метил 2-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-3-(3-метилпиридин-2-ил)-3-оксопропионата.
1Н-ЯМР (CDCl3) δ: 8,49 (1H, дд, J=4,8, 1,2 Гц), 7,59-7,28 (10H, м), 6,91 (1H, д, J=9,0 Гц), 5,23-5,16 (3H, м), 3,91 (3H, с), 3,65 (3H, с), 3,37-3,18 (2H, м,) 2,59 (3H, с).
Пример 136
5,5 г метил 2-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-3-(3-метилпиридин-2-ил)-3-оксопропионата, полученного в примере 135, растворяли в 20 мл этанола, к смеси добавляли 80 мл 5н. водного раствора хлористоводородной кислоты и смесь перемешивали при нагревании при 80°C в течение 1,5 часов. При одновременном перемешивании и при охлаждении льдом реакционную смесь нейтрализовали с использованием 5н. водного раствора гидроксида натрия и осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой, концентрировали при пониженном давлении и полученные неочищенные кристаллы перекристаллизовывали с использованием смеси 20 мл этанола и 40 мл н-гексана с получением, таким образом, 1,92 г бледно-желтого порошкообразного 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,49 (1H, дд, J=4,5, 1,2 Гц), 7,60-7,51 (3H, м), 7,44 (1H, д, J=0,9 Гц), 7,41-7,29 (1H, м), 6,89 (1H, дд, J=7,8, 1,2 Гц), 5,68 (1H, с), 3,93 (3H, с), 3,58 (2H, т, J=7,5 Гц), 3,00 (2H, т, J=7,5 Гц), 2,57 (3H, с).
Пример 137
0,3 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она, полученного в примере 136, и 0,4 мл 1,8-диазабицикло[5.4.0]ундец-7-ена растворяли в 5 мл этанола, к смеси добавляли 0,24 г (бромметил)циклопропана и смесь нагревали и кипятили с обратным холодильником в течение 4,5 часов. Смесь оставляли для охлаждения и затем к реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Экстракт дважды промывали водой, органический слой затем концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 2:1) с получением, таким образом, 0,2 г белого порошкообразного 3-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,5, 1,2 Гц), 7,60-7,54 (2H, м), 7,49 (1H, д, J=1,8 Гц), 7,45 (1H, с), 7,34-7,29 (1H, м), 6,91 (1H, д, J=8,7 Гц), 3,94-3,91 (5H, м), 3,60 (2H, т, J=7,5 Гц), 3,00 (2H, т, J=7,5 Гц), 2,57 (3H, с), 1,40-1,32 (1H, м), 0,69-0,62 (2H, м), 0,41-0,35 (2H, м).
Пример 138
0,23 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она, полученного в примере 136, и 0,3 мл 1,8-диазабицикло[5.4.0]ундец-7-ена растворяли в 5 мл этанола, к смеси добавляли 0,21 г этилиодида и смесь нагревали и кипятили с обратным холодильником в течение 4 часов. Смесь оставляли для охлаждения и затем к реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Экстракт дважды промывали водой, органический слой затем концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 2:1) с получением, таким образом, 0,17 г белого порошкообразного 3-[2-(3-этокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,24 (1H, д, J=4,2 Гц), 7,58-7,55 (2H, м), 7,51 (1H, д, J=2,1 Гц), 7,45 (1H, с), 6,90 (1H, д, J=8,4 Гц), 4,19 (2H, кв, J=7,2 Гц), 3,91 (3H, с), 3,59 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 2,57 (3H, с), 1,49 (3H, т, J=7,2 Гц).
Пример 139
0,3 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она, полученного в примере 136, и 0,4 мл 1,8-диазабицикло[5.4.0]ундец-7-ена растворяли в 5 мл этанола, к смеси добавляли 0,23 г 2-бромпропана и смесь нагревали и кипятили с обратным холодильником в течение 4,5 часов. Смесь оставляли для охлаждения, затем к реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Экстракт дважды промывали водой, органический слой затем концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 2:1) с получением, таким образом, 0,16 г белого порошкообразного 3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,5, 1,2 Гц), 7,59-7,53 (3H, м), 7,45 (1H, с), 7,34-7,31 (1H, м), 6,91 (1H, д, J=8,7 Гц), 4,65 (1H, септ., J=6,0 Гц), 3,89 (3H, с), 3,59 (2H, т, J=7,5 Гц), 3,00 (2H, т, J=7,5 Гц), 2,62 (3H, с), 1,39 (6H, д, J=6,0 Гц).
Пример 140
0,3 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она, полученного в примере 136, и 0,3 мл 1,8-диазабицикло[5.4.0]ундец-7-ена растворяли в 6 мл этанола, к смеси добавляли 0,22 г аллилбромида и смесь нагревали и кипятили с обратным холодильником в течение 4 часов. Смесь оставляли для охлаждения и затем к реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Экстракт дважды промывали водой, органический слой затем концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 2:1) с получением, таким образом, 0,18 г белого порошкообразного 3-[2-(3-аллилокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,51-8,48 (1H, м), 7,60-7,56 (2H, м), 7,52 (1H, д, J=2,1 Гц), 7,45 (1H, с), 7,34-7,29 (1H, м), 6,92 (1H, д, J=8,7 Гц), 6,16-6,05 (1H, м), 5,48-5,28 (2H, м), 4,69-4,66 (2H, м), 3,92 (3H, с), 3,60 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 2,57 (3H, с).
Пример 141
0,15 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она, полученного в примере 136, и 0,15 мл 1,8-диазабицикло[5.4.0]ундец-7-ена растворяли в 5 мл этанола, к смеси добавляли 0,13 г (бромметил)циклобутана и смесь нагревали и кипятили с обратным холодильником в течение ночи. Смесь оставляли для охлаждения и затем к реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Экстракт дважды промывали водой, органический слой затем концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 2:1) с получением, таким образом, 90 мг белого порошкообразного 3-[2-(3-циклобутилметокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,5, 1,2 Гц), 7,60-7,51 (3H, м), 7,45 (1H, д, J=2,1 Гц), 7,34-7,29 (1H, м), 6,89 (1H, д, J=8,7 Гц), 4,07 (2H, д, J=6,9 Гц), 3,89 (3H, с), 3,60 (2H, т, J=7,5 Гц), 3,01 (2H, т, J=7,5 Гц), 2,89-2,83 (1H, м), 2,57 (3H, с), 2,22-2,13 (2H, м), 2,00-1,84 (4H, м).
Используя 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он, полученный в примере 136, соединения примеров 142-154 получали таким же способом, как в примере 137.
Пример 142
3-[2-(3-изобутокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,5, 1,2 Гц), 7,60-7,53 (2H, м), 7,50 (1H, д, J=1,8 Гц), 7,45 (1H, с), 7,34-7,28 (1H, м), 6,90 (1H, д, J=8,4 Гц), 3,90 (3H, с), 3,84 (2H, д, J=6,9 Гц), 3,60 (2H, т, J=7,8 Гц), 3,01 (2H, т, J=7,8 Гц), 2,57 (3H, с), 2,20 (1H, кв.т, J=6,9 Гц), 1,05 (6H, д, J=6,9 Гц).
Пример 143
3-[2-(4-метокси-3-пропоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,5, 1,2 Гц), 7,59-7,54 (2H, м), 7,51 (1H, д, J=1,8 Гц), 7,50 (1H, с), 7,34-7,29 (1H, м), 6,90 (1H, д, J=8,4 Гц), 4,05 (2H, т, J=6,9 Гц), 3,91 (3H, с), 3,60 (2H, т, J=7,5 Гц), 3,01 (2H, т, J=7,5 Гц), 2,57 (3H, с), 1,90 (2H, кв.т, J=6,9 Гц), 1,24 (3H, т, J=6,9 Гц).
Пример 144
3-[2-(3-циклопентилокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,5, 1,2 Гц), 7,59-7,50 (3H, м), 7,44 (1H, д, J=1,2 Гц), 7,34-7,31 (1H, м), 6,89 (1H, д, J=8,4 Гц), 4,90-4,84 (1H, м), 3,88 (3H, с), 3,59 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 2,57 (3H, с), 2,03-1,80 (6H, м), 1,64-1,58 (2H, м).
Пример 145
3-[2-(4-метокси-3-(2-пропенилокси)фенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 8,50 (1H, д, J=4,5 Гц), 7,67-7,63 (2H, м), 7,58 (1H, д, J=8,1 Гц), 7,46 (1H, с), 7,34-7,30 (1H, м), 6,93 (1H, дд, J=6,6, 2,4 Гц), 4,82 (2H, д, J=2,4 Гц), 3,92 (3H, с), 3,60 (2H, т, J=7,2 Гц), 3,01 (2H, т, J=7,2 Гц), 2,58 (3H, с), 2,53 (1H, т, J=2,4 Гц).
Пример 146
3-[2-(3-(3-бутенилокси)-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,2, 1,5 Гц), 7,59-7,55 (2H, м), 7,52 (1H, д, J=2,1 Гц), 7,45 (1H, д, J=2,1 Гц), 7,34-7,29 (1H, м), 5,97-5,85 (1H, м), 5,23-5,09 (2H, м), 4,14 (2H, т, J=6,9 Гц), 3,91 (3H, с), 3,60 (2H, т, J=7,5 Гц), 3,00 (2H, т, J=7,5 Гц), 2,68-2,57 (5H, м).
Пример 147
3-[2-(3-бутокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 8,50 (1H, д, J=4,8 Гц), 7,59-7,51 (3H, м), 7,45 (1H, с), 7,34-7,30 (1H, м), 6,90 (1H, д, J=8,7 Гц), 4,09 (2H, т, J=6,6 Гц), 3,90 (3H, с), 3,60 (2H, т, J=7,2 Гц), 3,01 (2H, т, J=7,2 Гц), 2,57 (3H, с), 1,86 (2H, тд, J=7,2, 6,6 Гц), 1,56-1,45 (2H, м), 0,99 (3H, т, J=7,2 Гц).
Пример 148
3-[2-(3-циклогексилметокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 8,50 (1H, д, J=4,5 Гц), 7,61-7,53 (2H, м), 7,49 (1H, д, J=1,8 Гц), 7,45 (1H, с), 7,34-7,28 (1H, м), 6,89 (1H, д, J=8,7 Гц), 3,90-3,86 (5H, м), 3,60 (2H, т, J=7,5 Гц), 3,01 (2H, т, J=7,5 Гц), 2,57 (3H, с), 1,94-1,85 (3H, м), 1,79-1,57 (3H, м), 1,38-0,88 (5H, м).
Пример 149
3-[2-(4-метокси-3-(4-пентенилокси)фенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,5, 1,2 Гц), 7,59-7,54 (2H, м), 7,51 (1H, д, J=2,1 Гц), 7,45 (1H, с), 7,34-7,29 (1H, м), 6,91 (1H, д, J=8,4 Гц), 5,91-5,80 (1H, м), 5,11-4,97 (2H, м), 4,10 (2H, д, J=6,6 Гц), 3,91 (3H, с), 3,60 (2H, т, J=7,5 Гц), 3,01 (2H, т, J=7,5 Гц), 2,57 (3H, с), 2,30-2,22 (2H, м), 2,05-1,92 (2H, м).
Пример 150
3-[2-(4-метокси-3-фенэтилоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 8,48 (1H, дд, J=4,5, 0,9 Гц), 7,60-7,49 (3H, м), 7,43 (1H, с), 7,35-7,20 (6H, м), 6,91 (1H, д, J=8,7 Гц), 4,27 (2H, т, J=7,5 Гц), 3,91 (3H, с), 3,58 (2H, т, J=7,2 Гц), 3,19 (2H, т, J=7,5 Гц), 3,00 (2H, т, J=7,2 Гц), 2,55 (3H, с).
Пример 151
3-{2-[4-метокси-3-(3-фенилпропокси)фенил]оксазол-4-ил}-1-(3-метилпиридин-2-ил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,5, 1,2 Гц), 7,58 (1H, д, J=2,1 Гц), 7,55 (1H, д, J=2,1 Гц), 7,49 (1H, д, J=2,1 Гц), 7,44 (1H, с), 7,34-7,15 (6H, м), 6,91 (1H, д, J=8,4 Гц), 4,11 (2H, т, J=6,6 Гц), 3,92 (3H, с), 3,60 (2H, т, J=7,5 Гц), 3,00 (2H, т, J=7,5 Гц), 2,84 (2H, т, J=7,5 Гц), 2,57 (3H, с), 2,20 (2H, тт, J=7,5, 6,6 Гц).
Пример 152
Используя 0,5 г циклопентилметилметансульфоната, полученного в ссылочном примере 52, и 0,2 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она, полученного в примере 136, 90 мг белого порошкообразного 3-[2-(3-циклопентилметокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он получали таким же способом, как в примере 137.
1Н-ЯМР (CDCl3) δ: 8,49 (1H, д, J=3,9 Гц), 7,59-7,50 (3H, м), 7,45 (1H, с), 7,34-7,29 (1H, м), 6,90 (1H, д, J=8,4 Гц), 3,95 (2H, д, J=7,2 Гц), 3,90 (3H, с), 3,60 (2H, т, J=7,5 Гц), 3,01 (2H, т, J=7,5 Гц), 2,57 (3H, с), 2,54-2,41 (1H, м), 1,91-1,82 (2H, м), 1,68-1,56 (4H, м), 1,42-1,24 (2H, м).
Пример 153
Используя 0,16 г 2-циклопропилэтилметансульфоната, полученного в ссылочном примере 50, и 0,15 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она, полученного в примере 136, 0,1 г белого порошкообразного 3-{2-[3-(2-циклопропилэтокси)-4-метоксифенил]оксазол-4-ил}-1-(3-метилпиридин-2-ил)пропан-1-она получали таким же способом, как в примере 137.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,5, 1,5 Гц), 7,60-7,54 (3H, м), 7,46 (1H, с), 7,35-7,27 (1H, м), 6,91 (1H, д, J=8,1 Гц), 4,18 (2H, т, J=6,9 Гц), 3,91 (3H, с), 3,61 (2H, т, J=7,5 Гц), 3,02 (2H, т, J=7,5 Гц), 2,58 (3H, с), 1,78 (2H, кв, J=6,9 Гц), 0,91-0,80 (1H, м), 0,53-0,46 (2H, м), 0,16-0,11 (2H, м).
Пример 154
Используя 0,19 г 2-циклопентилэтилметансульфоната, полученного в ссылочном примере 51, и 0,15 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она, полученного в примере 136, 0,13 г белого порошкообразного 3-{2-[3-(2-циклопентилэтокси)-4-метоксифенил]оксазол-4-ил}-1-(3-метилпиридин-2-ил)пропан-1-она получали таким же способом, как в примере 137.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,5, 1,2 Гц), 7,60-7,50 (3H, м), 7,45 (1H, с), 7,34-7,30 (1H, м), 6,90 (1H, д, J=8,4 Гц), 4,10 (2H, т, J=6,9 Гц), 3,92 (3H, с), 3,60 (2H, т, J=7,5 Гц), 3,01 (2H, т, J=7,5 Гц), 2,57 (3H, с), 2,01-1,79 (5H, м), 1,67-1,50 (5H, м), 1,24-1,12 (2H, м).
Пример 155
0,23 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она, полученного в примере 136, и 0,28 г карбоната калия растворяли в 5 мл диметилформамида. К смеси добавляли 0,29 г 1,1,1-трифтор-2-йодэтана и смесь перемешивали при нагревании при 80°C в течение ночи. Реакционной смеси давали охладиться, затем к смеси добавляли воду и осуществляли экстракцию этилацетатом. Смесь два раза промывали водой и затем органический слой концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (дихлорметан:этилацетат = 1:1) с получением 0,14 г белого порошкообразного 3-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}-1-(3-метилпиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,5, 0,9 Гц), 7,70 (1H, дд, J=8,4, 2,1 Гц), 7,60-7,56 (2H, м), 7,46 (1H, д, J=2,1 Гц), 7,35-7,30 (1H, м), 6,96 (1H, д, J=8,4 Гц), 4,45 (2H, кв, J=8,4 Гц), 3,92 (3H, с), 3,60 (2H, т, J=7,5 Гц), 3,00 (2H, т, J=7,5 Гц), 2,57 (3H, с).
Пример 156
Используя 0,1 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она, полученного в примере 136, 45 мг бледно-желтого порошкообразного 3-{2-[4-метокси-3-(3-метил-2-бутенилокси)фенил]оксазол-4-ил}-1-(3-метилпиридин-2-ил)пропан-1-она получали таким же способом, как в примере 155.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,5, 1,2 Гц), 7,59-7,52 (3H, м), 7,45 (1H, с), 7,34-7,29 (1H, м), 6,90 (1H, д, J=8,4 Гц), 5,58-5,52 (1H, м), 4,64 (2H, д, J=6,9 Гц), 3,91 (3H, с), 3,60 (2H, т, J=7,5 Гц), 3,01 (2H, т, J=7,5 Гц), 2,57 (3H, с), 1,78 (3H, д, J=0,9 Гц), 1,77 (3H, с).
Пример 157
Используя 0,6 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она, полученного в примере 136, 0,31 г белого порошкообразного 3-{2-[3-(2-циклогексенилокси)-4-метоксифенил]оксазол-4-ил}-1-(3-метилпиридин-2-ил)пропан-1-он получали таким же способом, как в примере 155.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,5, 1,2 Гц), 7,60-7,56 (3H, м), 7,45 (1H, с), 7,34-7,29 (1H, м), 6,91 (1H, д, J=9,0 Гц), 5,99-5,88 (2H, м), 4,88 (1H, ушир.с), 3,89 (3H, с), 3,60 (2H, т, J=7,2 Гц), 3,01 (2H, т, J=7,2 Гц), 2,57 (3H, с), 2,17-1,84 (5H, м), 1,71-1,61 (1H, м).
Пример 158
0,3 г 3-{2-[3-(2-циклогексенилокси)-4-метоксифенил]оксазол-4-ил}-1-(3-метилпиридин-2-ил)пропан-1-она, полученного в примере 157, растворяли в 20 мл этанола. К смеси добавляли 50 мг 10% палладия-на-углероде в виде порошка и смесь перемешивали при комнатной температуре в течение 2 часов. Катализатор удаляли при помощи фильтрации и фильтрат затем концентрировали. Полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1) с получением 0,2 г бледно-желтого маслянистого 3-[2-(3-циклогексилокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, д, J=4,5 Гц), 7,59-7,54 (3H, м), 7,45 (1H, с), 7,34-7,30 (1H, м), 6,91 (1H, д, J=8,1 Гц), 4,35-4,25 (1H, м), 3,89 (3H, с), 3,60 (2H, т, J=7,5 Гц), 3,01 (2H, т, J=7,5 Гц), 2,57 (3H, с), 2,07-2,02 (2H, м), 1,84-1,80 (2H, м), 1,60-1,51 (4H, м), 1,43-1,23 (2H, м).
Пример 159
0,26 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она, полученного в примере 136, растворяли в 10 мл тетрагидрофурана. К полученному раствору добавляли 0,2 г 2-гидроксииндана, 0,75 мл диизопропилазодикарбоксилата (40%-ный раствор в толуоле) и 0,31 г три(н-бутил)фосфина и смесь перемешивали при 50°C. Через 3 часа к смеси снова добавляли 0,2 г 2-гидроксииндана, 0,75 мл диизопропилазодикарбоксилата (40%-ный раствор в толуоле) и 0,31 г три(н-бутил)фосфина и смесь перемешивали при 50°C в течение ночи. Реакционную смесь концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат:дихлорметан = 1:1:1) и перекристаллизовывали из смеси ацетон/диизопропиловый эфир с получением 0,13 г бесцветного порошкообразного 3-{2-[3-(индан-2-илокси)-4-метоксифенил]оксазол-4-ил}-1-(3-метилпиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,51 (1H, ушир.д, J=4,8 Гц), 7,62-7,16 (9H, м), 6,91 (1H, д, J=8,7 Гц), 5,29 (1H, тт, J=6,6, 3,9 Гц), 3,85 (3H, с), 3,63 (2H, т, J=7,2 Гц), 3,45 (2H, дд, J=16,8, 6,6 Гц), 3,26 (2H, дд, J=16,8, 3,9 Гц), 3,01 (2H, т, J=7,2 Гц), 2,58 (3H, с).
Пример 160
2 г метил 3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]пропионата, полученного в ссылочном примере 48, и 1,5 г метилпиколината растворяли в 40 мл диметоксиэтана. К смеси добавляли 0,33 г гидрида натрия при охлаждении льдом и перемешивании и перемешивание продолжали. Реакционную смесь нагревали и кипятили с обратным холодильником в течение 2 часов. По завершении реакции к смеси добавляли насыщенный водный раствор хлорида аммония при охлаждении льдом и перемешивании и смесь перемешивали. Реакционную смесь перемешивали в течение 30 минут, затем к смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой и концентрировали путем удаления растворителя при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1) с получением 2 г бесцветного маслянистого метил 2-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-3-оксо-3-пиридин-2-илпропионата.
1Н-ЯМР (CDCl3) δ: 8,67 (1H, дд, J=4,2, 0,9 Гц), 8,07 (1H, дд, J=7,8, 2,1 Гц), 7,83 (1H, тд, J=7,8, 1,8 Гц), 7,55-7,30 (9H, м), 6,90 (1H, д, J=9,0 Гц), 5,29 (1H, т, J=7,8 Гц), 5,16 (2H, с), 3,91 (3H, с), 3,66 (3H, с), 3,36-3,28 (2H, м).
Пример 161
Используя 2 г метил 2-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-3-оксо-3-(пиридин-2-ил)пропионат, полученный в примере 160, 0,48 г белого порошкообразного 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(пиридин-2-ил)пропан-1-она получали таким же способом, как в примере 136.
1Н-ЯМР (CDCl3) δ: 8,67 (1H, дд, J=4,2, 0,9 Гц), 8,05 (1H, дд, J=7,8, 2,1 Гц), 7,83 (1H, тд, J=7,8, 1,8 Гц), 7,55-7,43 (4H, м), 6,88 (1H, дд, J=7,8, 2,1 Гц), 5,72 (1H, с), 3,93 (3H, с), 3,64 (2H, т, J=7,5 Гц), 3,03 (2H, т, J=7,5 Гц).
Пример 162
0,15 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(пиридин-2-ил)пропан-1-она, полученного в примере 161, и 0,2 мл 1,8-диазабицикло[5.4.0]ундец-7-ена растворяли в 5 мл этанола. К смеси добавляли 0,14 г (бромметил)циклобутана и смесь нагревали и кипятили с обратным холодильником в течение ночи. Реакционной смеси давали охладиться, затем к смеси добавляли воду и осуществляли экстракцию этилацетатом. Смесь два раза промывали водой и затем органический слой концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (дихлорметан:этилацетат = 5:1) с получением 50 мг белого порошкообразного 3-[2-(3-циклобутилметокси-4-метоксифенил)оксазол-4-ил]-1-(пиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,68 (1H, д, J=4,5 Гц), 8,05 (1H, д, J=7,8 Гц), 7,83 (1H, тд, J=7,8, 1,8 Гц), 7,58-7,44 (4H, м), 6,90 (1H, д, J=8,4 Гц), 4,07 (2H, д, J=6,9 Гц), 3,89 (3H, с), 3,65 (2H, т, J=7,5 Гц), 3,05 (2H, т, J=7,5 Гц), 2,94-2,81 (1H, м), 2,24-2,04 (2H, м), 2,00-1,81 (4H, м).
Пример 163
Используя 0,3 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(пиридин-2-ил)пропан-1-она, полученного в примере 161, 0,28 г белого порошкообразного 3-[2-(4-метокси-3-(4-пентенилокси)фенил)оксазол-4-ил]-1-(пиридин-2-ил)пропан-1-она получали таким же способом, как в примере 102.
1Н-ЯМР (CDCl3) δ: 8,69 (1H, дд, J=4,2, 1,5 Гц), 8,05 (1H, д, J=7,8 Гц), 7,85 (1H, т, J=7,8 Гц), 7,60-7,46 (4H, м), 6,91 (1H, д, J=8,4 Гц), 5,92-5,83 (1H, м), 5,11-4,99 (2H, м), 4,11 (2H, д, J=6,9 Гц), 3,91 (3H, с), 3,65 (2H, т, J=7,5 Гц), 3,05 (2H, т, J=7,5 Гц), 2,28-2,23 (2H, м), 1,98 (2H, т, J=7,5 Гц).
Пример 164
10 г 2-(3-бензилокси-4-метоксифенил)-4-хлорметилоксазола, полученного в ссылочном примере 5, и 10,7 г 1-(2-аллилоксифенил)этанона, полученного в ссылочном примере 53, растворяли в 200 мл тетрагидрофурана. К смеси добавляли 1,82 г гидрида натрия при охлаждении льдом и перемешивании и продолжали перемешивание. Реакционную смесь нагревали и кипятили с обратным холодильником в течение 4 часов. По завершении реакции к смеси добавляли насыщенный водный раствор хлорида аммония при охлаждении льдом и перемешивании и смесь перемешивали. После перемешивания в течение 30 минут к смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой два раза промывали водой и концентрировали путем удаления растворителя при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1) с получением 1,4 г белого порошкообразного 1-(2-аллилоксифенил)-3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,8, 1,8 Гц), 7,62-7,58 (2H, м), 7,49-7,30 (7H, м), 7,02-6,91 (3H, м), 6,12-6,02 (1H, м), 5,42 (1H, дд, J=17,4, 1,5 Гц), 5,30 (1H, дд, J=10,5, 1,5 Гц), 5,19 (2H, с), 4,65-4,62 (2H, м), 3,92 (3H, с), 3,42 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц).
Пример 165
Используя 1,4 г 1-(2-аллилоксифенил)-3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]пропан-1-она, полученного в примере 164, 0,55 г бледно-желтого маслянистого 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-гидроксифенил)пропан-1-она получали таким же способом, как в примере 101.
1Н-ЯМР (CDCl3) δ: 12,5 (1H, с), 7,81 (1H, дд, J=7,8, 1,5 Гц), 7,57-7,30 (4H, м), 6,98 (1H, д, J=8,1 Гц), 6,92-6,86 (2H, м), 5,73 (1H, ушир.с), 3,94 (3H, с), 3,44 (2H, т, J=7,5 Гц), 3,02 (2H, т, J=7,5 Гц).
Пример 166
Используя 0,5 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-гидроксифенил)пропан-1-она, полученного в примере 165, 0,61 г белого порошкообразного 3-[2-(3-аллилокси-4-метоксифенил)оксазол-4-ил]-1-(2-аллилоксифенил)пропан-1-она получали таким же способом, как в примере 111.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 2,1 Гц), 7,58 (1H, дд, J=8,1, 2,1 Гц), 7,52 (1H, д, J=2,1 Гц), 7,45-7,40 (2H, м), 7,02-6,90 (3H, м), 6,16-6,03 (2H, м), 5,47-5,27 (4H, м), 4,68-4,62 (4H, м), 3,92 (3H, с), 3,42 (2H, т, J=6,9 Гц), 2,99 (2H, т, J=6,9 Гц).
Пример 167
Используя 1,1 г метил 3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]пропионата, полученного в ссылочном примере 48, 1 г желтого маслянистого метил 2-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-3-(2-метоксифенил)-3-оксопропионата получали таким же способом, как в примере 100.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, дд, J=7,8, 1,8 Гц), 7,57-7,53 (3H, м), 7,48-7,30 (6H, м), 6,97 (1H, т, J=7,2 Гц), 6,91 (2H, д, J=7,8 Гц), 5,17 (2H, с), 4,99 (1H, т, J=6,9 Гц), 3,92 (3H, с), 3,90 (3H, с), 3,69 (3H, с), 3,27-3,19 (2H, м).
Пример 168
Используя 1 г метил 2-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-3-(2-метоксифенил)-3-оксопропионата, полученного в примере 167, 0,63 г белого порошкообразного 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-метоксифенил)пропан-1-она получали таким же способом, как в примере 101.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=8,4, 2,1 Гц), 7,56-7,52 (2H, м), 7,44-7,41 (2H, м), 6,99-6,87 (3H, м), 3,95 (3H, с), 3,89 (3H, с), 3,38 (2H, т, J=7,2 Гц), 2,98 (2H, т, J=7,2 Гц).
Пример 169
Используя 0,22 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-метоксифенил)пропан-1-она, полученного в примере 168, 90 мг бесцветного маслянистого 3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]-1-(2-метоксифенил)пропан-1-она получали таким же способом, как в примере 102.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, д, J=7,5 Гц), 7,57 (1H, д, J=8,1 Гц), 7,54 (1H, с), 7,47-7,40 (2H, м), 7,01-6,89 (3H, м), 4,67-4,62 (1H, м), 3,91 (6H, с), 3,38 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,39 (6H, д, J=6,3 Гц).
Используя 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-метоксифенил)пропан-1-он, полученный в примере 168, соединения примеров 170-173 получали таким же способом, как в примере 102.
Пример 170
3-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]-1-(2-метоксифенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,69-7,40 (4H, м), 6,99-6,89 (4H, м), 3,94-3,89 (8H, м), 3,37 (2H, т, J=7,2 Гц), 3,01 (2H, т, J=7,2 Гц), 1,40-1,35 (1H, м), 0,67-0,65 (2H, м), 0,38-0,36 (2H, м).
Пример 171
3-[2-(3-циклопентилокси-4-метоксифенил)оксазол-4-ил]-1-(2-метоксифенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,56 (1H, дд, J=8,4, 2,1 Гц), 7,51 (1H, с), 7,43 (1H, тд, J=8,4, 1,8 Гц), 6,99-6,88 (3H, м), 4,48 (1H, ушир.с), 3,89 (3H, с), 3,88 (3H, с), 3,38 (2H, т, J=6,6 Гц), 2,98 (2H, т, J=6,6 Гц), 2,04-1,85 (4H, м), 1,63-1,55 (4H, м).
Пример 172
3-[2-(3-этокси-4-метоксифенил)оксазол-4-ил]-1-(2-метоксифенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,57 (1H, дд, J=8,1, 2,1 Гц), 7,51 (1H, д, J=1,8 Гц), 7,47-7,41 (2H, м), 7,01-6,89 (3H, м), 4,18 (2H, кв, J=7,8 Гц), 3,94 (3H, с), 3,90 (3H, с), 3,38 (2H, т, J=6,6 Гц), 2,99 (2H, т, J=6,6 Гц), 1,49 (3H, т, J=7,8 Гц).
Пример 173
3-[2-(3-изобутокси-4-метоксифенил)оксазол-4-ил]-1-(2-метоксифенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,58-7,36 (4H, м), 7,01-6,89 (3H, м), 3,90 (6H, с), 3,84 (2H, д, J=6,6 Гц), 3,38 (2H, т, J=6,9 Гц), 2,99 (2H, т, J=6,9 Гц), 2,22-2,10 (1H, м), 1,05 (6H, д, J=6,6 Гц).
Используя 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-метоксифенил)пропан-1-он, полученный в примере 168, соединения примеров 174-175 получали таким же способом, как в примере 111.
Пример 174
3-[2-(3-аллилокси-4-метоксифенил)оксазол-4-ил]-1-(2-метоксифенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,59 (1H, дд, J=8,4, 1,8 Гц), 7,52 (1H, д, J=1,8 Гц), 7,48-7,41 (2H, м), 7,02-6,90 (3H, м), 6,12-6,07 (1H, м), 5,43 (1H, дд, J=17, 1,5 Гц), 5,31 (1H, д, J=10 Гц), 4,68 (2H, д, J=5,4 Гц), 3,92 (3H, с), 3,90 (3H, с), 3,38 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц).
Пример 175
1-(2-метоксифенил)-3-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,69 (1H, дд, J=7,5, 1,8 Гц), 7,60 (1H, д, J=1,8 Гц), 7,48-7,42 (2H, м), 7,02-6,95 (3H, м), 4,43 (2H, кв, J=8,1 Гц), 3,92 (3H, с), 3,90 (3H, с), 3,38 (2H, т, J=6,9 Гц), 2,99 (2H, т, J=6,9 Гц).
Пример 176
0,4 г гидрида натрия суспендировали в 20 мл тетрагидрофурана и к смеси добавляли последовательно 1,13 г 1-(2-бензилокси)этанона и 1,46 г 4-хлорметил-2-(3-циклопропилметокси-4-метоксифенил)оксазола, полученного в ссылочном примере 11, при охлаждении льдом. Смесь перемешивали в течение 4 часов при нагревании и кипячении с обратным холодильником. К реакционной смеси добавляли насыщенный водный раствор хлорида аммония при охлаждении льдом. После перемешивания в течение 15 минут к смеси добавляли воду и осуществляли экстракцию этилацетатом. Осуществляли сушку с использованием безводного сульфата магния и растворитель удаляли. Очистку осуществляли с использованием колонки с силикагелем (н-гексан:этилацетат = 4:1) и полученное соединение растворяли в 12 мл этанола. Добавляли 35 мг 10% палладия-на-углероде в виде порошка и осуществляли перемешивание в атмосфере водорода в течение ночи. Катализатор удаляли при помощи фильтрации и полученный фильтрат концентрировали. Остаток очищали с использованием колонки с силикагелем (н-гексан:этилацетат = 4:1) с получением 0,43 г белого порошкообразного 3-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]-1-(2-гидроксифенил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 12,2 (1H, с), 7,83 (1H, д, J=1,5 Гц), 7,80-7,44 (4H, м), 7,00-6,87 (3H, м), 3,94-3,92 (5H, м), 3,44 (2H, т, J=7,2 Гц), 3,03 (2H, т, J=7,2 Гц), 1,37-1,26 (1H, м), 0,70-0,65 (2H, м), 0,41-0,37 (2H, м).
Пример 177
2 г 4-хлорметил-2-(3-циклопропилметокси-4-метоксифенил)оксазола, полученного в ссылочном примере 11, и 3,6 г 1-(2-аллилоксифенил)этанона, полученного в ссылочном примере 53, растворяли в 40 мл тетрагидрофурана. К смеси добавляли 0,55 г гидрида натрия при охлаждении льдом и перемешивании и смесь перемешивали. Реакционную смесь нагревали и кипятили с обратным холодильником в течение 6 часов. По завершении реакции добавляли насыщенный водный раствор хлорида аммония при охлаждении льдом и смесь перемешивали. Реакционную смесь перемешивали в течение 30 минут, затем к смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой два раза промывали водой и концентрировали путем удаления растворителя при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1) с получением 0,5 г порошкообразного 1-(2-аллилоксифенил)-3-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,8, 1,8 Гц), 7,57 (1H, дд, J=8,4, 2,1 Гц), 7,49 (1H, д, J=2,1 Гц), 7,45-7,39 (2H, м), 7,02-6,89 (3H, м), 6,09-6,02 (1H, м), 5,45-5,26 (2H, м), 4,65-4,62 (2H, м), 3,94-3,91 (5H, м), 3,42 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 1,45-1,35 (1H, м), 0,68-0,62 (2H, м), 0,40-0,36 (2H, м).
Пример 178
Используя 1,4 г 4-хлорметил-2-(3,4-диэтоксифенил)оксазола, полученного в ссылочном примере 35, и 0,88 г 1-(2-аллилоксифенил)этанона, полученного в ссылочном примере 53, 0,42 г белого порошкообразного 1-(2-аллилоксифенил)-3-[2-(3,4-диэтоксифенил)оксазол-4-ил]пропан-1-она получали таким же способом, как в примере 177.
1Н-ЯМР (CDCl3) δ: 7,69 (1H, дд, J=7,5, 2,1 Гц), 7,56-7,51 (2H, м), 7,45-7,39 (2H, м), 7,02-6,89 (3H, м), 6,14-6,01 (1H, м), 5,42 (1H, дд, J=17, 1,5 Гц), 5,29 (1H, дд, J=10,5, 1,5 Гц), 4,65-4,62 (2H, м), 4,20-4,10 (4H, м), 3,42 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 1,50 (6H, т, J=7,2 Гц).
Пример 179
Используя 0,31 г 1-(2-хлорфенил)этанона и 0,59 г 4-хлорметил-2-(3-циклопропилметокси-4-метоксифенил)оксазола, полученный в ссылочном примере 11, 0,11 г бесцветного маслянистого 1-(2-хлорфенил)-3-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]пропан-1-она получали таким же способом, как в примере 177.
1Н-ЯМР (CDCl3) δ: 7,60-7,55 (2H, м), 7,49-7,43 (2H, м), 7,40 (1H, с), 7,39-7,30 (2H, м), 6,91 (1H, д, J=8,7 Гц), 3,94-3,91 (5H, м), 3,36 (2H, т, J=6,9 Гц), 3,01 (2H, т, J=6,9 Гц), 1,37-1,29 (1H, м), 0,69-0,63 (2H, м), 0,40-0,37 (2H, м).
Пример 180
Используя 2 г метил 3-[2-(3,4-диэтоксифенил)оксазол-4-ил]пропионата, полученного в ссылочном примере 54, и 1,3 г этил 3-метилпиколината, 0,8 г желтого маслянистого метил 2-[2-(3,4-диэтоксифенил)оксазол-4-илметил]-3-(3-метилпиридин-2-ил)-3-оксопропионата получали таким же способом, как в примере 124,
1Н-ЯМР (CDCl3) δ: 8,50 (1H, м), 7,60-7,40 (4H, м), 7,30 (1H, м), 6,88 (1H, д, J=8,4 Гц), 5,20 (1H, т, J=7,2 Гц), 4,20-4,05 (4H, м), 2,99 (3H, с), 3,35-3,20 (2H, м), 2,59 (3H, с), 1,47 (3H, т, J=6,9 Гц), 1,47 (3H, т, J=6,9 Гц).
Пример 181
0,8 г метил 2-[2-(3,4-диэтоксифенил)оксазол-4-илметил]-3-(3-метилпиридин-2-ил)-3-оксопропионата, полученного в примере 180, добавляли к смеси 5 мл уксусной кислоты и 1,5 мл концентрированной хлористоводородной кислоты и полученную смесь перемешивали при 110°C в течение 4 часов. После охлаждения полученного раствора до комнатной температуры постепенно добавляли 30 мл этилацетата и 30 мл насыщенного раствора гидрокарбоната натрия при перемешивании и перемешивание затем продолжали. Органический слой сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат:н-гексан = 3:1) и затем перекристаллизовывали из смеси этилацетат/н-гексан с получением 0,28 г белого порошкообразного 3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,49 (1H, м), 7,60-7,50 (3H, м), 7,44 (1H, с), 7,32 (1H, м), 6,90 (1H, д, J=8,1 Гц), 4,17 (2H, кв, J=6,9 Гц), 4,13 (2H, кв, J=6,9 Гц), 3,51 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 2,57 (3H, с), 1,48 (3H, т, J=6,9 Гц), 1,47 (3H, т, J=6,9 Гц).
Пример 182
2 г метил 3-[2-(3,4-диэтоксифенил)оксазол-4-ил]пропионата, полученного в ссылочном примере 54, и 1,5 г этил 2-этоксибензоата растворяли в 10 мл диметилформамида. К смеси добавляли 1,81 г трет-пентоксида натрия при охлаждении льдом и перемешивании и смесь перемешивали в течение 30 минут. Реакционную смесь снова перемешивали при комнатной температуре в течение 5 часов и к смеси добавляли лед. К смеси добавляли насыщенный водный раствор хлорида аммония и смесь перемешивали. Реакционную смесь перемешивали в течение 30 минут, затем к смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой два раза промывали водой и концентрировали путем удаления растворителя при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 1:1). Полученное желтое маслянистое вещество добавляли к смеси 5 мл уксусной кислоты и 1,5 мл концентрированной хлористоводородной кислоты и полученную смесь перемешивали при 110°C в течение 4 часов. После охлаждения смеси до комнатной температуры постепенно добавляли 30 мл этилацетата и 30 мл насыщенного раствора гидрокарбоната натрия при перемешивании и перемешивание продолжали далее. Органический слой сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат:н-гексан = 3:1) и полученные неочищенные кристаллы перекристаллизовывали из смеси этилацетат/н-гексан с получением 0,46 г белого порошкообразного 3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 2,1 Гц), 7,60-7,50 (2H, м), 7,45-7,35 (2H, м), 7,00-6,80 (2H, м), 4,17 (2H, кв, J=7,2 Гц), 4,13 (2H, кв, J=7,2 Гц), 3,42 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 1,48 (3H, т, J=7,2 Гц), 1,48 (3H, т, J=7,2 Гц), 1,48 (3H, т, J=7,2 Гц).
Используя метил 3-[2-(3,4-диэтоксифенил)оксазол-4-ил]пропионат, полученный в ссылочном примере 54, соединения примеров 183-185 получали таким же способом, как в примере 182.
Пример 183
3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(3-этоксипиридин-2-ил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 8,23 (1H, дд, J=4,5, 1,2 Гц), 7,55-7,50 (2H, м), 7,40-7,25 (2H, м), 7,45 (1H, с), 6,90 (1H, д, J=8,1 Гц), 4,20-4,05 (6H, м), 3,49 (2H, т, J=7,2 Гц), 3,02 (2H, т, J=7,2 Гц), 1,47 (3H, т, J=7,2 Гц), 1,47 (3H, т, J=7,2 Гц), 1,46 (3H, т, J=7,2 Гц).
Пример 184
3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(3-этоксифенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 8,00-7,95 (2H, м), 7,60-7,50 (2H, м), 7,43 (1H, с), 6,95-6,85 (3H, м), 4,17 (2H, кв, J=7,2 Гц), 4,17 (2H, кв, J=7,2 Гц), 4,09 (2H, кв, J=7,2 Гц), 3,34 (2H, т, J=7,2 Гц), 3,01 (2H, т, J=7,2 Гц), 1,48 (3H, т, J=7,2 Гц), 1,48 (3H, т, J=7,2 Гц), 1,44 (3H, т, J=7,2 Гц).
Пример 185
3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(4-этоксифенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,60-7,50 (4H, м), 7,44 (1H, с), 7,35 (1H, т, J=7,8 Гц), 7,09 (1H, дд, J=9,0, 2,4 Гц), 6,10 (1H, д, J=5,4 Гц), 4,16 (2H, кв, J=7,2 Гц), 4,15 (2H, кв, J=7,2 Гц), 4,08 (2H, кв, J=7,2 Гц), 3,38 (2H, т, J=7,2 Гц), 3,02 (2H, т, J=7,2 Гц), 1,48 (3H, т, J=7,2 Гц), 1,48 (3H, т, J=7,2 Гц), 1,40 (3H, т, J=7,2 Гц).
Пример 186
Используя 2 г диметил 2-[2-(3,4-бис(бензилокси)фенил)оксазол-4-илметил]малоната, полученного в ссылочном примере 56, 2,2 г бледно-желтого маслянистого метил 2-[2-(3,4-бис-бензилоксифенил)оксазол-4-илметил]-3-(3-метилпиридин-2-ил)-3-оксопропионата получали таким же способом, как в примере 100.
1Н-ЯМР (CDCl3) δ: 8,49 (1H, дд, J=4,5, 1,2 Гц), 7,59-7,28 (15H, м), 6,94 (1H, д, J=8,4 Гц), 5,23-5,17 (5H, м), 3,69 (3H, с), 3,32-3,23 (2H, м), 2,59 (3H, с).
Пример 187
Используя 2,2 г метил 2-[2-(3,4-бис-бензилоксифенил)оксазол-4-илметил]-3-(3-метилпиридин-2-ил)-3-оксопропионата, полученного в примере 186, 0,24 г белого порошкообразного 3-[2-(3,4-дигидроксифенил)оксазол-4-илметил]-1-(3-метилпиридин-2-ил)пропан-1-она получали таким же способом, как в примере 136.
1Н-ЯМР (CDCl3) δ: 9,46 (1H, ушир.с), 9,32 (1H, ушир.с), 8,54 (1H, д, J=3,0 Гц), 7,80-7,76 (2H, м), 7,54-7,49 (1H, м), 7,32 (1H, д, J=2,1 Гц), 7,23 (1H, дд, J=8,4, 2,1 Гц), 6,82 (1H, д, J=8,4 Гц), 3,47 (2H, т, J=7,5 Гц), 2,83 (2H, т, J=7,5 Гц), 2,51 (3H, с).
Пример 188
Используя 0,12 г 3-[2-(3,4-дигидроксифенил)оксазол-4-илметил]-1-(3-метилпиридин-2-ил)пропан-1-она, полученного в примере 187, 35 мг белого порошкообразного 3-{2-[3,4-бис-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}-1-(3-метилпиридин-2-ил)пропан-1-она получали таким же способом, как в примере 111.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, д, J=4,5 Гц), 7,68 (1H, дд, J=8,4, 1,8 Гц), 7,63 (1H, д, J=1,8 Гц), 7,58 (1H, д, J=8,4 Гц), 7,49 (1H, с), 7,35-7,28 (1H, м), 7,04 (1H, д, J=8,4 Гц), 4,50-4,39 (4H, м), 3,60 (2H, т, J=7,2 Гц), 3,01 (2H, т, J=7,2 Гц), 2,59 (3H, с).
Пример 189
Используя 0,76 г 4-хлорметил-2-(3-этокси-4-метоксифенил)оксазола, полученного в ссылочном примере 58, и 0,5 г 1-(2-аллилоксифенил)этанона, полученного в ссылочном примере 53, 0,13 г белого порошкообразного 1-(2-аллилоксифенил)-3-[2-(3-этокси-4-метоксифенил)оксазол-4-ил]пропан-1-она получали таким же способом, как в примере 177.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 2,1 Гц), 7,56 (1H, дд, J=8,4, 2,1 Гц), 7,51 (1H, д, J=2,1 Гц), 7,45-7,40 (2H, м), 7,02-6,89 (3H, м), 6,12-6,01 (1H, м), 5,42 (1H, дд, J=17, 1,5 Гц), 5,28 (1H, дд, J=17, 1,5 Гц), 4,65-4,62 (2H, м), 4,18 (2H, кв, J=6,9 Гц), 3,92 (3H, с), 3,42 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 1,49 (3H, т, J=6,9 Гц).
Пример 190
2 г 4-хлорметил-2-(4-бензилокси-3-этоксифенил)оксазола, полученного в ссылочном примере 63, и 0,96 г 1-(2-этоксифенил)этанона растворяли в 20 мл тетрагидрофурана и к смеси добавляли 0,47 г гидрида натрия. После вспенивания реакционную смесь нагревали и кипятили с обратным холодильником в течение 3 часов. После охлаждения реакционную смесь добавляли в ледяную воду и осуществляли экстракцию этилацетатом. Органический слой промывали водой, сушили над сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1) с получением 0,4 г бесцветного порошкообразного 3-[2-(4-бензилокси-3-этоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,55-7,30 (8H, м), 6,97 (2H, т, J=7,5 Гц), 6,93 (1H, д, J=7,5 Гц), 5,19 (2H, с), 4,18 (2H, кв, J=6,9 Гц), 4,13 (2H, кв, J=6,9 Гц), 3,41 (2H, т, J=6,9 Гц), 2,99 (2H, т, J=6,9 Гц), 1,48 (3H, т, J=6,9 Гц), 1,47 (3H, т, J=6,9 Гц).
Пример 191
Используя 3-[2-(4-бензилокси-3-этоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-он, полученный в примере 190, бесцветный маслянистый 3-[2-(3-этокси-4-гидроксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-он получали таким же способом, как в примере 2.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,52 (1H, дд, J=8,1, 2,1 Гц), 7,49 (1H, д, J=2,1 Гц), 7,45-7,38 (2H, м), 6,97 (1H, т, J=7,5 Гц), 6,95 (1H, д, J=7,5 Гц), 6,93 (1H, д, J=8,1 Гц), 5,89 (1H, с), 4,20 (2H, кв, J=7,2 Гц), 4,13 (2H, кв, J=7,2 Гц), 3,41 (2H, т, J=7,2 Гц), 2,98 (2H, т, J=7,2 Гц), 1,47 (3H, т, J=7,2 Гц), 1,47 (3H, т, J=7,2 Гц).
Пример 192
Используя 3-[2-(3-этокси-4-гидроксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-он, полученный в примере 191, 3-[2-(3-этокси-4-изопропоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-он в виде бесцветных игольчатых кристаллов получали таким же способом, как в примере 111.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,54-7,51 (2H, м), 7,45-7,39 (2H, м), 6,97 (2H, ушир.т, J=7,5 Гц), 6,93 (1H, д, J=7,5 Гц), 4,55 (1H, септ., J=6,0 Гц), 4,14 (2H, кв, J=6,9 Гц), 4,13 (2H, кв, J=6,9 Гц), 3,42 (2H, т, J=7,5 Гц), 2,99 (2H, т, J=7,5 Гц), 1,47 (3H, т, J=6,9 Гц), 1,45 (3H, т, J=6,9 Гц), 1,37 (6H, д, J=6,0 Гц).
Пример 193
2,98 г 2-(3-бензилокси-4-метоксифенил)оксазол-4-карбальдегида, полученного в ссылочном примере 64, и 1,72 г 1-(2-пропоксифенил)этанона растворяли в 50 мл пиридина. К смеси добавляли 2,66 г карбоната калия и смесь нагревали и перемешивали при 120°C в течение 22 часов. После охлаждения реакционную смесь добавляли к насыщенному солевому раствору и осуществляли экстракцию этилацетатом. Органический слой промывали водой и затем сушили над безводным сульфатом магния и растворитель удаляли при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1) с получением 1,82 г бесцветного маслянистого (E)-3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)-2-пропен-1-она.
1Н-ЯМР (CDCl3) δ: 7,80 (1H, с), 7,79 (1H, д, J=15,3 Гц), 7,69-7,66 (3H, м), 7,51-7,32 (7H, м), 7,04-6,95 (3H, м), 5,21 (2H, с), 4,05 (2H, т, J=6,3 Гц), 3,94 (3H, с), 1,88 (2H, секст., J=6,3 Гц), 1,08 (3H, т, J=6,3 Гц).
Пример 194
1,82 г (E)-3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)-2-пропен-1-она, полученного в примере 193, растворяли в 50 мл метанола. К смеси добавляли 200 мг 5% палладия-на-углероде в виде порошка и смесь перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. Катализатор затем удаляли при помощи фильтрации. Фильтрат разбавляли 100 мл метанола и добавляли 500 мг 10% палладия-на-углероде в виде порошка. Смесь перемешивали в атмосфере водорода при комнатной температуре в течение 3 часов. Катализатор удаляли при помощи фильтрации и растворитель удаляли при пониженном давлении. К остатку добавляли диизопропиловый эфир для кристаллизации с получением 0,78 г бесцветного порошкообразного 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,55 (1H, д, J=2,1 Гц), 7,53 (1H, дд, J=8,1, 2,1 Гц), 7,42 (1H, ддд, J=8,1, 7,5, 1,8 Гц), 7,40 (1H, с), 6,97 (1H, тд, J=7,5, 0,9 Гц), 6,93 (1H, ушир.д, J=8,1 Гц), 6,89 (1H, д, J=8,1 Гц), 4,02 (2H, т, J=6,6 Гц), 3,94 (3H, с), 3,43 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 1,88 (2H, секст., J=6,6 Гц), 1,06 (3H, т, J=6,6 Гц).
Пример 195
Используя 0,15 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)пропан-1-она, полученного в примере 194, 67 мг бесцветного порошкообразного 3-[2-(3-этокси-4-метоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)пропан-1-она получали таким же способом, как в примере 102.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, дд, J=7,8, 1,8 Гц), 7,59-7,40 (4H, м), 6,97 (1H, т, J=7,8 Гц), 6,94 (1H, д, J=7,8 Гц), 6,91 (1H, д, J=7,8 Гц), 4,18 (2H, кв, J=6,6 Гц), 4,02 (2H, т, J=6,6 Гц), 3,92 (3H, с), 3,43 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,87 (2H, секст., J=6,6 Гц), 1,49 (3H, т, J=6,6 Гц), 1,06 (3H, т, J=6,6 Гц).
Пример 196
Используя 0,15 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)пропан-1-она, полученного в примере 194, 67 мг бесцветного маслянистого 3-[2-(3-циклопентилокси-4-метоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)пропан-1-она получали таким же способом, как в примере 102.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, дд, J=7,5, 1,8 Гц), 7,55 (1H, дд, J=8,4, 1,8 Гц), 7,51 (1H, д, J=1,8 Гц), 7,42 (1H, ушир.т, J=7,5 Гц), 7,39 (1H, с), 6,97 (1H, т, J=7,5 Гц), 6,93 (1H, д, J=7,5 Гц), 6,89 (1H, д, J=8,4 Гц), 4,90-4,84 (1H, м), 4,02 (2H, т, J=6,6 Гц), 3,88 (3H, с), 3,43 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 2,03-1,60 (10H, м), 1,05 (3H, т, J=7,2 Гц).
Пример 197
Используя 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)пропан-1-он, полученный в примере 194, бесцветный маслянистый 3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)пропан-1-он получали таким же способом, как в примере 102.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, дд, J=7,8, 1,8 Гц), 7,57 (1H, дд, J=8,4, 2,1 Гц), 7,54 (1H, д, J=2,1 Гц), 7,42 (1H, ддд, J=8,4, 7,2, 1,8 Гц), 7,39 (1H, с), 6,97 (1H, ушир.т, J=7,2 Гц), 6,96 (1H, ушир.д, J=8,4 Гц), 6,91 (1H, д, J=8,4 Гц), 4,65 (1H, септ., J=6,0 Гц), 4,02 (2H, т, J=7,2 Гц), 3,90 (3H, с), 3,43 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 1,87 (2H, секст., J=7,2 Гц), 1,40 (6H, д, J=6,0 Гц), 1,06 (3H, т, J=7,2 Гц).
Пример 198
Используя 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)пропан-1-он, полученный в примере 194, бесцветный порошкообразный 3-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)пропан-1-он получали таким же способом, как в примере 102.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,57 (1H, дд, J=8,4, 1,8 Гц), 7,50 (1H, д, J=1,8 Гц), 7,45-7,39 (2H, м), 6,97 (1H, ушир.т, J=7,5 Гц), 6,93 (1H, ушир.д, J=7,5 Гц), 6,91 (1H, ушир.д, J=8,4 Гц), 4,02 (2H, т, J=6,6 Гц), 3,92 (2H, д, J=7,2 Гц), 3,92 (3H, с), 3,43 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 1,87 (2H, секст., J=6,6 Гц), 1,41-1,32 (1H, м), 1,06 (3H, т, J=6,6 Гц), 0,69-0,63 (2H, м), 0,40-0,35 (2H, м).
Пример 199
Используя 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)пропан-1-он, полученный в примере 194, 3-[2-(3-(3-бутенилокси)-4-метоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)пропан-1-он в виде бесцветных игольчатых кристаллов получали таким же способом, как в примере 102.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, дд, J=7,7, 1,5 Гц), 7,58 (1H, дд, J=8,5, 2,0 Гц), 7,52 (1H, д, J=2,0 Гц), 7,42 (1H, ддд, J=7,7, 7,5, 1,8 Гц), 7,40 (1H, с), 6,97 (1H, ддд, J=7,7, 7,5, 0,9 Гц), 6,93 (1H, ушир.д, J=7,7 Гц), 6,91 (1H, д, J=8,5 Гц), 5,92 (1H, ддт, J=17,3, 10,3, 6,8 Гц), 5,19 (1H, ддд, J=17,3, 3,3, 1,5 Гц), 5,11 (1H, ддд, J=10,3, 3,3, 0,6 Гц), 4,14 (2H, т, J=7,2 Гц), 4,02 (2H, т, J=7,2 Гц), 3,91 (3H, с), 3,43 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 2,63 (2H, ушир.кв, J=6,9 Гц), 1,87 (2H, секст., J=7,2 Гц), 1,06 (3H, т, J=7,2 Гц).
Пример 200
Используя 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)пропан-1-он, полученный в примере 194, 3-[2-(3-аллилокси-4-метоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)пропан-1-он в виде бесцветных игольчатых кристаллов получали таким же способом, как в примере 102.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, дд, J=7,7, 1,8 Гц), 7,59 (1H, дд, J=8,5, 1,8 Гц), 7,52 (1H, д, J=1,8 Гц), 7,42 (1H, ддд, J=8,3, 7,7, 1,8 Гц), 7,40 (1H, с), 6,97 (1H, тд, J=7,7, 1,1 Гц), 6,93 (1H, ушир.д, J=8,3 Гц), 6,91 (1H, д, J=8,5 Гц), 6,12 (1H, ддт, J=17,3, 10,5, 5,5 Гц), 5,44 (1H, ддд, J=17,3, 3,0, 1,5 Гц), 5,31 (1H, ддд, J=10,5, 3,0, 1,5 Гц), 4,67 (2H, дт, J=5,5, 1,5 Гц), 4,02 (2H, т, J=6,3 Гц), 3,92 (3H, с), 3,43 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 1,87 (2H, секст., J=6,3 Гц), 1,06 (3H, т, J=6,3 Гц).
Пример 201
Используя 0,1 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)пропан-1-она, полученного в примере 194, 67 мг бесцветного порошкообразного 3-[2-(3-циклобутилметокси-4-метоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)пропан-1-она получали таким же способом, как в примере 111.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, дд, J=7,8, 1,8 Гц), 7,56 (1H, дд, J=7,8, 1,8 Гц), 7,52 (1H, д, J=1,8 Гц), 7,45-7,40 (2H, м), 6,98 (1H, т, J=7,8 Гц), 6,94 (1H, д, J=7,8 Гц), 6,90 (1H, д, J=7,8 Гц), 4,07 (2H, д, J=6,9 Гц), 4,02 (2H, т, J=6,6 Гц), 3,90 (3H, с), 3,44 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 2,86 (1H, квинт., J=7,2 Гц), 2,21-2,16 (2H, м), 1,96-1,84 (6H, м), 1,06 (3H, т, J=7,5 Гц).
Пример 202
Используя 2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-карбальдегид, полученный в ссылочном примере 65, бледно-желтый маслянистый (E)-3-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}-1-(2-пропоксифенил)-2-пропен-1-он получали таким же способом, как в примере 193.
1Н-ЯМР (CDCl3) δ: 7,83 (1H, д, J=15,0 Гц), 7,81 (1H, с), 7,76 (1H, дд, J=8,4, 2,1 Гц), 7,69 (1H, дд, J=7,8, 1,8 Гц), 7,69 (1H, д, J=2,1 Гц), 7,50 (1H, д, J=15,0 Гц), 7,45 (1H, ддд, J=8,4, 7,8, 1,8 Гц), 7,01 (1H, ушир.т, J=8,4 Гц), 6,99 (1H, д, J=8,4 Гц), 6,98 (1H, ушир.д, J=7,8 Гц), 4,46 (2H, кв, J=8,4 Гц), 4,06 (2H, т, J=6,3 Гц), 3,94 (3H, с), 1,90 (2H, секст., J=6,3 Гц), 1,09 (3H, т, J=6,3 Гц).
Пример 203
Используя (E)-3-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}-1-(2-пропоксифенил)-2-пропен-1-он, полученный в примере 202, бесцветный порошкообразный 3-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}-1-(2-пропоксифенил)пропан-1-он получали таким же способом, как в примере 194.
1Н-ЯМР (ДМСО-d6) δ: 7,83 (1H, с), 7,62 (1H, дд, J=7,8, 1,8 Гц), 7,57 (1H, дд, J=7,8, 1,5 Гц), 7,55 (1H, д, J=1,5 Гц), 7,51 (1H, ушир.т, J=7,8 Гц), 7,17 (1H, д, J=7,8 Гц), 7,15 (1H, д, J=7,8 Гц), 7,01 (1H, т, J=7,8 Гц), 4,80 (2H, кв, J=9,0 Гц), 4,06 (2H, т, J=6,6 Гц), 3,86 (3H, с), 3,33 (2H, т, J=7,2 Гц), 2,84 (2H, т, J=7,2 Гц), 1,79 (2H, секст., J=6,6 Гц), 0,99 (3H, т, J=6,6 Гц).
Пример 204
Используя 2-(3,4-диэтоксифенил)оксазол-4-карбальдегид, полученный в ссылочном примере 66, бледно-желтый порошкообразный (E)-3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)-2-пропен-1-он получали таким же способом, как в примере 193.
1Н-ЯМР (CDCl3) δ: 7,81 (1H, д, J=15,0 Гц), 7,79 (1H, ушир.д, J=7,5 Гц), 7,68 (1H, дд, J=7,8, 1,8 Гц), 7,62 (1H, д, J=1,8 Гц), 7,59 (1H, ушир.с), 7,49 (1H, д, J=15,0 Гц), 7,44 (1H, ушир.т, J=7,5 Гц), 7,01 (1H, ушир.т, J=7,5 Гц), 6,97 (1H, ушир.д, J=7,5 Гц), 6,93 (1H, д, J=7,8 Гц), 4,18 (2H, кв, J=6,9 Гц), 4,16 (2H, кв, J=6,9 Гц), 4,05 (2H, т, J=6,3 Гц), 1,89 (1H, ушир.секст., J=6,9 Гц), 1,50 (3H, т, J=6,9 Гц), 1,49 (3H, т, J=6,9 Гц), 1,09 (3H, т, J=7,2 Гц).
Пример 205
Используя (E)-3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)-2-пропен-1-он, полученный в примере 204, бесцветный порошкообразный 3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2-пропоксифенил)пропан-1-он получали таким же способом, как в примере 194.
1Н-ЯМР (CDCl3) δ: 7,60 (1H, дд, J=7,8, 1,8 Гц), 7,54 (1H, дд, J=8,4, 2,1 Гц), 7,52 (1H, д, J=2,1 Гц), 7,42 (1H, ддд, J=7,8, 7,2, 1,8 Гц), 7,39 (1H, с), 6,97 (1H, тд, J=7,8, 1,2 Гц), 6,93 (1H, ушир.д, J=7,2 Гц), 6,90 (1H, д, J=8,4 Гц), 4,17 (2H, кв, J=6,9 Гц), 4,14 (2H, кв, J=6,9 Гц), 4,02 (2H, т, J=6,6 Гц), 3,43 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 1,87 (2H, септ., J=6,6 Гц), 1,48 (6H, т, J=6,9 Гц), 1,05 (3H, т, J=6,6 Гц).
Пример 206
Используя 2-(3-бензилокси-4-метоксифенил)оксазол-4-карбальдегид, полученный в ссылочном примере 64, бледно-желтый порошкообразный (E)-3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)-2-пропен-1-он получали таким же способом, как в примере 193.
1Н-ЯМР (CDCl3) δ: 7,79 (1H, с), 7,79 (1H, д, J=15,3 Гц), 7,69-7,65 (3H, м), 7,50-7,32 (7H, м), 7,03-6,95 (3H, м), 5,21 (2H, с), 4,66 (1H, септ., J=6,0 Гц), 3,94 (3H, с), 1,41 (6H, д, J=6,0 Гц).
Пример 207
Используя (E)-3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)-2-пропен-1-он, полученный в примере 206, бесцветный порошкообразный 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)пропан-1-он получали таким же способом, как в примере 194.
1Н-ЯМР (CDCl3) δ: 7,67 (1H, дд, J=7,5, 1,8 Гц), 7,55 (1H, ушир.с), 7,54 (1H, дд, J=7,5, 1,8 Гц), 7,40 (1H, тд, J=7,5, 1,8 Гц), 7,40 (1H, с), 6,95 (1H, ушир.т, J=7,5 Гц), 6,93 (1H, ушир.д, J=7,5 Гц), 6,89 (1H, д, J=7,5 Гц), 5,64 (1H, с), 4,68 (1H, септ., J=6,0 Гц), 3,94 (3H, с), 3,40 (2H, т, J=7,2 Гц), 2,98 (2H, т, J=7,2 Гц), 1,40 (6H, д, J=6,0 Гц).
Указанное выше соединение также получали следующим способом. 10 г 2-(3-бензилокси-4-метоксифенил-4-хлорметилоксазола, полученного в ссылочном примере 5, и 5,4 г 1-(2-изопропоксифенил)этанона растворяли в 100 мл тетрагидрофурана и к смеси добавляли 2,42 г гидрида натрия. После вспенивания реакционную смесь нагревали и кипятили с обратным холодильником в течение 3 часов. После охлаждения реакционную смесь добавляли в ледяную воду и осуществляли экстракцию этилацетатом. Органический слой промывали водой, сушили над сульфатом магния и затем концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1) с получением 4,30 г бледно-желтого маслянистого 3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)пропан-1-она. Затем 1,84 полученного 3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)пропан-1-она растворяли в 100 мл метанола. К смеси добавляли 800 мг 10% палладия-на-углероде в виде порошка. Смесь перемешивали в атмосфере водорода при комнатной температуре в течение 1 часа. Катализатор удаляли при помощи фильтрации и растворитель удаляли. Остаток затем перекристаллизовывали из смеси ацетон/диизопропиловый эфир с получением 1,15 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)пропан-1-она.
Пример 208
Используя 0,15 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)пропан-1-она, полученного в примере 207, 0,12 г бледно-желтого маслянистого 3-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)пропан-1-она получали таким же способом, как в примере 102.
1Н-ЯМР (CDCl3) δ: 7,67 (1H, дд, J=7,8, 1,8 Гц), 7,57 (1H, дд, J=8,4, 2,1 Гц), 7,50 (1H, д, J=2,1 Гц), 7,41 (1H, тд, J=7,8, 1,8 Гц), 7,39 (1H, с), 6,95 (1H, ушир.т, J=7,8 Гц), 6,93 (1H, ушир.д, J=7,8 Гц), 6,91 (1H, д, J=8,4 Гц), 4,68 (1H, септ., J=6,0 Гц), 3,92 (2H, д, J=6,9 Гц), 3,92 (3H, с), 3,41 (2H, т, J=7,2 Гц), 2,98 (2H, т, J=7,2 Гц), 1,40 (6H, д, J=6,0 Гц), 1,46-1,32 (1H, м), 0,69-0,62 (2H, м), 0,40-0,35 (2H, м).
Пример 209
Используя 0,15 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)пропан-1-она, полученного в примере 207, 42 мг бесцветного порошкообразного 3-[2-(3-этокси-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)пропан-1-она получали таким же способом, как в примере 102.
1Н-ЯМР (CDCl3) δ: 7,68 (1H, дд, J=7,7, 1,8 Гц), 7,57 (1H, дд, J=8,5, 2,0 Гц), 7,52 (1H, д, J=2,0 Гц), 7,41 (1H, тд, J=7,7, 1,8 Гц), 7,40 (1H, с), 6,95 (1H, ушир.т, J=7,7 Гц), 6,94 (1H, ушир.д, J=7,7 Гц), 6,91 (1H, д, J=8,5 Гц), 4,69 (1H, септ., J=6,0 Гц), 4,18 (2H, кв, J=6,9 Гц), 3,92 (3H, с), 3,41 (2H, т, J=6,9 Гц), 2,99 (2H, т, J=6,9 Гц), 1,49 (3H, т, J=6,9 Гц), 1,40 (6H, д, J=6,0 Гц).
Пример 210
Используя 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)пропан-1-он, полученный в примере 207, бледно-желтый маслянистый 3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)пропан-1-он получали таким же способом, как в примере 102.
1Н-ЯМР (CDCl3) δ: 7,68 (1H, дд, J=7,5, 1,8 Гц), 7,57 (1H, дд, J=7,5, 1,8 Гц), 7,54 (1H, д, J=1,8 Гц), 7,44-7,38 (2H, м), 6,95 (1H, ушир.т, J=7,5 Гц), 6,94 (1H, д, J=7,5 Гц), 6,91 (1H, д, J=7,5 Гц), 4,67 (2H, септ., J=6,0 Гц), 3,90 (3H, с), 3,40 (2H, т, J=7,2 Гц), 2,98 (2H, т, J=7,2 Гц), 1,40 (12H, д, J=6,0 Гц).
Пример 211
Используя 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)пропан-1-он, полученный в примере 207, бесцветный маслянистый 3-[2-(3-аллилокси-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)пропан-1-он получали таким же способом, как в примере 102.
1Н-ЯМР (CDCl3) δ: 7,68 (1H, дд, J=7,7, 1,8 Гц), 7,58 (1H, дд, J=8,3, 1,8 Гц), 7,53 (1H, д, J=1,8 Гц), 7,41 (1H, ддд, J=7,9, 7,7, 1,8 Гц), 7,40 (1H, с), 6,98 (1H, тд, J=7,9, 1,8 Гц), 6,94 (1H, ушир.д, J=7,7 Гц), 6,92 (1H, д, J=8,3 Гц), 6,12 (1H, ддт, J=17,3, 10,5, 5,3 Гц), 5,44 (1H, ддд, J=17,3, 3,0, 1,7 Гц), 5,31 (1H, ддд, J=10,5, 3,0, 1,5 Гц), 4,75-4,60 (3H, м), 3,92 (3H, с), 3,41 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 1,40 (6H, д, J=6,0 Гц).
Пример 212
Используя 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)пропан-1-он, полученный в примере 207, 3-[2-(3-(3-бутенилокси)-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)пропан-1-он в виде бесцветных игольчатых кристаллов получали таким же способом, как в примере 102.
1Н-ЯМР (CDCl3) δ: 7,67 (1H, дд, J=7,9, 1,8 Гц), 7,57 (1H, дд, J=8,5, 2,0 Гц), 7,53 (1H, д, J=2,0 Гц), 7,40 (1H, ддд, J=7,9, 7,5, 1,8 Гц), 7,40 (1H, с), 6,95 (1H, ушир.т, J=7,5 Гц), 6,93 (1H, ушир.д, J=7,5 Гц), 6,91 (1H, д, J=8,5 Гц), 5,92 (1H, ддт, J=17,1, 10,3, 6,8 Гц), 5,19 (1H, ддд, J=17,3, 3,3, 1,5 Гц), 5,10 (1H, ддд, J=10,3, 3,3, 1,3 Гц), 4,68 (1H, септ., J=6,0 Гц), 4,14 (2H, т, J=7,2 Гц), 3,91 (3H, с), 3,41 (2H, т, J=7,2 Гц), 3,01 (2H, т, J=7,2 Гц), 2,63 (2H, ушир.кв, J=7,2 Гц), 1,40 (6H, д, J=6,0 Гц).
Пример 213
Используя 0,15 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)пропан-1-она, полученного в примере 207, 40 мг бесцветного порошкообразного 1-(2-изопропоксифенил)-3-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}пропан-1-она получали таким же способом, как в примере 111.
1Н-ЯМР (CDCl3) δ: 7,70-7,60 (2H, м), 7,44-7,38 (2H, м), 6,98-6,91 (4H, м), 4,69 (1H, септ., J=6,0 Гц), 4,48-4,41 (2H, м), 3,93 (3H, с), 3,42 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,41 (6H, д, J=6,0 Гц).
Пример 214
Используя 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)пропан-1-он, полученный в примере 207, бесцветный порошкообразный 3-[2-(3-циклобутилметокси-4-метоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)пропан-1-он получали таким же способом, как в примере 111.
1Н-ЯМР (CDCl3) δ: 7,68 (1H, дд, J=8,4, 1,8 Гц), 7,56 (1H, дд, J=8,4, 1,8 Гц), 7,52 (1H, д, J=1,8 Гц), 7,44-7,38 (2H, м), 6,95 (1H, ушир.т, J=8,4 Гц), 6,94 (1H, ушир.д, J=8,4 Гц), 6,90 (1H, д, J=8,4 Гц), 4,69 (1H, септ., J=6,0 Гц), 4,07 (2H, д, J=6,9 Гц), 3,90 (3H, с), 3,41 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 2,86 (1H, квинт., J=7,2 Гц), 2,22-2,14 (2H, м), 1,99-1,84 (4H, м), 1,40 (6H, д, J=6,0 Гц).
Пример 215
Используя 2-(3,4-диэтоксифенил)оксазол-4-карбальдегид, полученный в ссылочном примере 66, желтый маслянистый (E)-3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)-2-пропен-1-он получали таким же способом, как в примере 193.
1Н-ЯМР (CDCl3) δ: 7,81 (1H, д, J=15,3 Гц), 7,79 (1H, ушир.с), 7,69-7,53 (3H, м), 7,46 (1H, д, J=15,3 Гц), 7,43 (1H, тд, J=7,8, 1,2 Гц), 7,00 (1H, ушир.т, J=7,8 Гц), 6,93 (1H, ушир.д, J=7,8 Гц), 6,91 (1H, ушир.д, J=7,8 Гц), 4,67 (1H, септ., J=6,0 Гц), 4,22-4,11 (4H, м), 1,52-1,45 (6H, м), 1,41 (6H, д, J=6,0 Гц).
Пример 216
Используя (E)-3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)-2-пропен-1-он, полученный в примере 215, бледно-желтый маслянистый 3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2-изопропоксифенил)пропан-1-он получали таким же способом, как в примере 194.
1Н-ЯМР (CDCl3) δ: 7,67 (1H, дд, J=7,5, 1,5 Гц), 7,60-7,38 (4H, м), 6,97-6,89 (3H, м), 4,68 (1H, септ., J=6,0 Гц), 4,21-4,10 (4H, м), 3,41 (2H, т, J=7,2 Гц), 2,98 (2H, т, J=7,2 Гц), 1,48 (6H, ушир.т, J=7,2 Гц), 1,40 (6H, д, J=6,0 Гц).
Пример 217
Используя 2-(3,4-диэтоксифенил)оксазол-4-карбальдегид, полученный в ссылочном примере 66, бесцветный порошкообразный (E)-3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-o-толил-2-пропен-1-он получали таким же способом, как в примере 193.
1Н-ЯМР (CDCl3) δ: 7,81 (1H, с), 7,64-7,28 (8H, м), 6,93 (1H, д, J=8,1 Гц), 4,20 (2H, кв, J=6,9 Гц), 4,16 (2H, кв, J=6,9 Гц), 2,47 (3H, с), 1,50 (3H, т, J=6,9 Гц), 1,49 (3H, т, J=6,9 Гц).
Пример 218
Используя (E)-3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-o-толил-2-пропен-1-он, полученный в примере 217, 3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-o-толилпропан-1-он в виде бесцветных игольчатых кристаллов получали таким же способом, как в примере 194.
1Н-ЯМР (CDCl3) δ: 7,68 (1H, дд, J=7,5, 1,8 Гц), 7,55 (1H, дд, J=8,1, 1,8 Гц), 7,51 (1H, д, J=1,8 Гц), 7,43 (1H, ушир.с), 7,36 (1H, тд, J=7,5, 1,5 Гц), 7,27-7,22 (2H, м), 6,90 (1H, д, J=8,1 Гц), 4,17 (2H, кв, J=6,9 Гц), 4,14 (2H, кв, J=6,9 Гц), 3,32 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 2,49 (3H, с), 1,48 (6H, т, J=6,9 Гц).
Пример 219
Используя 2-(3-бензилокси-4-метоксифенил)оксазол-4-карбальдегид, полученный в ссылочном примере 64, бледно-желтый порошкообразный (E)-3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]-1-o-толил-2-пропен-1-он получали таким же способом, как в примере 193.
1Н-ЯМР (CDCl3) δ: 7,81 (1H, с), 7,69-7,26 (13H, м), 6,96 (1H, д, J=9,0 Гц), 5,23 (2H, с), 3,94 (3H, с), 2,47 (3H, с).
Пример 220
Используя (E)-3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]-1-o-толил-2-пропен-1-он, полученный в примере 219, бесцветный порошкообразный 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-o-толилпропан-1-он получали таким же способом, как в примере 194.
1Н-ЯМР (CDCl3) δ: 7,67 (1H, дд, J=7,2, 1,8 Гц), 7,56 (1H, д, J=1,8 Гц), 7,53 (1H, дд, J=8,1, 1,8 Гц), 7,43 (1H, с), 7,35 (1H, тд, J=7,2, 1,8 Гц), 7,26-7,22 (2H, м), 6,89 (1H, д, J=8,1 Гц), 5,69 (1H, с), 3,94 (3H, с), 3,31 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 2,49 (3H, с).
Пример 221
0,15 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-o-толилпропан-1-она, полученного в примере 220, растворяли в 10 мл изопропилового спирта. К смеси добавляли 86 мкл (бромметил)циклопропана и 200 мкл 1,8-диазабицикло[5.4.0]ундец-7-ена и смесь нагревали и кипятили с обратным холодильником в течение 24 часов. К реакционной смеси добавляли воду и затем осуществляли экстракцию этилацетатом. Органический слой промывали с насыщенным солевым раствором, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1) и перекристаллизовывали из смеси ацетон/диизопропиловый эфир/н-гексан с получением 71 мг 3-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]-1-o-толилпропан-1-она в виде бесцветных игольчатых кристаллов.
1Н-ЯМР (CDCl3) δ: 7,68 (1H, дд, J=7,5, 1,5 Гц), 7,57 (1H, дд, J=8,1, 2,1 Гц), 7,49 (1H, д, J=2,1 Гц), 7,43 (1H, т, J=0,9 Гц), 7,36 (1H, тд, J=7,5, 1,5 Гц), 7,25-7,22 (2H, м), 6,91 (1H, д, J=8,1 Гц), 3,93 (2H, д, J=6,9 Гц), 3,92 (3H, с), 3,32 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 2,49 (3H, с), 1,41-1,32 (1H, м), 0,69-0,63 (2H, м), 0,40-0,35 (2H, м).
Пример 222
Используя 2-(3-изопропокси-4-метоксифенил)оксазол-4-карбальдегид, полученный в ссылочном примере 69, желтый порошкообразный (E)-3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]-1-(2-бензилоксифенил)-2-пропен-1-он получали таким же способом, как в примере 193.
1Н-ЯМР (CDCl3) δ: 7,76 (1H, с), 7,69-6,92 (14H, м), 5,20 (2H, с), 4,63 (1H, септ., J=6,0 Гц), 1,38 (6H, д, J=6,0 Гц).
Пример 223
Используя (E)-3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]-1-(2-бензилоксифенил)-2-пропен-1-он, полученный в примере 222, бесцветный пластинчатокристаллический 1-(2-гидроксифенил)-3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]пропан-1-он получали таким же способом, как в примере 194.
1Н-ЯМР (CDCl3) δ: 12,25 (1H, с), 7,82 (1H, дд, J=8,4, 1,5 Гц), 7,58 (1H, дд, J=8,4, 1,8 Гц), 7,54 (1H, д, J=1,8 Гц), 7,46 (1H, ддд, J=8,4, 7,2, 1,5 Гц), 7,45 (1H, с), 6,98 (1H, дд, J=8,4, 1,2 Гц), 6,92 (1H, д, J=8,4 Гц), 6,89 (1H, ддд, J=8,4, 7,2, 1,2 Гц), 4,65 (1H, септ., J=6,0 Гц), 3,90 (3H, с), 3,44 (2H, т, J=7,5 Гц), 3,03 (2H, т, J=7,5 Гц), 1,40 (6H, д, J=6,0 Гц).
Пример 224
67 мг 1-(2-гидроксифенил)-3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]пропан-1-она, полученного в примере 223, растворяли в 5 мл диметилформамида. К смеси добавляли 31 мкл аллилбромида и 73 мг карбоната калия и смесь перемешивали при комнатной температуре в течение ночи. К смеси снова добавляли 50 мкл аллилбромида и смесь перемешивали при 50°C в течение 8 часов и при комнатной температуре в течение ночи. Реакционную смесь добавляли в воду и затем осуществляли экстракцию этилацетатом. Органический слой промывали насыщенным солевым раствором, сушили над безводным сульфатом магния и растворитель удаляли при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1) и кристаллизовали из н-гексана с получением 33 мг бесцветного порошкообразного 1-(2-аллилоксифенил)-3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,8, 1,8 Гц), 7,57 (1H, дд, J=8,4, 2,1 Гц), 7,54 (1H, д, J=2,1 Гц), 7,44 (1H, ддд, J=7,8, 7,5, 1,8 Гц), 7,40 (1H, ушир.с), 6,99 (1H, тд, J=7,8, 1,2 Гц), 6,94 (1H, ушир.д, J=7,5 Гц), 6,91 (1H, д, J=8,4 Гц), 6,08 (1H, ддт, J=17,1, 10,5, 5,4 Гц), 5,42 (1H, ддд, J=17,1, 3,0, 1,5 Гц), 5,29 (1H, ддд, J=10,5, 2,7, 1,5 Гц), 4,69-4,61 (3H, м), 3,89 (3H, с), 3,42 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 1,39 (6H, д, J=6,3 Гц).
Пример 225
Используя 0,3 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-o-толилпропан-1-она, полученного в примере 220, 0,15 г белого порошкообразного 3-[2-(3-этокси-4-метоксифенил)оксазол-4-ил]-1-o-толилпропан-1-она получали таким же способом, как в примере 3.
1Н-ЯМР (CDCl3) δ: 7,68 (1H, м), 7,57 (1H, дд, J=8,1, 2,1 Гц), 7,51 (1H, д, J=2,1 Гц), 7,44 (1H, д, J=0,9 Гц), 7,36 (1H, м), 7,30-7,20 (3H, м), 6,91 (1H, д, J=8,4 Гц), 4,18 (2H, кв, J=6,9 Гц), 3,92 (3H, с), 3,35-3,25 (2H, м), 3,05-2,95 (2H, м), 2,50 (3H, с), 1,50 (3H, т, J=6,9 Гц).
Пример 226
Используя 0,3 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-o-толилпропан-1-она, полученного в примере 220, 0,1 г белого порошкообразного 3-[2-(3-аллилокси-4-метоксифенил)оксазол-4-ил]-1-o-толилпропан-1-она получали таким же способом, как в примере 3.
1Н-ЯМР (CDCl3) δ: 7,68 (1H, м), 7,59 (1H, дд, J=8,4, 2,1 Гц), 7,52 (1H, д, J=2,1 Гц), 7,43 (1H, с), 7,38 (1H, м), 7,35-7,25 (2H, м), 6,92 (1H, д, J=8,4 Гц), 6,13 (1H, ддд, J=17,1, 10,5, 5,4 Гц), 5,44 (1H, ддд, J=17,1, 2,7, 1,5 Гц), 5,31 (1H, ддд, J=10,5, 2,7, 1,5 Гц), 4,68 (1H, дт, J=5,4, 1,5 Гц), 3,92 (3H, с), 3,32 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 2,50 (3H, с).
Пример 227
Используя 0,2 г 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-o-толилпропан-1-она, полученного в примере 220, 0,1 г бледно-желтого маслянистого 3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]-1-o-толилпропан-1-она получали таким же способом, как в примере 3.
1Н-ЯМР (CDCl3) δ: 7,69 (1H, м), 7,60-7,50 (2H, м), 7,50-7,30 (3H, м), 7,24 (1H, м), 6,91 (1H, дд, J=5,1, 3,0 Гц), 4,65 (1H, м), 3,90 (3H, с), 3,35-3,25 (2H, м), 3,05-2,95 (2H, м), 2,49 (3H, с), 1,40 (6H, д, J=6,0 Гц).
Пример 228
65 мг гидрида натрия суспендировали в 5 мл тетрагидрофурана. К смеси последовательно добавляли 0,27 г 1-(2-этоксифенил)этанона и 0,3 г 2-(3-бензилокси-4-дифторметоксифенил)-4-хлорметилоксазола, полученного в ссылочном примере 44, при охлаждении льдом и перемешивании и смесь перемешивали в течение 3 часов при нагревании и кипячении с обратным холодильником. К реакционной смеси добавляли насыщенный водный раствор хлорида аммония при охлаждении льдом и перемешивании. После перемешивания в течение 15 минут к смеси добавляли воду и осуществляли экстракцию этилацетатом. Смесь сушили над безводным сульфатом магния и растворитель удаляли. Полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 4:1) с получением 75 мг бесцветного маслянистого 3-[2-(3-бензилокси-4-дифторметоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,72-7,69 (2H, м), 7,59 (1H, дд, J=8,1, 1,8 Гц), 7,47-7,32 (7H, м), 7,00-6,92 (3H, м), 6,61 (1H, т, J=74,7 Гц), 5,20 (2H, с), 4,15 (2H, кв, J=7,2 Гц), 3,43 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,48 (3H, т, J=7,2 Гц).
Пример 229
75 мг 3-[2-(3-бензилокси-4-дифторметоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-она, полученного в примере 228, растворяли в 1 мл этанола. К смеси добавляли 7 мг 10% палладия-на-углероде в виде порошка и смесь перемешивали в атмосфере водорода при комнатной температуре в течение 45 минут. Катализатор удаляли при помощи фильтрации, фильтрат концентрировали и полученный остаток очищали колоночной хроматографией на силикагеле (дихлорметан:этанол = 100:1) с получением 32 мг белого порошкообразного 3-[2-(4-дифторметокси-3-гидроксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,5, 1,8 Гц), 7,65 (1H, д, J=1,8 Гц), 7,56-7,43 (3H, м), 7,16 (1H, д, J=6,0 Гц), 6,98-6,92 (2H, м), 6,57 (1H, т, J=74,7 Гц), 5,57 (1H, с), 4,13 (2H, кв, J=7,2 Гц), 3,42 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,48 (3H, т, J=7,2 Гц).
Пример 230
30 мг 3-[2-(4-дифторметокси-3-гидроксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-она, полученного в примере 229, растворяли в 0,5 мл диметилформамида. К смеси добавляли 18 мг 2-бромпропана и 30 мг карбоната калия и смесь перемешивали при комнатной температуре в течение ночи. К реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Осуществляли сушку с использованием безводного сульфата магния и растворитель удаляли. Полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 4:1) с получением 23 мг белого порошкообразного 3-[2-(4-дифторметокси-3-изопропоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,8, 1,8 Гц), 7,61 (1H, д, J=1,8 Гц), 7,55 (1H, дд, J=8,4, 1,8 Гц), 7,50-7,38 (2H, м), 7,19 (1H, д, J=8,1 Гц), 7,00-6,70 (2H, м), 6,60 (1H, т, J=74,7 Гц), 4,72-4,64 (1H, м), 4,13 (2H, кв, J=7,2 Гц), 3,42 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,48 (3H, т, J=7,2 Гц), 1,39 (6H, д, J=6,0 Гц).
Пример 231
С использованием 2-(3-бензилокси-4-метоксифенил)-4-хлорметилоксазола, полученного в ссылочном примере 5, и 1-(2-метоксиметоксифенил)этанона, полученного в ссылочном примере 70, желтый маслянистый 3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]-1-(2-метоксиметоксифенил)пропан-1-он получали таким же способом, как в примере 190.
1Н-ЯМР (CDCl3) δ: 7,66 (1H, дд, J=7,8, 1,8 Гц), 7,59 (1H, дд, J=7,8, 1,8 Гц), 7,51 (1H, ушир.с), 7,49-7,27 (7H, м), 7,17 (1H, ушир.д, J=7,8 Гц), 7,04 (1H, тд, J=7,5, 1,2 Гц), 6,93 (1H, ушир.д, J=7,8 Гц), 5,25 (2H, с), 5,19 (2H, с), 3,92 (3H, с), 3,48 (3H, с), 3,39 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц).
Пример 232
С использованием 3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]-1-(2-метоксиметоксифенил)пропан-1-она, полученного в примере 231, 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-метоксиметоксифенил)пропан-1-он получали таким же способом, как в примере 194.
1Н-ЯМР (CDCl3) δ: 7,66 (1H, дд, J=7,8, 1,8 Гц), 7,55 (1H, д, J=2,1 Гц), 7,53 (1H, дд, J=8,1, 2,1 Гц), 7,41 (1H, с), 7,41 (1H, ддд, J=7,8, 7,5, 1,8 Гц), 7,17 (1H, ушир.д, J=7,8 Гц), 7,04 (1H, тд, J=7,5, 0,8 Гц), 6,89 (1H, д, J=8,1 Гц), 5,64 (1H, с), 5,26 (2H, с), 3,94 (3H, с), 3,49 (3H, с), 3,40 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц).
Пример 233
С использованием 3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]-1-(2-метоксиметоксифенил)пропан-1-она, полученного в примере 232, бесцветный маслянистый 3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]-1-(2-метоксиметоксифенил)пропан-1-он получали таким же способом, как в примере 102.
1Н-ЯМР (CDCl3) δ: 7,66 (1H, дд, J=7,5, 1,8 Гц), 7,57 (1H, дд, J=8,4, 1,8 Гц), 7,53 (1H, д, J=1,8 Гц), 7,42 (1H, ддд, J=8,4, 7,5, 1,8 Гц), 7,41 (1H, с), 7,17 (1H, дд, J=8,4, 1,2 Гц), 7,04 (1H, тд, J=7,5, 1,2 Гц), 6,91 (1H, д, J=8,4 Гц), 5,26 (2H, с), 4,64 (1H, септ., J=6,0 Гц), 3,90 (3H, с), 3,49 (3H, с), 3,40 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,39 (6H, д, J=6,0 Гц).
Пример 234
С использованием 0,76 г 4-хлорметил-2-(3-этокси-4-метоксифенил)оксазола, полученного в ссылочном примере 58, 60 мг белого порошкообразного 3-[2-(3-этокси-4-метоксифенил)оксазол-4-ил]-1-[2-(2,2,2-трифторэтокси)фенил]пропан-1-она получали таким же способом, как в примере 228.
1Н-ЯМР (CDCl3) δ: 7,76 (1H, дд, J=7,8, 2,1 Гц), 7,58-7,48 (3H, м), 7,39 (1H, с), 7,12 (1H, т, J=7,5 Гц), 6,92-6,88 (2H, м), 4,46 (2H, кв, J=7,8 Гц), 4,18 (2H, кв, J=7,2 Гц), 3,92 (3H, с), 3,40 (2H, т, J=7,5 Гц), 3,00 (2H, т, J=7,5 Гц), 1,49 (3H, т, J=7,2 Гц).
Пример 235
С использованием 0,76 г 4-хлорметил-2-(3-этокси-4-метоксифенил)оксазола, полученного в ссылочном примере 58, и 0,58 г 1-(2-трифторметоксифенил)этанона 0,18 г бледно-желтого маслянистого 3-[2-(3-этокси-4-метоксифенил)оксазол-4-ил]-1-(2-трифторметоксифенил)пропан-1-она получали таким же способом, как в примере 228.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, дд, J=7,5, 1,8 Гц), 7,58-7,50 (3H, м), 7,42 (1H, с), 7,38-7,30 (2H, м), 6,91 (1H, д, J=8,4 Гц), 4,17 (2H, кв, J=6,6 Гц), 3,91 (3H, с), 3,45 (2H, т, J=7,2 Гц), 3,01 (2H, т, J=7,2 Гц), 1,49 (3H, т, J=6,6 Гц).
Пример 236
С использованием 0,5 г 3-[2-(3,4-диметоксифенил)оксазол-4-ил]пропионовой кислоты, полученной в ссылочном примере 71, 0,32 г белого порошкообразного 3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-пирролидин-1-илпропан-1-она получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 7,55 (1H, дд, J=6,75, 1,8 Гц), 7,52 (1H, д, J=1,8 Гц), 7,44 (1H, с), 6,91 (1H, д, J=8,1 Гц), 4,20-4,10 (4H, м), 3,50-3,40 (4H, м), 3,00-2,90 (2H, м), 2,70-2,60 (2H, м), 1,95-1,75 (4H, м), 1,48 (3H, т, J=7,2 Гц), 1,48 (3H, т, J=7,2 Гц).
Пример 237
С использованием 0,3 г 3-[2-(3,4-диметоксифенил)оксазол-4-ил]пропионовой кислоты, полученной в ссылочном примере 71, 0,28 г белого порошкообразного 3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(3-гидроксипирролидин-1-ил)пропан-1-она получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 7,55 (1H, дд, J=6,75, 1,8 Гц), 7,52 (1H, д, J=1,8 Гц), 7,44 (1H, с), 6,91 (1H, д, J=8,1 Гц), 4,20-4,10 (4H, м), 3,50-3,40 (4H, м), 3,00-2,90 (2H, м), 2,70-2,60 (2H, м), 2,10-1,90 (3H, м), 1,48 (3H, т, J=6,9 Гц), 1,48 (3H, т, J=6,9 Гц).
Пример 238
С использованием 1 г 3-[2-(4-бензилокси-3-метоксифенил)оксазол-4-ил]пропионовой кислоты, полученной в ссылочном примере 73, 1,03 г бледно-желтого порошкообразного 3-[2-(4-бензилокси-3-метоксифенил)оксазол-4-ил]-1-пирролидин-1-илпропан-1-она получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 7,61-7,27 (8H, м), 6,93 (1H, д, J=8,4 Гц), 5,20 (2H, с), 3,97 (3H, с), 3,49-3,39 (4H, м), 2,94 (2H, т, J=7,5 Гц), 2,65 (2H, т, J=7,5 Гц), 1,95-1,78 (4H, м).
Пример 239
С использованием 1 г 3-[2-(4-бензилокси-3-метоксифенил)оксазол-4-ил]-1-пирролидин-1-илпропан-1-она, полученного в примере 238, 0,59 г белого порошкообразного 3-[2-(4-гидрокси-3-метоксифенил)оксазол-4-ил]-1-пирролидин-1-илпропан-1-она получали таким же способом, как в примере 2.
1Н-ЯМР (CDCl3) δ: 7,56-7,51 (2H, м), 7,44 (1H, с), 6,90 (1H, д, J=8,4 Гц), 5,97 (1H, с), 3,97 (3H, с), 3,49-3,39 (4H, м), 2,94 (2H, т, J=7,5 Гц), 2,66 (2H, т, J=7,5 Гц), 1,97-1,79 (4H, м).
Пример 240
С использованием 0,15 г 3-[2-(4-гидрокси-3-метоксифенил)оксазол-4-ил]-1-пирролидин-1-ил-пропан-1-она, полученного в примере 239, 0,13 г белого порошкообразного 3-[2-(4-этокси-3-метоксифенил)оксазол-4-ил]-1-пирролидин-1-илпропан-1-она получали таким же способом, как в примере 3.
1Н-ЯМР (CDCl3) δ: 7,57 (1H, дд, J=8,1, 2,1 Гц), 7,52 (1H, д, J=1,8 Гц), 7,45 (1H, с), 6,91 (1H, д, J=8,1 Гц), 4,15 (2H, кв, J=6,9 Гц), 3,96 (3H, с), 3,49-3,40 (4H, м), 2,94 (2H, т, J=7,2 Гц), 2,66 (2H, т, J=7,2 Гц), 1,97-1,79 (4H, м), 1,49 (3H, т, J=6,9 Гц).
Пример 241
N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-2-трифторметилбензамид, полученный в примере 25, растворяли в 1 мл диметилформамида. К смеси добавляли 30 мг гидрида натрия при охлаждении льдом и перемешивании и смесь перемешивали в течение 30 минут. К смеси добавляли 30 мг метилиодида и реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Затем к смеси добавляли воду и этилацетат и осуществляли экстракцию. Органический слой два раза промывали водой и концентрировали путем удаления растворителя при пониженном давлении. Остаток очищали хроматографией на силикагеле (н-гексан:этилацетат = 3:1) с получением 35 мг бесцветного маслянистого N-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-илметил]-N-метил-2-трифторметилбензамида.
1Н-ЯМР (CDCl3) δ: 7,72-7,34 (7H, м), 6,94 (1H, дд, J=8,4, 1,8 Гц), 4,88-4,11 (1H, м), 3,98-3,89 (5H, м), 3,17-2,88 (3H, м), 1,43-1,34 (1H, м), 0,71-0,64 (2H, м), 0,42-0,36 (2H, м).
Пример 242
С использованием 0,14 г [2-(3,4-диэтоксифенил)оксазол-4-илметил]метиламина, полученного в ссылочном примере 74, 70 мг бесцветного маслянистого N-[2-(3,4-диметоксифенил)оксазол-4-илметил]-2-этокси-N-метилбензамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 7,60-7,26 (5H, м), 7,00-6,87 (3H, м), 4,23-4,02 (8H, м), 3,19-2,96 (3H, м), 1,52-1,40 (6H, м), 1,36 (3H, т, J=6,9 Гц).
Пример 243
С использованием 0,2 г 2-[2-(3,4-диэтоксифенил)оксазол-4-ил]этиламина, полученного в ссылочном примере 78, и 0,18 г 2- этоксибензойной кислоты 0,14 г белого порошкообразного N-{2-[2-(3,4-диметоксифенил)оксазол-4-ил]этил}-2-этоксибензамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 8,22 (1H, дд, J=7,5, 4,8 Гц), 7,60-7,50 (2H, м), 7,47 (1H, с), 7,39 (1H, м), 7,06 (1H, м), 6,95-6,85 (2H, м), 4,30-4,05 (6H, м), 4,09 (2H, кв, J=6,9 Гц), 3,85 (2H, кв, J=6,6 Гц), 2,91 (2H, т, J=6,6 Гц), 1,48 (6H, т, J=6,9 Гц), 1,28 (6H, т, J=6,9 Гц).
Пример 244
С использованием 0,3 г 2-(3,4-диэтоксифенил)оксазол-4-карбоновой кислоты, полученной в ссылочном примере 80, и 0,28 г 1-(2-амино)этанона 0,32 г белого порошкообразного N-(2-оксо-2-фенилэтил)-2-(3,4-диэтоксифенил)оксазол-4-карбоксамида получали таким же способом, как в примере 1.
1Н-ЯМР (ДМСО-d6) δ: 8,67 (1H, д, J=0,9 Гц), 8,49 (1H, т, J=5,7 Гц), 8,10-8,00 (2H, м), 7,70-7,50 (5H, м), 7,16 (1H, м), 4,81 (2H, д, J=5,7 Гц), 4,13 (4H, кв, J=6,9 Гц), 1,38 (6H, т, J=6,9 Гц), 1,37 (3H, т, J=6,9 Гц).
Пример 245
С использованием 2-(3,4-диэтоксифенил)оксазол-4-карбоновой кислоты, полученной в ссылочном примере 80, 0,32 г белого порошкообразного 1-(4-{4-[2-(3,4-диэтоксифенил)оксазол-4-карбонил]пиперазин-1-ил}фенил)этанона получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 8,20 (1H, с), 7,95-7,85 (2H, м), 7,62 (1H, дд, J=8,4, 2,1 Гц), 7,54 (1H, д, J=2,1 Гц), 7,00-6,85 (3H, м), 4,40-4,20 (2H, м), 4,19 (2H, кв, J=6,9 Гц), 4,16 (2H, кв, J=6,9 Гц), 4,00-3,80 (2H, м), 3,50-3,45 (4H, м), 2,53 (3H, с), 1,50 (3H, т, J=6,9 Гц), 1,50 (3H, т, J=6,9 Гц).
Пример 246
С использованием 0,28 г 2-(3,4-диэтоксифенил)оксазол-4-карбоновой кислоты, полученной в ссылочном примере 80, и 0,2 г 1-(4-метоксифенил)пиперазина 0,36 г белого порошкообразного 4-(2-(3,4-диэтоксифенил)оксазол-4-ил)-1-(4-метоксифенил)пиперазина получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 8,16 (1H, с), 7,61 (1H, дд, J=8,7, 2,1 Гц), 7,54 (1H, с), 6,95-6,84 (5H, м), 4,40-4,30 (2H, м), 4,21-4,12 (4H, м), 4,00-3,93 (2H, м), 3,78 (3H, с), 3,14 (4H, т, J=4,8 Гц), 1,47 (6H, т, J=7,2 Гц).
Пример 247
С использованием 0,28 г 2-(3,4-диэтоксифенил)оксазол-4-карбоновой кислоты, полученной в ссылочном примере 80, и 1-(4-гидроксифенил)пиперазина белый порошкообразный 4-(2-(3,4-диэтоксифенил)оксазол-4-ил)-1-(4-гидроксифенил)пиперазин получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 8,16 (1H, с), 7,61 (1H, дд, J=8,7, 2,1 Гц), 7,54 (1H, с), 6,95-6,78 (5H, м), 4,40-4,30 (2H, м), 4,21-4,12 (4H, м), 4,00-3,93 (2H, м), 3,14 (4H, т, J=4,8 Гц), 1,49 (6H, т, J=7,2 Гц).
Пример 248
С использованием 0,28 г 2-(3,4-диэтоксифенил)оксазол-4-карбоновой кислоты, полученной в ссылочном примере 80, и 0,14 г 2-фенилэтиламина 0,21 г белого порошкообразного N-фенетил-2-(3,4-диметоксифенил)оксазол-4-карбоксамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 8,17 (1H, с), 7,56 (1H, дд, J=8,4, 2,1 Гц), 7,50 (1H, д, J=2,1 Гц), 7,36-7,21 (5H, м), 7,12 (1H, ушир.с), 6,93 (1H, д, J=8,4 Гц), 4,22-4,12 (4H, м), 3,74-3,66 (2H, м), 2,95 (2H, т, J=7,2 Гц), 1,57-1,46 (6H, м).
Пример 249
С использованием 0,28 г 2-(3,4-диэтоксифенил)оксазол-4-карбоновой кислоты, полученной в ссылочном примере 80, и 0,13 г 1-(2-аминоэтил)пирролидина 0,15 г бледно-желтого порошкообразного N-(2-(пирролидин-1-ил)этил)-2-(3,4-диметоксифенил)оксазол-4-карбоксамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 8,17 (1H, с), 7,60 (1H, дд, J=8,4, 1,8 Гц), 7,55 (1H, д, J=1,8 Гц), 7,44 (1H, ушир.с), 6,92 (1H, д, J=8,4 Гц), 4,23-4,12 (4H, м), 3,65-3,58 (2H, м), 2,79 (2H, т, J=6,6 Гц), 2,70-2,58 (4H, м), 1,87-1,75 (4H, м), 1,53-1,46 (6H, м).
Пример 250
С использованием 0,15 г [2-(3,4-диэтоксифенил)оксазол-4-ил]уксусной кислоты, полученной в ссылочном примере 81, и 0,11 г o-фенетидина 0,12 г белого порошкообразного 2-[2-(3,4-диэтоксифенил)оксазол-4-ил]-N-(2-этоксифенил)ацетамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 8,74 (1H, ушир.с), 8,37 (1H, дд, J=7,2, 1,8 Гц), 7,70-7,65 (2H, м), 7,61(1H, д, J=1,8 Гц), 7,00-6,90 (3H, м), 6,80 (1H, дд, J=7,8, 1,2 Гц), 4,18 (2H, кв, J=6,9 Гц), 4,16 (2H, кв, J=6,9 Гц), 3,97 (2H, кв, J=7,2 Гц), 3,74(2H, с), 1,49 (3H, т, J=6,9 Гц), 1,49 (3H, т, J=6,9 Гц), 1,18 (3H, т, J=7,2 Гц).
Пример 251
С использованием 0,15 г [2-(3,4-диэтоксифенил)оксазол-4-ил]уксусной кислоты, полученной в ссылочном примере 81, и 85 мг 2-амино-3-гидроксипиридина 0,11 г белого порошкообразного 2-[2-(3,4-диэтоксифенил)оксазол-4-ил]-N-(3-гидроксипиридин-2-ил)ацетамида получали таким же способом, как в примере 1.
1Н-ЯМР (CDCl3) δ: 10,37 (1H, ушир.с), 9,88 (1H, ушир.с), 7,84 (1H, дд, J=4,8, 1,2 Гц), 7,65-7,60 (3H, м), 7,31 (1H, дд, J=4,2, 1,2 Гц), 6,94 (1H, д, J=9,0 Гц), 4,22 (2H, кв, J=6,9 Гц), 4,16 (2H, кв, J=6,9 Гц), 1,51 (3H, т, J=6,9 Гц), 1,49 (3H, т, J=6,9 Гц).
Пример 252
0,5 г 4-хлорметил-2-(3,4-диэтоксифенил)оксазола, полученного в ссылочном примере 35, 0,36 г пиперазин-2-она и 0,28 г карбоната калия добавляли к 10 мл ацетонитрила и смесь нагревали и кипятили с обратным холодильником в течение 7 часов. Остаток разбавляли этилацетатом и промывали водой, а затем насыщенным солевым раствором. Органический слой сушили над безводным сульфатом магния и концентрировали путем удаления растворителя при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (дихлорметан:метанол = 1:0 до 50:1) и полученные неочищенные кристаллы перекристаллизовывали из этилацетата с получением 0,25 г бесцветного кристаллического 4-[2-(3,4-диэтоксифенил)оксазол-4-илметил]пиперазин-2-она.
1Н-ЯМР (CDCl3) δ: 7,59 (1H, д, J=8,1, 2,1 Гц), 7,56 (1H, д, J=2,1 Гц), 6,91 (1H, д, J=8,1 Гц), 6,03 (1H, ушир.с), 4,17 (2H, кв, J=6,9 Гц), 4,15 (2H, кв, J=6,9 Гц), 3,61 (2H, с), 3,45-3,35 (2H, м), 3,27 (2H, с), 2,80-2,75 (2H, м), 1,48 (6H, т, J=6,9 Гц).
Пример 253
С использованием 0,5 г 4-хлорметил-2-(3,4-диэтоксифенил)оксазола, полученного в ссылочном примере 35, и 0,5 г морфолина 0,31 г белого порошкообразного 4-[2-(3,4-диэтоксифенил)оксазол-4-илметил]морфолина получали таким же способом, как в примере 252.
1Н-ЯМР (CDCl3) δ: 7,70-7,50 (2H, м), 7,54 (1H, с), 6,91 (1H, д, J=8,4 Гц), 4,25-4,10 (4H, м), 3,80-3,70 (4H, м), 3,51 (2H, с), 2,60-2,50 (4H, м), 1,48 (6H, т, J=6,9 Гц).
Пример 254
0,5 г 4-хлорметил-2-(3,4-диэтоксифенил)оксазола, полученного в ссылочном примере 35, 0,28 г 2-меркаптопиридина и 0,28 г карбоната калия добавляли к 10 мл диметилформамида и смесь перемешивали при комнатной температуре в течение 24 часов. Реакционную смесь разбавляли этилацетатом и промывали водой, а затем с насыщенным солевым раствором. Органический слой сушили над безводным сульфатом магния и концентрировали путем удаления растворителя при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат:н-гексан = 1:4 до 1:2) и полученные неочищенные кристаллы перекристаллизовывали из смеси этилацетата и н-гексана с получением 0,63 г бесцветного кристаллического 2-[2-(3,4-диэтоксифенил)оксазол-4-илметилсульфанил]пиридина.
1Н-ЯМР (CDCl3) δ: 8,45 (3H, м), 7,60-7,50 (3H, м), 7,47 (1H, м), 7,18 (1H, д, J=8,1 Гц), 6,99 (1H, м), 6,89 (1H, д, J=8,1 Гц), 4,38 (2H, с), 4,17 (2H, кв, J=6,9 Гц), 4,14 (2H, кв, J=6,9 Гц), 1,47 (6H, т, J=6,9 Гц).
Пример 255
0,58 г 2-[2-(3,4-диэтоксифенил)оксазол-4-илметилсульфанил]пиридина, полученного в примере 254, добавляли к 20 мл дихлорметана. К смеси постепенно добавляли 0,55 г мета-хлорпербензойной кислоты при охлаждении льдом и смесь затем перемешивали. Реакционную смесь разбавляли 30 мл дихлорметана и промывали с 10%-ным водным раствором гидроксида натрия, а затем насыщенным солевым раствором. Органический слой сушили над безводным сульфатом магния и концентрировали путем удаления растворителя при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат:н-гексан = 2:1 до 3:1) и полученные неочищенные кристаллы перекристаллизовывали из смеси этилацетата и н-гексана с получением 0,49 г бесцветного кристаллического 2-[2-(3,4-диэтоксифенил)оксазол-4-илметансульфонил]пиридина.
1Н-ЯМР (CDCl3) δ: 8,81 (1H, м), 8,00 (1H, м), 7,91 (1H, м), 7,61 (1H, с), 7,55 (1H, м), 7,50-7,40 (2H, м), 6,87 (1H, д, J=8,4 Гц), 4,71 (2H, с), 4,13 (4H, кв, J=6,9 Гц), 1,47 (6H, т, J=6,9 Гц).
Пример 256
0,27 г [2-(3,4-диэтоксифенил)оксазол-4-ил]метиламина, полученного в ссылочном примере 37, и 0,3 мл триэтиламина растворяли в 10 мл ацетонитрила. К смеси добавляли 0,19 г o-толуолсульфонилхлорида и смесь перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой два раза промывали водой и растворитель удаляли. Полученный остаток очищали с использованием колонки с силикагелем (н-гексан:этилацетат = 1:1). Полученные неочищенные кристаллы перекристаллизовывали из смеси н-гексана и этилацетата с получением 0,3 г белого порошкообразного N-[2-(3,4-диэтоксифенил)оксазол-4-илметил]-2-метилбензолсульфонамида.
1Н-ЯМР (CDCl3) δ: 7,96 (1H, дд, J=7,5, 1,5 Гц), 7,48-7,16 (6H, м), 6,90 (1H, д, J=8,4 Гц), 5,11 (1H, ушир.с), 4,21-4,11 (6H, м), 2,64 (3H, с), 1,52-1,46 (6H, м).
Пример 257
0,5 г 3-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-она, полученного в примере 102, и 0,18 мл гидразинмоногидрата добавляли к диэтиленгликолю. К смеси добавляли 0,14 г гидроксида калия и смесь перемешивали при 150°C в течение 1 часа. Реакционной смеси давали охладиться, затем к смеси добавляли воду и осуществляли экстракцию этилацетатом. Осуществляли сушку с использованием безводного сульфата магния и растворитель удаляли. Остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 4:1) с получением 0,1 г бесцветного маслянистого 2-(3-циклопропилметокси-4-метоксифенил)-4-[3-(2-этоксифенил)пропил]оксазола.
1Н-ЯМР (CDCl3) δ: 7,58 (1H, дд, J=8,4, 1,8 Гц), 7,51 (1H, д, J=1,8 Гц), 7,39 (1H, с), 7,17-7,12 (2H, м), 6,93-6,81 (3H, м), 4,03 (2H, кв, J=6,9 Гц), 3,94-3,92 (5H, м), 2,72 (2H, т, J=7,5 Гц), 2,62 (2H, т, J=7,5 Гц), 2,03-1,96 (2H, м), 1,43-1,25 (4H, м), 0,69-0,63 (2H, м), 0,40-0,35 (2H, м).
Пример 258
1,6 г гидрида натрия суспендировали в 100 мл тетрагидрофурана. К смеси при охлаждении льдом и перемешивании последовательно добавляли 2,68 г 1-(2-метилфенил)этанона и 6,58 г 2-(3-бензилокси-4-метоксифенил)-4-хлорметилоксазола, полученного в ссылочном примере 5, и смесь нагревали и кипятили с обратным холодильником в течение 4 часов. К смеси добавляли насыщенный водный раствор хлорида аммония при охлаждении льдом. После перемешивания в течение 15 минут к смеси добавляли воду и осуществляли экстракцию этилацетатом. Затем осуществляли сушку с использованием безводного сульфата магния и растворитель удаляли. Остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 4:1) и 1,6 г полученного неочищенного продукта растворяли в 20 мл этанола. К смеси добавляли 0,16 г 10% палладия-на-углероде в виде порошка и смесь перемешивали в атмосфере водорода в течение 18 часов. Реакционную смесь фильтровали и полученный фильтрат концентрировали. Остаток очищали колоночной хроматографией на силикагеле (дихлорметан:этанол = 100:1) с получением 0,47 г желтого маслянистого 2-(3-гидрокси-4-метоксифенил)-4-(3-o-толилпропил)оксазола.
1Н-ЯМР (CDCl3) δ: 7,60-7,54 (2H, м), 7,38 (1H, с), 7,15-7,08 (4H, м), 6,90 (1H, д, J=8,4 Гц), 5,65 (1H, с), 3,94 (3H, с), 2,72-2,62 (4H, м), 2,37 (3H, с).
Пример 259
С использованием 0,47 г 2-(3-гидрокси-4-метоксифенил)-4-(3-o-толилпропил)оксазола, полученного в примере 258, 0,37 г бесцветного маслянистого 2-(3-циклопропилметокси-4-метоксифенил)-4-(3-o-толилпропил)оксазола получали таким же способом, как в примере 111.
1Н-ЯМР (CDCl3) δ: 7,58 (1H, дд, J=8,1, 2,1 Гц), 7,51 (1H, д, J=2,1 Гц), 7,38 (1H, с), 7,15-7,08 (4H, м), 6,92 (1H, д, J=8,1 Гц), 3,94-3,92 (5H, м), 2,72-2,62 (4H, м), 2,31 (3H, с), 2,04-1,92 (2H, м), 1,40-1,35 (1H, м), 0,69-0,63 (2H, м), 0,40-0,35 (2H, м).
Пример 260
0,21 г 3-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-она, полученного в примере 102, добавляли к 5 мл этанола и смесь перемешивали при охлаждении льдом. К смеси постепенно добавляли 37 мг боргидрида натрия. После того как температура реакционной смесь достигала комнатной температуры, осуществляли перемешивание в течение 2 часов. К реакционной смеси добавляли 5н. водный раствор хлористоводородной кислоты и растворитель затем удаляли. Осуществляли экстракцию дихлорметаном и экстракт промывали насыщенным солевым раствором. Экстракт затем сушили над безводным сульфатом магния, растворитель удаляли и остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1) с получением 0,18 г бесцветного маслянистого 3-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-ола.
1Н-ЯМР (CDCl3) δ: 7,58 (1H, дд, J=8,4, 2,1 Гц), 7,50 (1H, д, J=1,8 Гц), 7,39-7,35 (2H, м), 7,23-7,18 (1H, м), 6,97-6,84 (3H, м), 5,00 (1H, ушир.с), 4,07 (2H, кв, J=6,6 Гц), 3,94-3,92 (5H, м), 3,44 (1H, ушир.с), 2,80-2,60 (2H, м), 2,20-2,15 (2H, м), 1,43-1,37 (4H, м), 0,69-0,63 (2H, м), 0,40-0,37 (2H, м).
Пример 261
80 мг 3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она, полученного в примере 139, растворяли в 3 мл диметилформамида. К смеси добавляли 0,2 г гидрида натрия при охлаждении льдом и перемешивании и смесь перемешивали в течение 30 минут. К смеси добавляли 75 мг метилиодида и реакционную смесь перемешивали при комнатной температуре в течение 8 часов. К реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой два раза промывали водой и растворитель удаляли. Полученный остаток очищали с использованием колонки с силикагелем (н-гексан:этилацетат = 3:1) с получением 35 мг бесцветного маслянистого 3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]-2,2-диметил-1-(3-метилпиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,41 (1H, дд, J=4,5, 1,2 Гц), 7,38-7,60 (3H, м), 7,34 (1H, с), 7,21-7,24 (1H, м), 6,90 (1H, д, J=8,7 Гц), 4,63 (1H, септ., J=6,0 Гц), 3,94 (3H, с), 3,15 (2H, с), 2,28 (3H, с), 1,38-1,49 (12H, м).
Пример 262
С использованием 0,9 г метил 3-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}пропионата, полученного в ссылочном примере 83, 1,05 г желтого маслянистого метил 3-(3-метоксипиридин-2-ил)-2-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}-3-оксопропината получали таким же способом, как в примере 100.
1Н-ЯМР (CDCl3) δ: 8,25 (1H, дд, J=4,5, 1,5 Гц), 7,65 (1H, дд, J=8,4, 2,1 Гц), 7,55 (1H, д, J=2,1 Гц), 7,47-7,33 (3H, м), 6,94 (1H, д, J=8,4 Гц), 5,17 (1H, т, J=6,9 Гц), 4,43 (2H, кв, J=8,4 Гц), 3,93 (3H, с), 3,92 (3H, с), 3,65 (3H, с), 3,32-3,23 (2H, м).
Пример 263
С использованием 0,7 г метил 3-(3-метоксипиридин-2-ил)-2-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}-3-оксопропионата, полученного в примере 262, 0,42 г бесцветного маслянистого метил 2-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}-2-метил-3-(3-метилпиридин-2-ил)-3-оксопропината получали таким же способом, как в примере 261.
1Н-ЯМР (CDCl3) δ: 8,18 (1H, дд, J=6,9, 1,8 Гц), 7,64 (1H, дд, J=8,4, 2,1 Гц), 7,54 (1H, д, J=2,1 Гц), 7,42-7,34 (3H, м), 6,93 (1H, д, J=8,7 Гц), 4,43 (2H, кв, J=8,4 Гц), 3,93 (3H, с), 3,91 (3H, с), 3,64 (3H, с), 3,40 (1H, д, J=15 Гц), 3,26 (1H, д, J=15 Гц).
Пример 264
С использованием 0,42 г метил 2-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}-2-метил-3-(3-метилпиридин-2-ил)-3-оксопропината, полученного в примере 263, 0,25 г бесцветного маслянистого 1-(3-метоксипиридин-2-ил)-3-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}-2-метилпропан-1-она получали таким же способом, как в примере 136.
1Н-ЯМР (CDCl3) δ: 8,24 (1H, дд, J=4,5, 1,5 Гц), 7,67 (1H, дд, J=8,4, 2,1 Гц), 7,57 (1H, д, J=2,1 Гц), 7,43-7,28 (3H, м), 6,94 (1H, д, J=8,7 Гц), 4,45 (1H, кв, J=8,4 Гц), 4,21 (1H, кв, J=6,9 Гц), 3,91 (3H, с), 3,88 (3H, с), 3,15-3,06 (1H, м), 2,73-2,64 (1H, м), 1,23 (3H, д, J=7,2 Гц).
Пример 265
С использованием 0,2 г 1-(3-метоксипиридин-2-ил)-3-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}-2-метилпропан-1-она, полученного в примере 264, 80 мг бесцветного маслянистого 1-(3-метоксипиридин-2-ил)-3-{2-[4-метокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-ил}-2,2-диметилпропан-1-она получали таким же способом, как в примере 261.
1Н-ЯМР (CDCl3) δ: 8,17 (1H, дд, J=4,5, 1,5 Гц), 7,70 (1H, дд, J=8,4, 1,8 Гц), 7,60 (1H, д, J=1,8 Гц), 7,31-7,21 (2H, м), 6,96 (1H, д, J=8,4 Гц), 4,45 (2H, кв, J=8,4 Гц), 3,92 (3H, с), 3,78 (3H, с), 3,05 (2H, с), 1,34 (6H, с).
Пример 266
60 мл трифторуксусной кислоты перемешивали при охлаждении льдом, добавляли 12,3 г соединения, полученного в примере 231, и осуществляли перемешивание в течение одного часа. По завершении реакции реакционную смесь нейтрализовали добавлением насыщенного водного раствора бикарбоната натрия и к полученной смеси добавляли этилацетат. Органический слой дважды промывали водой, отделяли, концентрировали при пониженном давлении и полученные неочищенные кристаллы перекристаллизовывали из этанола с получением, таким образом, 5,9 г белого порошкообразного 3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]-1-(2-гидроксифенил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 12,2 (1H, с), 7,81 (1H, д, J=8,1 Гц), 7,62-7,26 (9H, м), 6,99-6,85 (3H, м), 5,19 (2H, с), 3,92 (3H, с), 3,43 (2H, т, J=7,5 Гц), 3,02 (2H, т, J=7,5 Гц).
Пример 267
С использованием соединения, полученного в примере 266, и хлордифторметана белый порошкообразный 3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]-1-(2-дифторметоксифенил)пропан-1-он получали, следуя процедуре примера 19.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, дд, J=7,8, 1,8 Гц), 7,90-6,60 (7H, м), 6,34 (1H, т, J=73,8 Гц), 5,20 (2H, с), 3,92 (3H, с), 3,36 (2H, т, J=7,2 Гц), 2,29 (2H, т, J=7,2 Гц).
Ссылочный пример 84
С использованием 2-фторэтанола бесцветный маслянистый 2-фторэтилметансульфонат получали, следуя процедуре, описанной в ссылочном примере 50.
1Н-ЯМР (CDCl3) δ: 4,76-4,73 (1H, м), 4,60-4,58 (1H, м), 4,53-4,50 (1H, м), 4,43-4,41 (1H, м), 3,08 (3H, с).
Ссылочный пример 85
С использованием 2,2-дифторэтанола бесцветный маслянистый 2,2-дифторэтилметансульфонат получали, следуя процедуре, описанной в ссылочном примере 50.
1Н-ЯМР (CDCl3) δ: 6,01 (1H, тт, J=54,3, 3,9 Гц), 4,38 (2H, тд, J=12,9, 3,9 Гц), 3,12 (3H, с).
Пример 268
С использованием соединения, полученного в примере 266, и соединения, полученного в ссылочном примере 84, белый порошкообразный 3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]-1-[2-(2-фторэтокси)фенил]пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,74 (1H, дд, J=7,8, 1,8 Гц), 7,61-7,59 (2H, м), 7,49-7,31 (7H, м), 7,07 (1H, т, J=7,8 Гц), 6,92 (2H, д, J=8,7 Гц), 5,20 (2H, с), 4,90-4,87 (1H, м), 4,74-4,71 (1H, м), 4,37-4,35 (1H, м), 4,28-4,26 (1H, м), 3,92 (3H, с), 3,44 (2H, т, J=7,5 Гц), 2,99 (2H, т, J=7,5 Гц).
Пример 269
С использованием соединения, полученного в примере 266, и соединения, полученного в ссылочном примере 85, белый порошкообразный 3-[2-(3-бензилокси-4-метоксифенил)оксазол-4-ил]-1-[2-(2,2-дифторэтокси)фенил]пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,74 (1H, дд, J=7,8, 1,8 Гц), 7,61-7,28 (9H, м), 7,08 (1H, т, J=7,8 Гц), 6,95-6,89 (2H, м), 6,22 (1H, тт, J=54,9, 3,9 Гц), 5,19 (2H, с), 4,29 (1H, тд, J=12,9, 3,9 Гц), 3,92 (3H, с), 3,38 (2H, т, J=7,5 Гц), 2,98 (2H, т, J=7,5 Гц).
Пример 270
С использованием соединения, полученного в примере 267, белый порошкообразный 1-(2-дифторметоксифенил)-3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]пропан-1-он получали, следуя процедуре примера 2.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, т, J=7,5 Гц), 7,54-7,41 (4H, м), 7,38-7,16 (2H, м), 6,89 (1H, д, J=8,1 Гц), 6,59 (1H, т, J=74,7 Гц), 5,69 (1H, с), 3,93 (3H, с), 3,36 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц).
Пример 271
С использованием соединения, полученного в примере 268, белый порошкообразный 1-[2-(2-фторэтокси)фенил]-3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]пропан-1-он получали, следуя процедуре примера 2.
1Н-ЯМР (CDCl3) δ: 7,73 (1H, дд, J=7,8, 1,8 Гц), 7,55-7,42 (4H, м), 7,05 (1H, т, J=7,8 Гц), 6,91 (2H, д, J=8,7 Гц), 4,91-4,88 (1H, м), 4,75-4,72 (1H, м), 4,38-4,35 (1H, м), 4,29-4,26 (1H, м), 3,94 (3H, с), 3,43 (2H, т, J=7,5 Гц), 2,99 (2H, т, J=7,5 Гц).
Пример 272
С использованием соединения, полученного в примере 269, белый порошкообразный 1-[2-(2,2-дифторэтокси)фенил]-3-[2-(3-гидрокси-4-метоксифенил)оксазол-4-ил]пропан-1-он получали, следуя процедуре примера 2.
1Н-ЯМР (CDCl3) δ: 7,73 (1H, дд, J=7,8, 1,8 Гц), 7,56-7,41 (4H, м), 7,08 (1H, т, J=7,8 Гц), 6,92-6,87 (2H, м), 6,21 (1H, тт, J=54,9, 3,9 Гц), 5,67 (1H, с), 4,29 (1H, тд, J=12,9, 3,9 Гц), 3,94 (3H, с), 3,38 (2H, т, J=7,2 Гц), 2,98 (2H, т, J=7,2 Гц).
Пример 273
С использованием соединения, полученного в примере 270, и 2-бромпропана белый порошкообразный 1-(2-дифторметоксифенил)-3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,70-7,25 (5H, м), 7,20-6,80 (2H, м), 6,59 (1H, т, J=73,5 Гц), 4,64 (1H, м), 3,93 (3H, с), 1,39 (3H, д, J=6,0 Гц).
Пример 274
С использованием соединения, полученного в примере 270, и этилиодида белый порошкообразный 1-(2-дифторметоксифенил)-3-[2-(3-этокси-4-метоксифенил)оксазол-4-ил]пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, дд, J=7,8, 1,8 Гц), 7,60-7,46 (3H, м), 7,42 (1H, с), 7,31-7,16 (2H, м), 6,91 (1H, д, J=8,1 Гц), 6,59 (1H, т, J=73,5 Гц), 4,18 (2H, кв, J=7,2 Гц), 3,92 (3H, с), 3,37 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,49 (3H, т, J=7,2 Гц).
Пример 275
С использованием соединения, полученного в примере 271, и 2-бромпропана белый порошкообразный 1-(2-фторэтоксифенил)-3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,73 (1H, д, J=7,2 Гц), 7,58-7,54 (2H, м), 7,45-7,41 (2H, м), 7,04 (1H, т, J=7,2 Гц), 6,92 (2H, т, J=8,1 Гц), 4,81 (2H, дт, J=47,4, 4,2 Гц), 4,64-4,60 (1H, м), 4,32 (2H, дт, J=23,1, 4,2 Гц), 3,89 (3H, с), 3,43 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,39 (6H, д, J=5,7 Гц).
Пример 276
С использованием соединения, полученного в примере 271, и 4-бром-1-бутена белый порошкообразный 3-[2-(3-бут-3-енилокси-4-метоксифенил)оксазол-4-ил]-1-[2-(2-фторэтокси)фенил]пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,73 (1H, д, J=7,5 Гц), 7,58-7,53 (2H, м), 7,45-7,42 (2H, м), 7,03 (1H, т, J=7,8 Гц), 6,92 (2H, т, J=8,4 Гц), 6,00-5,84 (1H, м), 5,21-5,09 (2H, м), 4,81 (2H, дт, J=47,4, 4,2 Гц), 4,32 (2H, дт, J=23,1, 4,2 Гц), 4,14 (2H, т, J=7,2 Гц), 3,90 (3H, с), 3,43 (2H, т, J=7,5 Гц), 3,00 (2H, т, J=7,5 Гц), 2,64-2,61 (2H, м).
Пример 277
С использованием соединения, полученного в примере 271, и изобутил бромида белый порошкообразный 1-[2-(2-фторэтокси)фенил]-3-[2-(3-изобутокси-4-метоксифенил)оксазол-4-ил]пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,73 (1H, дд, J=7,8, 1,8 Гц), 7,57-7,51 (2H, м), 7,48-7,42 (2H, м), 7,40 (1H, т, J=7,5 Гц), 6,92 (2H, т, J=8,7 Гц), 4,81 (2H, дт, J=47,4, 4,2 Гц), 4,32 (2H, дт, J=23,1, 4,2 Гц), 3,90 (3H, с), 3,84 (2H, д, J=6,9 Гц), 3,43 (2H, т, J=7,5 Гц), 3,00 (2H, т, J=7,5 Гц), 2,23-2,14 (1H, м), 1,04 (6H, д, J=5,7 Гц).
Пример 278
С использованием соединения, полученного в примере 272, и 2-бромпропана белый порошкообразный 1-[2-(2,2-дифторэтокси)фенил]-3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,74 (1H, дд, J=7,5, 1,8 Гц), 7,59-7,44 (3H, м), 7,41 (1H, с), 7,08 (1H, т, J=7,5 Гц), 6,91 (1H, д, J=8,4 Гц), 6,22 (1H, тт, J=54,6, 3,9 Гц), 4,65 (1H, септ., J=6,0 Гц), 4,29 (2H, тд, J=12,9, 3,9 Гц), 3,90 (3H, с), 3,38 (2H, т, J=7,5 Гц), 2,99 (2H, т, J=7,5 Гц), 1,40 (6H, д, J=6,0 Гц).
Пример 279
С использованием соединения, полученного в примере 272, и 1-бромпропана белый порошкообразный 1-[2-(2,2-дифторэтокси)фенил]-3-[2-(3-пропокси-4-метоксифенил)оксазол-4-ил]пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,74 (1H, дд, J=7,8, 1,8 Гц), 7,61-7,43 (3H, м), 7,41 (1H, с), 7,08 (1H, т, J=7,5 Гц), 6,92-6,89 (2H, м), 6,23 (1H, тт, J=54,6, 3,9 Гц), 4,29 (2H, тд, J=12,9, 3,9 Гц), 4,06 (2H, т, J=6,9 Гц), 3,91 (3H, с), 3,38 (2H, т, J=7,5 Гц), 2,99 (2H, т, J=7,5 Гц), 1,90 (2H, кв.т, J=7,2 Гц), 1,06 (3H, т, J=7,2 Гц).
Пример 280
С использованием соединения, полученного в примере 272, и этилиодида белый порошкообразный 1-[2-(2,2-дифторэтокси)фенил]-3-[2-(3-этокси-4-метоксифенил)оксазол-4-ил]пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,74 (1H, дд, J=7,8, 1,8 Гц), 7,61-7,44 (3H, м), 7,41 (1H, с), 7,08 (1H, т, J=7,8 Гц), 6,93-6,90 (2H, м), 6,23 (1H, тт, J=54,6, 3,9 Гц), 4,29 (2H, тд, J=12,9, 3,9 Гц), 4,18 (2H, кв, J=6,9 Гц), 3,92 (3H, с), 3,38 (2H, т, J=7,5 Гц), 2,99 (2H, т, J=7,5 Гц), 1,50 (3H, т, J=6,9 Гц).
Пример 281
С использованием соединения, полученного в примере 272, и аллилбромида белый порошкообразный 3-[2-(3-аллилокси-4-метоксифенил)оксазол-4-ил]-1-[2-(2,2-дифторэтокси)фенил]пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,74 (1H, дд, J=7,8, 1,8 Гц), 7,60-7,44 (3H, м), 7,41 (1H, с), 7,08 (1H, т, J=7,5 Гц), 6,94-6,89 (2H, м), 6,41-6,04 (2H, м), 5,44 (1H, дд, J=17,4, 1,5 Гц), 5,31 (1H, дд, J=10,2, 1,5 Гц), 4,29 (2H, тд, J=12,9, 3,9 Гц), 3,92 (3H, с), 3,38 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц).
Пример 282
С использованием соединения, полученного в примере 272, и 4-бром-1-бутена белый порошкообразный 3-[2-(3-бут-3-енилокси-4-метоксифенил)оксазол-4-ил]-1-[2-(2,2-дифторэтокси)фенил]пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,75 (1H, дд, J=7,8, 1,8 Гц), 7,60-7,44 (3H, м), 7,42 (1H, с), 7,09 (1H, т, J=7,5 Гц), 6,93-6,89 (2H, м), 6,23 (1H, тт, J=54,6, 3,9 Гц), 5,99-5,85 (1H, м), 5,23-5,10 (2H, м), 4,29 (2H, тд, J=12,9, 3,9 Гц), 4,14 (2H, т, J=7,2 Гц), 3,91 (3H, с), 3,39 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 2,68-2,60 (2H, м).
Пример 283
С использованием соединения, полученного в примере 272, и (бромметил)циклопропана белый порошкообразный 3-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]-1-[2-(2,2-дифторэтокси)фенил]пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,75 (1H, дд, J=7,8, 1,8 Гц), 7,58-7,44 (3H, м), 7,41 (1H, с), 7,09 (1H, т, J=7,5 Гц), 6,93-6,90 (2H, м), 6,24 (1H, тт, J=54,6, 3,9 Гц), 4,29 (2H, тд, J=12,9, 3,9 Гц), 3,94-3,91 (5H, м), 3,39 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 1,43-1,33 (1H, м), 0,70-0,63 (2H, м), 0,41-0,35 (2H, м).
Пример 284
С использованием соединения, полученного в примере 272, и соединения, полученного в ссылочном примере 85, белый порошкообразный 3-{2-[3-(2,2-дифторэтокси)-4-метоксифенил]оксазол-4-ил}-1-[2-(2,2-дифторэтокси)фенил]пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,74 (1H, дд, J=7,8, 1,8 Гц), 7,65 (1H, дд, J=7,8, 1,8 Гц), 7,50 (1H, д, J=2,1 Гц), 7,50-7,42 (1H, м), 7,42 (1H, с), 7,08 (1H, т, J=7,5 Гц), 6,96-6,89 (2H, м), 6,42-5,95 (2H, м), 4,35-4,23 (4H, м), 3,92 (3H, с), 3,39 (2H, т, J=7,5 Гц), 3,00 (2H, т, J=7,5 Гц).
Пример 285
С использованием соединения, полученного в примере 272, и изобутилбромида белый порошкообразный 1-[2-(2,2-дифторэтокси)фенил]-3-[2-(3-изобутокси-4-метоксифенил)оксазол-4-ил]пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,74 (1H, д, J=7,5 Гц), 7,57-7,44 (3H, м), 7,41 (1H, с), 7,08 (1H, т, J=7,5 Гц), 6,92-6,89 (2H, м), 6,23 (1H, тт, J=54,6, 3,9 Гц), 4,29 (2H, тд, J=12,9, 3,9 Гц), 3,90 (3H, с), 3,85 (2H, д, J=6,6 Гц), 3,38 (2H, т, J=7,5 Гц), 2,99 (2H, т, J=7,5 Гц), 2,19 (1H, кв.т, J=6,6 Гц), 1,05 (6H, д, J=6,6 Гц).
Пример 286
С использованием соединения, полученного в ссылочном примере 35, и соединения, полученного в ссылочном примере 70, бледно-желтый маслянистый 3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2-метоксиметоксифенил)пропан-1-он получали, следуя процедуре примера 190.
1Н-ЯМР (CDCl3) δ: 7,66 (1H, дд, J=7,8, 1,8 Гц), 7,56-7,38 (3H, м), 7,17 (1H, д, J=8,4 Гц), 7,04 (1H, т, J=7,5 Гц), 6,92-6,88 (2H, м), 5,26 (2H, с), 4,21-4,08 (4H, м), 3,49 (3H, с), 3,40 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,51-1,45 (6H, м).
Пример 287
С использованием соединения, полученного в примере 286, белый порошкообразный 3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2-гидроксифенил)пропан-1-он получали, следуя процедуре примера 266.
1Н-ЯМР (CDCl3) δ: 12,25 (1H, с), 7,82 (1H, дд, J=8,1, 1,5 Гц), 7,60-7,43 (4H, м), 6,98 (1H, д, J=8,4 Гц), 6,92-6,86 (2H, м), 4,21-4,10 (4H, м), 3,44 (2H, т, J=7,2 Гц), 3,03 (2H, т, J=7,2 Гц), 1,51-1,43 (6H, м).
Пример 288
С использованием соединения, полученного в примере 287, и хлордифторметана белый порошкообразный 3-[2-(3,4-диэтоксифенилоксазол-4-ил)-1-(2-дифторметоксифенил)пропан-1-он получали, следуя процедуре примера 19.
1Н-ЯМР (CDCl3) δ: 7,51 (1H, д, J=8,7 Гц), 7,60-7,45 (3H, м), 7,30 (1H, с), 7,28-7,19 (2H, м), 6,90 (1H, д, J=8,7 Гц), 6,58 (1H, т, J=75 Гц), 4,15 (4H, кв, J=7,2 Гц) 3,36 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,47 (6H, т, J=7,2 Гц).
Пример 289
С использованием соединения, полученного в примере 287, и соединения, полученного в ссылочном примере 84, белый порошкообразный 3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-[2-(2-фторэтокси)фенил]пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,74 (1H, дд, J=7,8, 1,8 Гц), 7,56-7,41 (4H, м), 7,04 (1H, тд, J=7,5, 0,9 Гц), 6,95-6,88 (2H, м), 4,81 (2H, дт, J=47,1, 4,2 Гц), 4,32 (2H, дт, J=27,3, 4,2 Гц), 4,21-4,10 (4H, м), 3,43 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,50-1,45 (6H, м).
Пример 290
С использованием соединения, полученного в примере 287, и соединения, полученного в ссылочном примере 85, белый порошкообразный 3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-[2-(2,2-дифторэтокси)фенил]пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,74 (1H, дд, J=7,5, 1,8 Гц), 7,56-7,43 (3H, м), 7,41 (1H, с), 7,08 (1H, т, J=7,5 Гц), 6,90 (1H, д, J=7,8 Гц), 6,23 (1H, тт, J=54,9, 3,9 Гц), 4,29 (2H, тд, J=13,2, 3,9 Гц), 4,21-4,10 (4H, м), 3,38 (2H, т, J=7,5 Гц), 2,98 (2H, т, J=7,5 Гц), 1,50-1,45 (6H, м).
Пример 291
0,2 г соединения, полученного в примере 223, и 0,1 мл триэтиламина растворяли в 5 мл дихлорметана, к полученному раствору добавляли 0,1 мл ацетилхлорида и смесь перемешивали в течение 6 часов при комнатной температуре. По завершении реакции к реакционной смеси добавляли воду и полученную смесь экстрагировали этилацетатом. Органический слой дважды промывали водой и растворитель отгоняли дистилляцией. Остаток очищали с использованием колонки с силикагелем (н-гексан:этилацетат = 2:1) и полученные неочищенные кристаллы перекристаллизовывали из этанола с получением, таким образом, 15 мг белого порошкообразного 2-{3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]пропионил}фенилацетата.
1Н-ЯМР (CDCl3) δ: 7,83 (1H, дд, J=7,8, 1,5 Гц), 7,60-7,50 (3H, м), 7,42 (1H, с), 7,34-7,28 (1H, м), 7,12 (1H, дд, J=8,1, 0,9 Гц), 6,92 (1H, д, J=8,4 Гц), 4,69-4,61 (1H, м), 3,90 (3H, с), 3,32 (2H, т, J=7,2 Гц), 2,97 (2H, т, J=7,2 Гц), 2,35 (3H, с), 1,40 (6H, д, J=6,0 Гц).
Пример 292
С использованием соединения, полученного в ссылочном примере 35, и 1-(2-трифторметоксифенил)этанона белый порошкообразный 3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2-трифторметоксифенил)пропан-1-он получали, следуя процедуре примера 190.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,8, 1,8 Гц), 7,58-7,41 (3H, м), 7,38 (1H, с), 7,35-7,29 (2H, м), 6,90 (1H, д, J=8,4 Гц), 4,20-4,10 (4H, м), 3,34 (2H, т, J=6,9 Гц), 3,00 (2H, т, J=6,9 Гц), 1,48 (6H, т, J=6,9 Гц).
Пример 293
С использованием соединения, полученного в ссылочном примере 11, и 1-(2-трифторметоксифенил)этанона белый порошкообразный 3-[2-(3-циклопропилметокси-4-метоксифенил)оксазол-4-ил]-1-(2-трифторметоксифенил)пропан-1-он получали, следуя процедуре примера 190.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, д, J=8,7 Гц), 7,57-7,53 (3H, м), 7,49 (1H, с), 7,42-7,30 (2H, м), 6,90 (1H, д, J=8,7 Гц), 3,94-3,91 (5H, м), 3,34 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,42-1,30 (1H, м), 0,67-0,64 (2H, м), 0,40-0,36 (2H, м).
С использованием соединения, полученного в ссылочном примере 35, и соответствующих производных ацетофенона получали соединения примеров 294-299, следуя процедуре примера 190.
Пример 294
3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2,5-диметоксифенил)пропан-1-он
Белый порошок
1Н-ЯМР (CDCl3) δ: 7,57-7,52 (2H, м), 7,40 (1H, с), 7,01 (1H, дд, J=9,0, 3,3 Гц), 6,90 (2H, т, J=8,4 Гц), 4,20-4,10 (4H, м), 3,85 (3H, с), 3,78 (3H, с), 3,39 (2H, т, J=7,2 Гц), 2,98 (2H, т, J=7,2 Гц), 1,47 (6H, т, J=6,9 Гц).
Пример 295
3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2-этокси-5-метилфенил)пропан-1-он
Белый порошок
1Н-ЯМР (CDCl3) δ: 7,61-7,49 (3H, м), 7,40 (1H, с), 7,25-7,20 (2H, м), 6,90 (1H, д, J=8,1 Гц), 6,83 (1H, д, J=8,4 Гц), 4,21-4,06 (6H, м), 3,41 (2H, т, J=7,5 Гц), 2,99 (2H, т, J=7,5 Гц), 2,28 (3H, с), 1,53-1,40 (9H, м).
Пример 296
3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2,4-диметилфенил)пропан-1-он
Бесцветный порошок
1Н-ЯМР (CDCl3) δ: 7,63 (1H, д, J=8,4 Гц), 7,54 (1H, дд, J=8,4, 1,8 Гц), 7,51 (1H, д, J=1,8 Гц), 7,42 (1H, с), 7,06-7,02 (2H, м), 6,90 (1H, д, J=8,4 Гц), 4,17 (2H, кв, J=6,9 Гц), 4,14 (2H, кв, J=6,9 Гц), 3,30 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 2,49 (3H, с), 2,34 (3H, с), 1,48 (6H, т, J=6,9 Гц).
Пример 297
3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2,5-диметилфенил)пропан-1-он
Бесцветные игольчатые кристаллы
1Н-ЯМР (CDCl3) δ: 7,55 (1H, ушир.с, J=8,7 Гц), 7,52 (1H, ушир.с), 7,44 (1H, ушир.д, J=8,7 Гц), 7,17-7,09 (2H, м), 6,90 (1H, д, J=8,7 Гц), 4,17 (2H, кв, J=6,9 Гц), 4,14 (2H, кв, J=6,9 Гц), 3,29 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 2,44 (3H, с), 2,33 (3H, с), 1,47 (6H, т, J=6,9 Гц).
Пример 298
3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2-этокси-4-метилфенил)пропан-1-он
Белый порошок
1Н-ЯМР (CDCl3) δ: 7,66 (1H, д, J=7,8 Гц), 7,60-7,51 (2H, м), 7,39 (1H, с), 6,90 (1H, д, J=8,4 Гц), 6,79 (1H, д, J=8,4 Гц), 6,73 (1H, с), 4,21-4,08 (6H, м), 3,40 (2H, т, J=7,2 Гц), 2,98 (2H, т, J=7,2 Гц), 2,36 (3H, с), 1,53-1,45 (9H, м).
Пример 299
3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2-этокси-4-фторфенил)пропан-1-он
Бесцветные игольчатые кристаллы
1Н-ЯМР (CDCl3) δ: 7,78 (1H, дд, J=8,7, 7,2 Гц), 7,54 (1H, дд, J=8,4, 2,1 Гц), 7,51 (1H, д, J=2,1 Гц), 7,39 (1H, ушир.с), 6,90 (1H, д, J=8,4 Гц), 6,71-6,61 (2H, м), 4,16 (2H, кв, J=6,9 Гц), 4,14 (2H, кв, J=6,9 Гц), 4,11 (2H, кв, J=6,9 Гц), 3,39 (2H, т, J=7,2 Гц), 2,98 (2H, т, J=7,2 Гц), 1,49 (3H, т, J=6,9 Гц), 1,47 (6H, т, J=6,9 Гц).
Пример 300
Использовали соединение, полученное в ссылочном примере 54, и метил (2-метоксиметил)бензоат и обрабатывали, следуя процедуре примера 100, с последующей обработкой в соответствии со ссылочным примером 48 с получением белого порошкообразного 3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2-метоксиметилфенил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,74 (1H, дд, J=7,8, 1,2 Гц), 7,64-7,27 (6H, м), 6,91 (1H, д, J=8,4 Гц), 4,73 (2H, с), 4,21-4,10 (4H, м), 3,43 (3H, с), 3,34 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,51-1,43 (6H, м).
С использованием соединения, полученного в ссылочном примере 54, и соответствующих метилбензоатных производных получали соединения примеров 301-303, следуя процедуре примера 300.
Пример 301
3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2-этилфенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,62-7,51 (4H, м), 7,43 (1H, с), 7,38-7,30 (2H, м), 6,90 (1H, д, J=8,7 Гц), 4,18-4,13 (4H, м), 3,31 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 2,81 (2H, кв, J=7,5 Гц), 1,48 (6H, т, J=6,9 Гц), 1,20 (3H, т, J=7,5 Гц).
Пример 302
3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2,3-диметоксифенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,56-7,51 (2H, м), 7,41 (1H, с), 7,18-7,01 (3H, м), 6,90 (1H, д, J=8,4 Гц), 4,21-4,10 (4H, м), 3,89 (6H, с), 3,38 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 1,48 (6H, т, J=6,9 Гц).
Пример 303
3-[2-(3,4-диэтоксифенил)оксазол-4-ил]-1-(2-этокси-3-метилфенил)пропан-1-он
1Н-ЯМР (CDCl3) δ: 7,55-7,51 (2H, м), 7,40 (1H, с), 7,36-7,29 (2H, м), 7,04 (1H, т, J=7,2 Гц), 6,90 (1H, д, J=8,1 Гц), 4,20-4,11 (4H, м), 3,83 (2H, кв, J=7,5 Гц), 3,39 (2H, т, J=7,2 Гц), 2,98 (2H, т, J=7,2 Гц), 2,30 (3H, с), 1,48 (6H, т, J=6,9 Гц), 1,26 (3H, т, J=6,9 Гц).
Пример 304
С использованием соединения, полученного в ссылочном примере 58, и 1-(2-этокси-4-фторфенил)этанона бледно-желтый порошкообразный 1-(2-этокси-4-фторфенил)-3-[2-(3-этокси-4-метоксифенил)оксазол-4-ил]пропан-1-он получали, следуя процедуре примера 190.
1Н-ЯМР (CDCl3) δ: 7,77 (1H, т, J=7,8 Гц), 7,56 (1H, дд, J=8,4, 1,8 Гц), 7,51 (1H, д, J=1,8 Гц), 7,40 (1H, с), 6,91 (1H, д, J=8,4 Гц), 6,71-6,61 (2H, м), 4,21-4,07 (4H, м), 3,92 (3H, с), 3,39 (2H, т, J=7,2 Гц), 2,98 (2H, т, J=7,2 Гц), 1,52-1,47 (6H, м).
Пример 305
С использованием соединения, полученного в ссылочном примере 58, и 1-(4-фтор-2-изопропоксифенил)этанона бесцветный маслянистый 3-[2-(3-этокси-4-метоксифенил)оксазол-4-ил]-1-(4-фтор-2-изопропоксифенил)пропан-1-он получали, следуя процедуре примера 190.
1Н-ЯМР (CDCl3) δ: 7,77 (1H, т, J=7,8 Гц), 7,57 (1H, дд, J=8,4, 1,8 Гц), 7,51 (1H, д, J=1,8 Гц), 7,40 (1H, с), 6,91 (1H, д, J=8,4 Гц), 6,71-6,61 (2H, м), 4,63 (1H, септ., J=6,0 Гц), 4,18 (2H, кв, J=6,9 Гц), 3,92 (3H, с), 3,38 (2H, т, J=7,2 Гц), 2,98 (2H, т, J=7,2 Гц), 1,50 (3H, т, J=6,9 Гц), 1,42 (6H, д, J=6,0 Гц).
Пример 306
С использованием соединения, полученного в ссылочном примере 68, и 1-(2-этокси-5-метилфенил)этанона белый порошкообразный 1-(2-этокси-5-метилфенил)-3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]пропан-1-он получали, следуя процедуре примера 190.
1Н-ЯМР (CDCl3) δ: 7,60-7,40 (3H, м), 7,39 (1H, с), 7,24-7,19 (1H, м), 6,91 (1H, д, J=8,1 Гц), 6,83 (1H, д, J=8,4 Гц), 4,69-4,58 (1H, м), 4,10 (2H, кв, J=6,9 Гц), 3,89 (3H, с), 3,41 (2H, т, J=7,2 Гц), 2,98 (2H, т, J=7,2 Гц), 2,29 (3H, с), 1,48-1,38 (9H, м).
Пример 307
С использованием соединения, полученного в ссылочном примере 68, и 1-(2-этокси-4-метилфенил)этанона белый порошкообразный 1-(2-этокси-4-метилфенил)-3-[2-(3-изопропокси-4-метоксифенил)оксазол-4-ил]пропан-1-он получали, следуя процедуре примера 190.
1Н-ЯМР (CDCl3) δ: 7,66 (1H, д, J=8,1 Гц), 7,59-7,53 (2H, м), 7,39 (1H, с), 6,91 (1H, д, J=8,4 Гц), 6,79 (1H, д, J=8,1 Гц), 6,73 (1H, с), 4,58-4,71 (1H, м), 4,12 (2H, кв, J=6,9 Гц), 3,90 (1H, с) 3,40 (2H, т, J=7,5 Гц), 2,98 (2H, т, J=7,5 Гц), 2,36 (3H, с), 1,48 (3H, т, J=6,9 Гц), 1,40 (6H, д, J=6,0 Гц).
Пример 308
С использованием соединения, полученного в примере 136, и хлордифторметана белый порошкообразный 3-[2-(3-дифторметокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он получали, следуя процедуре примера 4.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, м), 7,83 (1H, дд, J=8,4, 2,1 Гц), 7,78 (1H, д, J=2,1 Гц), 7,58 (1H, д, J=7,8 Гц), 7,47 (1H, с), 7,32 (1H, м), 7,00 (1H, д, J=8,4 Гц), 6,58 (1H, т, J=74,7 Гц), 3,93 (3H, с), 3,59 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 2,57 (3H, с).
Пример 309
С использованием соединения, полученного в примере 136, и соединения, полученного в ссылочном примере 85, белый порошкообразный 3-{2-[3-(2,2-дифторэтокси)-4-метоксифенил]оксазол-4-ил}-1-(3-метилпиридин-2-ил)пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,5, 0,9 Гц), 7,66 (1H, дд, J=8,4, 2,1 Гц), 7,60-7,54 (2H, м), 7,46 (1H, с), 7,35-7,31 (1H, м), 6,94 (1H, д, J=8,7 Гц), 6,16 (1H, тт, J=54,9, 1,2 Гц) 4,29 (2H, тд, J=12,9, 1,2 Гц), 3,92 (3H, с), 3,61 (2H, т, J=6,9 Гц), 3,01 (2H, т, J=6,9 Гц), 2,58 (3H, с).
Пример 310
С использованием соединения, полученного в примере 136, и соединения, полученного в ссылочном примере 84, белый порошкообразный 3-{2-[3-(2-фторэтокси)-4-метоксифенил]оксазол-4-ил}-1-(3-метилпиридин-2-ил)пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,50-8,49 (1H, м), 7,63-7,54 (3H, м), 7,45 (1H, с), 7,34-7,27 (1H, м), 6,93 (1H, д, J=8,7 Гц), 4,88 (1H, т, J=4,2 Гц), 4,72 (1H, т, J=4,2 Гц) 4,39 (1H, т, J=4,2 Гц), 4,30 (1H, т, J=4,2 Гц), 3,92 (3H, с), 3,60 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 2,57 (3H, с).
Пример 311
С использованием соединения, полученного в примере 136, и 2-бромбутана желтый маслянистый 3-[2-(3-втор-бутокси-4-метоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,5, 1,2 Гц), 7,59-7,55 (3H, м), 7,54 (1H, с), 7,45-7,30 (1H, м), 6,91 (1H, д, J=8,4 Гц), 4,43-4,37 (1H, м), 3,89 (3H, с), 3,60 (2H, т, J=7,5 Гц), 3,01 (2H, т, J=7,5 Гц), 2,57 (3H, с), 1,86-1,62 (2H, м), 1,34 (3H, д, J=6,6 Гц), 1,00 (3H, т, J=6,6 Гц).
Пример 312
С использованием соединения, полученного в примере 136, и 3-бромпентана белый порошкообразный 3-{2-[3-(1-этилпропокси)-4-метоксифенил]оксазол-4-ил}-1-(3-метилпиридин-2-ил)пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,5, 1,2 Гц), 7,61-7,53 (3H, м), 7,45 (1H, с), 7,34-7,30 (1H, м), 6,91 (1H, д, J=8,1 Гц), 4,28-4,20 (1H, м), 3,89 (3H, с), 3,60 (2H, т, J=7,5 Гц), 3,01 (2H, т, J=7,5 Гц), 2,57 (3H, с), 1,78-1,68 (4H, м), 0,98 (6H, т, J=6,6 Гц).
Пример 313
С использованием соединения, полученного в примере 101, и хлордифторметана белый порошкообразный 3-[2-(3-дифторметокси-4-метоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-он получали, следуя процедуре примера 4.
1Н-ЯМР (CDCl3) δ: 7,85-7,80 (2H, м), 7,70 (1H, м), 7,50-7,40 (2H, м), 7,0-6,9 (3H, м), 6,58 (1H, т, J=74,4 Гц), 4,14 (2H, кв, J=6,9 Гц), 3,93 (3H, с), 3,42 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 1,48 (3H, т, J=6,9 Гц).
Пример 314
С использованием соединения, полученного в примере 101, и соединения, полученного в ссылочном примере 85, белый порошкообразный 3-{2-[3-(2,2-дифторэтокси)-4-метоксифенил]оксазол-4-ил}-1-(2-этоксифенил)пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,73-7,63 (2H, м), 7,55 (1H, д, J=2,1 Гц), 7,46-7,39 (2H, м), 7,01-6,91 (3H, м), 6,16 (1H, тт, J=54,9, 1,2 Гц), 4,29 (2H, тд, J=12,9, 1,2 Гц), 4,14 (2H, кв, J=6,9 Гц), 3,91 (3H, с), 3,43 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,48 (3H, т, J=7,2 Гц).
Пример 315
С использованием соединения, полученного в примере 101, и соединения, полученного в ссылочном примере 84, белый порошкообразный 1-(2-этоксифенил)-3-{2-[3-(2-фторэтокси)-4-метоксифенил]оксазол-4-ил}пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,69 (1H, дд, J=7,8, 1,8 Гц), 7,61 (1H, дд, J=8,4, 1,8 Гц), 7,55 (1H, с), 7,44-7,39 (2H, м), 7,00-6,91 (3H, м), 4,81 (2H, дт, J=47,4, 4,2 Гц), 4,32 (2H, дт, J=23,1, 4,2 Гц), 4,17-4,10 (2H, м), 3,90 (3H, с), 3,41 (2H, т, J=7,2 Гц), 2,99 (2H, т, J=7,2 Гц), 1,46 (3H, т, J=5,7 Гц).
Ссылочный пример 86
С использованием соединения, полученного в ссылочном примере 59, и соединения, полученного в ссылочном примере 85, белый порошкообразный этил 4-бензилокси-3-(2,2-дифторэтокси)бензоат получали, следуя процедуре примера 4.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, дд, J=8,4, 2,1 Гц), 7,61 (1H, д, J=2,1 Гц), 7,44-7,29 (5H, м), 6,95 (1H, д, J=8,4 Гц), 6,11 (1H, тт, J=54,9, 4,2 Гц), 5,19 (2H, с), 4,38-4,21 (4H, м), 1,39 (3H, т, J=7,2 Гц).
Ссылочный пример 87
С использованием соединения, полученного в ссылочном примере 86, белую порошкообразную 4-бензилокси-3-(2,2-дифторэтокси)бензойную кислоту получали, следуя процедуре, описанной в ссылочном примере 3.
1Н-ЯМР (ДМСО-d6) δ: 7,61 (1H, дд, J=8,4, 1,8 Гц), 7,54 (1H, д, J=1,8 Гц), 7,50-7,30 (5H, м), 7,18 (1H, д, J=8,4 Гц), 6,38 (1H, тт, J=54,3, 3,6 Гц), 5,22 (2H, с), 4,37 (2H, тд, J=14,7, 3,6 Гц).
Ссылочный пример 88
С использованием соединения, полученного в ссылочном примере 87, белый порошкообразный 4-бензилокси-3-(2,2-дифторэтокси)бензамид получали, следуя процедуре, описанной в ссылочном примере 4.
1Н-ЯМР (ДМСО-d6) δ: 7,86 (1H, ушир.с), 7,56-7,29 (7H, м), 7,25 (1H, ушир.с), 7,14 (1H, д, J=8,4 Гц), 6,40 (1H, тт, J=54,3, 3,6 Гц), 5,20 (2H, с), 4,34 (2H, тд, J=14,7, 3,6 Гц).
Ссылочный пример 89
С использованием соединения, полученного в ссылочном примере 88, белый порошкообразный 2-[4-бензилокси-3-(2,2-дифторэтокси)фенил]-4-хлорметилоксазол получали, следуя процедуре, описанной в ссылочном примере 5.
1Н-ЯМР (CDCl3) δ: 7,68-7,60 (3H, м), 7,45-7,30 (5H, м), 7,01 (1H, д, J=8,4 Гц), 6,12 (1H, тт, J=54,9, 4,2 Гц), 5,18 (2H, с), 4,56 (2H, с), 4,30 (2H, тд, J=13,2, 4,2 Гц).
Ссылочный пример 90
С использованием соединения, полученного в ссылочном примере 89, белый порошкообразный диметил 2-{2-[4-бензилокси-3-(2,2-дифторэтокси)фенил]оксазол-4-илметил}малонат получали, следуя процедуре, описанной в ссылочном примере 47.
1Н-ЯМР (CDCl3) δ: 7,63-7,57 (2H, м), 7,45-7,30 (6H, м), 6,99 (1H, д, J=8,1 Гц), 6,12 (1H, тт, J=54,9, 4,2 Гц), 5,18 (2H, с), 4,29 (2H, тд, J=13,2, 4,2 Гц), 3,89 (2H, т, J=7,5 Гц), 3,75 (6H, с), 3,18 (2H, т, J=7,5 Гц).
Ссылочный пример 91
С использованием соединения, полученного в ссылочном примере 90, коричневатый маслянистый метил 3-{2-[4-бензилокси-3-(2,2-дифторэтокси)фенил]оксазол-4-ил}пропионат получали, следуя процедуре, описанной в ссылочном примере 48.
1Н-ЯМР (CDCl3) δ: 7,64-7,59 (2H, м), 7,42-7,33 (6H, м), 6,99 (1H, д, J=8,1 Гц), 6,12 (1H, тт, J=54,9, 4,2 Гц), 5,18 (2H, с), 4,29 (2H, тд, J=13,2, 4,2 Гц), 3,68 (3H, с), 2,91 (2H, т, J=7,5 Гц), 2,72 (2H, т, J=7,5 Гц).
Пример 316
С использованием соединения, полученного в ссылочном примере 91, бледно-желтый маслянистый метил 2-{2-[4-бензилокси-3-(2,2-дифторэтокси)фенил]оксазол-4-илметил}-3-(3-метилпиридин-2-ил)-3-оксопропионат получали, следуя процедуре примера 100.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, д, J=4,5 Гц), 7,60-7,52 (3H, м), 7,46-7,30 (7H, м), 6,97 (1H, д, J=8,1 Гц), 6,11 (1H, тт, J=54,9, 4,2 Гц), 5,24-5,16 (3H, м), 4,27 (2H, тд, J=13,2, 4,2 Гц), 3,66 (3H, с), 3,34-3,22 (2H, м), 2,60 (3H, с).
Пример 317
С использованием соединения, полученного в примере 316, белый порошкообразный 3-{2-[3-(2,2-дифторэтокси)-4-гидроксифенил]оксазол-4-ил}-1-(3-метилпиридин-2-ил)пропан-1-он получали, следуя процедуре примера 136.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, д, J=4,5 Гц), 7,61-7,57 (2H, м), 7,52 (1H, с), 7,45 (1H, с), 7,34-7,30 (1H, м), 7,00 (1H, д, J=8,1 Гц), 6,11 (1H, тт, J=54,9, 4,2 Гц), 6,07 (1H, с), 4,32 (2H, тд, J=13,2, 4,2 Гц), 3,59 (2H, т, J=7,5 Гц), 3,00 (2H, т, J=7,5 Гц), 2,57 (3H, с).
Пример 318
С использованием соединения, полученного в примере 317, и метилиодида белый порошкообразный 3-{2-[3-(2,2-дифторэтокси)-4-этоксифенил]оксазол-4-ил}-1-(3-метилпиридин-2-ил)пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,51 (1H, д, J=4,5 Гц), 7,66-7,57 (3H, м), 7,46 (1H, с), 7,34-7,30 (1H, м), 6,94 (1H, д, J=8,4 Гц), 6,14 (1H, тт, J=54,6, 3,9 Гц), 4,28 (2H, тд, J=12,9, 3,9 Гц), 4,13 (2H, кв, J=6,9 Гц), 3,60 (2H, т, J=7,5 Гц), 3,02 (2H, т, J=7,5 Гц), 2,57 (3H, с), 1,47 (3H, т, J=6,9 Гц).
Пример 319
С использованием соединения, полученного в примере 317, и 2-бромпропана белый порошкообразный 3-{2-[3-(2,2-дифторэтокси)-4-изопропоксифенил]оксазол-4-ил}-1-(3-метилпиридин-2-ил)пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,51 (1H, д, J=4,5 Гц), 7,65-7,57 (3H, м), 7,46 (1H, с), 7,34-7,30 (1H, м), 6,95 (1H, д, J=8,4 Гц), 6,12 (1H, тт, J=54,6, 3,9 Гц), 4,62-4,54 (1H, м), 4,26 (2H, тд, J=12,9, 3,9 Гц), 3,60 (2H, т, J=7,5 Гц), 3,01 (2H, т, J=7,5 Гц), 2,57 (3H, с), 1,37 (6H, д, J=6,0 Гц).
Пример 320
С использованием соединения, полученного в ссылочном примере 7, и 2-дифторметоксибензойной кислоты белый порошкообразный N-[2-(3-бензилокси-4-метоксифенил)оксазол-4-илметил]-2-дифторметоксибензамид получали, следуя процедуре примера 1.
1Н-ЯМР (CDCl3) δ: 8,10 (1H, дд, J=7,8, 1,8 Гц), 7,64-7,57 (3H, м), 7,51-7,45 (4H, м), 7,40-7,26 (4H, м), 7,15 (1H, д, J=8,4 Гц), 6,95 (1H, д, J=9,0 Гц), 6,59 (1H, т, J=72,9 Гц), 5,20 (2H, с), 4,61 (2H, д, J=5,4 Гц), 3,93 (3H, с).
Пример 321
С использованием соединения, полученного в примере 320, белый порошкообразный 2-дифторметокси-N-[2-(3-гидрокси-4-метоксифенил)оксазол-4-илметил]бензамид получали, следуя процедуре примера 2.
1Н-ЯМР (CDCl3) δ: 8,09 (1H, д, J=7,8 Гц), 7,64-7,45 (5H, м), 7,32 (1H, т, J=7,8 Гц), 7,15 (1H, д, J=7,8 Гц), 6,91 (1H, д, J=8,4 Гц), 6,60 (1H, т, J=72,9 Гц), 5,77 (1H, с), 4,61 (2H, д, J=5,1 Гц), 3,94 (3H, с).
Пример 322
С использованием соединения, полученного в примере 321, и аллилбромида белый порошкообразный N-[2-(3-аллилокси-4-метоксифенил)оксазол-4-илметил]-2-дифторметоксибензамид получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,10 (1H, д, J=7,8 Гц), 7,64-7,30 (6H, м), 7,15 (1H, д, J=8,4 Гц), 6,94 (1H, д, J=8,1 Гц), 6,61 (1H, т, J=75 Гц), 6,17-6,08 (1H, м), 5,45 (1H, дд, J=17,1, 1,5 Гц), 5,32 (1H, дд, J=10,5, 1,5 Гц), 4,70 (2H, т, J=5,4 Гц), 4,62 (2H, т, J=5,4 Гц), 3,93 (3H, с).
Пример 323
С использованием соединения, полученного в примере 321, и 2-бромпропана белый порошкообразный 2-дифторметокси-N-[2-(3-изопропокси-4-метоксифенил)оксазол-4-илметил]бензамид получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,10 (1H, д, J=7,8 Гц), 7,64-7,30 (6H, м), 7,15 (1H, д, J=8,4 Гц), 6,94 (1H, д, J=8,1 Гц), 6,61 (1H, т, J=75 Гц), 4,70-4,61 (5H, м), 3,91 (3H, с), 1,39 (6H, д, J=6,0 Гц).
Пример 324
С использованием соединения, полученного в примере 17, и 3-бромпентана белый порошкообразный N-{2-[3-(1-этилпропокси)-4-метоксифенил]оксазол-4-илметил}-3-метилпиколинамид получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,58 (1H, ушир.с), 8,39 (1H, д, J=4,5 Гц), 7,63-7,55 (4H, м), 7,32-7,28 (1H, м), 6,92 (1H, д, J=8,4 Гц), 4,59 (2H, д, J=6,0 Гц), 4,28-4,20 (1H, м), 3,90 (3H, с), 2,76 (3H, с), 1,82-1,68 (4H, м), 0,99 (6H, т, J=7,5 Гц).
Пример 325
С использованием соединения, полученного в примере 2, и 3-бромпентана белый порошкообразный 2-этокси-N-{2-[3-(1-этилпропокси)-4-метоксифенил]оксазол-4-илметил}бензамид получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,57 (1H, ушир.с), 8,24 (1H, дд, J=8,1, 1,8 Гц), 7,62-7,56 (3H, м), 7,45-7,39 (1H, м), 7,07 (1H, т, J=8,1 Гц), 6,96-6,91 (2H, м), 4,63 (2H, дд, J=5,4, 0,9 Гц), 4,26-4,14 (3H, м), 3,90 (3H, с), 1,79-1,69 (4H, м), 1,49 (3H, т, J=7,2 Гц), 1,00 (6H, т, J=7,2 Гц).
Ссылочный пример 92
С использованием соединения, полученного в ссылочном примере 44, бесцветный маслянистый диметил 2-[2-(3-бензилокси-4-дифторметоксифенил)оксазол-4-илметил]малонат получали, следуя процедуре, описанной в ссылочном примере 47.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, с), 7,59 (1H, д, J=7,8 Гц), 7,48-7,22 (6H, м), 6,62 (1H, т, J=74,7 Гц), 5,21 (2H, с), 3,90 (1H, т, J=7,5 Гц), 3,73 (6H, с), 3,20 (2H, т, J=7,5 Гц).
Ссылочный пример 93
С использованием соединения, полученного в ссылочном примере 92, бледно-желтый маслянистый метил 3-[2-(3-бензилокси-4-дифторметоксифенил)оксазол-4-ил]пропионат получали, следуя процедуре, описанной в ссылочном примере 48.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, д, J=1,8 Гц), 7,48-7,31 (6H, м), 7,24 (1H, д, J=8,4 Гц), 6,62 (1H, т, J=74,7 Гц), 5,21 (2H, с), 3,70 (3H, с), 2,93 (2H, т, J=7,2 Гц), 2,71 (2H, т, J=7,2 Гц).
Пример 326
С использованием соединения, полученного в ссылочном примере 93, бесцветный маслянистый метил 2-[2-(3-бензилокси-4-дифторметоксифенил)оксазол-4-илметил]-3-(3-метилпиридин-2-ил)-3-оксопропионат получали, следуя процедуре примера 100.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,8, 1,2 Гц), 7,67-7,30 (10H, м), 7,21 (1H, д, J=8,4 Гц), 6,60 (1H, т, J=74,7 Гц), 5,18 (2H, с), 4,11 (1H, т, J=7,2 Гц), 3,65 (3H, с), 3,45-3,20 (2H, м), 2,60 (3H, с).
Пример 327
Использовали соединение, полученное в примере 326, и обрабатывали, следуя процедуре примера 125, с последующей обработкой в соответствии с процедурой примера 2 с получением белого порошкообразного 3-[2-(4-дифторметокси-3-гидроксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,5, 1,2 Гц), 7,67-7,45 (4H, м), 7,33-7,30 (1H, м), 7,16 (1H, д, J=8,1 Гц), 6,58 (1H, т, J=75 Гц), 5,76 (1H, с), 3,60 (2H, т, J=7,5 Гц), 3,01 (2H, т, J=7,5 Гц), 2,57 (3H, с).
Пример 328
0,15 соединения, полученного в примере 327, и 0,18 мл 1,8-диазабицикло[5.4.0]ундец-7-ена растворяли в 3 мл этанола, затем к полученному раствору добавляли 0,15 г (бромметил)циклопропана и полученную смесь нагревали и кипятили с обратным холодильником в течение ночи. После охлаждения к полученной реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой и концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1). Полученные кристаллы перекристаллизовывали из 80%-ного водного раствора этанола с получением, таким образом, 42 мг белого порошкообразного 3-[2-(3-циклопропилметокси-4-дифторметоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,51 (1H, дд, J=4,8, 1,2 Гц), 7,60-7,53 (3H, м), 7,50 (1H, с), 7,35-7,31 (1H, м), 7,21 (1H, д, J=8,1 Гц), 6,68 (1H, т, J=75,3 Гц), 3,95 (2H, д, J=6,9 Гц), 3,60 (2H, т, J=7,5 Гц), 3,02 (2H, т, J=7,5 Гц), 2,58 (3H, с), 1,37-1,25 (1H, м), 0,69-0,63 (2H, м), 0,40-0,34 (2H, м).
Пример 329
80 мг соединения, полученного в примере 327, и 0,09 мл 1,8-диазабицикло[5.4.0]ундец-7-ена растворяли в 2 мл этанола, затем к полученному раствору добавляли 80 мг 1-бромпропана, нагревали и кипятили с обратным холодильником в течение ночи. После охлаждения к полученной реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой, концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1). Полученные кристаллы перекристаллизовывали из 80%-ного водного раствора этанола с получением, таким образом, 25 мг белого порошкообразного 3-[2-(4-дифторметокси-3-пропоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,51 (1H, дд, J=4,8, 1,2 Гц), 7,61-7,53 (3H, м), 7,50 (1H, с), 7,35-7,31 (1H, м), 7,20 (1H, д, J=8,1 Гц), 6,61 (1H, т, J=75 Гц), 4,07 (2H, т, J=6,6 Гц), 3,60 (2H, т, J=7,5 Гц), 3,02 (2H, т, J=7,5 Гц), 2,58 (3H, с), 1,87 (2H, тд, J=7,5, 6,6 Гц), 1,07 (3H, т, J=7,5 Гц).
Пример 330
0,15 г соединения, полученного в примере 327, и 0,18 мл 1,8-диазабицикло[5.4.0]ундец-7-ена растворяли в 3 мл этанола, затем к полученному раствору добавляли 0,15 г аллилбромида и осуществляли нагревание и кипячение с обратным холодильником в течение 2 часов. После охлаждения к полученной реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой, концентрировали и полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1). Полученные кристаллы перекристаллизовывали из 80%-ного водного раствора этанола с получением, таким образом, 70 мг белого порошкообразного 3-[2-(3-аллилокси-4-дифторметоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,51 (1H, дд, J=4,5, 1,2 Гц), 7,62-7,56 (3H, м), 7,50 (1H, с), 7,50-7,31 (1H, м), 7,22 (1H, д, J=8,4 Гц), 6,62 (1H, т, J=75 Гц), 6,12-6,02 (1H, м), 5,46 (1H, дд, J=17,4, 1,5 Гц), 5,33 (1H, дд, J=10,8, 1,5 Гц), 4,68 (2H, д, J=8,1 Гц), 3,61 (2H, т, J=7,2 Гц), 3,02 (2H, т, J=7,2 Гц), 2,58 (3H, с).
Пример 331
80 мг соединения, полученного в примере 327, и 0,09 мл 1,8-диазабицикло[5.4.0]ундец-7-ена растворяли в 2 мл этанола и затем к полученному раствору добавляли 80 мг 4-бром-1-бутена и осуществляли нагревание и кипячение с обратным холодильником в течение ночи. После охлаждения к полученной реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой, концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1). Полученные кристаллы перекристаллизовывали из 80%-ного водного раствора этанола с получением, таким образом, 22 мг белого порошкообразного 3-[2-(3-бут-3-енилокси-4-дифторметоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,51 (1H, дд, J=4,8, 1,2 Гц), 7,61-7,54 (3H, м), 7,50 (1H, с), 7,35-7,31 (1H, м), 7,20 (1H, д, J=8,4 Гц), 6,62 (1H, т, J=75 Гц), 5,98-5,83 (1H, м), 5,24-5,12 (2H, м), 4,16 (2H, т, J=6,6 Гц), 3,61 (2H, т, J=7,2 Гц), 3,03 (2H, т, J=7,2 Гц), 2,64-2,58 (5H, м).
Пример 332
0,15 г соединения, полученного в примере 327, и 0,18 мл DBU растворяли в 3 мл этанола, затем к полученному раствору добавляли 0,15 г 2-бромпропана и осуществляли нагревание и кипячение с обратным холодильником в течение ночи. После охлаждения к реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой, концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1). Полученные кристаллы перекристаллизовывали из 80%-ного водного раствора этанола с получением, таким образом, 70 мг белого порошкообразного 3-[2-(4-дифторметокси-3-изопропоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 8,51 (1H, дд, J=4,8, 0,9 Гц), 7,63-7,53 (3H, м), 7,50 (1H, с), 7,35-7,31 (1H, м), 7,20 (1H, д, J=8,1 Гц), 6,61 (1H, т, J=75 Гц), 4,73-4,65 (1H, м), 3,61 (2H, т, J=7,2 Гц), 3,02 (2H, т, J=7,2 Гц), 2,58 (3H, с), 1,39 (6H, д, J=6,0 Гц).
Пример 333
С использованием соединения, полученного в примере 327, и этилиодида белый порошкообразный 3-[2-(4-дифторметокси-3-этоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он получали, следуя процедуре примера 330.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,5, 1,2 Гц), 7,61-7,49 (4H, м), 7,35-7,30 (1H, м), 7,20 (1H, д, J=8,4 Гц), 6,62 (1H, т, J=75 Гц), 4,18 (2H, кв, J=6,9 Гц), 3,61 (2H, т, J=7,2 Гц), 3,02 (2H, т, J=7,2 Гц), 2,58 (3H, с), 1,47 (3H, т, J=6,9 Гц).
Пример 334
60 мг соединения, полученного в примере 229, и 0,2 мл DBU растворяли в 4 мл этанола, затем к полученному раствору добавляли 0,2 мл этилиодида и осуществляли нагревание и кипячение с обратным холодильником в течение 2 часов. После охлаждения к реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой, концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1). Полученные кристаллы перекристаллизовывали из этанола с получением, таким образом, 36 мг белого порошкообразного 3-[2-(4-дифторметокси-3-этоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, дд, J=7,5, 1,8 Гц), 7,60-7,34 (4H, м), 7,01-6,91 (2H, м), 7,20 (1H, д, J=8,1 Гц), 6,62 (1H, т, J=75 Гц), 4,22-4,07 (4H, м), 3,43 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,50-1,40 (6H, м).
Пример 335
0,15 г соединения, полученного в примере 229, и 0,17 мл DBU растворяли в 4 мл этанола, затем к полученному раствору добавляли 0,14 г аллилбромида и осуществляли нагревание и кипячение с обратным холодильником в течение 2 часов. После охлаждения к полученной реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой, концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1). Полученные кристаллы перекристаллизовывали из 80%-ного водного раствора этанола с получением, таким образом, 90 мг белого порошкообразного 3-[2-(3-аллилокси-4-дифторметоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, дд, J=7,5, 1,8 Гц), 7,62-7,56 (2H, м), 7,46-7,40 (2H, м), 7,22 (1H, д, J=8,1 Гц), 7,01-6,92 (2H, м), 6,62 (1H, т, J=75 Гц), 6,15-6,00 (1H, м), 5,45 (1H, дд, J=17,1, 1,5 Гц), 5,32 (1H, дд, J=10,5, 1,5 Гц), 4,67 (2H, д, J=8,1 Гц), 4,14 (2H, кв, J=6,9 Гц), 3,42 (2H, т, J=7,5 Гц), 3,00 (2H, т, J=7,5 Гц), 1,48 (3H, т, J=6,9 Гц).
Пример 336
0,12 г соединения, полученного в примере 229, и 0,14 мл DBU растворяли в 3 мл этанола, затем к полученному раствору добавляли 0,12 г (бромметил)циклопропана и осуществляли нагревание и кипячение с обратным холодильником в течение ночи. После охлаждения к полученной реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой, концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1). Полученные кристаллы перекристаллизовывали из этанола с получением, таким образом, 80 мг белого порошкообразного 3-[2-(3-циклопропилметокси-4-дифторметоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,71 (1H, дд, J=7,8, 1,8 Гц), 7,59-7,54 (2H, м), 7,46-7,40 (2H, м), 7,21 (1H, д, J=8,1 Гц), 7,01-6,95 (2H, м), 6,68 (1H, т, J=75 Гц), 4,14 (2H, кв, J=6,9 Гц), 3,95 (2H, д, J=6,9 Гц), 3,42 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 1,47 (3H, т, J=6,9 Гц), 1,34-1,28 (1H, м), 0,69-0,63 (2H, м), 0,40-0,34 (2H, м).
Пример 337
0,12 г соединения, полученного в примере 229, и 0,14 мл DBU растворяли в 3 мл этанола, затем к полученному раствору добавляли 0,12 г 4-бром-1-бутена и осуществляли нагревание и кипячение с обратным холодильником в течение ночи. После охлаждения к полученной реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой, концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1). Полученные кристаллы перекристаллизовывали из этанола с получением, таким образом, 80 мг белого порошкообразного 3-[2-(3-бут-3-енилокси-4-дифторметоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,70 (1H, дд, J=7,8, 1,8 Гц), 7,61-7,54 (2H, м), 7,45-7,40 (2H, м), 7,20 (1H, д, J=8,1 Гц), 7,00-6,92 (2H, м), 6,62 (1H, т, J=75 Гц), 5,97-5,83 (1H, м), 5,23-5,12 (2H, м), 4,18-4,10 (4H, м), 3,42 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 2,63-2,56 (4H, м), 1,47 (3H, т, J=6,9 Гц).
Пример 338
С использованием соединения, полученного в примере 97, и этилиодида белый порошкообразный N-[2-(4-дифторметокси-3-этоксифенил)оксазол-4-илметил]-3-метилпиколинамид получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,60 (1H, ушир.с), 8,39 (1H, д, J=3,6 Гц), 7,67-7,57 (4H, м), 7,33-7,20 (2H, м), 6,63 (1H, т, J=75 Гц), 4,60 (2H, д, J=5,7 Гц), 4,20 (2H, кв, J=6,9 Гц), 2,76 (3H, с), 1,48 (3H, т, J=6,9 Гц).
Пример 339
С использованием соединения, полученного в примере 97, и аллилбромида белый твердый N-[2-(3-аллилокси-4-дифторметоксифенил)оксазол-4-илметил]-3-метилпиколинамид получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,60 (1H, ушир.с), 8,40-8,39 (1H, м), 7,67 (1H, с), 7,65-7,58 (3H, м), 7,33-7,22 (3H, м), 6,63 (1H, т, J=75 Гц), 6,13-6,03 (1H, м), 5,50-5,32 (2H, м), 4,70-4,68 (2H, м), 4,60 (2H, д, J=8,7 Гц), 2,76 (3H, с).
Пример 340
С использованием соединения, полученного в примере 97, и 1-бромпропана белый порошкообразный N-[2-(4-дифторметокси-3-пропоксифенил)оксазол-4-илметил]-3-метилпиколинамид получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,58 (1H, ушир.с), 8,39 (1H, д, J=7,8, Гц), 7,67-7,57 (4H, м), 7,33-7,20 (2H, м), 6,62 (1H, т, J=75 Гц), 4,60 (2H, д, J=6,0 Гц), 4,08 (2H, т, J=6,6 Гц), 2,76 (3H, с), 1,94-1,82 (2H, м), 1,07 (3H, т, J=7,5 Гц).
Пример 341
С использованием соединения, полученного в примере 97, и 2-бромпропана белый твердый N-[2-(4-дифторметокси-3-изопропоксифенил)оксазол-4-илметил]-3-метилпиколинамид получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,58 (1H, ушир.с), 8,39-8,38 (1H, м), 7,67-7,57 (4H, м), 7,33-7,19 (2H, м), 6,62 (1H, т, J=75 Гц), 4,74-4,67 (1H, м), 4,59 (2H, д, J=6,0 Гц), 2,76 (3H, с), 1,39 (6H, д, J=6,0 Гц).
Пример 342
С использованием соединения, полученного в примере 97, и 3-бромпентана бесцветный маслянистый N-{2-[4-дифторметокси-3-(1-этилпропокси)фенил]оксазол-4-илметил}-3-метилпиколинамид получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,58 (1H, ушир.с), 8,40-8,38 (1H, м), 7,67 (1H, с), 7,63-7,55 (3H, м), 7,33-7,20 (3H, м), 6,61 (1H, т, J=75 Гц), 4,59 (2H, д, J=6,0 Гц), 4,33 (1H, кв.т, J=6,0 Гц), 2,76 (3H, с), 1,79-1,70 (4H, м), 0,98 (6H, т, J=7,2 Гц).
Пример 343
С использованием соединения, полученного в примере 97, и 4-бром-1-бутена бесцветный маслянистый N-[2-(3-бут-3-енилокси-4-дифторметоксифенил)оксазол-4-илметил]-3-метилпиколинамид получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,58 (1H, ушир.с), 8,40-8,38 (1H, м), 7,67 (1H, с), 7,64-7,58 (3H, м), 7,33-7,20 (2H, м), 6,63 (1H, т, J=75 Гц), 5,95-5,84 (1H, м), 5,23-5,13 (2H, м), 4,61-4,59 (2H, м), 4,18 (2H, т, J=6,6 Гц), 2,76 (3H, с), 2,64-2,58 (2H, м).
Пример 344
С использованием соединения, полученного в примере 97, и изобутилбромида бесцветный маслянистый N-[2-(4-дифторметокси-3-изобутоксифенил)оксазол-4-илметил]-3-метилпиколинамид получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,60 (1H, ушир.с), 8,39 (1H, ушир.с), 7,68 (1H, с), 7,62-7,57 (3H, м), 7,33-7,20 (2H, м), 6,61 (1H, т, J=75 Гц), 4,60 (2H, д, J=6,0 Гц), 3,88 (2H, д, J=6,3 Гц), 2,76 (3H, с), 2,19-2,04 (1H, м), 1,06 (6H, д, J=6,3 Гц).
Пример 345
С использованием соединения, полученного в примере 97, и (бромметил)циклобутана бесцветный маслянистый N-[2-(3-циклобутилметокси-4-дифторметоксифенил)оксазол-4-илметил]-3-метилпиколинамид получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,60 (1H, ушир.с), 8,40 (1H, ушир.с), 7,68 (1H, с), 7,64-7,59 (3H, м), 7,33-7,20 (2H, м), 6,61 (1H, т, J=75 Гц), 4,60 (2H, д, J=6,0 Гц), 4,08 (2H, д, J=6,6 Гц), 2,89-2,76 (4H, м), 2,25-2,12 (2H, м), 2,04-1,92 (4H, м).
Пример 346
С использованием соединения, полученного в ссылочном примере 46, и 2-этоксибензойной кислоты белый порошкообразный N-[2-(3-бензилокси-4-дифторметоксифенил)оксазол-4-илметил]-2-этоксибензамид получали, следуя процедуре примера 96.
1Н-ЯМР (CDCl3) δ: 8,56 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,8 Гц), 7,73 (1H, д, J=1,8 Гц), 7,68-7,61 (2H, м), 7,48-7,24 (7H, м), 7,07 (1H, т, J=8,1 Гц), 6,95 (1H, д, J=8,4 Гц), 6,63 (1H, т, J=75 Гц), 5,21 (2H, с), 4,63 (2H, д, J=5,4 Гц), 4,18 (2H, кв, J=6,9 Гц), 1,48 (3H, т, J=6,9 Гц).
Пример 347
С использованием соединения, полученного в примере 346, белый порошкообразный N-[2-(4-дифторметокси-3-гидроксифенил)оксазол-4-илметил]-2-этоксибензамид получали, следуя процедуре примера 97.
1Н-ЯМР (CDCl3) δ: 8,60 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 1,8 Гц), 7,71-7,60 (2H, м), 7,57 (1H, дд, J=8,4, 1,8 Гц), 7,46-7,39 (1H, м), 7,19 (1H, д, J=8,4 Гц), 7,07 (1H, т, J=8,1 Гц), 6,95 (1H, д, J=8,4 Гц), 6,61 (1H, т, J=73,2 Гц), 6,02 (1H, ушир.с), 4,64 (2H, дд, J=5,4, 0,9 Гц), 4,19 (2H, кв, J=6,9 Гц), 1,49 (3H, т, J=6,9 Гц).
Пример 348
80 мг соединения, полученного в примере 347, и 0,1 мл DBU растворяли в 2 мл этанола, затем к полученному раствору добавляли 80 мг изобутилбромида и осуществляли нагревание и кипячение с обратным холодильником в течение ночи. После охлаждения к полученной реакционной смеси добавляли воду и осуществляли экстракцию этилацетатом. Органический слой дважды промывали водой, концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (н-гексан:этилацетат = 3:1). Полученные кристаллы перекристаллизовывали из 80%-ного водного раствора этанола с получением, таким образом, 30 мг белого порошкообразного N-[2-(4-дифторметокси-3-изобутоксифенил)оксазол-4-илметил]-2-этоксибензамида.
1Н-ЯМР (CDCl3) δ: 8,54 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,8 Гц), 7,67 (1H, с), 7,66-7,57 (2H, м), 7,45-7,39 (1H, м), 7,23 (1H, д, J=8,1 Гц), 7,07 (1H, т, J=8,1 Гц), 6,95 (1H, д, J=7,5 Гц), 6,62 (1H, т, J=75 Гц), 4,64 (2H, д, J=5,1 Гц), 4,19 (2H, кв, J=6,9 Гц), 3,87 (2H, д, J=6,6 Гц), 2,17 (1H, кв.т, J=6,6 Гц), 1,49 (3H, т, J=6,9 Гц), 1,07 (6H, д, J=6,9 Гц).
Пример 349
С использованием соединения, полученного в примере 347, и этилиодида белый порошкообразный N-[2-(4-дифторметокси-3-этоксифенил)оксазол-4-илметил]-2-этоксибензамид получали, следуя процедуре примера 348.
1Н-ЯМР (CDCl3) δ: 8,56 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,8 Гц), 7,67-7,58 (3H, м), 7,46-7,40 (1H, м), 7,24-7,21 (1H, м), 7,08 (1H, т, J=7,8 Гц), 6,95 (1H, д, J=7,8 Гц), 6,64 (1H, т, J=75 Гц) 4,63 (1H, д, J=5,1 Гц), 4,23-4,15 (4H, м), 1,52-1,46 (6H, м).
Пример 350
С использованием соединения, полученного в примере 347, и 1-бромпропана белый порошкообразный N-[2-(4-дифторметокси-3-пропоксифенил)оксазол-4-илметил]-2-этоксибензамид получали, следуя процедуре примера 348.
1Н-ЯМР (CDCl3) δ: 8,56 (1H, ушир.с), 8,24 (1H, дд, J=7,5, 1,8 Гц), 7,67 (1H, с), 7,64-7,57 (2H, м), 7,46-7,40 (1H, м), 7,23 (1H, д, J=7,8 Гц), 7,07 (1H, т, J=7,5 Гц), 6,95 (1H, д, J=8,4 Гц), 6,63 (1H, т, J=75 Гц), 4,64 (2H, д, J=5,4 Гц), 4,19 (2H, кв, J=7,2 Гц), 4,07 (2H, т, J=6,6 Гц), 1,90 (2H, кв.т, J=7,2, 6,6 Гц), 1,49 (3H, т, J=6,9 Гц), 1,08 (3H, т, J=7,2 Гц).
Пример 351
С использованием соединения, полученного в примере 347, и аллилбромида белый порошкообразный N-[2-(3-аллилокси-4-дифторметоксифенил)оксазол-4-илметил]-2-этоксибензамид получали, следуя процедуре примера 348.
1Н-ЯМР (CDCl3) δ: 8,55 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,8 Гц), 7,68 (1H, с), 7,65-7,60 (2H, м), 7,46-7,40 (1H, м), 7,25-7,23 (1H, м), 7,08 (1H, т, J=7,8 Гц), 6,96 (1H, д, J=8,4 Гц), 6,64 (1H, т, J=74,7 Гц), 6,10-6,03 (1H, м), 5,47 (1H, дд, J=17,4, 1,5 Гц), 5,34 (1H, дд, J=10,5, 1,5 Гц), 4,69 (2H, дт, J=5,1, 1,5 Гц), 4,63 (2H, дд, J=5,4, 1,2 Гц), 4,19 (2H, кв, J=6,9 Гц), 1,49 (3H, т, J=6,9 Гц).
Пример 352
С использованием соединения, полученного в примере 347, и 2-бромпропана белый порошкообразный N-[2-(4-дифторметокси-3-изопропоксифенил)оксазол-4-илметил]-2-этоксибензамид получали, следуя процедуре примера 348.
1Н-ЯМР (CDCl3) δ: 8,57 (1H, ушир.с), 8,24 (1H, дд, J=7,5, 1,8 Гц), 7,67 (1H, с), 7,65-7,57 (2H, м), 7,46-7,40 (1H, м), 7,26-7,21 (1H, м), 7,08 (1H, т, J=7,5 Гц), 6,95 (1H, д, J=8,4 Гц), 6,63 (1H, т, J=75 Гц), 4,74-4,62 (3H, м), 4,19 (2H, кв, J=6,9 Гц), 1,49 (3H, т, J=6,9 Гц), 1,40 (6H, д, J=6,3 Гц).
Пример 353
С использованием соединения, полученного в примере 347, и (бромметил)циклопропана белый порошкообразный N-[2-(3-циклопропилметокси-4-дифторметоксифенил)оксазол-4-илметил]-2-этоксибензамид получали, следуя процедуре примера 348.
1Н-ЯМР (CDCl3) δ: 8,55 (1H, ушир.с), 8,24 (1H, дд, J=8,1, 1,8 Гц), 7,67 (1H, с), 7,61-7,58 (2H, м), 7,46-7,39 (1H, м), 7,26-7,21 (1H, м), 7,07 (1H, т, J=7,5 Гц), 6,95 (1H, д, J=8,4 Гц), 6,70 (1H, т, J=75 Гц), 4,63 (2H, дд, J=5,4, 0,9 Гц), 4,19 (2H, кв, J=6,9 Гц), 1,49 (3H, т, J=6,9 Гц), 1,35-1,30 (1H, м), 0,71-0,64 (2H, м), 0,41-0,35 (2H, м).
Пример 354
С использованием соединения, полученного в примере 347, и 4-бром-1-бутена белый порошкообразный N-[2-(3-бут-3-енилокси-4-дифторметоксифенил)оксазол-4-илметил]-2-этоксибензамид получали, следуя процедуре примера 348.
1Н-ЯМР (CDCl3) δ: 8,56 (1H, ушир.с), 8,24 (1H, дд, J=7,5, 1,8 Гц), 7,67 (1H, с), 7,64-7,58 (2H, м), 7,46-7,40 (1H, м), 7,26-7,21 (1H, м), 7,08 (1H, т, J=7,5 Гц), 6,95 (1H, д, J=8,4 Гц), 6,64 (1H, т, J=75 Гц), 5,92-5,86 (1H, м), 5,24-5,13 (2H, м), 4,64 (2H, д, J=5,1 Гц), 4,22-4,14 (4H, м), 2,65-2,58 (2H, м), 1,49 (3H, т, J=6,9 Гц).
Пример 355
С использованием соединения, полученного в примере 347, и 3-бромпентана белый порошкообразный N-{2-[4-дифторметокси-3-(1-этилпропокси)фенил]оксазол-4-илметил}-2-этоксибензамид получали, следуя процедуре примера 348.
1Н-ЯМР (CDCl3) δ: 8,57 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,8 Гц), 7,67 (1H, с), 7,63-7,58 (2H, м), 7,46-7,40 (1H, м), 7,23 (1H, д, J=8,4 Гц), 7,07 (1H, т, J=8,1 Гц), 6,95 (1H, д, J=8,1 Гц), 6,63 (1H, т, J=75 Гц), 4,64 (2H, д, J=5,1 Гц), 4,33 (1H, кв.т, J=6,0, 5,1 Гц), 4,19 (2H, кв, J=6,9 Гц), 1,79-1,70 (4H, м), 1,49 (3H, т, J=6,9 Гц), 0,99 (6H, т, J=7,5 Гц).
Ссылочный пример 94
С использованием соединения, полученного в ссылочном примере 59, и хлордифторметана белый порошкообразный этил 4-бензилокси-3-дифторметоксибензоат получали, следуя процедуре примера 4.
1Н-ЯМР (CDCl3) δ: 7,90-7,80 (2H, м), 7,45-7,30 (5H, м), 7,03 (1H, д, J=8,4 Гц), 6,59 (1H, т, J=74,4 Гц), 5,23 (2H, с), 4,35 (2H, кв, J=7,2 Гц), 1,38 (3H, т, J=7,2 Гц).
Ссылочный пример 95
С использованием соединения, полученного в ссылочном примере 94, белый порошкообразный 2-(4-бензилокси-3-дифторметоксифенил)-4-хлорметилоксазол получали, следуя процедурам ссылочных примеров 3-5.
1Н-ЯМР (CDCl3) δ: 7,90-7,80 (2H, м), 7,65 (1H, с), 7,45-7,30 (5H, м), 7,06 (1H, д, J=7,2 Гц), 6,60 (1H, т, J=74,7 Гц), 5,20 (2H, с), 4,56 (2H, с).
Пример 356
С использованием соединения, полученного в ссылочном примере 95, белый порошкообразный 3-{2-(3-дифторметокси-4-гидроксифенил)оксазол-4-ил}-1-(3-метилпиридин-2-ил)пропан-1-он получали, следуя процедурам ссылочных примеров 92 и 93 и примеров 326 и 327.
1Н-ЯМР (CDCl3) δ: 8,49 (1H, д, J=4,5 Гц), 7,76-7,72 (2H, м), 7,59 (1H, д, J=8,4 Гц), 7,57 (1H, с), 7,37-7,30 (1H, м), 7,02 (1H, д, J=8,4 Гц), 6,59 (1H, т, J=75 Гц), 3,59 (2H, т, J=7,5 Гц), 3,01 (2H, т, J=7,5 Гц), 2,57 (3H, с).
Пример 357
С использованием соединения, полученного в примере 356, и 2-бромпропана белый порошкообразный 3-[2-(3-дифторметокси-4-изопропоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, д, J=4,5 Гц), 7,83-7,78 (2H, м), 7,58 (1H, д, J=8,4 Гц), 7,47 (1H, с), 7,34-7,30 (1H, м), 7,01 (1H, д, J=8,4 Гц), 6,58 (1H, т, J=75 Гц), 4,67-4,57 (1H, м), 3,59 (2H, т, J=7,5 Гц), 3,01 (2H, т, J=7,5 Гц), 2,57 (3H, с), 1,39 (6H, д, J=6,0 Гц).
Пример 358
С использованием соединения, полученного в примере 356, и аллилбромида белый порошкообразный 3-[2-(4-аллилокси-3-дифторметоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,8, 1,2 Гц), 7,84-7,80 (2H, м), 7,60-7,56 (1H, м), 7,47 (1H, д, J=1,2 Гц), 7,34-7,30 (1H, м), 7,01 (1H, д, J=8,4 Гц), 6,60 (1H, т, J=74,7 Гц), 6,10-6,00 (1H, м), 5,44 (1H, дд, J=17,4, 1,5 Гц), 5,33 (1H, дд, J=10,5, 1,5 Гц), 4,65 (2H, дт, J=5,1, 1,5 Гц), 3,60 (2H, т, J=7,5 Гц), 3,01 (2H, т, J=7,5 Гц), 2,58 (3H, с).
Пример 359
С использованием соединения, полученного в примере 356, и 4-бром-1-бутена белый порошкообразный 3-[2-(4-бут-3-енилокси-3-дифторметоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,8, 1,2 Гц), 7,84-7,78 (2H, м), 7,58 (1H, д, J=7,5 Гц), 7,46 (1H, с), 7,34-7,30 (1H, м), 7,00 (1H, д, J=8,4 Гц), 6,59 (1H, т, J=75 Гц), 5,94-5,85 (1H, м), 5,23-5,12 (2H, м), 4,12 (2H, т, J=6,6 Гц), 3,60 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 2,63-2,56 (5H, м).
Пример 360
С использованием соединения, полученного в примере 356, и (бромметил)циклопропана белый порошкообразный 3-[2-(4-циклопропилметокси-3-дифторметоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,8, 1,2 Гц), 7,83-7,79 (2H, м), 7,57 (1H, д, J=7,5 Гц), 7,46 (1H, с), 7,34-7,30 (1H, м), 6,98 (1H, д, J=8,1 Гц), 6,65 (1H, т, J=75 Гц), 3,92 (2H, д, J=7,2 Гц), 3,59 (2H, т, J=7,2 Гц), 3,00 (2H, т, J=7,2 Гц), 2,57 (3H, с), 1,33-1,27 (1H, м), 0,69-0,63 (2H, м), 0,40-0,34 (2H, м).
Пример 361
С использованием соединения, полученного в примере 356, и 1-бромпропана белый порошкообразный 3-[2-(3-дифторметокси-4-пропоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, дд, J=4,8, 1,2 Гц), 7,84-7,78 (2H, м), 7,58 (1H, д, J=8,1 Гц), 7,47 (1H, с), 7,43-7,30 (1H, м), 7,00 (1H, д, J=8,4 Гц), 6,59 (1H, т, J=75 Гц), 4,03 (2H, т, J=6,6 Гц), 3,59 (2H, т, J=7,5 Гц), 3,01 (2H, т, J=7,5 Гц), 2,58 (3H, с), 1,87 (2H, кв.т, J=7,2 Гц), 1,06 (3H, т, J=7,2 Гц).
Пример 362
С использованием соединения, полученного в примере 356, и этилиодида белый порошкообразный 3-[2-(3-дифторметокси-4-этоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 8,50 (1H, д, J=4,5 Гц), 7,84-7,78 (2H, м), 7,59 (1H, д, J=8,4 Гц), 7,47 (1H, с), 7,34-7,30 (1H, м), 6,99 (1H, д, J=8,4 Гц), 6,60 (1H, т, J=75 Гц), 4,15 (2H, кв, J=6,9 Гц), 3,59 (2H, т, J=7,2 Гц), 3,01 (2H, т, J=7,2 Гц), 2,57 (3H, с), 1,47 (3H, т, J=6,9 Гц).
Пример 363
Использовали соединение, полученное в ссылочном примере 95, и обрабатывали, следуя процедуре примера 228, с последующей обработкой в соответствии с процедурой примера 229 с получением белого порошкообразного 3-[2-(3-дифторметокси-4-гидроксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-она.
1Н-ЯМР (CDCl3) δ: 7,80-7,75 (2H, м), 7,71 (1H, дд, J=7,8, 1,8 Гц), 7,46-7,40 (2H, м), 7,22-6,69 (3H, м), 6,59 (1H, т, J=75 Гц), 5,91 (1H, ушир.с), 4,14 (2H, кв, J=7,2 Гц), 3,42 (2H, т, J=7,5 Гц), 2,99 (2H, т, J=7,5 Гц), 1,48 (3H, т, J=7,2 Гц).
Пример 364
С использованием соединения, полученного в примере 363, и 4-бром-1-бутена белый порошкообразный 3-[2-(4-бут-3-енилокси-3-дифторметоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,84-7,79 (2H, м), 7,71 (1H, дд, J=7,8, 1,8 Гц), 7,46-7,39 (2H, м), 7,01-6,92 (3H, м), 6,59 (1H, т, J=75 Гц), 5,91-5,85 (1H, м), 5,23-5,12 (2H, м), 4,18-4,09 (4H, м), 3,42 (2H, т, J=6,9 Гц), 2,99 (2H, т, J=6,9 Гц), 2,60 (2H, м), 1,48 (3H, т, J=6,9 Гц).
Пример 365
С использованием соединения, полученного в примере 363, и аллилбромида белый порошкообразный 3-[2-(4-аллилокси-3-дифторметоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,83-7,79 (2H, м), 7,70 (1H, дд, J=7,8, 1,8 Гц), 7,46-7,39 (2H, м), 7,02-6,92 (3H, м), 6,60 (1H, т, J=74,7 Гц), 6,06-6,00 (1H, м), 5,47-5,30 (2H, м), 4,66-4,63 (2H, м), 4,14 (2H, кв, J=6,9 Гц), 3,42 (2H, т, J=6,9 Гц), 2,99 (2H, т, J=6,9 Гц), 1,48 (3H, т, J=6,9 Гц).
Пример 366
С использованием соединения, полученного в примере 363, и этилиодида белый порошкообразный 3-[2-(3-дифторметокси-4-этоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-он получали, следуя процедуре примера 3.
1Н-ЯМР (CDCl3) δ: 7,84-7,80 (2H, м), 7,71 (1H, дд, J=7,8, 1,8 Гц), 7,45-7,39 (2H, м), 7,00-6,91 (3H, м), 6,60 (1H, т, J=75 Гц) 4,18-4,10 (4H, м), 3,42 (2H, т, J=7,5 Гц), 2,99 (2H, т, J=7,5 Гц), 1,50-1,44 (6H, м).
Ссылочный пример 96
Использовали соединение, полученное в ссылочном примере 95, и обрабатывали, следуя процедуре, описанной в ссылочном примере 45, с последующей обработкой в соответствии с процедурой ссылочного примера 46 с получением бледно-желтого маслянистого [2-(4-бензилокси-3-дифторметоксифенил)оксазол-4-ил]метиламина.
1Н-ЯМР (CDCl3) δ: 7,89-7,82 (2H, м), 7,61 (1H, с), 7,56-7,31 (5H, м), 7,07 (1H, д, J=8,1 Гц), 6,62 (1H, т, J=75 Гц), 5,19 (2H, с), 3,83 (2H, с).
Пример 367
Использовали соединение, полученное в ссылочном примере 96, и обрабатывали, следуя процедуре примера 96, с последующей обработкой в соответствии с процедурой примера 97 с получением белого порошкообразного N-[2-(3-дифторметокси-4-гидроксифенил)оксазол-4-илметил]-3-метилпиколинамида.
1Н-ЯМР (CDCl3) δ: 8,59 (1H, ушир.с), 8,39 (1H, д, J=4,5 Гц), 7,79-7,76 (2H, м), 7,63-7,58 (2H, м), 7,37-7,28 (1H, м), 7,07 (1H, д, J=8,1 Гц), 6,61 (1H, т, J=75 Гц), 6,16 (1H, с), 4,58 (2H, д, J=5,4 Гц), 2,76 (3H, с).
Пример 368
С использованием соединения, полученного в примере 367, и аллилбромида белый порошкообразный N-[2-(4-аллилокси-3-дифторметоксифенил)оксазол-4-илметил]-3-метилпиколинамид получали, следуя процедуре примера 98.
1Н-ЯМР (CDCl3) δ: 8,60 (1H, ушир.с), 8,39 (1H, д, J=4,5 Гц), 7,87-7,83 (2H, м), 7,65 (1H, с), 7,60-7,57 (1H, м), 7,33-7,29 (1H, м), 7,10 (1H, д, J=8,4 Гц), 6,61 (1H, т, J=75 Гц), 6,10-5,99 (1H, м), 5,55 (1H, дд, J=17,1, 1,5 Гц), 5,34 (1H, дд, J=10,5, 1,5 Гц), 4,65 (2H, д, J=5,4 Гц), 4,58 (2H, д, J=5,4 Гц), 2,76 (3H, с).
Пример 369
С использованием соединения, полученного в примере 367, и (бромметил)циклобутана белый порошкообразный N-[2-(4-циклобутилметокси-3-дифторметоксифенил)оксазол-4-илметил]-3-метилпиколинамид получали, следуя процедуре примера 98.
1Н-ЯМР (CDCl3) δ: 8,58 (1H, ушир.с), 8,39 (1H, д, J=4,5 Гц), 7,87-7,82 (2H, м), 7,64 (1H, с), 7,59 (1H, д, J=8,4 Гц), 7,33-7,29 (2H, м), 7,01 (1H, д, J=8,4 Гц), 6,59 (1H, т, J=75 Гц), 4,59 (1H, д, J=5,4 Гц), 4,03 (2H, д, J=6,9 Гц), 2,90-2,82 (1H, м), 2,76 (3H, с), 2,22-2,13 (2H, м), 2,00-1,84 (4H, м).
Пример 370
С использованием соединения, полученного в примере 367, и изобутилбромида белый порошкообразный N-[2-(3-дифторметокси-4-изобутоксифенил)оксазол-4-илметил]-3-метилпиколинамид получали, следуя процедуре примера 98.
1Н-ЯМР (CDCl3) δ: 8,58 (1H, ушир.с), 8,39 (1H, д, J=4,5 Гц), 7,87-7,83 (2H, м), 7,64 (1H, с), 7,60-7,57 (1H, м), 7,33-7,28 (1H, м), 7,00 (1H, д, J=8,4 Гц), 6,59 (1H, т, J=75 Гц), 4,59 (1H, д, J=5,4 Гц), 3,81 (2H, д, J=6,9 Гц), 2,76 (3H, с), 2,22-2,09 (1H, м), 1,06 (6H, д, J=6,6 Гц).
Пример 371
С использованием соединения, полученного в примере 367, и 4-бром-1-бутена белый порошкообразный N-[2-(4-бут-3-енилокси-3-дифторметоксифенил)оксазол-4-илметил]-3-метилпиколинамид получали, следуя процедуре примера 98.
1Н-ЯМР (CDCl3) δ: 8,59 (1H, ушир.с), 8,39 (1H, д, J=4,5 Гц), 7,88-7,83 (2H, м), 7,65 (1H, с), 7,60-7,57 (1H, м), 7,33-7,29 (1H, м), 7,01 (1H, д, J=8,4 Гц), 6,61 (1H, т, J=75 Гц), 5,94-5,83 (1H, м), 5,24-5,12 (2H, м), 4,59 (1H, д, J=5,4 Гц), 4,13 (2H, т, J=6,6 Гц), 2,76 (3H, с), 2,63-2,57 (2H, м).
Пример 372
С использованием соединения, полученного в примере 367, и (бромметил)циклопропана белый порошкообразный N-[2-(4-циклопропилметокси-3-дифторметоксифенил)оксазол-4-илметил]-3-метилпиколинамид получали, следуя процедуре примера 98.
1Н-ЯМР (CDCl3) δ: 8,58 (1H, ушир.с), 8,39 (1H, д, J=4,5 Гц), 7,86-7,83 (2H, м), 7,65 (1H, с), 7,59 (1H, д, J=8,4 Гц), 7,33-7,28 (1H, м), 7,00 (1H, д, J=8,4 Гц), 6,66 (1H, т, J=75 Гц), 4,59 (2H, д, J=5,4 Гц), 3,93 (2H, д, J=6,9 Гц), 2,76 (3H, с), 1,33-1,24 (1H, м), 0,70-0,64 (2H, м), 0,41-0,35 (2H, м).
Пример 373
Использовали соединение, полученное в ссылочном примере 96, и обрабатывали, следуя процедуре примера 96, с последующей обработкой в соответствии с процедурой примера 97 с получением белого порошкообразного N-[2-(3-дифторметокси-4-гидроксифенил)оксазол-4-илметил]-2-этоксибензамида.
1Н-ЯМР (CDCl3) δ: 8,59 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,2 Гц), 7,81-7,78 (2H, м), 7,63 (1H, с), 7,46-7,40 (1H, м), 7,11-7,05 (2H, м), 6,96 (1H, д, J=8,4 Гц), 6,62 (1H, т, J=75 Гц), 5,87 (1H, ушир.с), 4,62 (2H, д, J=5,4 Гц), 4,19 (2H, кв, J=6,9 Гц), 1,50 (3H, т, J=6,9 Гц).
Пример 374
С использованием соединения, полученного в примере 373, и 2-бромпропана белый порошкообразный N-[2-(3-дифторметокси-4-изопропоксифенил)оксазол-4-илметил]-2-этоксибензамид получали, следуя процедуре примера 98.
1Н-ЯМР (CDCl3) δ: 8,60 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 2,1 Гц), 7,85-7,82 (2H, м), 7,64 (1H, с), 7,45-7,39 (1H, м), 7,09-7,01 (2H, м), 6,95 (1H, д, J=8,1 Гц), 6,59 (1H, т, J=75 Гц), 4,71-4,61 (5H, м), 4,19 (2H, кв, J=6,9 Гц), 1,51 (3H, т, J=6,9 Гц), 1,40 (6H, д, J=6,9 Гц).
Пример 375
С использованием соединения, полученного в примере 373, и (бромметил)циклопропана белый порошкообразный N-[2-(4-циклопропилметокси-3-дифторметоксифенил)оксазол-4-илметил]-2-этоксибензамид получали, следуя процедуре примера 98.
1Н-ЯМР (CDCl3) δ: 8,59 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 2,1 Гц), 7,85-7,82 (2H, м), 7,64 (1H, с), 7,45-7,39 (1H, м), 7,09-6,94 (3H, м), 6,66 (1H, т, J=75 Гц), 4,62 (2H, д, J=5,4 Гц), 4,19 (2H, кв, J=6,9 Гц), 3,93 (2H, д, J=8,4 Гц), 1,50 (3H, т, J=6,9 Гц), 1,34-1,24 (1H, м), 0,71-0,64 (2H, м), 0,41-0,35 (2H, м).
Пример 376
С использованием соединения, полученного в примере 373, и 1-бромпропана белый порошкообразный N-[2-(3-дифторметокси-4-пропоксифенил)оксазол-4-илметил]-2-этоксибензамид получали, следуя процедуре примера 98.
1Н-ЯМР (CDCl3) δ: 8,60 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 1,8 Гц), 7,87-7,83 (2H, м), 7,64 (1H, с), 7,42 (1H, т, J=7,5 Гц), 7,09-6,85 (3H, м), 6,35 (1H, т, J=75 Гц), 4,62 (2H, д, J=6,0 Гц), 4,19 (2H, кв, J=6,6 Гц), 4,04 (2H, т, J=6,0 Гц), 1,91-1,84 (2H, м), 1,50 (3H, т, J=6,9 Гц), 1,07 (3H, т, J=6,9 Гц).
Пример 377
С использованием соединения, полученного в примере 373, и аллилбромида белый порошкообразный N-[2-(4-аллилокси-3-дифторметоксифенил)оксазол-4-илметил]-2-этоксибензамид получали, следуя процедуре примера 98.
1Н-ЯМР (CDCl3) δ: 8,60 (1H, ушир.с), 8,23 (1H, дд, J=7,8, 1,8 Гц), 7,86-7,83 (2H, м), 7,64 (1H, с), 7,42 (1H, т, J=7,5 Гц), 7,10-6,97 (3H, м), 6,61 (1H, т, J=75 Гц), 6,07-6,01 (1H, м), 5,49-5,32 (2H, м), 4,68-4,61 (4H, м), 4,19 (2H, кв, J=6,9 Гц), 1,50 (3H, т, J=6,9 Гц).
Ссылочный пример 97
С использованием этил 3,4-дигидроксибензоата и хлордифторметана белый порошкообразный этил 3,4-бис-дифторметоксибензоат получали, следуя процедуре примера 4.
1Н-ЯМР (CDCl3) δ: 8,00-7,90 (2H, м), 7,31 (1H, д, J=8,1 Гц), 6,60 (1H, т, J=72,9 Гц), 6,57 (1H, т, J=72,9 Гц), 4,39 (2H, кв, J=7,2 Гц), 1,40 (3H, т, J=7,2 Гц).
Ссылочный пример 98
С использованием соединения, полученного в ссылочном примере 97, белый порошкообразный 2-(3,4-бис-дифторметоксифенил)-4-хлорметилоксазол получали, следуя процедурам ссылочных примеров 3-5.
1Н-ЯМР (CDCl3) δ: 7,95-7,90 (2H, м), 7,73 (1H, с), 7,35 (1H, д, J=8,4 Гц), 6,60 (1H, т, J=72,9 Гц), 6,59 (1H, т, J=72,9 Гц), 4,57 (2H, с).
Пример 378
С использованием соединения, полученного в ссылочном примере 98, белый порошкообразный 3-[2-(3,4-бис-дифторметоксифенил)оксазол-4-ил]-1-(2-этоксифенил)пропан-1-он получали, следуя процедуре примера 190.
1Н-ЯМР (CDCl3) δ: 7,89-7,84 (2H, м), 7,71 (1H, дд, J=7,5, 1,8 Гц), 7,48-7,41 (2H, м), 7,32 (1H, д, J=8,4 Гц), 7,01-6,93 (2H, м), 6,58 (1H, т, J=75 Гц), 6,57 (1H, т, J=75 Гц), 4,14 (2H, кв, J=6,9 Гц), 3,43 (2H, т, J=6,9 Гц), 3,00 (2H, т, J=6,9 Гц), 1,48 (3H, т, J=6,9 Гц).
Ссылочный пример 99
Использовали соединение, полученное в ссылочном примере 98, и обрабатывали, следуя процедуре, описанной в ссылочном примере 45, с последующей обработкой в соответствии с процедурой ссылочного примера 46 с получением бледно-желтого маслянистого [2-(3,4-бис-дифторметоксифенил)оксазол-4-ил]метиламина.
1Н-ЯМР (CDCl3) δ: 7,92-7,88 (2H, м), 7,58 (1H, с), 7,34 (1H, д, J=8,4 Гц), 6,60 (1H, т, J=75 Гц), 6,59 (1H, т, J=75 Гц), 3,85 (2H, с).
Пример 379
С использованием соединения, полученного в ссылочном примере 99, белый порошкообразный N-[2-(3,4-бис-дифторметоксифенил)оксазол-4-илметил]-3-метилпиколинамид получали, следуя процедуре примера 96.
1Н-ЯМР (CDCl3) δ: 8,61 (1H, ушир.с), 8,40 (1H, дд, J=7,5, 1,5 Гц), 7,93-7,88 (2H, м), 7,70 (1H, с), 7,60 (1H, д, J=1,5 Гц), 7,58-7,31 (2H, м), 6,60 (1H, т, J=75 Гц), 6,58 (1H, т, J=75 Гц), 4,60 (2H, дд, J=6,0, 1,2 Гц), 2,77 (3H, с).
Пример 380
С использованием соединения, полученного в ссылочном примере 99, белый порошкообразный N-[2-(3,4-бис-дифторметоксифенил)оксазол-4-илметил]-2-этоксибензамид получали, следуя процедуре примера 1.
1Н-ЯМР (CDCl3) δ: 8,59 (1H, ушир.с), 8,23 (1H, дд, J=7,5, 1,8 Гц), 7,94-7,88 (2H, м), 7,70 (1H, с), 7,46-7,33 (2H, м), 7,07 (1H, т, J=7,5 Гц), 6,95 (1H, д, J=8,4 Гц), 6,60 (1H, т, J=75 Гц), 6,59 (1H, т, J=75 Гц), 4,63 (2H, д, J=6,0 Гц), 4,19 (2H, кв, J=6,9 Гц), 1,50 (3H, т, J=6,9 Гц).
Пример 381
С использованием соединения, полученного в ссылочном примере 98, белый порошкообразный 3-[2-(3,4-бис-дифторметоксифенил)оксазол-4-ил]-1-(3-метилпиридин-2-ил)пропан-1-он получали, следуя процедуре примера 356.
1Н-ЯМР (CDCl3) δ: 8,51 (1H, ушир.с), 7,88-7,85 (2H, м), 7,59 (1H, д, J=8,4 Гц), 7,53 (1H, с), 7,35-7,30 (2H, м), 6,58 (1H, т, J=75 Гц), 6,57 (1H, т, J=75 Гц), 3,60 (2H, т, J=6,3 Гц), 3,02 (2H, т, J=6,3 Гц), 2,58 (3H, с).
Пример 382
С использованием соединения, полученного в примере 347, и соединения, полученного в ссылочном примере 85, белый порошкообразный N-{2-[4-дифторметокси-3-(2,2-дифторэтокси)фенил]оксазол-4-илметил}-2-этоксибензамид получали, следуя процедуре примера 348.
1Н-ЯМР (CDCl3) δ: 8,55 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,8 Гц), 7,71-7,65 (3H, м), 7,46-7,41 (1H, м), 7,29 (1H, с), 7,08 (1H, т, J=8,1 Гц), 6,96 (1H, д, J=8,1 Гц), 6,59 (1H, т, J=74,1 Гц), 6,15 (1H, тт, J=54,9, 4,2 Гц) 4,64 (2H, д, J=5,4 Гц), 4,32 (2H, тд, J=12,9, 4,2 Гц), 4,20 (2H, кв, J=6,9 Гц), 1,50 (3H, т, J=6,9 Гц).
Пример 383
С использованием соединения, полученного в примере 347, и 1,1,1-трифтор-2-йодэтана белый порошкообразный N-{2-[4-дифторметокси-3-(2,2,2-трифторэтокси)фенил]оксазол-4-илметил}-2-этоксибензамид получали, следуя процедуре примера 348.
1Н-ЯМР (CDCl3) δ: 8,56 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,8 Гц), 7,75-7,68 (3H, м), 7,46-7,40 (1H, м), 7,30 (1H, д, J=8,4 Гц), 7,08 (1H, т, J=8,1 Гц), 6,96 (1H, д, J=8,1 Гц), 6,60 (1H, т, J=74,1 Гц), 4,63 (2H, д, J=5,4 Гц), 4,49 (2H, кв, J=8,1 Гц), 4,20 (2H, кв, J=6,9 Гц), 1,50 (3H, т, J=6,9 Гц).
Пример 384
С использованием соединения, полученного в примере 17, и 2-бромпропана бесцветный маслянистый N-[2-(4-метокси-3-изопропоксифенил)оксазол-4-илметил]-3-метилпиколинамид получали, следуя процедуре примера 19.
1Н-ЯМР (CDCl3) δ: 8,58 (1H, ушир.с), 8,39 (1H, дд, J=4,8, 1,2 Гц), 7,63-7,57 (4H, м), 7,33-7,28 (1H, м), 6,93 (1H, д, J=8,4 Гц), 4,68 (1H, септ., J=6,3 Гц), 4,59 (2H, д, J=5,7 Гц), 3,89 (3H, с), 2,76 (3H, с), 1,41 (6H, д, J=6,3 Гц).
Пример 385
С использованием соединения, полученного в примере 347, и (бромметил)циклобутана белый порошкообразный N-[2-(3-циклобутилметокси-4-дифторметоксифенил)оксазол-4-илметил]-2-этоксибензамид получали, следуя процедуре примера 348.
1Н-ЯМР (CDCl3) δ: 8,56 (1H, ушир.с), 8,24 (1H, дд, J=7,8, 1,8 Гц), 7,67-7,58 (3H, м), 7,50-7,40 (1H, м), 7,23 (1H, д, J=8,4 Гц), 7,08 (1H, т, J=8,1 Гц), 6,96 (1H, д, J=8,1 Гц), 6,63 (1H, т, J=75 Гц), 4,64 (2H, д, J=5,1 Гц), 4,19 (2H, кв, J=6,9 Гц), 4,08 (2H, д, J=6,6 Гц), 2,86-2,82 (1H, м), 2,19-2,12 (2H, м), 2,04-1,87 (4H, м), 1,50 (3H, т, J=6,9 Гц).
Химические структуры соединений, полученных выше в ссылочных примерах и примерах, представлены ниже в таблицах 1-40.
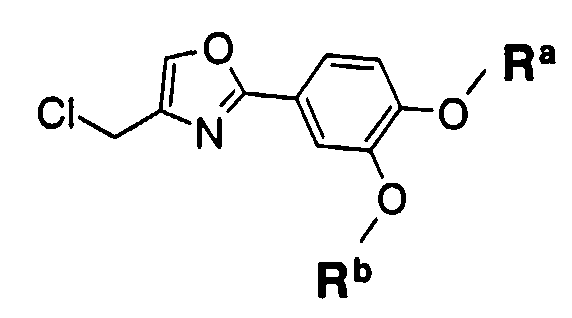
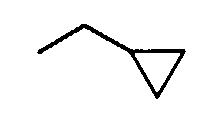
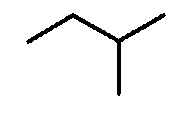
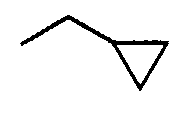
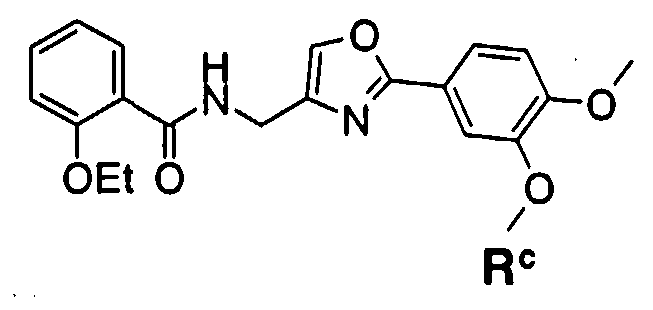
-OEt: этокси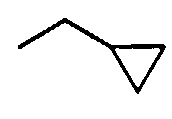
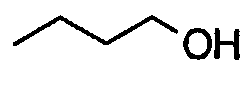
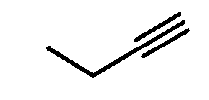
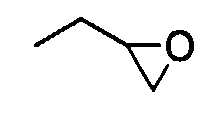
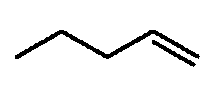
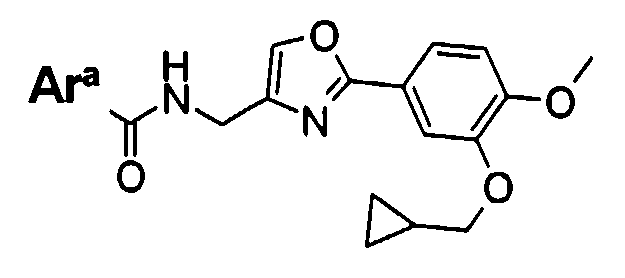
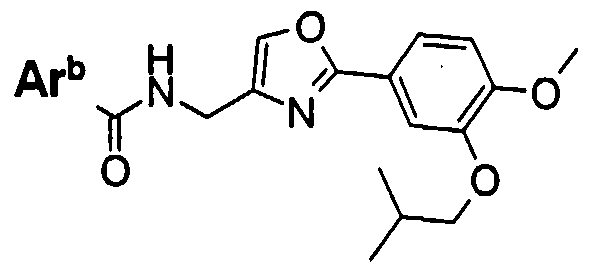
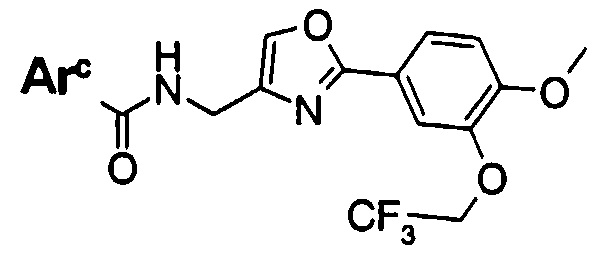
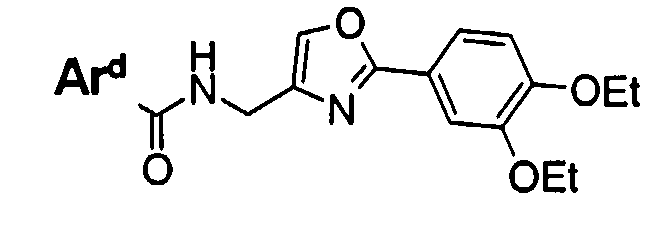
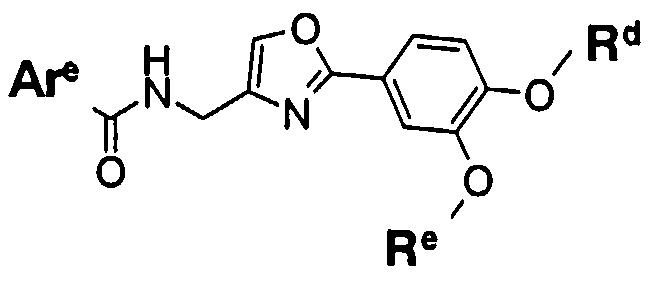
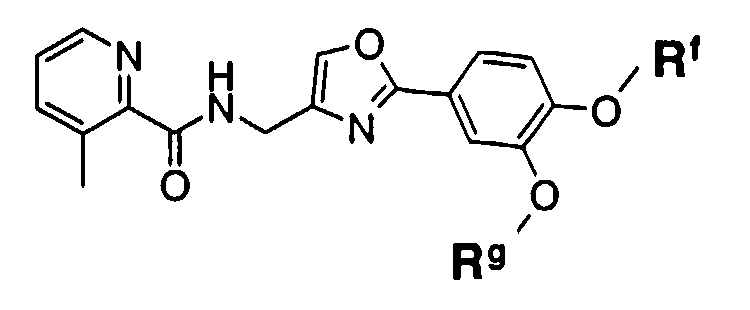
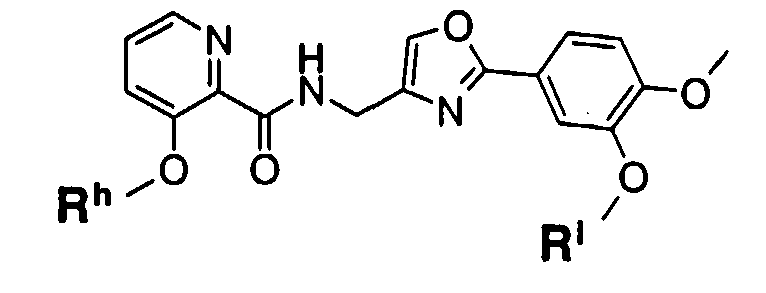
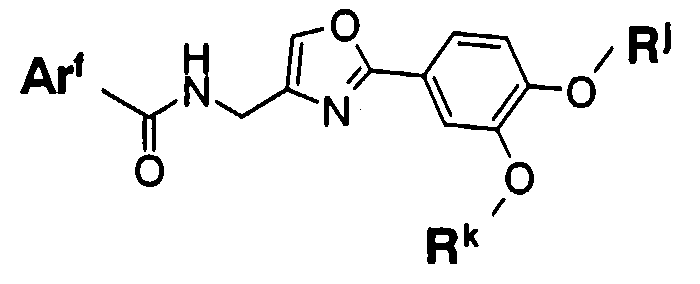
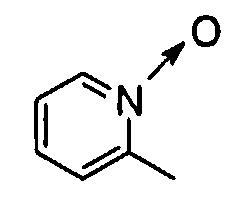
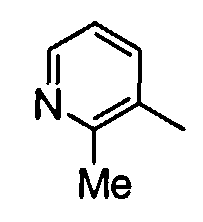
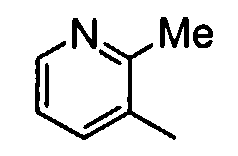
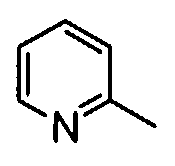
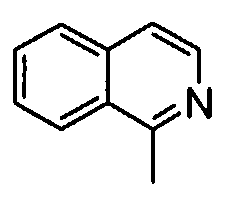
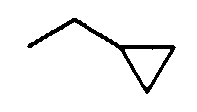
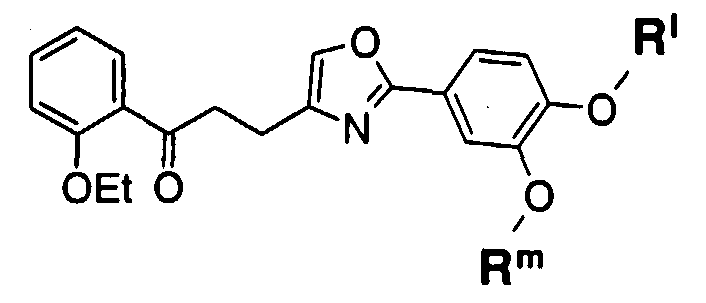
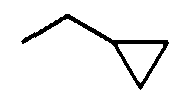
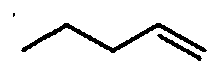
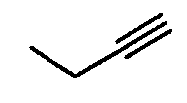
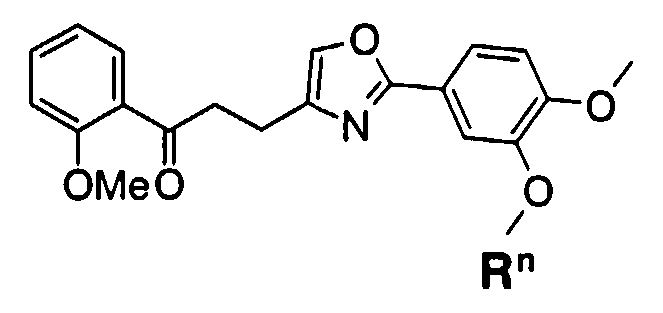
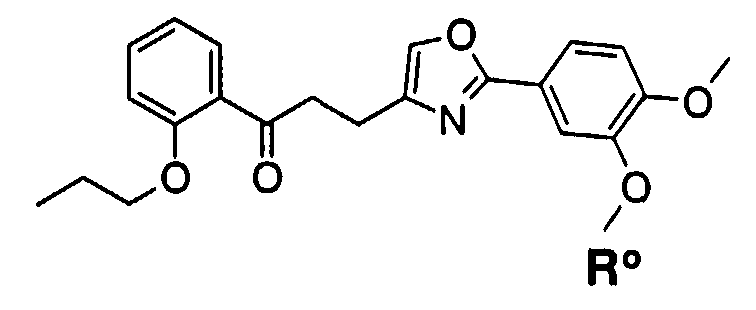
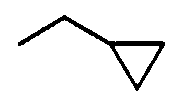

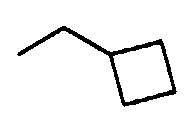
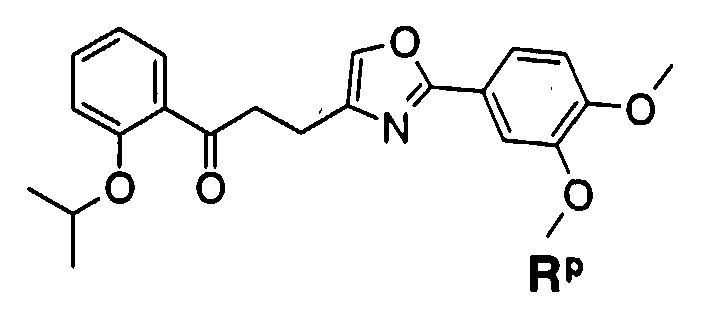
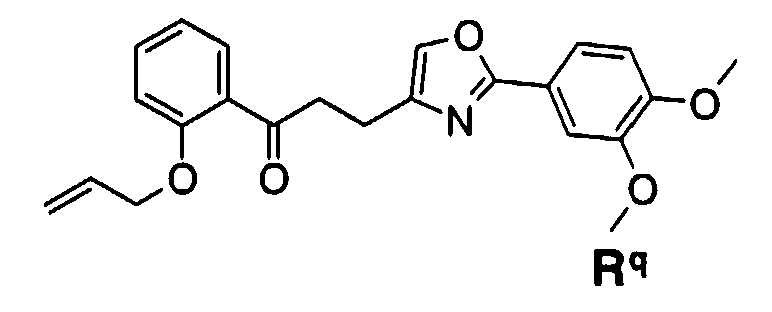
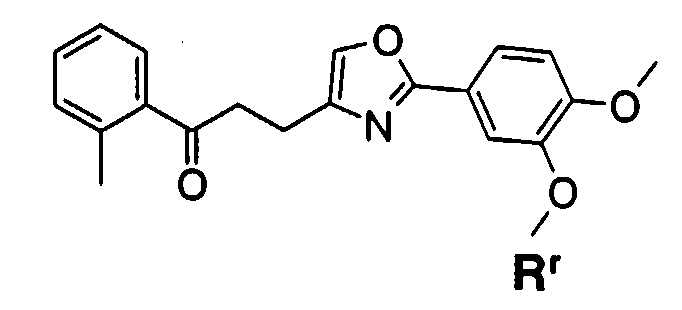
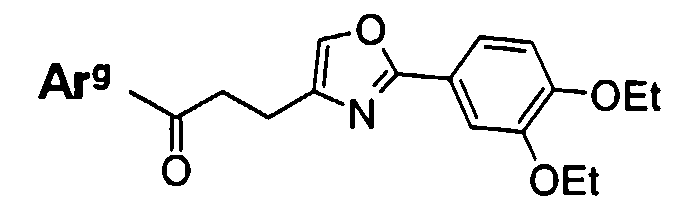
-OEt: этокси
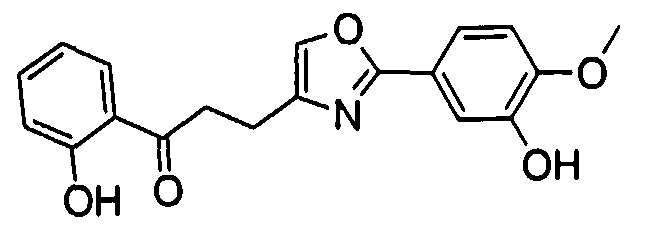
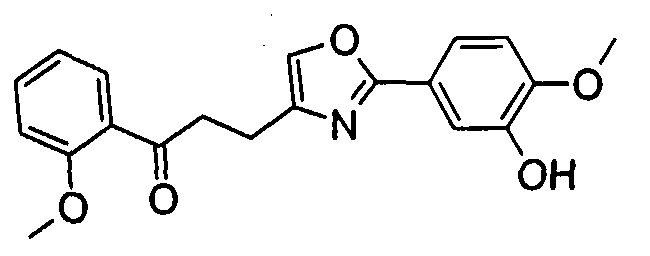
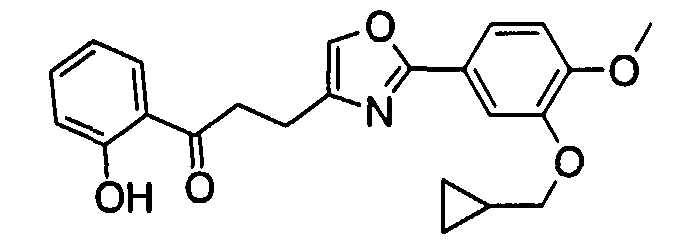
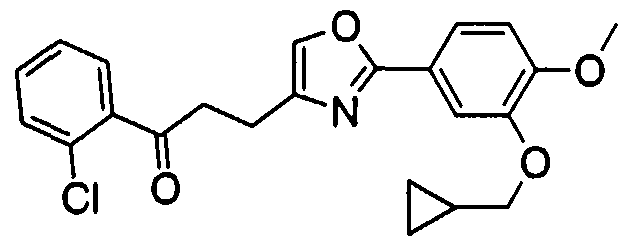
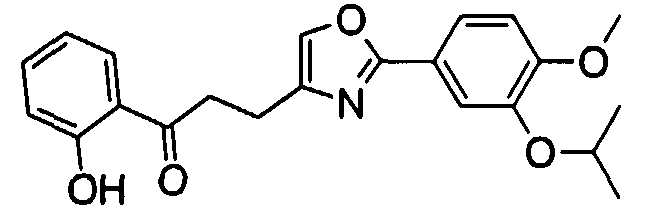
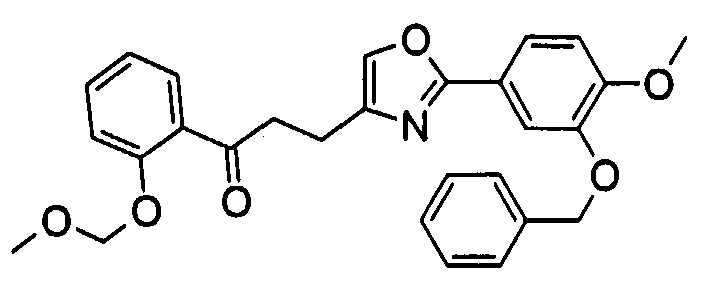
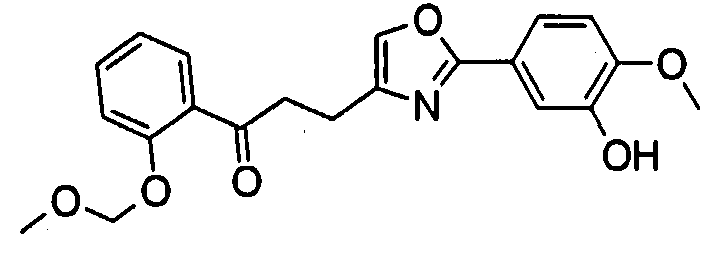
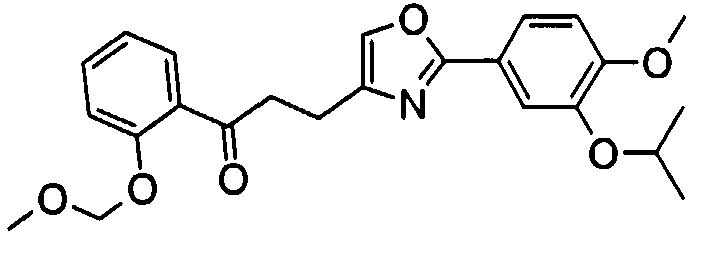
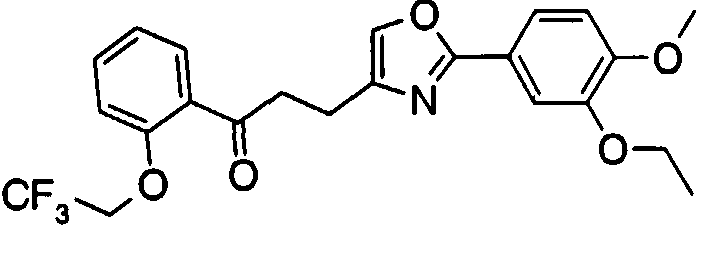
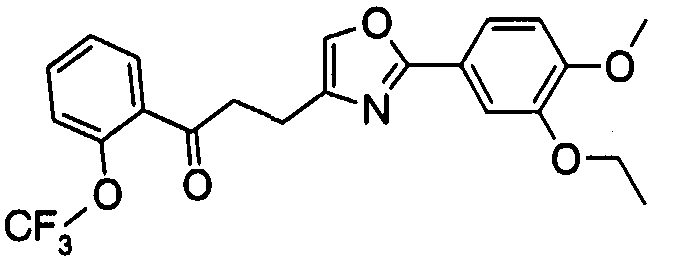
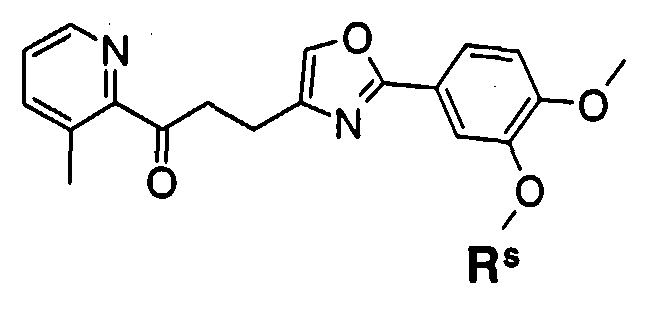
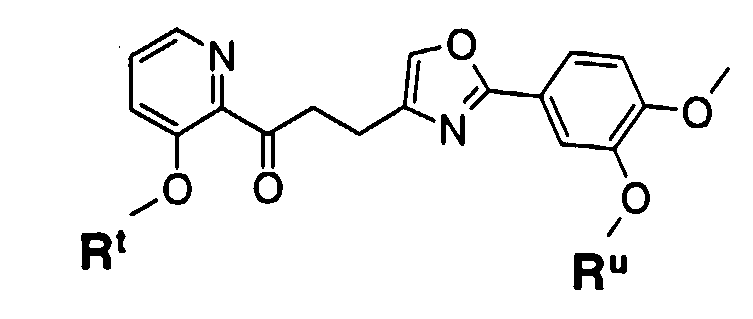
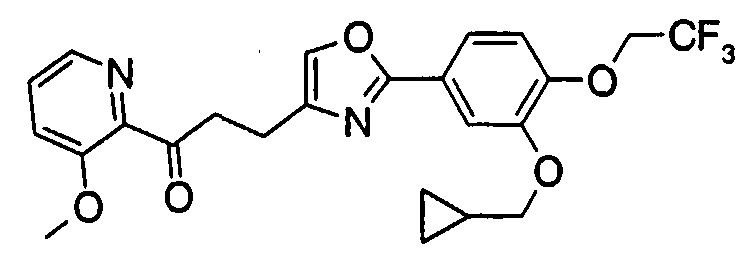
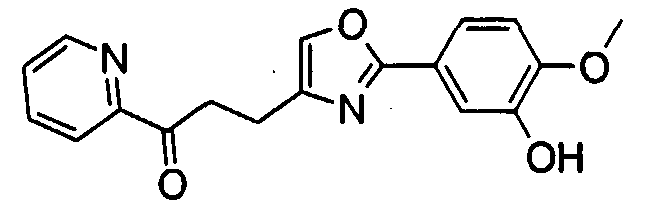
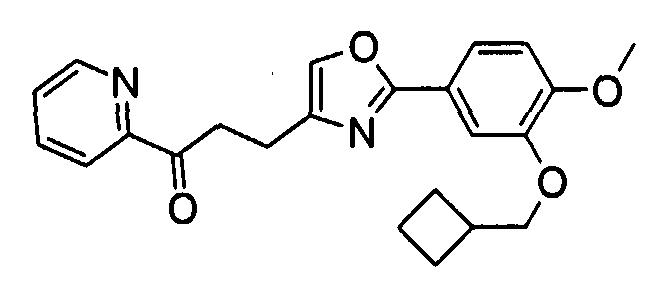
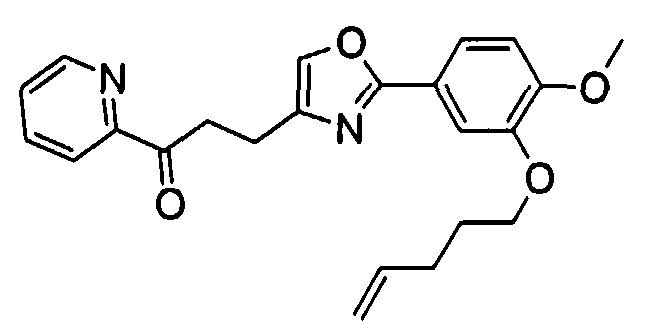
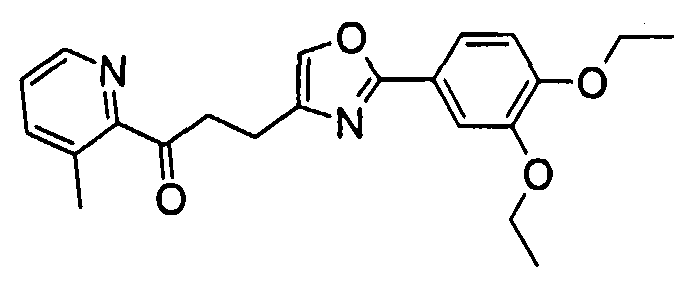
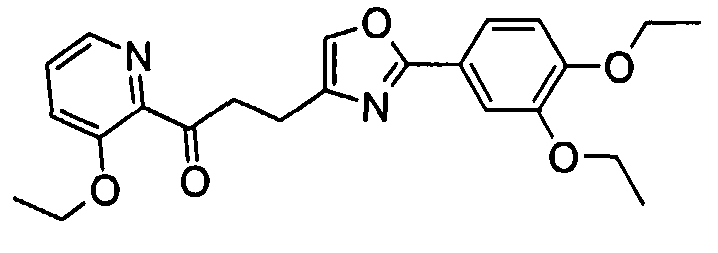
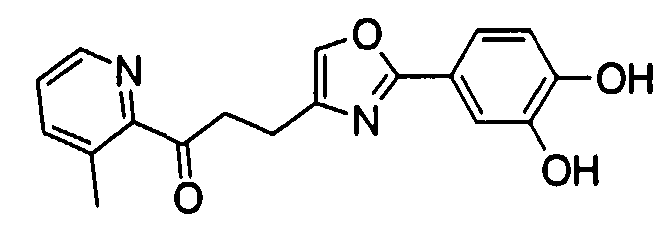
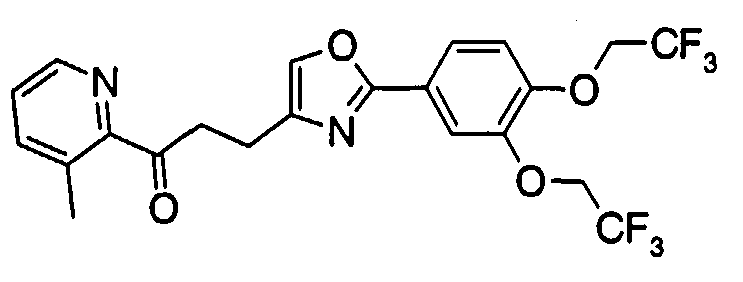
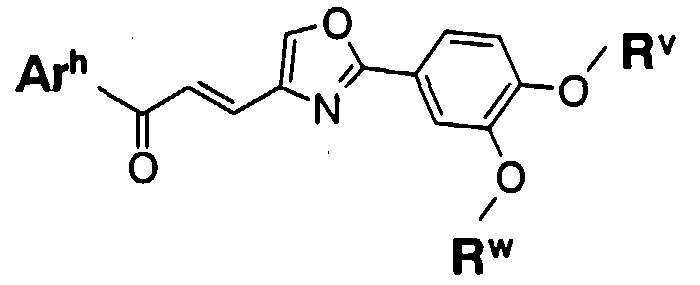
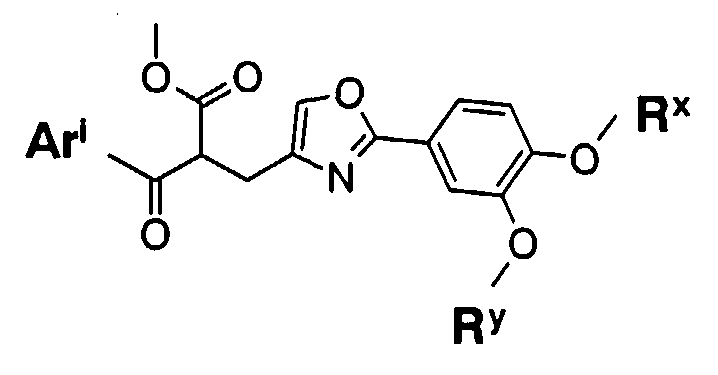
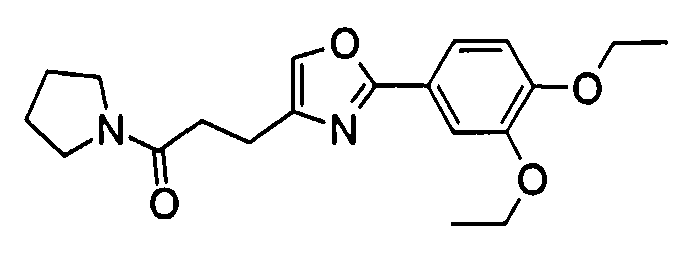
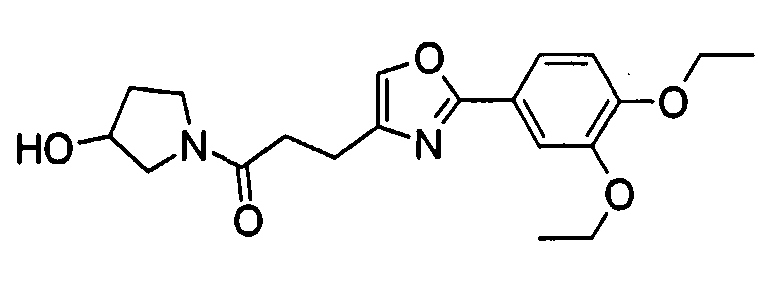
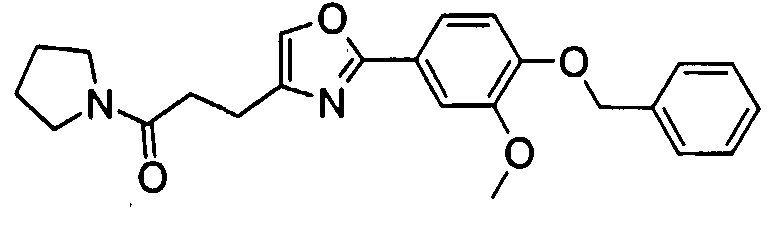
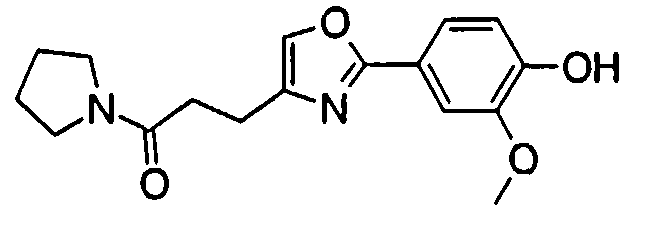
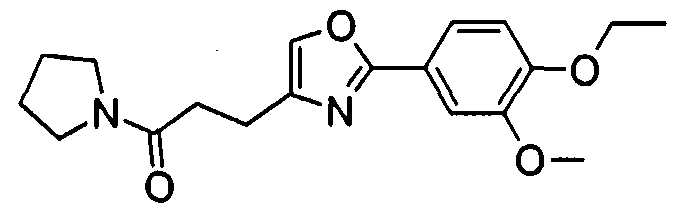
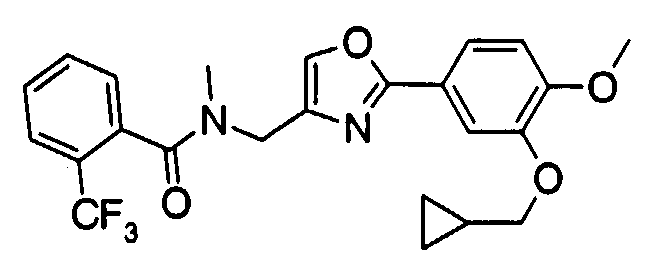
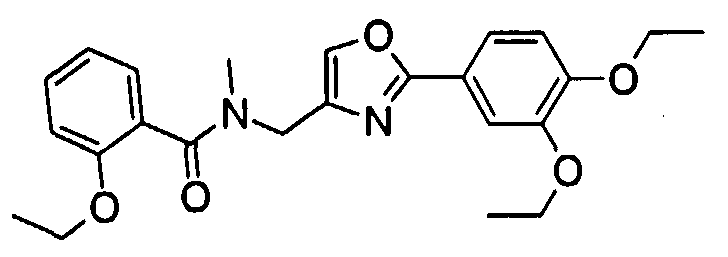
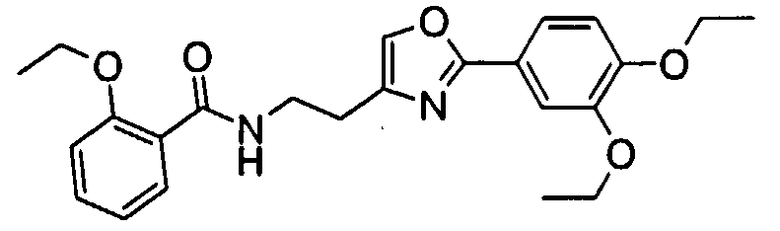
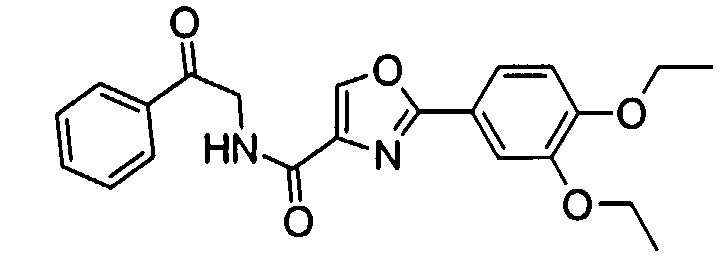
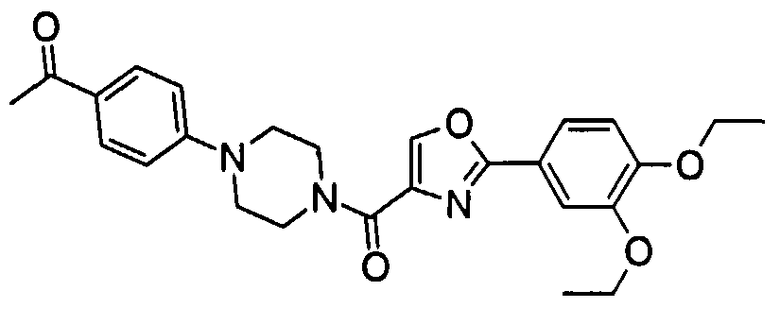
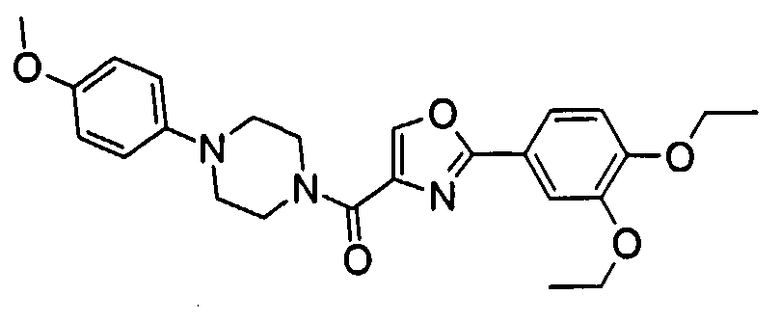
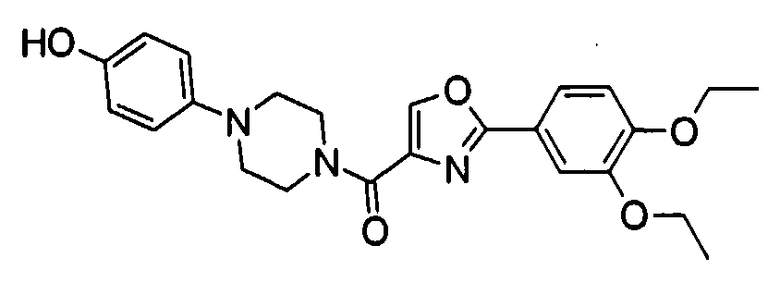
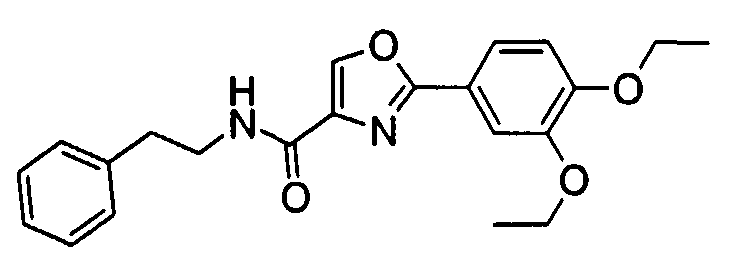
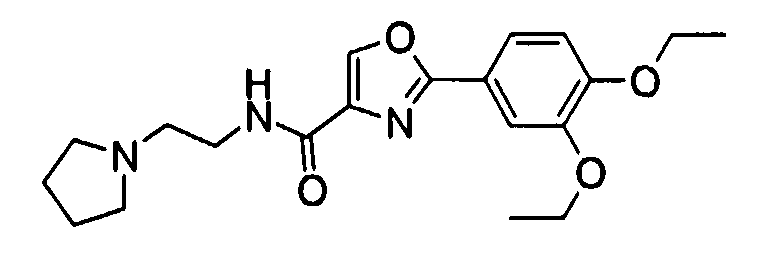
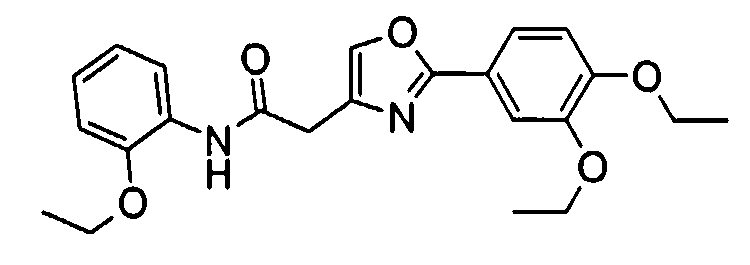
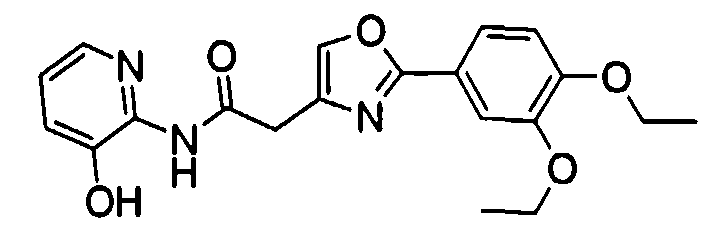
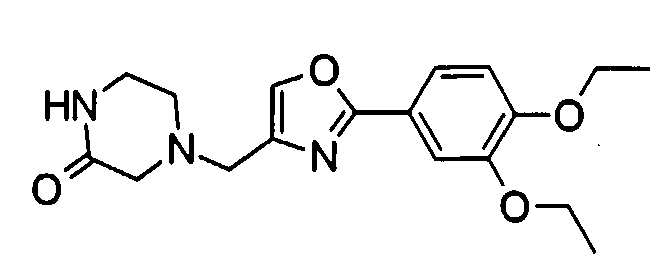
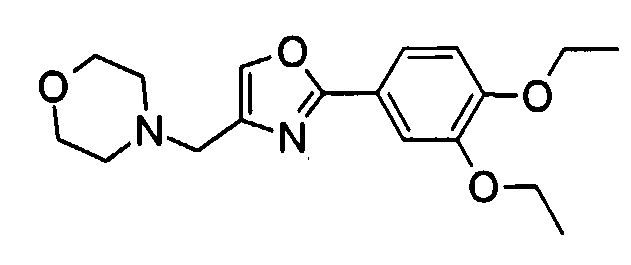
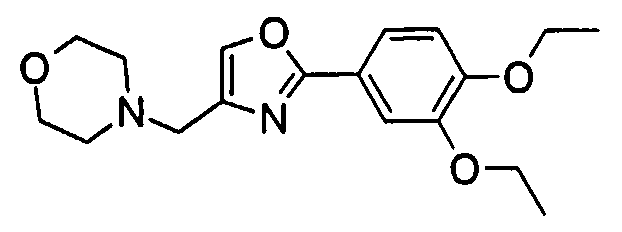
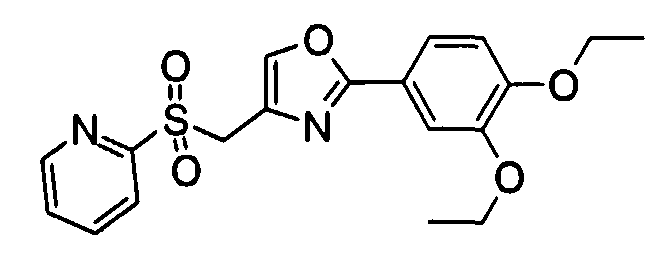
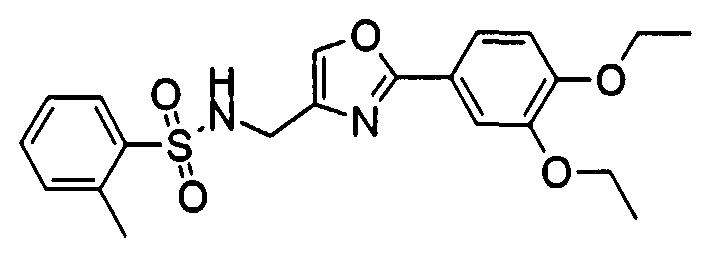
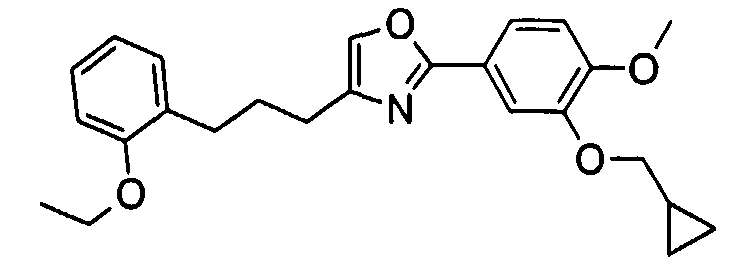
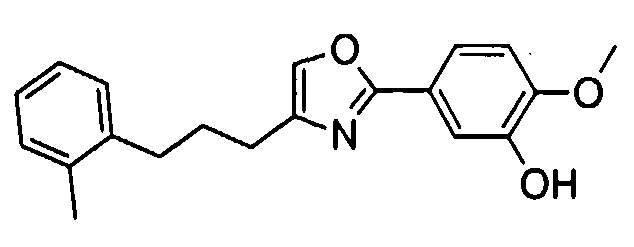
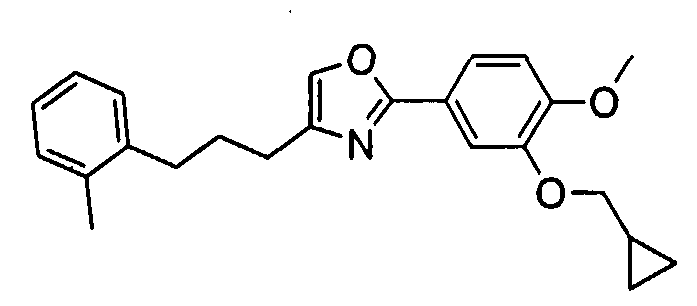
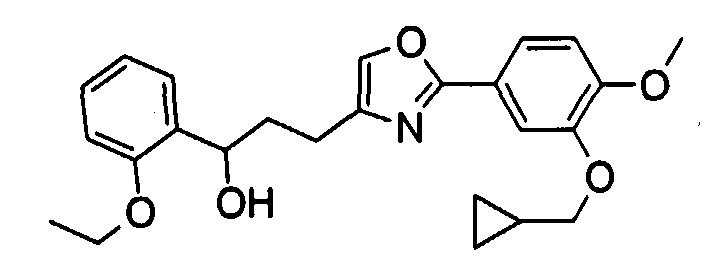
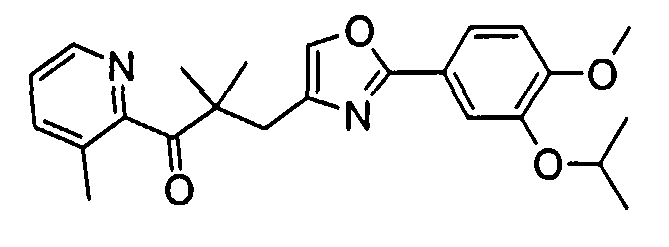
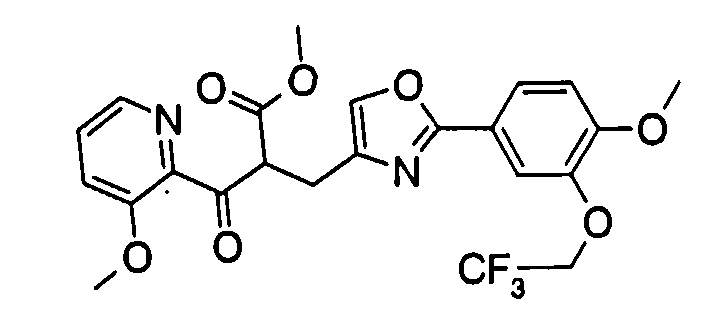
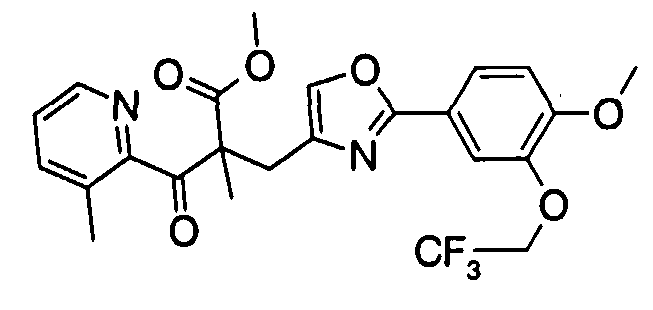
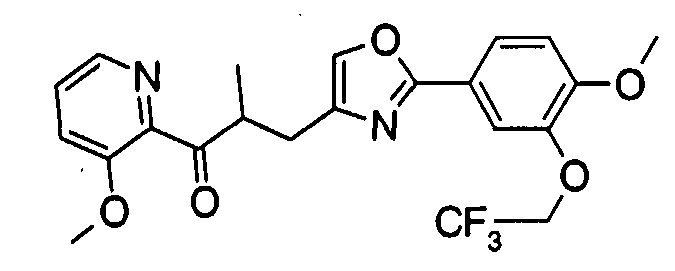
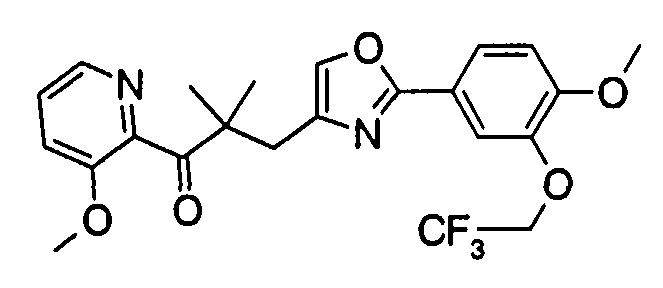
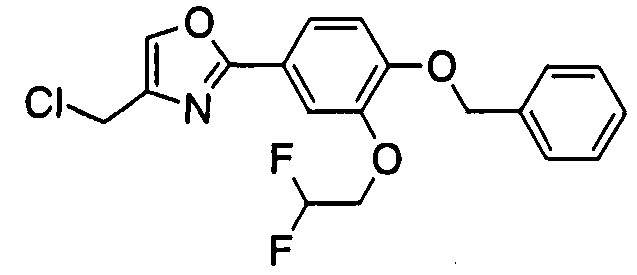
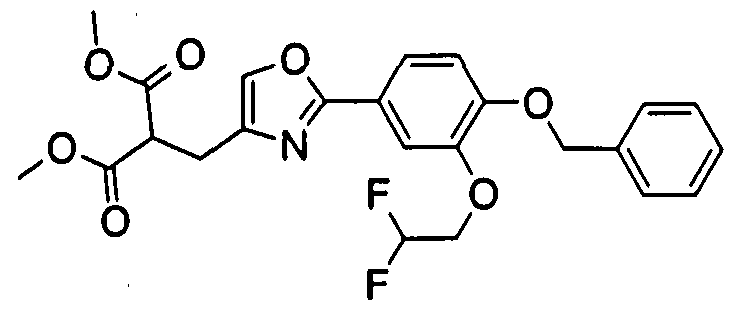
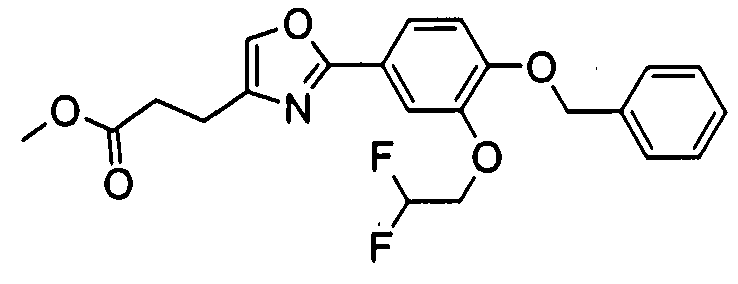
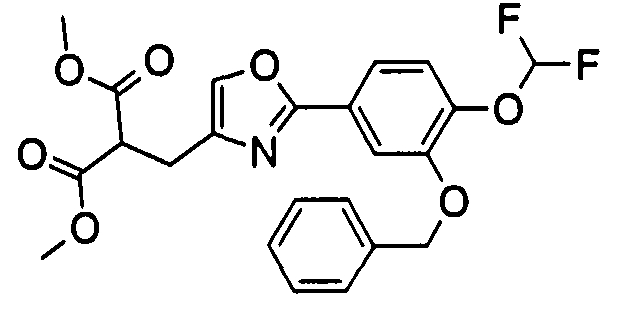
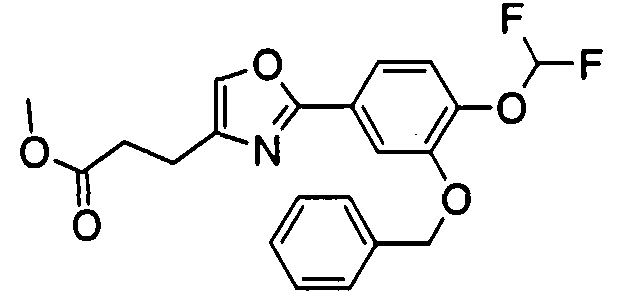
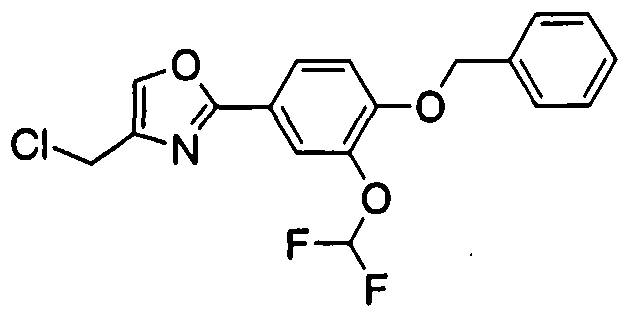
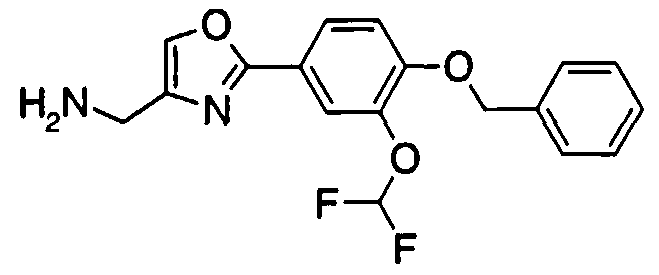
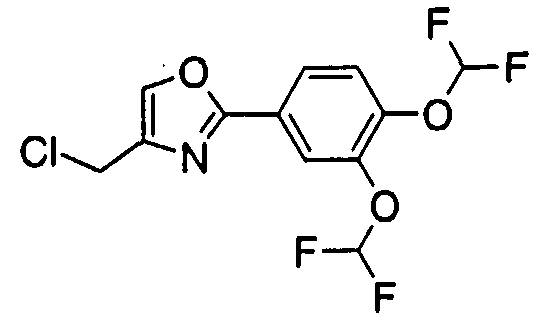
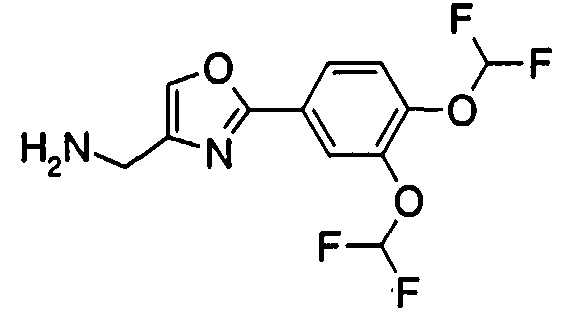
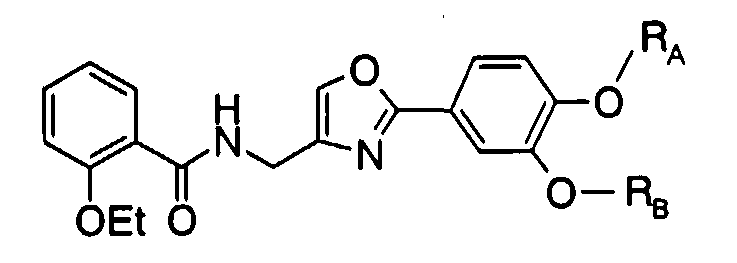
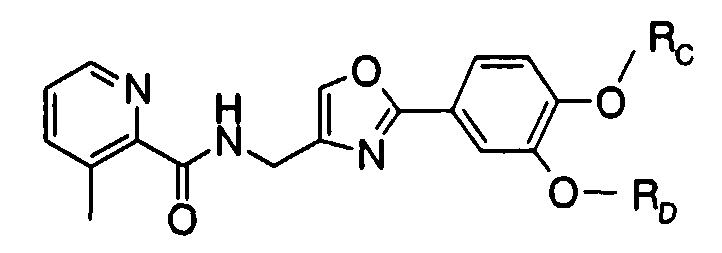
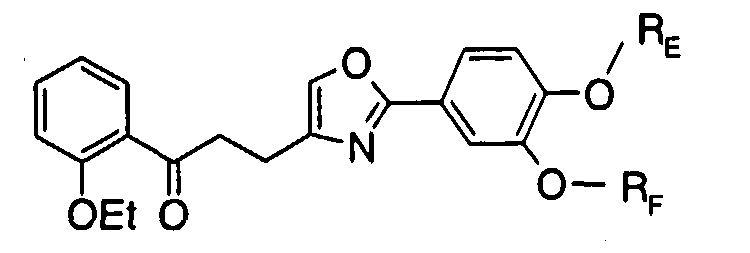
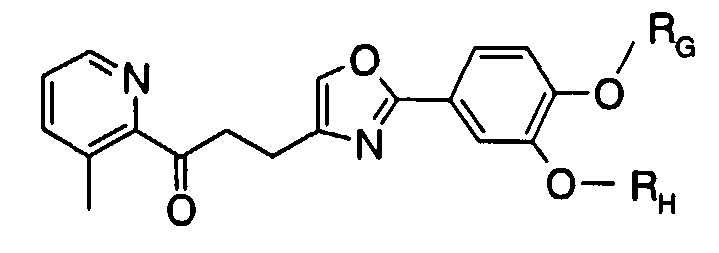
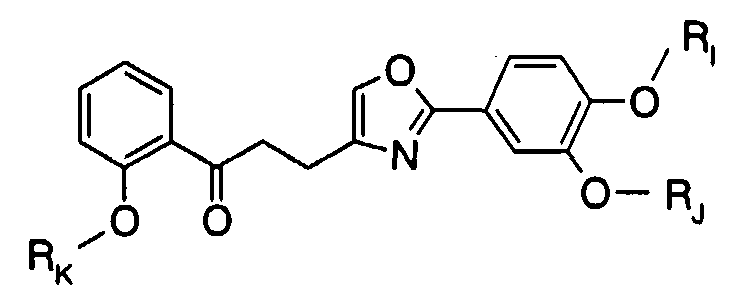
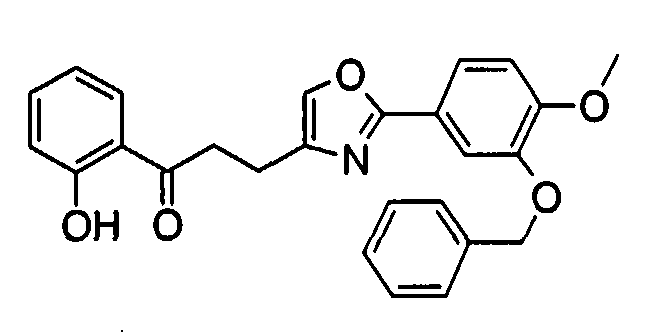
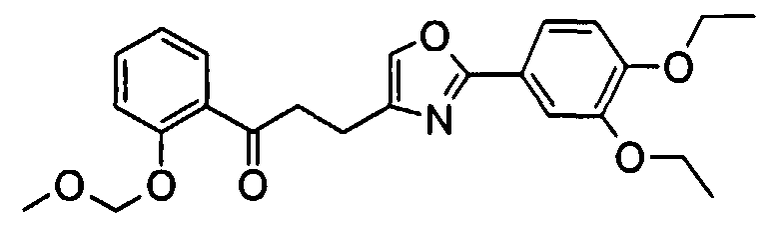
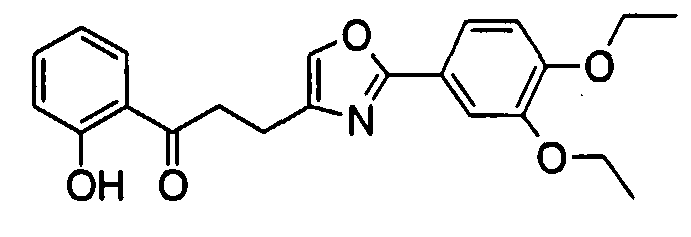
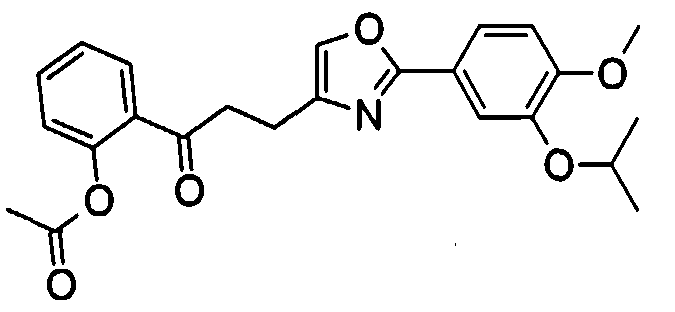
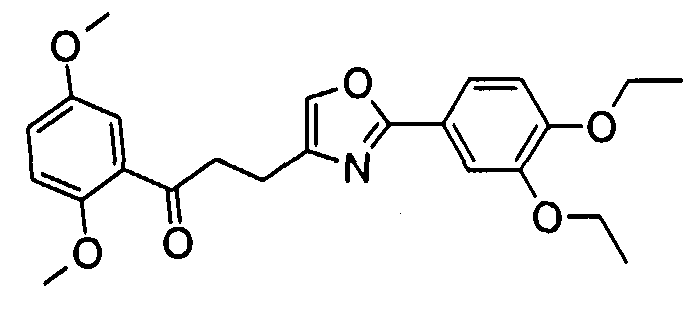
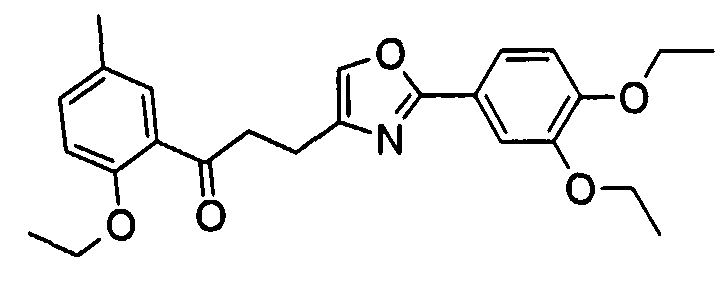
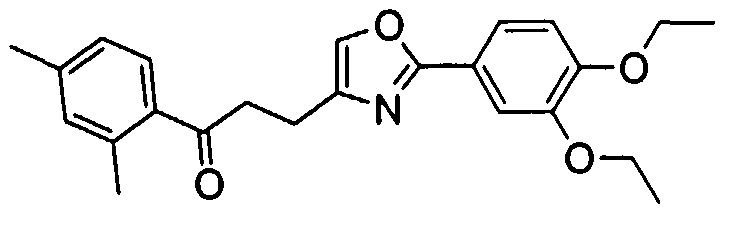
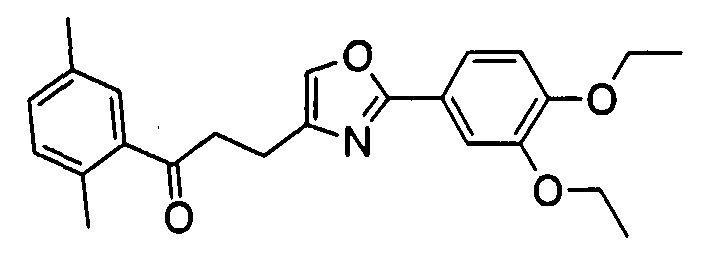
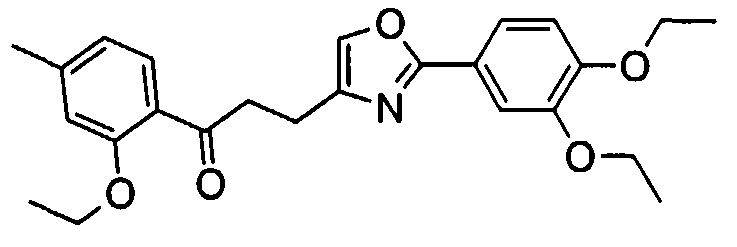
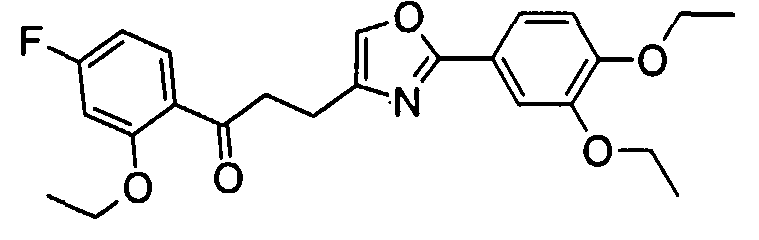
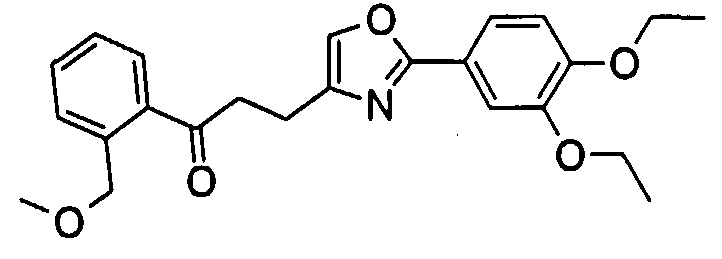
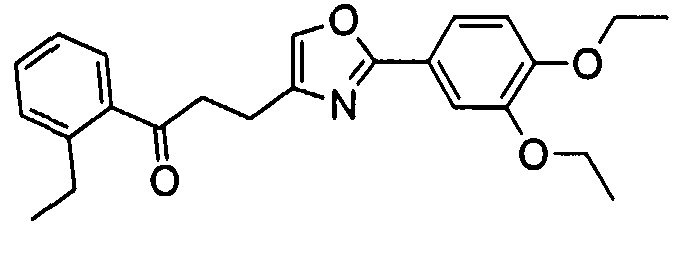
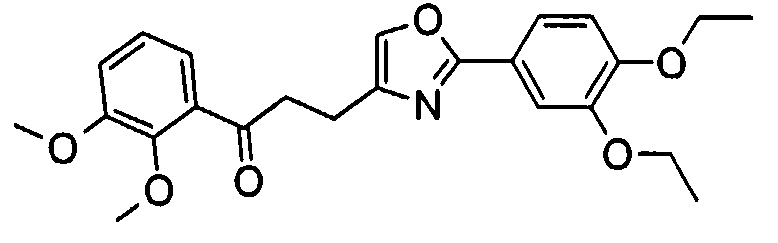
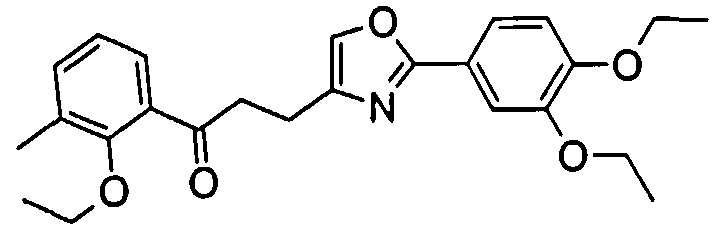
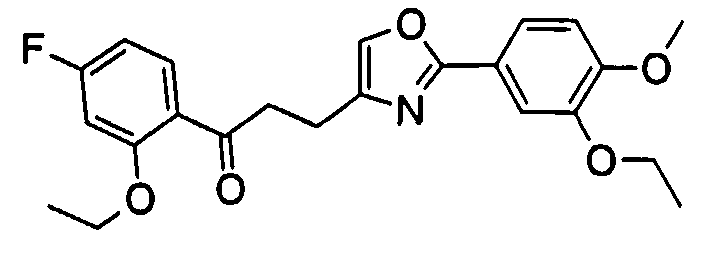
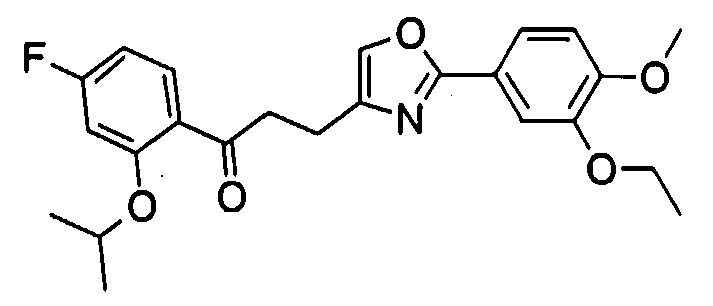
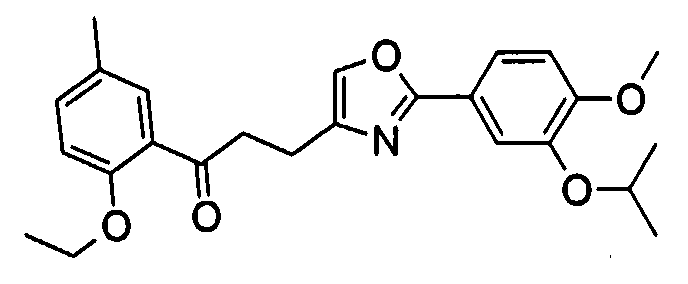
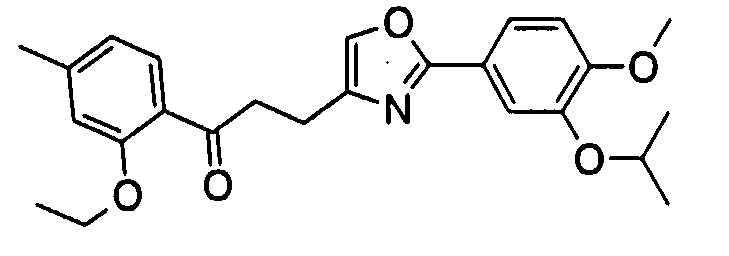
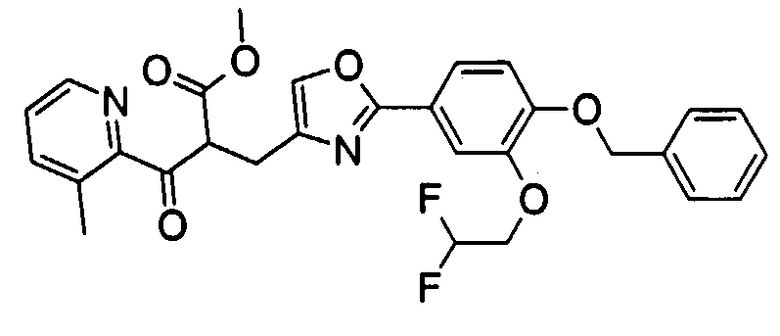
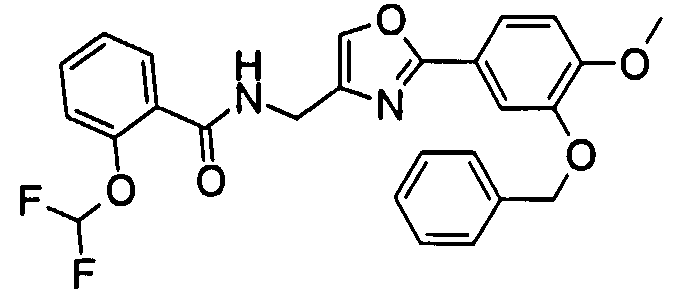
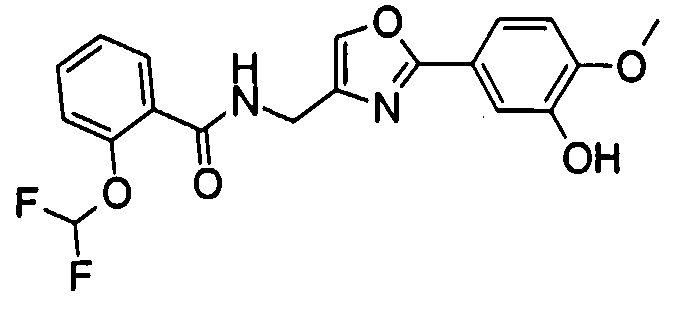
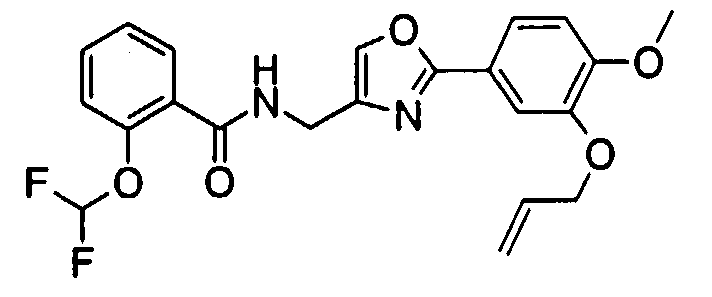
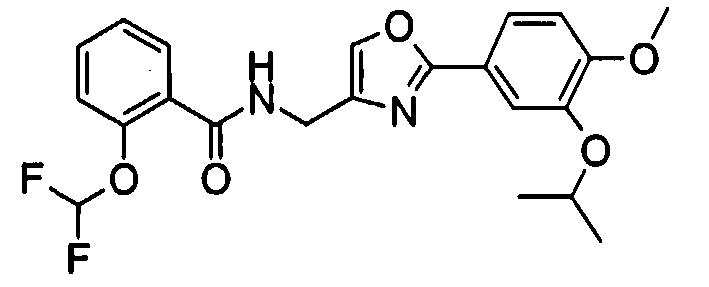
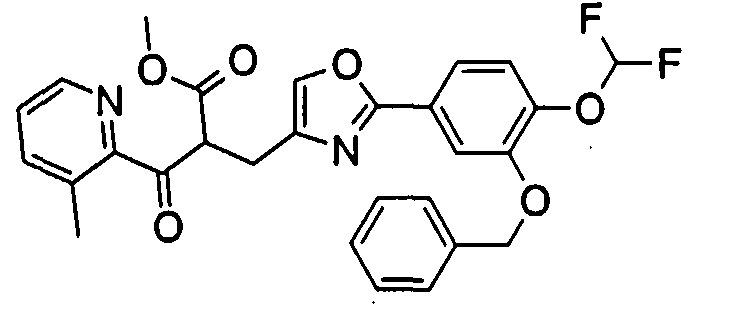
Пример испытания 1
Испытание по определению активности ингибирования фосфодиэстеразы(PDE)4
(1) Получение плазмид в крупном масштабе
Плазмиду, содержащую гены (HPDE4D), кодирующие кДНК PDE4D3 человека (хранится в Otsuka America Pharmaceutical, Inc., Maryland Research Laboratories), трансформировали в E. coli, культивируемые в большом количестве, и очищали с использованием набора EndoFree™ Plasmid Maxi Kit (Qiagen).
(2) Обильная экспрессия и очистка PDE4D
Клетки COS-7, выделенные из почек африканских зеленых мартышек, культивировали с пересевами в среде D-MEM, содержащей 100 единиц/мл пенициллина, 100 мкг/мл стрептомицина и 10% FBS. Клетки трансфицировали плазмидой, полученной в (1) выше, с использованием Lipofectamine™ 2000 (далее указан как “LF2000”, Invitrogen), следуя протоколу изготовителя. Клетки COS-7 инокулировали в 10-см чашки для культивирования за день до трансфекции для получения в день осуществления трансфекции 90% конфлюентности клеток. Чашки для культивирования, где каждая содержала раствор плазмиды (раствор A), в котором 24 мкг плазмиды было разведено в 1,5 мл среды Opti-MEM I Reduced Serum Medium (Invitrogen), и раствор LF2000 (раствор B), в котором 60 мкл LF2000 было разведено в 1,5 мл среды Opti-MEM I Reduced Serum Medium, отдельно оставляли выстаиваться в течение 5 минут при комнатной температуре. Растворы A и B затем смешивали и смеси давали выстояться в течение 20 минут при комнатной температуре. Смесь добавляли к культивируемым клеткам и инкубировали при 37°C (5% CO2) в течение ночи. На следующий день среду заменяли и смесь снова инкубировали в течение ночи для сбора клеток следующим образом. Клетки промывали один раз при помощи PBS (Sigma) и в каждую чашку для культивирования добавляли 10 мл раствора Трипсин-EDTА (Sigma). После того как раствор распределяли в каждую чашку для культивирования, клетки отслаивались, и чашкам давали выстояться в течение примерно 5 минут при 37°C. Отделенные от чашек клетки суспендировали в среде, собирали в пробирки для центрифугирования и центрифугировали при 1200 об./мин в течение 5 минут при 4°C и надосадочные жидкости удаляли при помощи фильтрации. Клетки затем снова промывали при помощи PBS и хранили при -80°C. Буфер KHEM (100 мМ Hepes, 50 мМ KCl, 10 мМ EGTA, 1,92 мМ MgCl2, pH 7,4), содержащий 1 мМ DTT, 1 мкг/мл антипаина, 1 мкг/мл апротинина, 1 мкг/мл лейпептина, 1 мкг/мл пепстатина A, 157 мкг/мл бензамидина и 120 мкг/мл Pefabloc SC, добавляли к собранным клеткам и все это переносили в стеклянный гомогенизатор для гомогенизации на льду. Клеточную суспензию центрифугировали при 1000 об./мин в течение 5 минут при 4°C и надосадочные жидкости снова центрифугировали при 14000 об./мин в течение одного часа. После центрифугирования надосадочные жидкости распределяли в новые пробирки в качестве PDE4D ферментных растворов и хранили в морозильнике для глубокой заморозки.
(3) Определение степени разбавления PDE4D ферментных растворов
Ферментные растворы PDE4D, полученные в (2) выше, растворяли в растворе 20 мМ Трис-HCl (pH 7,4) с получением 10-, 25-, 50-, 100-, 200-, 400- и 800-кратных разведений ферментных растворов. Активность PDE4D измеряли, как указано в (4) ниже. Рассчитывали процент катализируемого cAMP к общему количеству cAMP, и такое разведение, при котором процент составлял от 10% до 30%, использовали в испытании ингибирования, описанном ниже.
(4) Измерение активности ингибирования PDE4D
Отвешивали необходимые количества испытываемых соединений и добавляли к ним 100% диметилсульфоксид (DMSO) для доведения концентрации до 10 мМ. Растворы хранили в морозильнике в качестве исходных растворов каждого испытываемого соединения. После оттаивания, когда это было необходимо, растворы 20-кратно разбавляли при помощи 100% DMSO с получением концентрации 500 мкМ. Затем получали 10-кратные серийные разведения с использованием 100% DMSO для получения испытываемых соединений в различных концентрациях. По 2 мкл растворов, содержащих одну из концентраций испытываемого соединения, отдельно добавляли в 1,2-мл пробирки, в которые заранее было внесено 23 мкл 20 мМ Трис-HCl (pH 7,4). 25 мкл PDE4D ферментного раствора с оптимальной степенью разбавления, определенной в (3) выше, добавляли в каждую пробирку на льду и в пробирки добавляли 50 мкл раствора субстрата, содержащего 2 мкМ[3H]cAMP, полученного путем разбавления буфером 20 мМ Трис-HCl (pH 7,4), содержащим 10 мМ MgCl2. Конечная концентрация DMSO в реакционной жидкости составляла 2%. После смешивания смесь инкубировали в течение 10 минут при 30°C. По завершении инкубации пробирки помещали на баню с кипящей водой на 3 минуты и реакцию останавливали. После охлаждения пробирок на льду в них добавляли 25 мкл раствора 0,2 мг/мл змеиного яда и после смешивания смесь инкубировали в течение 10 минут при 30°C. По завершении инкубации добавляли 0,4 мл раствора смолы Dowex 1×8, полученного в EtOH:H2O (1:1). После смешивания пробиркам давали выстояться при комнатной температуре, по меньшей мере, в течение часа. 50 мкл надосадочной жидкости из каждой пробирки помещали в одну из лунок счетного планшета topCount и планшет сушили в течение ночи. 3H радиоактивность (имп./мин) измеряли с использованием TopCountTM.
Значения ИК50 (концентрация, обеспечивающая 50% ингибирование гидролиза субстрата) для испытываемых соединений определяли при помощи пакета статистических программ Excel (Microsoft Excel 2000 SR-1), с использованием регрессионного анализа.
Результаты представлены в таблице 41. Таблица показывает, что соединения, представленные формулой (I), обладают отличной активностью ингибирования PDE4.
В структурных формулах, представленных в таблице ниже, -Me означает метильную группу, -Et означает этильную группу, -OMe означает метоксигруппу, -OEt означает этоксигруппу и -SMe означает метилтиогруппу.
Таблица 41
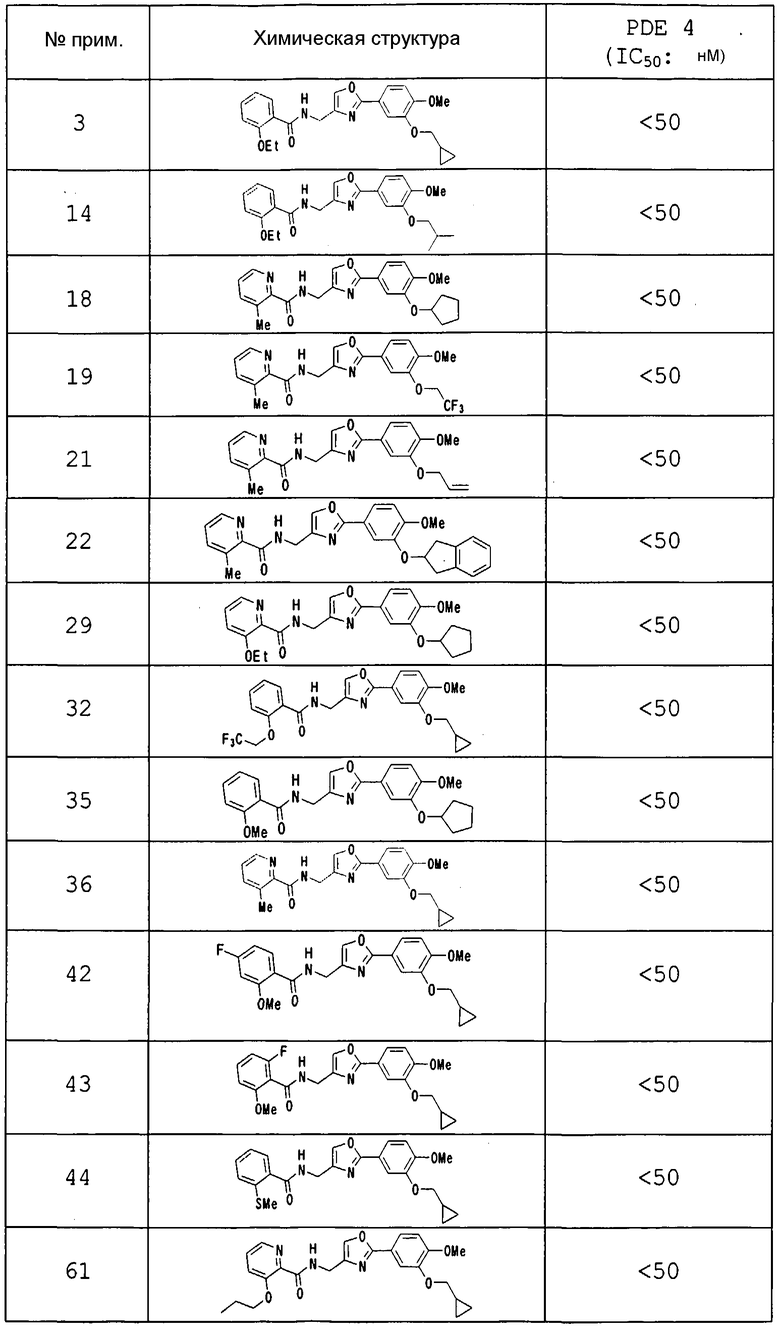
Таблица 41 (продолжение)
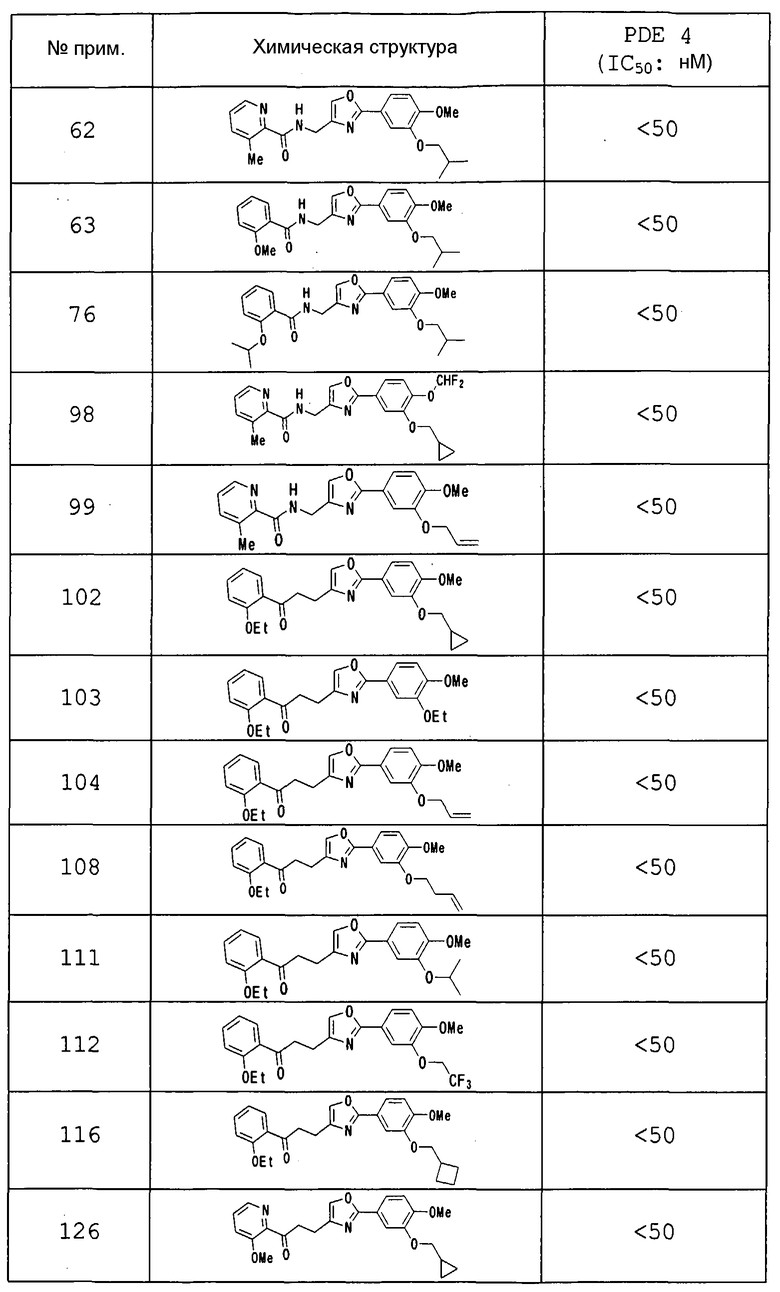
Таблица 41 (продолжение)
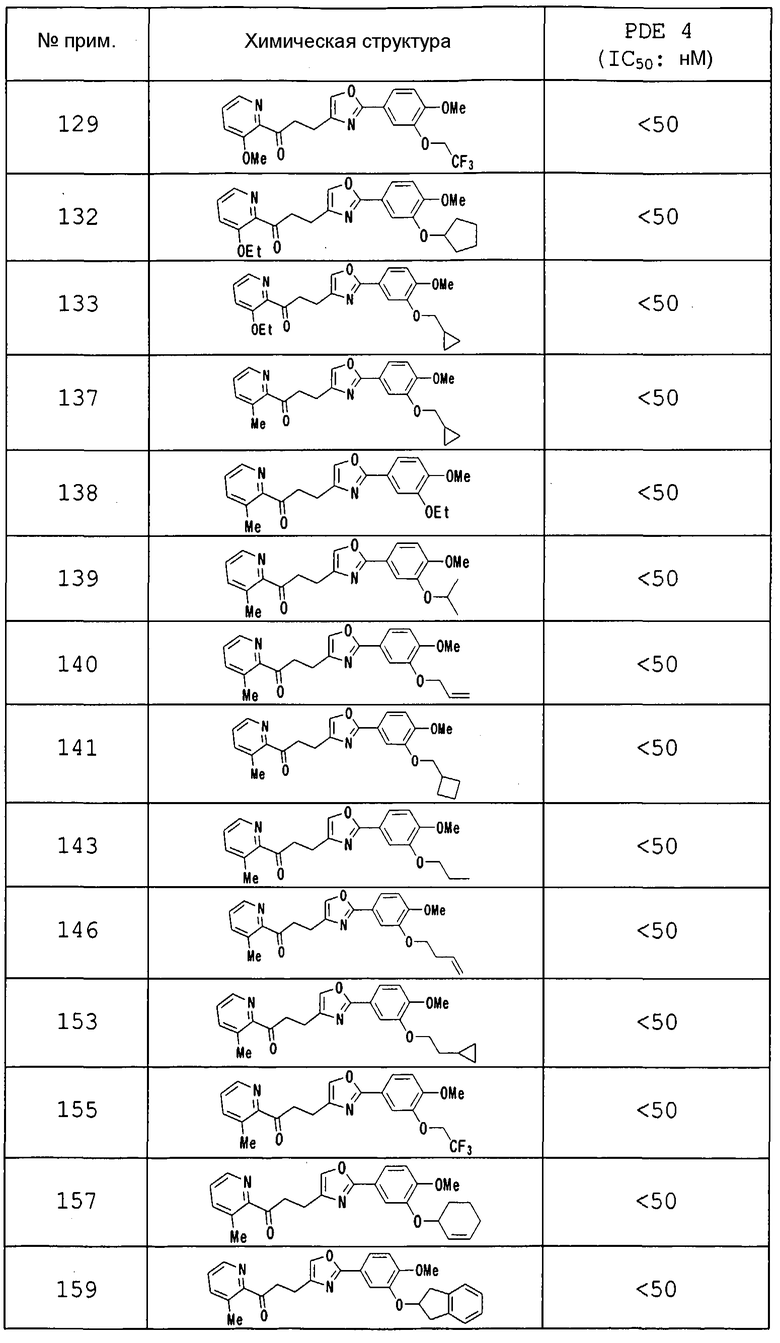
Таблица 41 (продолжение)
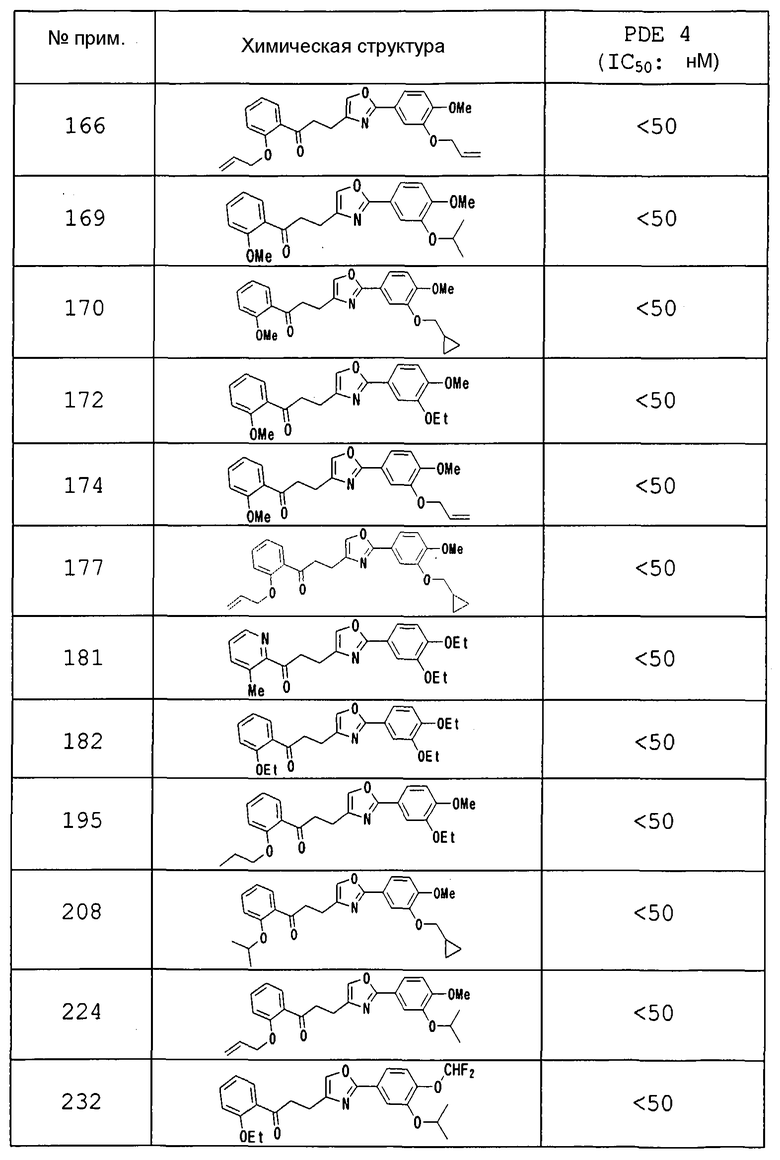
Таблица 41 (продолжение)
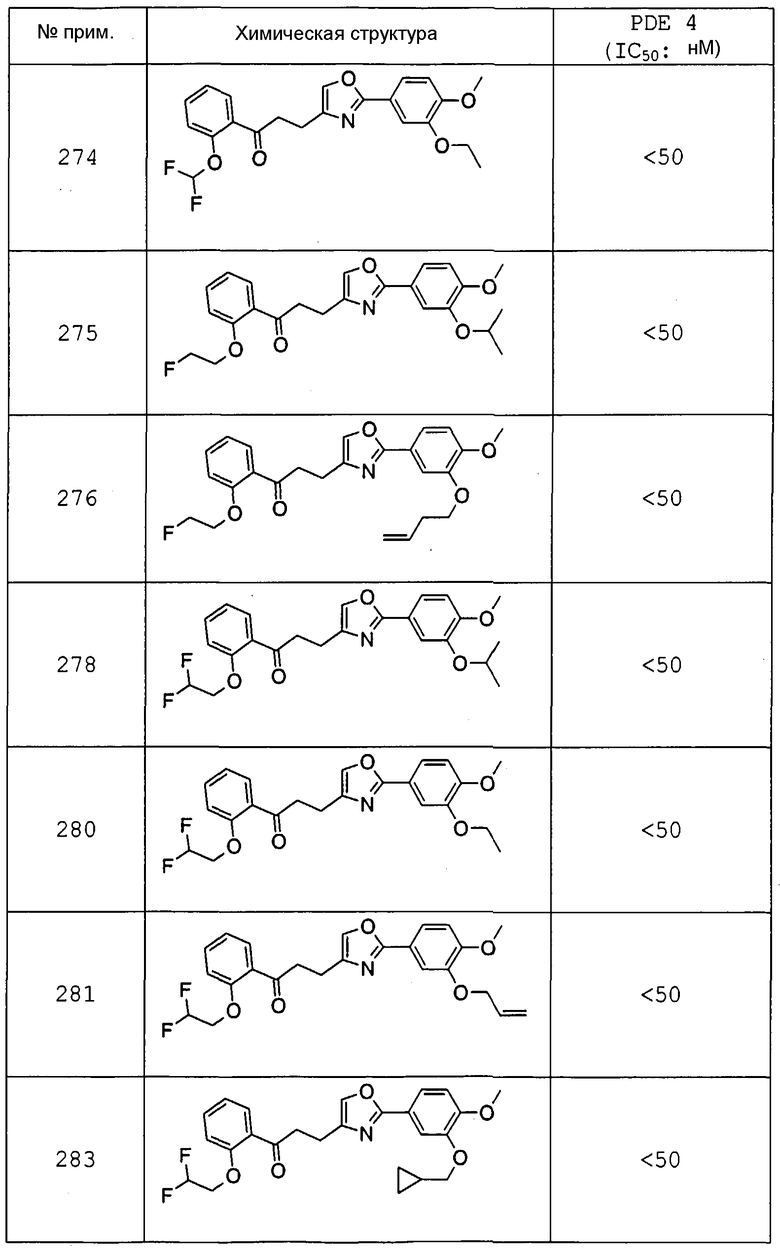
Таблица 41 (продолжение)
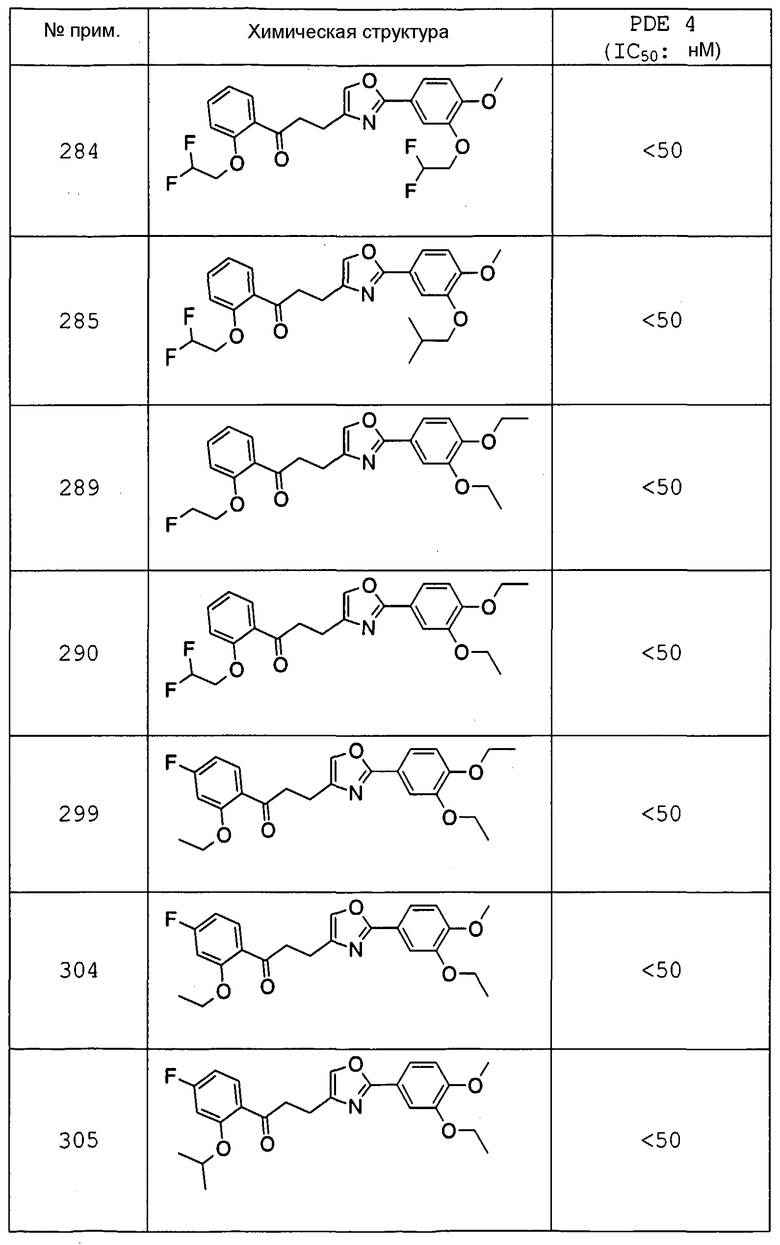
Таблица 41 (продолжение)
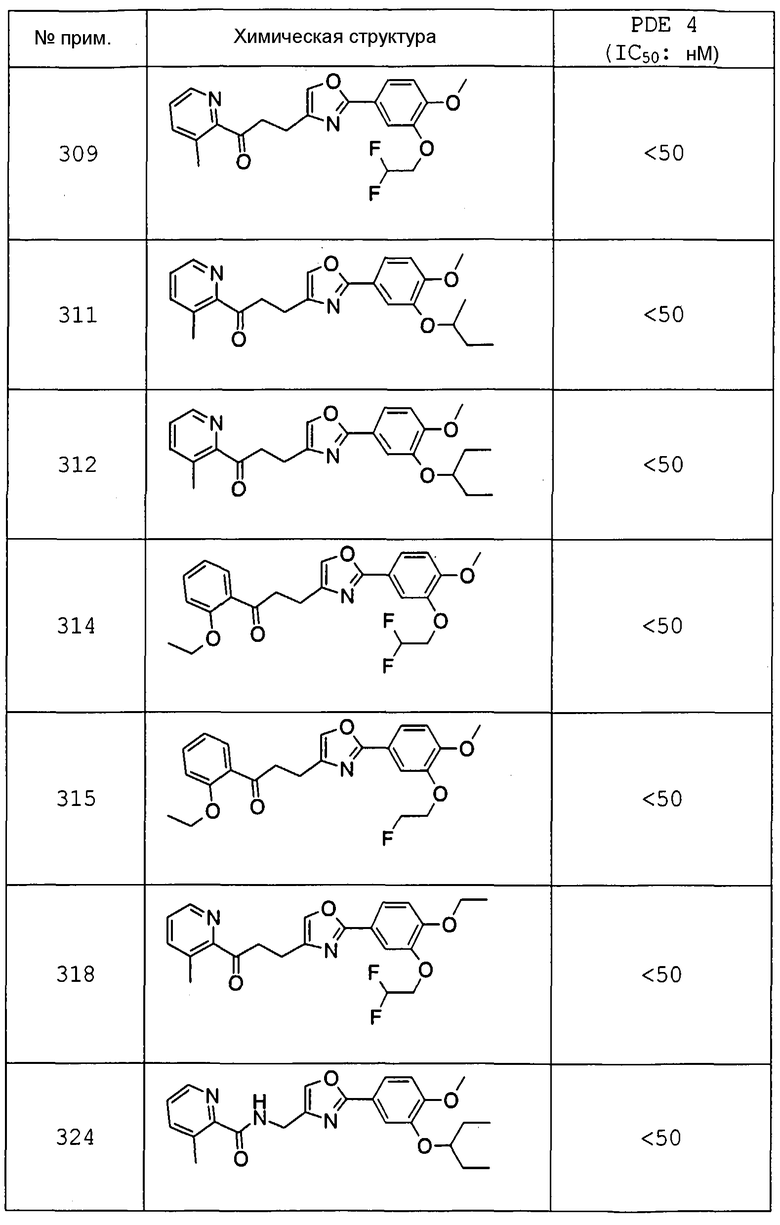
Таблица 41 (продолжение)
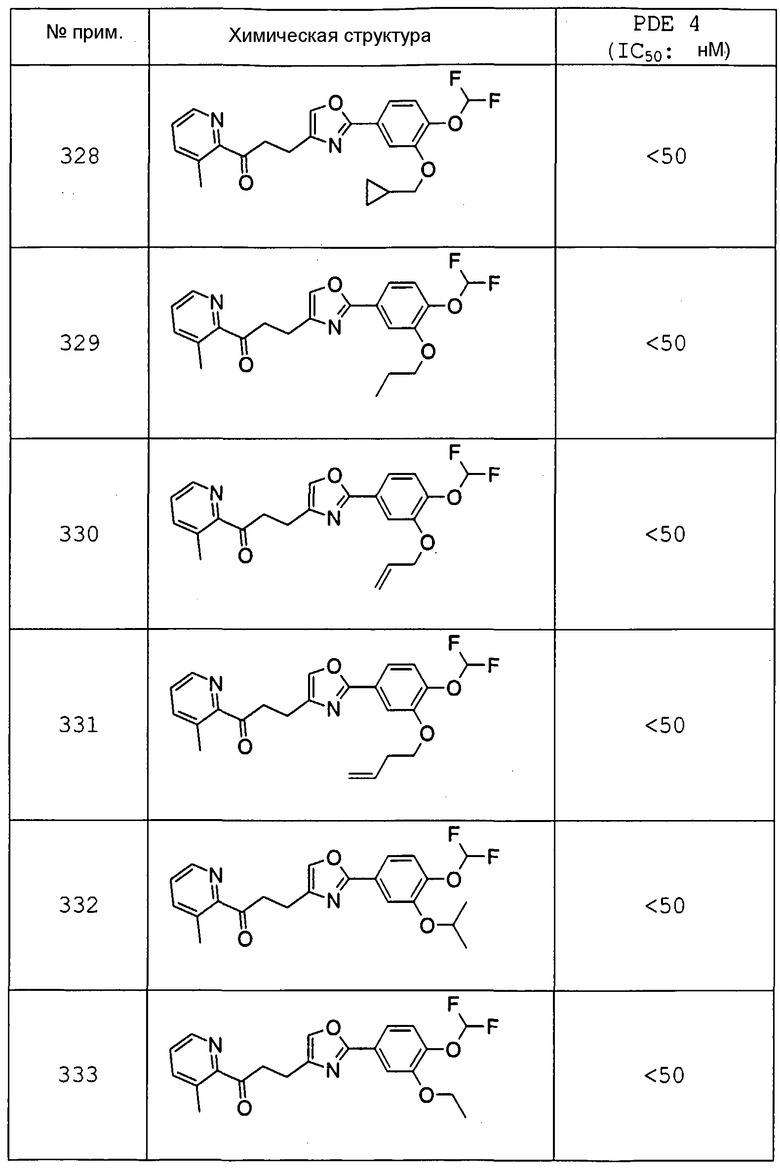
Таблица 41 (продолжение)
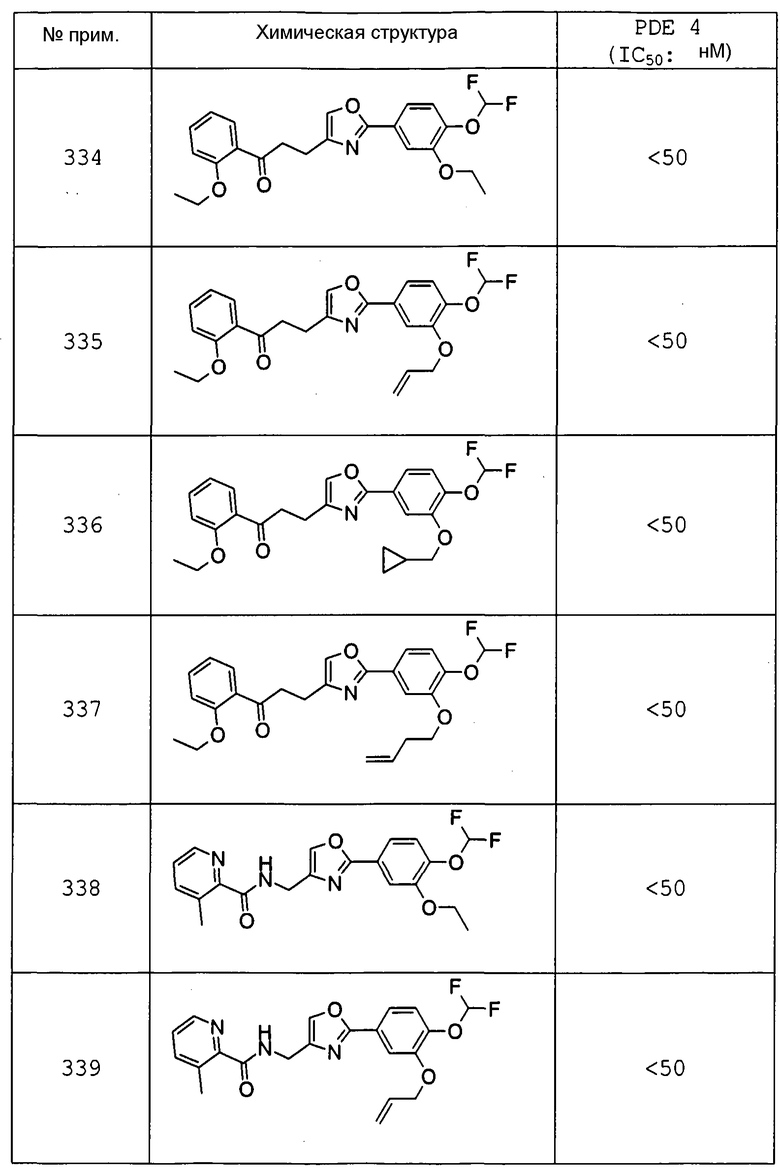
Таблица 41 (продолжение)
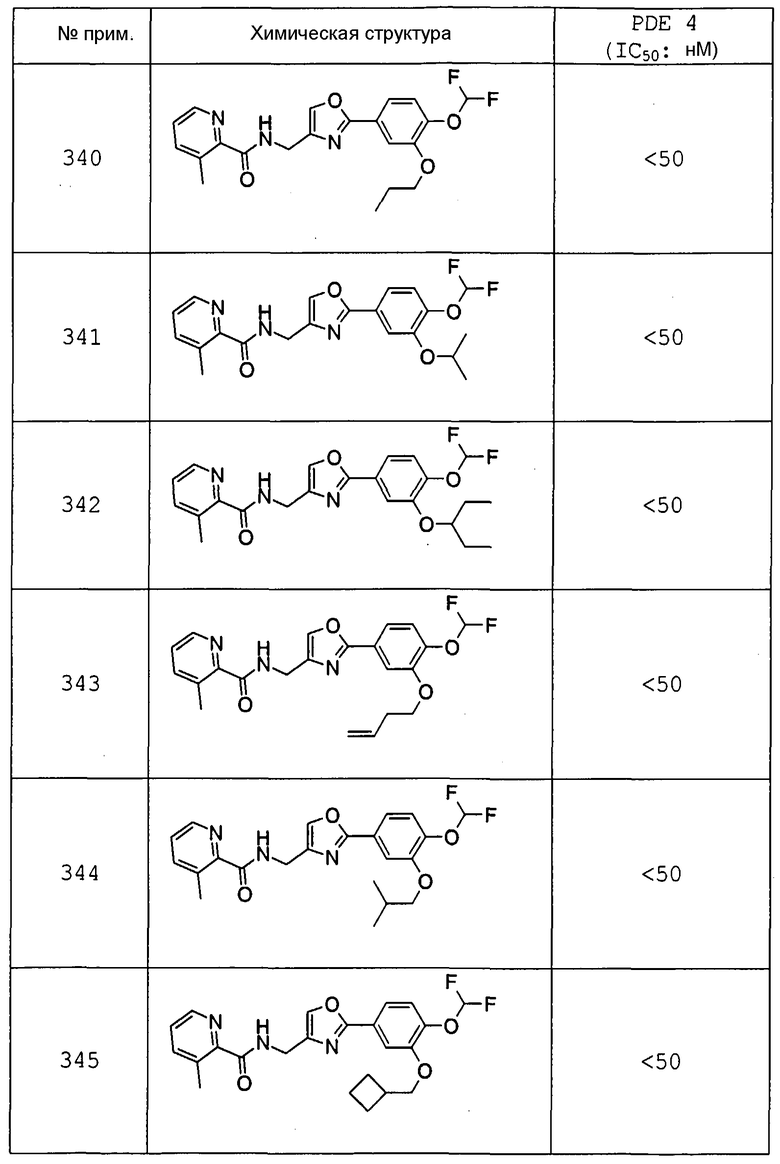
Таблица 41 (продолжение)
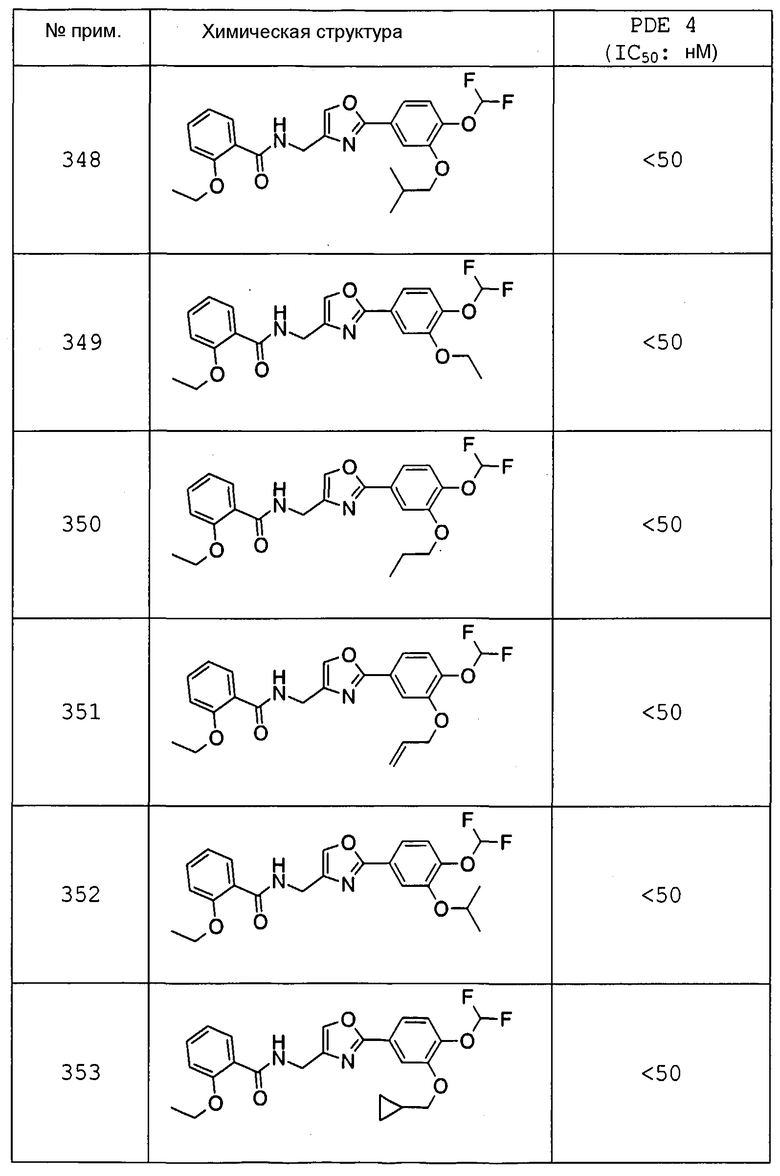
Таблица 41 (продолжение)
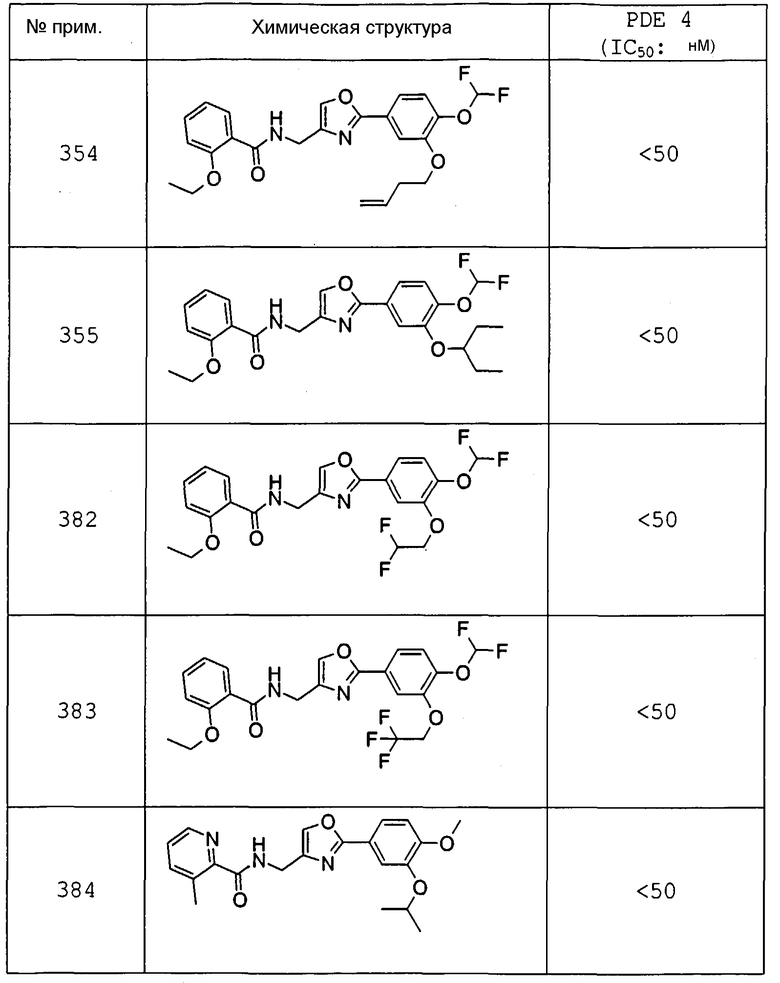
Пример испытания 2
Измерение активности ингибирования продукции TNF-α
Активность ингибирования продукции TNF-α определяли в соответствии со следующими испытаниями.
(1) Выделение мононуклеарных клеток из периферической крови мыши
Мононуклеарные клетки выделяли из гепаринизированной крови, взятой у самцов мышей BALB/c (Charles River Laboratories, Japan), путем центрифугирования в градиенте плотности с использованием Lympholyte-M (Cedarlane Laboratories). Количество жизнеспособных клеток в мононуклеарных клетках периферической крови подсчитывали с использованием красителя трипанового синего и подготавливали в клеточной культуральной среде (среда RPMI 1640, содержащая 10% FCS) до 1,25×106 клеток/мл.
(2) Индукция продукции TNF-α
Испытываемые соединения растворяли в ДМСО и растворы испытываемых соединений разбавляли для использования в клеточной культуральной среде. 20 мкл растворов испытываемых соединений различных концентраций и 160 мкл суспензий мононуклеарных клеток периферической крови помещали в 96-луночный планшет и культивировали в течение 30 минут. Добавляли 20 мкл (конечная концентрация 1 мкг/мл) липополисахарида (LPS), полученного из E. coli (серотип 055:B5), чтобы индуцировать продукцию TNF-α. Смеси затем культивировали при 37°C в течение 5 часов и культуральный супернатант удаляли из каждой лунки.
(3) Измерение концентрации TNF-α
Концентрации TNF-α в культуральных супернатантах измеряли методом ELISA (OptEIATM Set Mouse TNF-α, BD Pharmingen). Значения ИК50 (концентрация, которая обеспечивала 50% ингибирование продукции TNF-α) для испытываемых соединений определяли при помощи пакета статистических программ Excel (Microsoft Excel 2000 SR-1) с использованием регрессионного анализа.
Полученные результаты представлены в таблице 42.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ И ФАРМАЦЕВТИЧЕСКОЕ СРЕДСТВО, СОДЕРЖАЩЕЕ ИХ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2002 |
|
RU2315746C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ЦИКЛИЧЕСКОГО АМИДА | 2001 |
|
RU2257384C2 |
| КОНДЕНСИРОВАННОЕ ГЕТЕРОЦИКЛИЧЕСКОЕ ПРОИЗВОДНОЕ, СОДЕРЖАЩАЯ ЕГО ЛЕЧЕБНАЯ КОМПОЗИЦИЯ И ЕЕ ПРИМЕНЕНИЕ В МЕДИЦИНЕ | 2006 |
|
RU2418803C2 |
| ПРОИЗВОДНОЕ 8-АЗАПРОСТАГЛАНДИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, АГЕНТ ДЛЯ ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ | 2003 |
|
RU2306309C2 |
| ПРОИЗВОДНЫЕ ПИПЕРИДИНА И СРЕДСТВО, СОДЕРЖАЩЕЕ ПРОИЗВОДНОЕ ПИПЕРИДИНА В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2001 |
|
RU2275359C2 |
| ПРОИЗВОДНЫЕ 1,3-ДИОКСОИНДЕНА, ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ АНТИВИРУСНАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ИХ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2012 |
|
RU2566761C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, ИХ ПРИМЕНЕНИЕ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ СОСТОЯНИЙ, ОПОСРЕДОВАННЫХ СХСR4 И CCR5 | 2001 |
|
RU2277092C2 |
| ПИРАЗОЛО [1, 5-А] ПИРИДИНЫ И СОДЕРЖАЩИЕ ИХ ЛЕКАРСТВЕННЫЕ СРЕДСТВА | 2002 |
|
RU2308457C2 |
| СОЕДИНЕНИЯ, КОМПОЗИЦИИ И СПОСОБЫ ПРЕДУПРЕЖДЕНИЯ МЕТАСТАЗОВ РАКОВЫХ КЛЕТОК | 2010 |
|
RU2519123C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, МОДЕЛИРУЮЩИЕ АКТИВНОСТЬ ХЕМОКИНОВОГО РЕЦЕПТОРА, ИХ ПРИМЕНЕНИЕ И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2001 |
|
RU2297413C2 |
Настоящее изобретение относится к соединению оксазола, представленному формулой (1) и его фармацевтически приемлемым солям. В формуле (1)
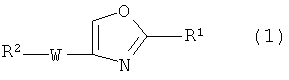
R1 представляет собой фенильную группу, которая может содержать один или два заместителя, выбранных из следующих групп (1-1)-(1-11): (1-1) гидроксигруппы, (1-2) незамещенные или галогензамещенные низшие алкоксигруппы, (1-3) низшие алкенилоксигруппы, (1-4) низшие алкинилоксигруппы, (1-5) циклоС3-8алкил (низший) алкоксигруппы, (1-6) циклоС3-8алкилоксигруппы, (1-7) циклоС3-8алкенилоксигруппы, (1-8) дигидроинденилоксигруппы, (1-9) гидрокси(низший)алкоксигруппы, (1-10) оксиранил(низший)алкоксигруппы, и (1-11) фенил(низший)алкоксигруппы; R2 представляет собой фенильную группу или гетероциклическую группу, выбранную из пиридина, пиразина, изохинолина, пирролидина, пиперазина, морфолина, каждая из которых может содержать один или два заместителя, выбранных из следующих групп (2-1)-(2-10): (2-1) гидроксигруппы, (2-2) незамещенные или галогензамещенные низшие алкоксигруппы, (2-3) незамещенные или галогензамещенные низшие алкильные группы, (2-4) низшие алкенилоксигруппы, (2-5) атомы галогена, (2-6) низшие алканоильные группы, (2-7) низшие алкилтиогруппы, (2-8) низшие алкилсульфонильные группы, (2-9) оксогруппы и (2-10) группы низший алкокси-низший алкокси; и W представляет собой двухвалентную группу, представленную формулой (i) или (ii): формула (i) -Y1-A1-, формула (ii) -Y2-С(=O)-, где А1 представляет собой низшую алкениленовую группу или низшую алкиленовую группу, которая может содержать один заместитель, выбранный из группы, состоящей из гидроксигруппы и низшей алкоксикарбонильной группы, Y1 представляет собой простую связь,
-С(=O)-, -C(=O)-N(R3)-, -N(R4)-C(=O)-, -S(O)m-NH- или -S(O)n-, где R3 и R4, каждый независимо, представляют собой атом водорода или низшую алкильную группу, и m и n, каждый независимо, представляют собой целое число, имеющее значение 2, и Y2 представляет собой пиперазиндиильную группу, или двухвалентную группу, представленную формулой (iii) или (iv): формула (iii) -С(=О)-А2-N(R5)-, формула (iv) А3-N(R6)-, где А2 и А3, каждый независимо, представляют собой низшую алкиленовую группу, и R5 и R6, каждый независимо, представляют собой атом водорода. Изобретение также относится к фармацевтической композиции для лечения или профилактики заболеваний, опосредованных фосфодиэстеразой 4 и/или опосредованных фактором некроза опухоли α, содержащей соединение изобретения в качестве активного ингредиента, к фармацевтической композиции для лечения или профилактики атопического дерматита, включающей соединение изобретения, к применению соединения в качестве лекарственного средства, к применению соединения в качестве ингибитора фосфодиэстеразы 4 и/или ингибитора продукции фактора некроза опухоли α и к способу лечения или профилактики заболеваний, опосредованных фосфодиэстеразой 4 и/или опосредованных фактором некроза опухоли α, включающему введение эффективной дозы соединения изобретения. 6 н. и 6 з.п. ф-лы, 42 табл.
1. Соединение оксазола, представленное формулой (1)

где R1 представляет собой фенильную группу, которая может содержать один или два заместителя, выбранных из следующих групп (1-1)-(1-11):
(1-1) гидроксигруппы,
(1-2) незамещенные или галогензамещенные низшие алкоксигруппы,
(1-3) низшие алкенилоксигруппы,
(1-4) низшие алкинилоксигруппы,
(1-5) циклоС3-8алкил(низший)алкоксигруппы,
(1-6) циклоС3-8алкилоксигруппы,
(1-7) циклоС3-8алкенилоксигруппы,
(1-8) дигидроинденилоксигруппы,
(1-9) гидрокси(низший)алкоксигруппы,
(1-10) оксиранил(низший)алкоксигруппы, и
(1-11) фенил(низший)алкоксигруппы;
R2 представляет собой фенильную группу или гетероциклическую группу, выбранную из пиридина, пиразина, изохинолина, пирролидина, пиперазина, морфолина, каждая из которых может содержать один или два заместителя, выбранных из следующих групп (2-1)-(2-10):
(2-1) гидроксигруппы,
(2-2) незамещенные или галогензамещенные низшие алкоксигруппы,
(2-3) незамещенные или галогензамещенные низшие алкильные группы,
(2-4) низшие алкенилоксигруппы,
(2-5) атомы галогена,
(2-6) низшие алканоильные группы,
(2-7) низшие алкилтиогруппы,
(2-8) низшие алкилсульфонильные группы,
(2-9) оксогруппы и
(2-10) группы низший алкокси-низший алкокси; и
W представляет собой двухвалентную группу, представленную формулой (i) или (ii):
-Y1-A1- (i)
-Y2-C(=O)- (ii)
где А1 представляет собой низшую алкениленовую группу или низшую алкиленовую группу, которая может содержать один заместитель, выбранный из группы, состоящей из гидроксигруппы и низшей алкоксикарбонильной группы,
Y1 представляет собой простую связь, -С(=O)-, -C(=O)-N(R3)-, -N(R4)-C(=O)-, -S(O)m-NH- или -S(O)n-,
где R3 и R4, каждый независимо, представляют собой атом водорода или низшую алкильную группу, и m и n, каждый независимо, представляют собой целое число, имеющее значение 2,
Y2 представляет собой пиперазиндиильную группу, или двухвалентную группу, представленную формулой (iii) или (iv)
-С(=О)-А2-N(R5)- (iii)
А3-N(R6)- (iv)
где А2 и А3, каждый независимо, представляют собой низшую алкиленовую группу, R5 и R6, каждый независимо, представляют собой атом водорода;
или его фармацевтически приемлемая соль.
2. Соединение по п.1, где R1 представляет собой фенильную группу, которая имеет 1 или 2 заместителя, выбранных из следующих групп: (1-2), (1-3), (1-4) и (1-5):
(1-2) незамещенные или галогензамещенные низшие алкоксигруппы,
(1-3) низшие алкенилоксигруппы,
(1-4) низшие алкинилоксигруппы и
(1-5) циклоС3-8алкил(низший)алкоксигруппы;
R2 представляет собой фенильную группу или пиридильную группу, каждая из которых может содержать 1 или 2 заместителя, выбранных из группы, состоящей из следующих: (2-2), (2-3), (2-4) и (2-5):
(2-2) незамещенные или галогензамещенные низшие алкоксигруппы,
(2-3) незамещенные или галогензамещенные низшие алкильные группы,
(2-4) низшие алкенилоксигруппы и
(2-5) атомы галогена;
W представляет собой двухвалентную группу, представленную формулой (i)
-Y1-А1-, (i)
в которой А1 представляет собой низшую алкиленовую группу, и
Y1 представляет собой -С(=O)- или -C(=O)-N(R3)-,
где R3 представляет собой атом водорода.
3. Соединение по п.2, где R1 представляет собой фенильную группу, содержащую два заместителя, выбранных из следующих групп: (1-2), (1-3), (1-4) и (1-5):
(1-2) незамещенные или галогензамещенные низшие алкоксигруппы,
(1-3) низшие алкенилоксигруппы,
(1-4) низшие алкинилоксигруппы и
(1-5) циклоС3-8алкил(низший)алкоксигруппы;
R2 представляет собой фенильную группу или пиридильную группу, каждая из которых может содержать от 1 до 2 заместителей, выбранных из следующих групп: (2-2), (2-3), (2-4) и (2-5):
(2-2) незамещенные или галогензамещенные низшие алкоксигруппы,
(2-3) незамещенные или галогензамещенные низшие алкильные группы,
(2-4) низшие алкенилоксигруппы и
(2-5) атомы галогена; и
W представляет собой двухвалентную группу, представленную формулой (i)
-Y1-A1-, (i)
в которой А1 представляет собой низшую алкиленовую группу и Y1 представляет собой -С(=O)- или -C(=O)-N(R3)-, где R3 представляет собой атом водорода.
4. Соединение по п.3, где R1 представляет собой фенильную группу, замещенную в фенильном кольце двумя низшими алкоксигруппами, фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одной циклоС3-8алкил-(низший)алкоксигруппой, фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одной галогензамещенной низшей алкоксигруппой, фенильную группу, замещенную в фенильной группе одной низшей алкоксигруппой и одной низшей алкенилоксигруппой, фенильную группу, замещенную в фенильном кольце одной галогензамещенной низшей алкоксигруппой и одной циклоС3-8алкил(низший)алкоксигруппой, фенильную группу, замещенную в фенильном кольце одной галогензамещенной низшей алкоксигруппой и одной низшей алкенилоксигруппой, или фенильную группу, замещенную в фенильном кольце двумя галогензамещенными низшими алкоксигруппами;
R2 представляет собой низшую алкоксифенильную группу, низшую алкенилоксифенильную группу, галогензамещенную низшую алкоксифенильную группу, низшую алкилпиридильную группу или фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одним атомом галогена; и
W представляет собой двухвалентную группу, представленную формулой (i)
-Y1-A1-, (i)
в которой А1 представляет собой С1-4алкиленовую группу и
Y1 представляет собой -С(=O)- или -C(=O)-N(R3)-,
где R3 представляет собой атом водорода.
5. Соединение по п.4, где R1 представляет собой фенильную группу, замещенную в фенильном кольце двумя низшими алкоксигруппами, фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одной циклоС3-8алкил-(низший)алкоксигруппой, фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одной галогензамещенной низшей алкоксигруппой, фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одной низшей алкенилоксигруппой, фенильную группу, замещенную в фенильном кольце одной галогензамещенной низшей алкоксигруппой и одной циклоС3-8алкил(низший)алкоксигруппой, фенильную группу, замещенную в фенильном кольце одной низшей галогензамещенной низшей алкоксигруппой и одной низшей алкенилоксигруппой, или фенильную группу, замещенную в фенильном кольце двумя галогензамещенными низшими алкоксигруппами;
R2 представляет собой низшую алкоксифенильную группу, низшую алкенилоксифенильную группу, галогензамещенную низшую алкоксифенильную группу, низшую алкилпиридильную группу или фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одним атомом галогена; и
W представляет собой двухвалентную группу, представленную формулой (i)
-Y1-A1-, (i)
в которой А1 представляет собой С1-4алкиленовую группу и
Y1 представляет собой -С(=O)-.
6. Соединение по п.4, где R1 представляет собой фенильную группу, замещенную в фенильном кольце одной низшей алкоксигруппой и одной галогензамещенной низшей алкоксигруппой, фенильную группу, замещенную в фенильном кольце одной галогензамещенной низшей алкоксигруппой и одной циклоС3-8алкил(низший)алкоксигруппой, или фенильную группу, замещенную в фенильном кольце одной галогензамещенной низшей алкоксигруппой и одной низшей алкенилоксигруппой;
R2 представляет собой низшую алкоксифенильную группу или низшую алкилпиридильную группу; и
W представляет собой двухвалентную группу, представленную формулой (i)
-Y1-А1-, (i)
в которой А1 представляет собой C1-4алкиленовую группу и
Y1 представляет собой -C(=O)-N(R3)-,
где R3 представляет собой атом водорода.
7. Фармацевтическая композиция для лечения или профилактики заболеваний, опосредованных фосфодиэстеразой 4 и/или опосредованных фактором некроза опухоли а, содержащая соединение или фармацевтически приемлемую соль по любому из пп.1-6 в качестве активного ингредиента и фармацевтически приемлемый носитель.
8. Фармацевтическая композиция для лечения или профилактики атопического дерматита, где композиция включает соединение или фармацевтически приемлемую соль по любому из пп.1-6.
9. Применение соединения или фармацевтически приемлемой соли по любому из пп.1-6 в качестве лекарственного средства, обладающего свойствами ингибитора фосфодиэстеразы (PDE) 4 и/или ингибитора фактора некроза опухоли α (TNF-α).
10. Применение соединения или фармацевтически приемлемой соли по любому из пп.1-6 в качестве ингибитора фосфодиэстеразы 4 и/или ингибитора продукции фактора некроза опухоли α.
11. Способ лечения или профилактики заболеваний, опосредованных фосфодиэстеразой 4 и/или опосредованных фактором некроза опухоли α, включающий введение эффективной дозы соединения или фармацевтически приемлемой соли по любому из пп.1-6 человеку или животному.
12. Соединение или его фармацевтически приемлемая соль по п.6, которое выбирают из группы, состоящей из следующих соединений:
N-[2-(4-дифторметокси-3-изобутоксифенил)оксазол-4-илметил]-3-метилпиколинамид,
N-[2-(3-циклобутилметокси-4-дифторметоксифенил)оксазол-4-илметил]-3-метилпиколинамид,
N-[2-(4-дифторметокси-3-изобутоксифенил)оксазол-4-илметил]-2-этоксибензамид,
N-[2-(4-дифторметокси-3-этоксифенил)оксазол-4-илметил]-2-этоксибензамид,
N-[2-(3-аллилокси-4-дифторметоксифенил)оксазол-4-илметил]-2-этоксибензамид,
N-[2-(4-дифторметокси-3-изопропоксифенил)оксазол-4-илметил]-2-этоксибензамид,
N-[2-(3-циклопропилметокси-4-дифторметоксифенил)оксазол-4-илметил]-2-этоксибензамид и
N-[2-(3-бут-3-енилокси-4-дифторметоксифенил)оксазол-4-илметил]-2-этоксибензамид.
| MALAMAS M.S | |||
| et al | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Jounal of Medicinal Chemistry | |||
| Машина для изготовления проволочных гвоздей | 1922 |
|
SU39A1 |
| RU 2004105925 A, 10.07.2005 | |||
| WO 9808830 A1, 05.03.1998 | |||
| US 5814651 A, 29.09.1998 | |||
| WO 9600218 A1, 04.01.1996. | |||
Авторы
Даты
2011-05-20—Публикация
2006-11-14—Подача