Эта заявка испрашивает приоритет предварительной заявки на патент США 60/718906, озаглавленной "Удаление диоксида углерода из потоков отходов путем совместного образования синтетических карбонатных минералов", выданной 20 сентября 2005 г.; предварительной заявки на патент США 60/642698, выданной 10 января 2005 г.; и предварительной заявки на патент США 60/612355, выданной 23 сентября 2004 г. Полный текст каждой из вышеуказанных заявок (включая приложения) с формулами изобретения приводится здесь, в частности, путем соответствующей ссылки на них.
УРОВЕНЬ ТЕХНИКИ
1. Область техники, к которой относится изобретение
Настоящее изобретение в целом относится к удалению диоксида углерода и, кроме того, других загрязняющих веществ из потоков отходов. Более конкретно, настоящее изобретение относится к удалению диоксида углерода и других загрязняющих веществ из потоков отходов путем абсорбции диоксида углерода и других загрязняющих веществ из сконцентрированных потоков топочных газов и затем совместного получения карбонатных и/или бикарбонатных материалов, которые захватывают и нейтрализуют любые абсорбированные попутные загрязняющие вещества.
2. Предшествующий уровень техники
В течение последних четырех десятилетий промышленные выбросы в атмосферу вызывают все большую озабоченность на национальном и международном уровне как в частном, так и промышленных секторах. В частности, внимание было сосредоточено на газах, вызывающих парниковый эффект, которые обладают свойством удерживать солнечное тепло в атмосфере, приводя к "парниковому эффекту". Парниковый эффект возникает тогда, когда поступающее от солнца тепло поглощается в атмосфере и гидросфере земли, повышая среднюю температуру атмосферы, температуру океана, и другие срединные и средние величины температур планеты, вплоть до возникновения проблемы изменения климата; этот эффект обычно связывают с воздействием на тепловой баланс Земли, хотя по поводу скоростей, степени, в которой сжигаемые человеком материалы на него воздействуют, и степени, направления и величины эффекта единое мнение отсутствует. Несмотря на расхождение в оценках, для всех очевидно, что удаления CO2 (и других химических веществ) из основных источников выбросов будет выгодным в том случае, если затраты на это будут достаточно небольшими.
Газы, вызывающие парниковый эффект, в основном состоят из диоксида углерода и образуются на городских энергетических установках и крупномасштабных производствах на месте их расположения, однако они также образуются и при любом обычном сжигании углерода (например, в автомобилях, при расчистках дождевого леса, просто горении и так далее), хотя их самые концентрированные точечные выбросы происходят по всему миру на энергетических установках, делая решение проблемы снижения или удаления выбросов из этих конкретных мест привлекательной для осуществления технологии удаления. Так как производство энергии является главной причиной выбросов газов, вызывающих парниковый эффект, в течение последних тридцати лет различными методами исследовались и интенсивно изучались такие способы, как снижение углеродной нагрузки, повышение эффективности и секвестр углерода из топочных газов энергетической установки.
Снижение интенсивности применения углерода включает использование альтернативных источников энергии, не содержащих углерод, таких как ядерные, гидроэлектрические, фотоэлектрические, геотермальные и другие источники электроэнергии, для уменьшения доли энергии, производимой за счет исключительно сжигания углерода. В то время как каждый из этих способов производства энергии продолжает вносить свой вклад в суммарный объем производства энергии, прогнозы темпов роста мирового потребления электроэнергии превышают темпы роста производства энергии этими методами. Поэтому, ожидается, что выбросы газов, вызывающих парниковый эффект, будут увеличиваться, несмотря на рост использования источников энергии, не связанных с применением углерода.
Повышение эффективности обычно сводилось к способам улучшения сжигания углерода путем предварительного сжигания, декарбонизации, сжигания с кислородом и так далее, сначала снижая количество производимого CO2 и затем окисляя как можно более полно все потенциальные загрязняющие вещества. Кроме того, способ приводит к повышенному количеству получаемой на выброс диоксида углерода энергии, высвобождаемой для повышения эффективности. В то время как успехи в этой области привели к повышению эффективности сжигания, в области извлечения тепла имеется мало достижений.
Попытки секвестра углерода (в исходной форме газообразного CO2) привели к разработке многих различных способов, которые можно в целом классифицировать в качестве геологических, земных или океанических систем. Эти способы в основном связаны с перемещением образовавшегося диоксида углерода в реально существующие места и закачиванием диоксида углерода в геологические, подземные или океанические хранилища. Каждый из этих способов удаления требует больших затрат на приготовление CO2 для транспортировки осуществление транспортировки, и осуществление закачки в "хранилище углерода". По существу, эти способы экономически не обоснованы и во многих случаях потребляют больше энергии, чем производит исходный углерод.
Удаление может быть также осуществлено различными промышленными способами, которые включают скрубберную очистку, мембраны, дешевый O2 и гидраты. Однако недостатками каждой из этих технологий являются большие капиталовложения, возрастающие до нерентабельных уровней, и чрезвычайно высокое влияние удаления CO2 на стоимость электричества.
Нет оснований полагать, что выше перечислены все недостатки, скорее они являются одними из многих, которые могут уменьшать эффективность ранее известных способов удаления диоксида углерода из потоков отходов; однако упомянутые здесь недостатки в достаточной мере демонстрируют то, что все известные в технике подходы не являются удовлетворительными и что существует большая потребность в способах, раскрытых и заявленных в этом описании.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение предлагает способы и установки для удаления диоксида углерода из потоков отходов, которые решают проблемы, описанные выше. В целом, изобретение относится к способам удаления диоксида углерода из газового потока путем использования гидроксидного соединения с образованием карбоната и/или бикарбоната. Карбонат и/или бикарбонат могут затем быть использованы в любых различных вариантах или просто сброшены.
Различные варианты осуществления настоящего изобретения обеспечивают преимущества по сравнению с известными в настоящее время технологиями удаления углекислого газа из потоков отходов. Несколькими потенциальными преимуществами, которые достигаются в соответствии с изобретением, являются следующие.
В отличие от процессов, которые чисто физически удаляют углерод в отдаленное место, совместное получение в промышленном масштабе карбонатов натрия и/или бикарбонатов синтезом из хлорида натрия и диоксида углерода превращает нежелательный углекислый газ в химические продукты непосредственно на месте производства энергии, потенциально исключая затраты на транспортировку к месту извлечения.
В отличие от других способов декарбонизации потоков топочных газов, которые не поддаются модернизации, варианты осуществления настоящего изобретения могут быть применены для модернизации существующих энергетических установок, при значительном снижении капиталовложений, необходимых для осуществления способа декарбонизации. Кроме того, способ декарбонизации является масштабируемым и может быть осуществлен в масштабе: пилотная установка - полупромышленная установка - промышленная установка за счет постепенного увеличения количества реакторов.
В отличие от других известных в технике способов, способ декарбонизации по определенным вариантам осуществлений позволяет извлекать диоксид углерода в виде экономически полезных химических продуктов и при этом производить полезные побочные продукты, такие как газообразный хлор, карбонат натрия и газообразный водород. Поскольку побочные продукты процесса декарбонизации являются востребованными с экономической точки зрения, их стоимость возмещают затраты на извлечение и в разработанных должным образом системах делают способ секвестра углерода потенциально выгодным сам по себе.
Благодаря соответствующему способу активной скрубберной очистки выпускаемых топочных газов другие нежелательные загрязняющие вещества кислого характера, такие как SOx, NOx, HgOx и другие, активно извлекаются в процессе. Кроме того, способ скрубберной очистки может приводить к улавливанию и/или уносу других компонентов газового потока и/или загрязняющих примесей в карбонат натрия (например, угольной золы, и т.д.), удаляя их таким образом из газового потока.
Конкретные варианты осуществления настоящего изобретения включают способ удаления диоксида углерода из газового потока, включающий: получение гидроксида в водной смеси; смешивание гидроксида с газовым потоком с получением карбонатных продуктов (определяемых как продукты, содержащие карбонатную группу, CO3), бикарбонататных продуктов (определяемых как продукты, содержащие бикарбонатную группу, HCO3), или смесь карбонатных и бикарбонатных продуктов в смеси; и выделение указанных карбонатных и/или бикарбонатных продуктов из смеси, тем самым, удаляя диоксид углерода из газового потока. Гидроксидом может быть любая форма гидроксида, включая, но этим не ограничивая, гидроксид натрия, гидроксид калия, гидроксид кальция, гидроксид магния, и гидроксид алюминия. Специалисты в этой области понимают, что можно осуществить аналогичное химическое взаимодействие и декарбонизацию с любым числом гидроксидов или смесей гидроксидов. В ряде предпочтительных вариантов осуществления, гидроксидом является гидроксид натрия.
В конкретных вариантах осуществления, способ дополнительно включает процесс регулирования способа с целью получения в основном только карбонатных продуктов, или в основном только бикарбонатных продуктов. В ряде вариантов осуществления, способ дополнительно включает процесс регулирования способа с целью получения смеси карбонатных и бикарбонатных продуктов, смесь которых может состоять приблизительно из X% карбоната и Y% бикарбоната, причем комбинации X-Y могут быть любыми из следующих: 1-99, 2-98, 3-97, 4-96, 5-95, 6-94, 7-93, 8-92, 9-91, 10-90, 15-85, 20-80, 25-75, 30-70, 35-65, 40-60, 45-55, 50-50, 55-45, 60-40, 65-35, 70-30, 75-25, 80-20, 85-15, 90-10, 91-9, 92-8, 93-7, 94-6, 95-5, 96-4, 97-3, 98-2 или 99-1.
В определенных вариантах осуществления, смешение происходит в двух отдельных камерах, причем одну камеру используют для получения карбонатных продуктов, а другую камеру используют для получения бикарбонатных продуктов. В других вариантах осуществления, смешение происходит в барботажной колонне или серии барботажных колонн. В еще одних вариантах осуществления, выделение карбонатных и/или бикарбонатных продуктов из смеси включает способ выделения в результате горячего осаждения. В ряде вариантов осуществления, тепло для способа выделения получают в результате теплообмена с поступающими топочными газами. При выделении отделяемый карбонат может быть в виде водной суспензии или в виде раствора гидроксида, карбоната и воды при различных концентрациях, и в этом виде он может затем быть высушен любым из многочисленных методов. В ряде вариантов осуществления, карбонат можно не сушить. Например, суспензия карбоната натрия может быть использована для обработки жесткой воды. Несомненно, что специалистам в этой области известны многочисленные варианты применения карбоната, полученного по способу изобретения, например смеси суспензий бикарбоната натрия и карбоната натрия могут быть суспендированы в автоцистерне для использования в различных формах производства моющего средства, при производстве стекла в качестве флюса, и т.д., а также для упомянутого выше использования в процессе водоподготовки.
В конкретных вариантах осуществления, способ дополнительно включает транспортировку карбонатных продуктов к отдаленному месту захоронения, объединение карбонатных продуктов с кислотой в реакции нейтрализации с получением чистого диоксида углерода и закачивание диоксида углерода в хранилище углерода. В других вариантах осуществления, в способе получения карбоната нейтрализуют и/или уносят/захватывают другие компоненты газового потока, включая SOx, NOx и ртутьсодержащий материал
В некоторых вариантах осуществления, получение гидроксида включает получение соли; смешивание соли с водой, паром или с обоими с получением раствора; и электролиз раствора с получением гидроксида. В конкретных вариантах осуществления, раствор подвергают электролизу при напряжении, большем или равном 5 В, в то время как в других вариантах осуществления раствор подвергают электролизу при напряжении, меньшем чем 5 В. В ряде вариантов осуществления, раствор подвергают электролизу при напряжении от 1 В до 5 В, включая 1,5 В, 2,0 В, 2,5 В, 3,0 В, 3,5 В, 4,0 В или 4,5 В, или в любом интервале между любыми из этих точек.
В определенных вариантах осуществления, кислоту добавляют к раствору прежде чем его подвергают электролизу. Кислота может быть любой кислотой, которая может обеспечить протонирование раствора, включая, но этим не ограничивая, соляную кислоту. Для специалистов в этой области очевидно, что можно осуществить аналогичное химическое превращение и электролиз с любым числом кислот или смесей кислот. В ряде предпочтительных вариантов осуществления, кислотой является соляная кислота. В других вариантах осуществления, количество кислоты, которое добавляют к раствору, основывается на определении оптимальной степени протонирования, при которой затрачивается самая низкая энергия при получении реагентов и извлекается самая высокая энергия из продуктов.
В еще одних вариантах осуществления, стадию электролиза проводят в электролизере, имеющем пространство католита и пространство анолита, и карбонатные и/или бикарбонатные продукты возвращают в католитное пространство электролизера. В других вариантах осуществления, энергия, необходимая для этого способа, дополняется за счет отходящего тепла газового потока.
К другим вариантам осуществления изобретения относится способ удаления диоксида углерода из газового потока, включающий получение гидроксида натрия в водной смеси; смешение гидроксида натрия с газовым потоком с получением карбоната натрия, бикарбоната натрия или смеси карбоната натрия и бикарбоната натрия; и выделение указанного карбоната натрия и/или бикарбоната натрия из смеси, удаляя таким образом диоксид углерода из газового потока
В ряде вариантов осуществления, способ дополнительно включает процесс регулирования способа с целью получения в основном только карбоната натрия или в основном только бикарбоната натрия. В других вариантах осуществления, способ дополнительно включает процесс регулирования способа с целью получения смеси карбоната натрия и бикарбоната натрия, которая может состоять из X% карбоната натрия и Y% бикарбоната натрия, причем комбинации X-Y могут быть любыми их следующих: 1-99, 2-98, 3-97, 4-96, 5-95, 6-94, 7-93, 8-92, 9-91, 10-90, 15-85, 20-80, 25-75, 30-70, 35-65, 40-60, 45-55, 50-50, 55-45, 60-40, 65-35, 70-30, 75-25, 80-20, 85-15, 90-10, 91-9, 92-8, 93-7, 94-6, 95-5, 96-4, 97-3, 98-2 или 99-1.
В конкретных вариантах осуществления, смешивание происходит в двух отдельных камерах, причем одну камеру используют для получения карбоната натрия, а другую камеру используют для получения бикарбоната натрия. В других вариантах осуществления, смешивание происходит в барботажной колонне или в серии барботажных колонн. В еще одних вариантах осуществления, выделение карбоната натрия и/или бикарбоната натрия из смеси включает способ выделения путем горячего осаждения. В ряде вариантов осуществления, тепло для способа выделения получают путем теплообмена с поступающими топочными газами.
В конкретных вариантах осуществления, способ дополнительно включает транспортировку карбоната натрия к отдаленному месту захоронения, объединение карбонатных продуктов с кислотой в реакции нейтрализации с получением чистого диоксида углерода и закачивание диоксида углерода в хранилище углерода.
В некоторых вариантах осуществления, получение гидроксида натрия включает получение хлорида натрия; смешивание хлорида натрия с водой, паром или с обоими, с получением рассола; и электролиз рассола с получением гидроксида натрия и газообразного хлора. В конкретных вариантах осуществления, рассол подвергается электролизу при напряжении, большем чем или равным приблизительно 5 В, в то время как в других вариантах осуществления, электролиз проводят при напряжении, меньшем чем 5 В. В некоторых вариантах осуществления, раствор подвергают электролизу при напряжении от 1 В до 5 В, включая 1,5 В, 2,0 В, 2,5 В, 3,0 В, 3,5 В, 4,0 В, или 4,5 В, или в любом интервале между любыми из этих точек.
В некоторых вариантах осуществления, перед электролизом в рассол добавляют кислоту. Кислотой может быть любая кислота, которая может обеспечить протонирование раствора, включая, но этим не ограничивая, соляную кислоту. Для специалистов в этой области очевидно, что можно обеспечить аналогичное химическое взаимодействие и электролиз с любым числом кислот или смесей кислот. В некоторых предпочтительных вариантах осуществления, кислотой является соляная кислота. В еще одних вариантах осуществления, количество добавляемой к рассолу кислоты основано на оптимальной степени протонирования, при которой затрачивается самая низкая энергия при получении реагентов и извлекается самая высокая энергия из продуктов.
В некоторых вариантах осуществления, стадия электролиза происходит в электролизе, имеющем пространство католита и пространство анолита, и карбонат натрия, и/или бикарбонат натрия рециркулирует в пространство католита электролизера. В других вариантах осуществления, энергию, необходимую для реализации способа, добавляют за счет отходящего тепла, извлекаемого из газового потока. В еще одних вариантах осуществления, способ дополнительно включает сбор газообразного хлора, в то время как в других вариантах осуществления получают газообразный водород. В некоторых вариантах осуществления, газообразный водород и газообразный хлор подвергают взаимодействию с получением хлористоводородной кислоты, которую добавляют в рассол перед электролизом. В других вариантах осуществления, газообразный водород сжигают с атмосферным кислородом или кислородом со склада химических продуктов с получением воды, в то время как в других вариантах осуществления, способы включают использование газообразного водорода для получения энергии. В некоторых вариантах осуществления, выделение карбоната натрия и/или бикарбоната натрия из смеси включает способ выделения путем горячего осаждения, в котором тепло для способа выделения получают из энергии, произведенной газообразным водородом. В других вариантах осуществления, газообразный водород сжигают вместе с углем, чтобы улучшить выбросы в результате сжигания угля, или его используют для сжигания в топливном элементе при получении постоянного электрического тока.
В некоторых вариантах осуществления, газовый поток является потоком выхлопных газов установки, в то время как в других вариантах осуществления, установкой является энергетическая установка, которая использует в качестве источника топлива уголь. В некоторых вариантах осуществления, поток выхлопных газов включает CO2 и H2O.
К конкретным вариантам осуществления настоящего изобретения также относится установка, включающая при использовании камеру электролиза, включающую, по меньшей мере, один катод и, по меньшей мере, один анод, камеру для получения гидроксида; смесительное оборудование, операционно связанное с камерой электролиза, и трубопровод для газового потока, смесительное оборудование для смешивания гидроксида из камеры электролиза с газовым потоком, для получения смеси, в которой соединения углерода, серы, и/или азота в газовом потоке могут реагировать с гидроксидом; и камеру выделения, операционно связанную со смесительным оборудованием и приспособленную для выделения смеси на отдельные газовую фазу и твердую и/или жидкую фазу.
В некоторых вариантах осуществления, камера электролиза включает мембранный электролизер, диафрагменный электролизер и/или электролизер с ртутным катодом. В конкретных вариантах осуществления, смесительным оборудованием является периодический реактор или серия периодических реакторов, в то время как в других вариантах осуществления, камера смешения является аппаратом для абсорбции газа жидкостью с протеканием химической реакции или серией таких аппаратов. В других вариантах осуществления, камера смешения является аппаратом для кристаллизации или серией аппаратов для кристаллизации, в то время как в других вариантах осуществления она является барботажной колонной или серией барботажных колонн.
В конкретных вариантах осуществления, установка дополнительно включает сушильную камеру, операционно связанную с камерой выделения, приспособленную при использовании для удаления жидкости из твердой и/или жидкой фазы, в то время как в других вариантах осуществления, сушильная камера при использовании приспособлена для нагрева твердой и/или жидкой фазы. В еще одних вариантах осуществления, установку дополнительно определяют как операционно связанную с энергетической установкой.
В некоторых вариантах осуществления, камера электролиза при использовании приспособлена для получения газообразного хлора и гидроксида натрия из хлорида натрия и воды. В других вариантах осуществления, смесительное оборудование при использовании приспособлено для смешения гидроксида из камеры электролиза с диоксидом углерода из газового потока для получения карбонатных и/или бикарбонатных продуктов.
В еще одних вариантах осуществления, настоящее изобретение включает способ определения оптимального рабочего напряжения и величины электрического тока электролизера при его низковольтной эксплуатации относительно области повышенных значений для данной характеристики V/I при данной степени протонировании. В других вариантах осуществления, изобретение включает способ определения нижнего термодинамического предела для рабочего напряжения для данного электролизера, используемого в способе. В конкретных вариантах осуществления, предлагается способ определения экологической эффективности (∂CO2/∂E) в целом для устройств, которые осуществляют удаление CO2 из потоков отходов, в то время как другие варианты осуществления включают способ определения экологической эффективности (∂CO2/∂E) конкретно для устройств, которые используются в настоящем изобретении в любом из его вариантов осуществления. Другие варианты осуществления включают способ получения чрезвычайно чистого газообразного водорода при низком значении цены безразличия, его стоимости, равной содержанию извлекаемой энергии.
Термины "включает" (в любой форме), "имеет" (в любой форме), "содержит" (в любой форме) и "заключает" (в любой форме) являются не ограничивающими глаголами-связками. В результате, способ или установка, которые "включают", "имеют", "содержат" или "заключают" одну или более стадий, или элементы, обладают этими одной или более стадией или элементами, но не ограничены обладанием только этими одной или более стадией или элементами. Аналогично, элемент устройства или способа, который "включает", "имеет", "содержит" или "заключает" одну или более характерных черт, обладает этой одной или более характерных черт, но не ограничен обладанием только этой одной или более характерных черт. Термин "использование" следует интерпретировать таким же образом. Поэтому, например, стадия способа, которая включает "использование" конкретной информации, означает, что, по меньшей мере, используется изложенная информация, но не исключается возможность использования также другой, не приведенной информации. Кроме того, структура, которая формируется некоторым способом, должна формироваться, по меньшей мере, этим способом, но также может формироваться способом или способами, которые не указаны.
Неопределенный артикль относится к одному или более чем к одному предмету, если в описании изобретения ясно не указано иначе. Термин "другой" означает, по меньшей мере, второй или более. Термины "в основном" и "около" означают, по меньшей мере, величину, близкую к данному значению (и включающее его) или состоянию (предпочтительно в пределах 10%, более предпочтительно в пределах 1%, и наиболее предпочтительно в пределах 0,1%).
Используемые здесь термины "карбонаты" или "карбонатные продукты" в целом относятся к минеральным компонентам, содержащим карбонатную группу, CO3. Поэтому термины охватывают как смеси карбонат/бикарбонат, так и соединения, содержащие исключительно ион карбоната. Термины "бикарбонаты" и "бикарбонатные продукты" в целом относятся к минеральным компонентам, содержащим бикарбонатную группу HCO3. Поэтому термины охватывают как смеси карбонат/бикарбонат, так и соединения, содержащие исключительно ион бикарбоната.
При образовании бикарбонатов и карбонатов в некоторых вариантах осуществления настоящего изобретения, термин "ионное отношение" обозначает отношение ионов натрия в продукте к присутствующему в этом продукте числу атомов углерода. Следовательно, может быть указано, что поток продукта, сформированный из чистого бикарбоната (NaHCO3), имеет "ионное отношение", равное 1,0 (Na/C), но может быть указано, что поток продукта, сформированный из чистого карбоната (Na2CO3), имеет "ионное отношение" 2,0 (Na/C). С целью расширения диапазона может быть указано, что бесконечное число непрерывных смесей карбоната и бикарбоната имеют ионные отношения в интервале от 1,0 до 2,0.
В некоторых предпочтительных вариантах осуществления изобретения, хлористоводородную кислоту добавляют к подаваемому рассолу хлорида натрия в электролизер, применяемый для производства хлора и гидроксида натрия, вызывая протекание следующей реакции:
H2O+NaCl+aHCl+энергия→NaOH+(1/2+a/2)H2+(1/2+a/2)Cl2
В этом уравнении символ "a" обозначает "степень протонирования", и он является отношением протонов (ионы H+) к ионам натрия (ионы Na+).
Используемый здесь термин "секвестр" в целом обозначает способы или применения, которые частично или полностью удаляют CO2 из выбросов точечных источников и позволяют хранить этот CO2 в некоторой форме с тем, чтобы предотвратить его возврат в атмосферу. Применение этого термина не исключает рассмотрение какой-либо формы описываемых вариантов осуществления в качестве способов "секвестра".
Используемый здесь термин "экологическая эффективность" применяют в качестве синонима термина "термодинамическая эффективность" и он обозначает количество CO2, подвергнутое секвестру в конкретном варианте осуществления настоящего изобретения на затраченную энергию (представленный уравнением "∂CO2/∂E"). Секвестр CO2 выражают в процентах от суммарного количества CO2 установки; энергопотребление также выражают от суммарного энергопотребления установки.
Используемые здесь термины "низковольтный электролиз" и "НВЭ" обозначают электролиз при напряжениях ниже 5 В.
Описания известных способов переработки, компонентов и оборудования опущены для того чтобы излишне не затенять настоящие способы и устройства излишними деталями. Описания настоящих способов и устройств, включая их описания в приложениях, являются иллюстративными примерами и не ограничивают изобретение. Для специалистов в этой области на основе этого описания изобретения могут быть очевидными некоторые замены, модификации, дополнения и/или перестановки, подпадающие под объем патентной формулы, но не перечисленные в явном виде в этом описании.
Другие характерные черты и связанные с ними преимущества станут очевидными в результате ознакомления со следующим подробным описанием конкретных вариантов осуществления в сочетании с сопровождающими чертежами.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Следующие чертежи являются иллюстративными примерами и не являются ограничениями. Чертежи являются частью настоящего описания и они включены для дополнительной демонстрации некоторых аспектов настоящего изобретения. Изобретение может стать более понятным в результате ссылок на один или более из этих чертежей в сочетании с описанием представленных здесь иллюстративных вариантов осуществлений:
На фиг.1 представлена принципиальная технологическая схема, иллюстрирующая конкретные варианты осуществления настоящего изобретения.
На фиг.2A показана установка для иллюстрации основных характерных черт одного варианта осуществления части декарбонизации настоящего изобретения.
На фиг.2B представлены экспериментальные результаты по абсорбции/конверсии.
На фиг.2C приведены экспериментальные результаты по абсорбции/конверсии.
На фиг.2D представлена графическая зависимость, показывающая расстояние при контактировании газ/жидкость (м, глубина жидкости), необходимое для удаления 90% CO2.
На фиг.2E приведена графическая зависимость ионного отношения в продукте от процента CO2, абсорбированного в испытуемом реакторе.
На фиг.3 представлена графическая зависимость температурного режима жидкости в камере реактора в зависимости от указанного времени протекания реакции.
На фиг.4 приведена диаграмма, иллюстрирующая исследование захлебывания колонны 5'.
На фиг.5 представлены типичные рабочие кривые вольт-амперных характеристик для различных pH анолита и температур.
На фиг.6 приведена блок-схема системы, включающей реактор, в котором в соответствии с вариантами осуществления настоящего изобретения водород не извлекают.
На фиг.7 представлена блок-схема системы, включающей реактор, в котором в соответствии с вариантами осуществления настоящего изобретения водород извлекают путем рецикла в топливный элемент для получения постоянного тока.
На фиг.8 приведена графическая зависимость процента абсорбции CO2 в барботажной колонне в зависимости от глубины жидкости и поверхностной скорости газа при низких поверхностных скоростях.
На фиг.9A представлена диаграмма, показывающая максимальную теоретическую абсорбцию CO2 и экспериментальные результаты согласно вариантам осуществления настоящего изобретения.
На фиг.9B приведены ориентировочные расчеты и вычисления для модели топочного газа для установки, включающей конкретные варианты осуществления настоящего изобретения.
На фиг.9C представлена технологическая загрузка декарбонизатора и промежуточная потребность в гидроксиде натрия для установки, включающей конкретные варианты осуществления настоящего изобретения.
На фиг.9D приведена загрузка секции электролиза и расходы для установки, включающей конкретные варианты осуществления настоящего изобретения.
На фиг.9E представлены расчеты отходящего тепла для установки, включающей конкретные варианты осуществления настоящего изобретения.
На фиг.9F приведены вычисления энергетического баланса и экологической эффективности для установки, включающей конкретные варианты осуществления настоящего изобретения.
На фиг.10 представлена экологическая эффективность различных моделируемых энергетических установок, включающих конкретные варианты осуществления настоящего изобретения.
На фиг.11 приведен график, показывающий процент мощности, сэкономленный на 1 м2 площади для установки с нормализованным НВЭ.
ОПИСАНИЕ ИЛЛЮСТРАТИВНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Настоящее изобретение относится к способам секвестра углерода, в которых диоксид углерода удаляют из потоков отходов и превращают в карбонатные и/или бикарбонатные продукты. Варианты осуществления способов и установок изобретения включают один или более из следующих общих компонентов: (1) процесс водной декарбонизации, в котором газообразный CO2 абсорбируют водной каустической смесью и затем подвергают взаимодействию с гидроксидом с образованием карбонатных и/или бикарбонатных продуктов; (2) процесс выделения, в котором карбонатные и/или бикарбонатные продукты отделяют из жидкой смеси; (3) процесс электролиза рассола для получения гидроксида натрия, который используют в качестве жидкого абсорбента в процессе декарбонизации; и (4) получение и использование побочных продуктов процессов декарбонизации и электролиза, включая газообразный хлор, карбонат и бикарбонат натрия, и газообразный водород. Каждый из этих общих компонентов объясняется более подробно ниже.
I. Обзор преимуществ
Подобно любому другому способу или установке, которые позволяют достигать поставленной цели, многие варианты осуществления настоящего изобретения потребляют энергию для осуществления абсорбции CO2 и других химических продуктов из потоков топочных газов и достижения описанных здесь других целей вариантов осуществления настоящего изобретения. Однако одним преимуществом конкретных вариантов осуществления настоящего изобретения является то, что они обеспечивают экологическую эффективность, которая превосходит уже известную в технике, как это подробно объяснено в примерах 5 и 6. Как очевидно из данных примеров 5 и 6, дополнительная утилизация отходящего тепла или получение энергии для энергоснабжения способа без проявления парникового эффекта, использование распределенного низковольтного электролиза и повышение отдачи электрической энергии при извлечении энергии водорода, могут дополнительно повышать экологическую эффективность способа, вплоть до значения или выше его, при котором способ полностью обеспечивается энергией за счет утилизации отходящего тепла (и извлечения энергии водорода), и обеспечивают абсорбцию фактически 100% выбрасываемого энергетической установкой CO2.
Кроме того, одно преимущество использования химизма конечного взаимодействия в конкретных вариантах осуществления настоящего изобретения, такое как абсорбция слабокислого CO2, заключается в том, что в способе фактически полностью абсорбируются сильные кислоты, SOх и NOx, и, в меньшей степени, ртуть. Исследования с использованием загрузки SOх/Ar и NOx/Ar в одноступенчатые декарбонизаторы продемонстрировали 99%+ удаление этих компонентов топочного газа ("99%+" означает, что присутствие каждого загрязняющего вещества в случае обработки отходящего газа при скорости 14 л/мин не обнаруживали в конечном воздушном потоке методом газовой хроматографии, то есть они эффективно удалялись). В конкретных вариантах осуществления настоящего изобретения, может иметь большее экономическое значение сопутствующая скрубберная очистка от соединений NOx, SOx, и ртути; то есть в результате использования вариантов осуществления настоящего изобретения в энергетической установке могут сжигаться угли, которые содержат большие количества этих соединений, в некоторых вариантах осуществления с меньшим загрязняющим эффектом, чем в случае высокосортных углей, сжигаемых без использования преимущества способа абсорбции CO2 конкретных вариантов осуществлений настоящего изобретения.
Кроме того, масштабируемость конкретных вариантов осуществлений настоящего изобретения может достигать чрезвычайно больших размеров; то есть, так как в конкретных вариантах осуществлений, в способе регулируется расход электроэнергии, то расход электроэнергии может быть фактически соизмерим с молекулой конкретного абсорбента, получаемого в любой данный момент времени. Кроме того, можно на практике легко определить точное количество абсорбированного CO2: взвесьте образовавшиеся карбонатные/бикарбонатные продукты, определите их ионное отношение с помощью анализа, проведите вычисление для определения количества молей абсорбированного CO2, и в результате легко определяется и подтверждается количество абсорбированного CO2 (фактор, который может иметь дополнительное преимущество для интенсификации режимов удаления CO2 и других химических веществ из топочного газа).
Другое дополнительное преимущество конкретных вариантов осуществления настоящего изобретения, которое отличает их от других способов удаления CO2, заключается в том, что при некоторых конъюнктурах рынка, стоимость продуктов будет значительно превышать стоимость затраченных реагентов, или стоимость затраченной электроэнергии или амортизационные расходы на установку. Другими словами, конкретные варианты осуществления являются промышленными способами рентабельного получения хлора, водорода и карбонатных продуктов, при удалении значительного количества CO2 и сопутствующих загрязняющих веществ. Реализация всех других конкурирующих способов связана просто с дополнительными эксплуатационными затратами.
II. Принципиальная технологическая схема
На фиг.1 изображена упрощенная принципиальная технологическая схема, иллюстрирующая примеры главных вариантов осуществления установок и способов настоящего описания. Эта схема предлагается только для иллюстративных целей и поэтому она только изображает конкретные варианты осуществления настоящего изобретения и ни коим образом не ограничивает объем формулы изобретения. Как показано на фиг.1, топочный газ (ТГ) поступает в процесс в точке 901, обычно, после того как он передает отходящее тепло системе, генерирующей из отходящего тепла постоянный электрический ток (ПТ). ТГ, вводимый в этом примере в качестве смеси газов с температурой 300°C, сначала подают по трубе 902 в теплообменник ТГ/бикарбонат 903, в котором температура ТГ уменьшается в этом примере до 120-140°C. Аналогично, ТН проходит через теплообменник анолит/ТГ 904 и теплообменник католита/ТГ 905, с понижением его температуры до 95°C, и затем через теплообменник вода/FG 929, с понижением его температуры дополнительно до 30°C. ТГ, выходящий из теплообменника вода/ТГ 929, затем вводят в систему клапанов, систему корректировки температуры смеси топочного газа 931, в которой ТГ с температурой 30°C может быть смешен с топочным газом с температурой 120-140°C, подаваемым также в систему корректировки температуры смеси топочного газа 931 посредством трубы обработки горячего топочного газа 906. ТГ смеси с температурой 30-140°C могут затем быть дифференциально введены в нижнюю часть абсорбционной колонны карбонизации 907, которая может представлять собой насадочную или безнасадочную барботажную колонну, в которой газ вдувают или барботируют, в результате чего газ образует пузырьки, которые поднимаются вверх через жидкость, собираясь в верхнем отводном отверстии 908. В этом варианте осуществления, частично или полностью декарбонизированный газ затем вводят и пропускают через колонну конверсии в бикарбонат 909, барботируют через жидкость в этой колонне, извлекают далее с помощью вентилятора и подают в отводное отверстие 910.
Поток, используемый в теплообменнике ТГ/бикарбонат 903, является бикарбонатом/карбонатом натрия и сульфатом, нитратом, ртутью и частицами и аэрозолями, абсорбированными из топочного газа в колоннах абсорбции/конверсии (907 и 909). За счет его контактирования с входящим ТГ с температурой 300°C этот жидкий поток нагревается до температур, достаточных для выработки водяного пара со значительным давлением, производя пар, когда поток вводят в резервуар 911, который затем конденсируют в конденсаторе 912, с получением дистиллированной воды, которую рециркулируют в резервуар регенерированной H2O 913, которую далее используют, после любой необходимой обработки, для получения рассола в смесителе рассола 914. Поток, используемый в теплообменнике анолит/ТГ 904, является рассолом, полученным при добавлении солей группы-1 и группы-2 (в этом примере NaCl) к воде, подаваемой или из подачи воды из водопроводной магистрали 915, или частично или полностью подаваемой из резервуара регенерированной H2O 913. Этот раствор протонируют (подкисляют) путем добавления HCl в виде газообразного HCl, абсорбируемого водой или из HCl со склада, которое регулируют с помощью регулятора pH с обратной связью 916. Этот поток циркулирует через зону анолита 917 электролизера 933. Аналогично, поток, используемый в теплообменнике католит/ТГ 905, является NaOH (водным), который циркулирует через зону католита 918 электролизера 933. Когда pH католита превышает минимальное значение pH (характеризующее концентрацию) в точке измерения 919, концентрированный NaOH подают в резервуар для хранения гидроксида 920.
Поток, используемый в теплообменнике вода/ТГ 929, идет из достаточно большого резервуара воды при достаточно низкой температуре для осуществления теплообмена. В некоторых вариантах осуществления, эта система теплообмена может быть использована в качестве "предварительного подогрева" растворов бикарбонат/карбонат перед дальнейшим теплообменом в теплообменнике топочный газ/бикарбонат 905. Кроме того, в некоторых вариантах осуществлений, могут быть частично или полностью объединены закачка в резервуар воды из водопроводной магистрали 915, резервуар для хранения H2O HX 937 и резервуар регенерированной H2O 913.
Протонированный рассол, циркулирующий через зону анолита 917 электролизера 933, подвергают электролизу с образованием газообразного хлора, который собирают и перемещают по линии газообразного хлора 921, в этом примере, в реактор гипохлорита натрия 924. Ионы натрия и ионы водорода (протоны) переносятся через мембрану электролизера 933 в зону католита 918. Там ионы натрия заменяют ионы водорода в воде, что приводит к образованию газообразного водорода, который отводят через магистраль введения чистого газообразного водорода 922 в топливный элемент H2/O2 923, где его сжигают в атмосферном O2 с получением постоянного электрического тока ПТ, который подают в этом примере к электролизеру 933, и чистой воды, которую рециркулируют через замкнутый цикл извлечения чистой воды 935 в резервуар регенерированной H2O 913. Газообразный хлор, подаваемый в реактор гипохлорита натрия 924, контактируют (барботируют) через гидроксид натрия, подаваемый в реактор из резервуара хранения гидроксида 920. В результате образуется гипохлорит натрия и его складируют для продажи или дальнейшего использования в качестве исходного сырья. Некоторое количество образовавшихся газообразного хлора и HCl (используя сверх стехиометрическое количество, a, будет создавать непрерывный рецикл HCl, исключая возмещение потерь) здесь сжигают с получением HCl в топливном элементе 925, который затем рециркулируют по линии возврата кислого газообразного HCl 926 в смеситель рассола 914.
Произведенный или хранимый гидроксид, или полученный из исходных химических веществ и загруженный в резервуар хранения гидроксида 920 используется в качестве потока абсорбента, вводимого в колонну карбонизации/абсорбции 907. Затем его пропускают через колонну бикарбонизации/конверсии 909 и затем направляют (в виде смеси бикарбонат/карбонат в воде) в теплообменник ТГ/бикарбонат 903. После удаления воды путем испарения продукт в виде суспензии концентрированных бикарбоната/карбоната направляют в резервуар продуктового бикарбоната 927, где он может быть осушен для дальнейшей обработки или очистки, или он может быть направлен для захоронения или на продажу.
Каждый из вышеописанных и приведенных на фиг.1 общих компонентов установок и способов настоящего описания описан более подробно ниже.
III. Водная декарбонизация (абсорбция) CO2 из потоков отходов и его конверсия в карбонат и бикарбонат
Как отмечено выше, в конкретных вариантах осуществления, в установках и способах настоящего описания используется процесс водной декарбонизации, в результате которого газообразный CO2 абсорбируют водной смесью гидроксида натрия, и затем он взаимодействует с гидроксидом с образованием карбонатного и бикарбонатного продуктов. Во многих вариантах осуществления настоящего изобретения, в отличие от других схем захвата/секвестра углерода, гидроксид натрия используют в качестве основного абсорбента. Гидроксид натрия в различных концентрациях известен в качестве легкодоступного абсорбента CO2. При контактировании диоксида углерода с водным гидроксидом натрия могут образовываться непрерывный ряд продуктов, от чистого бикарбоната натрия (NaHCO3) до чистого карбоната натрия (Na2CO3), и могут быть созданы различные условия для сдвига равновесия в любом направлении, даже полностью (или почти полностью), и для осаждения бикарбоната, карбоната или смешанного осадка, содержащего оба соединения, при достаточной концентрации (или в результате химической обработки или удалением воды различными средствами).
Когда диоксид углерода контактируют с водным гидроксидом натрия, поток в пределах реакционной камеры соответствует поведению, показанному на фиг.3, по мере протекания реакции в течение обозначенного времени. Две стадии резкого роста температуры соответствуют и определяют два различных режима реакции:
(1) Первичная стадия абсорбции, на которой CO2 легко абсорбируется. Абсорбционная способность потока уменьшается по мере снижения концентрации ОН, и абсорбция прекращается, а в некоторых случаях начинается и десорбция, когда содержание ОН полностью исчерпывается. В течение этой стадии реакция является экзотермической и образуется почти исключительно один карбонат.
(2) Вторичная стадия конверсии, на которой CO2 абсорбируется с трудом. Проход топочного газа через смесь не приводит ни к какой-либо существенной абсорбции CO2 потоком, но поток значительно охлаждается в результате потери тепла испарения из-за испарения воды, любой потери CO2 в паровом состоянии, и протекания любых эндотермических реакций. В течение этой стадии, уже образовавшийся в растворе карбонат натрия превращается в бикарбонат натрия, в соответствии с суммарной стехиометрии реакции:
Na2CO3(вод)+H2О(ж)+CO2(вод)→2NaHCO3(вод)
Эта последовательность, сначала карбонизации, а затем бикарбонизации подтверждается при многократной работе установки, показанной на фиг.2A (как объяснено подробно в примере 3), для пределов и за пределами абсорбции для жидкости с различными концентрациями абсорбента.
Эти две стадии отличаются характеристиками, приведенными в таблице 1 ниже.
В вариантах осуществления настоящего изобретения может быть использована одна и та же камера для осуществления двух процессов in situ, но различная природа реакций предполагает, что выделение реакций на две камеры и раздельная их оптимизация являются соответствующим путем для предпочтительных вариантов осуществления. Независимо от "внутреннего расположения" устройств передачи (то есть степени периодичности или непрерывности, небольшого числа камер, емкостей, стадий, и т.д.), в этой последовательности происходят два фундаментальных процесса при мольных концентрациях, достаточных для обеспечения хорошей абсорбции.
Следовательно, так как в некоторых вариантах осуществления настоящих способов и установок могут быть реализованы процессы регулирования получения чистого и почти чистого бикарбоната натрия, то в некоторых вариантах осуществления настоящего изобретения, поэтому происходит абсорбция одного атома углерода одним атомом натрия, получаемого электролизом, вместо Ѕ атома углерода (повышение достигаемой экологической эффективности номинально в 2 раза по сравнению с получением карбоната). Таким образом, количество энергии для электролиза и переработки, затраченной на получение моля гидроксида, имеет в два раза большую "нормальную" абсорбционную способность в случае ее использовании для получения бикарбоната, по сравнению с эффективностью абсорбция/энергия в случае получения карбоната.
В различных вариантах осуществления настоящего изобретения, может быть получена вся область отношений концентраций бикарбонат/карбонат. В предпочтительных вариантах осуществления, можно регулировать концентрации, температуры, давления, объемные скорости и так далее, потоков для оптимизации доли абсорбированного "имеющегося" CO2, чтобы оптимизировать образование бикарбоната.
В нескольких вариантах осуществления изобретения, в качестве способа регулирования скорости абсорбции CO2 и других газов может применяться регулирование pH жидкого абсорбента (концентрации ионов OH). В некоторых предпочтительных вариантах осуществления, может быть использована повышенная концентрация солей/карбонатов для дополнительного направления реакции в сторону образования бикарбоната. Установление рыночных цен на продукты и экономические факторы могут обуславливать получение на установке продукта, обогащенного карбонатом, в течение одного периода времени, и получение продукта, обогащенного бикарбонатом, в течение другого периода времени, и так далее, со средним Na/C, при формировании его средней величины эффективного использования ионных соединений, созданных для абсорбции/конверсии.
В результате выделения двух процессов на две отдельные камеры и перемещения между камерами в момент истощения OH, становления и падения температуры, и ослабления абсорбции, может изменять способ проектирования и оптимизации установки декарбонизации. Для специалиста в этой области очевидно, что могут быть спроектированы периодический, псевдонепрерывный, непрерывный и так далее варианты этого простого двухстадийного процесса декарбонизации.
Кроме того, желая реализовать абсорбцию с наименьшей затратой энергии, во многих предпочтительных вариантах осуществления изобретения могут использоваться барботажные реакторные колонны (насадочные и безнасадочные, с горизонтальным и без горизонтального потока жидкости, с горизонтальным или без горизонтального потока жидкости), которые благодаря своей конструкции создают большую площадь контакта жидкость/газ для облегчения массообмена. Суммарными преимуществами такой конструкции является свобода использования ступеней с небольшой высотой (3 м или менее), при которых, тем не менее, достигается 90%+ абсорбция при небольшом сопротивлении или преодолении избыточного давлении при перекачивании потоков насосом. Поэтому их проектируют с широкой горизонтальной поверхностью для достижения промышленной производительности (широкие неглубокие динамические области или эквивалентные им реакторы), желательно с горизонтальным движением потоков для возможности их использования в непрерывном режиме. В некоторых вариантах осуществления изобретения могут использоваться газожидкостные контакторы многих других конфигураций, если эти устройства позволяют достигать требуемого контакта газ-жидкость.
На фиг.4 представлено исследование захлебывания колонны 5', в которой сопротивление составляет приблизительно 0,01 psig, плюс 1,52 psig избыточного давления для преодоления глубины жидкости 5'. Предполагается, что на эти потери и другие затраты на сжатие расходуется менее чем 1% энергии энергетической установки, и считается, что сами по себе они минимальны и их не вычисляют в примерах. На фиг.4 подтверждается, что чрезвычайно низкие сопротивления в потоке приводят к чрезвычайно экономичной компрессии в случае эффекта, при котором экологическая эффективность устройства не нарушается в результате избыточной энергии, расходуемой на компрессию или перемещение газов.
Экологическая эффективность вариантов осуществления настоящих способов и установок увеличивается за счет совершения наименьшего количества работы, позволяющей абсорбировать CO2, и одним фактором, который снижает эту эффективность, является степень сжатия, перекачка жидкости и воздуха, которое требуется для осуществления того способа. Для этого разработаны два абсорбера высокой эффективности (способные к удалению 99% CO2 от поступающего потока топочного газа, которым является 60% CO2 в N2) для работы с "короткими ступенями", в которых достигают высоких скоростей абсорбции CO2.
В предпочтительных вариантах осуществления изобретения используют большую площадь поверхности массообмена жидкость-газ (барботажная колонна, насадочная или без насадки, или эквивалентные реакторы с неподвижной или движущейся жидкостью), чтобы достигнуть высокой скорости абсорбции при небольшой высоте жидкого абсорбента, тем самым понижая сопротивление, необходимое для приведения в контакт потоков, и поэтому эта "конструкция с короткими ступенями" требует использования широких, коротких "динамических областей" или их эквивалентов в трубопроводе, углублениях, реакторах и т.д., для эффективной абсорбции больших количеств CO2.
В крупнотоннажной промышленности и всей относящейся к ней справочной литературе реакции декарбонизации настоящего описания обычно рассматриваются как лимитируемые за счет массообмена. На практике, используя насадочные или безнасадочные колоны для абсорбции при широкой площади поверхности контакта газ-жидкость в методах подымающегося пузырька через жидкость, реакция, по-видимому, имеет небольшие ограничения по массообмену, или, иначе говоря, использование настоящего метода проектирования барботажной колонны для контакта жидкость-газ, по-видимому, позволяет умело преодолевать лимитирующий массообмен: было продемонстрировано, что барботирование от нулевого уровня насадки через барботер с расстоянием контакта газ-жидкость только 30 см, обеспечивает мгновенные скорости при 98% + абсорбции CO2 (см. фиг.2B и 2C, обсуждаемые в примере 3), и в течение значимых для промышленности периодов времени, 15-25 минут, поток сохраняет способность к 80%+ абсорбции. Это вряд ли сильно лимитируется массообменом и практический эксперимент даже с простым исчезновением загрузки демонстрирует быстрый массобмен при этой хемосорбции.
Три примера конструкции абсорберов с высокой степенью абсорбции CO2/NaOH описываются подробно в примерах 1-3. Выводы, сделанные в примерах 1-3, говорят о том, что доказаны и продемонстрированы высокие скорости абсорбции с короткими ступенями NaOH, применимые для удаления в промышленном масштабе высокого содержания входящего CO2 при низком сопротивлении в реакторах с изготовляемыми производителями размерами.
Итак, конкретные варианты осуществления настоящего изобретения, касающиеся части способов и установок декарбонизации, включают один или более из следующих признаков:
(1) использование коротких ступеней для достижения высоких скоростей абсорбции CO2 на стадии карбонизации реакции;
(2) выделение и переработка карбонизированного потока в способе бикарбонизации путем непрерывного контакта с CO2-несущим технологическим газом (или другим CO2-несущим газом с концентрациями CO2 больше чем парциальное давление CO2-образующегося из потока абсорбента);
(3) владение последовательностью способа, который может использоваться путем текущего регулирования переменных состояния и концентрации для получения чистого бикарбоната чистого карбоната, и всех различных их смесей; и
(4) варианты осуществления изобретения могут быть столь же эффективны, как отношение 1:1 натрий/углерод при абсорбции; это оптимизирует абсорбированный CO2 на кВт·ч (вариант экологической эффективности, (∂CO2/∂E)), расходуемый при производстве реагента.
IV. Выделение продуктов
Как отмечено выше, в конкретных вариантах осуществления, в установках и способах настоящего описания используют способ выделения, с помощью которого карбонатный и бикарбонатный продукты отделяют из жидкого раствора. Выделение продуктов жидкого раствора требует соответствующего способа. Образование в жидкой фазе двууглекислого натрия (NaHCO3 или бикарбоната натрия) и карбоната натрия (Na2CO3 или кальцинированной соды) в равновесии с гидроксидом натрия (NaOH или каустической содой) происходит в широком диапазоне температур и давлений и обеспечивает различные конечные точки равновесия при различных парциальных давлениях CO2. Управляя концентрацией щелочи, температурой, давлением, размером реактора, глубиной жидкости и степенью насыщения диоксидом углерода, можно вызвать осаждение карбоната и бикарбоната. Альтернативно, в некоторых предпочтительных вариантах осуществления, продукты карбоната/бикарбоната могут быть отделены от воды путем теплообмена с поступающими топочными газами. Кроме того, из-за различий в произведениях растворимостей для карбоната натрия и бикарбоната натрия могут быть достигнуты конкретные неинтуитивные точки переработки; например, одной из особенностей равновесия карбонатов натрия в конкретных растворах каустической соды является то, что подвод тепла приводит к осаждению твердого вещества; также, при конкретных условиях было показано, что высокой (93%+) чистоты карбонаты самопроизвольно осаждаются из водного раствора.
Альтернативно, в конкретных вариантах осуществления, тепло для способа выделения может быть получено из водорода, произведенного путем электролиза или путем творческого подхода к использованию тепла топочных газов, содержавшегося в поступающем потоке топочного газа. Способ кристаллизации по своей сути позволяет очищать кристаллизующийся минерал путем известного способа очистки кристаллизацией.
Выходящие жидкие потоки, в зависимости от конструкции реактора, могут включать воду, NaOH, NaHCO3, Na2CO3, и другие растворенные газы при различных равновесиях. Растворенные следовые компоненты выбросов, такие как H2SO4, HNO3, и Hg, могут также быть обнаружены. В одном варианте осуществления, для выделения/удаления выходящих жидких потоков, например удаления/выделения воды от карбонатов (в этом смысле слова, "карбонаты" означают смеси карбоната и бикарбоната, потенциально с присутствием также гидроксида) любой метод выделения, применяемый к любой такой смеси, вероятно, включал бы добавление тепловой энергии для испарения воды из смеси, вода может быть подвергнута кипению с целью испарения воды с использованием ребойлера 106, показанного на фиг.6. Альтернативно, поддерживая частичную щелочность раствора (например, NaOH при концентрации приблизительно 1 моль) и затем, нагревая раствор в камере выделения, можно вызвать осаждение относительно чистого Na2CO3 в емкости для хранения, и оставшийся NaOH рециркулировать назад в реактор 200. В других вариантах осуществления, чистый карбонат, чистый бикарбонат и их смеси в равновесных концентрациях и/или в суспензии или в концентрированной форме могут затем периодически отгружаться в грузовик/автоцистерну. В других вариантах осуществления, жидкие потоки могут быть перемещены в испарительные бассейны/поля, где такая жидкость, как вода, может быть удалена путем испарения.
Согласно фиг.6 с помощью приводимой конструкции реактора показанная конструкция реактора может извлекать энергию, имеющуюся в полученном электролизом водороде или в виде горючего топлива, бойлерного газа, или в H2/O2 топливных элементах. Реактор 200 может быть использован для получения установившегося режима работы, когда NaOH и NaHCO3 могут быть получены в пропорциях приблизительно 50:50. Газообразный водород, полученный путем исходного электролиза, может быть использован для обеспечения тепла, NaHCO3 может быть осажден в камере осаждения 108 с оставшимся NaOH, возвращаемым в реактор 200. Суспензия из камеры выделения 108 может быть подана в камеру водоподготовки 110, которая может быть соединена с камерой выделения 108. Альтернативно, при необходимости суспензия может храниться и затем подаваться в камеру водоподготовки 110.
На фиг.7 показана другая конструкция реактора согласно варианту осуществления настоящего изобретения. В частности, на фиг.7 показан повторный захват некоторого избытка энергии, использованной для получения побочного продукта водорода. Использование в тандеме на месте высокоэффективного топливного элемента может позволить получение постоянного электрического тока, который может быть использован для добавления и частичного обеспечения электрическим током электролиза. Из камеры смешения 300 смесь, включая, но этим не ограничивая, процент NaOH, NaHCO3, и NOx, SOx, и Hg подается в камеру выделения 308. Камера выделения 308 может разделять смесь на твердую и/или жидкую фазы путем подведения тепла к смеси. Сушильная камера (не показана) камеры выделения 308 может удалять жидкости из твердой и/или жидкой фазы во время процесса подачи тепла. Образующуюся разбавленную форму NaOH направляют в бойлер 306, в котором разбавленный NaOH концентрируют в результате выпаривания и направляют концентрат в смесительную камеру 300 по линии цикла возврата. Вода из бойлера 306 может быть подана в камеру электролиза 302, в частности в смеситель рассола 302A. Образующаяся Na2CO3/NaHCO3 (суспензия) из камеры выделения 308 может быть подана для промышленного применения. В одном варианте осуществления, суспензия карбоната может быть непосредственно или косвенно (например, сохраняя NaHCO3 для более позднего использования в таком процессе как обработка жесткой воды) подана в установку водоподготовки 310. Альтернативно, NaHCO3 может быть дополнительно очищен, высушен, отгружен и отправлен для использования в других промышленных целях.
Выпуск газообразных продуктов вызывает озабоченность по поводу того, насколько безопасен выброс или NaOH или вышеупомянутых компонентов, то есть выброс "щелочного дождя" из энергетической установки должен быть также исключен, как и выброс "кислотного дождя". Однако гидроксид натрия обычно используют в качестве элемента скрубберной очистки при работе энергетической установки и он одобрен для использования Управлением по охране окружающей среды США (EPA). Транспортировка гидроксида натрия к энергетическим установкам, а также методы предотвращения щелочного выброса хорошо известны в технике. Например, простой и недорогой обратный холодильник может предотвратить любой значительный выброс NaOH в газовых выхлопах.
В способе выделения осаждением карбоната согласно конкретным вариантам осуществления настоящего изобретения, карбонатное равновесие постоянно связывает диоксид углерода и абсорбирует газ при контакте с практически мгновенной конверсией в карбонат ион. Цепь химических реакций может быть лимитирована массообменом, поэтому, как только диоксид углерода абсорбируется основанием, последующие ионные реакции происходят с высокой скоростью.
Равновесие карбоната натрия имеет ту особенность, что когда поднимают температуру, Na2CO3 сам по себе осаждается, что делает возможным его вывод в виде суспензии, с некоторым частичным удалением с суспензией NaOH. В одном варианте осуществления, обработка этой суспензии некоторым количеством влажного хлора, полученного в цикле хлора, может быть использована для уменьшения содержания NaOH до следовых количеств NaCl в NaHCO3 до уровней, которые или соответствуют, или меньше чем в карбонате натрия, полученном добычей подземной "троны" или залежей. По существу, равновесие карбонат натрия/гидроксид натрия обеспечивает углерод законченной транспортной цепочкой из газа в жидкость и в твердое состояние. В других вариантах осуществления, карбонатный цикл может выгодно использовать в качестве среды для аккумуляции суспензии золы, гидроксида натрия и других различных карбонатов и примесей и вывоза суспензии для использования в качестве дорожного основания.
V. Электролиз рассола для получения жидкого абсорбента при низких энергиях
Как указано выше, в определенных вариантах осуществления, в установках и способах настоящего описания используется электролиз рассола для получения гидроксида натрия, который применяют в качестве жидкого абсорбента в процессе декарбонизации. Электролиз рассола является электрохимическим процессом, в основном используемым в производстве концентрированного гидроксида натрия (каустической соды) и газообразного хлора, и он обычно описывается в соответствующей литературе следующим уравнением:
2 NaCl+2 H2О+e-→2 NaOH+H2(г)+Cl2(г)
Электролиз рассола может быть осуществлен в трех главных типах стандартных электролизеров: диафрагменном, с ртутным катодом, и мембранном. Каждый из этих типов электролизеров производит одни и те же конечные продукты из одних и тех же исходных реагентов. Они отличаются друг от друга в основном способом, с помощью которого разделяют друг от друга исходные реагенты и конечные продукты.
В одном варианте осуществления, в силу ряда факторов может быть использован мембранный электролизер. Во-первых, экологические соображения по поводу опасности ртути уменьшили спрос на электролизер с ртутным катодом. Во-вторых, диафрагменные электролизеры могут производить относительно разбавленный гидроксид натрия, который содержит значительные концентрации соли и хлорид иона, и требует значительной повторной обработки/выделения для удаления значительного содержания соли из гидроксида натрия. В-третьих, усовершенствования в технологии фторированных полимеров увеличили ресурс и электрический коэффициент полезного действия технологии с использованием мембранного электролизера, в котором ресурс свыше 5 лет принято гарантировать на рынках товаров промышленного назначения. Кроме того, в предпочтительных вариантах осуществления эффективность использования энергии на тонну гидроксида натрия превышает эффективность как для диафрагменного, так и для электролизера с ртутным катодом.
Мембранные электролизные установки характеризуются, но этим не ограничивая, следующими обобщенными входными и выходными показателями:
Анод: ввод 26% NaCl+2275 кВт·ч/тонна Cl2→Cl2 (г)+24% NaOH
Катод: ввод H2O+e-→30-33% NaOH+H2(г)
Следует отметить, что расход электроэнергии (например, 2275 кВт·ч на тонну хлора) может зависеть от индивидуальных конструкций электролизеров. По существу, расходы могут изменяться.
Многие предпочтительные варианты осуществлений могут использовать мембранные электролизеры в этой функции. Мембранные электролизеры имеют несколько преимуществ над другими процессами электролиза рассола. Во-первых, мембранные электролизеры не содержат и не производят никаких чувствительных для окружающей среды выбросов (например, ртуть) и являются электрически эффективными по сравнению с диафрагменными и ртутными электролизерами. Они также используют замкнутый цикл концентрированный/разбавленный/доукрепленный NaCl, так что они могут хорошо подходить для использования в качестве непрерывной технологической установки "с замкнутым циклом по соли". Далее, NaOH, полученный в мембранных электролизерах, без дополнительного испарения/концентрирования может естественным образом соответствовать уровню концентрации для использования в процессе декарбонизации (например, 30-33% NaOH по массе). Кроме того, водород, получаемый в мембранных электролизерах, является "чистым", приблизительно соответствуя "электронной чистоте", и относительно чистым по NaCl или другим примесям. По существу, водород может быть сжат и закачен в резервуар в качестве газообразного водорода электронной чистоты, использован для производства энергии на месте, например для сжигания в смеси с низкосортным углем или для повышения эффективности технологии сжигания. Альтернативно, водород может быть использован в качестве котельного топлива для процессов выделения, которые могут проводить после декарбонизации. Технология с мембранным электролизером может также быть легко масштабирована от лабораторной установки до масштабов промышленного производства путем добавления небольших дополнительных установок. Кроме того, газообразный хлор, получаемый в мембранном процессе, является менее "влажным", чем хлор, полученный другими стандартными электролитическими процессами. По существу, одностадийный цикл сжатия может быть достаточным для производства хлора с чистотой, требуемой при водоподготовке.
Вышеизложенное относится к состоянию техники, описанному в литературе и применяемому на практике, относящемуся к промышленному производству газообразного хлора и гидроксида натрия. Однако цели конкретных вариантов осуществлений настоящего изобретения отличаются в некоторых аспектах, что приводит к отличающимся химическим методам, применяемым для совершения различных окончаний конкретных вариантов осуществлений настоящего изобретения.
A. Использование методов низковольтного электролиза
В некоторых вариантах осуществления настоящего изобретения, электролиз рассола включает методы низковольтного электролиза (НВЭ), таким образом улучшая термодинамическую эффективность способа. Конкретные варианты осуществления настоящего изобретения не производят гидроксид натрия исключительно в качестве конечного продукта, а используют NaOH, прежде всего в качестве промежуточного абсорбента для абсорбции CO2 из топочного газа перед его выпуском в окружающую среду. Так как промышленное производство хлора и щелочи обычно включает транспортировку гидроксида натрия с завода-изготовителя в место его использования, транспортировка больших количеств воды в гидроксиде натрия является неэкономичной, поэтому каустик обычно концентрируют до приблизительно 55 мас.% для транспортировки в виде жидкости путем энергоемкого удаления воды в результате выпарки, и в некоторых случаях его концентрируют до безводного твердого вещества, обычно в гранулированной форме. Эта концентрация достигается обычно путем эксплуатации электролизеров при напряжениях выше 5 в (называемое "при значительном перенапряжении"), при котором достигается вышеупомянутая концентрация 30-35% NaOH, за которым затем следует цикл выпарки для достижения 55% (или для получения полностью высушенного продукта в безводном, гранулированном состоянии и так далее).
В большинстве вариантов осуществлений настоящего изобретения NaOH не транспортируют в качестве конечного продукта, и он производится при пригодных к использованию концентрациях (в качестве потока водного абсорбента) при напряжениях значительно ниже стандартных 5 В+, используемых при эксплуатации установок для производства хлора и щелочи. Воздействие использования НВЭ на термодинамическую эффективность настоящего изобретения невозможно переоценить, так как потребляемая энергия точно определяется по простому уравнению для постоянного электрического тока:
P=V (напряжение)×I (ток)×(выход по току)
Так как ток устанавливается электрохимическим процессом (одна пара электронов на каждую молекулу и так далее), электропитание почти полностью регулируется напряжением, необходимым для электролиза (дополнительным важным фактором является выход по току, который также является функцией приложенного напряжения). Так как варианты осуществления настоящего изобретения используют НВЭ с напряжениями, которые легко достигаются в стандартных электролизерах, путем изменения режимов эксплуатации до наиболее низкого уровня 2,1 В, путем модификации процесса и размеров стандартного мембранного электролизера, в вариантах осуществления настоящего изобретения потребляется меньше электроэнергии (кВт·ч) для каждого количества образовавшегося NaOH, чем в случае традиционного высоковольтного электролиза с целью получения хлора и щелочи. По этим причинам предпочтительные варианты настоящего изобретения включают электролизеры, которые сконструированы для использования всех доступных методов осуществления низковольтной эксплуатации, включая, но этим не ограничивая эксплуатацию при малом расстоянии между электродами, при повышенном давлении, при большой площади поверхности мембраны, при изменяемых концентрациях анолита и католита и отношениях протонирование-ион. Дополнительные аспекты НВЭ подробно объясняются в примере 4.
B. "Точка безразличия" использования водорода
Типичный процесс получения хлора и щелочи производит газообразный водород, который или сжигают на месте в качестве котельного топлива для выпарки (см. выше), или во многих случаях его выделение полностью подавляют путем использования воздушного электрода; например устройства, которое подает воздух, содержащий кислород, на катод, вызывая немедленное протекание реакции восстановления:
H2(г)+1/2O2(г)→H2O(ж/г),
что изменяет электрохимическое суммирование энергий и понижает напряжение, необходимое для производства каустика и хлора (в некоторых случаях ниже 2,8 В в различной промышленной литературе) за счет того, что не производится водород. Преимущество для предпочтительных вариантов осуществления настоящего изобретения заключается в том, что для них не требуется водород в качестве котельного топлива для выпарки.
Некоторые варианты осуществления настоящего изобретения могут включать процесс с "воздушным электродом", который подавляет производство водорода (и сводит к нулю возможность извлечения энергии из этого водорода), но многие предпочтительные варианты осуществления утилизируют производство водорода для или возврата энергии, или для использования в качестве исходного химического сырья для других процессов.
Поэтому установки, использующие конкретные варианты осуществлений настоящего изобретения, имеют "точку безразличия" относительно использования водорода, полученного таким образом; то есть установка производит водород для возврата его энергии (например, 60% содержания его энергии в случае примера), и это количество энергии имеет конкретную экономическую величину, и вместо использования водорода для возврата энергии водород может быть обменен или продан в количестве, которое превышает или равно этой экономической величине только одной энергии. Таким образом, установки этого типа представляют своего рода "источники водорода". Водород производят и потребляют в качестве источника для получения электрического тока и любой желающий использовать водород для других целей должен только возместить его ценность как источника электричества или ее экономический эквивалент для поддержания экономики процесса. Этот вариант осуществления имеет выгодные последствия для будущих схем "водородной экономики"; имея доступный источник водорода, доступный в точке безразличия стоимости к цене, которая ниже чем природное содержание энергии в нем, можно доказать полезную и выгодную характерную особенность этой технологии.
C. Использование методов оптимизации протонированного рассола
Конкретные варианты осуществления настоящего изобретения специально оптимизируют производство водорода вместо его подавления путем следующих средств оптимизации протонированного рассола. Обычная промышленность производства хлора и щелочи в некоторых случаях использует добавление HCl в виде хлористоводородной кислоты в рассол (NaCl) электролизера, называемый пространством анолита. Это "протонирование" рассола имеет эффект понижения напряжения, требуемого для производства нормированного количества гидроксида натрия, заключающийся в том, что он понижает электроэнергию, требуемую для получения реагента/абсорбента конкретных вариантов осуществлений настоящего изобретения. При нормальной работе установок по производству хлора и щелочи, причину этого понижающего напряжения эффекта приписывают "нейтрализации NaOH, который возвращается через мембрану," процессу, который был изучен в зависимости от селективности мембраны, и так далее, и хорошо понят. Вообще говоря, считают, что эта "нейтрализация" производит только соленую воду [NaOH (возвращающийся)+HCl (анолит)→NaCl+H2O] и не доказано, что она изменяет стехиометрию продуктов. Однако одним моментом, который хорошо не изучен или не применяем в технике, является то, что добавление HCl действительно фундаментально изменяет стехиометрию уравнения следующим образом:
NaCl+aHCl+H2O→NaOH+(1/2+a/2)H2+(1/2+a/2)Cl2
Это дополнительное количество произведенного водорода и хлора представляет особый интерес для настоящего изобретения, так как варианты осуществления настоящего изобретения полагаются на рекуперацию энергии из водорода (которая усиливается, когда производится больше водорода, и является более экономичной, когда образуется больше газообразного хлора на моль произведенного абсорбента NaOH). То, что это производит дополнительное количество водорода для извлечения энергии и хлора для продажи, в то время как суммарное электрическое напряжение (следовательно, электроэнергия и стоимость) уменьшается, приводит конкретные варианты осуществления настоящего изобретения к оптимизации "a" для достижения самых низких затрат энергии для получения реагентов и самому высокому извлечению энергии из продуктов. Оптимум обычно лежит между 0,5 и 1,0 M HCl в растворе NaCl (вод.). Однако оптимизация является специфической для каждой конструкции электролизера, размеров, концентрации, температуры и режима давления. Однако для каждого электролизера существует оптимальная степень протонирования ("a"), при которой достигается эксплуатация с наименьшими затратами энергии. На практике, чрезвычайно высокие значения "a" (>0,15M при 90°C, например) будут, вероятно, моментально вызывать образование пузырей на большинстве выпускаемых в промышленности мембран. Разумеется, что хотя HCl является предпочтительной кислотой для протонирования рассола в изобретении, многие другие кислоты, известные специалистам в этой области, могут также быть использованы для протонирования рассола.
D. Самообразование HCl, которое используется для протонирования
Так как конкретные варианты осуществления настоящего изобретения и используют подвод HCl и производство газообразных H2 и Cl2, протонирование рассола может быть осуществлено за счет самообмена; то есть газообразные продукты H2 и Cl2 могут быть сожжены (в эффективных топливных элементах или в обыкновенных обжиговых печах) с получением газообразного HCl, который может затем быть рециркулирован в анолит для протонирования рассола. Энергия, извлекаемая при сжигания H2/Cl2, выше чем энергия, извлекаемая при сжигании H2/O2. Это повышает термодинамическую эффективность изобретения.
В некоторых предпочтительных вариантах осуществления настоящего изобретения используется путь абсорбция/конверсия/регенерация в качестве "начального процесса концентрирования/абсорбции", который затем используют для абсорбции и концентрирования CO2 для использования в методах геологических, океанических, или земных секвестров (например, методах, которые закачивают CO2 в хранилища углерода) с помощью следующих способов или аналогично:
(1) Весь водород сжигают с получением газообразного HCl.
(2) Весь полученный таким образом газообразный HCl взаимодействует с бикарбонатом натрия.
(3) В результате соответствующей реакции нейтрализации высвобождается почти 100% чистого CO2 и происходит регенерирация соленой воды, которая может быть рециркулирована для дальнейших циклов абсорбции.
(4) В результате этого процесса изобретение используется для абсорбции, конверсии и затем высвобождения CO2 с результирующим эффектом удаления газа из потока топочного газа и концентрировании его для дальнейших методов секвестра после этого процесса.
E. Добавление карбонатов и бикарбонатов обратно в среду католита
В отличие от того, как в промышленности производства хлора и щелочи используют топливные элементы хлор/водород, в некоторых вариантах осуществления настоящего изобретения реализуется также рециркуляция смеси карбоната и бикарбоната в пространство католита (гидроксид натрия) электролизера. Такие методы имеют широкий диапазон изменений, но каждый рабочий режим для полного процесса имеет оптимальную величину рецикла смесей бикарбонат/карбонат в католит, так как это может при некоторых концентрациях и условиях понижать напряжение на электролизере и, следовательно, потребление электроэнергии электролизером.
F. Использование утилизации отходящего тепла для нагрева жидкостей
Так как конкретные варианты осуществлений настоящего изобретения используются в присутствии энергетической установки или большого выброса CO2 в виде топочного газа или других горячих газов от сжигания, имеются широкие возможности для теплообмена, в отличие от стандартных процессов хлор-щелочь. Например, температура типичного топочного газа (например, после обработки путем электростатического пылеулавливания) может вполне быть 300°C. Охлаждение этого отходящего газа до температуры ниже 300°C при нагревании жидкостей анолита и католита (которые, для НВЭ, должны обычно поддерживаться при температурах >90°C) позволяет конкретным вариантам осуществлений настоящего изобретения работать без потерь электроэнергии, связанных с нагревателями анолита и католита.
G. Использование утилизации отходящего тепла для энергоснабжения технологического оборудования
Обычно, так как отходящий газ, который доступен на энергетических установках, выходит при температурах между 100°C (типичной для скруберной очистки), 300°C (после процесса пылеулавливания) и 900°C (вход в установку для пылеулавливания), или других таких значений, в результате обработки значительное количество отходящего тепла может быть извлечено путем охлаждения входящего топочного газа путем теплообмена с помощью цикла извлечения электроэнергии, примером которого является цикл аммиак-вода (запатентованный процесс "Kalina", например), паровой цикл, или любой такой цикл, который выполняет аналогичные термодинамические задачи. Так как конкретные варианты осуществления настоящего изобретения основаны на электроэнергии постоянного тока для осуществления производства реагент/абсорбент для настоящего изобретения, процесс может непосредственно снабжаться электроэнергией, частично или полностью, за счет утилизации отходящего тепла, которое осуществляется без нормальных потерь в трансформаторе, связанных с превращением этой электроэнергии постоянного тока в энергию переменного тока для других использований. Кроме того, путем использования отходящего тепла для работы двигателей могут быть достигнуты значительные коэффициенты полезного действия вообще без использования стадии получения электричества. В некоторых условиях эти количества энергии могут быть найдены при утилизации тепла для полного энергообеспечения вариантов осуществления настоящего изобретения.
VI. Образование и использование побочных продуктов в результате процессов декарбонизации и электролиза
Как отмечено выше, конкретные варианты осуществлений установок и способов настоящего описания позволяют получать ряд полезных побочных продуктов в результате процессов декарбонизации и электролиза, включая газообразный хлор, бикарбонат натрия и газообразный водород. В некоторых вариантах осуществления, газообразный водород, получаемый вариантами осуществления настоящего изобретения, вводят в цикл повторного использования энергии водорода. В одном варианте осуществления, настоящее изобретение может включать современные технологии использования мембран из фторированных полимеров для уменьшения миграции иона хлора для процесса декарбонизации. Следовательно, процесс может функционировать без больших затрат энергии и издержек для отделения иона хлора; циклы декарбонизации и выделения не содержат хлоридов. По существу, вариант осуществления реактора декарбонизации настоящего изобретения может использовать поваренную соль, воду и отработанный диоксид углерода, объединенные с электроэнергией для образования газообразного хлора, бикарбоната натрия и утилизации энергии путем сжигания водорода следующим образом:
2 NaCl+H2O+2 CO2+e-→2 NaHCO3+Cl2+[1/2H2+атм.O2→e-]
A. Цикл повторного извлечения энергии водорода
Были разработаны два метода, которые могут использовать энергию водорода, извлеченную вариантами осуществления настоящего изобретения. Первым является совместное сжигание водорода с углем для улучшения выбросов угольных топок, а второй метод включает получение постоянного электрического тока в топливном элементе водород/кислород. Приблизительно от 22% до 32% затрачиваемой на электролиз энергии может быть извлечено за счет сжигания H2/O2. Альтернативно, H2 и Cl2 могут сгорать в Cl2 и HCl непосредственно или с помощью топливного элемента, или извлечения постоянного электрического тока. Источники тепла из извлечения отходящего тепла, или из реакции электролиза, по которой производится в резервуар гидроксид натрия с температурой приблизительно 135°C, или из самого процесса декарбонизации, в котором абсорбируются различные теплоты растворения, теплоты испарения, и тепло, высвобождаемое в экзотермической реакции, могут быть утилизированы с помощью хорошо известных методов (то есть, ребойлеры, и так далее) в местах расположения энергетической установки для подогрева газообразных продуктов сгорания или других использований.
В одном варианте осуществления, промышленное получение постоянного электрического тока в топливном элементе может быть выгодным из-за удобства в обращении и безопасной эксплуатации при давлениях ниже атмосферного. Безотлагательное потребление полученного водорода может также непосредственно уменьшить затраты электроэнергии на электролиз рассола. Кроме того, так как цикл извлечения водорода может быть произведен в период внепикового электрического производства H2, Cl2, и NaOH, а H2 может быть затем использован для обеспечения электричеством пиковых нагрузок, настоящее описание обеспечивает получение реагентов при низких затратах при последующем производстве вспомогательных высоких затрат при пиковой нагрузке электроэнергии и одновременном осуществлении процесса декарбонизации. Экономическая эффективность цикла извлечения энергии H2 для увеличения пикового производства энергии установки путем увеличения производительности производства электрического тока путем сжигания H2 в качестве или топлива или в топливном элементе может обеспечивать утилизацию на основе самопотребления.
Альтернативно, данный очищенный произведенный из углерода источник газообразного водорода электронной чистоты может с успехом использоваться муниципальными энергопредприятиями, промышленными компаниями и в энергетических установках в муниципальных автобусных парках, поездах и других общественных или частных областях использования водородного топлива.
B. Другие использования побочных продуктов процесса декарбонизации
В одном варианте осуществления, газообразный хлор может быть первичным окислителем, используемым для уничтожения бактерий в установках водоподготовки по всему миру. Хлор и некоторые 100+ производные исходные сырьевые химические продукты, которые получают из него, часто упоминают как образующие до 30%+ ВВП США. Он может также быть использован в производстве самого большого промышленного химического продукта, хлористоводородной кислоты. Хлор также широко используется в промышленности пластмасс в качестве самого распространенного неуглеродного реагента.
Карбонат натрия является побочным продуктом способа, описанного в настоящем изобретении, который широко используют в производстве мыла, моющих средств и шампуней по всему миру, а также в качестве присадки в производстве. Кроме того, энергосистемы, а также частные дома используют бикарбонат натрия для смягчения жесткой воды в результате следующей реакции:
CaCl2(вод)+NaHCO3(вод)→CaCO3(осадок)+NaCl(вод)+HCl(вод)
Аналогичный способ может быть использован с применением карбонатов и бикарбонатов натрия из этого способа для осуществления обмена ионов с многочисленными солями группы 1 и группы 2 для осаждения различных карбонатов.
Другим примером побочных продуктов, получаемых из процесса декарбонизации, является газообразный водород. Газообразный водород электронной чистоты является высшей формой энергоносителя. С другой стороны, производимое водородное топливо может быть сожжено с более "грязными" углями для уменьшения выброса от этого топлива, может быть сожжено в качестве питания котла в процессе выделения или может быть использовано в автопарках на водородном топливе.
В дополнительных вариантах осуществления, возможно осуществление эффекта транспортирования диоксида углерода до удаленных мест секвестра следующим способом или его эквивалентом:
(1) На месте энергетической установки абсорбируют CO2 и другие загрязняющие вещества с помощью способа или любого его варианта, наряду с производством водорода, хлора, карбонатов.
(2) В месте удаленного секвестра хлористоводородную кислоту и карбонаты снова объединяют в реакции нейтрализации для генерации фактически чистого CO2. Полученный этими методами CO2 может затем быть закачен в хранилище углерода.
С помощью этих методов аналогичный результирующий эффект транспортировки CO2 между местом энергетической установки и местом секвестра достигается без физического транспорта CO2 в результате сжижения и транспорта по трубопроводу, автомобильными перевозками и так далее.
ПРИМЕРЫ
Следующие примеры включены для демонстрации предпочтительных вариантов осуществления изобретения. Эти варианты осуществления обеспечивают практически реализуемое экономическое решение для уменьшения или даже практически удаления диоксида углерода и других загрязняющих веществ из энергетических установок путем получения и использования образующихся реагентов для продаж или в промышленных процессах и/или путем возврата энергии.
Для специалистов в этой области должно быть очевидно, что описанные в примерах способы, которые следуют за уже представленными способами, раскрытыми автором изобретения для надлежащего функционирования при практическом применении, могут считаться предпочтительными режимами для его применения. Однако для специалистов в этой области должно быть очевидно, что много изменений могут быть сделаны в свете настоящего описания в описанных конкретных вариантах осуществлений и дополнительно могут быть получены похожие или аналогичные результаты без выхода за пределы существа и объема изобретения.
Пример 1
Проектирование барботажной реакторной колонны CO2/NaOH графическими способами
В барботажной реакторной колонне, спроектированной для этого примера, имеется четыре основных потока, а именно:
(1) Жидкость, текущая в потоке барботажной колонны при данном объемном расходе (Vl = объем жидкости за время); в выбранном случае, объемный расход на входе равняется объемному расходу на выходе. Поэтому оба обозначены как Vl). В этом примере Vl=0,001 м3/сек.
(2) Vg0 = объемный расход входящего газа, который будет частично или полностью абсорбирован жидким абсорбентом. В этом примере Vg0=0,05 м3/сек.
(3) Vg = объемный расход выходящего газа. В этом примере, Vg=0,02 м3/сек.
Барботажный колонный реактор был спроектирован на основе вышеуказанных условий. Шестьдесят процентов входящего CO2 в топочном газе должно было удаляться при барботировании через раствор концентрированного гидроксида натрия. Реакция лимитируется массообменом. Целью примера было рассчитать размеры реактора (высоту и диаметр), необходимые для удаления 99,9% диоксида углерода. P=2 атм, T=298K. Используя графические данные, приведенные на фиг.8, этот пример описывает конструкцию как высокого реактора (2,36 м), так и невысокого реактора (0,41 м). На фиг.8 представлена диаграмма, показывающая процент абсорбции CO2 в барботажной колонне в зависимости от глубины жидкости и межфазной скорости газа при низких межфазных скоростях (Schumpe et al., 1979).
Решение для колонны с высотой 2,36 м
Конверсия достигает 100% при приведенной скорости (Ug0), приблизительно равной 0,04 с/сек. Эта скорость находится в области барботирования (в растворах, аналогичных воде, она приблизительно составляет 0,05 м/сек). Зная требуемый объемный расход газа (Vg0), вычисляли диаметр колонны:
Ас=Vg0/Ug0=0,05/0,04=1,25 м2
Dc=2√Ac/π=2√1,25/π=1,26 м2
Следовательно, конверсия 99% входящего 60% CO2 требует колонну высотой 2,36 м, площадью 1,25 м2, имеющую диаметр 1,26 м и общий объем 2,95 м3.
Решение для колонны с высотой 0,41 м
Конверсия в колонне высотой 0,41 м требует приведенной скорости газа около 0,02 м/сек. Подобно вышеприведенным расчетам:
Ас=Vg0/Ug0=0,05/0,02=2,50 м2
Dc=2√Ac/π=2√2,5/π=1,78 м2
Следовательно, конверсия 99% входящего 60% CO2 требует колонну высотой 0,41 м, площадью 2,50 м2, имеющую диаметр 1,78 м и общий объем 1,03 м3.
Итак, путем этого примера продемонстрировано, что более короткие колонны являются более эффективными на единицу объема при удалении диоксида углерода из отходящего газа; для этого примера в 3 раза. Следовательно, для предпочтительных вариантов осуществлений настоящего изобретения проектирование ставит целью короткие ступени и/или многоступенчатые реакторы, состоящие из коротких ступеней.
Пример 2
Проектирование барботажной колонны CO2/NaOH путем определения коэффициента массообмена
Цель этого примера заключалась в определении коэффициента массопередачи, kla (моли/сек/объем), из теоретического построения. Из этого примера было определено, что этот корреляционный метод может потенциально приводить к неубедительным результатам; то есть этот пример подчеркнул трудность предсказания реальных результатов из теории в силу неопределенности измерения некоторых основных параметров. Поэтому только экспериментальное масштабирование может окончательно определять результат для крупной установки декарбонизации.
Следующие уравнения для захвата газа (εg) и мольного переноса (kLa) вытекают из корреляций, установленных Akita and Yoshida (1973), и они применимы для систем диоксида углерода и воды для колонн с относительно большой высотой и диаметром (то есть >0,1 м):
Захват газа
εg
-----=C*[g*Dc2*ρL/σ]1/8*[g*Dc2/νl1]1/12*[µg/√g*Dc]
(1-εg)4
и
коэффициент массообмена
kLa(1/сек)=[Ссo2*Dco2-h20/Dc2]*[νL/Dco2-h20]0,02*[g*Dc2* ρL/σ]0,62*[g*Dc3/νl2]*ε11
Где εg - коэффициент захвата газа
Cco2 = концентрация CO2 в отходящем газе
Dc=диаметр колонны
νL=0,0001 м2/сек
σ=1cP=0,1Па·сек
ρL=998 кг/м3
и так как Dco2-h20P=1,661 м2·Пa/сек,
то, Dco2-HO=1,661/5,067·105=3,278·10-6 м2/сек
Движущая сила является разницей между равновесной концентрацией диоксида углерода (Cco2*) и текущей концентрацией диоксида углерода в жидкой фазе (Cco2), которая в этом примере принимается равной нулю; то есть присутствующий гидроксид натрия мгновенно нейтрализует водный диоксид углерода, "кислоту". Скорость мольного переноса на единицу объема реактора может, поэтому быть записана как:
Nco2=kLa*[Cco2*-Cco2]=kLa(Cco2*)
Скорость мольного переноса, необходимая для удаления 99,99% диоксида углерода в отходящем газе. Полагают, что CO2 является идеальным газом при условиях в колонне.
Кубический объем/сек:
Vg0=0,05 м3/сек∴Vco2=0,6*Vg0=0,03 м3/сек
Моль/сек:
Vco2*P/RT=[0,03M3/сек*5 атм]/
[0,082m3атм/кмольK*298]*1000 гмоль/1 кмоль=6,14 моль/сек
Nco2(моль/сек)=0,999(мольCO2удаленного/мольCO2поступившего)*6,14 моль/сек=6,13 моль/сек
Другие свойства жидкости, необходимые для корреляционной модели.
Установив исходную приведенную скорость на пределе потока барботирования (Vg0=0,05 м/сек), вычисляли площадь и диаметр колонны:
Ас=Vg0/Ug0=0,05/0,05=1,0 м2
Dc=2√Ac/π=2√1,0/π=1,13 м2
Для газофазных реакций захвата этот пример устанавливает C=0,2 и предполагается, что приведенная скорость (Ug) является средней между входящими и выходящими скоростями; Ug=0,035 м/сек=среднее арифметическое от (0,05 м/сек и 0,02 м/сек), и, используя программу для решения уравнения, было найдено, что εg=0,055.
Далее, была вычислена постоянная скорости мольного переноса:
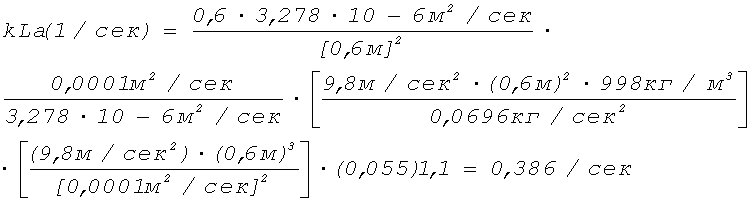
kLa=0,386/сек
Возвращаясь к уравнению для движущей силы, был вычислен объем реактора (V):
V=Nco2/[(kLa)(Cco2*)]=6,13 моля/сек/(0,386/сек*(103,6 моль/м 3 ))= 0,15 м 3
и
Hc=0,15 м3/1 м2=0,15 м
Таким образом, размерами барботажной колонны являются Dc=1,13 м и Hc=0,15 м, приводя к значительному различию от реальных результатов в реальных барботажных колоннах.
Несколько допущений могут объяснить различия корреляционных моделей (которые считаются лучшими моделями для этого режима работы) и реальных результатов:
(1) Предполагалось, что гидроксид натрия имеет свойства воды (плотность, поверхностное натяжение и так далее); и
(2) Концентрация CO2 в растворе не может хорошо характеризоваться как нулевая; она является более вероятной величиной вычислений; например, если эффективная концентрация CO2 не равна нулю, то движущая сила будет меньше, и требуется более высокая колонна.
Следует также отметить, что эта теоретическая корреляция нарушается при условии, которое также является ее эффективностью: так как такие термины, как (νL=0,0001 м2/сек) часто возводятся в квадрат в знаменателе, небольшие изменения в этих числах приводят к гигантским эффектам. Этот тип теоретического построения является хорошим для подбора аппроксимирующей функции постфактум, но не является хорошим предсказателем массообмена для целей проектирования. Кроме того, имеются поразительные гидродинамические влияния на скорость абсорбции/конверсии CO2, так что следует проектировать при отличающихся и пропорционально увеличивающихся масштабах.
Пример 3
Проектирование барботажной колонны (глубины) CO2/NaOH из экспериментальных данных
Замечание, что опора конкретных вариантов осуществлений настоящего изобретения на "теорию эффективности короткой ступени", описанную здесь (3 м или менее расстояния контакта газ-жидкость, или высоты жидкой фазы, для достижения >90% абсорбции), подтверждается двумя различными методами вычисления, которые находятся в соответствии с применяемым в химической технологии проектированием. Однако в конкретных случаях (как отмечено выше) были сделаны определенные упрощающие допущения в этих проектных вычислениях, поэтому была необходима и осуществлена экспериментальная проверка с результатами, приведенными на фиг.2B и 2C (объясненными более подробно ниже).
В каждом из этих технологических экспериментов достигалась определенная абсорбция CO2 при определенном расстоянии контакта газ-жидкость (то есть высота жидкости в случаях безнасадочной, открытой барботажной колонны); например 20% абсорбция через 30 см жидкости.
Если газ затем пропускали через вторую колонну аналогичной конструкции и при таких же условиях, то такая же абсорбция происходила бы снова; то есть, 20% от оставшихся 80% исходного CO2 снова бы абсорбировалось. Эта зависимость в конечном счете ослабевает; однако, при данных высоких абсорбционных характеристиках жидкого абсорбента, и тенденции протекания хемосорбции при стабильной абсорбции даже разбавленного CO2 в топочном газе, для этого примера этот эффект игнорируется и в конструкции достигается удаление 90% СО2.
Очевидно, что дополнительные пропускания потока через абсорбционную жидкость снова уменьшили бы оставшийся CO2 на 20%, и так далее, пока не будет осуществлено достаточное количество пропусканий потока для достижения требуемого уровня абсорбции (в этом случае 90%).
Это приводит к проектированию "ряда основных ступеней", при котором определяют глубину жидкости (глубин множества ступеней с высотой 30 см), которая необходима для достижения 90%. При предположении, что каждая ступень абсорбирует при таком же %CO2/расстояние, как и предыдущая, были получены результаты, представленные на фиг.2B и 2C, и графически представленные на фиг.2D и 2E.
На фиг.2A показана установка для исследования основных характерных особенностей одного варианта осуществления стадии декарбонизации настоящего изобретения. Установка на фиг.2A (или установка с аналогичным действием) может эксплуатироваться согласно методике, приведенной ниже:
(1) В установку карбонизации 801, содержащую насадку или без насадки, загружают NaOH (например, 1M NaOH в воде при 25°C) до глубины 30 см с исследуемой нагрузкой.
(2) Топочный газ, смоделированный или реальный, в этом случае, типичный выхлоп топочного газа угольного отопления (16% CO2, 84% N2, SOх/NOх <1% или в природных уровнях ppm) вводят в установку карбонизации 801, эффективно орошают в колонне без насадки, эффективно орошают или распределяют в насадочных колоннах, перемещают через жидкость, и удаляют. Газ находится при температуре 25°C, CO2 с расходом 2 л/мин смешивают пропорционально с другими газами, поднимается вверх по колонне с диаметром окружности 4"; давления в системе может быть 1 атм psig или ниже.
(3) Может быть отмечено в результате измерения концентрации входящего CO2 (путем газовой хроматографии отобранной пробы, например, или путем измерения концентрации CO2 в потоке), что CO2 абсорбируется жидкостью, что температуры возрастают (экзотермическая реакция), а анализ отобранной жидкой пробы покажет присутствие равновесий карбонат/бикарбонат/гидроксид, указывая, что происходит не только абсорбция CO2, но происходит и его конверсия в карбонатную или бикарбонатную форму. Опыт практической эксплуатации указывает, что эти ключевые "точки перехода" находятся в равновесии с pH:
a. При pH<=8,3, преимущественно образуется бикарбонат.
b. При pH>=10, преимущественно образуется карбонат.
(4) Реакция абсорбции/конверсии в карбонат продолжается активно и экзотермично до тех пор пока, при данной динамике потока газа, при какой бы скорости CO2 не абсорбировали/конвертировали, не закончится экзотермическая фаза реакции, температура сначала не меняется и затем падает, и абсорбционная способность жидкости, которая падает по мере понижения концентрации OH иона, быстро достигает нуля в этой точке. Когда уровни абсорбции начинаю падать, обычно значение pH приближается к 8,3 или близкому значению; при pH>8,3 абсорбция является относительно активной.
(5) Жидкость перемещают в колонну бикарбонизации 803 и отходящий газ снова вводят в жидкость. Абсорбция CO2 прекращается и в некоторых случаях, как будет показано, становится отрицательной (жидкость отдает некоторое количество CO2 газовому потоку, проходящему через нее). Температура жидкости продолжает падать, частично из-за некоторого несущественного испарения в перемещающийся поток газа, но также из-за реакции бикарбонизации, которая происходит между ранее образовавшимся карбонатом натрия и оставшимся "зависшим" CO2, который растворен в жидкости.
(6) Равновесие продолжает сдвигаться в сторону бикарбоната и оптимизации концентрации исходного гидроксида, температур жидкости и газа, давлений, расходы потоков и скорости, крутизны и так далее могут быть осуществлены, вплоть до точки получения чистого бикарбоната (99%+).
На фиг.2B и 2C приведены результаты нескольких серий испытаний, проведенных с загрузкой-нагрузкой (в системе декарбонизации была создана конкретная концентрация NaOH, как показано на фиг.2A). Несколько ключевых точек иллюстрируются данными на фиг.2B и 2C:
(1) Условия могут быть соответственно применены для воспроизводимого получения или чистого карбоната (эксперименты 4 и 14), или чистого бикарбоната (эксперименты 28 и 32) и могут быть отрегулированы для достижения различных результатов (или "ионных отношений" между крайними значениями 1,0-2,0).
(2) Найдено, что размеры реактора, которые являются результатом этого исследования, для всех случаев со значительной абсорбцией, обеспечивающие расстояния для контакта газ-жидкость, обычно меньше чем 3 м, являются достаточными для достижения 90% абсорбции поступающих газов. Поэтому показано, что для того чтобы достигать скоростей абсорбции, соответствующих пределам термодинамической эффективности, следует проектировать короткие ступени с низким сопротивлением. Другими словами, физический способ удаления CO2 работает при уровнях абсорбции, которые могут, очевидно, соответствовать или превышать термодинамическую эффективность системы. Такие высокие скорости абсорбции (входящего газа, выходящего газа) не относят за счет энергии и, следовательно, за счет производства CO2. Поэтому поддержание скоростей абсорбции CO2 из потока и термодинамической эффективности установки в качестве двух четко различаемых величин является важным во избежание путаницы.
Результаты, приведенные на фиг.2B и 2C (абсорбция CO2 жидкостью) и ионное отношение в продукте (1,0 = бикарбонат, 2,0 = карбонат), изображены на фиг.2D и 2E. Несколько важных выводов может быть сделано на основании фиг.2B и 2C.
(1) Отмечаются мгновенные скорости абсорбции порядка 98% при одностадийной абсорбции входящего CO2.
a) Чистый бикарбонат (NaHCO3) получали в растворе в условиях, при которых абсорбировалось 25% входящего CO2 в одноступенчатой барботажной колонне при контакте газ-жидкость с глубиной 0,30 м глубина жидкости/расстояние контакта газ-жидкость. Экстраполяцией на 90% абсорбцию получаем, что 3 метра расстояния контакта является достаточным для абсорбции 90% входящего CO2.
b) Чистый карбонат (Na2CO3) получали в растворе в условиях, при которых абсорбировалось 70% входящего CO2 в одноступенчатой барботажной колонне при контакте газ-жидкость с глубиной 0,30 м глубина жидкости/расстояние контакта газ-жидкость. Экстраполяцией на 90% абсорбцию получаем, что <2 метра расстояния контакта является достаточным для абсорбции 90% входящего CO2.
c) Различная абсорбция в зависимости от соотношений карбонат иона в продуктах указывает, что между этими крайними точками существует непрерывный ряд растворов.
(2) Жидкий абсорбент сохраняет свои абсорбционные характеристики в течение приемлемого для промышленности периодов времени (например, 15-240 минут в этих примерах).
(3) Входные переменные параметры реактора (концентрация, температура, давление, скорость газового потока, время контактирования и так далее) могут регулироваться для получения чистого бикарбоната, чистого карбоната или любой их смеси.
(4) Использование этих лабораторных результатов для проектирования реактора с 90% абсорбцией CO2 приводит к величине меньше 3 м для расстояния контактирования газ-жидкость (например, приблизительно глубина жидкости, высота колонны) и 1 м для приемлемых промышленных процессов во многих областях.
Пример 4
Анализ НВЭ для различных химических условий
На фиг.5 приведена диаграмма, показывающая рабочие характеристики электролиза при низком напряжении для различных химических условий. На ней приведены некоторые типичные результаты, при которых мембранный электролизер для получения хлора и щелочи эксплуатируется при нестандартных условиях, а именно:
(1) pH анолита (протонированного рассола) корректируют с помощью замкнутого цикла pH, регулируемого путем добавления HCl (хлористоводородная кислота в воде) при pH 1,0, 2,5, и 5,0;
(2) температуру анолита поддерживают при заданном значении с помощью замкнутого цикла потоков жидкости, нагреваемых электронагревателями; и
(3) напряжение регулируют для каждого условия жидкость/протонирование/температура с помощью регистрации электрического тока, достигаемого 0,01 м2 электролизером для получения хлора и щелочи.
На фиг.5 обращает на себя внимание набор экспериментальных данных этого примера, которыйе является графиками реального экспериментального напряжения в зависимости от тока (выраженного в плотностях тока, килоампер/м2, указанных на графике) для 0,01 м2 электролизера, 13 мм расстояние между электродами, эксплуатируемого при различных комбинациях температуры и степени протонирования жидкого рассола анолита (регулируемой в этой серии экспериментов с помощью замкнутого цикла pH, регулируемого путем добавления HCl(л) к циклу рассола).
Обращает внимание следующие моменты, относящиеся к этим типичным результатам на фиг.5:
(1) При высоких напряжениях (5 В), которые обычно используют в таких электролизерах для получения хлора и щелочи, достигается максимальный ток (и для данного электролизера, следовательно, максимальная плотность тока).
(2) При более высокой температуре рассола при одном и том же pH устанавливается более высокая плотность тока при данном напряжении.
(3) При более низком pH рассола устанавливается более высокая плотность тока при данном напряжении по сравнению с более высоким pH рассола.
(4) Эти общие тенденции (более высокая температура, более высокая концентрация кислоты) могут быть оптимизированы с помощью стандартных методик планирования экспериментов для проектирования размеров/компонентов каждого индивидуального электролизера с получением оптимума (kA/м2·В) для этого электролизера. Аналогичный эксперимент на любом электролизере для получения хлора и щелочи при повышенном рабочем давлении приводит к выводу, что повышенное рабочее давление также повышает (kA/м2·В).
(5) Наклон этих линий (ΔV/ΔA) исходно является большим, с относительно большими падениями напряжения, происходящими с относительно низкими падениями тока/плотности тока; однако после того как достигается точка перегиба кривой (приблизительно (2,5 В, 10 A/0,01 м2) последующие снижения напряжения приводят к более резким снижениям тока и, следовательно, плотности тока.
(6) Эта точка перегиба и ее окрестности для рабочих условий представляет собой оптимальное компромиссное решение для соотношения напряжение и силы тока и плотности тока для эффективности с экономической точки зрения. Оптимизация при стандартном методе планирования эксперимента позволяет достигать оптимального условия низкого напряжения для любого реального электролизера варианта осуществления изобретения.
(7) В контексте только этого примера, условие для анолита, включающие pH 1,0, 90°C, имеют наилучшую вольт-амперную характеристику и, следовательно, оптимальную рабочую линию, представленную среди этих различных приводимых рабочих линий.
(8) Главным недостатком электролиза при низком напряжении является сопутствующее снижение плотности тока; kA/м2 снижается со снижением напряжения. Так как система может производить одинаковое число Na+ ионов для абсорбции одинакового количества диоксида углерода, м2 площадь поверхностей мембран должна пропорционально увеличиваться; например, если плотность тока упадет на 50%, тогда потребуется мембрана с площадью поверхности в два раза больше для производства достаточного количества жидкого абсорбента. Это сильно влияет на стоимость установки, так как стоимость установки получения хлора и щелочи почти пропорциональна площади поверхности мембраны. Электролиз при низком напряжении дает ряд преимуществ, которые могут, в конкретных вариантах осуществления изобретения, позволить оптимизировать режимы при низком напряжении, которые компенсируют значительно или полностью этот недостаток необходимости большой площади поверхности мембран. А именно, срок службы мембран и компонентов электролизера, которые эксплуатируются в более мягких/менее энергоемких условиях, которые могут увеличить срок службы электролизера и/или мембраны, может быть проверен на практике. Проектирование специально для условий с низким напряжением может сопровождаться некоторой возможностью предъявлять менее строгие требования к определенным материалам и эксплуатационным показателям, которые не являются такими важными в вариантах осуществления, в которых используют низкое напряжение. Некоторые из этих степеней свободы при проектировании могут приводить к электролизерам с низкой стоимостью, которые частично или полностью компенсируют увеличение стоимости мембран электролизеров, изначально происходящее из-за эксплуатации при низком напряжении/низкой плотности тока. В этих и многих других путях, системы НВЭ, несмотря на то что они требуют большей площади поверхности мембраны, чем стандартные электролизеры с мембранной для получения хлора и щелочи для производства одно и того же количества NaOH, могут полностью или частично снизить некоторые из этих дополнительных затрат и эксплуатационные расходы.
(9) Компромисс между преимуществом (низким напряжением и, следовательно, более низким потреблением электроэнергии) и недостатком (более высокая площадь поверхности и снижение плотности тока) может быть оптимизирован с помощью методики, описанной в примере 7. Для рабочей характеристики рН 1,0/90°C, изображенной на фиг.5 (которая для этого небольшого набора условий примера является наилучшей V/I характеристикой для эксплуатации НВЭ), можно вычислить Voptlve, и из вышеприведенной зависимости может быть получено Ioptlve. Следовательно, для данных размеров конструкции электролизера могут быть осуществлены все условия по температуре, давлению, концентрации рассола, степени протонирования, выборок мембраны и так далее, для получения наилучшей V/I кривой или рабочей линии, и затем оптимальная точка на этой кривой может быть вычислена методом из примера 7. В этом случае Voptlve составляет 2,88 В и плотность тока Ioptlve составляет 1,04 kA/м2.
(10) В примере 7 ток при Vopt=2,88 в составляет приблизительно 5 A в случаях небольшого протонирования и/или низкой температуры. В этом же примере этот ток (и, следовательно, плотность тока) был более чем в два раза больше, то есть 10,4 A.
(11) Дополнительное протонирование рассола, температура, давление, концентрация, геометрическая компоновка компонентов электролизера, электрические поля и условия могут быть аналогично оптимизированы для получения наилучшего показателя (kA/м2·В), но само по себе протонирование увеличивает количество получаемого стехиометрического водорода, тем самым повышая окупаемость энергии системы. Важно отметить, что оптимизация для наименьшей энергии абсорбции/конверсии CO2 может быть достигнута путем также оптимизации показателя (kA/м2·В) системы, который понижает энергию, требуемую для получения жидкого абсорбента, но который одновременно оптимизирует водород, доступный для рекуперации энергии (и затем оптимизирует эффективность, с которой извлекают энергию этого доступного водорода), полная энергия для процесса может быть оптимизирована до ее самого низкого значения для данного электролизера конкретной конструкции.
(12) Исходя из того, что варианты осуществления настоящего изобретения могут эффективно абсорбировать CO2 чрезвычайно разбавленными гидроксидами (было продемонстрировано 0,2M и ниже) по сравнению с концентрированным гидроксидом, обычно получаемым при производстве хлора и щелочи (обычно 33-35% по массе, затем концентрируют дополнительно с помощью выпарки), конструкция электролизеров для получения хлора щелочи для эксплуатации при низкой концентрации (а также эксплуатации при низком напряжении) может обеспечивать новые степени свободы для оптимизации конструкции при этих нестандартных условиях.
Варианты осуществления настоящего изобретения неспособны получать больше энергии водорода, чем энергия, пошедшая на получение этого водорода. В противном случае результатом будет нарушение второго закона термодинамики. Это накладывает ограничение на минимальное напряжение, которое может быть приложено к электролизеру. Предполагая 100% эффективность при возврате водорода и используя энергосодержание 39000 кВч/тонна H2 (справочное значение Службы энергетической информации, EIA, США), для минимального напряжения можно получить значение 1,55 В. Специалист в этой области может для любой системы с данной эффективностью возврата водород/электричество и выбранным значением для энергосодержанием системы рассчитать минимально достигаемое напряжение для этой системы.
На практике, термодинамические неэффективности (включая, но этим не ограничивая, I2R потери, неэффективное использование тока в электролизере, потери отходящего тепла и так далее) и требование небольшого перенапряжения для эксплуатации повышает минимальное напряжение, достижимое для данного электролизера. Вышеприведенные цифры изменяются слабо в зависимости от величины "a," степени протонирования, хотя она изменяет количество водорода, доступного для рекуперации энергии.
При этом плотность тока при низком напряжении определяет величину площадей электролиза (сильно влияющих на капитальные затраты), требуемых для производства количества каустика, и при минимальном напряжении требуемая площадь является чрезвычайно большой. Следовательно, для эксплуатации требуется некоторое напряжение выше минимального напряжения, величина, выбираемая при проектировании в зависимости от компромисса капитальные затраты/экологическая эффективность. Выход по току (доля тока, потраченная на производство продукта) падает при низком напряжении, поэтому оптимизация эксплуатации электролиза при низком напряжении не является тем же самым, что и достижение условия эксплуатации только при низком напряжении. Действующие процессы проектируют для эксплуатации при НВЭ режиме (ниже 5 В) и при этих напряжениях ниже 5 в расход электроэнергии относительно традиционных методов значительно увеличивается.
Пример 5
Термодинамика проектирования крупномасштабной установки
Для этого примера описана модельная установка (включающая конкретные варианты осуществления настоящего изобретения), характеризующаяся режимом для полномасштабной работающей установки, и определяется количественно энергия, необходимая для извлечения данного количества CO2, которая ограничивается внутри статистических пределов различными средствами и методами, включая следующие:
(1) Термодинамическая эффективность (∂CO2/∂E) может быть аппроксимирована как ΔCO2/ΔE для достаточно коротких интервалов изменений E (энергий).
(2) Определенные упрощающие допущения могут быть сделаны относительно проектирования установки, такие как представленные на фиг.9A, среди них:
a) Основное расходование энергии происходит в процессе электролиза; расход энергии на перекачивание, сжатие, регулирование и так далее считают минимальным относительно затрачиваемой энергии на получение реагентов (электролиз) и при рекуперации энергии водорода. Эти величины принимают равными нулю или <0,1% от энергии, потребляемой в операциях электролиза.
b) Потребляемая электролизом энергия может быть представлена приблизительно следующим уравнением:
Eout=V*I*EFFcurrent,
где V=напряжение на работающем электролизере,
I=ток, необходимый для получения химических продуктов электрохимической полуреакцией, включая больше чем 1:1 стехиометрию, вызванную протонированием рассола. В примере используется 0,05 HCl/NaCl отношение протонирующих ионов, потребляемых в электролизе.
EFFcurrent=выход по току, определяемый количеством тока, использованного в фактическом получении химических соединений, причем остаток теряют с I2R потерями и так далее. Величиной, используемой в примере, является 97%; каждый электролизер имеет свой собственный уникальный выход по току, который понижается и изменяется в течение срока службы электролизера.
c) Энергия, извлекаемая при сжигании водорода (независимо от того каким образом, сжигание в виде котельного газа, сжигание в топливном элементе и так далее), выражается как:
Ein=39000 кВт·ч/тонна сжатого H2*тонну H2*EFFdc,
где тонны H2=тонны водорода, полученные при помощи процесса, включая водород, полученный при стехиометрии более чем 1:1, вызванной протонированием рассола.
EFFdc=эффективность процесса извлечения водорода при превращении начальной энергии газообразного водорода в постоянный электрический ток. 60% произведенной энергии водорода извлекается в постоянный ток. Это является эффективностью по готовому к использованию постоянному току топливных элементов водород/атмосферный кислород; аналогичное значение получают для процесса сжатия водорода (стоимость которого составляет 15% его энергии для осуществления) и затем, полагая, что 85% энергии водорода возвращается в процессах, потребляющих водород, таких как процессы гидрирования, процессы реформинга бензина и так далее.
d) Возвращаемую энергию из утилизации отходящего тепла извлекали из тепла входящего потока топочного газа. Входящие нагретые газы охлаждают при их поступлении в процесс. В некоторых вариантах осуществления изобретения это охлаждение может быть осуществлено путем абсорбции отходящего тепла и превращения этого тепла в постоянный электрический ток, который может быть использован для того, чтобы дополнить/полностью обеспечить энергию/повысить энергию процесса, который составляет изобретение. В этом примере дополнительная утилизация отходящего тепла не предусмотрена.
Модель установки для этого примера включает моделирование топочного газа, выходящего из энергоустановки при нормальном рабочем режиме, как показано на фиг.9B. Это включает значительные допущения относительно состава топлив, эффективности самих процессов сжигания, относительную пропорцию элементов в процессах сжигания и так далее. Допущения для этого примера приведены на фиг.9B и они соответствуют выходу топочного газа типичной энергоустановки, работающей на буром угле с тепловой мощностью 10000 BTU/кВт·ч.
Для данного выхода топочного газа необходим гидроксид, потребность в котором может быть вычислена. Здесь следует ввести несколько допущений. Отношение ионов ("ионное отношение" является отношением Na/C в абсорбции/реакции конверсии) является таким же, как и отношение этих элементов в образующихся твердых продуктах. В случае чистого бикарбоната величина будет равна 1,0, в случае чистого карбоната величина будет равна 2,0, и для смесей бикарбоната и карбоната величина будет лежать между 1,0 и 2,0. Вычисление потребности в щелочи для этого примера приведено на фиг.9C. Для примера, приведенного на фиг.9C, ионное отношение составляет 1,0.
Для данной потребности в гидроксиде существует соответствующие потребности при электролизе, основанные на количестве воды, соли, квадратных метров площади поверхности мембраны (скалярная величина для электролизеров этого рода) и плотности тока (сама по себе является функцией конструкции электролизера, химизма процесса и условий эксплуатации; здесь используется показатель 3 кA/м2). Эти вычисления потребностей при электролизе для этого примера приведены на фиг.9D.
Для данного количества тока электролиза при условиях протонирования образуется данное количество газообразного водорода, который сам по себе представляет количество энергии, доступной для извлечения, или водород используют химически в других технологиях. В этом примере водород превращают в постоянный ток, используя топливный элемент, работающий при EFFdc=60%.
Для данного количества перерабатываемого топочного газа имеется определенное содержание отходящего тепла, которое может быть извлечено из него при определенной эффективности конверсии в постоянный ток, и это извлекаемое электричество может быть использовано для того, чтобы дополнять постоянный ток, потребляемый в электролизе. Отходящее тепло для этого примера приведено на фиг.9E, с эффективностью, выбранной в этом случае равной 25%, величиной, которую превышают различные методы получения постоянного тока из отходящего тепла, существующие в настоящее время в этой области.
Приведенные здесь индивидуальные компоненты ввода и вывода энергии, результирующий эффект этих переносов энергии может быть суммирован, как на фиг.9F. Здесь, энергии представлены в кВт-часах и в качестве процентов от мощности основной установки, и показано вычисление экологической эффективности для этого примера.
В некоторых вариантах осуществления настоящего изобретения, дополнительный H2/Cl2 топливный элемент может быть использован для сжигания газообразных водорода и хлора с целью возврата HCl, используемой для протонирования рассола. В частности, может быть рециркулировано "сверхстехиометрическое" количество HCl, и теоретически, может быть устранена необходимость в запасе HCl, добавляемой в систему. В реальной практике, определенное количество подпитывающей HCl должно периодически добавляться в систему. Сжигание H2 в Cl2 дает больше энергии, чем сжигание H2/O2. Таким образом получается небольшое количество дополнительной энергии. Однако топливные элементы не являются по своей природе абсолютно эффективными, поэтому "выигрыш" в энергии от использования хлора в качестве окислителя более чем перекрывается потерями, присущими методу извлечения. Следовательно, в этом примере считают, что эти эффекты взаимно уничтожаются и сводятся к нулю. Поэтому два эффекта в некоторой степени компенсируют друг друга, но, однако, приводят к общим потерям. Однако эффект присутствия дополнительных протонов при электролизе должен резко катализировать получение NaOH при низких напряжениях и приводить к высокому значению (кA/м2·В) при этих низких напряжениях. Следовательно, для любой данной установки может быть проведена оптимизация переработки данного количества H2/Cl2 в HCl и протонирования входящего рассола этим количеством HCl. При некотором оптимальном значении (которое обычно находится между a=0,05 и a=1,0 M, или около pH 1 при 90°C) потери топливного элемента водород/хлор (которые превосходят небольшой выигрыш, обеспечиваемый хлором по сравнению с окислением кислородом) и выигрыши в энергии для гидроксида (лучшее значение кA/м2·В) будут одновременно оптимальными для всей системы. Следует отметить, что в этом примере рассчитано только сжигание H2/O2; сжигание H2/Cl2 имеет небольшой термодинамический выигрыш из-за более высокой интенсивности окисления хлором, но противодействующий эффект неэффективности топливного элемента способствует слегка отрицательному, но рассматриваемому как минимальному эффекту.
A. Вычисление экологической эффективности
Вычисление экологической эффективности (∂CO2/∂E) и ΔCO2/ΔE для этого примера было осуществлено следующим образом:
(1) Было предположено, что имеется три установки:
a) Основная энергетическая установка (приведенная в качестве примера в модели отходящего газа на фиг.9B).
b) Установка абсорбции/конверсии CO2 (которая требует дополнительной энергии для переработки топочного газа из основной энергетической установки и возвращает часть этой энергии путем сжигания водорода или за счет рассчитанной энергии водорода, если водород является конечным продуктом и его не сжигают).
c) Третья дополнительная энергетическая установка, которая обеспечивает энергию, необходимую для установки абсорбции/конверсии CO2. В этом примере предполагалось, что характеристики этой энергетической установки являются такими же, как и у основной установки.
(2) Следующие аспекты, относящиеся к CO2 и израсходованной энергии при переработке 100% основной энергетической установки, были затем вычислены:
a) CO2 из основной установки (модель топочного газа).
b) Энергия, производимая основной установкой.
c) Чистая затрата энергии, потребляемой процессом абсорбции/конверсии CO2.
d) Чистая затрата энергии, потребляемой дополнительной энергетической установкой, предполагается такой же, как и чистая затрата энергии, потребляемой процессом абсорбции/конверсии CO2.
e) Предполагается, что CO2, производимый дополнительной установкой, пропорционален энергии, производимой дополнительной установкой, и с такими же ΔCO2/ΔE, как и для основной установки.
(3) Следующие результаты для выше приведенных вычислений были получены:
a) Основная установка - установка с тепловой мощностью 10000, производящая 1 ГВт непрерывно в течение одного года в качестве базиса, производит 8,76 гигаватт-час каждый год и производит в качестве базиса 7446068 тонн CO2 в год, в среднем 1176 кВт-час/тонна CO2.
b) Установка абсорбции/конверсии CO2 - для этого примера вычисления (a=0,10, режим 2,1 В, производится чистый бикарбонат, 15% энергии водорода потребляется для сжатия, затраты на перекачивание/сжатие и преимущества утилизации отходящего тепла не учитываются), 3,648 гигаватт-час требуется для абсорбции/конверсии 100% основной установки.
c) Дополнительная энергетическая установка - установка в этом примере производит энергию, потребляемую установкой абсорбции/конверсии CO2, 3,648 гигаватт-час, и сама производит (исходя из выше указанной величины 1176 кВт-час/тонна CO2) суммарно 3101209 тонн CO2, которые, как предполагается, выбрасываются в атмосферу.
d) Суммарная генерируемая энергия составляет следовательно 12,48 гигаватт-час. Суммарная поставляемая энергия составляет следовательно, 8,76 гигаватт-час. Суммарный генерируемый CO2 составляет, следовательно, 10,55 мегатонн. Суммарный выброс CO2 составляет, следовательно, 3,101 мегатонны. 29,1% суммарной энергии потребляется в процессе абсорбции/конверсии CO2. Потребляется 71,9% суммарного CO2.
Несколько ключевых точек иллюстрируются вышеприведенными вычислениями:
(1) Арифметически продемонстрировано, что могут быть использованы следующие формулы:
% потребленной энергии = 1-% потребленного CO2
% потребленного CO2 = 1-% потребленной энергии
Это образует рабочую линию, называемую единой рабочей линией, приведенной на фиг.9A.
(2) Для этого примера (∂CO2/∂E) и ΔCO2/ΔE алгебраически идентичны, а именно:
ΔCO2/ΔE=(∂CO2/∂E)=0,291/0,719=0,41
Далее могут быть дополнительно смоделированы экстраполированные случаи, в которых, CO2, выбрасываемый дополнительной энергетической установкой, сам подвергается процессу абсорбции/конверсии СO2 в другой установке #2 соответственно меньшей мощности, и эта установка #2 абсорбции/конверсии соответственно снабжается энергией с дополнительной энергетической установки #2 и так далее, что приводит к таким результатам, как в таблице 2 для первых пяти серий итераций.
установка
CO2
(мегатонн)
энергию
(кВт-час)
подводимая
энергия
установка
CO2
эффективность
(∂CO2/∂E)
Несколько точек, касающихся таблицы 2, являются важными для модели:
(1) Следует отметить, что эффективность процесса, или в случае базиса, или в любых случаях последовательных итераций, постоянно дают одно и то же значение (∂CO2/∂E) для системы; этот показатель считают постоянным для систем, которые аппроксимируют ограничения этой модели, и его называют для этих целей экологической эффективностью процесса.
(2) Ясно, что значение (∂CO2/∂E) является постоянным для всех решений, поэтому решение может быть получено, когда число итераций предполагают бесконечным; то есть, когда установка эксплуатируется так, что потребляет 100% CO2, произведенных установкой, путем просто использования следующего уравнения:
1/(∂CO2/∂E)=% мощности установки, требуемой для абсорбции/захвата 100% произведенного CO2
В случае примера, вычисление приводит к величине 41,6%.
(3) С другой стороны, очевидно, что когда полезная мощность, израсходованная на абсорбцию/конверсию, равна нулю (пренебрегая утилизацией отходящего тепла), для данного условия процесса, абсорбированный и конвертированный CO2 также равен нулю. Следовательно, все рабочие линии для установок этого типа теоретически пересекаются в точке (0% энергии, 0% CO2).
(4) Для данных любых двух точек в линейной системе могут быть построены прямолинейные решения для рабочих линий, которые определяют рабочие характеристики процесса абсорбции/конверсии CO2 с помощью следующих методов:
a) для каждого рабочего условия проводят решение базисного случая, и полученную точку решения единого случая (% энергии, % CO2) наносят на зависимость % CO2 (ось y) от % потребленной полезной мощности (ось x);
b) для этого случая вычисляют (∂CO2/∂E) и решают для х-координаты случай при y=100%; и
c) полагают, что все линии проходят через начало координат. В реальных системах может быть некоторое потребление энергии (регулирование, окружающая среда и так далее) даже при нулевой абсорбции, поэтому этот случай является идеализированным. На практике эти линии могут быть слегка искривлены и не выходят из начала координат.
(5) Таким образом, может быть создано семейство рабочих линий для процессов абсорбции/конверсии CO2 этого типа.
(6) На таком же типе графика могут быть также нанесены и сравнены графически конкурирующие технологии, например:
a) Конкурирующая технология абсорбции с помощью МЭА (метилэтиламина) потребляет 30% мощности установки для осуществления абсорбции 58% CO2, выбрасываемого до того, как была применена абсорбция.
b) Кроме того, оцененные 15% мощности установки расходуются на сжижение этого CO2 в результате применения сверхвысокого давления и холодильного цикла (45% мощности/58% CO2).
c) Далее это дало бы значение для (∂CO2/∂E), равное 1,24; однако есть неучтенная энергия, требующаяся для транспортировки/закачки/содержания CO2 в месте секвестра углерода.
d) Графически показано, что эта конкурирующая технология является менее эффективной, чем пример установки абсорбции/конверсии CO2, использующий способ, который является одним вариантом осуществления изобретения; то есть эта модель показывает, что конкурирующая технология потребовала бы 70%+ энергии установки для удаления 100% вырабатываемого ею CO2. Следует обратить внимание на эти точки в отношении конкурирующей технологии, представленные графически на фиг.9A (в соответствии с надписями на диаграмме).
i) Согласно 2005 EIA оценкам, абсорбция CO2 с помощью технологии с МЭА требует 30% энергии установки для абсорбции 58% CO2 из производимого топочного газа. (Обращает внимание положение на диаграмме на фиг.9A (30%, 58%) только для абсорбции-переработки).
ii) Путем аналогичных оценок, сжатие/сжижение этого CO2 потребляет еще 15% мощности установки, сдвигая рабочую точку такой установки к значению (45%, 58%).
iii) Нет достоверной оценки ни для энергии, требуемой для транспортировки жидкого CO2 по трубопроводу или с помощью других средств транспортировки, ни для количества энергии, необходимой для перекачки или закачки этого CO2 в хранилище углерода различной природы, ни для количества энергии, которая может потребоваться для вечного хранения CO2 в указанных хранилищах. Однако, несмотря на то, что эти дополнительные энергии не поддаются оценке, по-видимому, разумно предположить, что они не равняются нулю. Следовательно, экологическая эффективность такого способа логически хуже, чем (45%/58%) компромисс в энергия-расход для обеспечения определенного преимущества при снижении CО2. Экстраполируя это до случая 100% удаления СО2, способ МЭА/сжижение/захоронение потребовал более чем 70% энергии установки. Следует отметить, что типичные конкурирующие абсорбционные технологии не могут достигать 100% абсорбции; то есть величина 58% CO2 абсорбции была для установки, которая подвергала обработке 100% выходящего топочного газа.
B. Вычисление пределов экологической эффективности [(∂CO2/∂E)max]
На практике, для данной системы, которая эффективно превращает весь произведенный NaOH в NaHCO3 в результате абсорбции CO2, главной составляющей энергии является кВт-ч/моль NaOH. Несмотря на то, что энергия на моль NaOH является пропорциональной как напряжению, так и току, ток устанавливается стехиометрией химии. Таким образом, энергию, расходуемую на моль CO2, первично оптимизируют путем достижения условия наименьшего напряжения, при котором эффективно получают гидроксид.
Минимальное напряжение, при котором электролизная система согласно вариантам осуществления настоящего изобретения работает (формируемая изменяющимися концентрациями, геометрическими размерами, расходами потоков и так далее), может быть определено путем наблюдения плотности тока (kA/м2) от V характеристик системы и определения наименьшего напряжения, при котором достаточные, ненулевые плотности тока получают при производстве продукта. Изменение физических размеров, устройств генерации электрического поля, размеров электролизера, состава материалов и технологических режимов для оптимизации этого характеристического показателя (kA2/м2В) является главным методом для оптимизации этих систем, и для оптимизации промышленного процесса для данной физической установки используют типичные методы планирования эксперимента.
Оставив в стороне ограничения практического характера, есть одно фундаментальное ограничение, которое будет применимо ко всем системам с данным отношением H/Na (степенью протонирования), а именно:
(1) Никакое устройство не может работать, если оно производит больше энергии в результате извлечения энергии водорода, чем вводится в систему для электролиза. Для тех, кто знаком с принципами термодинамики, это будет означать "нарушение второго закона".
(2) В результате этого факта фундаментальный термодинамический предел может служить границей, задаваясь выбором отношения H/Na, используемым в расходе анолита:
a) Для этого предела предполагалось, что H/Na составляло 0,10.
b) Устанавливали эффективность возврата энергии водорода равной 100%.
c) Вычисляли самое низкое напряжение, при котором может идти процесс, в котором результирующие затраты энергии, потребляемой системой, равна нулю ("Vmintheo") (то есть точка, в которой затраты на электролиз равны предполагаемой 100% эффективности возврата водорода).
d) В этом примере это низкое напряжение составляет 1,5526 В. Это число сильно зависит от отношения Na/C, отношения H/C и эффективности возврата энергии водорода. В этом оптимальном случае Na/C равняется 1,0 и H/C равняется 1,0.
e) Доводя это вычисление прямо к экологической эффективности, единственным решением является приблизительно 7% мощности для 93% абсорбции/конверсии CO2.
f) Эксплуатация в более эффективных рабочих точках, чем этот теоретический минимум, возможна за счет:
i) пополнения расхода энергии за счет утилизации отходящего тепла; и
ii) энергоснабжения процесса абсорбции/конверсии или частично или полностью за счет энергии, производство которой не приводит к выбросу CO2 (гидроэлектрической, солнечной, ветряной, ядерной и так далее).
Аналогично, предполагая идеальную эффективность возврата энергии водорода, и так далее как в вышеприведенном случае, рассчитывали максимальное напряжения, при котором эксплуатация может быть "экологической" ("Vmaxeco") (то есть при котором процесс абсорбции/конверсии CO2 удаляет больше CO2, чем он его создает):
a) Отношения H/Na, Na/C и эффективность возврата энергии водорода устанавливали 1,0, 1,0, и 100% соответственно, как в вышеприведенном случае.
b) Рассчитывали напряжение, при котором удаление CO2 составляло бы 50%.
c) В этом примере это значение Vmaxeco составляет 4,457 В. При этом напряжении и условии процесс идет по линии ∂CO2=∂E, границе между экологически благоприятной и экологически опасной эксплуатацией.
Следовательно, экологически благоприятная эксплуатация будет осуществляться тогда, когда электролизная система эксплуатируется между Vmintheo (1,5526 В) и Vmaxeco (4,457 В). Эксплуатация между этими двумя точками может быть воспроизведена во многих типичных электролизных системах. Лабораторные результаты при напряжении, равном или ниже 2,1, в могут быть легко воспроизведены путем изменения размеров, концентрации, температуры, давления, скорости потока, и так далее, электролизеров, спроектированных таким образом.
C. Влияние энергии, получаемой без парникового эффекта, на экологическую эффективность
Когда дополнительная энергия (которая снабжает энергией способ) обеспечивается за счет энергии, производимой без выбросов парникового газа (ПГ) {например, энергии ветра, гидроэлектрической, солнечной, ядерной и так далее), тогда выбросы дополнительного CO2 равны нулю и экологическая эффективность настоящего изобретения значительно улучшается. Для этого примера, удаляют величину 3101209 тонн CO2 в таблице 2 в ходе всех последующих итераций и так далее, получая этот упрощенный результат: весь CO2 абсорбирован/конвертирован (7446069 тонн), и суммарная требуемая энергия составляет просто 8760000000 базис плюс 3648448267 кВт·ч, требуемых для выполнения работы, необходимой для абсорбции/конвертирования этого базисного количества CO2, требуя при этом только 29% от суммарной энергии для обеспечения 100% CO2 выбросов в способе, снабжаемом энергией с выбросом непарниковых газов, по сравнению с 41% от суммарной энергии для обеспечения 100% CO2 выбросов в способе, снабжаемом энергией с выбросом парниковых газов. Это означает, что варианты осуществления настоящего изобретения обеспечивают значительный фактор "рычага", когда процесс снабжают энергией, получаемой без выбросов парниковых газов. Вместо того чтобы использовать энергию, получаемую без выброса парниковых газов, для замены энергии, генерирующей выброс парниковых газов, на основе 1%:1%, если энергию, получаемую без выбросов парниковых газов, используют взамен для энергоснабжения процессов, которые являются некоторыми вариантами осуществления настоящего изобретения, 1% энергии, получаемый без выбросов парниковых газов, затем предотвращает образование парниковых газов в количестве, возведенном в степень, даже больше, чем в описанных здесь примерах энергии, получаемой с образованием парниковых газов. Можно легко представить случаи, в которых данная нация, государство или хозяйствующий субъект с помощью определенной части энергии, получаемой без выброса парниковых газов, при использовании таким замечательным образом, могла бы более эффективно достигать любую цель снижения CO2; то есть можно использовать в очень действенной манере "чистую" энергию для очистки выбросов другой "грязной энергии".
Если в некоторых применениях доступно получение энергии без образования парниковых газов, иногда в спорадических формах (например, солнечной, "ветроэнергоцентров" и так далее) является чрезвычайно выгодной возможность утилизировать эту энергию, чтобы произвести большие количества абсорбента во время периодов неполной нагрузки.
Пример 6
Экологическая эффективность различных моделируемых энергетических установок
На фиг.10 приведена экологическая эффективность различных моделируемых энергетических установок, включающих варианты осуществления настоящего изобретения, и представлены различные условия, которые являются главными факторами при определении экологической эффективности, (∂CO2/∂E).
Из этих вычислений можно в целом придти к выводу, что:
(1) В случае образования карбоната натрия и использования стандартных условий производства хлора и щелочи, способ имел бы экологическую эффективность >1, и, несмотря на то, что такая эксплуатация может быть экономически приемлема, он производит больше CO2, чем его абсорбирует.
(2) Изменение продуктового равновесия в пользу получения бикарбоната натрия повышает экологическую эффективность способа. В случае изменения условий так, чтобы производить фактически чистый бикарбонат натрия, это преимущество полностью оптимизировано.
(3) Внедрение технологии электролиза с низким напряжением сильно сдвигает способ в рабочую область, характеризующуюся экологическими эффективностями ниже, чем 1,0 (то есть экологически выгодные процессы абсорбции и конверсии CO2). Оптимизация каждой физической модели электролизной системы для оптимума (kA/m2В) и максимума производства энергии водорода приводит к дополнительному улучшению экологической эффективности.
(4) Сочетание процесса абсорбции/конверсии вариантов осуществлений настоящего изобретения с любым числом доступных или специально созданных агрегатов, которые конвертируют отходящее тепло в постоянный электрический ток, первоначальные энергетические капиталовложения в электролиз при постоянном токе и в перекачку при переменном токе и так далее может быть дополнительным или полностью осуществлять за счет утилизации отходящего тепла.
Следует отметить, что обеспечение изобретения энергией из источников энергии, получаемых без выбросов парниковых газов, позволяет способу непосредственно достигать 100% абсорбции CO2 (см. обсуждение в примере 5).
Пример 7
Определение Voptlve (оптимальная эксплуатация при низком напряжении относительно производительности электролизера или его площади) и Ioptlve (ток при рабочем напряжении) при данной V/I характеристической рабочей линии для оптимизированного НВЭ электролизера хлор-щелочь
Здесь было показано, что эксплуатация при низком напряжении понижает энергию, требуемую для производства гидроксида натрия, который используют в качестве жидкого абсорбента. В таблице 3 приведены вычисления, сделанные для VI рабочей линии в случае анолита с рН 1,0/90°C на фиг.5 (обсужденной выше в примере 4).
Следует отметить несколько точек, касающихся содержания таблицы 3:
(1) Третья колонка, выход по току (безразмерный) представляет часть генерируемого тока, который используют в производстве химических продуктов; потери, такие как I2R потери и отходящее тепло электролитических жидкостей, являются главной причиной потерь энергий. Выход по току падает с падением напряжения.
(2) Площадь электролизера нормализуется для случая напряжения 3,975 В (где плотность тока и, следовательно, потребность процесса в площади является идентичной стандартному 5 в электролизу, работающему с характеристикой 3,0 kA/m2). Вычисляют A2/A1 (безразмерное).
Последний показатель, % сэкономленной энергии на безразмерную площадь, приведен в виде графика на фиг.11. Для такой функции точка, при которой максимальный наклон (изменение в использовании энергии на изменение напряжения) представляет оптимум; то есть при низком напряжении (например, 2,1-2,5 В) наклон (Δ энергия/Δ м2) является относительно малым, затем при более высоких напряжениях (например, от 2,5 до приблизительно 3), наклон (Δ энергия/Δ м2) увеличивается до большей величины, и затем падает до меньших наклонов по мере того, как напряжение продолжает возрастать. Это иллюстрирует то, что есть область больших наклонов, ограниченная областью малых наклонов с каждой стороны; то есть по обе стороны от точки Voptlve изменение в использовании энергии на изменение напряжения является менее эффективным.
Сначала была получена функция, которая весьма близко аппроксимирует поведение при эксплуатации (обратите внимание на формулу линии полиномиального тренда, полученную методом наименьших квадратов). В этом примере: y=-10,164x3+88,256x2-235,06x+198,37 является достаточно хорошим приближением. Затем вычисляли первую производную функции путем типичного разложения многочленов: dy/dx=(3)(-10,164)x2+(2)(88,256)x-235,06=max. Значения x (Volts) могут быть итерированы для нахождения максимума этой первой производной, которое может быть осуществлено различными методиками, давая в качестве решения 2,894 В.
Заметьте, что могут быть использованы напряжения ниже, чем 2,894 В, и в результате получены дополнительные экономии энергии. Некоторые предпочтительные варианты осуществления будут оптимизировать эксплуатацию при низкой энергии ниже этой "естественной оптимальной точки". В этих случаях дополнительная площадь используемой мембраны приведет к "частично оптимизированной" электролизной системе, но эксплуатация при низкой энергии для суммарного процесса декарбонизации может быть дополнительно выгодной за счет эксплуатации ниже этого естественного оптимума для данной электролизной подсистемы. Однако если так делать, то преимущество напряжение/энергия после этого пропадает, при этом фактор площади продолжает пропорционально ухудшать эффективность эксплуатации на единицу площади.
Могут быть определены электрический ток и плотность тока, которые соответствуют этому Voptlve, или получена аналогичная зависимость для V и I с помощью метода наименьших квадратов, или графически, используя рабочую кривую для определения Ioptlve. В этом примере вычисленное значение равняется 10,419 A (или для 0,01 м2 площади электролизера, как в этом случае), 1,042 кA/м2.
Все способы и устройства, описанные здесь и приведенные в формуле изобретения, могут быть созданы и осуществлены в свете настоящего описания без дополнительного эксперимента. В процессе того, как способы и устройства этого изобретения раскрывались через предпочтительные варианты осуществления, для специалистов в этой области становилось бы очевидным, что описанные здесь способы и устройства, и стадии или последовательности стадий способа могут быть изменены без отклонения от идеи, сущности и объема изобретения. Более конкретно, становилось бы очевидным, что могут достигаться аналогичные результаты при замене описанных здесь композиций на родственные химические композиции. Предполагается, что все эти аналогичные замены и модификации, очевидные для специалистов в этой области, подпадают под сущность, объем и идею изобретения, определенные в прилагаемой формуле изобретения.
МАТЕРИАЛЫ, ИСПОЛЬЗОВАННЫЕ В ОПИСАНИИ
Следующие материалы, в той степени в которой они обеспечивают справочные данные или другие детали дополнительно к тем, которые представлены в описании, специально приводятся здесь путем ссылки на них.
"Annual Energy Outlook 2005 (AEO2005)," prepared by the Energy Information Administration, available through National Energy Information Center, EI-30, Washington, DC.
"Carbonate Chemistry for Sequestering Fossil Carbon," by Klaus S. Lackner, in Annual Review of Energy Environment, 2002, by Annual reviews.
"Effects of the Operating Pressure On The Performance of Electrolytic Cell at Elevated Temperatures," by Y. Ogata, M.Yasuda, and F.Hine, Nagoya Institute of Technology, Japan. In Proceedings of the Symposium on Electrochemical Engineering in the Chlor-Alkali and Chlorate Industries, The Electrochemical Society, 1988.
"Electrochemical Hydrogen Technologies - Electrochemical Production and Combustion of Hydrogen," edited by Hartmut Wendt, Institute fur Chemische Technologie, Stuttgart, Elsevier Press 1990.
"Electrochemical Process Engineering - A Guide to the Design of Electrolytic Plant," by F.Goodridge and K.Scott, University of Newcastle upon Tyne, 1995.
"Exergy Study of the Kalina Cycle," by Goran Wall, Chia-Chin Chuang, and Masaru Ishida, presented at 1989 American Society of Mechanical Engineers (ASME), Winter Annual Meeting, San Francisco, California, December 1989, published in "Analysis and Design of Energy Systems: Analysis of Industrial Processes AES Vol.10-3, pp 73-77 ASME.
"Industrial Electrochemistry," 2<nd> Edition, edited by Derek Plefcher and Frank Walsh, 1990.
"Modern Chlor-Alkali Technology," edited by M.O. Coultier, Society for the Chemical Industry, London, 1980.
"Modern Chlor-Alkali Technology," Volumes 1-7, The Royal Society of Chemistry Information Services, 1998.
"Some Guidelines for Analysis, Design, and Operational Principles of Bubble Column Reactors," and other selected information contained in "Bubble Column Reactors," by Wolf-Dieter Deckwer, Gesellschaft fur Biotechnologische Forschung mbH, Braunsweig, Germany, translated by Robert Field, 1991 ISBN 0-471-91811-3.
"Transport and Structure in Fuel Cell Proton Exchange Membranes," by Michael Anthony Hickner, dissertation submitted to the faculty of Virginia Polytechnic Institute and State University, 2003.
Figure 8. "CO2 Absorption vs. (Low) Interfacial Gas Velocity at Various Column Heights of 0.18M Sodium Hydroxide Solution in an Unpacked Sparged Bubble Column," from A. Schumpe thesis, University of Hanover, 1978.
Klara in: EIA Emissions of Greenhouse Gases in the U.S. 2000, EPGA 3rd Annual Power Generation Conference, Hershey PA, 2002.
Mandal, et al., J. Chem. Engineering (Canada), 81:212-219, 2003.
Shah et al, AiCHE J., 28(3):353-379, 1982.
Unit Operations of Chemical Engineering, McGraw-Hill, 3rd edition (c) 1976, "Gas Absorption" pp. 707-743, after Eckert.
Wie-rong et al, J. Zhejiang University Science, ISSN 1009-3095, 2004.
| название | год | авторы | номер документа |
|---|---|---|---|
| УДАЛЕНИЕ ДИОКСИДА УГЛЕРОДА ИЗ ПОТОКОВ ОТХОДОВ ПУТЕМ СОВМЕСТНОГО ПОЛУЧЕНИЯ КАРБОНАТНЫХ И/ИЛИ БИКАРБОНАТНЫХ МИНЕРАЛОВ | 2005 |
|
RU2569093C2 |
| УДАЛЕНИЕ ДИОКСИДА УГЛЕРОДА ИЗ ПОТОКОВ ОТХОДЯЩЕГО ГАЗА ПОСРЕДСТВОМ СОВМЕСТНОГО ОБРАЗОВАНИЯ КАРБОНАТНЫХ И/ИЛИ БИКАРБОНАТНЫХ МИНЕРАЛОВ | 2008 |
|
RU2477168C2 |
| СПОСОБ ОТДЕЛЕНИЯ ТЯЖЕЛЫХ МЕТАЛЛОВ ОТ ВОДЫ В КОНДЕНСАТЕ ДЫМОВЫХ ГАЗОВ | 2008 |
|
RU2531827C2 |
| СПОСОБ И УСТРОЙСТВО ДЛЯ УЛАВЛИВАНИЯ УГЛЕРОДА И УДАЛЕНИЯ МУЛЬТИЗАГРЯЗНЕНИЙ В ТОПОЧНОМ ГАЗЕ ИЗ ИСТОЧНИКОВ УГЛЕВОДОРОДНОГО ТОПЛИВА И ИЗВЛЕЧЕНИЯ МНОЖЕСТВЕННЫХ ПОБОЧНЫХ ПРОДУКТОВ | 2008 |
|
RU2461411C2 |
| Способ получения моногидрата гидроксида лития из рассолов | 2019 |
|
RU2713360C2 |
| СПОСОБ ПОЛУЧЕНИЯ КРИСТАЛЛОВ КАРБОНАТА НАТРИЯ | 2007 |
|
RU2466934C2 |
| Способ получения литиевого концентрата из литиеносных природных рассолов и его переработки в хлорид лития или карбонат лития | 2017 |
|
RU2659968C1 |
| СЕЛЕКТИВНОЕ КАТАЛИТИЧЕСКОЕ ВОССТАНОВЛЕНИЕ ПУТЕМ ЭЛЕКТРОЛИЗА МОЧЕВИНЫ | 2011 |
|
RU2538368C2 |
| Способ получения моногидрата гидроксида лития из рассолов и установка для его осуществления | 2016 |
|
RU2656452C2 |
| УСТАНОВКА АБСОРБЦИИ И ЭЛЕКТРОХИМИЧЕСКОЙ ДЕСОРБЦИИ УГЛЕКИСЛОГО ГАЗА | 2017 |
|
RU2654755C1 |
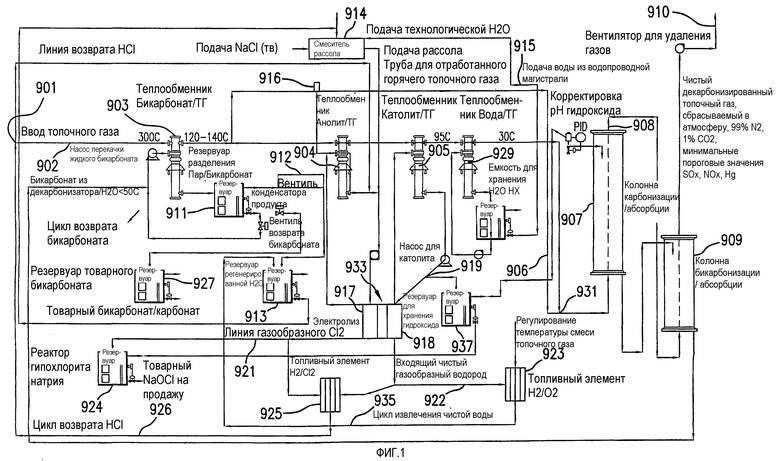
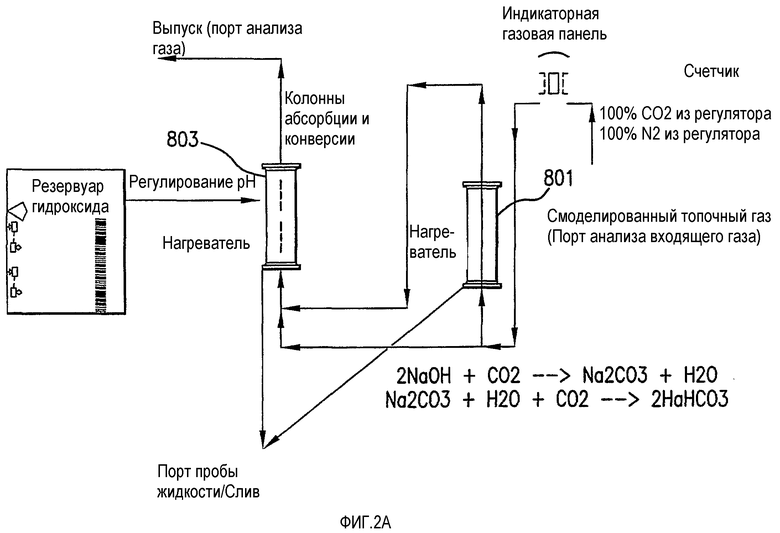
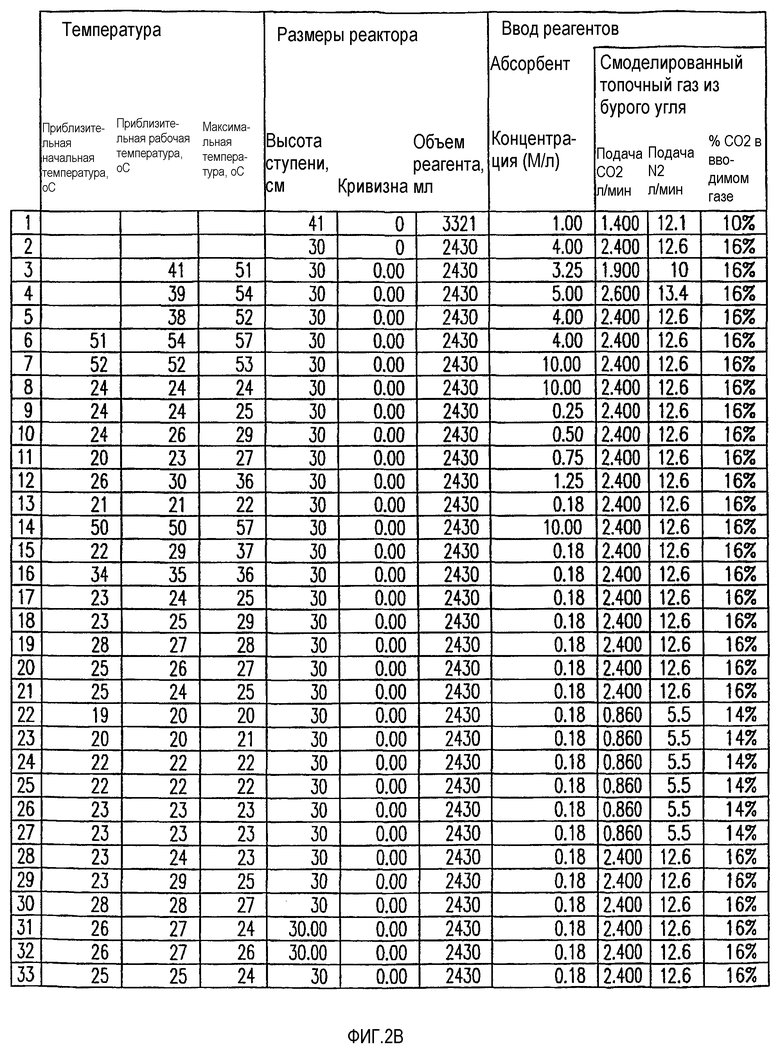
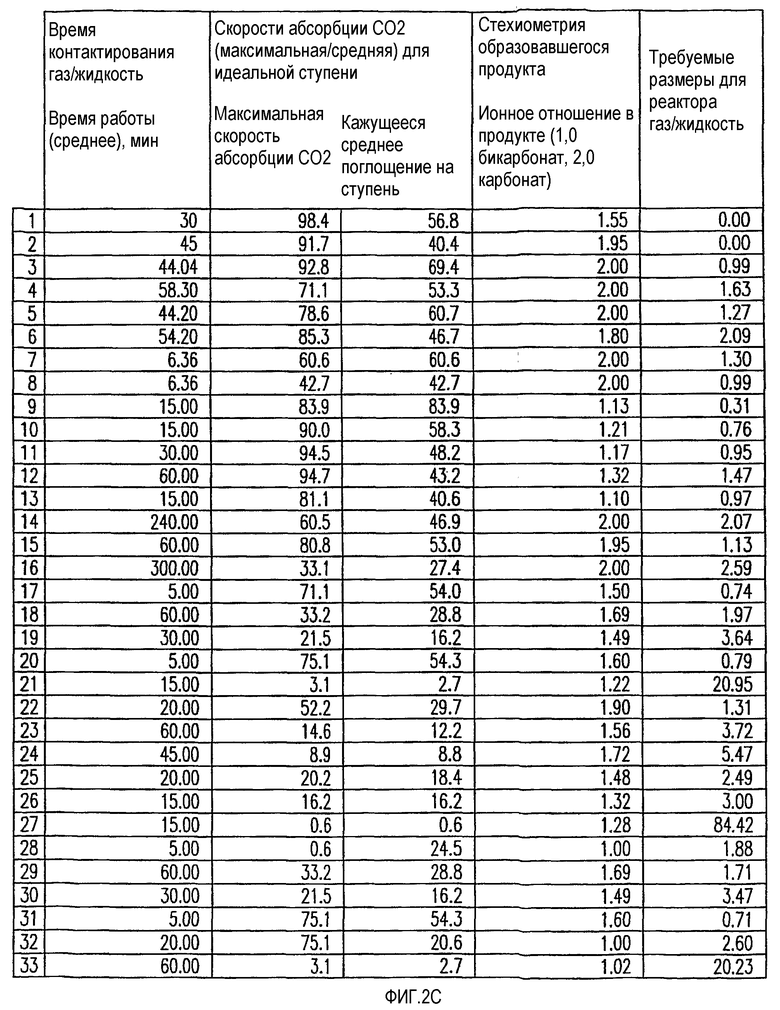
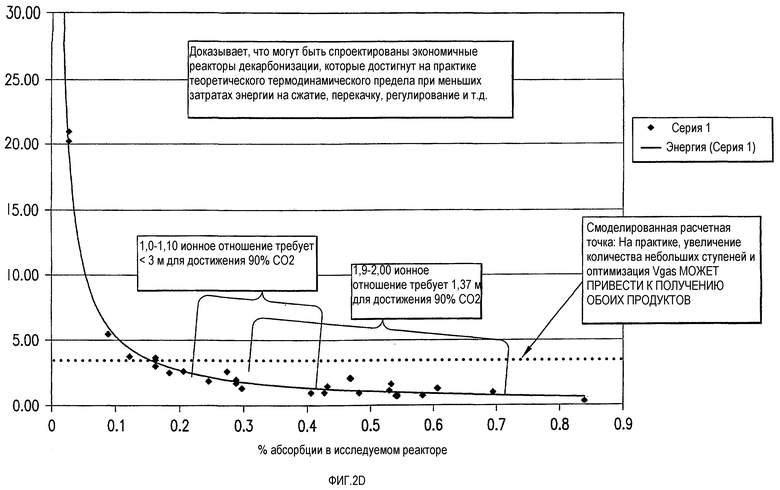
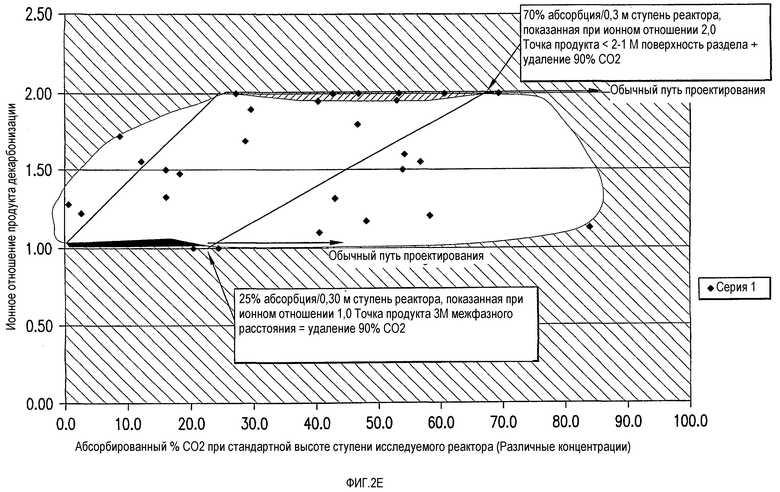

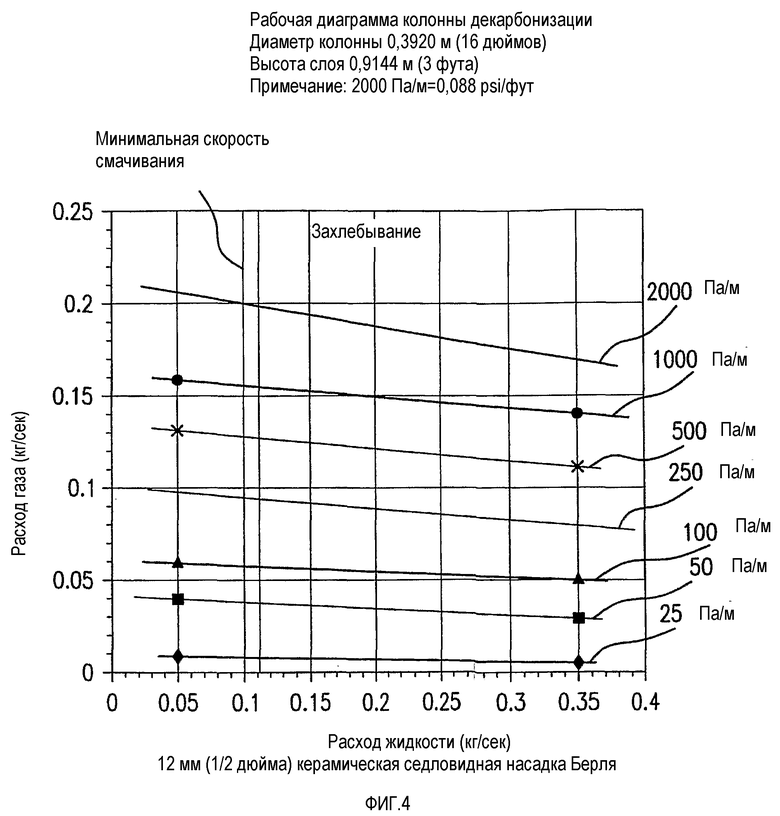
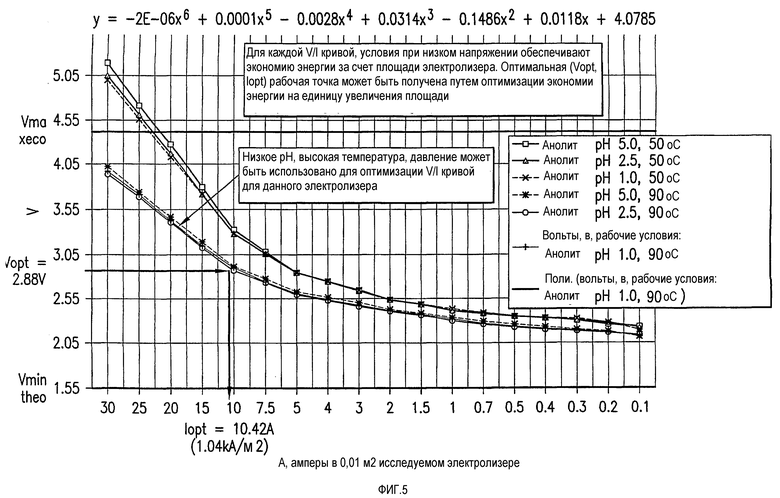

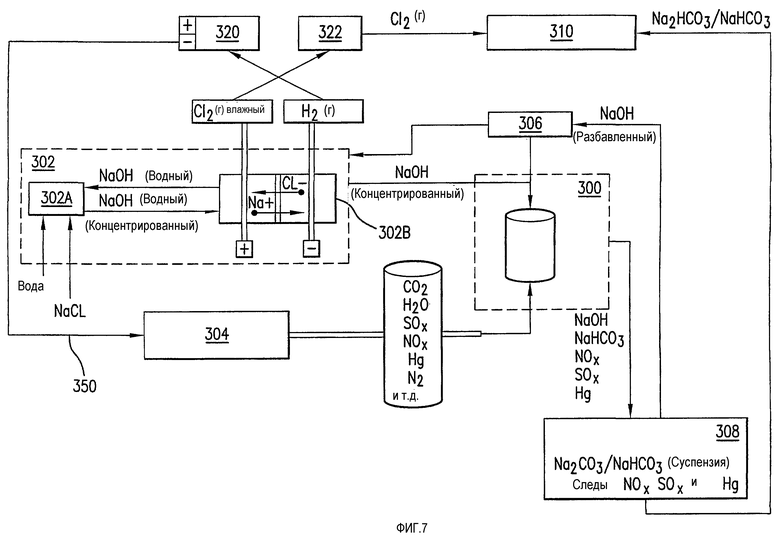
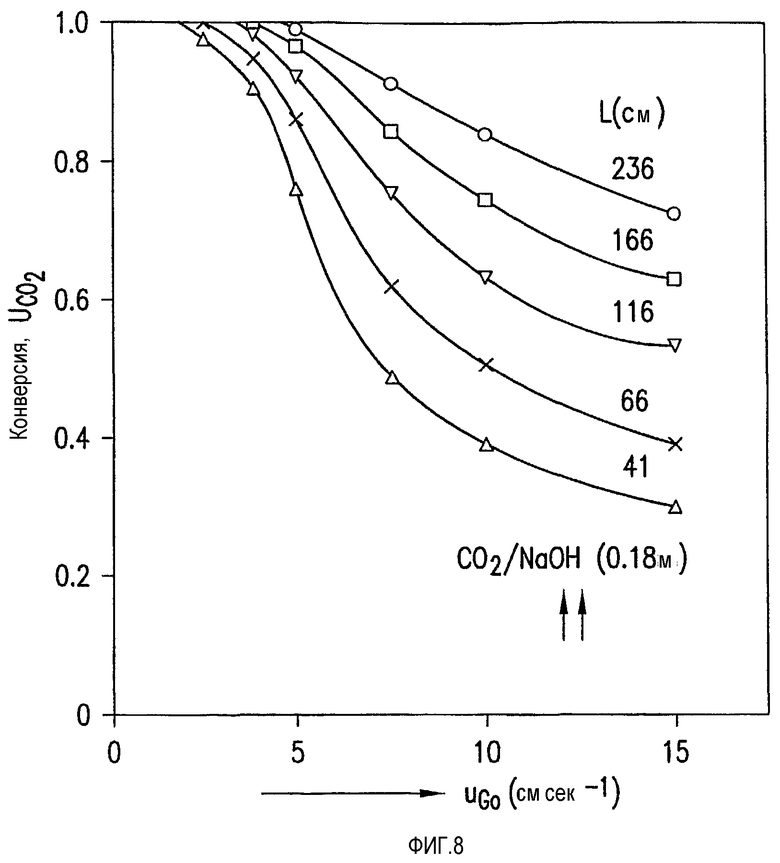



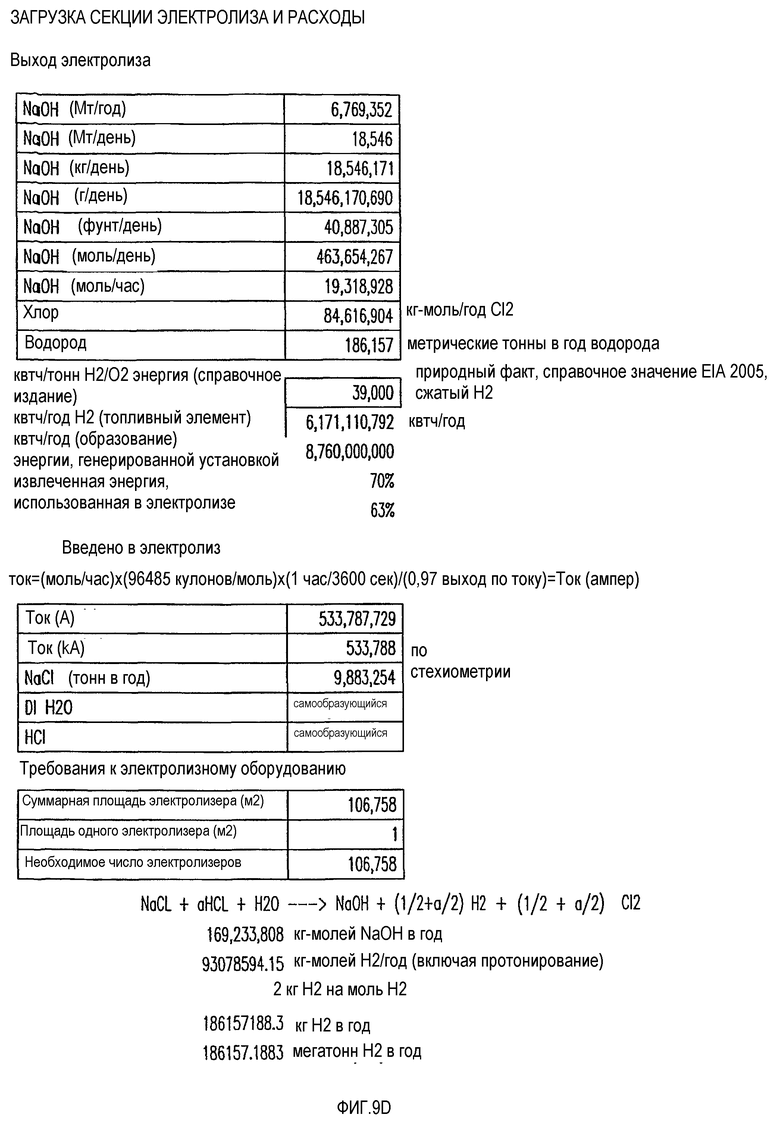



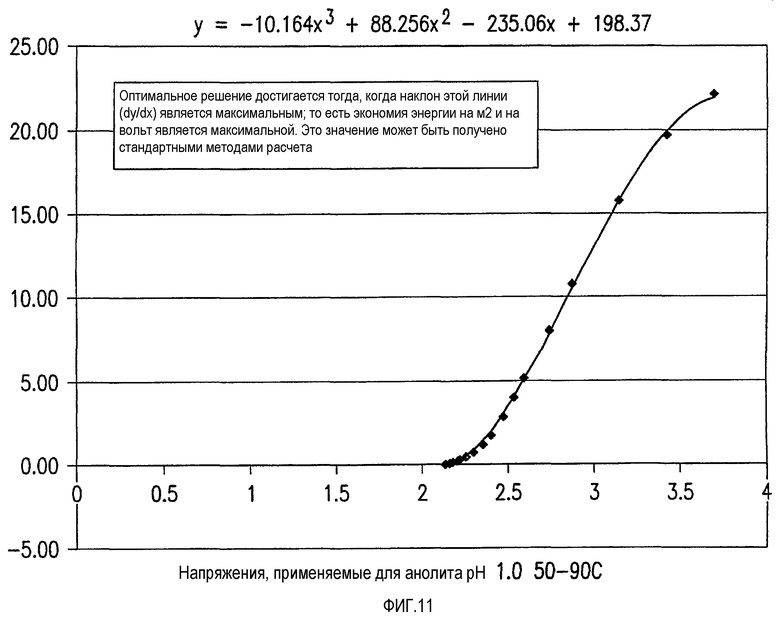
Предлагаются установки и способы для удаления диоксида углерода и других загрязняющих веществ из газового потока. Способы включают получение гидроксида в водной смеси и смешение гидроксида с газовым потоком с получением карбоната и/или бикарбоната при проведении процесса в двух раздельных камерах, где одну камеру используют для производства карбонатных продуктов, а другую камеру используют для производства бикарбонатных продуктов или смеси карбонатных и бикарбонатных продуктов. Установки настоящего изобретения включают электролизную камеру для получения гидроксида и смесительное оборудование для смешения гидроксида с газовым потоком, включающим диоксид углерода, с образованием смеси, включающей карбонат и/или бикарбонат. Предложенный способ обеспечивает эффективное извлечение диоксида углерода с одновременным извлечением других нежелательных примесей выпускаемых топочных газов, а также получение полезных побочных продуктов с одновременным потреблением энергии тепла топочных газов, извлекаемых из газового потока, что является техническим результатом изобретения. 3 н. и 37 з.п. ф-лы, 20 ил., 3 табл.
1. Способ удаления диоксида углерода из газового потока, включающий:
(a) получение гидроксида в водной смеси;
(b) смешение гидроксида с газовым потоком с получением карбонатных продуктов, бикарбонатных продуктов, или смеси карбонатных и бикарбонатных продуктов в смеси; и
(c) выделение указанных карбонатных и/или бикарбонатных продуктов из смеси, тем самым удаляя диоксид углерода из потока газа;
где смешение происходит в двух раздельных камерах, причем одну камеру используют для производства карбонатных продуктов, а другую камеру используют для производства бикарбонатных продуктов.
2. Способ по п.1, дополнительно включающий процесс регулирования способа получения практически только карбонатных продуктов, практически только бикарбонатных продуктов, или смеси карбонатных и бикарбонатных продуктов.
3. Способ по п.1 или 2, в котором получают смесь, включающую около пятидесяти процентов карбонатных продуктов и около пятидесяти процентов бикарбонатных продуктов, около двадцати пяти процентов карбонатных продуктов и около семидесяти пяти процентов бикарбонатных продуктов, или около семидесяти пяти процентов карбонатных продуктов и около двадцати пяти процентов бикарбонатных продуктов.
4. Способ по п.1 или 2, в котором смешение происходит в барботажной колонне или серии барботажных колонн.
5. Способ по п.1 или 2, в котором выделение карбонатных и/или бикарбонатных продуктов из смеси включает процесс выделения в результате горячего осаждения.
6. Способ по п.1 или 2, в котором тепло для процесса выделения получают в результате теплообмена с входящими топочными газами.
7. Способ по п.1 или 2, дополнительно включающий:
транспортировку карбонатных продуктов к удаленным местам секвестра;
объединение карбонатных продуктов с кислотой в реакции нейтрализации с получением чистого диоксида углерода; и
закачку диоксида углерода в хранилище углерода.
8. Способ по п.1 или 2, в котором другие компоненты газового потока нейтрализуют и/или захватывают, и/или улавливают в процессе образования карбоната.
9. Способ по п.8, в котором другие компоненты газового потока, которые нейтрализуют и/или захватывают, и/или улавливают в процессе образования карбоната, включают SOx, NOx, и ртутьсодержащий материал.
10. Способ по п.1 или 2, в котором получение гидроксида включает:
получение соли;
смешение соли с водой, паром, или ими обоими, с получением раствора; и
электролиз раствора с получением гидроксида.
11. Способ по п.10, в котором раствор подвергают электролизу с использованием напряжения большего или равного 5 вольтам.
12. Способ по п.10, в котором рассол подвергают электролизу при напряжении ниже чем 5 вольт, например, от 1,5 вольт до 4 вольт или от 2 вольт до 3 вольт.
13. Способ по п.10, в котором кислоту, предпочтительно хлористоводородную кислоту, добавляют к раствору перед тем как его подвергают электролизу.
14. Способ по п.10, в котором
стадия электролиза происходит в электролизере, имеющем пространство католита и пространство анолита; где
карбонатные или бикарбонатные продукты рециркулируют в пространство католита электролизера.
15. Способ по п.10, в котором потребляемая в способе энергия дополняется теплом топочных газов, извлекаемым из газового потока.
16. Способ по п.1 или 2, дополнительно определяемый как способ удаления диоксида углерода из газового потока, включающий:
получение гидроксида натрия в водной смеси;
смешение гидроксида натрия с газовым потоком с получением карбоната натрия, бикарбоната натрия, или смеси карбоната натрия и бикарбоната; и
выделение указанного карбоната натрия и/или бикарбоната из смеси тем самым, удаляя диоксид углерода из газового потока.
17. Способ по п.16, дополнительно включающий:
транспортирование карбоната натрия в отдаленное место секвестра;
объединение карбонатных продуктов с кислотой в реакции нейтрализации с получением чистого диоксида углерода; и
закачивание диоксида углерода в хранилище углерода.
18. Способ по п.16, в котором получение гидроксида натрия включает:
получение хлорида натрия;
смешение хлорида натрия с водой, паром или с обоими с получением рассола; и
электролиз рассола с получением гидроксида натрия и газообразного хлора.
19. Способ по п.18, в котором рассол подвергают электролизу при напряжении большем чем или равным 5 вольтам.
20. Способ по п.19, в котором рассол подвергают электролизу при напряжении меньшем чем 5 вольт, например, от 1,5 вольт до 4 вольт, от 2 вольт до 3 вольт.
21. Способ по п.18, в котором кислоту, предпочтительно хлористоводородную кислоту, добавляют к рассолу перед тем, как его подвергают электролизу.
22. Способ по п.18, в котором:
стадия электролиза происходит в электролизере, имеющем пространство католита и пространство анолита; где
карбонатные или бикарбонатные продукты рециркулируют в пространство католита электролизера.
23. Способ по п.18, в котором потребляемая в способе энергия дополняется теплом топочных газов, извлекаемым из газового потока.
24. Способ по п.18, дополнительно включающий сбор газообразного хлора.
25. Способ по п.18, в котором получают газообразный водород.
26. Способ по п.18, в котором газообразный водород и газообразный хлор сжигают с получением хлористоводородной кислоты, которую добавляют к рассолу перед тем, как его подвергают электролизу.
27. Способ по п.25, в котором газообразный водород сжигают с атмосферным кислородом или кислородом со склада химических материалов с получением воды.
28. Способ по п.25, дополнительно включающий использование газообразного водорода для производства энергии.
29. Способ по п.18, в котором выделение карбоната натрия и/или бикарбоната из смеси включает процесс горячего осаждения, в котором тепло для процесса выделения получают от энергии, производимой в результате сжигания газообразного водорода.
30. Способ по п.18, в котором газообразный водород сжигают совместно с углем для улучшения выбросов угольных топок или используют в процессе сжигания для получения постоянного электрического тока в топливном элементе.
31. Способ по п.1, в котором газовым потоком является поток выхлопных газов из установки, например, энергетической установки, которая использует исходное топливо на основе углерода, предпочтительно в котором поток выхлопных газов включает СО2 и Н2О.
32. Установка для удаления диоксида углерода из газового потока, включающая:
электролизную камеру, включающую, по меньшей мере, один катод и, по меньшей мере, один анод, приспособленную при использовании для получения гидроксида;
смесительное оборудование, операционно соединенное с электролизной камерой и трубопроводом, приспособленным для удерживания газового потока в процессе использования, которое приспособлено при использовании для смешения гидроксида из электролизной камеры с газовым потоком с получением смеси, в которой соединения углерода, серы и/или азота газового потока могут реагировать с гидроксидом;
где смешение происходит в двух раздельных камерах, причем одну камеру используют для производства карбонатных продуктов, а другую камеру используют для производства бикарбонатных продуктов;
и
камеру выделения, операционно соединенную со смесительным оборудованием и приспособленную для выделения смеси на отдельную газовую фазу и твердую и/или жидкую фазу.
33. Установка по п.32, в которой электролизная камера включает мембранный электролизер, диафрагменный электролизер и/или электролизер с ртутным катодом.
34. Установка по п.32, в котором смесительное оборудование включает периодический реактор или серию периодических реакторов, устройство для осуществления жидкостной абсорбции и/или химической реакции газа или серию устройств для осуществления жидкостной абсорбции и/или химической реакции газа, кристаллизационную колонну или серию кристаллизационных колонн, или барботажную колонну или серию барботажных колонн.
35. Установка по п.34, дополнительно включающая сушильную камеру, операционно соединенную с камерой для выделения, и приспособленную при использовании для удаления жидкости из твердой и/или жидкой фазы.
36. Установка по п.35, в котором сушильная камера при использовании приспособлена для нагрева твердой и/или жидкой фазы.
37. Установка по п.32, дополнительно определяемая как операцинно соединенная с энергетической установкой.
38. Установка по п.32, в которой электролизная камера при использовании приспособлена для получения газообразного хлора и гидроксида натрия из хлорида натрия и воды.
39. Установка по п.32, в которой смесительное оборудование при использовании приспособлено для смешения гидроксида из электролизной камеры с диоксидом углерода из газового потока для получения карбонатных и/или бикарбонатных продуктов.
40. Способ удаления диоксида углерода из газового потока, включающий:
(a) получение гидроксида в водной смеси;
(b) смешение гидроксида с газовым потоком с получением карбонатных продуктов, бикарбонатных продуктов или смеси карбонатных и бикарбонатных продуктов в смеси; и
(c) выделение указанных карбонатных и/или бикарбонатных продуктов из смеси, тем самым удаляя диоксид углерода из потока газа;
где потребляемая в способе энергия дополняется теплом топочных газов, извлекаемая теплом топочных газов, извлекаемых из газового потока.
| DE 19631794 A1, 07.08.1997 | |||
| СПОСОБ ЩЕЛОЧНОЙ ОЧИСТКИ ГАЗОВ ПИРОЛИЗА | 2001 |
|
RU2199374C1 |
| СПОСОБ ОЧИСТКИ ОТХОДЯЩИХ ГАЗОВ ОТ ОКСИДА УГЛЕРОДА И УГЛЕВОДОРОДОВ И СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1992 |
|
RU2054959C1 |
| RU 94036783 A1, 27.08.1996 | |||
| US 2004096384 A1, 20.05.2004 | |||
| WO 2004037391 A1, 06.05.2004 | |||
| US 6689332 B1, 10.02.2004. | |||
Авторы
Даты
2011-06-10—Публикация
2005-09-23—Подача