Изобретение относится к штамму вируса иммунодефицита человека первого типа, принадлежащему к рекомбинантному субтипу 02_AG, и может быть использовано в вирусологии, медицине и биотехнологии. Штамм является удобной природной моделью и может быть использован для разработки и усовершенствования методов диагностики ВИЧ-инфекции, изучения эффективности лечебных и профилактических химиотерапевтических и вакцинных препаратов, а также для создания национальной панели штаммов ВИЧ-1.
Высокая степень генетической гетерогенности вируса иммунодефицита человека - основная проблема, с которой сталкиваются исследователи. Вариабельность нуклеотидной структуры вируса способствует быстрому возникновению изолятов, устойчивых к нейтрализующим антителам, цитотоксическим Т-лимфоцитам и противовирусным препаратам. При разработке различных вакцин необходимо учитывать высокую вариабельность вирусного генома. В настоящее время в России отсутствует репрезентативный банк характеризованных штаммов ВИЧ-1. Поэтому необходимо проводить работы по выделению, молекулярно-биологической характеризации изолятов ВИЧ-1 и созданию коллекции ВИЧ-1, которая необходима для исследования свойств новых вакцинных и терапевтических препаратов. Такая коллекция должна включать эпидемиологически значимые варианты вируса, отражающие гетерогенность ВИЧ-1, наиболее характерные для отдельных регионов или групп риска (наркоманов, мужчин гомосексуальной ориентации, инфицированных в нозокомиальном очаге и т.д.).
В развитии эпидемического процесса по распространению ВИЧ в Российской Федерации основную роль играет субтип А ВИЧ-1. Однако в 2008 г. зарегистрировано резкое увеличение доли рекомбинантного варианта 02_AG среди циркулирующих генетических вариантов ВИЧ-1. Стремительный рост распространения нового генетического варианта ВИЧ-1 на территории России придает повышенную актуальность для получения и изучения штаммов этого субтипа, поскольку отечественные изоляты и штаммы субтипа 02_AG в литературе не описаны.
Известен штамм hominis immunodeficit vims ВИЧ-1/Россия ГМ-12-95 (Ru-1295) субтипа В подгруппы lentiviridae семейства Retroviridae для приготовления диагностических и вакцинных препаратов (патент РФ №2121502, МПК C12N7/00, опубл. 10.11.1998 г.), содержащий следующую аминокислотную последовательность области V3: CTRPNNNTRKRIHIGPGRAYFTGRIIGD IRQAYC.
Однако поскольку наибольшее распространение в Российской Федерации приобретают вирусы иммунодефицита человека 1 типа, принадлежащие к субтипам А и 02_AG, которые обнаруживаются у большинства инфицированных людей, то указанный штамм малопригоден для целей диагностики и изучения эффективности лечебно-профилактических и вакцинных препаратов, используемых на территории России.
Известны изоляты вируса иммунодефицита человека 1 типа, включающие группу изолятов, относящихся к рекомбинантному субтипу 02_AG, полученные в Таиланде (Development of a Panel of Well-Characterized Human {mmunodeficiency Virus Type 1 Isolates from Newly Diagnosed Patients Including Acute and Recent Infections//AIDS RESEARCH AND HUMAN RETROVIRUSES. Volume 25, Number 1, 2009), которые используются в панели для исследования противовирусной активности препаратов.
Однако такие изоляты малопригодны для целей диагностики и изучения эффективности лечебно-профилактических и вакцинных препаратов, используемых на территории Российской Федерации, так как они отличаются по генетическим характеристикам от изолятов 02_AG ВИЧ-1, получивших распространение в России.
Наиболее близким аналогом (прототипом) являются изоляты вируса иммунодефицита человека 1 типа, включающие группу изолятов, относящихся к рекомбинантному субтипу 02_AG, полученные также в Таиланде той же группой исследователей (Biologic and Genetic Characterization of a Panel of 60 Human Immunodeficiency Virus Type 1 Isolates, Reprezenting Clades A, B, C, D, CRF02_AG, for the Development and Assesment of Candidate Vaccines // Jomal of virology, Mat 2005, p.6089-6101), которые используются в панели для исследования противовирусной активности препаратов.
Однако и такие изоляты из-за генетических различий малопригодны для целей диагностики и изучения эффективности лечебно-профилактических и вакцинных препаратов, используемых на территории Российской Федерации.
Техническим результатом предлагаемого изобретения является получение такого штамма ВИЧ-1, который был бы пригоден для целей диагностики и изучения эффективности лечебно-профилактических и вакцинных препаратов, используемых на территории Российской Федерации.
Указанный технический результат достигается получением нового штамма 02_AG.RU.09RU2383 вируса иммунодефицита человека 1 типа рекомбинантного субтипа 02_AG, который выделен на территории России от пациента 29 лет, инфицированного половым путем, с диагнозом острая ВИЧ-инфекция. Штамм предназначен для включения в состав национальной панели штаммов, а также может быть использован для изучения эффективности лечебных и профилактических химиотерапевтических и вакцинных препаратов, усовершенствования методов диагностики ВИЧ-инфекции.
Заявляемый штамм вируса иммунодефицита человека ВИЧ-1 02_AG.RU.09RU2383 депонирован в Коллекции микроорганизмов ФГУН ГНЦ ВБ «Вектор» Роспотребнадзора под номером V-413 от 15.06.09 г.
На фиг.1 приведена нуклеотидная последовательность гена ро1 штамма ВИЧ-1 02_AG.RU.09RU2383. На фиг.2 приведена динамика накопления вирусспецифического белка р24 в смешанной культуре МПК, инфицированной штаммом 02_AG.RU.09RU2383, а на фиг.3 - динамика накопления вирусоспецифического белка р24 в инфицированных штаммом 02_AG.RU.09RU2383 культурах клеток МТ-4 и U-937.
Характеристика заявляемого штамма
Полученный новый штамм обладает рядом вирусологических свойств, позволяющих рассматривать его как удобную природную модель для оценки эффективности новых средств диагностики и исследования новых лечебно-профилактических препаратов. Штамм обладает высокой репродуктивной активностью, по типу репликации относится к категории Rapid/high, легко размножается в неопластических Т-лимфоцитарных МТ-4 и моноцитарных клетках U-937. О продукции вируса можно легко судить по ярко выраженному цитопатическому действию и по накоплению вирусспецифического белка р24. Штамм хорошо хранится при -70°C.
Идентификация штамма ВИЧ-1 02_AG.RU.09RU2383 осуществляли методом определения нуклеотидных последовательностей фрагментов генома ВИЧ-1, кодирующих области гена ро1 и основного белка оболочки (ген env), на автоматическом секвенаторе ABI PRISM. Последующий филогенетический анализ и определение субтипа вирусного изолята осуществляли с помощью программы, представленной на интернет-сайте Стенфордского Университета (http://hivdb.stanford.edu). Определение тропности изолята к клеточным хемокиновым корецепторам проводили с помощью доступных на интернет-сайтах программ Geno2pheno (http://coreceptor.biomf.mpi-mf.mpg.de) и WebPSSM и (http://indra.mullins.microbiol.washington.edu/webpssm).
Культуральные свойства. Штамм вируса выделен из лимфоцитов периферической крови пациента с диагнозом острая ВИЧ-инфекция. При получении штамма использован метод сокультивирования лимфоцитов инфицированного пациента с лимфоцитами крови здорового донора, стимулированных митогеном, а также метод инфицирования человеческих неопластических суспензионных перевиваемых клеточных линий МТ-4 и U-937.
Репродукция. Штамм вируса реплицируется в лимфоцитах периферической крови, лимфобластоидных клеточных культурах МТ-4 и U-937. Репродукция вируса сопровождается характерным цитопатическим действием смешанного типа - гибелью отдельных клеток, образованием синцитиев из 5-10 клеток и накоплением вирусоспецифического белка р24. Штамм ВИЧ-1 02_AG.RU.09RU2383 может поддерживаться длительное время при пассировании в смешанной культуре лимфоцитов периферической крови здоровых доноров, в культуре клеток МТ-4 или U-937. Через 4-7 дней после инфицирования клеток вируссодержащей культуральной жидкостью инфицированная клеточная взвесь центрифугируется при 1500 об/мин и замораживается в растворе для криоконсервации (70% сыворотка крупного рогатого, 10% глицерин) при -70°C. После размораживания вносится в свежую клеточную суспензию в соотношении 1:10.
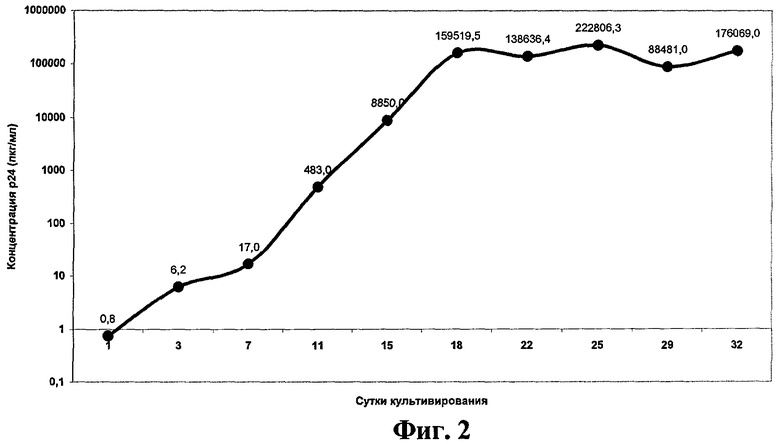
Репродуктивные характеристики штамма определяются методом твердофазного иммуноферментного анализа по накоплению вирусспецифического белка р24 на модели вышеуказанных клеточных культур (фиг.2, фиг.3).
Инфекционность вирусного штамма оценивали по накоплению вирусспецифического белка р24 в культуральной жидкости на 7 и 15 день культивирования смешанной культуры стимулированных фитогемагглютинином (ФГА) МПК от двух серонегативных доноров после инфицирования этих клеток ростовой средой, взятой на 7 и 15 день культивирования выделяемого изолята путем внесения ростовой среды в культуру МПК (1:10).
Антигенные свойства. ВИЧ-1 относится к семейству retroviridae, подгруппе lentiviridae. Вирусы этой подгруппы являются оболочечными РНК-содержащими вирусами с размером частиц около 100-150 нм. В составе частиц обнаруживают не менее 6 основных структурных антигенов, обладающих иммуногенными свойствами, которые могут быть выявлены в инфицированных клетках с помощью различных иммунологических и вирусологических методов.
Анализ нуклеотидной последовательности генома, филогенетический анализ и определение субтипа вирусного изолята осуществляли с помощью программы, представленной на интернет-сайте Стенфордского Университета (http://hivdb.stanford.edu). Генотипирование полученного штамма ВИЧ-1 02_AG.RU.09RU2383 проводили путем анализа нуклеотидных последовательностей участка генов po1. Выбор данных генетических участков определялся тем, что их анализ позволяет различать основные варианты ВИЧ-1, циркулирующие на территории бывшего СССР. Для определения и анализа нуклеотидной последовательности гена po1 использовали наборы "Виросек" ("Viroseq HIV-1 Genotyping System") фирмы "Celera Diagnostics" (США) и "АмплиСенс ВИЧ-генотип" компании "ИнтерЛабСервис" (Россия). Определение тропности изолята к клеточным хемокиновым корецепторам проводили с помощью доступных на интернет-сайтах программ Geno2pheno (http://coreceptor.biomf.mpi-inf.mpg.de) и WebPSSM (http://indra.mullins.microbiol.washington.edu/webpssm).
Пример 1. Генотипирование изолята ВИЧ-1 02_AG.RU.09RU2383. Генотипирование полученного штамма ВИЧ-1 02_AG.RU.09RU2383 проводили путем анализа нуклеотидных последовательностей участка гена ро1. Выбор данных генетического участка определялся тем, что его анализ позволяет различать основные варианты ВИЧ-1, циркулирующие на территории бывшего СССР. Для определения и анализа нуклеотидной последовательности гена po1 используют наборы "Виросек" ("Viroseq HIV-1 Genotyping System") фирмы "Celera Diagnostics" (США) и "АмплиСенс ВИЧ-генотип" компании "ИнтерЛабСервис" (Россия).
Вирусспецифическую РНК выделяют из образцов сыворотки. Вирусспецифическую ДНК получают методом обратной транскрипции вирусной РНК и используют для последующей амплификации методом гнездовой полимеразной цепной реакции. Определение нуклеотидных последовательностей проводят автоматически на приборе модели 3130х1 фирмы "Аплайд Байосистемс" (США).
Полученная последовательность гена po1 генома ВИЧ-1 включает в себя полноразмерную нуклеотидную последовательность гена протеазы длиной 371 - нуклеотидный остаток (фиг.1).
Полученные данные показывают, что штамм ВИЧ-1 02_AG.RU.09RU2383 является оригинальным штаммом ВИЧ-1 и относится к субтипу 02_AG.
Проведенный с помощью программ Geno2pheno и WebPSSM анализ указывает на то, что изолят ВИЧ-1 02_AG.RU.09RU2383 обладает наибольшей тропностью к клеточным хемокиновым корецепторам ССК5-типа.
Пример 2. Для выделения первичных изолятов ВИЧ-1 мононуклеары периферической крови (МПК) от больного культивируют со смешанной культурой стимулированных фитогемагглютинином (ФГА) МПК от двух серонегативных доноров. Выделение МПК проводят центрифугированием цельной крови на градиенте Ficoll. ФГА стимуляцию донорских МПК проводят 2-3 суток (5 мкг ФГА/мл). Для сокультивирования смешивают 4-6×106 МПК клеток пациента с 8-12×106 МПК клеток донора в 10 мл ростовой среды (PC) следующего состава - RPMI-1640, 20% эмбриональной сыворотки крупного рогатого скота (КРС), 100 е.а./мл IL-2, 300 мг/мл глутамина, 150 мкг/мл линкомицина и 100 мкг/мл гентамицина. Через каждые 3-4 суток проводят замену культуральной среды. Отобранную культуральную жидкость анализируют на содержание р24 антигена и криоконсервируют при -70°C. На 7 и 15 день сокультивирования после замены культуральной среды к оставшимся инфицированным клеткам добавляют 4-6×106 ФГА-активированных донорских МПК. Репликацию вируса оценивают по накоплению вирусспецифического белка р24. Вирусспецифический белок р24 выявляют в культуральной жидкости методом твердофазного иммуноферментного анализа с помощью иммуноферментной тест-системы для определения и подтверждения присутствия р24-антигена ВИЧ-1 «ВектоВИЧ-1 р24-антиген-подтверждающий тест ФСП 42-0117-5686-04», с чувствительностью - 5 пг/мл по ОСО ГИСК или набора реагентов для иммуноферментного выявления антител к ВИЧ-1,2 и антигена р24 ВИЧ-1 «КомбиБест ВИЧ-1,2 АГ/АТ, ТУ 9398-098-23548172-2007».
На фигуре 2 представлены результаты накопления р24 в культуральной жидкости в процессе культивирования изолята ВИЧ-1 в смешанной, активированной митогеном культуре МПК, отражающие динамику репродукции вируса. Штамм характеризуется высокой скоростью накопления вирусного белка р24, и концентрация белка достигает максимального значения (159520 пкг/мл) на 18 сутки. По типу репликации этот изолят можно отнести к категории Rapid/high.
Пример 3. Изучение накопления вируса в различных культурах клеток. Суспензию клеток МТ-4 или U-937 инфицируют культуральной жидкостью от инфицированной смешанной культуры МПК методом совместной инкубации в соотношении 5×106 клеток на 1 мл культуральной жидкости в течение 1 ч при температуре 37°C. Центрифугируют при 1000 об/мин 5 мин, супернатант удаляют, клетки ресуспендируют в питательной среде RPMI-1640 с добавлением 10% фетальной сыворотки, предварительно инактивированной прогреванием при 56°C в течение 30 минут, 300 мг/мл L-глютамина, 80 мкг/мл гентамицина и 30 мг/мл линкомицина до концентрации 0,5×106 клеток в миллилитре. Флаконы с культурой клеток инкубируют в термостате при 37°C. Контроль цитопатического действия вируса и синцитеобразования проводят методом инвертированной микроскопии клеточной суспензии в культуральных флаконах. Через каждые 3-4 суток проводят замену культуральной среды. Отобранную культуральную жидкость анализируют на содержание р24 антигена и криоконсервируют при -70°C. На 10 день культивирования после замены культуральной среды к оставшимся инфицированным клеткам добавляют суспензию неинфицированной клеточной культуры в ростовой среде с концентрацией 1×106 клеток/мл. Репликацию вируса оценивают по накоплению вирусоспецифического белка р24. Вирусспецифический белок р24 выявляют в культуральной жидкости методом твердофазного иммуноферментного анализа с помощью иммуноферментной тест-системы для определения и подтверждения присутствия р24-антигена ВИЧ-1 «ВектоВИЧ-1 р24-антиген-подтверждающий тест ФСП 42-0117-5686-04», с чувствительностью - 5 пг/мл по ОСО ГИСК или набора реагентов для иммуноферментного выявления антител к ВИЧ-1,2 и антигена р24 ВИЧ-1 «КомбиБест ВИЧ-1,2 AT/AT, ТУ 9398-098-23548172-2007».
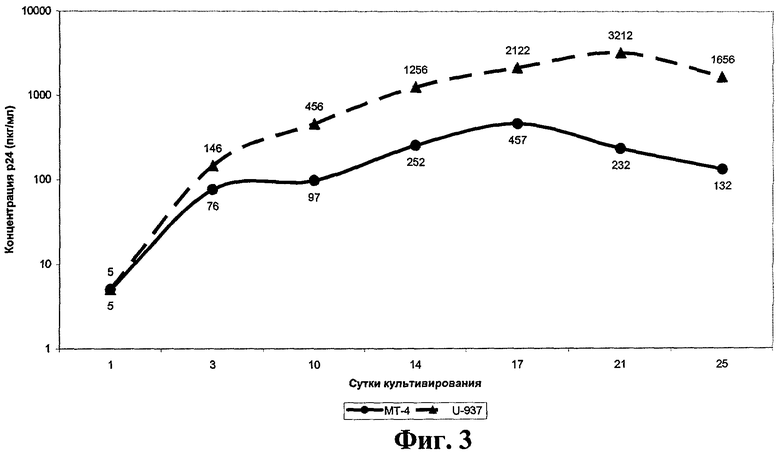
На фигуре 3 представлены результаты накопления р24 в культуральной жидкости в процессе культивирования изолята ВИЧ-1 в неопластических Т-лимфоцитарных клетках МТ-4 и моноцитарных U-937, отражающие динамику репродукции вируса. Изолят характеризуется различной скоростью и динамикой накопления вирусного белка р24 на разных культурах клеток. Максимальное значение концентрации на моноцитарной культуре и-937 достигается на 21 день культивирования, а на неопластических Т-лимфоцитарных клетках МТ-4 - на 17 день. Наблюдаемое превышение концентрации белка р24 при культивировании изолята на моноцитарной культуре U-937 по сравнению с культивированием на неопластических Т-лимфоцитарных клетках МТ-4, вероятно, объясняется тем, что данный изолят обладает наибольшей тропностью к клеточным хемокиновым корецепторам CCR5-rana. Хемокиновые корецепторы CCR5-типа, как и корецепторы CXCR4-rana, представлены на поверхности клеток U-937, тогда как на поверхности клеток МТ-4 присутствуют только корецепторы CXCR4-типа.
Заявляемый штамм ВИЧ-1 02_AG.RU.09RU2383 используется при разработке национальной панели генетически и биологически характеризованных штаммов ВИЧ-1, имеющих эпидемиологическую значимость на территории России для стандартизации оценки эффективности разрабатываемых вакцинных и противовирусных препаратов. Панель для оценки эффективности вакцин создается из штаммов, выделенных от больных в острой стадии ВИЧ-инфекции. Кроме того, панель должна включать генетически и биологически разнородные штаммы, относящиеся к одному субтипу ВИЧ-1, максимально представляющие разнообразие возможных циркулирующих на данной территории вирусных вариантов, что позволит проводить более адекватную и корректную оценку противовирусного эффекта препаратов на модели, максимально приближенной к реальным процессам, протекающим в организме инфицированного ВИЧ-1 человека.
Заявляемый штамм 02_AG.RU.09RU2383 ВИЧ-1 предполагается использовать также в панели для оценки эффективности противовирусных препаратов. Панель для оценки эффективности противовирусных препаратов включает генетически и биологически различные штаммы ВИЧ, выделенные от инфицированных ВИЧ-1 пациентов на разных стадиях заболевания и в том числе от больных, принимавших противовирусные препараты. Наличие такой панели в России позволит проводить стандартизованную адекватную оценку перспективных противовирусных препаратов для лечения ВИЧ-инфекции, что является актуальной проблемой для России, так как в нашей стране есть научный потенциал для разработки лекарственных препаратов, но нет сертифицированного инструмента для отбора препаратов по их эффективности в отношении ВИЧ-1 на модели живого вируса.
Кроме того, заявляемый штамм ВИЧ-1 может использоваться в качестве продуцента антигенов, входящих в диагностические наборы и тест-системы, в частности, антигенов ВИЧ-1, необходимых для производства иммуноферментных диагностических тест-систем на выявление ВИЧ-инфекции и наборов для иммунноблота, подтверждающего ВИЧ-инфекцию у вновь выявленных больных.
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ 02_AG.RU.09RU2410 ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА РЕКОМБИНАНТНОГО СУБТИПА 02_AG, ИСПОЛЬЗУЕМЫЙ ДЛЯ ДИАГНОСТИКИ И ИЗУЧЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2421518C1 |
| ШТАММ 02_AG.RU.09RU2308 ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА РЕКОМБИНАНТНОГО СУБТИПА 02_AG, ИСПОЛЬЗУЕМЫЙ ДЛЯ ДИАГНОСТИКИ И ИЗУЧЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2421517C1 |
| ШТАММ 02_AG.RU.09RU2273 ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА РЕКОМБИНАНТНОГО СУБТИПА 02_AG, ИСПОЛЬЗУЕМЫЙ ДЛЯ ДИАГНОСТИКИ И ИЗУЧЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2421515C1 |
| ШТАММ 02_AG.RU.09RU3124 ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА РЕКОМБИНАНТНОГО СУБТИПА 02_AG, ИСПОЛЬЗУЕМЫЙ ДЛЯ ДИАГНОСТИКИ И ИЗУЧЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2420574C1 |
| ШТАММ 02_AG.RU.09RU2204 ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА РЕКОМБИНАНТНОГО СУБТИПА 02_AG, ИСПОЛЬЗУЕМЫЙ ДЛЯ ДИАГНОСТИКИ И ИЗУЧЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2415931C1 |
| ШТАММ A1.RU.09RU2240 ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА СУБТИПА А, ИСПОЛЬЗУЕМЫЙ ДЛЯ ДИАГНОСТИКИ И ИЗУЧЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2420575C1 |
| ШТАММ A1.RU.09RU2225 ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА СУБТИПА А, ИСПОЛЬЗУЕМЫЙ ДЛЯ ДИАГНОСТИКИ И ИЗУЧЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2420573C1 |
| ШТАММ A1.RU.09RU2255 ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА СУБТИПА А, ИСПОЛЬЗУЕМЫЙ ДЛЯ ДИАГНОСТИКИ И ИЗУЧЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2421516C1 |
| ШТАММ А1.RU.09RU2065 ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА СУБТИПА А, ИСПОЛЬЗУЕМЫЙ ДЛЯ ДИАГНОСТИКИ И ИЗУЧЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2420572C1 |
| ШТАММ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1-ГО ТИПА ИВ742 СУБТИПА А ДЛЯ ДИАГНОСТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2012 |
|
RU2513693C1 |

Изобретение относится к штамму вируса иммунодефицита человека первого типа, принадлежащего к рекомбинантному субтипу 02_AG, и может быть использовано в вирусологии, медицине и биотехнологии. Представленный штамм вируса иммунодефицита человека ВИЧ-1 02_AG.RU.09RU2383 депонирован в Коллекции микроорганизмов ФГУН ГНЦ ВБ «Вектор» Роспотребнадзора под номером V-413. Штамм может быть использован для разработки и усовершенствования методов диагностики ВИЧ инфекции, изучения эффективности лечебных и профилактических химиотерапевтических и вакцинных препаратов, а также для создания национальной панели штаммов ВИЧ-1. 3 ил.
Штамм 02_AG.RU.09RU2383 вируса иммунодефицита человека 1 типа рекомбинантного субтипа 02_AG, используемый для диагностики и изучения эффективности лечебно-профилактических и вакцинных препаратов, депонированный в Коллекции микроорганизмов ФГУН ГНЦ ВБ «Вектор» Роспотребнадзора под номером V-413 и имеющий нуклеотидную последовательность гена роl, приведенную на фигуре 1.
| BROWN В.К., et al., Biologic and genetic characterization of a panel of 60 human immunodeficiency virus type 1 isolates, representing clades A, B, C, D, CRF01 AE, and CRF02 AG, for the development and assessment of candidate vaccines, J Virol | |||
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| ШТАММ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА I ТИПА, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПРИГОТОВЛЕНИЯ ДИАГНОСТИЧЕСКИХ ТЕСТ-СИСТЕМ | 1992 |
|
RU2046138C1 |
| ШТАММ HOMINIS IMMUNODEFICITI VIRUS (HIV-I) ВИЧ-1 /РОССИЯ/ГМ-12-95 (RU 1295) СУБТИПА В ДЛЯ ДИАГНОСТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 1996 |
|
RU2121502C1 |
Авторы
Даты
2011-06-10—Публикация
2010-01-18—Подача