Изобретение относится к новому электрохимическому способу получения галогенированного соединения, содержащего карбонильную группу, такого как карбоновая кислота. В частном варианте осуществления оно относится к хлорированию уксусной кислоты для производства монохлоруксусной кислоты.
В промышленности монохлоруксусную кислоту получают реакцией уксусной кислоты с хлором. Такой способ получения монохлоруксусной кислоты широко известен и обычно используют реактор, в котором смесь жидкой уксусной кислоты (HAc) реагирует с газообразным хлором в безводных условиях. Для создания таких безводных условий может использоваться большое число соединений. Если используется уксусный ангидрид, он немедленно будет превращен соляной кислотой в ацетилхлорид, который является катализатором для этого процесса. Процесс обычно проводится при давлении от 1 до 6 бар абс. и температуре от 80 до 180°C. В реакторе монохлоруксусная кислота (MCA) и газообразная HCl образуются вместе с побочными продуктами, примерами которых являются дихлоруксусная кислота (DCA) и трихлоруксусная кислота (TCA).
После того как содержащая MCA смесь продуктов реакции прошла через реактор(ы) и секцию регенерации катализатора, DCA присутствует в значительном количестве, обычно примерно 3-10%. Затем смесь продуктов, содержащую MCA/DCA, подают на установку для уменьшения количества DCA в MCA. Это может быть сделано физическим разделением, таким как кристаллизация из расплава, или химическим превращением, таким как восстановление, когда DCA восстанавливают водородом в присутствии катализатора гидрирования, например катализатора на основе металла. Этот катализатор не только восстанавливает DCA, но также до некоторой степени восстанавливает MCA, что, конечно, нежелательно. Кроме того, такая установка восстановления и ее эксплуатация дороги, и это повышает стоимость получения конечного продукта MCA.
Затем из MCA удаляют низкокипящие компоненты обычной вакуумной перегонкой.
Способ получения MCA электрохимическим процессом был описан в работе A. Youtz et al., "Depolarization of the Chlorine Electrode by Organic Compounds" в J. Am. Chem. Soc., 1924, 46, 549. Способ включает реакцию 70%-ной уксусной кислоты в водном растворе с соляной кислотой с получением хлоруксусной кислоты.
Электрохимический способ получения галогенированной карбоновой кислоты (производного) в водной среде имеет тот недостаток, что образуется низкое количество требуемой (моно)галогенированной карбоновой кислоты. Кроме того, в хлоридной водной среде основным продуктом электролиза часто является газообразный хлор, что нежелательно, так как это означает дополнительный поток отходов и, помимо этого, комбинация газообразного хлора и газообразного водорода может сделать смесь отходящих газов реакция взрывоопасной.
Целью изобретения является обеспечить способ получения галогенированного соединения, содержащего карбонильную группу, при использовании исходных материалов, которые дешевы и доступны в большом масштабе, причем в то же время не требуется дополнительная обработка образующихся побочных продуктов. Кроме того, целью настоящего изобретения является разработка способа, в котором содержащее карбонильную группу моногалогенированное соединение обеспечивает имеющее пониженное содержание ди-, три- или полигалогенированных побочных продуктов по сравнению вышеописанным промышленным способом. Также целью изобретения является предоставить способ, который можно легко реализовать на существующем оборудовании, используемом для описанного выше современного промышленного способа, не требуя жестких физических условий. Следующей целью является разработать способ, обеспечивающий получение соединения, содержащего карбонильную группу, которое селективно галогенировано в положении α-углеродного атом (т.е. атома углерода, ближайшего к карбонильной группе). Еще одной целью является разработать способ, обеспечивающий улучшенный выход продукта, например, по сравнению с водным электрохимическим способом Youtz и др. и который дает ценные побочные продуты.
Теперь настоящим изобретением предоставляется способ получения галогенированного соединения, содержащего карбонильную группу, путем электрохимической реакции соответствующего соединения, содержащего карбонильную группу, с гидрогалогенидом H-X, органическим галогенидом R'-X и/или галогенидной солью Mn+-Xn " в по существу безводных условиях, причем X означает атом хлора, брома или йода, R' означает алкильную или арильную группу, которая может быть линейной или разветвленной, содержащей факультативно один или более гетероатомов, таких как кислород, азот; хлорид, бромид, фторид или йодид, от которых атом галогена X может быть легко отщеплен электрохимически, Mn+ есть катион четвертичного аммония, щелочноземельного металла, щелочного металла или металла, и n есть целое число от 1 до 5, в зависимости от валентности катиона металла Mn+.
По существу безводные условия определяются как условия, при которых в реакционной смеси содержится менее 1 вес.% воды, предпочтительно - менее 0,1 вес.%, более предпочтительно - примерно ноль, наиболее предпочтительно, условия являются полностью безводные, что достигается, когда реакционная смесь содержит соединения, которые действуют как поглотители воды.
Неожиданно оказалось, что галоген X может быть выбран только из группы хлора, брома и йода, так как при применении способа по настоящему изобретению фторирование невозможно. В уровне техники (смотри, например, P. Sartori, N. Ignat'ev, "The Actual state of our knowledge about mechanism of electrochemical fluorination in anhydrous hydrogen fluoride (Simons process)", Journal of Fluorine Chemistry 87 (1998), pp. 157-162, описан способ фторирования нескольких органических соединений, однако эти реакции обычно приводят к полифторированию и не обеспечивают селективное фторирование по α-углеродному атому.
При применении способа по изобретению не требуется никакого газообразного галогена (такого как газообразный хлор), но вместо этого может использоваться гидрогалогенид, органические галогениды или галогенидные соли, которые, как правило, намного более доступны и дешевле, чем исходные материалы современного промышленного процесса. Способ по настоящему изобретению в качестве продуктов реакции дает галогенированное соединение, содержащее карбонильную группу, и водород. Любой непрореагировавший источник галогенида можно легко использовать повторно, это же справедливо и для непрореагировавшего соединения с карбонильной группой. Образующийся побочный продукт водород можно легко выделить и можно применять, например, как источник энергии или исходное соединение для других химических процессов, то есть он имеет промышленную ценность.
Неожиданно было обнаружено, что образовывалось только очень незначительное количество ди- и/или более галогенированных соединений, содержащих карбонильную группу; было найдено, что при галогенировании карбоновой кислоты количество дигалогенированной карбоновой кислоты было ниже 0,3 вес.%, а количество тригалогенированной или более галогенированной карбоновой кислоты, если такая вообще образовывалась, было ниже предела обнаружения (т.е., 50 ppm). Так как побочным продуктом реакции является газообразный водород (а именно пузырьки), реакционная смесь остается хорошо перемешанной, и смешения не требуется, что также является выгодным.
В способе по изобретению был достигнут 80%-ный выход по электрическому току для получения моногалогенированной карбоновой кислоты (производного). Ожидается, что может быть достигнут еще более высокий выход по току. В отличие от этого, электрохимическое хлорирование уксусной кислоты в водной среде приводит к низкому выходу, обычно ниже 1%.
Выход по току (называемый также к.п.д. по току) описан в публикации Bard-Stratman, Encyclopedia of Electrochemistry, Organic Electrochem., Vol. 8, Chapter 2,3.1, p. 31, на которую делается ссылка. Говоря коротко, к.п.д. по току, или выход по току, означает долю тока в электролизере или (интегрированную по времени) долю перенесенного заряда, которая используется для образования продукта.
Неожиданно было обнаружено, что в способе по изобретению ди- и/или более галогенированные соединения, содержащее карбонильную группу, также эффективно превращаются в моногалогенированное соединение, содержащее карбонильную группу. Соответственно, в одном варианте осуществления, исходный материал может быть смесью соединений, содержащих по меньшей мере ди- и/или более галогенированные соединения с карбонильными группами (R'-X) и негалогенированного соединения, содержащего карбонильную группу, причем количество ди- и/или более галогенированных соединений с карбонильными группами предпочтительно не более, чем эквимолярно количеству негалогенированного соединения, содержащего карбонильную группу. Было найдено, что применение такой исходной смеси все же приводит к продукту реакции, содержащему в основном моногалогенированное соединение с карбонильной группой, или, другими словами, к очень низкому количеству ди- и/или более галогенированных соединений, содержащих карбонильную группу. Гидрогалогенид получается in situ в результате электрохимической реакция ди- и/или более галогенированного соединения, содержащего карбонильную группу, на катоде в электрохимических условиях.
В двух документах, а именно: L.N. Nekrasov et al., "Effect of small amouts of tetramethyl- and tetraethylamonium ions on electroreduction kinetics of certain organic compounds in solutions of tetrabuthylamonium salts", Elektrokhimiya, Vol. 24, No. 4, pp. 560-563, 1988 и A. Inesi, L. Rampazzo, "Electrochemical reduction of halogen containing compounds at a mercury cathode: chloroacetic, dichloroacetic acids and corresponding ethylesters in dimethylformamide", Electroanalytical Chemistry and Interfacial Electrochemistry, 44 (1973), pp. 25-35, раскрывается, что трихлоруксусная кислота может быть восстановлена до дихлоруксусной кислоты при применении электрохимического процесса, но ни раскрывается, ни предполагается, что это соединение может применяться как источник галогена (т.е. как определенное выше соединение R'-X) для галогенирования содержащего карбонильную группу соединения, чтобы получить моногалогенированное соединение, содержащее карбонильную группу.
Таким образом, в одном варианте осуществления изобретение обеспечивает способ, в котором органический галогенид R'-X является ди- и/или более галогенированным соединением, содержащим карбонильную группу, или, другими словами, способ получения галогенированного соединения, содержащего карбонильную группу, электрохимической реакцией соответствующего соединения, содержащего карбонильную группу, с ди- и/или более галогенированным соединением, содержащим карбонильную группу, по выбору гидрогалогенидом H-X, дополнительным органическим галогенидом R'-X и/или галогенидной солью Mn+-Xn -, в по существу безводных условиях, причем X означает атом хлора, брома или йода, R' означает алкильную или арильную группу, которая может быть линейной или разветвленной, содержащий (факультативно) один или более гетероатомов, таких как кислород, азот; хлорид, бромид, фторид или йодид, от которых атом галогена X может быть отщеплен электрохимически, Mn+ означает катион четвертичного аммония, щелочноземельного металла, щелочного металла или металла, и n есть целое число от 1 до 5, в зависимости от валентности катиона металла Mn+.
Способ по изобретению может также применяться как вторая стадия в обычном процессе получения моногалогенированного соединения, содержащего карбонильную группу, путем химической реакции соединения, содержащего карбонильную группу, и источника галогена. Также способ по изобретению может применяться для обработки маточного раствора, который получается, например, когда моногалогенированную карбоновую кислоту (производное) отделяют от реакционной смеси, содержащей как моногалогенированные, так и ди- и/или более галогенированные карбоновые кислоты (производные), причем в этом случае такой маточный раствор содержит смесь оставшейся моногалогенированной карбоновой кислоты (производного) и относительно большого количества ди- и/или более галогенированных карбоновых кислот (или их производных).
Способы разделения включают традиционные способы разделения, доступные специалисту, такие как перегонка, экстракция и кристаллизация, причем наиболее предпочтительна кристаллизация.
В этом отношении изобретение дает способ получения галогенированного соединения, содержащего карбонильную группу, сначала приводя соединение, содержащее карбонильную группу, в химическую реакцию с молекулами хлора, брома или йода и затем электрохимически обрабатывая реакционную смесь в соответствии с описанным выше электрохимическим способом, изобретение дает способ, в котором исходная смесь является маточным раствором, получаемым, при отделении моногалогенированного соединения, содержащего карбонильную группу, от реакционной смеси, содержащего как моногалогенированное соединение с карбонильной группой, так и ди- и/или более галогенированные соединения, содержащие карбонильную группу.
В способе со смесью соединения, содержащего карбонильную группу, и соответствующих ди- и/или более галогенированных соединений, содержащих карбонильную группу, результирующей реакцией является реакция ди- и/или более галогенированного соединения, содержащего карбонильную группу, с соответствующим соединением, содержащим карбонильную группу, дающая моногалогенированное соединение, содержащее карбонильную группу.
Вариант осуществления, включающий обычный процесс с последующим электрохимическим процессом согласно изобретению, имеет важное преимущество в том, что продукты обычного процесса (т.е. гидрогалогенид и смесь соединения, содержащего карбонильную группу, моногалогенированного соединения, содержащего карбонильную группу, и ди- и/или более галогенированного соединения, содержащего карбонильную группу) являются исходным материалом для электрохимической стадии. Таким образом обработка потока продуктов обычного процесса не требуется; напротив, поток продуктов с обычного процесса может напрямую использоваться как поток исходного материала на электрохимической стадии.
Соответственно, "более высокогалогенированный" означает, что в соединении, содержащем карбонильную группу, присутствует до 10, предпочтительно от 3 до 6 атомов хлора, брома и/или йода.
Кроме того, изобретение дает устройство для осуществления указанных выше способов. В этой связи дается устройство, которое включает химический реактор (A), соединенный с электрохимическим реактором (B) по линии (5) и, факультативно, через линии (2), (3) и (4), причем реактор (B) соединен с установкой (C) физического разделения по линии (9). Устройство показано на фигуре 1.
Химический реактор (A) может быть реакционным аппаратом (например, нагреваемым, и/или охлаждаемым, и/или изолированным) из подходящего материала (например, из эмалированной стали). Предпочтительно химический реактор содержит внутренние устройства, такие как механические мешалки, теплообменные трубы, впускные трубы (например, для сырья и возвращаемых потоков), и/или содержит датчики (такие как датчики температуры, датчики давления, датчики уровня жидкости). Дополнительно химический реактор (A) может предусматривать устройство УФ-облучения, такое как УФ-лампа, для превращения газообразного галогена в атом галогена.
Более подробно, согласно фиг. 1 галогенид, соединение, содержащее карбонильную группу, факультативно катализатор и факультативно электролит подаются в химический реактор (A) по линиям (1), (2), (3) и (4) соответственно, причем две или более из них могут быть объединены в одну линию для реакции с промежуточным продуктом, подаваемым в электрохимический реактор (B) по линии (5). Газообразные компоненты, образованные в химическом реакторе (A) и отведенные из него, могут (факультативно) вводиться частично или полностью в электрохимический реактор (B) также по линии (6), в этом случае линия (6) может быть объединена с линией (5) в одну линию. Факультативно, больше или даже все содержащие карбонильную группу соединения, катализатор и электролит могут подаваться в электрохимический реактор (B) через входы (2), (3) и (4) соответственно, два или более из которых могут быть объединены в один вход. В одном варианте осуществления электрохимический реактор (B) может быть снабжен дополнительным входным потоком (7), содержащим галогенид (газ или жидкость).
Электрохимический реактор (B) является устройством, содержащим по меньшей мере один анод и по меньшей мере один катод из любого подходящего материала, какой описан выше, и предпочтительно является аппаратом, где расположение анода(ов) и катода(ов) имеет подходящую геометрию (например, параллельные пластины или концентрические цилиндры, ванны с уплотненным или псевдоожиженным межэлектродным пространством). В более предпочтительной реализации электрохимический реактор содержит один или более разделителей электролита, таких как диафрагмы или мембраны. В другой предпочтительной реализации электрохимический реактор (B) является реактором, содержащим параллельные электроды в аппарате с или без внутренней и наружной рециркуляции жидкости. Анод и катод соединены с источником снабжения постоянным током, который подает электрический ток на электроды. Электроды могут быть соединены с источником электроснабжения в монополярной или биполярной схеме расположения. В предпочтительной реализации в электрохимическом реакторе (B) одновременно образуются моногалогенированные соединения в результате галогенирования сырья на аноде и происходит дегалогенирование ди- и более галогенированных соединений на катоде. В некоторых вариантах реализации в электрохимическом реакторе на катоде образуется газообразный водород, который выводится из реактора по линии (8).
Существенно восстановленный ди- и/или более галогенированный продукт из электрохимического реактора (B) подается на установку (C) физического разделения по линии (9). Гидрогалогенид и другие компоненты, образованные в химическом реакторе (A) и/или электрохимическом реакторе (B), отделяются от продукта по линии (11) и возвращаются в химический реактор (A) и/или электрохимический реактор (B) по линии (10). Кроме того, электролит может подаваться в химический реактор (A) и/или электрохимический реактор (B) через вход (4), причем электролит может отделяться от продуктов реакции и реагентов в установке (C) физического разделения и при необходимости может возвращаться в реакторы A и B по линиям (10).
Установка (C) физического разделения является устройством, которое может содержать одну или более перегонных колонн, экстракционных колонн, абсорбционных колонн или их комбинацию, подходящим для отделения продукта электрохимического реактора, входящего в установку C по линии (9) в потоке галогенированного продукта, содержащего в основном моно- и дигалогенированные карбонильные производные, выходящие из устройства по изобретению через выход (11).
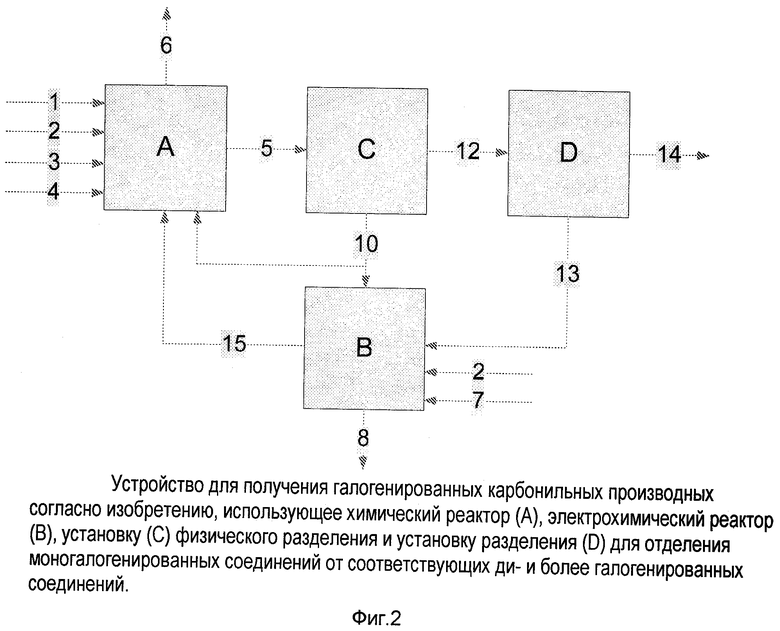
В другом варианте осуществления устройство содержит дополнительную установку разделения (D) для отделения моногалогенированных соединений от соответствующих ди- и более галогенированных соединений. Это устройство показано на фиг. 2.
Подробнее, согласно фиг. 2 в устройстве по этому варианту осуществления продукт из химического реактора (A) вводится в установку (C) физического разделения по линии (5), как описано выше, чтобы отделить электролит и другие компоненты или продукты, образованные в химическом реакторе A, от смеси моно-, ди- и/или более галогенированных карбонильных продуктов, перенесенных в установку разделения D по линии (12).
Установка разделения D содержит средства разделения, способные отделить моногалогенированные соединения от соответствующих ди- и более галогенированных соединений. Этими средствами разделения могут быть перегонные колонны, кристаллизационные установки, экстракционная установка или любая их комбинация, чтобы получить требуемое разделение. Установка D производит очищенный моногалогенированный продукт, выводимый по линии (14), и поток, существенно обогащенный ди- и/или более галогенированным продуктом, который вводится в электрохимический реактор (B), описанный выше, через вход (13).
В устройстве по варианту осуществления, показанном на фиг. 2, продукт из электрохимического реактора (B), существенно обогащенный моногалогенированным продуктом, может вводиться в химический реактор (A) по линии (15). Дополнительно поток, содержащий электролит и другие компоненты с установки (C) физического разделения, вводится в электрохимический реактор (B) и/или химический реактор (A) по линии (10). Факультативно поток, содержащий галогенид (газ или жидкость), и поток, включающий соединения, содержащие карбонильную группу, может вводиться в электрохимическую установку (B) также через входные линии (7) и (2) соответственно, которые могут быть объединены в одну входную линию. В электрохимическом реакторе (B) газообразный водород может образовываться на катоде и отводиться из реактора по линии (8).
В предпочтительной реализации способ по изобретению реализуют по существу в отсутствие растворителя. Под выражением "по существу в отсутствие растворителя" понимается, что в реакционной смеси присутствует самое большее 5% растворителя. Подразумевается, что термин "растворитель" охватывает любое вещество, в котором растворимы по меньшей мере исходные материалы реакции, но не включает никаких реагентов/продуктов. Более предпочтительно, в способе по изобретению реакционная смесь содержит менее 2% растворителя. Наиболее предпочтительно присутствует около 0% растворителя.
Подразумевается, что результирующими химическими реакциями в процессе по изобретению являются
H-X+R-COY->X-R-COY+H2
R'-X+R-COY->X-R-COY+R'-H или
MXn+n R-COOH->(X-R-COO)nM+nH2
Содержащее карбонильную группу соединение R-COY или R-COOH, которое будет галогенировано, может быть любым соединением, содержащим атом водорода у α-углерода, предпочтительно жидким при температуре реакции. Содержащее карбонильную группу соединение R-COY может быть альдегидом, кетоном, карбоновой кислотой, ангидрид карбоновой кислоты или ацилгалогенидом. Предпочтительно R-COY и R-COOH являются содержащими карбонильную группу соединениями, в которых R означает алкильную, алкиленовую или арильную группу, содержащую α-атомы водорода, которая может быть линейной, циклической или разветвленной, возможно содержащей один или более гетероатомов, таких как кислород, азот, хлорид, бромид или йодид, и Y означает водород, гидроксильную группу, атом галогена или группу R" или OCOR", причем каждый R" независимо означает атом водорода или алкильную, алкиленовую или арильную группу. Более предпочтительно, Y означает гидроксильную группу, атом галогена, группу R" или OCOR", причем R" есть C1-C10 алкильная или C1-C10 алкиленовая группа, и R есть C1-C26 алкильная или C1-C26 алкиленовая группа. Еще более предпочтительно, содержащее карбонильную группу соединение является незамещенной C2-C26 карбоновой кислотой, еще более предпочтительно уксусной кислотой, пропионовой кислотой или жирной кислотой, наиболее предпочтительно уксусной кислотой. Жирная кислота определяется как карбоновая кислота с гидрокарбильными группами, содержащими 1-22 атома углерода, предпочтительно 8-22 атома углерода, которые могут быть насыщенными или ненасыщенными, линейными или разветвленными. Предполагается, что жирные кислоты, полученные из натуральных жиров и масел, содержат по меньшей мере 8 атомов углерода. Предпочтительными в настоящем изобретении жирными кислотами являются неразветвленные C8-C26 карбоновые кислоты, еще более предпочтительной является группой натуральных жирных кислот, какие описаны, например, в CRC Handbook of Chemistry and Physics, 1989 ed., D-220.
Галогенид является хлоридом, бромидом или йодидом, более предпочтительно - это хлорид или бромид, наиболее предпочтительно хлорид.
Органический галогенид R'-X может быть любым соединением, которое может быть дегалогенировано на электрохимической стадии, таким, например, какие раскрыты в работе Lund, Hammerich, Organic Electrochemistry, 4th ed., Chapter 8, "Halogenated organic compounds" (Marcel Dekker, 2001). R'-X предпочтительно является галогенированным углеводородным соединением, которое может дополнительно содержать заместители, такие как азот или кислород. Наиболее предпочтительно, R'-X является ди- и/или более галогенированным соединением, содержащим карбонильную группу.
Галогенидная соль Mn+-Xn предпочтительно является такой галогенидной солью, в которой M является катионом щелочноземельного металла, щелочного металла или металла, более предпочтительно M означает катион Na, K, Li, Mg, Ca, Ba, еще более предпочтительно катион щелочного металла, наиболее предпочтительно катион лития, натрия или калия.
В еще более предпочтительной реализации реакционная смесь содержит в основном только реагенты, продукты и вспомогательные вещества, т.е. более 95 вес.% реакционной смеси составляют исходные материалы, продукты и вспомогательные вещества, и наиболее предпочтительно она содержит более 99 вес.% этих компонентов. Вспомогательные вещества определяются как агенты, которые могут действовать в процессе по изобретению, такие как катализатор и поддерживающий электролит.
В принципе, поддерживающий электролит не является необходимым в способе, если только в условиях процесса через жидкость может проходить достаточный ток. В предпочтительной реализации поддерживающий электролит присутствует в реакционной смеси. Этот электролит представляет собой неводное соединение (смесь таких соединений), которое достаточно растворимо и обеспечивает достаточную проводимость в используемой реакционной смеси, может быть легко отделено и возвращено в цикл и является достаточно стабильным к окислению и восстановлению. Примерами таких поддерживающих электролитов могут быть любые комбинации ионов, указанные, например, в F. Beck, Elektroorganische Chemie, Verlag Chemie GmbH, Weinheim, 1974, Chapter 3,3, pp. 104-110, или в D. Pletcher, A First Course in Electrode Processes, The Electrochemical Consultancy, Alresford Press Ltd., 1991, Chapter 2,3, pp. 57-72, и могут включать такие ионы, как OH-, I-, Br-, Cl-, F-, NO3 -, SO4 2-, HCO3-, Fe(CN)6 3-, ClO4 -, BF4 -, PF6 -, H+, Li+, Na+, K+, Rb+, Ca2+, Mg2+, Al3+, La3+, Ag+, NH4 +, [N(CH3)4]+, [N(C2H5)4]+, [N(C4H9)4]+, [N(C2H5)H]+. Более предпочтительно, электролит является солью, растворимой в галогенируемой карбоновой кислоте и либо не принимающей участия в реакции галогенирования, либо участвующей, но в этом случае содержащей тот же источник галогена, что и исходный галоген в реакции, чтобы предотвратить образование других галогенированных соединений, содержащих карбонильную группу. В еще более предпочтительной реализации электролит является галогенидной солью, такой как NaCl, NaBr, NaI, KCl, KBr, KI, LiCl, LiBr, LiI, MgCl2, MgBr2, MgI2, CaCl2, CaBr2, CaI2, BaCl2, BaBr2, BaI2. В наиболее предпочтительной реализации в качестве поддерживающего электролита действует соль металла MXn.
В другой предпочтительной реализации в реакционной смеси присутствует соединение, ускоряющее реакцию (называемое здесь также катализатором). В более предпочтительной реализации это соединение является ангидридом галогенируемой карбоновой кислоты (производного) или ее галогенангидридом. В варианте осуществления, включающем двухэтапный процесс, т.е. стадия химического галогенирования с последующей электрохимической стадией, указанный выше галогенангидридный катализатор может образовываться в реакционной смеси (то есть его не нужно добавлять) при использовании на химическом стадие таких продуктов как PCl3, или SOCl2, или SO2Cl2, COCl2, ангидрид кислоты или сера (в качестве катализатора). Как уже кратко отмечалось выше, эти типы ангидридов кислоты и галогенангидридов имеют дополнительное преимущество в том, что они связывают воду, давая карбоновую кислоту и, таким образом, способны делать условия реакции полностью безводными. Катализатор используется в обычных количествах от 2 до 30 вес.% от всей реакционной смеси.
Дополнительное преимущество способа по изобретению состоит в том, что, так как электрохимическая реакция проводится в неводной среде, каталитическое соединение не распадается под действием воды, присутствующей в реакционной смеси.
Применяемые электроды могут быть выбраны из любого материала, если только он не разрушается в реакционной смеси в условиях реакции с образованием нежелательных побочных продуктов. В этом отношении особенно важен выбор материала анода, так как анод наиболее чувствителен к деградации в условиях процесса. В предпочтительной реализации анод сделан из углерода (такого как легированный бором алмаз, графит, стекловидный уголь), керамики (такой как магнетит, т.е. Fe3O4 или Ebonex®, т.е. смешанные оксиды титана), металлического сплава (такого как платина/рутений) или благородного металла (такого как Au, Ag, Pd, Pt, Ti), возможно содержащего смешанный оксид металлов, такой как IrO2/RuO2 (например, IrO2/RuO2 на титане, нерасходуемые аноды - Dimension Stable Anodes: DSA®-электроды), а катод сделан из углерода (такого как легированный бором алмаз, графит, стекловидный уголь), металлов (таких как никель, свинец, ртуть, титан, железо, хром), металлического сплава (такого как нержавеющая сталь (Cr-Ni-Fe), монель (Cu-Ni), латунь (Cu-Zn), или оксидов металла (таких как Pb/PbO2), или может быть любым другим электродом, если только он стабилен в системе и не образует значительных количеств нежелательных побочных продуктов. Примеры материалов для электродов упоминаются в работе A.J. Bard, M. Stratmann, Eds., Encyclopedia of Electrochemistry, Organic Electrochem., Vol. 8, Chapter 2,4.1, p. 39, на которую делается ссылка.
Кроме того, в способе по изобретению электроды предпочтительно выбирать так, чтобы их удельная поверхность была как можно больше и чтобы расстояние между катодом и анодом было как можно меньше. У специалиста в данной области не будет никаких проблем в выборе электродов, подходящих для этой цели. В качестве неограничивающих примеров электродов, которые удовлетворяют одному или более из названных выше критериев, можно упомянуть концентрические электроды, пористые электроды, электроды в виде параллельных пластин, дисперсные электроды, псевдоожиженные электроды. Схема расположения электродов может быть однополярной или биполярной.
Плотность электрического тока в процессе по изобретению обычно составляет от 0,1 до 7 кА/м2, предпочтительно от 0,5 до 4 кА/м2 и наиболее предпочтительно от 1 до 2 кА/м2. Напряжение между электродами в электролизере типично составляет от 1 до 10 вольт, завися главным образом, но не исключительно, от приложенной плотности тока, проводимости реакционной среды и расстояния между электродами.
Способ по изобретению может объединяться со стадией УФ-обработки, на котором в реакционную систему добавляют газообразный галоген, превращающийся в атом галогена при УФ-облучении и становящийся также способным реагировать с соединением, содержащим карбонильную группу, чтобы получить желаемое галогенированное соединение, содержащее карбонильную группу.
Способ по изобретению может осуществляться в периодическом, полупериодическом или непрерывном режимах, предпочтительно, это непрерывный процесс.
Способ может осуществляться при давлении, которое обычно находится в диапазоне от 1 до 10 бар абс., предпочтительно, давление составляет от 0,9 до 5 бар абс., наиболее предпочтительно примерно 1-2 бар абс. Бар абс. означает абсолютное давление в барах.
Способ обычно осуществляться при температуре от 11 до 200°C, предпочтительно от 20 до 150°C, более предпочтительно от 75 до 140°C, наиболее предпочтительно от 80 до 120°C.
Далее изобретение иллюстрируется следующими примерами и сравнительными примерами.
Примеры
Пример 1: Хлорирование уксусной кислоты с использованием HCl
В реакторе, содержащем графитовые аноды и катоды (материал типа 6503, Le Carbonne Lorraine, Роттердам, Нидерланды) с эффективной площадью анода 580 см2 и эффективной площадью катода 530 см2 800 граммов смеси, содержащий 7 вес.% безводного хлорида кальция (JT. Baker, № 0070, мин. 95 вес.%), 69% уксусной кислоты (Fluka, № 45731, >99,8 вес.%), и 24 вес.% ацетилхлорида (Fluka, № 00990, >99%) предварительно нагревали до 70°C и подвергали электролизу при среднем токе 20 ампер. В процессе электролиза в реакционную смесь добавляли газообразный хлористый водород.
Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали методом высокоэффективной жидкостной хроматографии (ВЭЖХ).
Таблица 1 показывает концентрации монохлоруксусной кислоты (MCA) и дихлоруксусной кислоты (DCA), измеренные методом ВЭЖХ (в вес.% от суммарного количества уксусной кислоты (HAc), MCA и DCA), в зависимости от количества электрического заряда, перенесенного во время процесса.
Концентрации монохлоруксусной кислоты (MCA) и дихлоруксусной кислоты (DCA) от количества электрического заряда, перенесенного при электролизе смеси, которая вначале содержит уксусную кислоту, ацетилхлорид, хлорид кальция и хлористый водород (Пример 1)
Пример 2: Хлорирование уксусной кислоты с использованием CaCl2 (в отсутствие HCl)
В реакторе, какой упомянут в Примере 1, 650 граммов смеси 72 вес.% уксусной кислоты (Fluka, № 45731, >99,8 вес.%), 21 вес.% ацетилхлорида (Fluka, № 00990, >99%) и 7 вес.% безводного хлорида кальция (JT. Baker, № 0070, мин. 95 вес.%) предварительно нагревали до 70°C и подвергали электролизу при электрическом токе от 5 до 20 ампер. В отличие от Примера 1, в настоящем примере в реакционную смесь не добавляли газообразный хлористый водород.
Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали методом высокоэффективной жидкостной хроматографии (ВЭЖХ).
Результаты анализа показывают, что MCA может быть получена из этой смеси и в отсутствие хлористого водорода.
Таблица 2 показывает концентрации монохлоруксусной кислоты (MCA) и дихлоруксусной кислоты (DCA), измеренные методом ВЭЖХ (в вес.% от суммарного количества уксусной кислоты (HAc), MCA и DCA) в зависимости от количества электрического заряда, перенесенного во время процесса.
Концентрации монохлоруксусной кислоты (MCA) и дихлоруксусной кислоты (DCA) от количества электрического заряда, перенесенного при электролизе смеси, которая вначале содержит уксусную кислоту, ацетилхлорид и хлорид кальция (Пример 2)
Пример 3: Хлорирование уксусной кислоты с использованием дихлоруксусной кислоты
В реакторе, который упомянут в Примере 1, 700 граммов смеси 60 вес.% уксусной кислоты (Fluka, № 45731, >99,8 вес.%), 19 вес.% ацетилхлорида (Fluka, № 00990, >99%), 5 вес.% безводного хлорида кальция (JT. Baker, № 0070, мин. 95 вес.%) и 16 вес.% дихлоруксусной кислоты (Acros Chemicals, партия A0220473, 99+%) предварительно нагревали до 70°C и подвергали электролизу при электрическом токе 20 ампер. В реакционную смесь добавляли газообразный хлористый водород.
Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали методом высокоэффективной жидкостной хроматографии (ВЭЖХ).
Результаты анализа показывают, что по сравнению с Примером 2 скорость получения MCA в настоящем примере почти в два раза выше. Уксусная кислота хлорирована, а DCA гидрирована до MCA.
Таблица 3 показывает концентрации монохлоруксусной кислоты (MCA) и дихлоруксусной кислоты (DCA), измеренные по ВЭЖХ (в вес.% относительно суммарного количества уксусной кислоты (HAc), MCA и DCA), в зависимости от количества электрического заряда, перенесенного во время процесса.
Концентрации уксусной кислоты (HAc), монохлоруксусной кислоты (MCA) и дихлоруксусной кислоты (DCA) от количества электрического заряда, перенесенного при электролизе смеси, которая вначале содержит уксусную кислоту, ацетилхлорид, монохлоруксусную кислоту, дихлоруксусную кислоту и хлорид кальция (Пример 3)
Пример 4: Хлорирование пропионовой кислоты с использованием HCl
В реакторе, какой упомянут в Примере 1, 840 граммов смеси 65 вес.% пропионовой кислоты (Fluka, № партии 1241470, >99 вес.%), 30 вес.% пропионового ангидрида (Aldrich, партия № 05003 HC-026, 97%) и 5 вес.% безводного хлорида кальция (JT. Baker, № 0070, мин. 95 вес.%) предварительно нагревали до 70°C и подвергали электролизу при электрическом токе от 1 до 9 ампер. В процессе электролиза в реакционную смесь добавляли газообразный хлористый водород.
Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали методом высокоэффективной жидкостной хроматографии (ВЭЖХ).
Результаты анализа показывают, что из смеси может быть получена 1-хлорпропионовая кислота.
Таблица 4 показывает концентрации пропионовой кислоты и 1-хлорпропионовой кислоты, измеренные методом ВЭЖХ (в вес.% от суммарного количества пропионовой кислоты и 1-хлорпропионовой кислоты), в зависимости от количества электрического заряда, перенесенного во время процесса.
Концентрации пропионовой кислоты и 1-хлорпропионовой кислоты от количества электрического заряда, перенесенного при электролизе смеси, которая вначале содержит пропионовую кислоту, пропионовый ангидрид и хлорид кальция (Пример 4)
Сравнительный Пример 5: Хлорирование уксусной кислоты в водной среде
В 1-литровом лабораторном стакане смесь, содержащую 500 мл соляной кислоты (10 вес.% HCl в воде) заряжали и подвергали электролизу при комнатной температуре при токе 2 ампера, чтобы получить газообразный хлор. После двух часов электролиза в реакционную смесь добавляли 150 мл уксусной кислоты (70 вес.%), и подвергали электролизу еще 1,5 часа при 2 амперах при комнатной температуре.
Пробы, отобранные во время процесса, оценивали методом 1H-ЯМР. С помощью ЯМР можно было обнаружить лишь следовые количества MCA, количество DCA было ниже предела обнаружения (предел обнаружения MCA и DCA для этого прибора ЯМР составляет около 50 ppm).
Пример 6: Получение бромуксусной кислоты с использованием LiBr
В реакторе, содержащем графитовые аноды и катоды (материал типа 6503 Le Carbonne Lorraine, Роттердам, Нидерланды) с эффективной площадью анода 580 см2 и эффективной площадью катода 530 см2, 900 граммов смеси, содержащей 11% безводного бромида лития, 33% ацетилбромида и 56% уксусной кислоты (Fluka № 00990, >99%), предварительно нагревали до 70°C и подвергали электролизу при среднем токе 20 ампер. Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали методом высокоэффективной жидкостной хроматографии (ВЭЖХ). После прохождения через электроды заряда 83 А·ч образовано 12,97% бромуксусной кислоты и 0,017% дибромуксусной кислоты.
Пример 7: Хлорирование уксусной кислоты с использованием HCl и хлорида натрия в качестве электролита
В реакторе, содержащем графитовые аноды и катоды (материал типа 6503 Le Carbonne Lorraine, Роттердам, Нидерланды) с эффективной площадью анода 580 см2 и эффективной площадью катода 530 см2, 808 граммов смеси, содержащей 11% безводного хлорида натрия, 33% уксусного ангидрида и 56% уксусной кислоты (Fluka no. 00990, >99%) предварительно нагревали до 70°C и подвергали электролизу при среднем токе 3,8 ампер. В процессе электролиза в реакционную смесь добавляли газообразный хлористый водород. Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали методом высокоэффективной жидкостной хроматографии (ВЭЖХ). После прохождения через электроды заряда 15,9 А·ч образовано 3,66% MCA и 0,043% DCA.
Пример 8: Хлорирование уксусной кислоты с использованием HCl и хлорида лития в качестве электролита
В реакторе, содержащем графитовые аноды и катоды (материал типа 6503 Le Carbonne Lorraine, Роттердам, Нидерланды) с эффективной площадью анода 580 см2 и эффективной площадью катода 530 см2, 808 граммов смеси, содержащей 1,3% безводного хлорида лития, 6,6% ацетилхлорида и 92,1% уксусной кислоты (Fluka № 00990, >99%) предварительно нагревали до 70°C и подвергали электролизу при среднем токе 20 ампер. В процессе электролиза в реакционную смесь добавляли газообразный хлористый водород. Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали методом высокоэффективной жидкостной хроматографии (ВЭЖХ). После прохождения через электроды заряда 112 А·ч образовано 22,76% MCA и 0,108% DCA.
Пример 9: Хлорирование уксусной кислоты с использованием HCl и хлорида калия в качестве электролита
В реакторе, содержащем графитовые аноды и катоды (материал типа 6503 Le Carbonne Lorraine, Роттердам, Нидерланды) с эффективной площадью анода 580 см2 и эффективной площадью катода 530 см2, 808 граммов смеси, содержащей 10% безводного хлорида калия, 24% ацетилхлорида и 66% уксусной кислоты (Fluka № 00990, >99%) предварительно нагревали до 70°C и подвергали электролизу при среднем токе 10 ампер. В процессе электролиза в реакционную смесь добавляли газообразный хлористый водород. Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали методом высокоэффективной жидкостной хроматографии (ВЭЖХ). После прохождения через электроды заряда 57,7 А·ч образовано 13,39% MCA и 0,57% DCA.
Пример 10: Хлорирование уксусной кислоты с использованием трихлоруксусной кислоты и HCl.
В реакторе, содержащем графитовые аноды и катоды (материал типа 6503 Le Carbonne Lorraine, Роттердам, Нидерланды) с эффективной площадью анода 580 см2 и эффективной площадью катода 530 см2, 808 граммов смеси, содержащей 11,9% трихлоруксусной кислоты (TCA), 4,8% безводного хлорида лития, 11,9% ацетилхлорида и 71,4% уксусной кислоты (Fluka № 00990, >99%) предварительно нагревали до 70°C и подвергали электролизу при среднем токе 30 ампер. В процессе электролиза в реакционную смесь добавляли газообразный хлористый водород. Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали методом высокоэффективной жидкостной хроматографии (ВЭЖХ).
Результаты в Таблице 5 показывают, что в конце процесса содержание и DCA, и TCA уменьшались, а содержание MCA повышалось.
Концентрации монохлоруксусной кислоты (MCA), дихлоруксусной кислоты (DCA) и трифторуксусной кислоты (TCA) из Примера 10, измеренные методом ВЭЖХ (в вес.% от общего количества уксусной кислоты (Hac), MCA, TCA и DCA), в зависимости от количества электрического заряда, перенесенного во время процесса
Пример 11: Восстановление маточного раствора с литийхлоридом в качестве электролита (Хлорирование уксусной кислоты с использованием дихлоруксусной кислоты и HCl)
В реакторе, содержащем графитовые аноды и катоды (материал типа 6503 Le Carbonne Lorraine, Роттердам, Нидерланды) с эффективной площадью анода 580 см2 и эффективной площадью катода 530 см2, 1007 граммов смеси, содержащей 30% дихлоруксусной кислоты (DCA), 5% безводного хлорида лития, 15% ацетилхлорида, 30% монохлоруксусной кислоты (MCA) и 20% уксусной кислоты (Fluka № 00990, >99%) предварительно нагревали до 70°C и подвергали электролизу при среднем токе 30 ампер. В процессе электролиза в реакционную смесь добавляли газообразный хлористый водород.
Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали методом высокоэффективной жидкостной хроматографии (ВЭЖХ). Результаты в Таблице 6 показывают, что в конце процесса содержание и Hac, и DCA уменьшалось, а содержание MCA увеличивалось.
Концентрации монохлоруксусной кислоты (MCA), дихлоруксусной кислоты (DCA) и уксусной кислоты (HAc) из Примера 11, измеренные методом ВЭЖХ (в вес.% от суммарного количества HAc, MCA и DCA), в зависимости от количества электрического заряда, перенесенного во время процесса
Пример 12: Восстановление маточного раствора с хлоридом кальция в качестве электролита (Хлорирование уксусной кислоты с использованием дихлоруксусной кислоты и HCl)
В реакторе, содержащем графитовые аноды и катоды (материал типа 6503 Le Carbonne Lorraine, Роттердам, Нидерланды) с эффективной площадью анода 580 см2 и эффективной площадью катода 530 см2, 1007 граммов смеси, содержащей 30% дихлоруксусной кислоты (DCA), 5% безводного хлорида кальция, 15% ацетилхлорида, 30% монохлоруксусной кислоты (MCA) и 20% уксусной кислоты (Fluka № 00990, >99%) предварительно нагревали до 70°C и подвергали электролизу при среднем токе 30 ампер. В процессе электролиза в реакционную смесь добавляли газообразный хлористый водород.
Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали методом высокоэффективной жидкостной хроматографии (ВЭЖХ). Результаты в Таблице 7 показывают, что в конце процесса содержание и Hac, и DCA уменьшалось, а содержание MCA возрастало.
Концентрации монохлоруксусной кислоты (MCA), дихлоруксусной кислоты (DCA) и уксусной кислоты (HAc) из Примера 12, измеренные методом ВЭЖХ (в вес.% по отношению к суммарному количеству HAc, MCA, и DCA), в зависимости от количества электрического заряда, перенесенного во время процесса
Пример 13: Восстановление маточного раствора с хлоридом магния в качестве электролита (Хлорирование уксусной кислоты с использованием дихлоруксусной кислоты и HCl)
В реакторе, содержащем графитовые аноды и катоды (материал типа 6503 Le Carbonne Lorraine, Роттердам, Нидерланды) с эффективной площадью анода 580 см2 и эффективной площадью катода 530 см2, 1007 граммов смеси, содержащей 30% дихлоруксусной кислоты (DCA), 5,2% безводного хлорида магния, 15% ацетилхлорида, 30% монохлоруксусной кислоты (MCA) и 20% уксусной кислоты (Fluka № 00990, >99%) предварительно нагревали до 70°C и подвергали электролизу при среднем токе 30 ампер. В процессе электролиза в реакционную смесь добавляли газообразный хлористый водород. Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали методом высокоэффективной жидкостной хроматографии (ВЭЖХ). Результаты в Таблице 8 показывают, что в конце процесса содержание и Hac, и DCA уменьшается, а содержание MCA возрастает.
Концентрации монохлоруксусной кислоты (MCA), дихлоруксусной кислоты (DCA) и уксусной кислоты (HAc) из Примера 13, измеренные методом ВЭЖХ (в % от суммарного весового количества HAc, MCA, и DCA) в зависимости от количества электрического заряда, перенесенного во время процесса.
Пример 14: Хлорирование уксусной кислоты с использованием HCl и хлорида цинка в качестве электролита
В реакторе, содержащем графитовые аноды и катоды (материал типа 6503 Le Carbonne Lorraine, Роттердам, Нидерланды) с эффективной площадью анода 580 см2 и эффективной площадью катода 530 см2, 1607 граммов смеси, содержащей 5% безводного хлорида цинка, 13% ацетилхлорида и 82% уксусной кислоты (Fluka № 00990, >99%) предварительно нагревали до 70°C и подвергали электролизу при среднем токе 25 ампер. В процессе электролиза в реакционную смесь добавляли газообразный хлористый водород. Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали методом высокоэффективной жидкостной хроматографии (ВЭЖХ). После прохождения через электроды заряда 162 А·ч образовано 15,67% MCA и 0,10% DCA.
Пример 15: Хлорирование уксусной кислоты хлоридом железа(III) в качестве электролита
В реакторе, содержащем графитовые аноды и катоды (материал типа 6503 Le Carbonne Lorraine, Роттердам, Нидерланды) с эффективной площадью анода 580 см2 и эффективной площадью катода 530 см2, 1607 граммов смеси, содержащей 5% безводного хлорида железа(III), 13% ацетилхлорида и 82% уксусной кислоты (Fluka № 00990, >99%) предварительно нагревали до 70°C и подвергали электролизу при среднем токе 30 ампер. В процессе электролиза в реакционную смесь добавляли газообразный хлористый водород. Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали методом высокоэффективной жидкостной хроматографии (ВЭЖХ). После прохождения через электроды заряда 192 А·ч образовано 4,73% MCA и 0,10% DCA.
Пример 16: Хлорирование уксусной кислоты с использованием HCl и хлорида алюминия в качестве электролита
В реакторе, содержащем графитовые аноды и катоды (материал типа 6503 Le Carbonne Lorraine, Роттердам, Нидерланды) с эффективной площадью анода 580 см2 и эффективной площадью катода 530 см2, 1607 граммов смеси, содержащей 5% безводного хлорида алюминия, 13% ацетилхлорида и 82% уксусной кислоты (Fluka, № 00990, >99%) предварительно нагревали до 70°C и подвергали электролизу при среднем токе 30 ампер. В процессе электролиза в реакционную смесь добавляли газообразный хлористый водород. Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали методом высокоэффективной жидкостной хроматографии (ВЭЖХ). После прохождения через электроды заряда 119 А·ч образовано 12,29% MCA и 0,02% DCA.
Пример 17: Хлорирование диметилпентанона с использованием HCl
В реакторе, содержащем графитовые аноды и катоды (материал типа 6503 Le Carbonne Lorraine, Роттердам, Нидерланды) с эффективной площадью анода 47 см2 и эффективной площадью катода 16 см2, 61 грамм смеси, содержащей 6% безводного хлорида лития, 94% 2,4-диметилпентанона предварительно нагревали до 70°C и подвергали электролизу при среднем токе 0,3 ампер. В процессе электролиза в реакционную смесь добавляли газообразный хлористый водород. Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали посредством ЯМР.
Результаты в Таблице 9 показывают, что в конце процесса образуется 2-хлор-2,4-диметилпентанон.
Концентрации (в моль%) 2,4-диметилпентанона и 2-хлор-2,4-диметилпентанона из Примера 17, измеренные методом ЯМР
Сравнительный Пример 18: Фторирование уксусной кислоты с использованием трифторуксусной кислоты (TFA)
В реакторе, содержащем графитовые аноды и катоды (материал type 6503 Le Carbonne Lorraine, Роттердам, Нидерланды) с эффективной площадью анода 47 см2 и эффективной площадью катода 16 см2, 99 граммов смеси, содержащей 4% безводного хлорида лития, 35,4% TFA, 35,4% уксусной кислоты и 25,2% ацетилхлорида предварительно нагревали до 70°C и подвергали электролизу при среднем токе 2 ампер. Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали посредством ЯМР. В пробах не было найдено никаких свидетельств образования монофторуксусной кислоты или дифторуксусной кислоты. Были обнаружены только MCA и небольшие количества DCA.
Сравнительный Пример 19: Фторирование уксусной кислоты с использованием KF
В реакторе, содержащем графитовые аноды и катоды (материал типа 6503 Le Carbonne Lorraine, Роттердам, Нидерланды) с эффективной площадью анода 47 см2 и эффективной площадью катода 16 см2, 99 граммов смеси, содержащей 4,3% безводного фторида калия, 68,5% уксусной кислоты и 27,2% ацетилхлорида, предварительно нагревали до 70°C и подвергали электролизу при среднем токе 0,4 ампер. Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали посредством ЯМР. В пробах не было найдено никаких свидетельств об образовании монофторуксусной кислоты или дифторуксусной кислоты. Были обнаружены только MCA и небольшие количества DCA.
Пример 20: Хлорирование додекановой кислоты с использованием HCl и LiCl в качестве электролита
В реакторе, содержащем графитовые аноды и катоды (материал типа 6503 Le Carbonne Lorraine, Роттердам, Нидерланды) с эффективной площадью анода 47 см2 и эффективной площадью катода 16 см2, 92 граммов смеси, содержащей 4,9% безводного хлорида лития, 35,3% уксусной кислоты, 35,3% додекановой кислоты и 24,5% ацетилхлорида, предварительно нагревали до 70°C и подвергали электролизу при среднем токе 1 ампер. Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали посредством ЯМР. После прохождения через электроды заряда 3,4 А·ч образовано 1,3 моль% 2-хлордодекановой кислоты.
Пример 21: Хлорирование октодекановой кислоты с использованием HCl
В реакторе, содержащем графитовые аноды и катоды (материал типа 6503 Le Carbonne Lorraine, Роттердам, Нидерланды) с эффективной площадью анода 47 см2 и эффективной площадью катода 16 см2, 92 граммов смеси, содержащей 4,7% безводного хлорида лития, 38,3% уксусной кислоты, 33,6% октодекановой кислоты и 23,4% ацетилхлорида, предварительно нагревали до 70°C и подвергали электролизу при среднем токе 1 ампер. Пробы, отбиравшиеся из электролита в процессе электролиза, анализировали посредством ЯМР. После прохождения через электроды заряда 3,2 А·ч образовано 1,3 моль% 2-хлороктодекановой кислоты.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЕ HCl-СОДЕРЖАЩЕГО ГАЗОВОГО ПОТОКА | 2016 |
|
RU2710335C2 |
| ЭЛЕКТРОКАТАЛИТИЧЕСКИЙ СПОСОБ СИНТЕЗА УГЛЕВОДОРОДОВ И СПИРТОВ НА ОСНОВЕ РАСТИТЕЛЬНОГО СЫРЬЯ | 2011 |
|
RU2471890C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЙОДИРУЮЩЕГО АГЕНТА | 2010 |
|
RU2528402C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГАЛОГЕНИРОВАННЫХ ПАРАФИНОВ НА ОСНОВЕ ВЫСШИХ АЛЬФА-ОЛЕФИНОВ | 2005 |
|
RU2288908C1 |
| СПОСОБ ГИДРОДЕХЛОРИРОВАНИЯ ИСХОДНОГО МАТЕРИАЛА, СОДЕРЖАЩЕГО ДИХЛОРУКСУСНУЮ КИСЛОТУ | 2016 |
|
RU2724102C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОКИСЛЕННОГО ГРАФИТА, УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ И ЕГО ВАРИАНТ | 2003 |
|
RU2264983C2 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОГО ПОЛУЧЕНИЯ ФОСФИНА ИЗ НЕВОДНОГО РАСТВОРА БЕЛОГО ФОСФОРА | 2011 |
|
RU2469130C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОХЛОРУКСУСНОЙ КИСЛОТЫ | 2016 |
|
RU2674474C1 |
| СЕЛЕКТИВНОЕ ЭЛЕКТРОХИМИЧЕСКОЕ ВОССТАНОВЛЕНИЕ ГАЛОГЕНИРОВАННЫХ 4-АМИНОПИКОЛИНОВЫХ КИСЛОТ | 2001 |
|
RU2254401C2 |
| СПОСОБ СИНТЕЗА ЯДЕРНОГО ТОПЛИВА ДЛЯ ЭНЕРГЕТИЧЕСКИХ РЕАКТОРОВ НА БЫСТРЫХ НЕЙТРОНАХ С АКТИВНОЙ ЗОНОЙ ИЗ СОЛЕВОГО РАСПЛАВА | 2008 |
|
RU2450373C2 |
Изобретение относится к способу получения галогенированного соединения, содержащего карбонильную группу, путем электрохимической реакции соответствующего соединения, содержащего карбонильную группу, с гидрогалогенидом Н-Х, органическим галогенидом R′-X и/или галогенидной солью Мn+-Хn - в по существу безводных условиях, причем X означает атом хлора, брома или йода, R′ означает алкильную или арильную группу, которая может быть линейной или разветвленной, при необходимости содержащей один или более гетероатомов, таких как кислород, азот, хлорид, бромид, фторид или йодид, от которых атом галогена X может быть отщеплен электрохимически, Мn+ означает катион четвертичного аммония, щелочноземельного металла, щелочного металла или металла, и n есть целое число от 1 до 5 в зависимости от валентности катиона металла Мn+. Предложенный способ не требует дополнительной обработки образующихся побочных продуктов, обеспечивает пониженное содержание полигалогенированных побочных продуктов при простоте осуществления галогенирования соединений, содержащих карбонильную группу и водород. 2 н. и 11 з.п. ф-лы, 2 ил., 9 табл.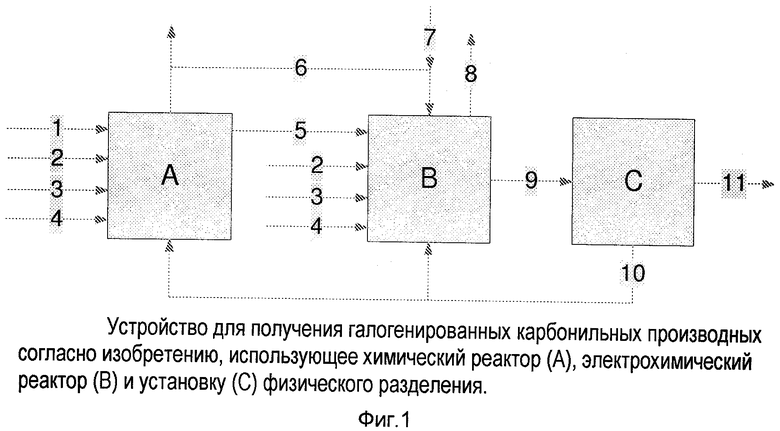
1. Способ получения галогенированного соединения, содержащего карбонильную группу, путем электрохимической реакции соответствующего соединения, содержащего карбонильную группу, с гидрогалогенидом Н-Х, органическим галогенидом R′-X и/или галогенидной солью Мn+-Хn ′′ в, по существу, безводных условиях, причем X означает атом хлора, брома или йода, R' означает алкильную или арильную группу, которая может быть линейной или разветвленной, по выбору содержащей один или более гетероатомов, таких, как кислород, азот; хлорид, бромид, фторид или йодид, от которых атом галогена X может быть отщеплен электрохимически, Мn+ означает катион четвертичного аммония, щелочноземельного металла, щелочного металла или металла, и n есть целое число от 1 до 5 в зависимости от валентности катиона металла Мn+.
2. Способ по п.1, причем органический галогенид R′-X является дважды и/или более галогенированным соединением, содержащим карбонильную группу.
3. Способ по п.1 или 2, причем полученное галогенированное соединение, содержащее карбонильную группу, является моногалогенированным соединением.
4. Способ по любому из пп.1-2, причем полученное галогенированное соединение, содержащее карбонильную группу, галогенировано у атома 6-углерода.
5. Способ получения галогенированного соединения, содержащего карбонильную группу, сначала путем химической реакции соединения, содержащего карбонильную группу, с молекулами хлора, брома или йода и последующей электрохимической обработкой реакционной смеси в соответствии со способом по п.1.
6. Способ получения галогенированного соединения, содержащего карбонильную группу, в котором маточный раствор, полученный при моногалогенировании соединения, содержащего карбонильную группу, отделяют от реакционной смеси, содержащей как моногалогенированное соединение с карбонильной группой, так и ди- и/или более галогенированное соединение, содержащее карбонильную группу, используют в способе, включающем электрохимическую реакции соответствующего соединения, содержащего карбонильную группу, с ди- и/или более галогенированным соединением, содержащим карбонильную группу, по выбору, гидрогалогенидом Н-Х, дополнительным органическим галогенидом R′-X и/или галогенидной солью Мn+-Хn ′′ в, по существу, безводных условиях, причем X означает атом хлора, брома или йода, R' означает алкильную или арильную группу, которая может быть линейной или разветвленной, по выбору содержащей один или более гетероатомов, от которых атом галогена X может быть отщеплен электрохимически, Мn+ означает катион четвертичного аммония, или металла, и n есть целое число от 1 до 5 в зависимости от валентности катиона металла Мn+.
7. Способ по п.6, в котором добавляют дополнительно соединение, содержащее карбонильную группу.
8. Способ по любому из пп.1, 2, 5, 6 или 7, причем X означает атом хлора.
9. Способ по любому из пп.1, 2, 5, 6 или 7, причем соединение, содержащее карбонильную группу, является уксусной кислотой, или пропионовой кислотой, или жирной кислотой.
10. Способ по п.1, в котором в реакционной смеси дополнительно присутствует поддерживающий электролит.
11. Способ по любому из пп.1, 2, 5, 6, 7 или 10, причем поддерживающий электролит является хлорной солью.
12. Способ по любому из пп.1, 2, 5, 6, 7 или 10, причем в реакционную смесь дополнительно добавляют катализатор, выбранный из группы ацилгалогенидов и ангидридов карбоновой кислоты.
13. Способ по любому из пп 1, 2, 5, 6, 7 или 10, проводимый, по существу, в отсутствие каких-либо растворителей.
| GB 1026187 А, 14.04.1966 | |||
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРЛИГНИНА | 1996 |
|
RU2109849C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГАЛОГЕНИРОВАННЫХ ПОЛИМЕРОВ | 2000 |
|
RU2217440C2 |
| DE 19849922 А1, 04.05.2000 | |||
| Сопло для точечной сварки плавлением | 1978 |
|
SU965660A1 |
| WO 9724473 А1, 10.07.1977 | |||
| GB 1424520 А, 18.12.1972. | |||
Авторы
Даты
2011-07-10—Публикация
2007-05-11—Подача