Данное изобретение относится к получению некоторых 4-аминопиколиновых кислот электрохимическим восстановлением. Более конкретно данное изобретение относится к селективному восстановлению галогенных заместителей в 5-положении галогенированных 4-аминопиколиновых кислот в присутствии галогенных заместителей в 3- и 6-положениях.
Недавно было установлено, что некоторые производные 4-амино-3-галогенпиколиновой кислоты, содержащие водород в 5-положении, используются в качестве гербицидов. Было бы желательно иметь возможность получать указанные гербициды из соответствующих 5-галогенпроизводных, многие из которых являются коммерчески доступными, такие как 4-амино-3,5,6-трихлорпиколиновая кислота (пиклорам).
Хотя химическое восстановление галогенированных пиридинов является известным, смотри, например, патент США 4087431, в котором гидразин используется в качестве восстановителя, эффективность использования материала является низкой, и стоимость является относительно высокой. Электролитическое восстановление, с другой стороны, может быть очень эффективным, а также селективным. Патент США 3694332 рассматривает селективное электролитическое восстановление галогенированных пиридинов и галогенированных цианпиридинов в 4-положении. Патент США 4217185 рассматривает электролитическое восстановление тетрахлорпиколиновой кислоты в 4- и 5-положениях. Патент США 4242183 рассматривает электролитическое восстановление симметричного тетрахлорпиридина до 2,3,5-трихлорпиридина с использованием активированного серебряного сетчатого электрода. Указанный патент также патентует способы активирования серебряного катода. Российский патент SU 1807686 А1 рассматривает электролитическое восстановление полихлорированных пиридинкарбоновых кислот. Такие селективные электролитические восстановления ограничиваются галогенированными пиридинами, которые содержат только карбоновую кислоту или цианзаместители. Было бы желательно иметь электрохимические способы, которые могут селективно восстанавливать галогенированные пиридины, содержащие другие заместители.
Теперь установлено согласно настоящему изобретению, что 4-амино-3-галогенпиколиновые кислоты могут быть получены электрохимическим восстановлением соответствующих 4-амино-3,5-дигалогенпиколиновых кислот. Более конкретно, настоящее изобретение относится к способу получения 4-амино-3-галогенпиколиновой кислоты формулы I
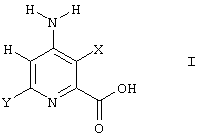
в которой
Х представляет Сl или Вr;
Y представляет Н, F, Сl, Вr или С1-С4-алкил; и
при этом способ предусматривает пропускание постоянного или переменного электрического тока от анода к катоду через раствор 4-амино-З,5-дигалогенпиколиновой кислоты формулы II:
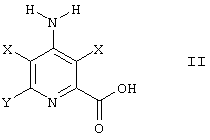
в которой
X, Y и R являются такими, как определено ранее, и в которой оба Х представляют либо Сl, либо Вr,
при катодном потенциале от -0,4 до -1/7 В относительно электрода сравнения Ag/AgCl (3,0 М Сl-) и извлечение продукта при условии, что когда Х представляет Сl, тогда Y не является Вr. Неожиданно было обнаружено, что галоген в 5-положении селективно удаляется в присутствии 4-аминогруппы с высоким выходом.
Как использовано здесь, термин "галоген" относится к Сl или Вr.
Реакции, заключающиеся в восстановлении 4-амино-3,5-дигалогенпиколиновой кислоты, могут быть изображены следующим образом:
А) Нейтрализация:
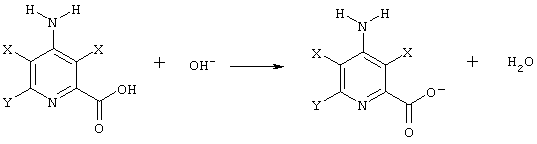
В) Катодная реакция:
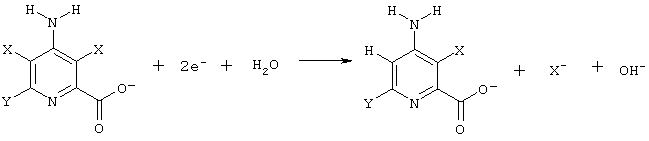
C) Анодная реакция:
2 (ОН-)→1/2 O2+Н2О+2е-;
D) Суммарная реакция:
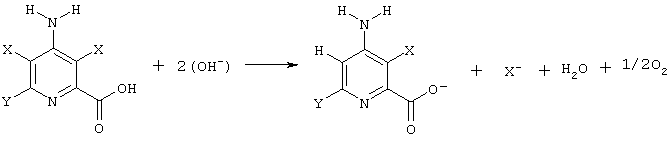
Карбоновую кислоту извлекают подкислением реакционной смеси и извлечением продукта по традиционной технологии.
Требуемое электролитическое восстановление осуществляют по технологии, которая хорошо известна в технике. В общем случае исходную 4-амино-3,5-дигалогенпиколиновую кислоту растворяют в растворителе с получением электролита, который вводят в электролитическую ячейку, после чего через электролит пропускают достаточный электрический ток до получения требуемой степени восстановления.
Специалисты в данной области техники отметят, что восстановительный потенциал брома примерно на 0,5 В превышает (менее отрицателен) сравнительный потенциал хлора. Бром всегда будет восстанавливаться первым. Таким образом, когда Х является Cl, Y не может быть Вr.
Конструкция электролизера не является определяющей. Электролиз может проводиться периодическим, непрерывным или полунепрерывным способом. Электролизером может быть реактор с перемешиванием, содержащий электроды, или проточный электролизер любой традиционной конструкции. В некоторых случаях может быть желательно использовать сепаратор для разделения электролизера на отдельные анодный отсек и катодный отсек. Примерами используемых сепараторных материалов являются различные анионообменные и катионообменные мембраны, пористый тефлон, асбесты и стекло. Хотя использование трех электродов, когда катодный потенциал регулируется относительно электрода сравнения, является предпочтительным, электролиз альтернативно может осуществляться с использованием только двух электродов (анода и катода) с регулированием либо тока электролизера, либо напряжения электролизера, либо того и другого. Для удобства 3-электродный неразделенный электролизер, в котором электролит служит как католитом, так и анолитом, является предпочтительным.
Анодом может быть любой химически инертный материал, включая, например, платину, графит, углерод, оксиды металлов, такие как оксид серебра на серебре, или сплавы, такие как сплав Хастеллой С, причем графит, углерод и сплав Хастеллой С являются предпочтительными. Аналогично катод может быть выполнен из ряда материалов, включая ртуть, свинец, железо, олово, цинк или серебро, причем серебро является предпочтительным. Электроды могут быть в виде пластин, стержней, проволоки, экранов, тонкой сетки, ваты или слоев, причем экраны из тянутой сетки являются предпочтительными. Анод или катод может также состоять из покрытия, нанесенного на другой материал, примером которого является оксид благородного металла, такой как оксид рутения, нанесенный на титан.
Наиболее предпочтительными катодами являются активированные серебряные катоды, полученные, как описано в патентах США 4217185 и 4242183. Такие активированные катоды могут быть получены нанесением слоя микрокристаллов серебра на проводящую подложку с формованием композитного электрода или анодированием самого серебряного электрода. Например, для иллюстрации последнего неактивированный серебряный электрод можно окунуть или погрузить в щелочной водный католитический раствор и анодировать с превращением в результате части серебра на поверхности электрода в коллоидный оксид серебра и с одновременным приданием поверхности шероховатости. Полярность электрода затем меняется на противоположную, и оксид электролитически превращается в частицы микрокристаллического серебра, адгезировавшие к поверхности электрода. Методика активирования заключается в увеличении потенциала от начального значения 0 В до конечного значения не менее +0,3 В и предпочтительно +0,7 В. Восстановление оксидного слоя требует отрицательной поляризации катода. Катодный потенциал постепенно снижается от значения +(0,3-0,7) В, ожидаемого в процессе стадии окисления, до значения -0,5 В или ниже. В данном способе нет необходимости вводить какое-либо количество серебра в католит или водное основание.
Вода является наиболее предпочтительным растворителем для электролиза, но в некоторых случаях можно использовать органический растворитель либо в отдельности, либо в качестве сорастворителя. Растворитель или система с сорастворителем должны растворять весь или большую часть исходного материала и электролита или, по меньшей мере, достаточную для обеспечения протекания восстановления с приемлемой скоростью. Кроме того, растворитель или система с сорастворителем должны быть инертными к условиям электролиза, т.е. они не должны отрицательно воздействовать или взаимодействовать с материалами катода или католита в недопустимой степени. Иные, чем вода, предпочтительные растворители/сорастворители смешиваются с водой и включают низкомолекулярные спирты, простые эфиры, такие как тетрагидрофуран, диоксан и эфиры полигликоля, и низшие амиды, такие как диметилформамид или диметилацетамид.
Гидроксиды щелочных металлов являются предпочтительными в качестве фонового электролита, но могут быть использованы многие другие вещества, такие как гидроксиды, хлориды, карбонаты четвертичного аммония или металлов и т.д. NaOH является наиболее предпочтительным фоновым электролитом.
В реакции один эквивалент основания требуется для нейтрализации исходного материала, и дополнительный эквивалент требуется для генерирования гидроксильных ионов, которые потребляются в электролизе. Реакция обычно протекает с избытком основания, предпочтительно с 0,05-2 % мас. избытка основания в процессе реакции.
Концентрация галогенированной 4-аминопиколиновой кислоты в католите или питании может быть от 1 до 20 % мас., предпочтительно от 8 до 12 % мас. Низкие концентрации снижают продуктивность, тогда как высокие концентрации обычно дают более низкие выходы, чистоту продукта и электрическую эффективность.
Подходящие температуры для электролиза обычно находятся в интервале от 5 до 90°С. Предпочтительный температурный интервал составляет от 20 до 60°С. Наиболее предпочтительным является интервал от 20 до 40°С.
Специалист в данной области техники отметит, что кажущийся катодный потенциал, при котором галоген будет селективно восстанавливаться, зависит от целого ряда факторов, включающих, например, структуру конкретной подложки, конфигурацию электролизера и расстояние, разделяющее электроды. В общем случае катодный потенциал относительно стандартного Аg/АgСl (3,0 М Сl-)-электрода должен находиться в интервале от -0,4 до -1,1 В для Вr и в интервале от -0,8 до -1,7 В для Сl. Для Вr катодный потенциал предпочтительно составляет от -0,6 до -0,9 В. Для Сl катодный потенциал предпочтительно составляет от -1,0 до -1,4 В. Плотность тока в амперах на квадратный сантиметр (А/см2) должна быть не менее 0,005, предпочтительно 0,05 А/см2 или более.
Хотя выделение молекулярного кислорода является предпочтительным, могут быть использованы многие другие анодные реакции. Примеры включают выделение молекулярного хлора или брома, окисление теряемых частиц, таких как формиат или оксалат, с получением углекислого газа, или окисление органического субстрата с образованием ценного сопродукта.
В предпочтительном в настоящее время варианте галогенированную 4-аминопиколиновую кислоту растворяют в водной щелочи с образованием щелочного водного раствора, который непрерывно циркулирует через разделенный электролизер, имеющий серебряный катод из тянутой сетки, активированный анодированием при +0,7 В в водном щелочном электролите. При поддержании реакционной смеси щелочной электролиз при катодном потенциале от -0,6 до -1,5 В относительно Ag/AgCl (3,0 М Сl-)-электрода сравнения продолжают до достижения требуемой степени восстановления. Требуемый продукт извлекают по традиционной технологии. Например, кислота может быть высаждена из реакционной смеси подкислением с последующей либо фильтрацией, либо экстракцией органическим растворителем, не смешивающимся с водой.
Следующие примеры иллюстрируют настоящее изобретение.
Примеры
Пример 1
Получение 4-амино-3,6-дихлорпиридин-2-карбоновой кислоты (проточный электролизер)
В 3-хлитровый (л) химический стакан загружают 2000 г горячей воды, 115,1 г 50 % мас. NaOH и 200 г сырой 4-амино-3,5,6-трихлорпиридин-2-карбоновой кислоты (79,4 %). Раствор перемешивают в течение 30 мин, фильтруют через бумажный фильтр и транспортируют в 5 л емкость питания/рециркуляции. Указанный раствор имеет массу 2315 г и содержит 6,8% 4-амино-3,5,6-трихлорпиридин-2-карбоновой кислоты. Указанное питание рециркулируют со скоростью примерно 9,46 л/мин и при температуре 30°С через разделенный электролизер, имеющий анод из сплава Хастеллой С (15 см × 4 см) и серебряный катод из тянутой сетки (15 см × 4 см). После обычного анодирования при +0,7 В меняют полярность электролизера на противоположную и начинают электролиз. Рабочий катодный потенциал регулируют в интервале от -1,1 до -1,4 В относительно Ag/AgCl (3,0 М Cl-)-электрода сравнения. Электрод сравнения физически размещают непосредственно позади серебряного электрода и соединяют электрически с водным солевым мостиком. При рециркуляции питания 50% раствор NaOH медленно прокачивают в емкость рециркуляции с поддержанием концентрации NaOH при избытке 1,5-2,0 %. Ток находится в интервале от 1,0 до 5,2 А.
После примерно 15 часов (ч) и пропускания примерно 213100 Кл через систему электролиз прекращают и выходящий из электролизера поток фильтруют через бумажный фильтр. Раствор нейтрализуют концентрированной НСl и концентрируют его до примерно 750 г сырого концентрата. Концентрат подогревают при 85°С при перемешивании и рН корректируют до менее 1 с помощью концентрированной НСl в течение 30 мин. Полученную суспензию охлаждают до температуры окружающей среды и фильтруют. Остаток на фильтре промывают 3×200 мл порциями воды и сушат в вакууме при 80°С. Высушенный продукт, 118,1 г, определен при 90,6% требуемого продукта; газовой хроматографией (ГХ) показано, что примерно 4% 4-амино-3,5,6-трихлорпиридин-2-карбоновой кислоты остается в качестве примеси. Очищенный образец 4-амино-3,6-дихлорпиридин-2-карбоновой кислоты имеет температуру плавления 185-187°С (декалин).
1H-ЯМР (ДМСО-d6): δ 13,9 (шир, 1Н), 7,0 (шир м, 2Н), 6,8 (с, 1Н) ; 13С-ЯМР {1Н} (ДМСО-d6): δ 165,4 (1C), 153,4 (1C), 149,5 (1С), 147,7 (1С), 111,0 (1C), 108,1 (1C).
Пример 2
Получение 4-амино-3,6-дихлорпиридин-2-карбоновой кислоты (электролизер периодического действия)
Электролизером является 180 мл химический стакан (2 дюйм (5,1 см) диаметр × 4,5 дюйм (11,4 см) высота). Серебряный сетчатый катод состоит из ленты 1 дюйм (2,5 см) × 4 дюйм (10,2 см), помещенной вокруг внутренней стенки химического стакана приблизительно на 0,5 дюйм (1,3 см) от дна, и имеет ленту шириной 0,5 дюйм (1,3 см), отходящую от верха химического стакана, к которому подключена подача энергии. Анодом является графитовый стержень диаметром 0,75 дюйм (1,9 см) и длиной 6 дюйм (15,2 см), поддерживаемый резиновой пробкой в середине химического стакана и отстоящий примерно на 0,5 дюйм (1/3 см) от дна. Рабочий потенциал катода регулируют относительно Аg/АgСl (3,0 М Сl-)-электрода сравнения, расположенного между серебряной сеткой и стенкой химического стакана.
Серебряный сетчатый катод активируют анодированием при +0,7 В в 2%-ном растворе гидроксида натрия и 1%-ном растворе хлорида натрия в воде с последующей обратной поляризацией. После активирования раствор заменяют раствором 81 мл воды, 5,1 г (0,0213 моль) 4-амино-3,5,6-трихлорпиколиновой кислоты и 2,8 г (0,0426 моль) 85% КОН. После продувки медленным током азота проводят электролиз при рабочем потенциале от -1,3 до -1,5 В в течение 2 часов при температуре окружающей среды. Ток имеет начальное значение 0,83 А, которое постепенно снижается до 0,25 А после 2 часов. Суммарное количество 5000 Кл пропускают через раствор (теоретическое количество для восстановления одного хлора из пиридинового кольца составляет 2050 Кл). Анализ сырого продукта методом градиентного элюирования ВЭЖХ показывает исчезновение исходного материала и появление единичного пика, позже идентифицированного как 4-амино-3,6-дихлорпиколиновая кислота.
Пример 3
Получение 4-амино-3,6-дибромпиридин-2-карбоновой кислоты (электролизер периодического действия)
Используют такой же электролизер периодического действия, как описано в примере 2.
В электролизер загружают 75 мл раствора 1% хлорида натрия и 2% гидроксида натрия в воде. Активируют серебряный катод и затем в раствор в электролизере вводят 0,635 г метилового эфира 4-амино-3,5,6-трибромпиколиновой кислоты. После нагревания раствора примерно при 75°С в течение 30 мин с гидролизом сложного эфира до карбоксилатного аниона раствор охлаждают до комнатной температуры. Проводят электролиз в течение 45 мин при рабочем катодном потенциале -0,7 В. Ток составляет 0,44 А в начале и падает до 0,12 А в конце реакции. Пропускают суммарно 400 Кл.
Извлекают электролитический раствор, корректируют рН раствора до нейтрального и выпаривают раствор до высыхания. Извлеченное твердое вещество растворяют в смеси ацетонитрил-вода и извлекают продукт препаративной ВЭЖХ. Получают образец 110 мг единственного изомера с чистотой >98 % по ВЭЖХ и 1H-ЯМР, идентифицированного как 4-амино-3,6-дибромпиколиновая кислота.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 3,6-дихлорпиколиновой кислоты | 1980 |
|
SU1077568A3 |
| СПОСОБ ОБОГАЩЕНИЯ ВОДЫ КИСЛОРОДОМ ПОСРЕДСТВОМ ЭЛЕКТРОЛИТИЧЕСКОГО ПРОЦЕССА, ВОДА ИЛИ НАПИТОК, ОБОГАЩЕННЫЕ КИСЛОРОДОМ, И ИХ ПРИМЕНЕНИЕ | 2008 |
|
RU2492146C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ И ВЫЩЕЛАЧИВАНИЯ МЕТАЛЛОВ ИЗ МИНЕРАЛЬНОГО СЫРЬЯ, УСТРОЙСТВО ДЛЯ ИХ ОСУЩЕСТВЛЕНИЯ | 1993 |
|
RU2111270C1 |
| Электрохимическая ячейка для получения 3,6-дихлорпиколиновой кислоты | 1987 |
|
SU1830086A3 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОГО ДЕХЛОРИРОВАНИЯ ПОЛИХЛОРПИРИДИНКАРБОНОВЫХ КИСЛОТ | 1990 |
|
SU1807686A1 |
| ЭЛЕКТРОЛИЗНАЯ ЯЧЕЙКА И ЭЛЕКТРОЛИЗЕР | 2013 |
|
RU2575343C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЦИНКА | 2002 |
|
RU2298585C9 |
| СПОСОБ ЭЛЕКТРОЛИТИЧЕСКОЙ РЕГЕНЕРАЦИИ СЕРЕБРА ИЗ СЕРЕБРЯНОГО ПОКРЫТИЯ НА МЕТАЛЛИЧЕСКОЙ ОСНОВЕ | 2000 |
|
RU2176290C1 |
| СПОСОБ ОЧИСТКИ ВОДНОГО РАСТВОРОВ ДВУОКИСИ ХЛОРА ОТ ХЛОРА | 1987 |
|
RU2042740C1 |
| АКТИВАЦИЯ КАТОДА | 2010 |
|
RU2518899C2 |
Изобретение относится к получению некоторых 4-аминопиколиновых кислот электрохимическим восстановлением. Более конкретно данное изобретение относится к селективному восстановлению галогенных заместителей в 5-положении галогенированных 4-аминопиколиновых кислот в присутствии галогенных заместителей в 3-и 6-положениях. Представлен способ получения 4-амино-З-галогенпиколиновой кислоты формулы I:
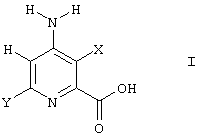
в которой Х представляет Cl или Br; Y представляет Н, Cl или Br, при этом способ предусматривает пропускание постоянного или переменного электрического тока от анода к катоду через раствор 4-амино-3,5-дигалогенпиколиновой кислоты формулы II:
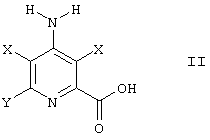
в которой X, Y являются такими, как определено ранее, и в которой оба Х представляют либо Cl, либо Br, при катодном потенциале от -0,4 до -1,7 В относительно электрода сравнения Ag/AgCl (3,0 М Cl-) и извлечение продукта при условии, что когда Х представляет Cl, тогда Y не является Br. Достигается возможность селективного восстановления галогенированных пиридинов, содержащих аминогруппу. 7 з.п. формулы.

в которой Х представляет Cl или Br;
Y представляет Н, Cl, или Br, причем способ предусматривает пропускание постоянного или переменного электрического тока от анода из химически инертного материала к катоду из ртути, свинца, олова, железа, цинка или серебра через 1-20 мас.% раствор в воде и/или органическом растворителе 4-амино-3,5-дигалогенпиколиновой кислоты формулы II
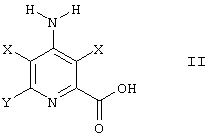
в которой Х и Y являются такими, как определено выше, и
в которой оба Х представляют либо Cl, либо Br, при катодном потенциале от -0,4 до -1,7 В относительно Ag/AgCl (3,0 М Cl-)-электрода сравнения, плотности тока не менее 0,005 А/см2 и температуре от 5 до 90°С и
извлечение продукта при условии, что, когда Х является хлором, то Y не является бромом.
| US 4217185 А, 12.08.1980 | |||
| Способ получения 3,6-дихлорпиколиновой кислоты | 1980 |
|
SU1077568A3 |
| Электрохимическая ячейка для получения 3,6-дихлорпиколиновой кислоты | 1987 |
|
SU1830086A3 |
| RU 94035669 A1, 20.07.1996 | |||
| БЕЙЗЕР М., ХУНД X | |||
| Органическая электрохимия | |||
| М.: Химия, 1988, т.2, с.536-541. | |||
Авторы
Даты
2005-06-20—Публикация
2001-01-12—Подача