Изобретение относится к медицине и может быть использовано в экспериментальной кардиологии.
Ишемия миокарда или другое патологическое состояние миокарда нередко сопровождается остановкой сердца в диастоле [1]. Как известно, при ишемии миокарда происходят существенное закисление цитоплазмы кардиомиоцитов и накопление конечных продуктов метаболизма, главным образом Н+ и лактата. Деполяризация мембраны вследствие накопления К+ приводит к закрытию Na+и Са2+каналов. Поэтому при глубокой ишемии происходит остановка сокращений сердца [2].
Методы восстановления сокращений сердца далеки от идеальных: кроме электроимпульсной терапии используется химическая стимуляция адреналином, хлоридом кальция и т.д. [3-5]. Главным недостатком этих методов является возможность повреждения миокарда вплоть до развития обширного инфаркта миокарда. Кроме того, восстановление сердечного ритма и сокращений миокарда происходит далеко не всегда [3-5].
Гистидинсодержащие пептиды (ацетилкарнозин, ансерин, ацетилансерин, офидин и гомокарнозин) содержатся в тканях человека и животных в высокой концентрации. Но имеется тканеспецифичное распределение в содержании этих пептидов [6]. Данные пептиды обладают широким спектром действия, которое изучается экспериментально - они обладают рН-буферным свойством, антиокидантным, радиозащитным, противораковым действием, предупреждают апоптоз и гибель нейроцитов [6, 7].
Техническим результатом изобретения является повышение эффективности и безопасности проведения химической стимуляции восстановления остановленного в диастоле сердца.
Технический результат изобретения достигается введением в коронарные артерии одного из гистидиновых дипептидов - гомокарнозина (1-10 мМ), или ацетилкарнозина (10-25 мМ), или ацетилансерина (10-25 мМ) или ансерина (10-25 мМ), или офидина (10-25 мМ), растворенных в растворе Рингера-Локка.
Меньшие концентрации гистидиновых дипептидов малоэффективны, использование концентраций пептидов выше указанных вызывает тахикардию, экстрасистолию и стойкое повышение диастолического давления.
Проведенные эксперименты показали высокую эффективность использования гистидинсодержащих пептидов в указанных концентрациях, пример 2.
Пример 1.
Эксперименты проводились на изолированных сердцах белых крыс линии Wistar, перфузированных через аорту по методу Лангендорфа оксигенированным раствором Рингера-Локка следующего состава (в мМ): NaCl - 140; NaH2PO4 - 0,5; КСl - 5; трис - ОН - 5, (рН 7,4); глюкозы - 11; СаСl2 - 2. Для этого крыс декапитировали под эфирным наркозом, вскрывали грудную клетку и сердце помещали в охлажденный раствор. В аорту вводили канюлю и со скоростью 10 мл/мин на 1 грамм влажной ткани подавали оксигенированный раствор (100% O2, t=37°С) в течение 15 минут для стабилизации сократительной функции. Параметры изолированного сердца в этот период времени считали исходными и принимали за 100%.
Маркер повреждения кардиомиоцитов - миоглобин и маркер распада адениннуклеотидов - аденозин изучали в оттекающем от сердца перфузионном растворе.
Сократительную активность миокарда изучали в изоволюмическом режиме с помощью латексного баллончика, введенного в полость левого желудочка. Развиваемое давление рассчитывали как разность систолического и диастолического давления. В работе был использован электроманометр фирмы "Bentley lab. Europe" и аналого-цифровой преобразователь для IBM PC.
Увеличение концентрации К+ в растворе до 20 мМ сопровождалось полной остановкой сердечных сокращений в диастоле в течение первой минуты перфузии такой средой.
Пример 2.
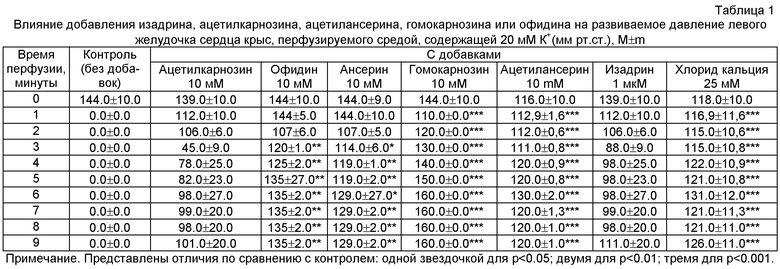
Эксперименты проводят по той же схеме, что и в примере 1, но после 5 минут полной остановки сокращений в перфузионный раствор добавляли карнозин, или ансерин, или офидин, или ацетилкарнозин, или ацетиансерин в концентрации 10 мМ, которая входит в диапазон рекомедуемых концентраций. Добавление в раствор 10 мМ ацетилкарнозина, или 10 мМ офидина, или 10 мМ ансерина, или 10 мМ ацетилансерина, или 10 мМ гомокарнозина немедленно восстанавливало развивающее давление левого желудочка сердца до 70-110% от исходного значения. Аналогичной силой восстановления сокращений сердца после его остановки обладали традиционно используемые препараты, обладающие положительным инотропным действием - хлорид кальция в концентрации 25 мМ или 1 мкМ изадрина (таблица 1).
Таким образом, использование в перфузионном растворе Рингера-Локка 10 мМ ацетилкарнозина, или 10 мМ офидина, или 10 мМ ансерина, или 10 мМ ацетилансерина, или 10 мМ гомокарнозина оказывало стимулирующее действие на остановленное сердце.
Пример 3.
Остановку сердечных сокращений изучали на модели ишемической остановки сердца. Для этого после периода адаптации (15 минут) глубокую ишемию в течение 40 минут моделировали уменьшением скорости перфузии с 10 до 0,1 мл/мин. Исследования показали, что снижение коронарной перфузии изолированного сердца крыс до 0,1 мл/мин приводит к уменьшению развиваемого давления левого желудочка и остановке сердечных сокращений к 3-й минуте ишемии. Начиная с 15-й минуты ишемии отмечалось увеличение диастолического давления в левом желудочке, что свидетельствовало о формировании ишемической контрактуры миокарда. Восстановление перфузии через коронарные сосуды с прежней скоростью (реперфузия) приводило к еще большему увеличению диастолического давления - до 80 мм рт.ст. Сокращения составляли всего 18% от преишемического уровня. Дальнейшее проведение гипоперфузионной ишемии - более 40 минут - нецелесообразно вследствие необратимых ишемических нарушений.
Пример 4.
Отличается от примера 3 тем, что в перфузионный раствор за 15 секунд и в течение всей ишемии добавляли один из пептидов: ацетилкарнозин 10 мМ, или ансерин 10 мМ, или ацетилансерин 10 мМ, или офидин 10 мМ, или гомокарнозин 1 мМ.
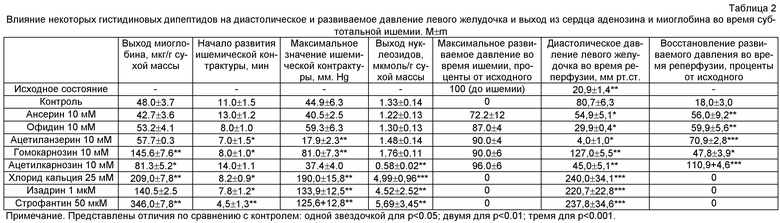
Ацетилкарнозин (10 мМ), или офидин (10 мМ) или ансерин (10 мМ), или ацетилансерин (10 мМ) в перфузионном растворе во время ишемии ослабляло развитие ишемической контрактуры миокарда (таблица 2). Ацетилкарнозин (в концентрации не менее 10 мМ) или офидин (10 мМ) или ансерин (10 мМ) или ацетилансерин (10 мМ) обладал свойством восстанавливать сокращения сердца во время ишемии. Свое действие по стимулированию сокращений миокарда ацетилкарнозин или другие пептиды проявлял только после 20-минутного латентного периода, во время которого сокращения отсутствовали. Начиная с 20-й минуты ишемии систолическое давление достигало 60-90% от преишемического уровня. Данный эффект - 10 мМ ацетилкарнозина, или офидина (10 мМ), или ансерина (10 мМ), или ацетилансерина (10 мМ) - не сопровождался увеличением диастолического давления миокарда выше контрольных значений. Действие ацетилкарнозина по вызыванию сокращений сердца, остановленного ишемией, не сопровождалось усилением выхода из сердца миоглобина и аденозина, не приводило к увеличению диастолического давления в левом желудочке (таблица 2). Последующая реперфузия приводила к полному восстановлению сократительной функции сердца (70-110% от преишемического значения).
Таким образом, ацетилкарнозин в концентрации 10 мМ, или офидин (10 мМ), или ансерин (10 мМ), или ацетилансерин (10 мМ) обладают способностью сохранять сократительную способность в ишемизированном миокарде и улучшать восстановление сократительной способности сердца во время реперфузии.
Гомокарнозин (10 мМ) незамедлительно после введения перфузионного раствора в коронарные артерии вызывал сокращения остановленной ишемией сердечной мышцы, но не предотвращал выход миоглобина и аденозина из сердца во время ишемии и частично усиливал проявления ишемической контрактуры. Восстановление сократительной активности левого желудочка изолированного сердца во время реперфузии было неполным.
Ни один из препаратов, обладающих положительным инотропным действием, - изадрин (1 мкМ), или строфантин (50 мкМ), или хлорид кальция (25 мМ) - не вызывал появление сокращений миокарда во время гипоперфузионной ишемии и усугублял ишемическое повреждение сердца, усиливая выход аденозина и миоглобина в оттекающий от сердца перфузионный раствор (таблица 2). Кроме того, указанные препараты усиливали ишемическую и реперфузионную контрактуру миокарда левого желудочка (таблица 2).
Таким образом, добавление в перфузионный раствор Рингера-Локка ацетилкарнозина (10 мМ), или офидина (10 мМ), или ансерина (10 мМ), или ацетилансерина (10 мМ) вызывало появление сокращений остановленного ишемией миокарда, не усиливало выход из миокарда аденозина и миоглобина и не усугубляло развития ишемической и реперфузионной контрактуры миокарда.
Литература
1. Allen D.G., Orchard С.Н. Myocardial contractile function during ischemia and hypoxia Circ. Res. 60.:153-168. 1987.
2. Kleber A.G. Consegunces of acute ischemia for the electrical and mechanical function of ventricular myocardium. Brief Review. Experiencia. 46(11-12). 1162-1167. 1990.
3. Zorzela L, Garros D, de Caen AR. The new guidelines for cardiopulmonary resuscitation: a critical analysis. J Pediatr (Rio J). 2007 May; 83 (2 Suppl):S64-70.
4. Cardiocerebral resuscitation: the optimal approach to cardiac arrest. Ewy GA. Cleve Clin J Med. 2007 Feb; 74 Suppl 1:S105-9.
5. Schmid A, Hoffman L, Happ MB, Wolf GA, DeVita M. Failure to rescue: a literature review. J Nurs Adm. 2007 Apr; 37(4):188-98.
6. Болдырев А.А. Карнозин. Биологическое значение и возможности применения в медицине. Издательство МГУ, 1998, 308 с.
7. Болдырев А.А. Гистидинсодержащие дипептиды возбудимых тканей. Издательство Биоинформсервис, М., 2001, 108 С.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МОДЕЛИРОВАНИЯ НЕКОРОНАРОГЕННЫХ НЕКРОЗОВ МИОКАРДА | 2005 |
|
RU2366004C2 |
| СПОСОБ ЗАЩИТЫ СЕРДЦА ОТ ИШЕМИИ В ЭКСПЕРИМЕНТЕ | 1996 |
|
RU2144825C1 |
| КАРДИОПЛЕГИЧЕСКИЙ РАСТВОР "АСН-БОКЕРИЯ-БОЛДЫРЕВА" | 2009 |
|
RU2413502C1 |
| СПОСОБ ОДНОВРЕМЕННОЙ РЕГИСТРАЦИИ Na-ЗАВИСИМЫХ ПОТОКОВ Ca И ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ ЦЕЛОГО ИЗОЛИРОВАННОГО СЕРДЦА В ЭКСПЕРИМЕНТЕ | 2009 |
|
RU2400825C1 |
| СПОСОБ ПРЕКОНДИЦИОНИРОВАНИЯ МИОКАРДА | 2006 |
|
RU2312691C1 |
| СПОСОБ ОЦЕНКИ СОСТОЯНИЯ МИОКАРДА ПРИ КАРДИОХИРУРГИЧЕСКИХ ВМЕШАТЕЛЬСТВАХ В УСЛОВИЯХ КАРДИОПЛЕГИЧЕСКОЙ ЗАЩИТЫ | 2017 |
|
RU2651364C1 |
| КАРДИОПЛЕГИЧЕСКИЙ РАСТВОР "ИНФУЗОЛ" | 2002 |
|
RU2226093C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ СОКРАТИТЕЛЬНОЙ ФУНКЦИИ СЕРДЦА ПОСЛЕ КАРДИОПЛЕГИИ С АНТАГОНИСТАМИ КАЛЬЦИЯ В ЭКСПЕРИМЕНТЕ | 1996 |
|
RU2133612C1 |
| СПОСОБ ИЗМЕРЕНИЯ НАБУХАНИЯ КАРДИОМИОЦИТОВ ЦЕЛОГО СЕРДЦА ПРИ УДАЛЕНИИ Са ИЗ ВНЕКЛЕТОЧНОЙ СРЕДЫ В ЭКСПЕРИМЕНТЕ | 2006 |
|
RU2368956C2 |
| СПОСОБ ПРЕЗЕРВИРОВАНИЯ МИОКАРДА ПРИ ТРАНСПЛАНТАЦИИ | 2013 |
|
RU2535036C1 |
Изобретение относится к экспериментальной медицине, а именно к кардиологии и реаниматологии, и может быть использовано при остановке сердца в диастолу. Для этого осуществляют перфузию сердца раствором Рингера-Локка. Причем раствор дополняют одним из гистидинсодержащих пептидов: гомокарнозин в концентрации 1-10 мМ, или ацетилкарнозин в концентрации 10-25 мМ, или ансерин в концентрации 10-25 мМ, или ацетилансерин в концентрации 10-25 мМ, или офидин в концентрации 10-25 мМ. Способ позволяет обеспечить полное восстановление сократительной функции сердца, остановленного вследствие ишемии, без усиления потери миоглобина и аденозина и увеличения давления в левом желудочке. 2 табл.
Способ восстановления сокращений сердца после остановки в диастоле в эксперименте, отличающийся тем, что для повышения эффективности восстановления сердце перфузируют раствором Рингера-Локка, дополненный одним из гистидин содержащих пептидов: гомокарнозин в концентрации 1-10 мМ, или ацетилкарнозин в концентрации 10-25 мМ, или ансерин в концентрации 10-25 мМ, или ацетилансерин в концентрации 10-25 мМ, или офидина в концентрации 10-25 мМ.
| СПОСОБ ЗАЩИТЫ СЕРДЦА ОТ ИШЕМИИ В ЭКСПЕРИМЕНТЕ | 1996 |
|
RU2144825C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ СОКРАТИТЕЛЬНОЙ ФУНКЦИИ СЕРДЦА ПОСЛЕ КАРДИОПЛЕГИИ С АНТАГОНИСТАМИ КАЛЬЦИЯ В ЭКСПЕРИМЕНТЕ | 1996 |
|
RU2133612C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ИШЕМИИ МИОКАРДА | 2002 |
|
RU2241463C2 |
| БОБРОВ О.В | |||
| и др | |||
| Кальцийзависимое повреждение миокарда и использование калия-магния аспарагината для его предотвращения и лечения | |||
| - Провизор, № 22, 2002 | |||
| СИМОНИЯ Г.В | |||
| и др | |||
| Влияние карнозина на активность Na, К-АТР-азы: перспективы применения в клинической | |||
Авторы
Даты
2011-07-20—Публикация
2010-02-08—Подача