Изобретение относится к области лазерной медицины, в частности к способам соединения поврежденных биологических тканей путем лазерной сварки.
Важнейшими задачами современной хирургии являются разработка и внедрение в клиническую практику новых способов соединения органов и тканей, простых в исполнении для хирурга и щадящих для больного. Для их осуществления требуется ряд необходимых условий, обеспечивающих надежность соединения органов или тканей, гарантирующего их функционирование в раннем послеоперационном периоде и скорейшее восстановление функций оперированного органа. Существующие традиционные способы восстановления целостности ткани с использованием шовных материалов, металлических скобок, сшивающих аппаратов, клеевых композиций и других средств несовершенны.
Один из наиболее важных разделов лазерной медицины - лазерную хирургию - отличает от большинства традиционных областей хирургии возможность рассечения, плавления (абляции) и испарения биологических тканей при минимальных сопутствующих повреждениях, наряду с уменьшением вероятности инфицирования раны и минимальными потерями крови во время проведения операции. Лазерная хирургическая инженерия продолжает развиваться в направлении соединения (бесшовной сварки) рассеченных биотканей, что может использоваться как с открытыми, так и с закрытыми операционными полями (через небольшой лапароскопический разрез).
Благодаря лазерной сварке обеспечивается герметичность раны, отсутствует сдавление швами тканей и их краевой некроз, заживление раны не сопровождается образованием грубого рубца. В хирургии сосудов и сердца лазерные швы могут использоваться для фиксации заплаты в области дефекта стенки сосуда, с целью гемостаза и герметизации линии шва сосудистого анастомоза; в легочной хирургии - для закрытия больших раневых поверхностей, возникших после резекции легкого или выделения легкого из спаек, для закрытия небольших бронхиальных свищей, для герметизации и укрепления линии шва анастомоза или культи бронха; в абдоминальной хирургии - для дополнительной герметизации анастомозов, в частности, при резекции прямой кишки; в урологии - как дополнение к кетгутовым швам, для закрытия разрезов почечной лоханки, мочеточника и мочевого пузыря, при трансплантации почки [1].
Особое значение имеет лазерная сварка мельчайших хирургических объектов, таких как нервные волокна, кровеносные капилляры, семяпроводящие протоки и т.п., где шовное соединение биотканей затруднительно и мало надежно [2].
В случае практического осуществления лазерной сварки для прочного и надежного сваривания применяются биоприпои, в состав которых входят связующие вещества, что позволяет заменить обычное сшивание операционной раны хирургической иглой и нитью. Нагрев биоприпоя лазерным излучением приводит к термической деформации клеток в области сварки с выходом клеточного матрикса, связующего биоткани в виде лазерного шва [3].
Тем не менее обычная методика лазерной сварки не всегда обеспечивает такую же прочность соединений, как обычный хирургический шов [4]. По этой причине вызывает интерес поиск новых способов лазерной сварки с использованием биоприпоев на основе углеродных нанотрубок. В этом случае можно ожидать структурирования шовного материала и увеличения его прочности за счет создания скрепляющего нанотрубочного каркаса, как это происходит в объемных нанокомпозитных материалах на основе углеродных нанотрубок, создаваемых действием лазерного излучения [5, 6].
Известно применение углеродных нанотрубок для соединения костных элементов и соседних костей в ортопедических имплантатах [7].
В указанном устройстве не предусмотрено использование действия лазерного излучения и биоприпоев, что делает его неприменимым для лазерной сварки биологических тканей.
Известен способ лазерной сварки биологических тканей с использованием биоприпоев, в которые вводят связующие вещества - белки, полисахариды, нуклеиновые кислоты, витамины, металлы или синтетические органические молекулы [8].
Недостаток этого способа лазерной сварки биологических тканей заключается в недостаточной прочности лазерных швов, что может быть преодолено с использованием биоприпоев, содержащих наночастицы, в частности углеродные нанотрубки.
Известно применение объемных наноструктур на основе углеродных нанотрубок, получаемых действием лазерного излучения, для лазерной сварки человеческих хрящей, что позволяет увеличить прочность лазерного шва по сравнению с использованием припоя на основе альбумина [9].
Недостаток этого способа лазерной сварки биологических тканей заключается в отсутствии в составе биоприпоев поверхностно-активных веществ, что приводит к беспорядочному соединению нанотрубок под действием ван-дер-ваальсовых сил, которое значительно снижает эффективность их применения в составе биоприпоев, не обеспечивая достаточно надежного соединения поврежденных биологических тканей.
Наиболее близким техническим решением заявляемого способа лазерной сварки биологических тканей является способ соединения биотканей, в которые вводят наночастицы, находящихся внутри белковых и биополимерных оболочек, которые нагреваются с помощью оптического излучения [10]. Однако такие оболочечные наночастицы, в частности нанозолото, наносеребро и фуллерены, являются дорогостоящим материалом и не могут быть использованы в широкой практике. Помимо этого помещение наночастиц в оболочки и отсутствие в составе биоприпоев поверхностно-активных веществ не позволяют обеспечить достаточно надежное соединение поврежденных биологических тканей.
По указанным выше причинам необходим поиск новых, более эффективных способов лазерной сварки.
Изобретение направлено на обеспечение надежного соединения поврежденных биологических тканей. Указанный технический результат достигают тем, что способ лазерной сварки биологических тканей включает использование биоприпоя, который представляет собой дисперсию связующих веществ в виде композита в воде на основе белков и/или биосовместимых полимеров, при лазерном облучении отличается тем, что в состав биоприпоя вводят углеродные нанотрубки и поверхностно-активные вещества при следующем количественном соотношении компонентов (в % по массе):
В состав биоприпоя может вводиться связующее вещество 10-50 мас.%; углеродные нанотрубки 0,1-0,5 мас.%; поверхностно-активное вещество 1-3 мас.%; вода - остальное.
В состав связующего вещества биоприпоя могут вводиться белки (альбумин), природный биосовместимый полимер хитозан, полисахариды (амилоза) и оксиэтилированный крахмал, коллагены.
В состав биоприпоя могут вводиться ионогенное поверхностно-активное вещество (ПАВ) - додецилбензолсульфонат натрия, неионогенный ПАВ Неонол АФ 9-12, цвиттерионный ПАВ - фосфатидилхолин, представляющий собой биосовместимое поверхностно-активное вещество, выполняющее определенные функции в человеческом организме.
Предложенный способ лазерной сварки биологических тканей с использованием указанного состава биоприпоя и облучения соединяемых биологических тканей ИК-лазером, охарактеризованный вышеприведенной совокупностью существенных признаков, гарантирует высокое качество сваренных образцов биотканей, удобство в осуществлении и не требует применения дорогостоящих реагентов.
Результаты по лазерной сварке биологических тканей in vitro, полученные с использованием заявляемого способа лазерной сварки биотканей (составов биоприпоя и условий лазерного облучения), приведены в табл.1.
Додецилбензолсульфонат натрий
Неонол АФ 9-12
Фосфатидилхолин
Пример осуществления
Сначала готовят лазерный припой следующим образом.
В дистиллированной воде при комнатной температуре растворяют связующее вещество, поверхностно-активное вещество, углеродные нанотрубки. Смесь помещают в ультразвуковую ванну и диспергируют в течение 2-5 часов при температуре 40-50°С до получения однородного коллоидного раствора припоя.
Сварка проводилась на образцах свиной кожи и хрящах бычьей трахеи.
Хрящи бычьей трахеи промывались в воде, затем от них отделялась мышечная ткань с помощью ножниц и хирургического скальпеля. После этого трахея делилась на более мелкие части и хирургическим скальпелем очищалась от жировой прослойки и пленок, после чего отделялась надхрящница с целью выделения чистого хряща.
Очищенные пластинки погружались в мыльную воду на 5-10 мин для окончательного удаления прослойки жировой ткани с образцов хряща. Спустя 10 мин пластинки хряща промывались в холодной воде и оставлялись в емкости с физиологическим раствором (5% водным раствором поваренной соли).
Подготовка к сварке образцов свиной кожи производилась аналогичным образом.
До начала лазерного облучения и сварки образцов биотканей емкость с образцами хранилась в холодильнике в течение не более одних суток. Непосредственно перед началом эксперимента пластинки извлекались из емкости с раствором и подсушивались 10 мин с целью испарения с них лишней влаги.
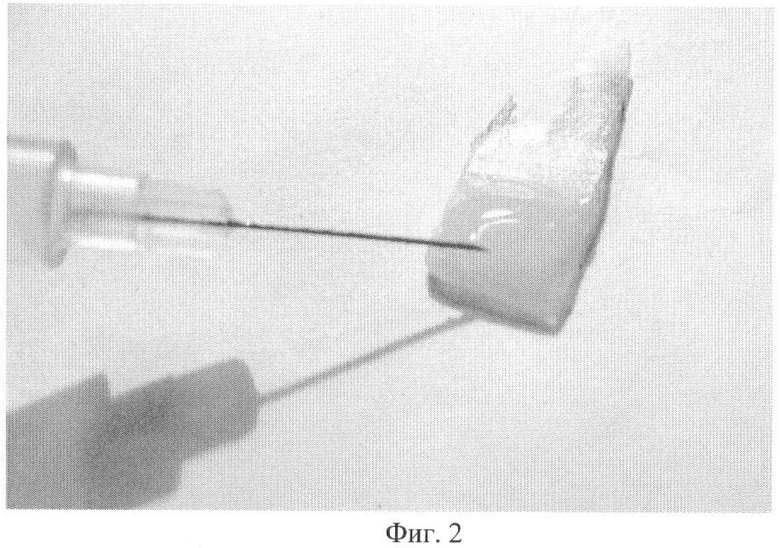
Перед сваркой на хрящ наносился поперечный разрез, разделяющий его на 2 части (фиг.1). По линии разреза образцов инсулиновым шприцом наносился лазерный припой (фиг.2) и хрящи плотно прижимали друг к другу на 20 с.
В качестве источника лазерного облучения использовался диодный инфракрасный лазер с оптоволоконным выходом излучения, с длиной волны генерации λген=0,97 мкм. Лазерная сварка образцов осуществлялась с помощью вышеуказанного прибора - планомерным продвижением по всей длине разреза с внешней стороны хряща до достижения определенного уровня прогрева и сцепления образцов (для предотвращения перегрева и подгорания ткани/припоя), после чего сваривалась обратная сторона пластин. Расстояние от наконечника лазерного оптоволоконного световода до свариваемой поверхности составляло ~5 мм (фиг.3).
Операции для образцов свиной кожи были аналогичны.
Измерение прочности на разрыв сваренных образцов свиной кожи и бычьих хрящей
Прочность на разрыв измерялась следующим образом.
Сначала в исследуемом участке сваренного образца делалось сужение с центром в предполагаемом месте разрыва таким образом, что образец принимал форму гантели. Концы образца закреплялись при помощи зажимов, к одному из которых был прикреплен динамометр, с помощью которого замерялось значение приложенной силы.
Прочность на разрыв определялась по формуле
 ,
,
где F - приложенная сила, при которой происходит разрыв биоткани, S - площадь сечения образца в области сужения.
Площадь сечения образцов S составляла примерно от 1,2 до 10 мм2. Сила нагрузки F - от 3 до 7 Н.
Для вычисления относительной прочности сваренных образцов на разрыв измерялась прочность на разрыв неповрежденной биоткани, а относительная прочность на разрыв рассчитывалась по формуле:
 ,
,
где Т - относительная прочность на разрыв,
σбт - прочность разрыва неповрежденной биоткани,
σсв - прочность разрыва сваренных образцов.
Результаты измерений прочности на разрыв сваренных образцов свиной кожи и бычьих хрящей приведены в табл.2.
Для статистической точности измерения прочности образцов, сваренных с различным составом припоя, проводились с использованием нескольких образцов в каждой испытуемой группе. Для расчета относительной прочности на разрыв использовались средние для каждой группы значения.
Результаты измерений прочности на разрыв сваренных образцов свиной кожи и бычьих хрящей приведены в табл.2 для состава биоприпоя на основе 25% водного раствора бычьего сывороточного альбумина с додецилбензолсульфонатом натрия (1,5 мас.%) и различными типами однослойных и многослойных углеродных нанотрубок.
Данные табл.2 указывают, что использование однослойных углеродных нанотрубок в составе биоприпоя увеличивает прочность сваренных лазерных швов по сравнению с биоприпоем на основе альбумина без нанотрубок [2, 10] ~ в 2 раза, в то время как применение многослойных углеродных нанотрубок дает увеличение прочности швов в 2-3 раза.
По сравнению с данными измерений прочности на разрыв лазерных швов свиной кожи, полученных с припоем на основе альбумина при использовании излучения CO2 лазера (длина волны 10,6 мкм) [4], получено увеличение прочности в 10-15 раз при использовании соответственно однослойных и многослойных углеродных нанотрубок в составе припоя.
Для проверки биосовместимости предлагаемых составов образцы биоприпоя на основе водного раствора бычьего сывороточного альбумина вводились под надхрящницу ушного хряща кролика in vivo. Отрицательной динамики животных не наблюдалось.
Таким образом, благодаря применению предлагаемого способа лазерной сварки биологических тканей с биоприпоем, содержащим дисперсию углеродных нанотрубок и поверхностно-активных веществ и связующие вещества в виде композита на основе белков и биосовместимых полимеров, с использованием лазерного источника излучения, обеспечивается надежное соединение поврежденных биологических тканей при удобстве в осуществлении лазерной сварки и без применения дорогостоящих реагентов.
Источники информации
1. Лазеры в хирургии под ред. О.К.Скобелкина // М.: Медицина, 1989.
2. Неворотин А.И. Введение в лазерную хирургию // СПб.: Спецлит, 2000.
3. C.B.Bleustein, D.Felsen, D.P.Poppas. Welding Characteristics of Different Albumin Species with and without Fatty Acids. - Lasers in Surgery and Medicine, 2000, v.27, No 2, p.82-86.
4. Simhon D., Halpern M., Brosh Т., Vasilyev Т., Ravid A., Tennenbaum Т., Nevo Z., Katzir A. Immediate Tight Sealing of Skin Incisions Using an Innovative Temperature-controlled Laser Soldering Device. - Annals of surgery, 2007, v.245, No.2, p.206-213.
5. В.М.Подгаецкий, В.В.Савранский, М.М.Симунин, М.А.Кононов. Получение объемных нанокомпозиций на основе водного раствора альбумина под действием лазерного излучения. - Квантовая электроника, 2007, т.37, № 9, 801-803.
6. Патент РФ № 2347740.
7. Заявка на патент США № 20070198090.
8. Евроазиатский патент № WO/1996/038093.
9. С.А.Агеева, В.А.Медведева, В.М.Подгаецкий, С.В.Селищев, А.Ю.Толбин, Л.Г.Томилова. Применение органических красителей при лазерной сварке биологических тканей. - Сб. научных трудов «Лазеры в науке, технике, медицине» под ред. В.А.Петрова // M.: МНТОРЭС им.А.С.Попова, 2007, т.18, с.96-100.
10. Патент США № 6685730 В2.
| название | год | авторы | номер документа |
|---|---|---|---|
| БИОПРИПОЙ ДЛЯ ЛАЗЕРНОЙ СВАРКИ БИОЛОГИЧЕСКИХ ТКАНЕЙ | 2016 |
|
RU2636222C1 |
| БИОСОВМЕСТИМЫЙ НАНОМАТЕРИАЛ ДЛЯ ЛАЗЕРНОГО ВОССТАНОВЛЕНИЯ ЦЕЛОСТНОСТИ РАССЕЧЕННЫХ БИОЛОГИЧЕСКИХ ТКАНЕЙ | 2017 |
|
RU2657611C1 |
| ТКАНЕИНЖЕНЕРНАЯ КОНСТРУКЦИЯ ДЛЯ РЕГЕНЕРАЦИИ СЕРДЕЧНОЙ ТКАНИ | 2019 |
|
RU2725860C1 |
| Способ изготовления нанокомпозитного имплантата связки сустава | 2019 |
|
RU2744710C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСОВМЕСТИМОГО НАНОМАТЕРИАЛА | 2016 |
|
RU2633088C1 |
| Способ лазерной обработки нанокомпозитного покрытия имплантанта связки коленного сустава | 2016 |
|
RU2632114C1 |
| УСТРОЙСТВО ДЛЯ ЛАЗЕРНОГО СВАРИВАНИЯ РАССЕЧЕННЫХ БИОЛОГИЧЕСКИХ ТКАНЕЙ | 2015 |
|
RU2611918C1 |
| СПОСОБ НАНОСТРУКТУРИРОВАНИЯ ОБЪЕМНЫХ БИОСОВМЕСТИМЫХ МАТЕРИАЛОВ | 2007 |
|
RU2347740C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСОВМЕСТИМОГО НАНОСТРУКТУРИРОВАННОГО КОМПОЗИЦИОННОГО ЭЛЕКТРОПРОВОДЯЩЕГО МАТЕРИАЛА | 2011 |
|
RU2473368C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОСТРУКТУРИРОВАННОГО КОМПОЗИЦИОННОГО ЭЛЕКТРОПРОВОДЯЩЕГО ПОКРЫТИЯ | 2015 |
|
RU2606842C1 |


Изобретение относится к медицине, а именно к лазерной медицине, и может быть использовано для лазерной сварки биологических тканей. Для этого лазерную сварку осуществляют с использованием биоприпоя, который представляет собой дисперсию связующих веществ в виде композита в воде на основе белков и/или биосовместимых полимеров, в состав которого дополнительно включают углеродные нанотрубки и поверхностно-активные вещества. Способ обеспечивает надежное соединение поврежденных биологических тканей, в том числе за счет создания в композитном материале внутреннего объемного нанокаркаса, определяющего высокую механическую прочность лазерных швов, а также удобство осуществления лазерной сварки без применения дорогостоящих материалов. 3 з.п. ф-лы, 3 ил., 2 табл.
1. Способ лазерной сварки с использованием биоприпоя, который представляет собой дисперсию связующих веществ в виде композита в воде на основе белков и/или биосовместимых полимеров, при лазерном облучении, отличающийся тем, что в состав биоприпоя вводят углеродные нанотрубки и поверхностно-активные вещества.
2. Способ лазерной сварки с использованием биоприпоя по п.1, отличающийся тем, что в состав биоприпоя вводят при следующем количественном соотношении (в % по массе):
3. Способ лазерной сварки с составом биоприпоев по п.1, отличающийся тем, что в состав связующего вещества биоприпоя вводят белки (альбумин), природный биосовместимый полимер хитозан, полисахариды (амилоза), оксиэтилированный крахмал, коллагены.
4. Способ лазерной сварки с составом биоприпоев по п.1, отличающийся тем, что в состав биоприпоя вводят ионогенное поверхностно-активное вещество (ПАВ) Додецилбензолсульфонат натрия, неионогенный ПАВ Неонол АФ 9-12, цвиттерионный ПАВ Фосфатидилхолин.
| ПОДГАЕЦКИЙ В.М | |||
| и др | |||
| Объемный альбуминовый композит на основе нанотрубок, получаемый действием непрерывного лазерного излучения // Известия высших учебных заведений | |||
| Электроника - научно-технический журнал, №5, 2008, с.33-39 | |||
| СПОСОБ ТРАНСЦЕРВИКАЛЬНОЙ ВНУТРИТРУБНОЙ СТЕРИЛИЗАЦИИ | 2005 |
|
RU2286733C1 |
| WO 2007115388 A1, 18.10.2007 | |||
| US 6685730, 03.02.2004 | |||
| BLEUSTEIN CB et al | |||
| «Semi-solid | |||
Авторы
Даты
2011-08-10—Публикация
2010-01-11—Подача