Изобретение относится к области лазерной техники, используемой в нанотехнологических целях, а именно к способам получения объемных биосовместимых наноматериалов под действием лазерного излучения.
Существует принципиальная возможность решения этих проблем путем использования имплантатов из заполняющих наноматериалов, в частности из композиций биологического материала и углеродных нанотрубок. Как следует из данных, на углеродных нанотрубках могут расти и размножаться нервные и костные клетки [1, 2].
Известен способ применения лазерного облучения для формирования структур на поверхности полимерных материалов (эффект лазерного свеллинга) [3]. Однако в этом случае возникают только поверхностные наноструктуры высотой до 0,1 мкм при диаметре около 0,2 мкм, а для практического применения необходимы объемные наноматериалы.
В медицинской практике часто используется медицинский цемент как имплантат костной ткани. Существуют различные виды медицинского цемента, и в их основе лежит полимер акрилат или искусственная керамика - гидрооксиапатит [4]. Эти материалы удовлетворяют механическим требованиям, однако по другим параметрам имплантаты на их основе значительно отличаются от натурной костной ткани. Действительно, любая биологическая среда, в том числе любая ткань, имеет характерную электрическую проводимость. Например, натурная костная ткань имеет удельную проводимость приблизительно 10-7 См/м, и такая среда является оптимальной для размножения костных клеток и регенерации ткани. Однако таким свойством используемые медицинские цементы не обладают, кроме того, их стоимость достаточно высока (>20 $/г) [5].
Известен способ получения объемного наноматериала из водной дисперсии бычьего сывороточного альбумина (БСА) и углеродных нанотрубок (УНТ) с применением лазерного излучения (ЛИ) [6]. Наноматериалы содержали БСА и различные типы нанотрубок (разные концентрации и производители УНТ): многостенные УНТ (МУНТ), одностенные УНТ (ОУНТ), функционализированные и нефункционализированные УНТ и т.д. Наноматериалы имели приемлемые механические свойства (например, твердость ~300 МПа), близкие к свойствам натурной костной ткани, однако их электропроводимость никак не контролировалась [7].
Наиболее близко к предлагаемому изобретению относится способ наноструктурирования объемного материала, характеризующийся тем, что проводят лазерное облучение коллоидного водного раствора альбумина, содержащего углеродные нанотрубки, вплоть до испарения жидкостной составляющей раствора [8]. Этот способ не учитывает электропроводящие параметры составляющих частей, а также электропроводимость конечного наноструктурированного объемного наноматериала.
Задача настоящего изобретения состоит в разработке способа получения объемного биосовместимого наноматериала под действием лазерного излучения, имеющего свойства, близкие к свойствам натурной костной ткани.
Способ получения биосовместимого наноматериала, включающий проведение лазерного облучения водной дисперсии альбумина, содержащей углеродные нанотрубки, вплоть до испарения жидкостной составляющей дисперсии. В состав наноматериала вводят одностенные углеродные нанотрубки в количестве 0,02-0,1 мас. % с электропроводимостью в слоях более 50000 См/м. В водной дисперсии альбумин берется в количестве 20-25 мас. %. Вводные дисперсии из альбумина и одностенных углеродных нанотрубок перемешивают и диспергируют в ультразвуковой бане. Водная дисперсия из альбумина и одностенных углеродных нанотрубок в течение 10-30 мин в режиме непрерывный облучают лазером, имеющим длину волны генерации 810 нм и удельную мощность излучения 0,02-0,1 МВт/м2. Полученный биосовместимый наноматериал в составе альбумина и одностенных углеродных нанотрубок имеет удельную электропроводимость в диапазоне 10-6÷10-7 См/м.
Сущность предлагаемого изобретения состоит в том, что действие лазерного излучения позволяет испарить жидкостную компоненту раствора, структурировать наполнитель в виде ОУНТ определенным образом и, после испарения жидкости, получить однородный объемный твердый композиционный наноматериал черного цвета, имеющий твердость и удельную электропроводимость, близкие к показателям натурной костной ткани.
Практическая применимость предлагаемого способа иллюстрируется указанными ниже шагами изготовления объемного твердого наноматериала:
1. К дистиллированной воде добавляют ОУНТ и дисперсию перемешивают в магнитной мешалке в течение 30 мин, а потом диспергируют в ультразвуковом диспергаторе при температуре ≤30°С в течение 30 мин до получения однородной дисперсии черного цвета. Концентрацию ОУНТ подбирают в области 0,02-0,1 мас. % таким образом, чтобы слои толщинами 0,2-10 мкм, образовавшиеся при нанесения дисперсии на кремниевые или стеклянные подложки, имели удельную электропроводимость >5⋅104 См/м. Такой контроль электропроводимости слоев из ОУНТ необходим, поскольку завод-изготовитель ОУНТ (в форме пасты, геля, порошка и др.) часто не приводит ориентировочные данные относительно индивидуальной удельной электропроводимости отдельных однослойных углеродных нанотрубок в составе вещества.
2. В водную дисперсию ОУНТ вводят порошок БСА в концентрации 20-25 мас. %, и затем дисперсию помещают в ультразвуковую баню и диспергируют при температуре ≤40°С в течение 60 мин до получения однородной дисперсии БСА/ОУНТ черного цвета.
3. Дисперсию БСА/ОУНТ деконтируют в течение 24 ч, фильтруют и переливают в другой сосуд.
4. Дисперсию БСА/ОУНТ заливают в стеклянный сосуд и облучают лазерным излучением в течение 10-30 мин до полного испарения жидкостной компоненты раствора и получения однородного объемного наноматериала черного цвета. При этом подбирают мощность лазерного излучения в области 0,02-0,1 МВт/м2 (диодный лазер с оптоволоконным выводом, длина волны генерации 810 нм, режим генерации - непрерывный) с таким расчетом, чтобы дисперсия БСА/ОУНТ потеряла жидкостную составляющую, т.е. не менее 2/3 от изначальной массы. Эмпирический подбор режима лазера (мощность лазерного излучения, длина волны генерации и др.) позволяет реализовать нужные механические и электрические параметры объемного наноматериала.
5. Объемный наноматериал с шага высушивают при температурах 25-30°С в течение 24 ч.
Из твердого наноматериала вырезают образцы виде пластинок с размерами 10-12×3-5×0,5-1,5 мм, шлифуют их и полируют. На образцах проводят измерения твердости, электропроводности и микроскопические исследования.
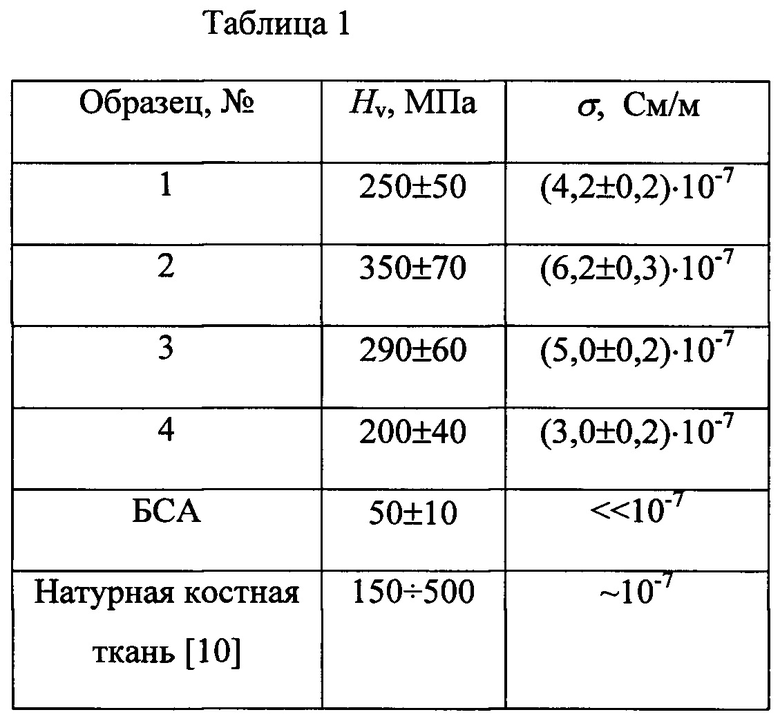
В таблице 1 приведены результаты измерения твердости Нv и удельной электропроводимости σ некоторых образцов наноматериала. При этом твердость Нv измеряют методом Виккерса на микротвердомере ПМТ-3М. Для этого образцы полируют на уровне шероховатости ≥10 класса. Величину σ измеряют 2-зондовым методом с применением мегаомметра МЕГЕОН 13125. Отметим, что удельную электропроводимость слоев из ОУНТ измеряют 4-зондовым методом, используя универсальные измерительные приборы Agilent 34405А.
На фиг. 1 показана типичная электромикроскопическая картина образца наноматериала БСА/ОУНТ. Видны углеродные нанотрубки. В большинстве случаях они свернуты в жгуты, диаметр которых на порядок и более превосходит диаметр индивидуальных однослойных нанотрубок (диаметр ~ 1,0-1,5 нм). Жгуты из ОУНТ и отдельные нанотрубки создают каркасообразную структуру, которая придает механическую твердость матрице наноматериала. С другой стороны, эта структура обеспечивает электропроводность наноматериала и представляется как электропроводящая сеть (каркас).
Таким образом, каркасообразная структура ОУНТ в матрице наноматериала обеспечивает ему высокую механическую твердость и приемлемую элетропроводимость. Действительно, согласно табл. 1, твердость и удельная электропроводимость наноматериала коррелируются между собой, и они сопоставимы со свойствами натурной костной ткани человека.
На фиг. 2 представлены изображения клеток костной ткани (остеобластов) на подложках из наноматериала БСА/ОУНТ и на поверхности БСА, полученные в оптическом микроскопе. В течение 24-72 ч число выросших клеток на подложке предложенного наноматериала больше, чем на поверхности БСА, что подтверждает преимущества предложенного наноматериала. Он создает оптимальную среду для размножения клеток костной ткани, тем самым оказывая положительный эффект на ее регенерацию. Несмотря на то что БСА является биологическим материалом, а БСА/ОУНТ биосовместимым наноматериалом, преимущество последнего очевидно. Также предложенный наноматериал имеет твердость в несколько раз больше, чем БСА (см. табл. 1), что очень важно для создания на его основе имплантата или заполняющего материала костной ткани.
Важными свойствами наноматериала, изготовленного предложенным способом, относительно известных материалов являются [4, 6]:
- матрица состоит из биологического материала (белок альбумин) и из наполнителя в виде одностенных углеродных нанотрубок, и, в целом, наноматериал является биосовместимым;
- наноматериал имеет приемлемые механические свойства и удельную электропроводимость, сопоставимые с параметрами натурной человеческой костной ткани;
- наноматериал представляет собой оптимальную среду для размножения клеток костной ткани;
- составляющие части являются легкодоступными и недорогими (<1-3 $/г), а технология приготовления наноматериала несложная и ее ожидаемая себестоимость <6-8 $/г.
Достоинством наноматериала, полученного предложенным способом, является также возможность варьирования консистенции, твердости и удельной электропроводимости полученного наноматериала от стекло- до пастообразной в зависимости от интенсивности и длительности лазерного облучения, а также от концентрации и свойств составных частей.
В частности, стеклообразный наноматериал удобен для непосредственного применения в составе хирургического имплантата, а пастообразный наноматериал удобен для формирования нужной конфигурации заполняющего материала для восстановления целостности костной ткани.
Таким образом, поставленная в настоящей заявке на патент цель выполнена. Предложен способ приготовления наноматериала на основе биологического материала альбумина и наполнителя из одностенных нанотрубок с использованием лазерного излучении. Наноматериал является биосовместимым и имеет свойства, близкие к свойствам натурной костной ткани человека (см. табл. 1).
Источники информации
1. Патент США No.6.670.179.
2. Ivan Bobrinetskiy, Alexander Gerasimenko, Levan Ichkitidze, Ol'ga Khrolova, and Vitaly Podgaetsky / Cell Adhesive Nanocomposite Materials Made of Carbon Nanotube Hybridized with Albumin // American Journal of Tissue Engineering and Stem Cell (2014) Vol. 1 No. 1 pp. 27-38.
http://paper.uscip.us/ajtesc/AJTESC.2014.1003.pdf
http://dx.doi.org/10.1021/cm051475y
3. Патент США No.6.853.075.
4. Хенч Л., Джонс Д. Биоматериалы, искусственные органы и инжиниринг тканей. М.: Техносфера. 2007. - 304 с.
5. Мидленко В.И., Шевалаев Г.А., Ефремов И.М. Применение костного цемента в комбинации с антибиотиком для лечения больных хроническим остеомиелитом костей конечностей // Современные проблемы науки и образования. - 2013. - №5. С. 1-8.
URL: http://www.science-education.ru/ru/article/view?id=10359 (дата обращения: 27.09.2016).
6. Ичкитидзе Л.П., Подгаецкий В.М., Пономарева О.В., Селищев СВ. / Механические свойства объемного нанокомпозита, полученного при лазерном облучении продукта // Изв. вузов. Физика, 2010, №3/2, с. 125-129.
7. Патент РФ №2561343.
8. Патент РФ №2347740 (прототип).
| название | год | авторы | номер документа |
|---|---|---|---|
| ТКАНЕИНЖЕНЕРНАЯ КОНСТРУКЦИЯ ДЛЯ РЕГЕНЕРАЦИИ СЕРДЕЧНОЙ ТКАНИ | 2019 |
|
RU2725860C1 |
| Способ изготовления нанокомпозитного имплантата связки сустава | 2019 |
|
RU2744710C2 |
| БИОСОВМЕСТИМЫЙ НАНОМАТЕРИАЛ ДЛЯ ЛАЗЕРНОГО ВОССТАНОВЛЕНИЯ ЦЕЛОСТНОСТИ РАССЕЧЕННЫХ БИОЛОГИЧЕСКИХ ТКАНЕЙ | 2017 |
|
RU2657611C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСОВМЕСТИМОГО НАНОСТРУКТУРИРОВАННОГО КОМПОЗИЦИОННОГО ЭЛЕКТРОПРОВОДЯЩЕГО МАТЕРИАЛА | 2011 |
|
RU2473368C1 |
| УНИПОЛЯРНЫЙ ДАТЧИК ДЕФОРМАЦИИ | 2018 |
|
RU2685570C1 |
| БИПОЛЯРНЫЙ ДАТЧИК ДЕФОРМАЦИИ НА ОСНОВЕ БИОСОВМЕСТИМОГО НАНОМАТЕРИАЛА | 2017 |
|
RU2662060C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОСТРУКТУРИРОВАННОГО КОМПОЗИЦИОННОГО ЭЛЕКТРОПРОВОДЯЩЕГО ПОКРЫТИЯ | 2015 |
|
RU2606842C1 |
| БИОПРИПОЙ ДЛЯ ЛАЗЕРНОЙ СВАРКИ БИОЛОГИЧЕСКИХ ТКАНЕЙ | 2016 |
|
RU2636222C1 |
| СПОСОБ НАНОСТРУКТУРИРОВАНИЯ ОБЪЕМНЫХ БИОСОВМЕСТИМЫХ МАТЕРИАЛОВ | 2007 |
|
RU2347740C1 |
| СПОСОБ ФОРМИРОВАНИЯ ЭЛЕКТРОПРОВОДЯЩЕГО СЛОЯ НА ОСНОВЕ ОКСИДА ГРАФЕНА И УГЛЕРОДНЫХ НАНОТРУБОК | 2021 |
|
RU2773731C1 |


Изобретение относится к медицине и может быть использовано для получения биосовместимого наноматериала. Для этого осуществляют проведение лазерного облучения водной дисперсии альбумина, содержащей углеродные нанотрубки, вплоть до испарения жидкостной составляющей дисперсии. При этом в состав наноматериала вводят одностенные углеродные нанотрубки в количестве 0,02-0,1 мас.% с электропроводимостью в слоях более 50000 См/м. Изобретение обеспечивает получение объемного биосовместимого наноматериала под действием лазерного излучения, имеющего свойства, близкие к свойствам натурной костной ткани. 3 з.п. ф-лы, 2 ил., 1 табл.
1. Способ получения биосовместимого наноматериала, включающий проведение лазерного облучения водной дисперсии альбумина, содержащей углеродные нанотрубки, вплоть до испарения жидкостной составляющей дисперсии, отличающийся тем, что в состав наноматериала вводят одностенные углеродные нанотрубки в количестве 0,02-0,1 мас.% с электропроводимостью в слоях более 50000 См/м.
2. Способ получения биосовместимого наноматериала по п. 1, отличающийся тем, что в водной дисперсии альбумин берется в количестве 20-25 мас.%.
3. Способ получения биосовместимого наноматериала по п. 1, отличающийся тем, что отдельные водные дисперсии из альбумина и одностенных углеродных нанотрубок перемешивают и диспергируют в ультразвуковой бане.
4. Способ получения биосовместимого наноматериала по п. 1, отличающийся тем, что водная дисперсия из альбумина и одностенных углеродных нанотрубок в течение 10-30 мин в непрерывном режиме облучают лазером, имеющим длину волны генерации 810 нм и удельную мощность излучения 0,02-0,1 МВт/м2.
| СПОСОБ НАНОСТРУКТУРИРОВАНИЯ ОБЪЕМНЫХ БИОСОВМЕСТИМЫХ МАТЕРИАЛОВ | 2007 |
|
RU2347740C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСОВМЕСТИМОГО НАНОСТРУКТУРИРОВАННОГО КОМПОЗИЦИОННОГО ЭЛЕКТРОПРОВОДЯЩЕГО МАТЕРИАЛА | 2011 |
|
RU2473368C1 |
| WO 2008070926 A1, 19.06.2008 | |||
| А.Ю | |||
| ГЕРАСИМЕНКО и др | |||
| Перспективные наноматериалы с углеродными нанотрубками в биомедицинских приложениях | |||
| // Медицинская техника, 2014, N6 (288), с.23-27. | |||
Авторы
Даты
2017-10-11—Публикация
2016-11-10—Подача