Изобретение относится к области медицины и, конкретно, к травматологии. Оно предназначено для обработки хирургических имплантатов, используемых при реконструкции связок и сухожилий, излучением инфракрасного (ИК) диапазона.
Хирургическая операция позволяет поврежденные связки коленного сустава заменить на искусственные имплантаты. Даже относительно инертные синтетические полимеры, являясь инородным телом в организме, часто поддерживают хроническую воспалительную реакцию и меняют свои физические свойства. Следовательно, длительное функционирование синтетических имплантатов нередко становиться невозможным. Следовательно, для избегания отторжения имплантата и снижения риска инфекции после трансплантации на поверхность имплантатов наносится специальное покрытие.
Известен способ заселения имплантата связки коленного сустава фибробластами, с пропитыванием имплантата вспомогательным веществом - коллагеном [1]. Существенным недостатком такого способа покрытия имплантата связки коленного сустава является сложность работы с клеточным компонентом, требующей длительной подготовки материала: забора клеток у пациента, культивирования и засеивания имплантата клетками.
Известен способ закрепления имплантата связки коленного сустава в отверстиях берцовых костей человека или животного, с передачей энергии во вспомогательный затвердевающий плавкий материал, проникающий в костную ткань [2]. Недостатком такого способа закрепления имплантата связки коленного сустава является неполная физиологическую совместимость предлагаемого плавкого материала, что может иметь следствием разрушение или отторжение имплантата.
Известен способ обработки искусственных связок суставов и сухожилий с использованием вспомогательных веществ - нановолокон, включающих графен, его производные и углеродные нанотрубки [3]. Недостаток этого способа изготовления и применения имплантатов связок заключается в отсутствии функциональной обработки применяемых углеродосодержащих материалов, которая только может придавать материалу имплантата связки остеиндуктивные свойства, определяющие устойчивую фиксацию имплантата в костном канале, но не обеспечивает биологическую совместимость имплантата с тканями организма.
Наиболее близким техническим решением заявляемого способа обработки искусственных связок суставов и сухожилий является формирование нанокомпозитного покрытия имплантата связки коленного сустава путем водоиспаряющего воздействия лазерным излучением [4]. Недостаток такого способа изготовления и применения имплантатов связок заключается в том, что трудно контролируется температура локального нагрева нанокомпозитного материала и возникает большой риск понижения его функциональных характеристик. Например, в нанокомпозитном материале из водно-белковой дисперсии углеродных нанотрубок в случае перегрева (температура более 80°С) белка альбумина начинается его денатурация. Действительно, лазерный луч локально, на площади несколько десятков квадратных микрометров, сильно нагревает материал, что может не отразиться на регистрируемой интегральной температуре покрытия. Вследствие этого на поверхности покрытия имплантата образуются локально денатурированные участки, наличие которых понижает возможность клеточной адгезии и пролиферации на поверхности покрытия. Это означает, что изначально высокая степень биосовместимости нанокомпозитного покрытия существенно понижается. Поэтому для такого имплантата связок суставов существует вероятность возникновения воспалительной реакции или иных осложнений.
Очевидно, что необходимо сохранить эффективность покрытия имплантата связок суставов и не допустить перегрева нанокомпозитного покрытия в процессе лазерной обработки.
Задача предлагаемого изобретения состоит в повышении степени биосовместимости нанокомпозитного имплантата связки с покрытием из композитного биосовместимого наноматериала и его прочности на разрыв относительно имплантатов связок без покрытия.
Поставленная задача решается тем, что осуществляют нанесение на поверхность заготовки имплантата связки вспомогательное вещество - водно-белковую дисперсию углеродных нанотрубок (УНТ), а затем формируют нанокомпозитное покрытие путем водоиспаряющего воздействия ИК-излучения в диапазоне длин волн 0,7-1,2 мкм, мощностью на единицу площади 0,1-0,5 Вт/см2. Концентрация белковой компоненты во вспомогательном веществе находится в пределах от 15 до 30 мас. %. Концентрация углеродных нанотрубок во вспомогательном веществе находится в пределах от 0,1 до 0,3 мас. %. В качестве белковой компоненты вспомогательного вещества используют альбумин и коллаген. ИК-облучение слоя вспомогательного вещества, нанесенного на заготовку имплантата связки коленного сустава, осуществляют при вращении заготовки имплантата.
Сущность предлагаемого изобретения состоит в следующем. Приготавливаются вспомогательное вещество - водно-белковая дисперсия углеродных нанотрубок. Оно используется для формирования нанокомпозитного покрытия имплантата связки коленного сустава. Для получения вспомогательного вещества осуществляются следующие шаги:
1. К дистиллированной воде добавляется одностенные УНТ (ОУНТ) или многостенные УНТ (МУНТ), и дисперсия перемешивается в магнитной мешалке в течение 60 мин, а потом диспергируется в ультразвуковом (УЗ) диспергаторе при температуре ≤ 30°С в течение 50 мин до получения однородной дисперсии черного цвета. Концентрация УНТ подбирается в области 1-2 мас. %.
2. В водную дисперсию УНТ вводится порошок бычий сывороточный альбумин (БСА) в концентрации 15-30 мас. %. Затем к дисперсии добавляется бычий коллаген (БК) в концентрации 1-2 мас. %. Полученная дисперсия в составе УНТ, БСА и БК тщательно перемещается в магнитной мешалке в течение 60 мин, потом диспергируется в УЗ бане при температуре ≤ 40°С в течение 60 мин.
3. Дисперсия БСА/БК/УНТ декантируется в течение 24 ч, фильтруется и переливается в другой сосуд.
Состав нанокомпозита на основе БСА, БК и УНТ подбирается из следующих соображений.
БСА - бычий сывороточный альбумин является биологическим полностью биосовместимым материалом и широко применяется в медицинской практике. Альбумин составляет около 60% белков плазмы крови, его средняя концентрация в плазме ~ 40 г/л. Транспортная функция альбумина состоит в переносе свободных жирных кислот, холестерина и других биологически активных веществ. Для альбумина типична конформация во вторичной или третичной структуре при незначительной загрузке белка токсическими продуктами. Картина высохшей капли свежеприготовленного водного раствора сывороточного альбумина характеризуется наличием значительного количества радиальных трещин, образующих арки по краю капли. Молекула альбумина хорошо изучена на атомарно-структурном уровне: имеет две модификации (изомера), представляющие собой эллипсоид вращения и неправильную треугольную призму. БСА служит биологической матрицей в используемом нами нанокомпозитном материале.
БК - бычий коллаген составляет более 30% общей массы белков организма и является главным компонентом соединительной ткани. Относительно молекулы БСА (~69 Да) молекула коллагена имеет гигантскую молекулярную массу 300 кДа. Основными достоинствами коллагена считаются: высокая механическая прочность, отсутствие токсических и канцерогенных свойств, слабая антигенность, способность образовывать комплексы с биологически активными веществами (гепарином, хондроитинсульфатом, антибиотиками и др.), способность к стимуляции регенерации собственных тканей организма, к набуханию, резорбции, к выполнению функции ионообменника: коллаген обеспечивает полупроницаемость мембран, стимуляцию репарации, гемостатический эффект. Одновременно, биополимер коллаген обладает положительными качествами синтетических полимеров и имплантатов, например, высокой механической прочностью на разрыв, низкой растяжимостью, ориентацией волокон, что обуславливает его применения в медицинских приложениях.
УНТ - углеродные нанотрубки обладают экстремально высокими механическими, физическим, оптическими и другими параметрами и уникальными функциональными возможностями. В частности, высокие прочность на разрыв ~50 ГПа, модуль упругости ~1 ТПа и удельная электропроводность, приведенная на плотность нанотрубки, ≥20000 См × м2/кг, а также приемлемая степень безопасности не хуже относительно сажи, в особенности для очищенных и функционализированных нанотрубок. В нанокомпозитах широко распространено два типа УНТ: ОУНТ и МУНТ. Значительные высокие значения механических параметров в нанокомпозитах реализуется при наполнителях МУНТ или ОУНТ, но более высокая степень очистки реализуется в ОУНТ.
Перечисленные положительные свойства составных композитов, позволяет на их основе реализовать нанокомпозитный материал БСА/БК/УНТ с требуемыми параметрами и функциональными свойствами и с возможностью медицинского применения.
Стандартная искусственная связка из синтетического материала, в частности, из полиэтилентерефталата (ПЭТ) служит основой, на которую наносится дисперсия БСА/БК/УНТ для получения покрытия. В целом, конечный продукт, именуемый как «имплантат», представляет собой связку из ПЭТ с покрытием нанокомпозитного материала из БСА/БК/УНТ.
На фиг. 1 показаны эскизы системы для предварительной очистки связки (фиг. 1а): 1 - УЗ баня, 2 - вода в УЗ бане, 3 - сосуд, в который помещается связка, 4 - этиловый спирт, 5 - связка; системы для очистки связки (фиг. 1 б): 6 - дистиллированная вода; системы для стерилизации связки в УФ камере (фиг. 1 в): 7 – УФ-камера.
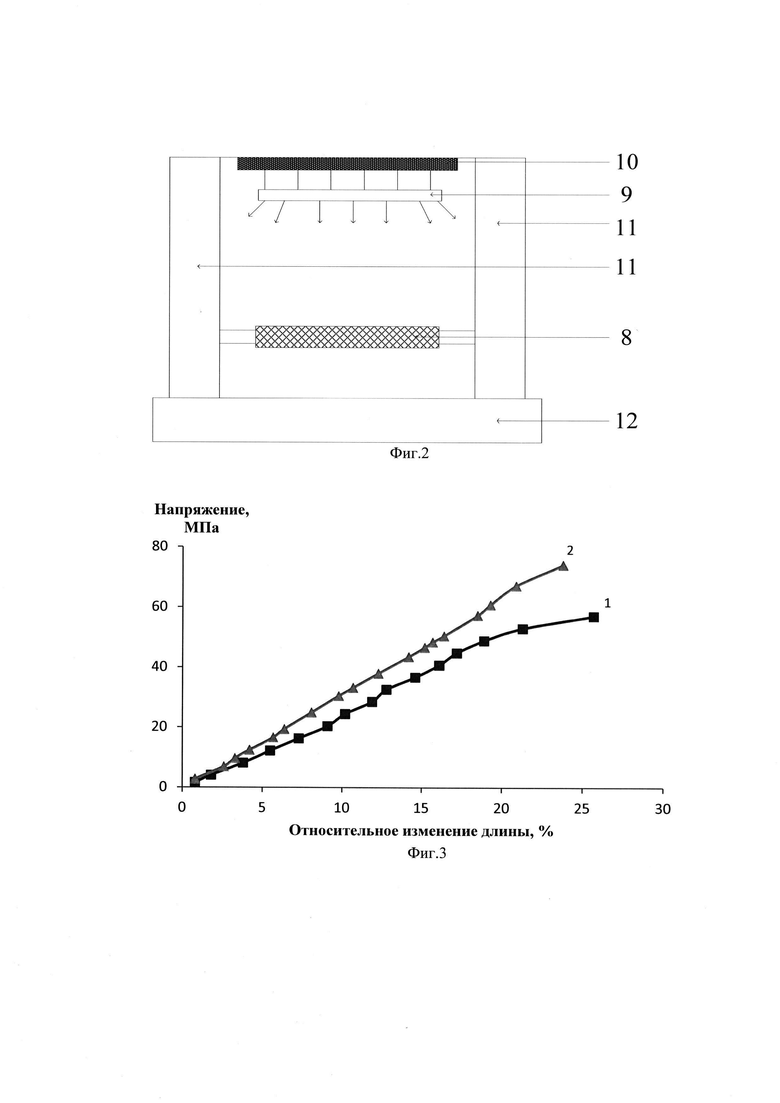
На фиг. 2 представлен эскиз камеры для ИК-облучения: 8 - связка с нанесенным слоем дисперсии БСА/БК/УНТ, 9 - ИК-облучатель, 10 - отражатель ИК-излучения, 11 - система крепления и вращения связки, 12 - общий стол, где вмонтированы все части камеры.
Для получения имплантата проводились следующие процедуры:
предварительная очистка связки в УЗ бане в среде этилового спирта в течение 30 мин;
очистка связки в УЗ бане в среде дистиллированной воды в течение 30 мин;
антибактериальная обработка связки в ультрафиолетовой (УФ) камере в течение 50 мин;
нанесение водной дисперсии БСА/БК/УНТ путем опускания в нее связку или распыления дисперсии с использованием дисперсионного распылителя;
облучение ИК-излучением слои дисперсии на связку;
тестирование механических параметров имплантата, т.е. связки с нанокомпозитным БСА/БК/УНТ покрытием.
После очистки и стерилизации концы связки закрепляются в специальном держателе и производится нанесение дисперсии БСА/БК/УНТ на поверхность связки с обеих сторон с использованием дисперсионного распылителя, или путем полного погружения связки в дисперсию.
Затем связка переносится в камеру для ИК-облучения, где происходит ее вращение, и этим достигается получение равномерного по толщине слоя нанокомпозитного покрытия. В процессе облучения дистанционно контролируется температура поверхности слоя на поверхности связки, и показания передаются электронному блоку, который управляет вращением связки 8. Также контролируется мощность излучения ИК-излучателя 9. Обратная связь между устройством контроля температуры и устройством контроля мощности позволяет легко удерживать температуру на поверхности связки около 50°С с точностью ±3°С. На фиг. 2 не отражены электронный блок управления, пирометрический регистратор температуры, а также электрические связи между ними и с другими частями камеры для ИК-облучения. В результате подбора технологических параметров, например: состава водной дисперсии БСА/БК/УНТ, скорости вращения связки, мощности ИК-излучателя и регистрируемой температуры на поверхности связки; обеспечивается формирование на поверхности связки высушенного слоя нанокомпозитного покрытия толщиной 0,2-1 мкм. Такая толщина достаточна для увеличения прочности имплантата связки, при этом она не оказывает негативного влияния на эластичность связки.
В высушенном слое нанокомпозитного покрытия БСА/БК/УНТ, имеются составные части: матрица БСА - ≥ 90 мас. %, БК - ~ 6 мас. %, УНТ - ≤ 3 мас. %.
Пример.
В дистиллированной воде размещается гель ОСУНТ95ТА (производство OCSiAl), представляющий собой водную дисперсию ОУНТ с концентрацией ОУНТ 2,5 мас. %. Перемешивание геля с дистиллированной водой производится в магнитной мешалке в течение 30 мин, затем осуществляется гомогенизация данного состава в УЗ гомогенизаторе в течение 30 мин. С учетом всех частей воды (дистиллированная и входящая в состав геля) полученный состав состоит приблизительно из 0,05 мас. % ОУНТ и 99,95 мас. % воды. Затем добавляется порошок БСА фирмы AMRESCO и нейтральная водная суспензия БК производства фирмы ООО «Макмеди». Полученная водная дисперсия в составе БСА, БК и ОУНТ перемешается в магнитной мешалке и в УЗ бане по 30 мин, соответственно. Следует отметить, что обработка дисперсии в УЗ гомогенизаторе и УЗ бане осуществлялась с контролем температуры, при котором не допускалось повышение температуры выше 30°С. Массовый состав подбирается таким образом, что конечная водная дисперсия содержит: 15-30 мас. % БСА, 1-2 мас. % БК и 0,2-1,0 мас. % ОУНТ, остальное - вода.
Полоски имплантата связки коленного сустава из ПЭТФ, с приблизительными размерами: длина 300 мм, ширина 10 мм, толщина 1,5 мм, служили тестовыми образцами, на которые наносились слои композитного наноматериала БСА/БК/ОУНТ, и которые затем испытывались на механическую прочность. На обеих краях полоски посередине делаются небольшие надрезы глубиной около 1 мм. Следовательно, в этом месте образуется сужение, ширина которого на 2 мм меньше относительно ширины полоски в других местах, и образец разрывается именно в этом месте при испытаниях на разрывной машине. Это позволяет определить прочность на разрыв с точностью несколько процентов.
После очистки и стерилизации концы связки закрепляются в специальном держателе и производится нанесение дисперсии БСА/БК/УНТ на поверхность связки с обеих сторон с использованием дисперсионного распылителя. После окончания процесса нанесения дисперсии связка переносится в камеру для ИК-облучения (см. фиг. .2). Здесь производится облучение при следующем режиме: скорость вращения связки - 0,5 об/с; удельная мощность облучения - 0,5 Вт/см2, время облучения 60 с. В данном режиме на поверхности связки образуется слой нанокомпозитного материала БСА/БК/ОУНТ толщиной 0,5 мкм путем его нагрева приблизительно до 50°С. Этот температурный режим автоматически контролируется и поддерживается с помощью электронного блока управления. После завершения ИК-облучения образец высушивался в комнатных условиях в течение 60 мин и в дальнейшем проводились измерения его механических характеристик в разрывной машине. Напряжение определялось, как отношение нагруженной силы на площадь сечения в суженном месте образца, а относительное растяжение, как относительное изменение длины образца.
Отметим, что контрольным считался образец связки коленного сустава из ПЭТФ, на который не нанесено покрытие, а тестовым - на который нанесено покрытие. При этом общая масса слои оценивалась как ≤3 мг, а масса ОУНТ в нем - ≤10 мкг. В организме покрытие имплантата может резорбироваться в течение длительного времени (более месяца), поэтому содержание свободных частиц ОУНТ в организме не превышает общего фонового содержания углеродсодержащих веществ, которые содержатся в городском воздухе и которыми ежедневно дышит человек.
На фиг. 3 представлены графики, на которых отражены зависимости напряжения на разрыв от относительного растяжения. Приведенные здесь графики 1 и 2 соответствуют образцам связок без покрытия и со слоем покрытия соответственно. Видно, что в последнем случае заметно увеличивается прочность на разрыв (~ 20%), а также модуль упругости (~ 30%).
Отметим некоторые важные свойства предложенного способа нанесения покрытия:
слой покрытия из композитного биосовместимого наноматериала в составе матрицы из биологических материалов (альбумин, коллаген) и наполнителя углеродных нанотрубок образуется на поверхности синтетического имплантата связки путем нанесения водной дисперсии на поверхности и действия ИК-излучения в диапазоне длин волн 0,7-1,2 мкм и небольшой мощностью на единицу площади поверхности 0,1-0,5 Вт/см2;
небольшая мощность ИК-излучения не перегревает слой композитного биосовместимого наноматериала (температура ≤50°С), вследствие чего не нарушается и не понижается его высокая степень биосовместимости;
небольшое количество (≤ 3 мас. %) одностенных углеродных нанотрубок в наноматериале позволяет значительно повысить прочность на разрыв (≥20%) и модуль упругости (≥30%) синтетического имплантата связки и практически не снижает высокую степень биосовместимости матрицы наноматериала.
Таким образом, поставленная задача выполнена. Предложен способ изготовления имплантата связки сустава с нанокомпозитным покрытием, позволяющим повысить его механические свойства и степень биосовместимости. Данный способ является простым и доступным и перспективен для восстановления функции поврежденной связки коленного сустава, а также других суставов.
Источники информации
1. Патент Франции 2.651.99.
2. Патент РФ 2567603.
3. Патент США 8142501.
4. Патент РФ 2632114 - прототип.
| название | год | авторы | номер документа |
|---|---|---|---|
| БИОСОВМЕСТИМЫЙ НАНОМАТЕРИАЛ ДЛЯ ЛАЗЕРНОГО ВОССТАНОВЛЕНИЯ ЦЕЛОСТНОСТИ РАССЕЧЕННЫХ БИОЛОГИЧЕСКИХ ТКАНЕЙ | 2017 |
|
RU2657611C1 |
| Способ лазерной обработки нанокомпозитного покрытия имплантанта связки коленного сустава | 2016 |
|
RU2632114C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСОВМЕСТИМОГО НАНОМАТЕРИАЛА | 2016 |
|
RU2633088C1 |
| ТКАНЕИНЖЕНЕРНАЯ КОНСТРУКЦИЯ ДЛЯ РЕГЕНЕРАЦИИ СЕРДЕЧНОЙ ТКАНИ | 2019 |
|
RU2725860C1 |
| ИСКУССТВЕННАЯ МЫШЦА ДЛЯ СЕРДЕЧНОЙ ТКАНИ | 2017 |
|
RU2675062C1 |
| БИОПРИПОЙ ДЛЯ ЛАЗЕРНОЙ СВАРКИ БИОЛОГИЧЕСКИХ ТКАНЕЙ | 2016 |
|
RU2636222C1 |
| БИПОЛЯРНЫЙ ДАТЧИК ДЕФОРМАЦИИ НА ОСНОВЕ БИОСОВМЕСТИМОГО НАНОМАТЕРИАЛА | 2017 |
|
RU2662060C1 |
| СПОСОБ ЛАЗЕРНОЙ СВАРКИ БИОЛОГИЧЕСКИХ ТКАНЕЙ | 2010 |
|
RU2425700C1 |
| УНИПОЛЯРНЫЙ ДАТЧИК ДЕФОРМАЦИИ | 2018 |
|
RU2685570C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОСТРУКТУРИРОВАННОГО КОМПОЗИЦИОННОГО ЭЛЕКТРОПРОВОДЯЩЕГО ПОКРЫТИЯ | 2015 |
|
RU2606842C1 |

Изобретение относится к области медицины и, конкретно, к травматологии, и раскрывает способ изготовления нанокомпозитного имплантата связки сустава с покрытием из композитного биосовместимого наноматериала. Способ включает нанесение на поверхность заготовки имплантата связки сустава вспомогательного вещества - водно-белковой дисперсии углеродных нанотрубок с последующим формированием нанокомпозитного покрытия путем воздействия ИК-излучения в диапазоне длин волн 0,7-1,2 мкм, с мощностью на единицу площади 0,1-0,5 Вт/см2. Способ позволяет повысить механические свойства и степень биосовместимости имплантата связки сустава и может быть использован для восстановления функции поврежденной связки коленного сустава, а также других суставов. 4 з.п. ф-лы, 3 ил., 1 пр.
1. Способ изготовления имплантата связки коленного сустава, включающий нанесение на поверхность заготовки имплантата нанокомпозитного покрытия на основе вспомогательного вещества - водно-белковой дисперсии углеродных нанотрубок, отличающийся тем, что на основе водно-белковой дисперсии углеродных нанотрубок формируют нанокомпозитное покрытие имплантата связки коленного сустава путем водоиспаряющего воздействия инфракрасного излучения (ИК) в диапазоне длина волны 0,7-1,2 мкм и мощностью на единицу площади поверхности 0,1-0,5 Вт/см2.
2. Способ изготовления имплантата связки коленного сустава по п. 1, отличающийся тем, что концентрация белковой компоненты в водно-белковой дисперсии углеродных нанотрубок находится в пределах от 15 до 30 мас. %.
3. Способ изготовления имплантата связки коленного сустава по п. 1, отличающийся тем, что концентрация углеродных нанотрубок в водно-белковой дисперсии углеродных нанотрубок находится в пределах от 0,1 до 0,3 мас. %.
4. Способ изготовления имплантата связки коленного сустава по п. 1, отличающийся тем, что в качестве белковой компоненты водно-белковой дисперсии углеродных нанотрубок используют бычий сывороточный альбумин и бычий коллаген.
5. Способ изготовления имплантата связки коленного сустава по п. 1, отличающийся тем, что ИК-облучение слоя водно-белковой дисперсии углеродных нанотрубок, нанесенного на заготовку имплантата связки коленного сустава, осуществляют при вращении заготовки имплантата.
| Способ лазерной обработки нанокомпозитного покрытия имплантанта связки коленного сустава | 2016 |
|
RU2632114C1 |
| PODGAETSKII V | |||
| M | |||
| et.al | |||
| Laser-induced preparation of volume nanocompositions in aqueous albumin solutions | |||
| Quantum Electronics, 2007 | |||
| Пишущая машина | 1922 |
|
SU37A1 |
| Прибор для заливки подшипников баббитом | 1922 |
|
SU801A1 |
| ГЕРАСИМЕНКО А.Ю | |||
| и др | |||
| Перспективные наноматериалы с углеродными нанотрубками в биомедицинских приложениях | |||
| Медицинская техника, 2014, N6, с | |||
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
Авторы
Даты
2021-03-15—Публикация
2019-07-04—Подача