Настоящее изобретение относится к IL-17-связывающей молекуле, прежде всего к антителу к человеческому IL-17, более предпочтительно к человеческому антителу к человеческому IL-17 (который обозначают также IL-17A), и к применению таких антител при лечении опосредуемых IL-17 заболеваний и нарушений.
IL-17, продуцируемый Т-клетками цитокин, присутствующий, например, при ревматоидном артрите (РА), действует в качестве провоспалительного цитокина, прежде всего в сочетании с IL-1 и TNF-α (Chabaud M. и Miossec P., Arthritis Rheum 42, 1999 сс.963-970; Awane M. и др., J. Immunol 162, 1999, сс.5337-5344). IL-17 индуцирует производство ММР и осуществляет понижающую регуляцию TIMP (Jovanovic D.V. и др., J. Rheumatol. 28, 2001, сс.712-718), и блокада IL-1 и IL-17 оказывает синергетическое действие на воспаление и разрушение кости in vivo (Chabaud M. и Miossec, Arthritis Rheum 44, 2001, сс.1293-1303). Нарушение производства или избыточное производство IL-17 связано с патологией, характерной для различных заболеваний и нарушений, таких как ревматоидный артрит (Witowski и др., Cell Mol Life Sci 61, 2004, сс.567-579), остеоартрит, расшатывание костных имплантатов, острое отторжение трансплантатов (Antonysamy и др., J Immunol 162, 1999, сс.577-584; van Kooten и др., J Am Soc Nephrol 9, 1998, сс.1526-1534), септицемия, септический или эндотоксический шок, различные типы аллергий, астма (Molet и др., J Allergy Clin Immunol 108, 2001, сс.430-438), потеря костной ткани, псориаз (Teunissen и др., J Invest Dermatol 111, 1998, сс.645-649), ишемия, системный склероз (Kurasawa и др., Arthritis Rheum 43, 2000, сс.2455-2463), «удар» и другие воспалительные нарушения. Для лечения опосредуемых IL-17 заболеваний и нарушений были предложено применять антитела к IL-17; см., например, WO 95/18826 и обсуждение, приведенное во введении.
При создании настоящего изобретения были созданы обладающие улучшенными характеристиками антитела к человеческому IL-17, которые можно применять для лечения опосредуемых IL-17 заболеваний и нарушений.
Таким образом, изобретение относится к IL-17-связывающей молекуле, которая содержит антигенсвязывающий центр, включающий по меньшей мере одну вариабельную область тяжелой цепи (VH) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1, CDR2 и CDR3, где CDR1 имеет аминокислотную последовательность SEQ ID NO:I (N-Y-W-M-N), CDR2 имеет аминокислотную последовательность SEQ ID NO:2 (A-I-N-Q-D-G-S-E-K-Y-Y-V-G-S-V-K-G) и CDR3 имеет аминокислотную последовательность SEQ ID NO:3 (D-Y-Y-D-I-L-T-D-Y-Y-I-H-Y-W-Y-F-D-L);
или ее непосредственным эквивалентам, содержащим модифицированные CDR (CDR-эквиваленты).
Изобретение относится также к IL-17-связывающей молекуле, содержащей по меньшей мере одну вариабельную область легкой цепи (VL) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1', CDR2' и CDR3', где CDR1' имеет аминокислотную последовательность SEQ ID NO:4 (R-A-S-Q-S-V-S-S-S-Y-L-A), CDR2' имеет аминокислотную последовательность SEQ ID NO:5 (G-A-S-S-R-A-Т) и CDR3' имеет аминокислотную последовательность SEQ ID NO:6 (Q-Q-Y-G-S-S-P-C-T); или непосредственным CDR'-эквивалентам.
Другой вариант осуществления изобретения относится к IL-17-связывающей молекуле, которая содержит антигенсвязывающий центр, включающий по меньшей мере одну вариабельную область тяжелой цепи (VH) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1-x, CDR2-x и CDR3-x, где CDR1-x имеет аминокислотную последовательность SEQ ID NO:11 (G-F-T-F-S-N-Y-W-M-N), CDR2-x имеет аминокислотную последовательность SEQ ID NO:12 (A-I-N-Q-D-G-S-E-K-Y-Y) и CDR3-x имеет аминокислотную последовательность SEQ ID NO:
13 (C-V-R-D-Y-Y-D-I-L-T-D-Y-Y-I-H-Y-W-Y-F-D-L-W-G); или непосредственным CDR-x-эквивалентам.
Кроме того, изобретение относится также к IL-17-связывающей молекуле, которая содержит вариабельные области и тяжелой (VH) и легкой цепи (VL); при этом указанная IL-17-связывающая молекула содержит по меньшей мере один антигенсвязывающий центр, включающий:
а) вариабельную область тяжелой цепи (VH) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1, CDR2 и CDR3, где CDR1 имеет аминокислотную последовательность SEQ ID NO:1, CDR2 имеет аминокислотную последовательность SEQ ID NO:2 и CDR3 имеет аминокислотную последовательность SEQ ID NO:3, или непосредственные CDR-эквиваленты; и
б) вариабельную область легкой цепи (VL) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1', CDR2' и CDR3', где CDR1' имеет аминокислотную последовательность SEQ ID NO:4, CDR2' имеет аминокислотную последовательность SEQ ID NO:5 и CDR3' имеет аминокислотную последовательность SEQ ID NO:6, или непосредственные CDR'-эквиваленты.
Кроме того, изобретение относится также к IL-17-связывающей молекуле, которая содержит вариабельные области и тяжелой (VH) и легкой цепи (VL); при этом указанная IL-17-связывающая молекула содержит по меньшей мере один антигенсвязывающий центр, включающий:
а) вариабельную область тяжелой цепи (VH) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1-x, CDR2-x и CDR3-x, где CDR1-x имеет аминокислотную последовательность SEQ ID NO:11, CDR2-x имеет аминокислотную последовательность SEQ ID NO:12 и CDR3-x имеет аминокислотную последовательность SEQ ID NO:13, или непосредственные CDR-x-эквиваленты; и
б) вариабельную область легкой цепи (VL) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1', CDR2' и CDR3', где CDR1' имеет аминокислотную последовательность SEQ ID NO:4, CDR2' имеет аминокислотную последовательность SEQ ID NO:5 и CDR3' имеет аминокислотную последовательность SEQ ID NO:6, или непосредственные CDR'-эквиваленты.
Если не указано иное, любая представленная в описании полипептидная цепь имеет аминокислотную последовательность, которая начинается на N-конце и заканчивается на С-конце. Если антигенсвязывающий центр содержит и VH-, и VL-области, то они могут быть расположены на одной и той же полипептидной молекуле или предпочтительно каждая область может располагаться на разных цепях, VH-область может быть частью тяжелой цепи иммуноглобулина или ее фрагмента, а VL-область - частью легкой цепи иммуноглобулина или ее фрагмента.
Понятие «IL-17-связывающая молекула» обозначает любую молекулу, которая обладает способностью связываться с антигеном IL-17 либо индивидуально, либо в сочетании с другими молекулами. Реакцию связывания можно идентифицировать с помощью стандартных методов (качественные анализы), которые включают, например, анализ связывания, конкурентный анализ или биологический анализ, предназначенный для оценки ингибирования связывания IL-17 с его рецептором, или анализы связывания любого типа, в сравнении с отрицательным контролем, в котором используют антитело неродственной специфичности, но относящееся к тому же изотипу, например антитело к CD25 (см. пример 1).
Примеры антигенсвязывающих молекул включают антитела, продуцируемые В-клетками или гибридомами, и химерные антитела, антитела со встроенными путем трансплантации CDR или человеческие антитела или любые их фрагменты, например F(ab')2- и Fab-фрагменты, а также одноцепочечные или содержащие один домен антитела.
Одноцепочечное антитело состоит из вариабельных областей тяжелых и легких цепей антитела, ковалентно связанных пептидным линкером, который, как правило, состоит из 10-30 аминокислот, предпочтительно из 15-25 аминокислот. Таким образом, эта структура не включает константную область тяжелых и легких цепей, и можно предположить, что небольшой пептидный спейсер должен обладать менее выраженными антигенными свойствами, чем вся константная область. Понятие «химерное антитело» относится к антителу, в котором константные области тяжелых или легких цепей или и тех и других цепей получают из организма человека, а вариабельные области как тяжелых, так и легких цепей получают из организма кроме человека (например, мыши) или из организма человека, но которое представляет собой другое человеческое антитело. Понятие «антитело со встроенным путем трансплантации CDR» обозначает антитело, в котором гипервариабельные участки (CDR) получают из антитела-донора, такого как антитело из организма кроме человека (например, мыши) или другое человеческое антитело, в то время как все или практически все другие части иммуноглобулина, например константные области и высококонсервативные участки вариабельных областей, т.е. каркасные участки, получают из антитела-акцептора, например антитела из организма человека. Однако антитело с встроенным путем трансплантации CDR может включать небольшое количество аминокислот последовательности-донора в каркасных участках, например в частях каркасных участков, примыкающих к гипервариабельным участкам. Понятие «человеческое антитело» обозначает антитело, в котором все константные и вариабельные области как тяжелых, так и легких цепей получают из организма человека или они практически идентичны последовательностям антитела человека, но необязательно получены из этого же антитела, и включают полученные в организме мыши антитела, в которых мышиные гены вариабельных и константных областей иммуноглобулина заменены их человеческими копиями, например, как описано в ЕР 0546073 В1, US 5545806, 5569825, 5625126, 5633425, 5661016, 5770429. ЕР 0438474 В1 и ЕР 0463151 В1.
Особенно предпочтительные IL-17-связывающие молекулы, предлагаемые в изобретении, представляют собой человеческие антитела, прежде всего антитело AIN457, описанное ниже в примерах 1 и 2.
Так, в предпочтительных химерных антителах вариабельные области как тяжелой, так и легкой цепей получают из организма человека, например из антитела AIN457, последовательности которых представлены в SEQ ID NO:10 (вариабельная область легкой цепи, т.е. аминокислоты 1-109 SEQ ID NO:10) и SEQ ID NO:8 (вариабельная область тяжелой цепи, т.е. аминокислоты 1-127 SEQ ID NO:8). Домены константных областей предпочтительно также содержат приемлемые домены человеческих константных областей, например, как это описано в «Sequences of Proteins of Immunological Interest», Kabat E.A. и др., US Department of Health and Human Services, Public Health Service, National Institute of Health.
Гипервариабельные участки могут быть связаны с каркасными участками любого типа, хотя предпочтительно их получают из организма человека. Приемлемые каркасные участки описаны у Kabat E.A. и др., там же. Предпочтительный каркасный участок тяжелой цепи представляет собой каркасный участок человеческой тяжелой цепи, например антитела AIN457. Он состоит из последовательно расположенных участков FR1 (аминокислоты 1-30 SEQ ID NO:8), FR2 (аминокислоты 36-49 SEQ ID NO:8), FR3 (аминокислоты 67-98 SEQ ID NO:8) и FR4 (аминокислоты 117-127 SEQ ID NO:8). С учетом данных рентгеноструктурного анализа, с помощью которого определяли гипервариабельные участки AIN457, другой предпочтительный каркасный участок состоит из последовательно расположенных участков FR1-x (аминокислоты 1-25 SEQ ID NO:8), FR2-x (аминокислоты 36-49 SEQ ID NO:8), FR3-x (аминокислоты 61-95 SEQ ID NO:8) и FR4-x (аминокислоты 119-127 SEQ ID NO:8). Аналогично этому каркасный участок легкой цепи состоит из последовательно расположенных участков FR1' (аминокислоты 1-23 SEQ ID NO:10), FR2' (аминокислоты 36-50 SEQ ID NO:10), FR3' (аминокислоты 58-89 SEQ ID NO:10) и FR4' (аминокислоты 99-109 SEQ ID NO:10).
Таким образом, изобретение относится также к IL-17-связывающей молекуле, которая содержит по меньшей мере один антигенсвязывающий центр, включающий либо первый домен, аминокислотная последовательность которого практически идентична последовательности, представленной в SEQ ID NO:8, которая начинается с аминокислоты в положении 1 и заканчивается аминокислотой в положении 127, либо описанный выше первый домен и второй домен, аминокислотная последовательность которого практически идентична последовательности, представленной в SEQ ID NO:10, которая начинается с аминокислоты в положении 1 и заканчивается аминокислотой в положении 109.
Моноклональные антитела, которые вырабатываются против белка, встречающегося в естественных условиях у всех людей, как правило, получают в организме кроме человека, например в организме мыши, и поэтому они, как правило, представляют собой белки, не встречающиеся в организме человека. Непосредственным результатом этого является то, что полученное с помощью гибридомы ксеногенное антитело при введении людям вызывает нежелательный иммунный ответ, который главным образом опосредуется константной областью ксеногенного иммуноглобулина. Это существенно ограничивает применение таких антител, поскольку их нельзя вводить в течение длительных периодов времени. Вследствие этого особенно предпочтительно применять одноцепочечные, несущие один домен, химерные антитела, антитела со встроенным путем трансплантации CDR или, прежде всего, человеческие антитела, которые при введении людям, по-видимому, не должны вызывать выраженную аллогенную реакцию.
В свете вышеизложенного более предпочтительная IL-17-связывающаяя молекула, предлагаемая в изобретении, представляет собой человеческое антитело к IL-17, которое содержит по меньшей мере
а) тяжелую цепь иммуноглобулина или ее фрагмент, который включает (I) вариабельную область, содержащую последовательно расположенные гипервариабельные участки CDR1, CDR2 и CDR3, или непосредственные CDR-эквиваленты, и (II) константную область человеческой тяжелой цепи или ее фрагмент; где CDR1 имеет аминокислотную последовательность SEQ ID NO:I, CDR2 имеет аминокислотную последовательность SEQ ID NO:2 и CDR3 имеет аминокислотную последовательность SEQ ID NO:3; и
б) легкую цепь иммуноглобулина или ее фрагмент, который включает (I) вариабельную область, содержащую последовательно расположенные гипервариабельные участки и необязательно также гипервариабельные участки CDR1', CDR2' и CDR3' или непосредственные CDR'-эквиваленты, и (II) константную область человеческой легкой цепи или ее фрагмент, где CDR1' имеет аминокислотную последовательность SEQ ID NO:4, CDR2' имеет аминокислотную последовательность SEQ ID NO:5 и CDR3' имеет аминокислотную последовательность SEQ ID NO:6.
В другом варианте IL-17-связывающая молекула, предлагаемая в изобретении, может представлять собой одноцепочечную связывающую молекулу, которая содержит антигенсвязывающий центр антитела, включающий
а) первый домен, который содержит последовательно расположенные гипервариабельные участки CDR1, CDR2 и CDR3, или непосредственные CDR-эквиваленты, где CDR1 имеет аминокислотную последовательность SEQ ID NO:1, CDR2 имеет аминокислотную последовательность SEQ ID NO:2 и CDR3 имеет аминокислотную последовательность SEQ ID NO:3; и
б) второй домен, который содержит гипервариабельные участки CDR1', CDR2' и CDR3', или непосредственные CDR-эквиваленты, где CDR1' имеет аминокислотную последовательность SEQ ID NO:4, CDR2' имеет аминокислотную последовательность SEQ ID NO:5 и CDR3' имеет аминокислотную последовательность SEQ ID NO:6; и
в) пептидный линкер, который связан либо с N-концом первого домена и с С-концом второго домена, либо с С-концом первого домена и с N-концом второго домена.
Как хорошо известно, минорные изменения аминокислотной последовательности, такие как делеция, добавление или замена одной, небольшого количества или даже нескольких аминокислот, могут приводить к получению аллельной формы исходного белка, которая обладает практически идентичными свойствами.
Таким образом, понятие «их непосредственные CDR-эквиваленты» относится к IL-17-связывающим молекулам, содержащим последовательно расположенные гипервариабельные участки CDR1i, CDR2i и CDR3i, (вместо CDR1, CDR2, и CDR3), в которых
(I) гипервариабельный участок CDR1i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR1, последовательность которого представлена в SEQ ID NO:1; и
(II) гипервариабельный участок CDR2i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR2, последовательность которого представлена в SEQ ID NO:2; и
(III) гипервариабельный участок CDR3i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR3, последовательность которого представлена в SEQ ID NO:3; и
(IV) где такая молекула, содержащая последовательно расположенные гипервариабельные участки CDR1i, CDR2i и CDR3i, обладает способностью ингибировать на 50% активность 1 нМ (30 нг/мл) человеческого IL-17, которую измеряют по индуцируемому huIL-17 производству IL-6 в человеческих кожных фибробластах, при концентрации указанной молекулы, составляющей 50нМ, предпочтительно 20 нМ, более предпочтительно 10 нМ, еще более предпочтительно 5 нМ.
Аналогично этому понятие «их непосредственные CDR-x-эквиваленты» относится к IL-17-связывающим молекулам, содержащим последовательно расположенные гипервариабельные участки CDR1i-x, CDR2i-x и CDR3i-x (вместо CDR1-x, CDR2-x, и CDR3-x), в которых
(V) гипервариабельный участок CDR1i-x отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR1-x, последовательность которого представлена в SEQ ID NO:11; и
(VI) гипервариабельный участок CDR2i-x отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR2-x, последовательность которого представлена в SEQ ID NO:12; и
(VII) гипервариабельный участок CDR3i-x отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR3-x, последовательность которого представлена в SEQ ID NO:13; и
(VIII) где такая молекула, содержащая последовательно расположенные гипервариабельные участки CDR1i-x, CDR2i-x и CDR3i-x, обладает способностью ингибировать на 50% активность 1 нМ (30 нг/мл) человеческого IL-17, которую измеряют по индуцируемому huIL-17 производству IL-6 в человеческих кожных фибробластах, при концентрации указанной молекулы, составляющей 50 нМ, предпочтительно 20 нМ, более предпочтительно 10 нМ, еще более предпочтительно 5 нМ.
Аналогично этому понятие «его непосредственные CDR'-эквиваленты» относится к домену, содержащему последовательно расположенные гипервариабельные участки CDR1'i, CDR2'i и CDR3'i, в которых
(I) гипервариабельный участок CDR1'i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR1', последовательность которого представлена в SEQ ID NO:4; и
(II) гипервариабельный участок CDR2'i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR2', последовательность которого представлена в SEQ ID NO:5; и
(III) гипервариабельный участок CDR3'i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR3', последовательность которого представлена в SEQ ID NO:6; и
(IV) где такая молекула, содержащая последовательно расположенные гипервариабельные участки CDR1'i CDR2'i и CDR3'i, обладает способностью ингибировать на 50% активность 1 нМ (30 нг/мл) человеческого IL-17, которую измеряют по индуцируемому huIL-17 производству IL-6 в человеческих кожных фибробластах, при концентрации указанной молекулы, составляющей 50 нМ, предпочтительно 20нМ, более предпочтительно 10 нМ, еще более предпочтительно 5 нМ.
В альтернативном варианте IL-17-связывающая молекула, предлагаемая в изобретении, может представлять собой IL-17-связывающую молекулу, которая содержит по меньшей мере один антигенсвязывающий центр, включающий по меньшей мере одну вариабельную область тяжелой цепи (VH) иммуноглобулина, которая содержит последовательно расположенные
а) гипервариабельные участки CDR1 (SEQ ID NO:1), CDR2 (SEQ ID NO:2) и CDR3 (SEQ ID NO:3); или
б) гипервариабельные участки CDR1i, CDR2i, CDR3i, где гипервариабельный участок CDR1i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR1, последовательность которого представлена в SEQ ID NO:1; гипервариабельный участок CDR2i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR2, последовательность которого представлена в SEQ ID NO:2; и гипервариабельный участок CDR3i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR3, последовательность которого представлена в SEQ ID NO:3; и
указанная IL-17-связывающая молекула, содержащая последовательно расположенные гипервариабельные участки CDR1x, CDR2x и CDR3x, обладает способностью ингибировать на 50% активность 1 нМ (30 нг/мл) человеческого IL-17, которую измеряют по индуцируемому huIL-17 производству IL-6 в человеческих кожных фибробластах, при концентрации указанной молекулы, составляющей 50 нМ, предпочтительно 20 нМ, более предпочтительно 10 нМ, еще более предпочтительно 5 нМ.
Аналогично этому IL-17-связывающая молекула, предлагаемая в изобретении, может представлять собой IL-17-связывающую молекулу, которая содержит по меньшей мере один антигенсвязывающий центр, включающий по меньшей мере одну вариабельную область тяжелой цепи (VH) иммуноглобулина, которая содержит последовательно расположенные
а) гипервариабельные участки CDR1-x (SEQ ID NO:11), CDR2-x (SEQ ID NO:12) и CDR3-x (SEQ ID NO:13); или
б) гипервариабельные участки CDR1i-x, CDR2i-x, CDR3i-x, где гипервариабельный участок CDR1i-x отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR1-x, последовательность которого представлена в SEQ ID NO:11; гипервариабельный участок CDR2i-x отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR2-x, последовательность которого представлена в SEQ ID NO:12; и гипервариабельный участок CDR3i-x отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR3-x, последовательность которого представлена в SEQ ID NO:13; и
указанная IL-17-связывающая молекула, содержащая последовательно расположенные гипервариабельные участки CDR1i-x, CDR2i-x и CDR3i-x, обладает способностью ингибировать на 50% активность 1 нМ (30 нг/мл) человеческого IL-17, которую измеряют по индуцируемому huIL-17 производству IL-6 в человеческих кожных фибробластах, при концентрации указанной молекулы, составляющей 50 нМ, предпочтительно 20 нМ, более предпочтительно 10 нМ, еще более предпочтительно 5 нМ.
Аналогично этому IL-17-связывающая молекула, предлагаемая в изобретении, может представлять собой IL-17-связывающую молекулу, которая содержит по меньшей мере один антигенсвязывающий центр, включающий по меньшей мере одну вариабельную область легкой цепи (VL) иммуноглобулина, которая содержит последовательно расположенные
а) гипервариабельные участки CDR1' (SEQ ID NO:4), CDR2' (SEQ ID NO:5) и CDR3' (SEQ ID NO:6); или
б) гипервариабельные участки CDR1'i, CDR2'i, CDR3'i, где гипервариабельный участок CDR1'i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR1', последовательность которого представлена в SEQ ID NO:4; гипервариабельный участок CDR2'i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR2', последовательность которого представлена в SEQ ID NO:5; и гипервариабельный участок CDR3'i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR3', последовательность которого представлена в SEQ ID NO:6; и
указанная IL-17-связывающая молекула, содержащая последовательно расположенные гипервариабельные участки CDR1'i, CDR2'i и CDR3'i, обладает способностью ингибировать на 50% активность 1 нМ (30 нг/мл) человеческого IL-17, которую измеряют по индуцируемому huIL-17 производству IL-6 в человеческих кожных фибробластах, при концентрации указанной молекулы, составляющей 50 нМ, предпочтительно 20 нМ, более предпочтительно 10 нМ, еще более предпочтительно 5 нМ.
В альтернативном варианте IL-17-связывающая молекула, предлагаемая в изобретении, может представлять собой IL-17-связывающую молекулу, которая содержит вариабельные области как тяжелой цепи (VH), так и легкой цепи (VL), и IL-17-связывающая молекула содержит по меньшей мере один антигенсвязывающий центр, включающий:
а) вариабельную область тяжелой цепи (VH) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1 (SEQ ID NO:1), CDR2 (SEQ ID NO:2) и CDR3 (SEQ ID NO:3); и
вариабельную область легкой цепи (VL) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1' (SEQ ID NO:4), CDR2' (SEQ ID NO:5) и CDR3' (SEQ ID NO:6); или
б) вариабельную область тяжелой цепи (VH) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1i, CDR2i, CDR3i, где гипервариабельные участки CDR1i, CDR2i, CDR3i характеризуются тем, что гипервариабельный участок CDR1i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR1, последовательность которого представлена в SEQ ID NO:1; гипервариабельный участок CDR2i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR2, последовательность которого представлена в SEQ ID NO:2; и гипервариабельный участок CDR3i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR3, последовательность которого представлена в SEQ ID NO:3; и
вариабельную область легкой цепи (VL) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1'i, CDR2'i, CDR3'i, где гипервариабельный участок CDR1'i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR1', последовательность которого представлена в SEQ ID NO:4; гипервариабельный участок CDR2'i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR2', последовательность которого представлена в SEQ ID NO:5; и гипервариабельный участок CDR3'i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR3', последовательность которого представлена в SEQ ID NO:6; и
IL-17-связывающая молекула, указанная в подпункте б), которая содержит последовательно расположенные гипервариабельные участки CDR1i, CDR2i, CDR3i, CDR1i, CDR2'i и CDR3'i, обладает способностью ингибировать на 50% активность 1нМ (30 нг/мл) человеческого IL-17, которую измеряют по индуцируемому huIL-17 производству IL-6 в человеческих кожных фибробластах, при концентрации указанной молекулы, составляющей 50 нМ, предпочтительно 20 нМ, более предпочтительно 10 нМ, еще более предпочтительно 5 нМ.
В альтернативном варианте IL-17-связывающая молекула, предлагаемая в изобретении, может представлять собой IL-17-связывающую молекулу, которая содержит вариабельные области как тяжелой цепи (VH), так и легкой цепи (VL) иммуноглобулина, и IL-17-связывающая молекула содержит по меньшей мере один антигенсвязывающий центр, включающий:
а) вариабельную область тяжелой цепи (VH) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1-x (SEQ ID NO:11), CDR2-x (SEQ ID NO:12) и CDR3-x (SEQ ID NO:13); и
вариабельную область легкой цепи (VL) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1' (SEQ ID NO:4), CDR2' (SEQ ID NO:5) и CDR3' (SEQ ID NO:6); или
б) вариабельную область тяжелой цепи (VH) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1i-x, CDR2i-x и CDR3i-x, где гипервариабельные участки CDR1i, CDR2i, CDR3i характеризуются тем, что гипервариабельный участок CDR1i-x отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR1-x, последовательность которого представлена в SEQ ID NO:11; гипервариабельный участок CDR2i-x отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR2, последовательность которого представлена в SEQ ID NO:12; и гипервариабельный участок CDR3i-x отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR3-x, последовательность которого представлена в SEQ ID NO:13; и
вариабельную область легкой цепи (VL) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1'i, CDR2'i, CDR3'i, где гипервариабельный участок CDR1'i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR1', последовательность которого представлена в SEQ ID NO:4; гипервариабельный участок CDR2'i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR2', последовательность которого представлена в SEQ ID NO:5; и гипервариабельный участок CDR3'i отличается тремя, предпочтительно двумя, более предпочтительно одной аминокислотой от гипервариабельного участка CDR3', последовательность которого представлена в SEQ ID NO:6; и
IL-17-связывающая молекула, указанная в подпункте б), которая содержит последовательно расположенные гипервариабельные участки CDR1i, CDR2i, CDR3i, CDR1'i, CDR2'i и CDR3'i, обладает способностью ингибировать на 50% активность 1 нМ (30 нг/мл) человеческого IL-17, которую измеряют по индуцируемому huIL-17 производству IL-6 в человеческих кожных фибробластах, при концентрации указанной молекулы, составляющей 50 нМ, предпочтительно 20 нМ, более предпочтительно 10 нМ, еще более предпочтительно 5 нМ.
Ингибирование связывания IL-17 с его рецептором удобно тестировать путем проведения различных анализов, включая анализы, которые описаны ниже. Понятие «в такой же степени» обозначает, что молекула, с которой проводится сравнение, и эквивалентная молекула обладают практически одинаковой с точки зрения статистики активностью в отношении ингибирования IL-17 при исследовании с помощью одного из указанных в настоящем описании методов (см. пример 1). Например, IL-17-связывающие молекулы, предлагаемые в изобретении, как правило, имеют значения IC50, характеризующие ингибирование человеческого IL-17, которое оценивают по индуцируемому человеческим IL-17 производству IL-6 в человеческих кожных фибробластах, находящиеся в пределах +/- ×5, т.е. ниже 10 нМ, более предпочтительно 9, 8, 7, 6, 5, 4, 3 или 2 нМ (предпочтительно являются практически одинаковыми) относительно IC50 соответствующей молекулы, с которой проводится сравнение, при анализе с помощью методов, описанных в примере 1.
В альтернативном варианте применяемый анализ может представлять собой анализ конкурентного ингибирования связывания IL-17 с растворимыми IL-17-рецепторами (например, конструкциями человеческий IL-17 R/Fc, описанными в примере 1) и IL-17-связывающими молекулами, предлагаемыми в изобретении.
Наиболее предпочтительно человеческое антитело к IL-17 содержит по меньшей мере
а) одну тяжелую цепь, которая несет вариабельную область, аминокислотная последовательность которой практически идентична последовательности, представленной в SEQ ID NO:8, которая начинается с аминокислоты в положении 1 и заканчивается аминокислотой в положении 127, и константную область человеческой тяжелой цепи; и
б) одну легкую цепь, которая несет вариабельную область, аминокислотная последовательность которой практически идентична последовательности, представленной в SEQ ID NO:10, которая начинается с аминокислоты в положении 1 и заканчивается аминокислотой в положении 109, и константную область человеческой легкой цепи.
Константная область человеческой тяжелой цепи может быть γ1-, γ2-, γ3-, γ4-, µ-, α1-, α2-, δ- или ε-типа, предпочтительно γ-типа, более предпочтительно γ-типа, а константная область человеческой легкой цепи может быть κ- или λ-типа (включая λ1-, λ2- и λ3-подтипы), но предпочтительно κ-типа. Аминокислотные последовательности всех указанных константных областей приведены у Кэбота и др., выше.
Под объем изобретения подпадают также конъюгаты связывающих молекул, предлагаемых в изобретении, например конъюгаты с ферментом или токсином, или с радиоизотопом.
Понятие «полипептид», если в описании не указано иное, относится к любому пептиду или белку, который содержит аминокислоты, соединенные друг с другом пептидными связями, аминокислотная последовательность которого начинается на N-конце и заканчивается на С-конце. Предпочтительно полипептид, предлагаемый в настоящем изобретении, представляет собой моноклональное антитело, более предпочтительно химерное (также называемое антителом со встроенными путем трансплантации V-областями) или гуманизированное (также называемое антителом со встроенными путем трансплантации CDR) моноклональное антитело, наиболее предпочтительно полностью человеческое антитело, которое можно получать с помощью технологии, описанной в примере. Гуманизированное (со встроенными путем трансплантации гипервариабельными участками (CDR)) или полностью человеческое моноклональное антитело может содержать дополнительные мутации, введенные в последовательности каркасного участка (FR) акцепторного антитела, но может и не содержать их.
В контексте настоящего описания понятие «функциональное производное полипептида» относится к молекуле, обладающей качественной биологической активностью, присущей полипептиду, предлагаемому в настоящем изобретении, т.е. обладающей способностью связываться с человеческим IL-17. Понятие «функциональное производное» включает фрагменты и пептидные аналоги полипептида, предлагаемого в настоящем изобретении. Фрагменты представляют собой участки последовательности полипептида, предлагаемого в настоящем изобретении, например, конкретной последовательности. Понятие «производное» применяют для обозначения вариантов аминокислотной последовательности и ковалентных модификаций полипептида, предлагаемого в настоящем изобретении, например конкретной последовательности. Функциональные производные полипептида, предлагаемого в настоящем изобретении, например, конкретной последовательности, например гипервариабельного участка легкой и тяжелой цепи, предпочтительно имеют последовательности, которые гомологичны по меньшей мере примерно на 65%, более предпочтительно по меньшей мере примерно на 75%, еще более предпочтительно по меньшей мере примерно на 85%, наиболее предпочтительно по меньшей мере примерно на 95, 96, 97, 98, 99% полной аминокислотной последовательности полипептида, предлагаемого в настоящем изобретении, например конкретной последовательности, и сохраняют практически такую же способность связываться с человеческим IL-17 или, например, нейтрализовать индуцируемое IL-17 производство IL-6 в человеческих кожных фибробластах.
Понятие «ковалентная модификация» включает модификации полипептида, предлагаемого в настоящем изобретении, например, конкретной последовательности; или его фрагмента с использованием органического белкового или небелкового дериватизирующего агента, слияния с гетерологичными полипептидными последовательностями и посттрансляционные модификации. Ковалентно модифицированные полипептиды, например, имеющие конкретную последовательность, все еще сохраняют способность связываться с человеческим IL-17 или, например, нейтрализовать индуцируемое IL-17 производство IL-6 в человеческих кожных фибробластах. Как правило, ковалентные модификации интродуцируют путем взаимодействия аминокислотных остатков-мишеней с органическим дериватизирующим агентом, который обладает способностью взаимодействовать с выбранными боковыми или концевыми остатками, или путем использования механизмов посттрансляционных модификаций, функционирующих в выбранных рекомбинантных клетках-хозяевах. Определенные пост-трансляционные модификации являются результатом воздействия рекомбинантных клеток-хозяев на экспрессируемый полипептид. Глутаминильные и аспарагинильные остатки часто деамидируют после трансляции с получением соответствующих глутамильных и аспартильных остатков. В другом варианте эти остатки деаминируют в мягких кислотных условиях. Другие пост-трансляционные модификации включают гидроксилирование пролина и лизина, фосфорилирование гидроксильных групп остатков серила, тирозина или треонила, метилирование α-аминогрупп боковых цепей лизина, аргинина и гистидина (см., например, Т.Е.Creighton, Proteins: Structure и Molecular Properties, изд-во W.H.Freeman & Co., San Francisco, 1983, cc.79-86). Ковалентные модификации включают, например, слияние белков, содержащих полипептид, предлагаемый в настоящем изобретении, например, имеющий конкретную последовательность, и вариантов их аминокислотных последовательностей, например, с использованием иммуноадгезинов, и N-концевые слияния с гетерологичными сигнальными последовательностями.
Понятие «гомология» применительно к нативному полипептиду и его функциональному производному в контексте настоящего описания обозначает процент аминокислотных остатков в последовательности-кандидате, идентичных остаткам соответствующего нативного полипептида, после выравнивания последовательностей и при необходимости введения брешей для достижения максимального процента гомологии, и при оценке гомологии не учитываются никакие консервативные замены в качестве одного из критериев идентичности последовательностей. Ни N- или С-концевые удлинения, ни инсерции не рассматриваются в качестве элементов, снижающих идентичность или гомологию. Методы и компьютерные программы, применяемые для сравнительного анализа, хорошо известны.
Понятие «аминокислота(ы)» относится ко всем встречающимся в естественных условиях L-α-аминокислотам и, например, включает D-аминокислоты. Аминокислоты обозначают либо с помощью хорошо известного однобуквенного кода, либо с помощью трехбуквенного кода.
Понятие «вариант аминокислотной последовательности» относится к молекулам, которые имеют некоторые отличия по аминокислотным последовательностям по сравнению с полипептидом, предлагаемым в настоящем изобретении, например, имеющим конкретную последовательность. Варианты аминокислотной последовательности полипептида, предлагаемого в настоящем изобретении, например конкретной последовательности, все еще сохраняют способность связываться с человеческим IL-17 или, например, нейтрализовать индуцируемое IL-17 производство IL-6 в человеческих кожных фибробластах. Полученные с помощью замены варианты представляют собой варианты, у которых по меньшей мере один аминокислотный остаток удален и вместо него другая аминокислота встроена в это же положение в полипептиде, предлагаемом в настоящем изобретении, например, имеющем конкретную последовательность. Эти замены могут быть одиночными, когда заменена только одна аминокислота в молекуле, или они могут быть множественными, когда в одной и той же молекуле заменены две или большее количество аминокислот. Полученные с помощью инсерции варианты представляют собой варианты, в которых одна или несколько аминокислот встроены непосредственно по соседству с аминокислотой в определенном положении в полипептиде, предлагаемом в настоящем изобретении, например, имеющем конкретную последовательность. Понятие «непосредственно по соседству с аминокислотой» обозначает соединение с функциональной либо α-карбокси-, либо α-аминогруппой аминокислоты. Полученные с помощью делеции варианты представляют собой варианты, в которых одна или несколько аминокислот в полипептиде, предлагаемом в настоящем изобретении, например, имеющем конкретную последовательность, удалены. Как правило, полученные путем делеции варианты могут иметь одну или две делеции аминокислот в конкретной области молекулы.
IL-17-связывающую молекулу, предлагаемую в изобретении, можно создавать с помощью методов рекомбинантной ДНК. Так, можно конструировать одну или несколько молекул ДНК, кодирующих связывающую молекулу, помещать их под контроль соответствующих последовательностей и переносить в пригодный организм хозяина для экспрессии.
Таким образом, в наиболее широком смысле в изобретении предложены
(I) молекулы ДНК, кодирующие содержащую один домен IL-17-связывающую молекулу, предлагаемую в изобретении, одноцепочечную IL-17-связывающую молекулу, предлагаемую в изобретении, IL-17-связывающую молекулу, содержащую указанные в настоящем описании тяжелую и легкую цепи, или фрагменты IL-17-связывающей молекулы, предлагаемой в изобретении; и
(II) применение молекул ДНК, предлагаемых в изобретении, для получения IL-17-связывающей молекулы, предлагаемой в изобретении, с помощью методов рекомбинации.
Таким образом, в изобретении предложена молекула ДНК, кодирующая описанную выше IL-17-связывающую молекулу.
Кроме того, в изобретении предложена конструкция ДНК, содержащая молекулу ДНК, практически гомологичную SEQ ID NO:7 или SEQ ID NO:9.
Кроме того, в изобретении предложена конструкция ДНК, содержащая две молекулы ДНК, одна из которых практически гомологична SEQ ID NO:7 или ее непосредственному ДНКН-эквиваленту, а другая практически гомологична SEQ ID NO:9 или ее непосредственному ДНКL-эквиваленту.
Существующий уровень техники является таким, что позволяет специалисту в данной области синтезировать молекулы ДНК, предлагаемые в изобретении на основе представленной в настоящем описании информации, т.е. аминокислотных последовательностей гипервариабельных участков и кодирующих их последовательностей ДНК. Метод конструирования гена вариабельной области описан, например, в ЕРА 239400, и в целом состоит в следующем: клонируют ген, кодирующий вариабельную область МАт, независимо от его специфичности. Определяют сегменты ДНК, кодирующие каркасные и гипервариабельные участки, и сегменты ДНК, кодирующие гипервариабельные участки, удаляют таким образом, чтобы сегменты ДНК, кодирующие каркасные участки, сливать в стыках с приемлемыми сайтами рестрикции. Сайты рестрикции можно создавать в требуемых положениях путем мутагенеза молекулы ДНК с использованием стандартных процедур. Кассеты, несущие двухцепочечные синтетические CDR, получают путем синтеза ДНК на основе данных о последовательностях, представленных в SEQ ID NO:1 (CDR1), SEQ ID NO:2 (CDR2), SEQ ID NO:3 (CDR3), SEQ ID NO:4 (CDR1'), SEQ ID NO:5 (CDR2'). SEQ ID NO:6 (CDR6'), SEQ ID NO:11 (CDR1-x), SEQ ID NO:12 (CDR2-x), SEQ ID NO:13 (CDR3-x). Эти кассеты конструируют так, чтобы они имели «липкие» концы для встраивания путем лигирования в стыки каркаса.
Кроме того, для получения конструкции ДНК, кодирующей IL-17-связывающие молекулы, предлагаемой в изобретении, не требуется использовать мРНК из продуцирующей гибридому линии клеток. Так, в заявке РСТ WO 90/07861 представлены полные инструкции по получению антитела с помощью методов рекомбинантной ДНК на основе только письменной информации, например, о нуклеотидной последовательности гена. Метод заключается в синтезе нескольких олигонуклеотидов, их амплификации с помощью ПЦР и их сплайсинге с получением требуемой последовательности ДНК.
Научной общественности известны экспрессионные векторы, содержащие приемлемые промоторы или гены, кодирующие константные области тяжелой и легкой цепи. Так, после получения молекулы ДНК, предлагаемой в изобретении, ее можно принятым образом переносить в соответствующий экспрессионный вектор. Молекулы ДНК, кодирующие одноцепочечные антитела, можно получать также стандартными методами, например, описанными в WO 88/1649.
По аналогии с понятием «CDR-эквиваленты» понятие «ее непосредственные ДНКН-эквиваленты» обозначает первую конструкцию ДНК, кодирующую тяжелую цепь или ее фрагмент IL-17-связывающей молекулы, предлагаемой в изобретении, и включающую:
а) первый фрагмент, который кодирует вариабельную область, содержащую
чередующиеся каркасные и гипервариабельные участки, где гипервариабельные участки содержат последовательно расположенные CDR1i, CDR2i и CDR3i, где CDR1, гомологичен по меньшей мере на 50%, предпочтительно гомологичен по меньшей мере на 60, 70, 80, 85 или 90%, более предпочтительно гомологичен по меньшей мере на 95% гипервариабельному участку CDR1, имеющему SEQ ID NO:1, CDR2i гомологичен по меньшей мере на 50%, предпочтительно гомологичен по меньшей мере на 60, 70, 80, 85 или 90%, более предпочтительно гомологичен по меньшей мере на 95% гипервариабельному участку CDR2, имеющему SEQ ID NO:2, и CDR3i гомологичен по меньшей мере на 50%, предпочтительно гомологичен по меньшей мере на 60, 70, 80, 85 или 90%, более предпочтительно гомологичен по меньшей мере на 95% гипервариабельному участку CDR3, имеющему SEQ ID NO:3; этот первый фрагмент начинается с кодона, который кодирует первую аминокислоту вариабельной области, и заканчивается кодоном, который кодирует последнюю аминокислоту вариабельной области, и
б) второй фрагмент, кодирующий константную область тяжелой цепи или ее фрагмент, который начинается с кодона, который кодирует первую аминокислоту константной области тяжелой цепи, и заканчивается кодоном, который кодирует последнюю аминокислоту константной области или ее фрагмента, после которых расположен стоп-кодон; и при этом
в) указанная конструкция ДНК кодирует полипептид, который индивидуально или в сочетании с другим полипептидом обладает способностью ингибировать на 50% активность 1 нМ (30 нг/мл) человеческого IL-17, которую измеряют по индуцируемому huIL-17 производству IL-6 в человеческих кожных фибробластах, при концентрации указанной молекулы, составляющей 50 нМ, предпочтительно 20 нМ, более предпочтительно 10 нМ, еще более предпочтительно 5 нМ.
Аналогично этому понятие «ее непосредственные ДНКН-х-эквиваленты» обозначает первую альтернативную конструкцию ДНК, кодирующую тяжелую цепь или ее фрагмент IL-17-связывающей молекулы, предлагаемой в изобретении, и включающую:
а) первый фрагмент, который кодирует вариабельную область, содержащую
чередующиеся каркасные и гипервариабельные участки, где гипервариабельные участки содержат последовательно расположенные CDR1i-x, CDR2i-x и CDR3i-x, где CDR1i-x гомологичен по меньшей мере на 50%, предпочтительно гомологичен по меньшей мере на 60, 70, 80, 85 или 90%, более предпочтительно гомологичен по меньшей мере на 95% гипервариабельному участку CDR1, имеющему SEQ ID NO:11, CDR2i-x гомологичен по меньшей мере на 50%, предпочтительно гомологичен по меньшей мере на 60, 70, 80, 85 или 90%, более предпочтительно гомологичен по меньшей мере на 95% гипервариабельному участку CDR2-x, имеющему SEQ ID NO:12, и CDR3i гомологичен по меньшей мере на 50%, предпочтительно гомологичен по меньшей мере на 60, 70, 80, 85 или 90%, более предпочтительно гомологичен по меньшей мере на 95% гипервариабельному участку CDR3-x, имеющему SEQ ID NO:13; этот первый фрагмент начинается с кодона, который кодирует первую аминокислоту вариабельной области, и заканчивается кодоном, который кодирует последнюю аминокислоту вариабельной области, и
б) второй фрагмент, кодирующий константную область тяжелой цепи или ее фрагмент, который начинается с кодона, который кодирует первую аминокислоту константной области тяжелой цепи, и заканчивается кодоном, который кодирует последнюю аминокислоту константной области или ее фрагмент, после которой расположен стоп-кодон; и при этом
в) указанная конструкция ДНК кодирует полипептид, который индивидуально или в сочетании с другим полипептидом обладает способностью ингибировать на 50% активность 1 нМ (30 нг/мл) человеческого IL-17, которую измеряют по индуцируемому huIL-17 производству IL-6 в человеческих кожных фибробластах, при концентрации указанной молекулы, составляющей 50 нМ, предпочтительно 20 нМ, более предпочтительно 10 нМ, еще более предпочтительно 5 нМ.
Предпочтительно эти конструкции ДНК кодируют вариабельную область, содержащую чередующиеся каркасные и гипервариабельные участки, где гипервариабельные участки содержат последовательно расположенные CDR1, CDR2 и CDR3, где CDR1 имеет аминокислотную последовательность SEQ ID NO:1, CDR2 имеет аминокислотную последовательность SEQ ID NO:2 и CDR3 имеет аминокислотную последовательность SEQ ID NO:3. Более предпочтительно эти конструкции ДНК кодируют вариабельную область, содержащую чередующиеся каркасные и гипервариабельные участки, где гипервариабельные участки содержат последовательно расположенные CDR1-x, CDR2-x и CDR3-x, где CDR1-x имеет аминокислотную последовательность SEQ ID NO:11, CDR2-x имеет аминокислотную последовательность SEQ ID NO:12 и CDR3-x имеет аминокислотную последовательность SEQ ID NO:13. Более предпочтительно этот первый фрагмент кодирует вариабельную область, имеющую аминокислотную последовательность, практически идентичную аминокислотной последовательности, представленной в SEQ ID NO:8, начиная с аминокислоты в положении 1 и заканчивая аминокислотой в положении 127. Более предпочтительно первый фрагмент имеет нуклеотидную последовательность, представленную в SEQ ID NO:7, начиная с нуклеотида в положении 1 и заканчивая нуклеотидом в положении 381. Предпочтительно также второй фрагмент кодирует константную область человеческой тяжелой цепи, более предпочтительно константную область человеческой γ1-цепи. Этот второй фрагмент может представлять собой фрагмент ДНК геномного происхождения (который содержит интроны) или фрагмент кДНК (без интронов).
Аналогично этому понятие «ее непосредственные ДНКL-эквиваленты» обозначает вторую конструкцию ДНК, кодирующую легкую цепь или ее фрагмент IL-17-связывающей молекулы, предлагаемой в изобретении, и включает:
а) первый фрагмент, который кодирует вариабельную область, содержащую
чередующиеся каркасные и гипервариабельные участки; где гипервариабельные участки представляют собой CDR3i' и необязательно CDR1i' и CDR2i', где CDR1i' гомологичен по меньшей мере на 50%, предпочтительно гомологичен по меньшей мере 60, 70, 80, 85 или 90%, более предпочтительно гомологичен по меньшей мере на 95% гипервариабельному участку CDR1', имеющему SEQ ID NO:4, CDR2i' гомологичен по меньшей мере на 50%, предпочтительно гомологичен по меньшей мере на 60, 70, 80, 85 или 90%, более предпочтительно гомологичен по меньшей мере на 95% гипервариабельному участку CDR2', имеющему SEQ ID NO:5, и CDR3i' гомологичен по меньшей мере на 50%, предпочтительно гомологичен по меньшей мере на 60, 70, 80, 85 или 90%, более предпочтительно гомологичен по меньшей мере на 95% гипервариабельному участку CDR3', имеющему SEQ ID NO:6; этот первый фрагмент начинается с кодона, который кодирует первую аминокислоту вариабельной области, и заканчивается кодоном, который кодирует последнюю аминокислоту вариабельной области, и
б) второй фрагмент, кодирующий константную область легкой цепи или ее фрагмент, который начинается с кодона, который кодирует первую аминокислоту константной области легкой цепи, и заканчивается кодоном, который кодирует последнюю аминокислоту константной области или ее фрагмент, после которой расположен стоп-кодон; и при этом
в) указанная конструкция ДНК кодирует полипептид, который индивидуально или в сочетании с другим полипептидом обладает способностью ингибировать на 50% активность 1 нМ (30 нг/мл) человеческого IL-17, которую измеряют по индуцируемому huIL-17 производству IL-6 в человеческих кожных фибробластах, при концентрации указанной молекулы, составляющей 50 нМ, предпочтительно 20 нМ, более предпочтительно 10 нМ, еще более предпочтительно 5 нМ.
Предпочтительно указанная вторая конструкция ДНК кодирует вариабельную область, содержащую чередующиеся каркасные и гипервариабельные участки; где гипервариабельные участки содержат последовательно расположенные CDR1', CDR2' и CDR3', где CDR1' имеет аминокислотную последовательность SEQ ID NO:4, CDR2' имеет аминокислотную последовательность SEQ ID NO:5 и CDR3' имеет аминокислотную последовательность SEQ ID NO:6. Более предпочтительно указанный первый фрагмент второй конструкции ДНК кодирует вариабельную область, имеющую аминокислотную последовательность, практически идентичную аминокислотной последовательности, представленной в SEQ ID NO:10, начиная с аминокислоты в положении 1 и заканчивая аминокислотой в положении 109. Более предпочтительно первый фрагмент имеет нуклеотидную последовательность, представленную в SEQ ID NO:9, начиная с нуклеотида в положении 1 и заканчивая нуклеотидом в положении 327. Предпочтительно также второй фрагмент кодирует константную область человеческой легкой цепи, более предпочтительно константную область человеческой κ-цепи.
Предпочтительно первую и вторую конструкции ДНК используют совместно, однако их можно использовать также по отдельности.
Изобретение относится также к IL-17-связывающим молекулам, в которых один или несколько, как правило, лишь небольшое количество (например, 1-4) аминокислотных остатков в CDR1, CDR2, CDR3, CDR1-x, CDR2-x, CDR3-x, CDR1, CDR2' или CDR3', или в каркасных участках изменены, например путем мутации, например, с помощью сайт-направленного мутагенеза соответствующих последовательностей ДНК. Изобретение относится к последовательностям ДНК, кодирующим такие измененные IL-17-связывающие молекулы. В частности изобретение относится к IL-17-связывающим молекулам, в которых один или несколько остатков в CDR1' или CDR2' изменены по сравнению с остатками, представленными в SEQ ID NO:4 (для CDR1') и SEQ ID NO:5 (для CDR2').
В первой и второй конструкциях ДНК первый и второй фрагменты могут быть отделены друг от друга интроном, и в интрон между первым и вторым фрагментом может оказаться целесообразным встраивать энхансер. Присутствие энхансера, который транскрибируется, но не транслируется, может способствовать повышению эффективности транскрипции. В конкретных вариантах осуществления изобретения первая и вторая конструкции ДНК содержат энхансер гена тяжелой цепи предпочтительно из организма человека.
Каждую конструкцию ДНК помещают под контроль приемлемых контролирующих последовательностей, прежде всего под контроль приемлемого промотора. Можно использовать любой тип промотора при условии, что он адаптирован к организму-хозяину, в который конструкции ДНК должны быть перенесены для экспрессии.
Требуемое антитело можно получать в клеточной культуре или в организме трансгенного животного. Соответствующее трансгенное животное можно получать с помощью стандартных методов, которые включают микроинъекцию в яйцеклетки первой и второй конструкций ДНК, помещенных под контроль приемлемых контролирующих последовательностей, перенос полученных таким образом яйцеклеток в соответствующих псевдобеременных самок и отбор потомства, экспрессирующего требуемое антитело.
Когда цепи антитела получают в клеточной культуре, конструкции ДНК должны быть сначала встроены либо в один экспрессионный вектор, либо в два различных, но совместимых экспрессионных вектора, причем последний вариант является предпочтительным.
Таким образом, изобретение относится также к экспрессионному вектору, который может реплицироваться в линии прокариотических или эукариотических клеток и содержит по меньшей мере одну из описанных выше конструкций ДНК.
Каждый экспрессионный вектор, содержащий конструкцию ДНК, затем переносят в приемлемый организм-хозяин. Когда конструкции ДНК встроены индивидуально в два экспрессионных вектора, их можно переносить по отдельности, т.е. один тип вектора на клетку, либо посредством котрансформации, указанный последний вариант является предпочтительным. Приемлемый организм-хозяин может представлять собой линию клеток бактерий, дрожжей или млекопитающих, указанный последний вариант является предпочтительным. Более предпочтительно линию клеток млекопитающего получают из лимфомы, например миеломы, гибридомы или здоровых иммортализованных В-клеток, которые предпочтительно не экспрессируют тяжелую или легкую цепи никаких эндогенных антител.
Для экспрессии в клетках млекопитающих кодирующую последовательность IL-17-связывающей молекулы предпочтительно интегрируют в ДНК клетки-хозяина в локус, в котором может быть обеспечен высокий уровень экспрессии IL-17-связывающей молекулы или который является предпочтительным для обеспечения высокого уровня экспрессии IL-17-связывающей молекулы. Клетки, в которых кодирующая последовательность IL-17-связывающей молекулы интегрирована в такие предпочтительные локусы, можно выявлять и отбирать на основе данных об уровнях экспрессии IL-17-связывающей молекулы. Для получения клеток-хозяев, содержащих кодирующую последовательность IL-17-связывающей молекулы, можно применять любой селектируемый маркер; например, можно использовать ген dhfr/метотрексат, или эквивалентную систему отбора. Альтернативные системы для экспрессии IL-17-связывающих молекул, предлагаемых в изобретении, включают системы амплификации/селекции, основанные на применении GS, например, описанные в ЕР 0256055 В, ЕР 0323997 В и заявке на европейский патент ЕР-А 89303964.4.
Еще одним объектом изобретения является способ получения IL-17-связывающей молекулы, заключающийся в том, что (I) культивируют организм, трансформированный описанным выше экспрессионным вектором, и (II) выделяют IL-17-связывающую молекулу из культуры.
В контексте настоящего описания подразумевается, что антитело «способно ингибировать связывание IL-17, так же как и AIN457», если антитело обладает способностью ингибировать связывание IL-17 с его рецептором в той же степени, что и антитело AIN457, где понятие «в той же степени» имеет указанное выше значение.
Антитело AIN457 обладает аффинностью к связыванию с IL-17, которая превышает аффинности, известные ранее для антител к IL-17, в частности любых антител к человеческому IL-17. Так, AIN457 имеет константу равновесия диссоциации KD, характеризующую связывание с IL-17, составляющую примерно 0,188±0,036 нМ (по данным BIAcore-анализа, например, согласно методу, описанному в примере 2). Такая высокая аффинность к связыванию делает антитело AIN457 особенно привлекательным для применений в терапии.
В контексте настоящего описания фраза «опосредуемое IL-17 заболевание» включает все заболевания и медицинские состояния, которые прямо или косвенно связаны с IL-17, при этом понятие заболевание и медицинское состояние включает возникновение, развитие, прогресс, персистенцию или патологию заболевания или состояния.
В контексте настоящего описания понятия «лечение» или «лечить» относятся как к профилактическому или превентивному лечению, так и к исцеляющему или изменяющему течение болезни лечению, включая лечение пациента, который имеет риск заражения болезнью или для которого существует возможность заражения болезнью, а также пациентов, которые уже больны или у которых диагностировано наличие болезни или медицинского состояния, и включают подавление клинического рецидива.
IL-17-связывающие молекулы, как они определены выше, обладающие способностью специфически связываться с человеческим IL-17, прежде всего антитела, которые обладают способностью ингибировать связывание IL-17 с его рецептором; и антитела к IL-17, которые обладают способностью ингибировать на 50% активность 1 нМ (30 нг/мл) человеческого IL-17, которую измеряют по индуцируемому huIL-17 производству IL-6 в человеческих кожных фибробластах, при концентрации указанной молекулы, составляющей 50 нМ, предпочтительно 20 нМ, более предпочтительно 10 нМ, еще более предпочтительно 5 нМ, обозначены в настоящем описании как Антитела, предлагаемые в изобретении.
Предпочтительно Антитела, предлагаемые в изобретении, представляют собой человеческие антитела, наиболее предпочтительно антитело AIN457 или его непосредственные эквиваленты.
Антитела, предлагаемые в изобретении, блокируют воздействия IL-17 на его клетки-мишени и, таким образом, их можно применять для лечения опосредуемых IL-17 заболеваний и нарушений. Эти и другие виды фармакологической активности Антител, предлагаемых в изобретении, можно продемонстрировать с помощью стандартных методов тестирования, например, с помощью описанных ниже методов:
Нейтрализация зависимого от IL-17 производства интерлейкина-6 первичными человеческими фибробластами:
Производство IL-6 в первичных человеческих (кожных) фибробластах зависит от IL-17 (Hwang S.Y, и др., Arthritis Res Ther, 6, 2004, сс.120-128).
В целом метод заключается в следующем. Человеческие кожные фибробласты стимулируют рекомбинантным IL-17 в присутствии различных концентраций Антитела, предлагаемого в изобретении, или рецептора человеческого IL-17, содержащего Fc-фрагмент. Химерное антитело к CD25 Simulect® (басиликсимаб) используют в качестве негативного контроля. После стимуляции в течение 16 ч отбирают супернатант и анализируют IL-6 с помощью ELISA. Антитела, предлагаемые в изобретении, как правило, имеют значения IC50, характеризующие ингибирование производства IL-6 (в присутствии 1 нМ человеческого IL-17), составляющие примерно 50 нМ или менее (например, от примерно 0,01 до примерно 50 нМ), при тестировании согласно указанному выше методу, т.е. ингибирующую активность оценивают по индуцируемому hu-IL-17 производству IL-6 в человеческих кожных фибробластах. Предпочтительно Антитела, предлагаемые в изобретении, характеризуются значением IC50 ингибирования производства IL-6 при оценке указанным выше методом, составляющим примерно 20 нМ или менее, более предпочтительно примерно 10 нМ или менее, еще более предпочтительно примерно 5 нМ или менее, еще более предпочтительно примерно 2 нМ или менее, и еще более предпочтительно примерно 1 нМ или менее.
Как установлено с помощью описанного выше метода, Антитела, предлагаемые в изобретении, эффективно блокируют действия IL-17. Таким образом, Антитела, предлагаемые в изобретении, могут найти следующее применение в фармацевтике:
Антитела, предлагаемые в изобретении, можно применять для профилактики и лечения опосредуемых IL-17 заболеваний или медицинских состояний, например воспалительных состояний, аллергий и аллергических состояний, гиперчувствительных реакций, аутоиммунных заболеваний, серьезных инфекций и отторжения трансплантата органа или ткани.
Например, Антитела, предлагаемые в изобретении, можно применять для лечения реципиентов трансплантатов сердца, легкого, системы сердце-легкое, печени, почки, поджелудочной железы, кожи или роговицы, включая отторжение аллотрансплантата или отторжение ксенотрансплантата, и для предупреждения реакции «трансплантат против хозяина», например, возникающей после трансплантации костного мозга, а также связанного с артериосклерозом отторжения трансплантата органа.
Антитела, предлагаемые в изобретении, предпочтительно можно применять для лечения, предупреждения или облегчения аутоиммунного заболевания и воспалительных состояний, в частности воспалительных состояний, этиология которых включает аутоиммунный компонент, таких как артрит (например, ревматоидный артрит, хронический прогрессирующий артрит и деформирующий артрит), и ревматических заболеваний, включая воспалительные состояния и ревматические болезни, связанные с потерей костной ткани, связанную с воспалением боль, спондилоартропатии, включая анкилозирующий спондилоартрит, синдром Рейтера, реактивный артрит, псориатический артрит и энтерофатический артрит, гиперчувствительность (включая как гиперчувствительность дыхательный путей, так и кожную гиперчувствительность) и аллергии. Конкретные аутоиммунные заболевания, для лечения которых можно применять Антитела, предлагаемые в изобретении, включают аутоиммунные гематологические нарушения (такие, например, как гемолитическая анемия, апластическая анемия, истинная анемия эритроцитов и идиопатическая тромбоцитопения), системную красную волчанку, воспалительные мышечные нарушения, полихондрит, склеродермию, грануломатоз Вегенера, дерматомиозит, хронический активный гепатит, тяжелую псевдопаралитическую миастению, псориаз, синдром Стивенса-Джонсона, идиопатическую спру, аутоиммунное воспалительное заболевание кишечника (включая, например, неспецифический язвенный колит, болезнь Крона и синдром раздраженной толстой кишки), эндокринную офтальмопатию, болезнь Грейвса, саркоидоз, рассеянный склероз, первичный билиарный цирроз печени, юношеский диабет (сахарный диабет типа I), увеит (передний и задний), сухой кератоконъюнктивит и весенний кератоконъюнктивит, коллагеноз легкого, псориатический артрит и гломерулонефрит (без нефротического синдрома или с нефротическим синдромом, включая, например, идиопатический нефротический синдром или нефропатию с минимальным изменением), опухоли, рассеянный склероз, воспалительные заболевания кожи и роговицы, миозит, расшатывание костных имплантатов, нарушения метаболизма, такие как атеросклероз, диабет и дислипидемия.
Антитела, предлагаемые в изобретении, можно применять для лечения, предупреждения или облегчения астмы, бронхита, пневмокониоза, эмфиземы легкого и других обструктивных или воспалительных заболеваний дыхательных путей.
Антитела, предлагаемые в изобретении, можно применять для лечения нежелательных острых и гиперострых воспалительных реакций, которые опосредуются IL-17 или связаны с производством IL-17, или усиление секреции TNF под действием IL-17, например, острых инфекций, например, септического шока (например, эндотоксического шока и респираторного дистресс-синдрома взрослых), менингита, пневмоний; и серьезных ожогов; и для лечения кахексии или синдрома истощения, связанного с патологической секрецией TNF, что является следствием инфекции, рака или дисфункции органа, прежде всего, для лечения связанной со СПИДом кахексии, например, связанной с ВИЧ-инфекцией или являющейся ее следствием.
Антитела, предлагаемые в изобретении, особенно предпочтительно применять для лечения связанных с метаболизмом заболеваний костной ткани, включая остеоартрит, остеопороз и другие воспалительные артриты, и потерю костной ткани в целом, включая связанную с возрастом потерю костной ткани, и, прежде всего, заболевание периодонта.
Соответствующая доза, которую можно применять для лечения указанных выше показаний, естественно, должна варьироваться в зависимости, например, от конкретного применяемого Антитела, предлагаемого в изобретении, хозяина, пути введения и природы и серьезности состояния, подлежащего лечению. При этом для профилактики удовлетворительные результаты, как правило, получают при использовании доз от примерно 0,05 до примерно 10 мг на кг веса тела, более предпочтительно от примерно 0,1 до примерно 5 мг кг веса тела. Частота введения доз при применении в профилактических целях, как правило, составляет от примерно одного раза в неделю до примерно одного раза каждые 3 месяца, более предпочтительно от примерно одного раза каждые 2 недели до примерно 1 раза каждые 10 недель, например один раз каждые 4-8 недель. Антитело, предлагаемое в изобретении, целесообразно вводить парентерально, внутривенно, например, в находящуюся впереди от локтевого сустава или другую периферическую вену, внутримышечно или подкожно. Профилактическое лечение включает, как правило, введение Антитела, предлагаемого в изобретении, от одного раза в месяц до одного раза каждые 2-3 месяца или еще реже.
Антитела, предлагаемые в изобретении, можно вводить в качестве единственного действующего вещества или в сочетании с (например, в качестве адъюванта или в составе комбинации) другими лекарственными средствами, например, иммунодепрессантами или иммуномодуляторами или другими противовоспалительными агентами, например, для лечения или предупреждения указанных выше заболеваний. Например, Антитела, предлагаемые в изобретении, можно применять в комбинации с DMARD, например солями золота, сульфасалазином, противомалярийными средствами, метотрексатом, D-пеницилламином, азатиоприном, микофеноловой кислотой, циклоспорином А, такролимусом, сиролимусом, миноциклином, лефлуномидом, глюкокортикоидами; ингибитором кальцинеурина, например, циклоспорином А или FK 506; модулятором рециркуляции лимфоцитов, например, FTY720 и аналогами FTY720; ингибитором mTOR, например, рапамицином, 40-O-(2-гидроксиэтил)рапамицином, CCI779, АВТ578, АР23573 или TAFA-93; аскомицином, обладающим иммунодепрессантными свойствами, например, АВТ-281, ASM981 и т.д.; кортикостероидами; циклофосфамидом; азатиопреном; метотрексатом; лефлуномидом; мизорибином; микофеноловой кислотой; микофенолятом мофетила; 15-дезоксиспергуалином или его гомологом, аналогом или производным, обладающим иммунодепрессантными свойствами; иммунодепрессантными моноклональными антителами, например моноклональными антителами к рецепторам лейкоцитов, например, ГКГ, CD2, CD3, CD4, CD7, CD8, CD25, CD28, CD40, CD45, CD58, CD80, CD86 или их лигандам; другими иммуномодуляторами, например рекомбинантной связывающей молекулой, содержащей по меньшей мере фрагмент внеклеточного домена CTLA4 или его мутанта, например по меньшей мере внеклеточный фрагмент CTLA4 или его мутанта, присоединенный к последовательности белка, отличного от CTLA4, например CTLA4Ig (например, имеющего номер АТСС 68629) или его мутанта, например LEA29Y; ингибиторами адгезионных молекул, например, антагонистами LFA-1, антагонистами ICAM-1 или -3, антагонистами VCAM-4 или антагонистами VLA-4; или химиотерапевтическим агентом, например, паклитакселом, гемцитабином, цисплатином, доксорубицином или 5-фторурацилом; анти-ТКР-агентами, например моноклональными антителами к TNF, например инфликсимабом, адалимумабом, CDP870, или конструкциями к рецепторам TNF-RI или TNF-RII, например, Etanercept, PEG-TNF-RI; блокаторами провоспалительных цитокинов, блокаторами IL-1, например, Anakinra или «ловушкой» IL-1, AAL160, ACZ 885, блокаторами IL-6; блокаторами хемокинов, например ингибиторами или активаторами протеаз, например металлопротеаз, антителами к IL-15, антителами к IL-6, антителами к CD20, НСПВЛ, такими как аспирин или противоинфекционный агент (перечень не ограничен перечисленными агентами).
В соответствии с вышеизложенным следующими объектами настоящего изобретения являются:
Способ, как он описан выше, заключающийся в том, что совместно, например одновременно или последовательно, вводят в терапевтически эффективном количестве IL-17-связывающую молекулу, например Антитело, предлагаемое в изобретении, и по меньшей мере одну вторую лекарственную субстанцию, где вторая лекарственная субстанция представляет собой иммунодепрессант/иммуномодулятор, противовоспалительное химиотерапевтическое или противоинфекционное лекарственное средство, например, указанное выше.
Терапевтическая комбинация, например набор, содержащая(ий) в терапевтически эффективном количестве а) IL-17-связывающую молекулу, например Антитело, предлагаемое в изобретении, и б) по меньшей мере одну вторую субстанцию, выбранную из иммунодепрессанта/иммуномодулятора, противовоспалительного химиотерапевтического или противоинфекционного лекарственного средства, например, указанного выше. Набор может содержать инструкции по его применению.
Когда Антитела, предлагаемые в изобретении, вводят в сочетании с другими иммунодепрессантами/иммуномодуляторами, противовоспалительными химиотерапевтическими или противоинфекционными терапевтическими лекарственными средствами, очевидно, что дозы совместно вводимого в составе комбинации соединения должны варьироваться в зависимости от типа совместно применяемого лекарственного средства, например, от того, представляет оно DMARD, анти-TNF, блокатор IL-1 или другое лекарственное средство, от конкретного применяемого лекарственного средства, от состояния, подлежащего лечению и т.д.
Фармацевтические композиции, предлагаемые в изобретении, можно приготавливать обычным образом. Композиция, предлагаемая в изобретении, предпочтительно находится в лиофилизированной форме. Непосредственно перед введением лиофилизат растворяют в пригодном водном носителе, например, в стерильной воде для инъекций или в стерильном забуференном физиологическом растворе. Если требуется больший объем раствора для введения путем инфузии, например, для быстрого внутривенного введения больших объемов жидкости, предпочтительно в виде болюсной инъекции, целесообразно в физиологический раствор во время приготовления состава добавлять человеческий сывороточный альбумин или гепаринизированную собственную кровь пациента. В альтернативном варианте композицию вводят подкожно. Присутствие избытка такого физиологически инертного белка препятствует потере антитела в результате адсорбции стенками контейнера и пробирки, которые используются вместе с раствором для инфузии. Если применяют альбумин, то приемлемые концентрации составляют от 0,5 до 4,5% в пересчете на массу физиологического раствора. Другие композиции представляют собой жидкие или лиофилизированные композиции.
Ниже изобретение более подробно проиллюстрировано на примерах.
Примеры
Для получения антител к человеческому IL-17 используют трансгенную линию мышей, созданную для экспрессии человеческого спектра IgG/к вместо мышиного спектра иммуноглобулинов (Fishwild и др., Nat. Biotechnol., 14, 1996, сс.845-851). В-клетки этих мышей иммортализуют с помощью стандартных методов на основе гибридом и получают клетки мышиной гибридомы, которые секретируют человеческое антитело AIN457 изотипа IgG1/κ.
Пример 1: Получение гибридомы, очистка антител, отбор антитела AIN457
Получение рекомбинантного человеческого IL-17 (huIL-17):
Рекомбинантный huIL-17 либо получают в тельцах включения в Е.coli и восстанавливают укладку цепи обычными методами (получают в собственной лаборатории (без носителя, Е.coli; фирма Novartis Pharma, партия ВМ-Е3141/98) или покупают (без носителя, Е.coli; фирма R&D Systems, №317-IL/CF)), либо в виде секретированного и частично гликозилированного белка в клетках линии HEK/EBNA (рекомбинантный huIL-17, без носителя (IL-17 APP-C6 из трансфектированных клеток HEK/EBNA; фирма Novartis Pharma, партия En.Е-3382/82; 0,28 мг/мл; рекомбинантный huIL-17, без носителя (IL-17 АРР-С4 из трансфектированных клеток HEK/EBNA; фирма Novartis Pharma, партия En.Е-3382/83; 0,29 мг/мл)). Последняя форма отличается наличием состоящего из 4 аминокислот С-концевого удлинения, способствующего быстрому выделению из супернатантов культур с помощью иммуноаффинной хроматографии. В этом случае супернатанты культур вносят на колонку соответствующего размера, содержащую специфическое иммобилизованное антитело к метке, связанное с активированной с помощью CNBr сефарозой 4В с плотностью 10 мг/мл смолы, следуя инструкциям производителя (фирма Pharmacia). После отмывки до исходного уровня с помощью ЗФР связанный huIL-17 элюируют с помощью 100 мМ глицина, рН 2,7, и сразу нейтрализуют разбавленным NaOH.
Связывание huIL-17 с гемоцианином лимфы улитки (KLH):
HuIL-17, полученный либо в Е.coli, либо в HEK/EBNA, связывают с KLH, предварительно активированным с помощью избытка гомобифункционального перекрестносшивающего агента дисукцинимидилсуберата (DSS). В целом метод состоит в следующем. 20 мг лиофилизированной марикультуры KLH Imject® (фирма Pierce №77600) восстанавливают с помощью 2 мл Н2О, получая раствор (10 мг/мл), содержащий забуференный фосфатом физиологический раствор (ЗФР), рН 7,2. К этому раствору добавляют 400 мкл 250 мМ DSS в диметилсульфоксиде (ДМСО) и смесь перемешивают в течение примерно 1 ч при комнатной температуре (реагенты растворяются не полностью и образуется некоторое количество осадка). Затем после непродолжительного центрифугирования и фильтрации (0,45 мкм) раствор обессоливают на Sephadex G25 fine (фирма Pharmacia) в ЗФР (скорость потока 2 мл/мин), получая примерно 11 мг активированного KLH с концентрацией 1,5 мг/мл (по методу Брэдфорда (Bradford)). 1 мл активированного KLH (1,5 мг) смешивают с 1 мл водного раствора (9 мг/мл) лиофилизированного полученного в Е.coli huIL-17 (партия ВМ-Е3141/98). Раствор остается прозрачным и его инкубируют в течение 2 ч при комнатной температуре. Концентрация образовавшегося комплекса составляет 1,4 мг/мл (измеренная методом Брэдфорда). 1 мл активированного KLH (1,5 мг) смешивают с 1 мл полученного в HEK/EBNA huIL-17 (примерно 3 мг в воде; партия En.Е-3 382/83). Раствор остается прозрачным и его инкубируют в течение 2 ч при комнатной температуре. Концентрация (измеренная по методу Брэдфорда) составляет 2,9 мг/мл.
Иммунизация: Созданную с помощью генной инженерии мышь 27340 (самка; фирма MEDAREX Inc, Анандал, шт. Нью-Джерси), в которой мышиные гены вариабельной и константной областей иммуноглобулина функционально заменены их человеческими копиями (генотип Tg код 221100-TgH (CMD)++; TgN(Hco7)11952+; TgH(JKD)++; TgN(KC05)9272+ (см. также у Sherie L. Morrison, Nature, том. 368, 1994, сс.812-813; Nils Lonberg и др., Nature, том 368, 1994, сс.856-859), иммунизируют с использованием приведенной в таблице 1 схемы.

Образцы сыворотки берут в 35 и 99 дни после начала протокола иммунизации для измерения уровней антитела к huIL17 с помощью твердофазного иммуноферментного анализа (ELISA).
Получение гибридом: В день 120 мышь 27340 умерщвляют путем с ингаляции CO2. Общие клетки селезенки (1×108) сливают с клетками линии PAI-0 (5×107 клеток) с использованием PEG 4000. Слитые клетки высевают в 720 лунок (1 мл/лунку), содержащих питающий подслой мышиных клеток брюшины (мыши линии Balb/c), в НАТ-среде (среда RPMI 1640, содержащая 2 г/л бикарбоната натрия, 5×10-5 М β-меркаптоэтанол, 10-4 М гипоксантин, 1,6×10-5 М тимидин, 4×10-7 М аминоптерин, 10% инактивированной тепловой обработкой FCS и 50 мкг/мл гентамицина). В день 14 НАТ-среду заменяют НТ-средой, т.е. НАТ-средой без аминоптерина. Скрининг начинают в день 10 и осуществляют в течение двух недель. Из исходных засеянных 720 лунок 684 лунки (95%) оказываются позитивными в отношении роста гибридомы. Супернатанты собирают и осуществляют с помощью ELISA отбор МАт, реакционноспособных в отношении huIL-17, с использованием huIL-17, полученного как с помощью Е.coli, так и HEK/EBNA. Пятьдесят две исходные лунки оценивают как позитивные в отношении присутствия антител к huIL-17. Двадцать восемь гибридом клонируют, а остальные замораживают. Клонирование осуществляют в 4-х 96-луночных титрационных микропланшетах в НТ-среде с использованием питающего подслоя мышиных клеток брюшины. Гибридомы высевают из расчета 0,5 клетки/100 мкл на лунку. Лунки обследуют с помощью микроскопа в отношении роста и позитивные лунки подпитывают 100 мкл НТ-среды. На следующий день супернатанты оценивают в отношении производства антител с помощью специфического для huIL-17 ELISA. После клонирования большинство клонированных гибридом сохраняют способность секретировать моноклональное антитело (МАт), специфическое к huIL-17.
Производство и очистка антитела: Отобранные клоны переносят в бессывороточную среду (5 мл) в колбы площадью 25 см2, содержащие ТК (ТК: тканевая культура). Гибридомы прогрессивно размножают в бессывороточной среде в колбах площадью 75 см2, содержащих ТК, и в роллер-флаконах. Все различные МАт к huIL17, включая NVP-AIN457-NX, (340-110-28, что означает номер мыши-номер гибридомы-номер клона) очищают с помощью аффинной хроматографии с использованием протеина А. Значение рН супернатантов культур доводят до 7,3 и их вносят на колонку соответствующего размера с протеин А-сефарозой 4, предназначенную для измерения при большой скорости потока (фирма Pharmacia). После отмывки до исходного уровня с помощью 100 мМ фосфатного буфера, рН 7,3, связанные антитела элюируют с использованием 50 мМ цитрата, рН 2,7, 140 мМ NaCl. Элюированную фракцию сразу же нейтрализуют (рН 7,0) и стерилизуют фильтрацией. Концентрацию белка определяют по абсорбции при 280 нм с использованием коэффициента 1,35 единиц абсорбции (AU)/мг.
Ингибирующая активность МАт к huIL-17 в отношении индуцируемого huIL-17 производства IL-6 в человеческих кожных фибробластах: Человеческие кожные фибробласты культивируют в FBM-среде, дополненной 2% FCS, инсулином (5 мкг/мл), основным человеческим фактором роста фибробластов (huFGF-щелочной) (0,1 мкг/мл) и гентамицином (50 мкг/мл). Фибробласты отделяют от пластика с помощью раствора трипсин/ЭДТК. Фибробласты вносят в 96-луночные титрационные микропланшеты с плотностью 1×104 клеток/лунку в FBM-среде, дополненной 1% FCS. Фибробластам дают прилипнуть к планшетам в течение ночи. На следующее утро среду удаляют и добавляют свежую FBM-среду, дополненную 1% FCS, huIL-17 (в различных концентрациях от 30 до 500 нг/мл) и супернатантами гибридомы (конечное разведение 1/5) или очищенными антителами, до конечного объема 200 мкл. После инкубации в течение 24 ч супернатанты культур собирают и оценивают с помощью ELISA производство huIL-6.
ELISA для обнаружения антител к huIL-17: Титрационные микропланшеты для ELISA сенсибилизируют рекомбинантным huIL-17 (100 мкл/лунку, 3 мкг/мл; партия ВМ-Е3141/98 или En.Е-3382/82) в ЗФР, содержащем 0,02% NaN3, и инкубируют в течение ночи при комнатной температуре. На следующий день титрационные микропланшеты блокируют с помощью 300 мкл ЗФР/2% БСА/0,02% NaN3 в течение 2 ч при 37°С. Затем планшеты отмывают 4 раза с помощью ЗФР/0,05% Твин 20/0,02% NaN3. Добавляют разведения сыворотки мыши 27340 (конечный диапазон разведении в день 35: от 1/100 до 1/3200; конечный диапазон разведении в день 99: от 1/200 до 1/12800; 100 мкл/лунку) или супернатанты культур гибридом (конечное разведение 1:3; 100 мкл/лунку). После инкубации в течение ночи при комнатной температуре планшеты отмывают 4 раза с помощью ЗФР/0,05% Твин 20/0,02% NaN3. Конъюгированный с биотином Fc-фрагмент мышиного антитела, специфического к hu-IgG, добавляют в конечном разведении 1/20000 (100 мкл/лунку). Образцам дают прореагировать в течение 4 ч при комнатной температуре. После отмывки (4 раза) добавляют стрептавидин, конъюгированный со щелочной фосфатазой, в конечном разведении 1/8000 (100 мкл/лунку). После выдерживания в течение 40 мин при комнатной температуре планшеты снова отмывают 4 раза и добавляют субстрат (пара-нитрофенилфосфат в диэтиламиновом буфере, рН 9,8; 150 мкл/лунку). Через 30 или 45 мин в зависимости от протекания реакции планшеты считывают с помощью ридера для микропланшетов (фирма Bio-Rad) с использованием фильтров для 405 и 490 нм.
ELISA для обнаружения изотипа антитела: Для определения изотипа МАт супернатанты культур (100 мкл; конечное разведение 1/5) вносят в лунки титрационных микропланшетов, сенсибилизированных huIL-17 (см. выше), и инкубируют в течение ночи при комнатной температуре. После отмывки (4 раза) добавляют по 100 мкл/лунку конъюгированных с биотином мышиных МАт к человеческому IgGI (конечное разведение 1/1000), IgG2 (конечное разведение 1/1000), IgG3 (конечное разведение 1/1000), IgG4 (конечное разведение 1/2000) или к человеческой легкой κ-цепи (конечное разведение 1/1000) в течение 4 ч при комнатной температуре. В качестве контроля используют конъюгированное с биотином крысиное МАт, специфическое к мышиной легкой λ1- и λ2-цепи (конечное разведение 1/1000). После этого, как описано выше, осуществляют отмывку и добавление стрептавидина, конъюгированного со щелочной фосфатазой (100 мкл; конечное разведение 1/8000). После отмывки (4 раза) добавляют субстрат (пара-нитрофенилфосфат в диэтиламиновом буфере; 100 мкл). Через 30 или 45 мин в зависимости от протекания реакции планшеты считывают с помощью ридера для микропланшетов (фирма Bio-Rad) с использованием фильтров для 405 и 490 нм.
ELISA для обнаружения производства huIL-6:
Титрационные микропланшеты для ELISA сенсибилизируют мышиным МАт к huIL-6 (МАВ206 от фирмы R&D system; 100 мкл/лунку, 4 мкг/мл) в ЗФР, содержащем 0,02% NaN3, и инкубируют в течение ночи при комнатной температуре. На следующий день титрационные микропланшеты блокируют с помощью 300 мкл ЗФР/2% БСА/0,02% NaN3 в течение 2 ч при 37°С. Затем планшеты отмывают 4 раза с помощью ЗФР/0,05% Твин 20/0,02% NaN3. Добавляют супернатанты человеческих кожных фибробластов (конечное разведение 1:3; 100 мкл/лунку). Для получения кривой титрования осуществляют титрование huIL-6 (100 мкл/лунку) от 400 пг/мл до 3,1 пг/мл путем разведении 1:2. После инкубации в течение ночи при комнатной температуре планшеты отмывают 4 раза с помощью ЗФР/0,05% Твин 20/0,02% NaN3. Добавляют конъюгированное с биотином козье антитело к huIL-6 (ВАР206; фирма R&D Systems) (25 нг/мл; 100 мкл/лунку). Образцам дают прореагировать в течение 4 ч при комнатной температуре. После отмывки (4 раза) добавляют стрептавидин, конъюгированный со щелочной фосфатазой, в конечном разведении 1/8000 (100 мкл/лунку). После выдерживания в течение 40 мин при комнатной температуре планшеты снова отмывают 4 раза и добавляют субстрат (иоря-нитрофенилфосфат в диэтиламиновом буфере, рН 9,8; 150 мкл/лунку). Через 30 мин планшеты считывают с помощью ридера для микропланшетов (фирма Bio-Rad) с использованием фильтров для 405 и 490 нм.
Расчеты: Результаты представлены в виде измеренных величин ОП или в виде % ингибирования, рассчитанного на основе средних значений по двум повторностям. Представлены дополнительные данные в виде средних значений ± С.К.О. Для измерения концентрации huIL-6 в супернатантах культуры используют стандартную кривую для huIL-6, полученную путем подбора кубической зависимости.
Результаты
Сывороточные титры мыши 27340:

Сыворотку мыши 27340 анализируют с помощью ELISA на наличие антител к huIL-17 в дни 35 и 99 с использованием двух различных препаратов huIL-17 (таблица 2). Результаты свидетельствуют о том, что сывороточные титры мыши 27340 возрастают примерно в четыре раза в период времени между днем 35 и днем 99 и что можно распознавать оба препарата huIL-17.
Анализ связывания супернатантов гибридомы с помощью ELISA: 684 супернатанта анализируют с помощью ELISA на наличие антител к huIL-17 с использованием двух препаратов рекомбинантного huIL-17, первый из которых получают из Е. coli (BM-E3141/98), а последний из клеток HEK/EBNA (En.Е-3382/82). Пятьдесят два супернатанта дают позитивную реакцию в отношении присутствия антител к huIL-17 (таблица 3). В отдельных случаях выявлено предпочтительное связывание с тем или другим препаратом huIL-17. 28 гибридом, которые затем клонируют, подчеркнуты.
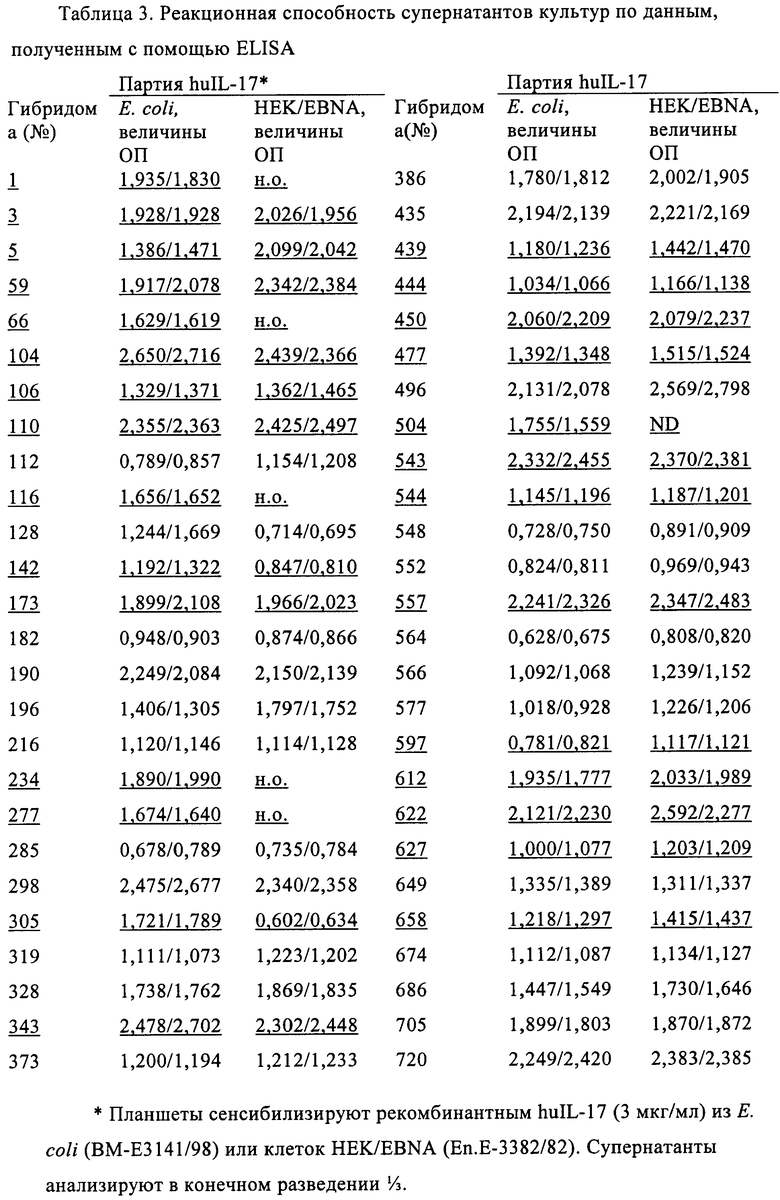
Анализ связывания супернатантов культур клонов гибридомы с помощью ELISA: Полученные с помощью ELISA результаты оценки реакционной способности супернатантов клонов 11 гибридом, которые сохраняли наиболее высокую способность продуцировать МАт к huIL-17, представлены в таблице. Клоны, выделенные жирным шрифтом, отбирают для получения ~1 л супернатанта в роллер-флаконах для очистки и анализа антител. За исключением клонов, полученных из гибридомы №5, которая продуцирует антитело huIgG3κ, все остальные клоны продуцируют МАт huIgG1κ, о чем свидетельствуют результаты определения изотипа специфических моноклональных антител.
Нейтрализующая активность супернатантов культур: Супернатанты культур анализируют в отношении ингибирования стимулируемого рекомбинантным huIL-17 производства huIL-6 в человеческих кожных фибробластах. Как представлено в таблице 5, большинство супернатантов культур обладает ингибирующей активностью.

Нейтрализующая активность AIN45: Отбор клона 110-28 для производства перспективного кандидата AIN457 (предпочтительный вариант осуществления изобретения) основан на измерении нейтрализующей активности и аффинности очищенных антител с помощью устройства типа BIACORE 2000 (см. пример 2, ниже).
Пример 2: AIN457 связывается с очень высокой аффинностью с рекомбинантным человеческим IL-17 (huIL-17): значение KD составляет 122±22 пМ (по данным измерений с помощью метода BIAcore), и нейтрализует индуцированное huIL-17 производство человеческого IL-6 в человеческих кожных фибробластах: значение IC50 составляет 2,1±0,1 нМ при концентрации huIL-17 1.87 нМ.
а) Методы
Реагенты: Основные лабораторные реагенты получают от фирмы Merck или Sigma и они имеют максимальную доступную степень чистоты; источники специальных реагентов подробно перечислены ниже.
Белки: Моноклональные антитела получают путем иммунизации трансгенных мышей линии MEDAREX рекомбинантным человеческим IL-17, и затем следуя стандартной процедуре получения клеточных линий, из которых секретируемый продукт можно очищать с помощью хроматографии на протеин А-сефарозе (в основном согласно методу, описанному в примере 1). AIN457 хранят в виде стерилизованного фильтрацией раствора в 50 мМ Na-цитратном буфере, рН 7,0, 140 мМ NaCl, при 4°С. Рекомбинантное человеческое AIN457 (партия КВ03303А) получают в стерильном маточном растворе либо 20 мМ Na-цитратном/40 мМ фосфатном буфере, рН 7, 150 мМ NaCl, либо 20 мМ уксусной кислоте, значение рН доводят до 5,5 с помощью 1М Трис-основания. Концентрации, как правило, составляют примерно 2 мг/мл и раствор разводят до конечной концентрации 5 мкг/мл с помощью BIA-буфера (20 мМ HEPES, рН 7,4, 150 мМ NaCl, 0,05% об./об. Твин-20) для экспериментов методом BIAcore.
Рекомбинантный человеческий IL-17 получают в собственной лаборатории условиях; партия En/Е 3882/83; 0,29 мг/мл.
Измерения методом BIAcore
Определение кинетических параметров связывания и уровней перекрестной реактивности производят путем измерений поверхностного плазменного резонанаса с использованием оптического биосенсора BIAcore 2000 (фирма BIAcore АВ, Упсалла, Швеция, более подробно см. Lit. HS 1, 2). Эта технология позволяет без использования метки определять с помощью микроскопического исследования константы скорости связывания (kon) и диссоциации (koff) лиганда с рецептором. Поэтому она особенно подходит для характеризации взаимодействий антитело-антиген. Эта технология дополняет и во многих отношениях превосходит метод измерений с помощью ELISA (Van Regenmortel, Dev Biol (Basel), 112, 2003, сс.141-151). Исследования связывания рекомбинантного IL-17 с антителом к IL-17 AIN457 осуществляют двумя путями. Согласно стандартному протоколу осуществляют захват AIN457 антителом к человеческому Fcγ (фирма Jackson Immunochemicals; каталожный номер 109-005-098), которое предварительно иммобилизуют на сенсорном чипе CM-5 BIAcore (степень чистоты для лабораторных исследований). Ковалентное связывание иммобилизованного антитела Fcγ осуществляют с помощью «набора для аминного сочетания», поставляемого фирмой BIAcore (фирма BIAcore, каталожный номер BR-1000-50). Как правило, 3000 крысиных единиц (КЕ) иммобилизованного антитела присоединяют к активированной декстраном поверхности с помощью 30 мкг/мл раствора антитела к Fcγ в 10 мМ ацетатном буфере, рН 4,5 при скорости потока 5 мкл/мин, что приводит к иммобилизации примерно 250 КЕ AIN457. В качестве справки следует отметить, что 1000 КЕ соответствуют переносу массы, составляющему 1 нг/мм2. В альтернативном варианте IL-17 (раздел 3.2; таблица 4), антитело AIN457 связывают непосредственно с поверхностью чипа без использования иммобилизованного антитела. Результаты сравнивают с протоколом, описанным в таблица 9 (см. ниже).
б) Результаты
Кинетические характеристики связывания комплекса IL-17/ AIN457
Константа равновесия диссоциации KD позволяет сделать некоторые заключения относительно стабильности комплексов, если они образуются in vivo. Поэтому при создании изобретения определяли кинетические константы связывания человеческого IL-17 с иммобилизованным антителом AIN457, и на их основе получали значение KD для такого процесса. В таблице 3 представлено обобщение полученных данных, где зависимости, полученные по двум экспериментам, аппроксимируют на основе модели Лэнгмюра с использованием программы BIAevaluation 3.0. Хотя очевидно, что антитело является бивалентным, связывание можно рассматривать как событие 1:1, где индивидуальные связывающие центры антитела, презентируемые на поверхности, оккупируются мономерными молекулами IL-17.
Этот эксперимент демонстрирует как очень быструю кинетику ассоциации, так и очень медленную кинетику диссоциации комплекса антитело-хемокин. Наилучшее соответствие данных получают, когда сенсограммы обрабатывают индивидуально (а не все в целом, как это предусматривается в программе BIAevaluation). Так, после объединения серий титрования были получены следующие значения по 12 сенсограммам: kon=(4,1±0,1)×105 1/Мс; koff=(3,8±0,5)×10-4 1/s; и KD=122±22 пМ.
Среднее значение KD рассчитано путем осреднения индивидуальных данных (по вертикали), а не с использованием уравнения KD=koff/kon.
Для AIN457, продуцируемого в рекомбинантных клетках (КВ03303А), измерения аффинности проводят с использованием цитокинов IL-17 из организма человека, игрунки, макаки резус и обезъян-крабоедов (cynomolgous) соответственно. Условия эксперимента при измерениях по методу Biacore являются такими же, что и условия, описанные выше для антитела МАВ110-28. Каждый эксперимент проводят в двух независимых повторностях, исследуя в каждом опыте по 6 концентраций IL-17. Концентрации человеческого IL-17 составляют 2, 4, 8, 12, 16, 20 нМ, а концентрации IL-17 для всех других видов животных 10, 20, 30, 40, 50, 60 нМ. Полный анализ данных позволяет получать по 12 (n=12) индивидуальных результатов измерений для каждого вида IL-17. Получают значения KD, а также С.К.О.
Полный набор результатов BIAcore-анализа для антитела КВ03303А представлен в таблицах 5-8, где приведены значения kon, koff и KD и указаны соответствующие виды IL-17.
После этого оценивают ингибирующую активность очищенного AIN457 (партия En/Е-1033 3/53; 0,54 мг/мл) в отношении huIL-17. Значения IC50 приведены в таблице 6. В этих экспериментах в качестве позитивного контроля используют huIL-17R/Fc и мышиной МАт к huIL-17, а в качестве негативного контроля используют Simulect.

Можно сделать вывод о том, что AIN457 прекращает зависящую от IL-17 секрецию huIL-6 человеческими кожными фибробластами. Его эффективность сравнима с эффективностью huIL-17R/Fc и превышает эффективность поступающего в продажу мышиного МАт к huIL-17. Интересно отметить, что использование AIN457 приводит к более сильному ингибированию, чем использование IL-17R/Fc.
Пример 3: Чистота и частичные аминокислотные последовательности тяжелой и легкой цепи
Секвенирование аминокислотных последовательностей
N-концевые аминокислотные последовательности VL- и VH-областей:
Первые 48 аминокислотных остатков тяжелой и легкой цепей двух антител к IL-17А, а именно клона 110-7 (см. таблицу 4) и 110-28 (см. таблицу 4), определяют с помощью расщепления по Эдману. Аминокислотные последовательности идентичны для обоих клонов. Осуществляют поиск в GeneBank с помощью blast-анализа и выявленную обладающую наибольшей гомологией последовательность ДНК используют для конструирования праймеров для клонирования.
Молекулярное клонирование VL- и VH-областей: Общую РНК элюируют из 2×107 клеток гибридомы (клон 110-7, клон 110-28) с использованием набора RNeasy Midi Kit согласно протоколу фирмы-поставщика (фирма Quiagen, Гилден, Германия). Общую РНК разводят в 200 мкл не содержащей РНазы воды и хранят при -80°С. Синтез первой цепи кДНК осуществляют с использованием обратной транскриптазы M-MLV (фирма Promega, Мэдисон, шт. Висконсин), олиго-дТ-праймера, смеси нуклеотидов (дНТФ) для ПЦР и ингибитора RNAsin (фирма Roche, Маннгейм). Пять мкг общей РНК смешивают с 1 мкл олиго-дТ-праймера (0,5 мкг/мкл) и добавляют не содержащую РНКазу воду до конечного объема 36 мкл. Смесь инкубируют при 70°С в течение 10 мин и затем хранят на льду. К находящейся на льду смеси добавляют следующие реагенты: 10 мкл 5-кратного RT-буфера, 2 мкл дНТФ (концентрация каждого 10 мМ), 2 мкл RNAsin и 1 мкл обратной транскриптазы M-MLV. Реакцию проводят при 42°С в течение 1 ч.
ПЦР-реакцию осуществляют с использованием 4 мкл кДНК-матрицы, 2 мкл каждого праймера с концентрацией каждого 10 мкМ (см. ниже и обобщение, приведенное в таблицах 10 и 11), 20 мкл 2×Qiamix (содержащей буфер, дНТФ, полимеразу TAQ) и 1 мкл ДНК-полимеразы Pwo в общем объеме 40 мкл. Условия ПЦР: 35 циклов: 94°С в течение 15 с, 55°С в течение 20 с и 72°С в течение 30 с. ПЦР-продукт субклонируют в клонирующем векторе pCR4-TOPO-Zero (фирма Stragagene, Ла Джолла, шт. Калифорния). Из каждой реакционной смеси отбирают несколько клонов и определяют нуклеотидную последовательность с помощью Solvias AG (Базель) с использованием праймеров MV432 (SEQ ID NO:21), MV433 (SEQ ID NO:22), MV434 (SEQ ID NO:23), MV435 (SEQ ID NO:14) и стандартных праймеров в векторной ДНК.
кДНК, кодирующую тяжелую цепь, амплифицируют с использованием пары праймеров MV416 (SEQ ID NO:15)/№265 (SEQ ID NO:16) и MV418 (SEQ ID NO:17)/№265 (SEQ ID NO:16). Праймеры включают нуклеотидные последовательности, соответствующие следующим положениям аминокислот тяжелой цепи: MV416 положение -19/-13 (сигнальный пептид); MV418 положение +1/+7; №265 положение +253/+259. Положение +1 соответствует первой аминокислоте зрелого белка.
кДНК, кодирующую легкую цепь, амплифицируют с использованием пары праймеров MV417 (SEQ ID NO:18)/№223 (SEQ ID NO:19) и MV419 (SEQ ID NO:20)/№223 (SEQ ID NO:19). Праймеры включают нуклеотидные последовательности, соответствующие следующим положениям аминокислот легкой цепи: MV417 положение -20/-14 (сигнальный пептид); MV419 положение +1/+7; №223 положение +210/+215. Этот подход позволяет осуществлять две независимые ПЦР-амплификации для каждой цепи иммуноглобулина, получая две независимо созданные последовательности ДНК.
Результаты и обсуждение
Клонированные ПЦР-продукты, кодирующие тяжелую и легкую цепи из двух гибридом (110-7 и 110-28, см. таблица 4, выше) характеризуют путем секвенирования ДНК. Пять и шесть независимых последовательностей используют для сборки последовательностей легкой и тяжелой цепей. Все кДНК легкой цепи являются идентичными и включают полную кодирующую последовательность (положения аминокислот -20 - +215). кДНК тяжелой цепи имеют 2 различных ошибочных спаривания по одному в каждой кДНК. Их исключают из конечной последовательности, которая простирается от стартового кодона до конца шарнирной области, расположенной после константной области 1 (положения аминокислот -19 - +238).
Последовательности для обеих гибридом являются идентичными. Отбирают кДНК, полученную из гибридомы 110-28, и используют для всех дальнейших работ по оценке экспрессии. В SEQ ID NO:7 (кДНК тяжелой цепи AIN457), SEQ ID NO:8 (аминокислотная последовательность тяжелой цепи AIN457), SEQ ID NO:9 (кДНК легкой цепи AIN457) и SEQ ID NO:10 (аминокислотная последовательность AIN457) представлены последовательность ДНК, кодирующая легкую и тяжелую цепь AIN457, а также последовательность белка и положение праймеров, используемых для ПЦР-амплификации и секвенирования ДНК. Последовательности ДНК зарегистрированы в PlasNova, регистрационный номер тяжелой цепи NPL003689, а регистрационный номер легкой цепи NPL003690.
Аминокислотная последовательность, полученная путем клонирования кДНК, идентична последовательности, полученной ранее путем расщепления по Эдману очищенных тяжелой и легкой цепей иммуноглобулина, что свидетельствует о том, что клонирована правильная кДНК.
Таблица 10: Нуклеотидная и аминокислотная последовательность легкой цепи
Аминокислотная последовательность, кодирующая вариабельную область, выделена жирным шрифтом и подчеркнута. Указаны олигонуклеотидные праймеры, используемые для клонирования (подчеркнуты).


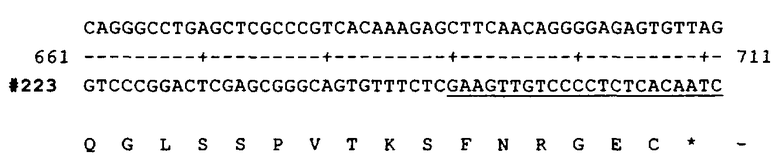
Таблица 11: Нуклеотидная и аминокислотная последовательность тяжелой цепи
Аминокислотная последовательность, кодирующая вариабельную область, выделена жирным шрифтом и подчеркнута. Указаны олигонуклеотидные праймеры, используемые для клонирования и секвенирования.
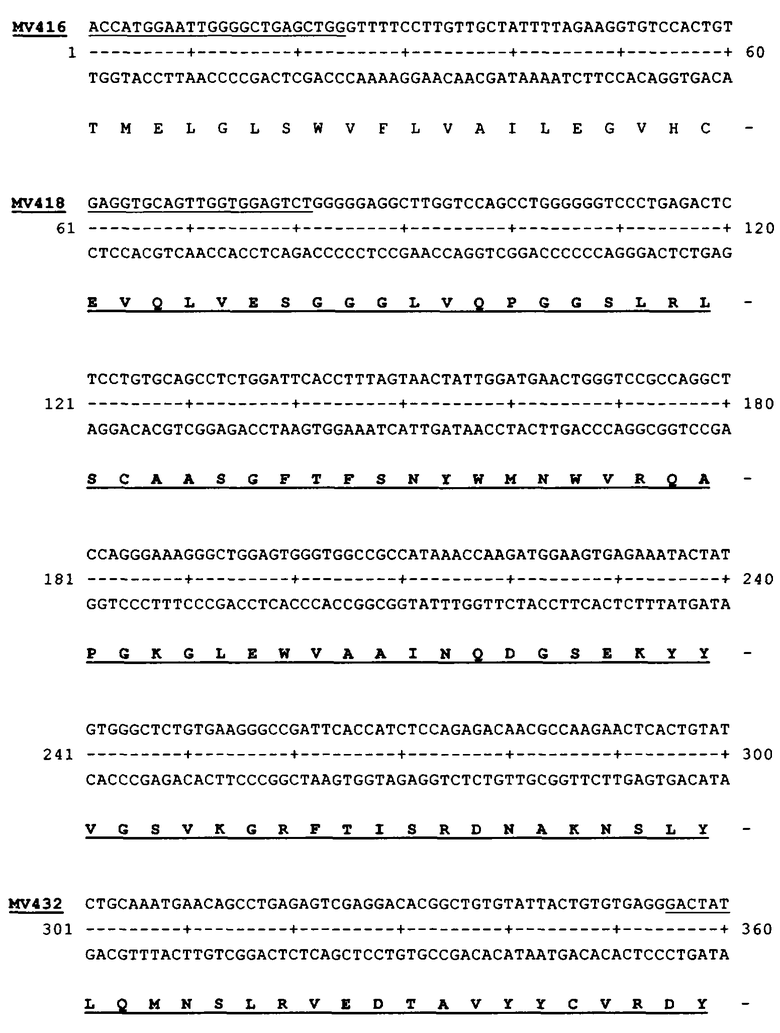

Пример 4: Трехмерная структура Fab-фрагмента моноклонального антитела AIN457 к человеческому IL-17A
Для определения конформации гипервариабельных участков (CDR) и структуры антигенсвязывающего центра AIN457 конструируют Fab-фрагмент, кристаллизуют и определяют его структуру с помощью кристаллографического рентгеноструктурного анализа белка.
Метод: Fab-фрагмент NVP-AIN457 получают путем расщепления папаином полного антитела и очищают с помощью хроматографии на протеине А и последующей гель-фильтрации. Затем очищенный продукт концентрируют с помощью ультрафильтрации до 20 мг/мл в 10 мМ Трис-HCl, рН 7,4, 25 мМ NaCl, 5 мМ ТСЕР. Кристаллы выращивают с помощью метода паровой диффузии в висящих каплях при 19°С из 2,0 М сульфата аммония, 5% ПЭГ 400, 0,1 М Na MES, рН 6,5. Они относятся к пространственной группе P212121 с размерами элементарной ячейки а=90,3 Å, b=106,7 Å, с=131,4 Å, которая содержит 2 Fab-молекулы на один асимметричный элемент. Перед сбором данных рентгеноструктурного анализа индивидуальный кристалл Fab-фрагмента AIN457 сшивают с глутаровым альдегидом методом, описанным у Lusty, J. Appl. Cryst., 32, 1999, сс.106-112, и затем переносят в раствор, содержащий 2,0 М Li2SO4, 2% ПЭГ 400 и 0,1 М Na MES, рН 6,5. После этого кристалл закрепляют в криопетле и быстро замораживают для сбора данных при 95 К. Регистрируют 180 дифракционных изображений, каждое из которых соответствует колебанию 1,0°. Результаты дифракционных измерений обрабатывают с помощью пакета программ HKL. Структуру определяют при разрешении 2,5 Å путем молекулярного замещения. Затем структуру уточняют путем учета динамики углового закручивания и минимизации энергии с использованием программы CNX.
Результаты: В асимметричном элементе кристалла присутствуют две Fab-молекулы AIN457, причем H-CDR3-петля обеих Fab-молекул участвует в контактах белок-белок с Н-SDR3-петлей Fab-молекул, имеющих строение, близкое к симметричному. Две Fab-молекулы имеют разные углы изгиба, но в остальном имеют практически идентичные конформации CDR-петли (см. таблицу 12, в которой представлена аминокислотная последовательность CDR-петель). H-CDR1-петля имеет ожидаемую каноническую структуру Н1:1, в то время как конформация Н-СОК2-петли соответствует канонической структуре Н2:3А. Н-CDR3-петля антитела AIN457 является необычно длинной и содержит 18 остатков между положениями (по Кэботу) 94 (Arg H98) и 101 (Asp H115). Она имеет типичную структуру с выпуклым телом, стабилизированную с помощью солевого мостика между боковой цепью Arg в положении 94 (Arg H98) и карбоксилатной группой Asp в положении H101 (Asp H115), и взаимодействия посредством водородной связи между боковой цепью Trp в положении H117 и карбонильной группой Phe основной цепи в положении H114. Голова H-CDR3-цепи имеет структуру длинной скрученной бета-«шпильки», характеризующейся наличием второй бета-выпуклости у ее основания и бета-поворотом типа I' у ее вершины. Отличительной особенностью Н-CDR3-петли AIN457 является очень высокое содержание в ней ароматических остатков: 6 остатков тирозина, 2 остатка триптофана, 1 остаток фенилаланина. Поскольку все другие CDR-петли содержат еще по одному остатку тирозина каждая, то в целом антигенсвязывающий центр AIN457 содержит 11 остатков тирозина. Конформации L-CDR1- и L-CDR2-петель соответствуют каноническим структурам L1:6 и L2:1 соответственно. В отличие от H-CDR-3-петли L-CDR3-петля является короткой (6 остатков) и имеет обычную каноническую структуру L3:1, содержащую цис-пролин на ее конце (Pro L96), глутамин в положении 90 (по Кэботу) (Gin L91) и треонин в положении 97 (по Кэботу) (Thr L98). Однако совершенно необычной особенностью L-CDR3-петли AIN457 является наличие остатка цистеина после цис-пролина (Cys L97). Боковая цепь Cys L97 находится на дне небольшого углубления, расположенного на границе раздела VL-VH и выстланного остатками Trp H112, Trp Н47 и Tyr L92.
Таблица 12: Аминокислотные последовательности гипервариабельных участков моноклональных антител AIN457 на основе определения по Кэботу и с помощью рентгеноструктурного анализа с использованием подхода Chothia с соавторами. Аминокислоты, выделенные жирным шрифтом, являются частью CDR-петель, в то время как аминокислоты, обозначенные простым шрифтом, являются частью каркасного участка антитела.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА - АНТАГОНИСТЫ ИНТЕРЛЕЙКИНА-17 (ИЛ-17) ДЛЯ ЛЕЧЕНИЯ РАКА | 2007 |
|
RU2430110C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ПСОРИАЗА С ИСПОЛЬЗОВАНИЕМ АНТАГОНИСТОВ IL-17 | 2011 |
|
RU2591083C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ПСОРИАЗА С ИСПОЛЬЗОВАНИЕМ АНТАГОНИСТОВ IL-17 | 2011 |
|
RU2665954C1 |
| СПОСОБЫ ЛЕЧЕНИЯ РЕВМАТОИДНОГО АРТРИТА С ПРИМЕНЕНИЕМ АНТАГОНИСТОВ IL-17 | 2011 |
|
RU2582937C2 |
| АНТИТЕЛА К ЧЕЛОВЕЧЕСКОМУ IL-1БЕТА | 2001 |
|
RU2286351C2 |
| РЕКОМБИНАНТНОЕ АНТИТЕЛО К ЧЕЛОВЕЧЕСКОМУ ИНТЕРЛЕЙКИНУ 1β | 2001 |
|
RU2264413C2 |
| ТЕРАПЕВТИЧЕСКИЕ СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2002 |
|
RU2328506C2 |
| АНТИ-IL-17F АНТИТЕЛА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2010 |
|
RU2605318C2 |
| АНТИТЕЛА К ЧЕЛОВЕЧЕСКОМУ МСР-1 | 2001 |
|
RU2314316C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИСПЕЦИФИЧЕСКИХ АНТИТЕЛ, БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА И ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ ТАКИХ АНТИТЕЛ | 2018 |
|
RU2795240C2 |












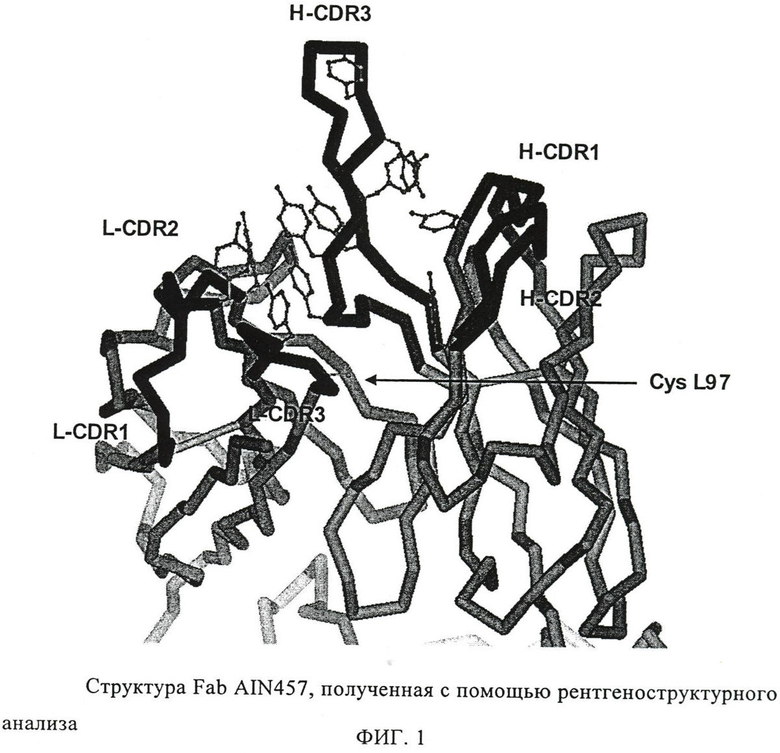
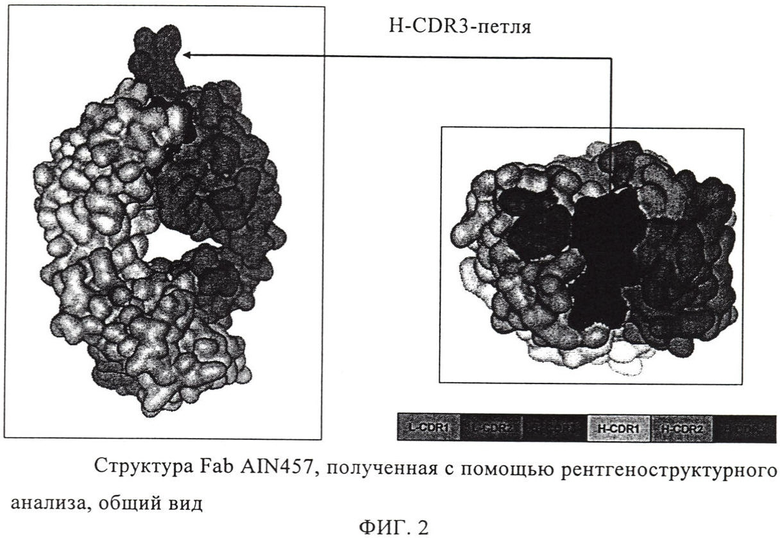
Изобретение относится к биотехнологии и представляет собой IL-17-связывающее антитело или его активный фрагмент. Также представлены конструкция ДНК, кодирующая антитело, способ получения антитела, применение антитела, фармацевтическая композиция, вектор экспрессии. Изобретение может эффективно использоваться для получения лекарственного средства для лечения опосредуемого IL-17 заболевания или нарушения. 13 н. и 1 з.п. ф-лы, 2 ил., 15 табл.
1. IL-17-связывающее антитело или его активный фрагмент, содержащий вариабельные области как тяжелой цепи (VH), так и легкой цепи (VL) иммуноглобулина, где IL-17-связывающее антитело или его активный фрагмент содержит по меньшей мере один антигенсвязывающий центр, включающий:
а) вариабельную область тяжелой цепи (VH) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1, CDR2 и CDR3, где CDR1 имеет аминокислотную последовательность SEQ ID NO:1, CDR2 имеет аминокислотную последовательность SEQ ID NO:2 и CDR3 имеет аминокислотную последовательность SEQ ID NO:3, и
б) вариабельную область легкой цепи (VL) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1', CDR2' и CDR3', где CDR1' имеет аминокислотную последовательность SEQ ID NO:4, CDR2' имеет аминокислотную последовательность SEQ ID NO:5 и CDR3' имеет аминокислотную последовательность SEQ ID NO:6,
причем CDR последовательность соответствует обозначению Kabat.
2. IL-17-связывающее антитело или его активный фрагмент, содержащий вариабельные области как тяжелой цепи (VH), так и легкой цепи (VL) иммуноглобулина, где IL-17-связывающее антитело или его активный фрагмент содержит по меньшей мере один антигенсвязывающий центр, включающий:
а) вариабельную область тяжелой цепи (VH) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1-x, CDR2-x и CDR3-x, где CDR1-x имеет аминокислотную последовательность SEQ ID NO:11, CDR2-x имеет аминокислотную последовательность SEQ ID NO:12 и CDR3-x имеет аминокислотную последовательность SEQ ID NO:13, и
б) вариабельную область легкой цепи (VL) иммуноглобулина, которая содержит последовательно расположенные гипервариабельные участки CDR1', CDR2' и CDR3', где CDR1' имеет аминокислотную последовательность SEQ ID NO:4, CDR2' имеет аминокислотную последовательность SEQ ID NO:5 и CDR3' имеет аминокислотную последовательность SEQ ID NO:6,
причем CDR последовательность соответствует обозначению Chotia.
3. IL-17-связывающее антитело или его активный фрагмент по п.1 или 2, представляющее собой человеческое антитело.
4. IL-17-связывающее антитело или его активный фрагмент, которое содержит по меньшей мере один антигенсвязывающий центр, включающий первый домен, имеющий аминокислотную последовательность, представленную в SEQ ID NO:8, начиная с аминокислоты в положении 1 и заканчивая аминокислотой в положении 127, или представленную в SEQ ID NO:10, начиная с аминокислоты в положении 1 и заканчивая аминокислотой в положении 109.
5. Конструкция ДНК, кодирующая IL-17-связывающее антитело или его активный фрагмент по любому из пп.1-4.
6. Конструкция ДНК, содержащая молекулу ДНК, которая кодирует вариабельную область тяжелой цепи (VH) иммуноглобулина, имеющую аминокислотную последовательность, представленную в SEQ ID NO:8.
7. Конструкция ДНК, содержащая 2 молекулы ДНК, первую молекулу ДНК, которая кодирует вариабельную область тяжелой цепи (VH) иммуноглобулина, имеющую аминокислотную последовательность, представленную в SEQ ID NO:8, и вторую молекулу ДНК, которая кодирует вариабельную область легкой цепи (VL) иммуноглобулина, имеющую аминокислотную последовательность, представленную в SEQ ID NO:10.
8. Способ получения IL-17-связывающего антитела или его активного фрагмента, заключающийся в том, что
(I) культивируют организм, трансформированный
(а) экспрессионным вектором, способным реплицироваться в прокариотической или эукариотической клетке, включающим конструкцию ДНК по п.5,
(б) экспрессионным вектором, способным реплицироваться в прокариотической или эукариотической клетке, включающим первую молекулу ДНК, которая кодирует вариабельную область тяжелой цепи (VH) иммуноглобулина, имеющую аминокислотную последовательность, представленную в SEQ ID NO:8, и вторую молекулу ДНК, которая кодирует вариабельную область легкой цепи (VL) иммуноглобулина, имеющую аминокислотную последовательность, представленную в SEQ ID NO:10,
(в) экспрессионным вектором, способным реплицироваться в прокариотической или эукариотической клетке, включающим молекулу ДНК, которая кодирует вариабельную область тяжелой цепи (VH) иммуноглобулина, имеющую аминокислотную последовательность, представленную в SEQ ID NO:8, и экспрессионным вектором, способным реплицироваться в прокариотической или эукариотической клетке, включающим молекулу ДНК, которая кодирует вариабельную область легкой цепи (VL) иммуноглобулина, имеющую аминокислотную последовательность, представленную в SEQ ID NO:10;
(II) выделяют IL-17-связывающее антитело или его активный фрагмент из культуры.
9. Применение IL-17-связывающего антитела или его активного фрагмента по любому из пп.1-4 для получения лекарственного средства для лечения опосредуемого IL-17 заболевания или нарушения.
10. Применение IL-17-связывающего антитела или его активного фрагмента по любому из пп.1-4 для лечения псориаза, увеита, остеоартрита, ревматоидного артрита, остеопороза и других воспалительных поражений кожи ревматического или подагрического происхождения.
11. Фармацевтическая композиция, содержащая IL-17-связывающее антитело или его активный фрагмент по любому из пп.1-4 в сочетании с фармацевтически приемлемым эксципиентом, разбавителем или носителем, предназначенная для лечения опосредуемого IL-17 заболевания или нарушения.
12. Фармацевтическая композиция, содержащая IL-17-связывающее антитело или его активный фрагмент по любому из пп.1-4 в сочетании с фармацевтически приемлемым эксципиентом, разбавителем или носителем, предназначенная для лечения псориаза, увеита, остеоартрита, ревматоидного артрита, остеопороза и других воспалительных поражений кожи ревматического или подагрического происхождения.
13. Конструкция ДНК, включающая молекулу ДНК, которая кодирует вариабельную область легкой цепи (VL) иммуноглобулина, имеющую аминокислотную последовательность, представленную в SEQ ID NO:10.
14. Вектор экспрессии, способный реплицироваться в прокариотической или эукариотической клетке, включающий по меньшей мере одну конструкцию ДНК по любому из пп.5, 6, 7 или 13.
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| Chabaud M, et al | |||
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
| Cytokine | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| Lubberts E., et al | |||
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
| Curr | |||
| Opin | |||
| Investig | |||
| Drugs | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| РОЙТ А | |||
| и др | |||
| Иммунология | |||
| - M.: Мир, 2000, с.97-109. | |||
Авторы
Даты
2011-08-20—Публикация
2005-08-04—Подача