Текст описания приведен в факсимильном виде.






























































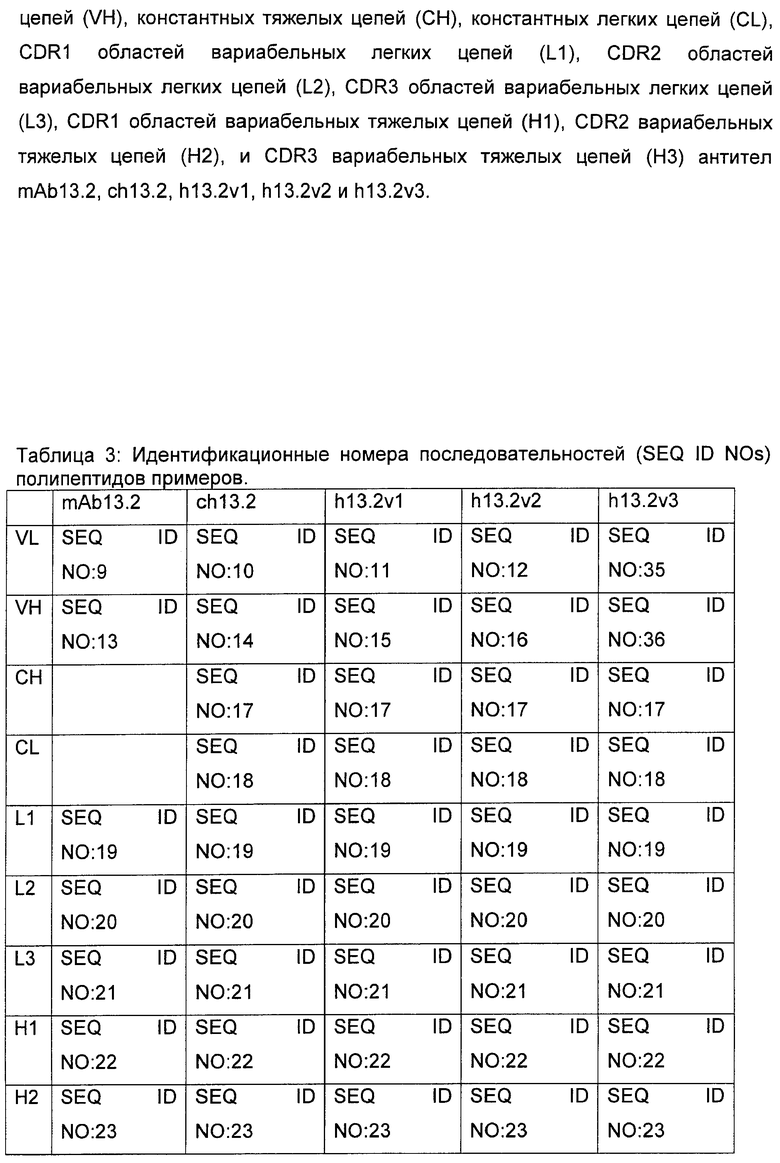














































































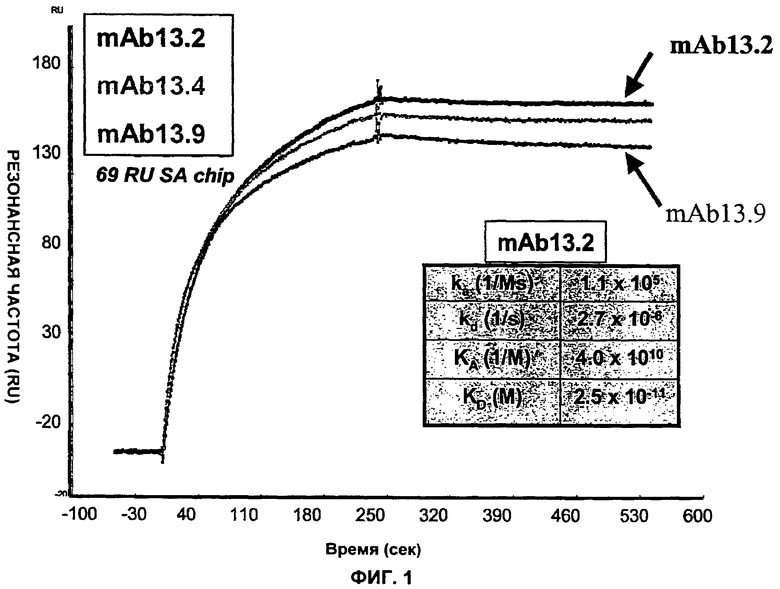
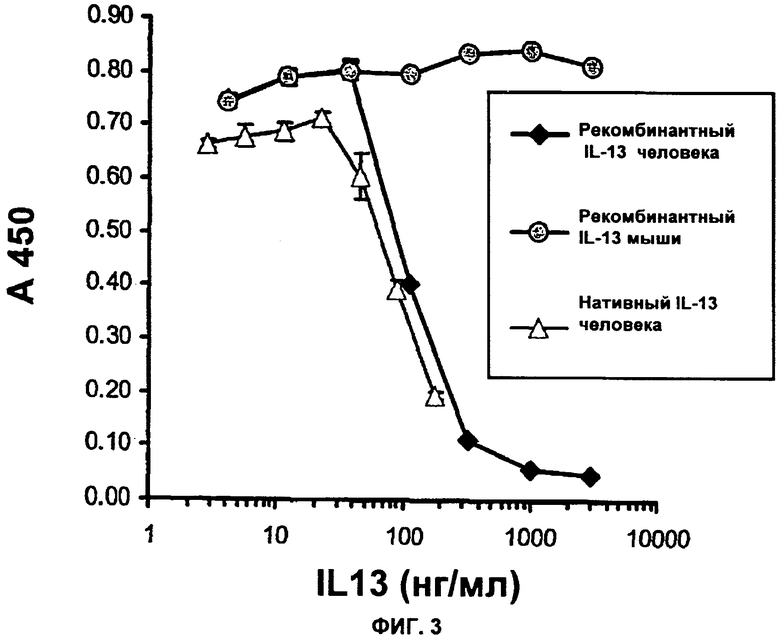
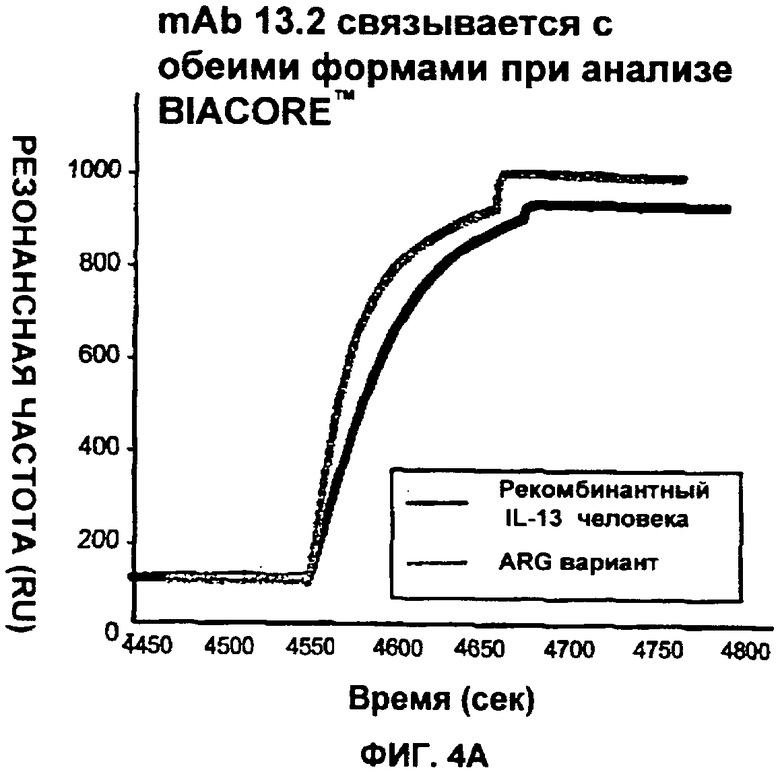
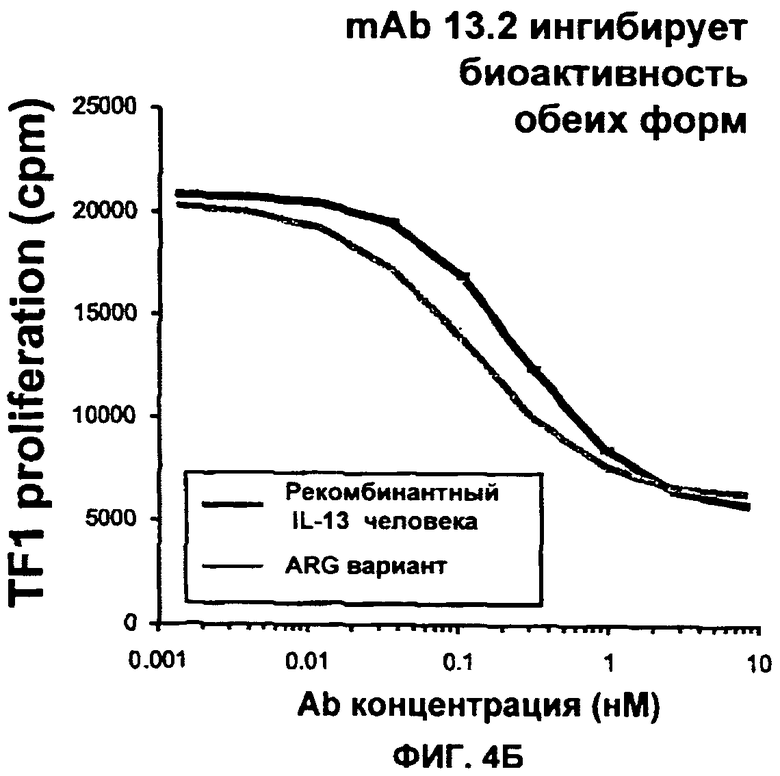
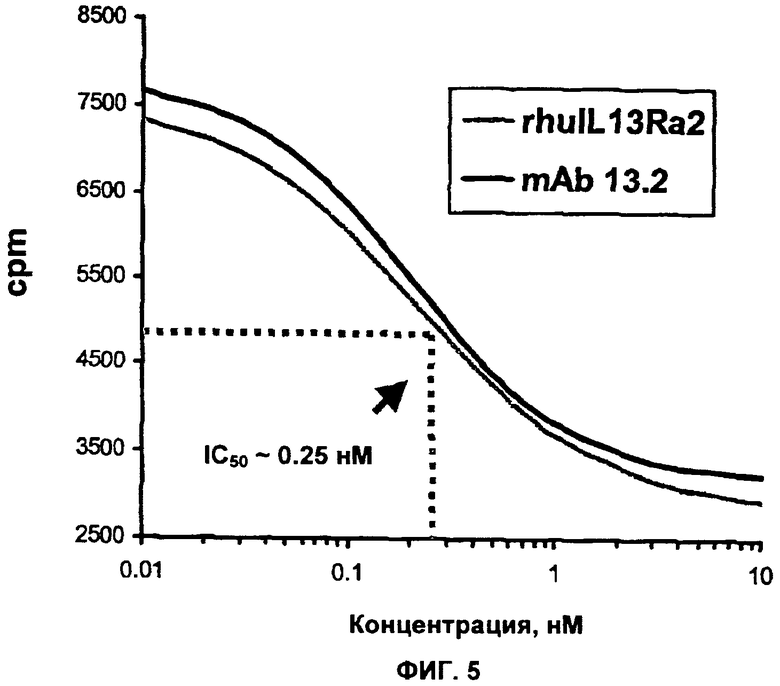
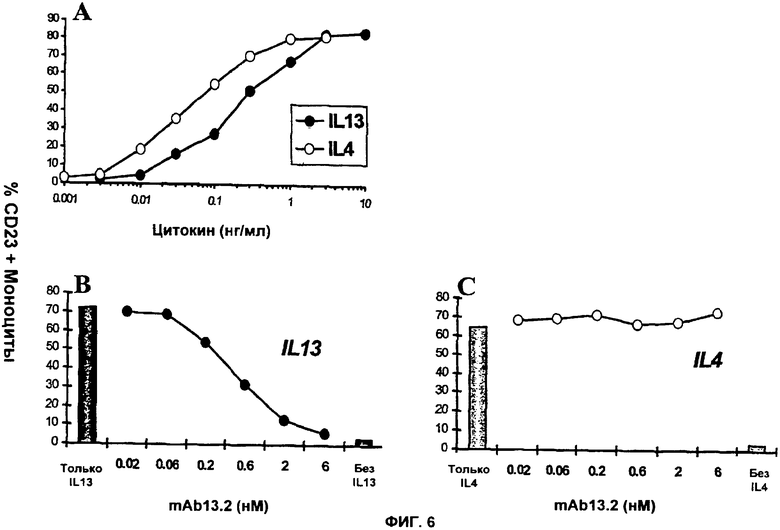
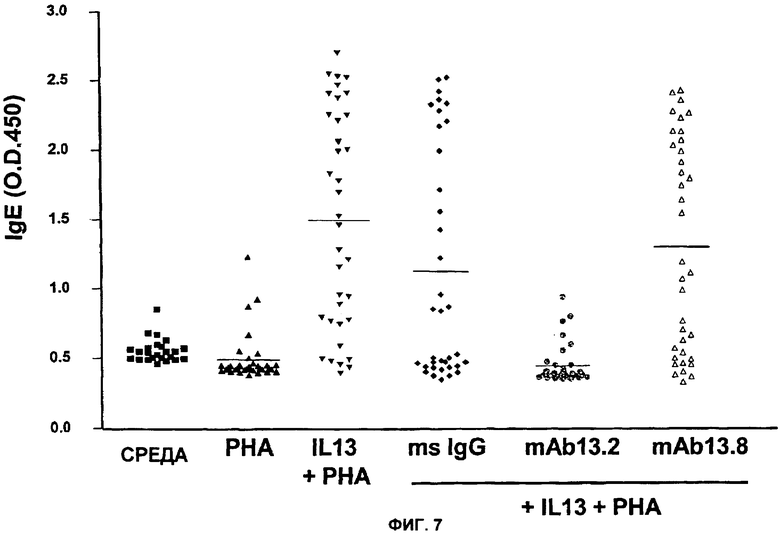
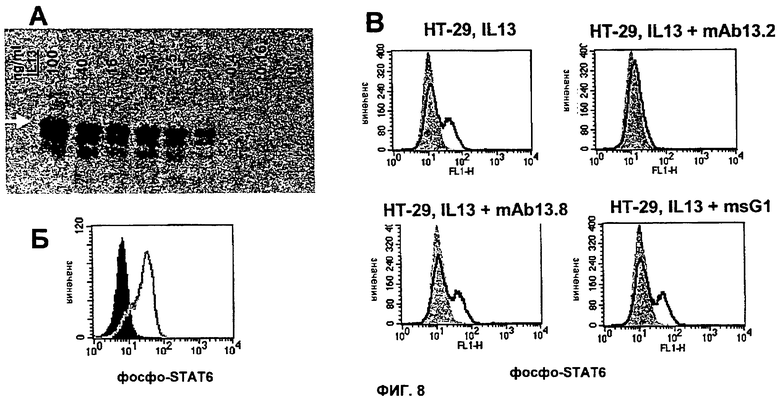

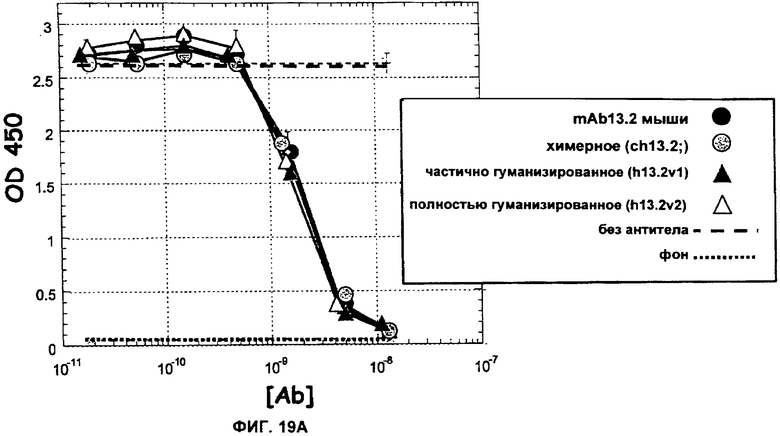
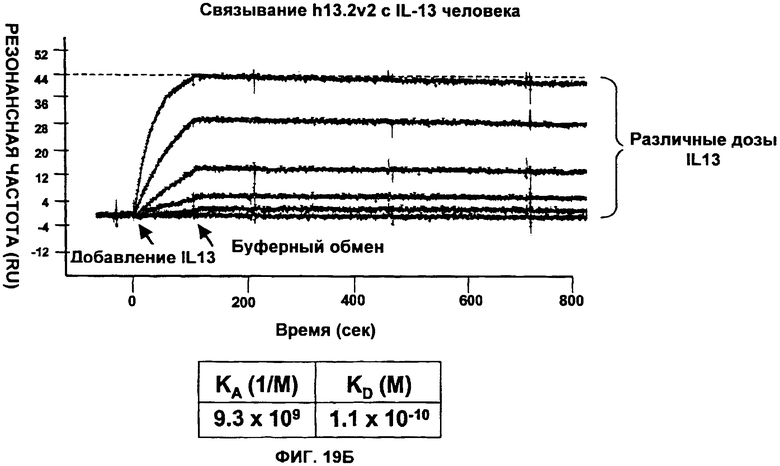
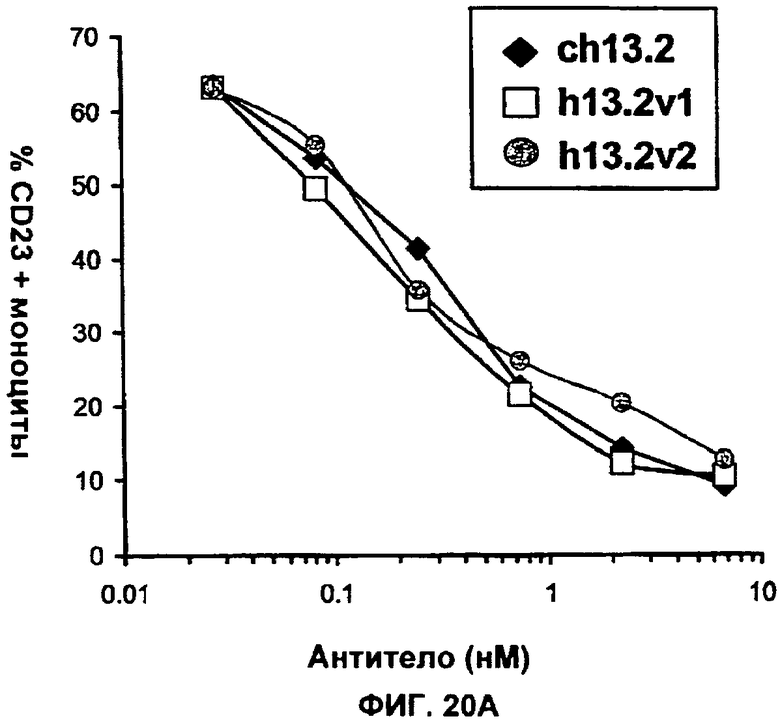
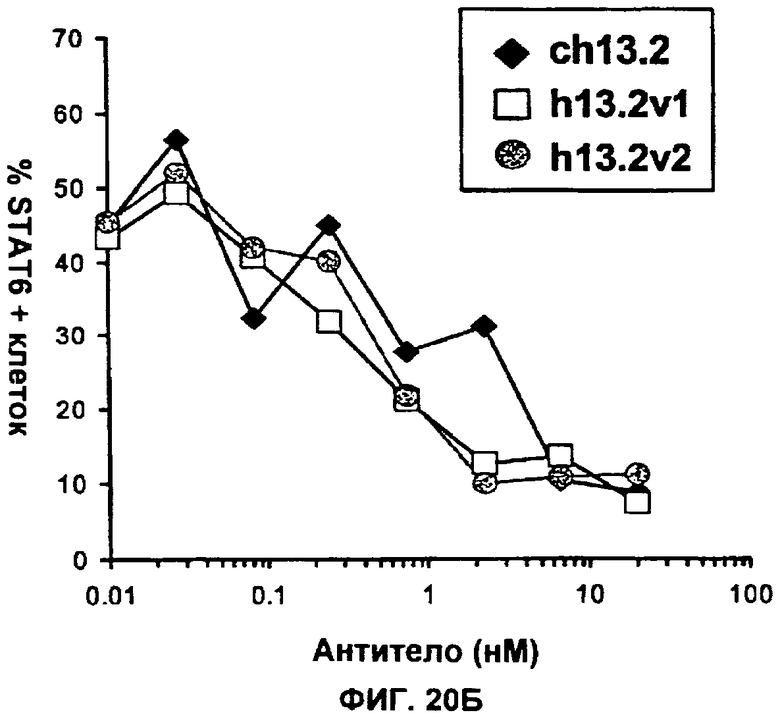
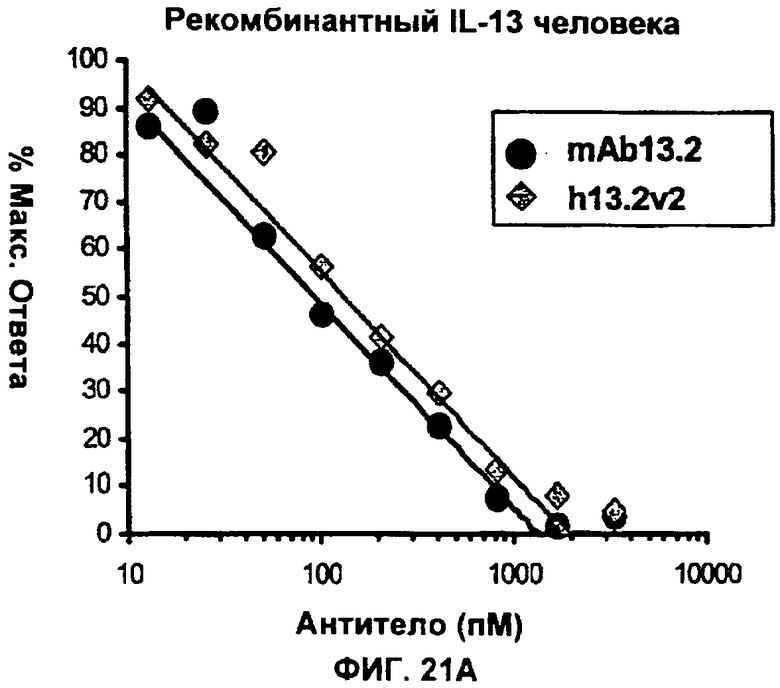
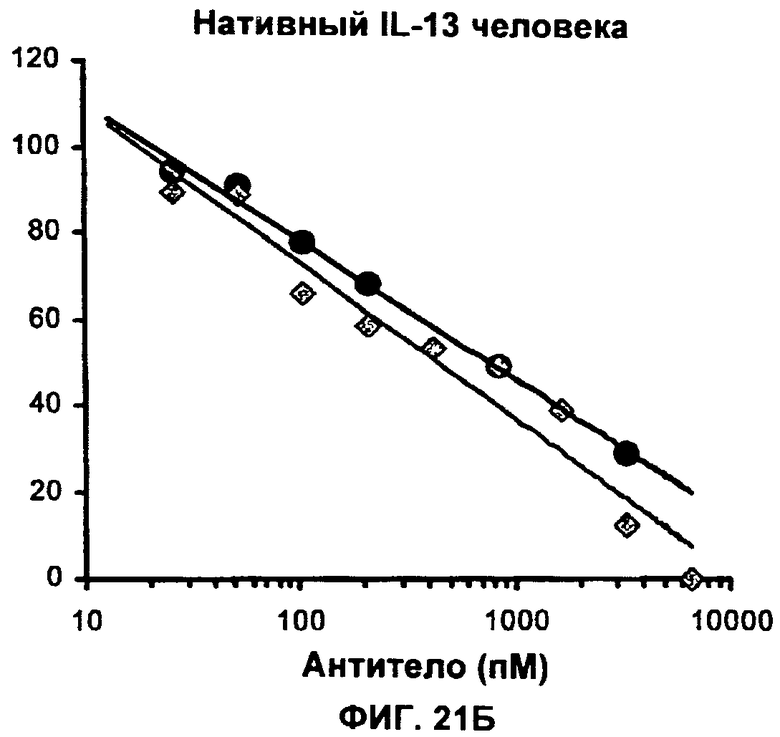
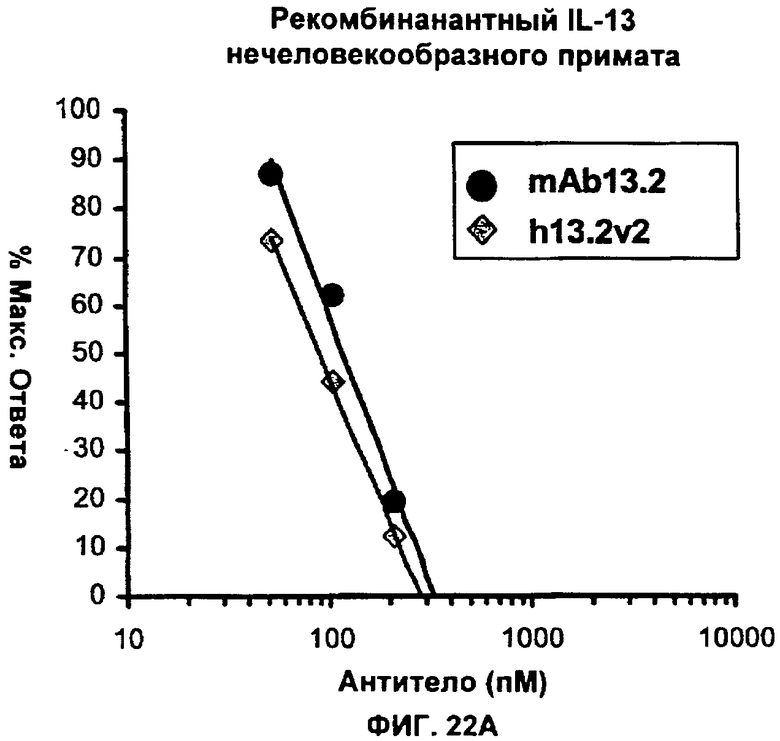
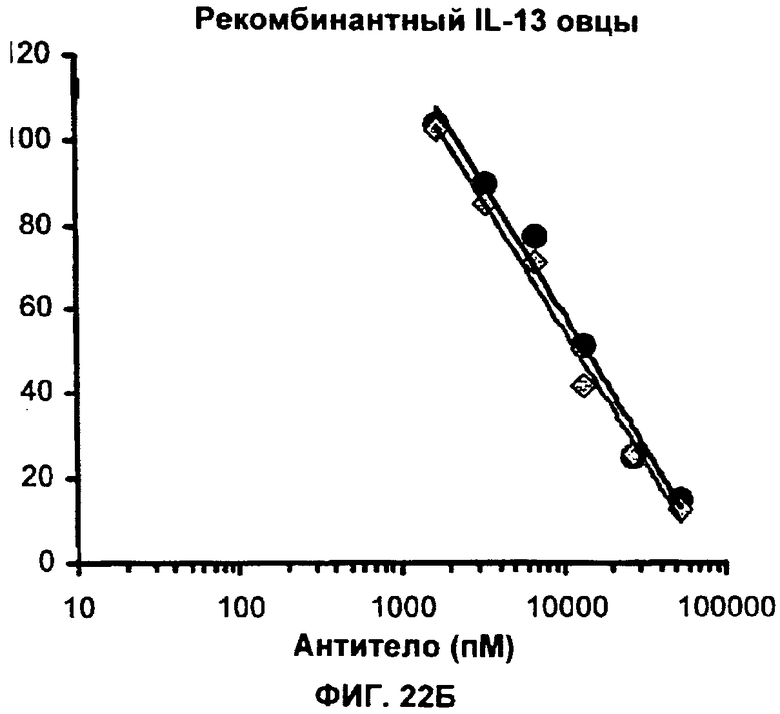
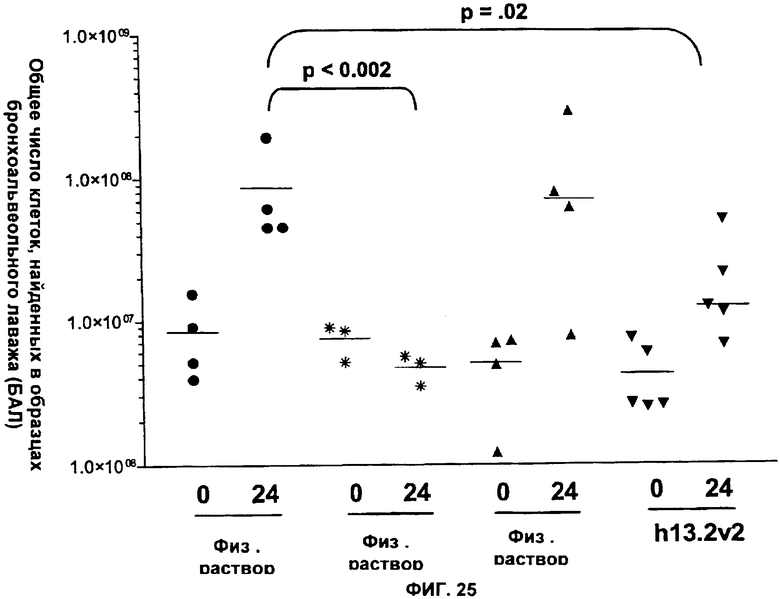

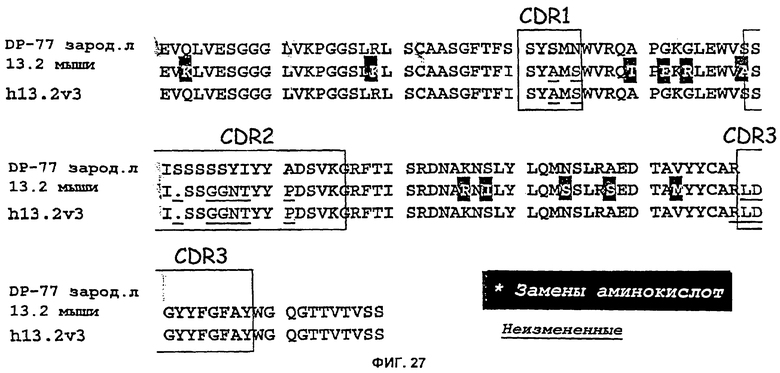
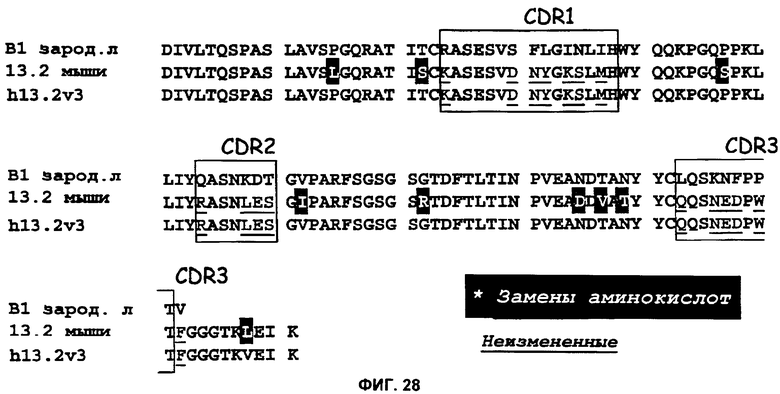
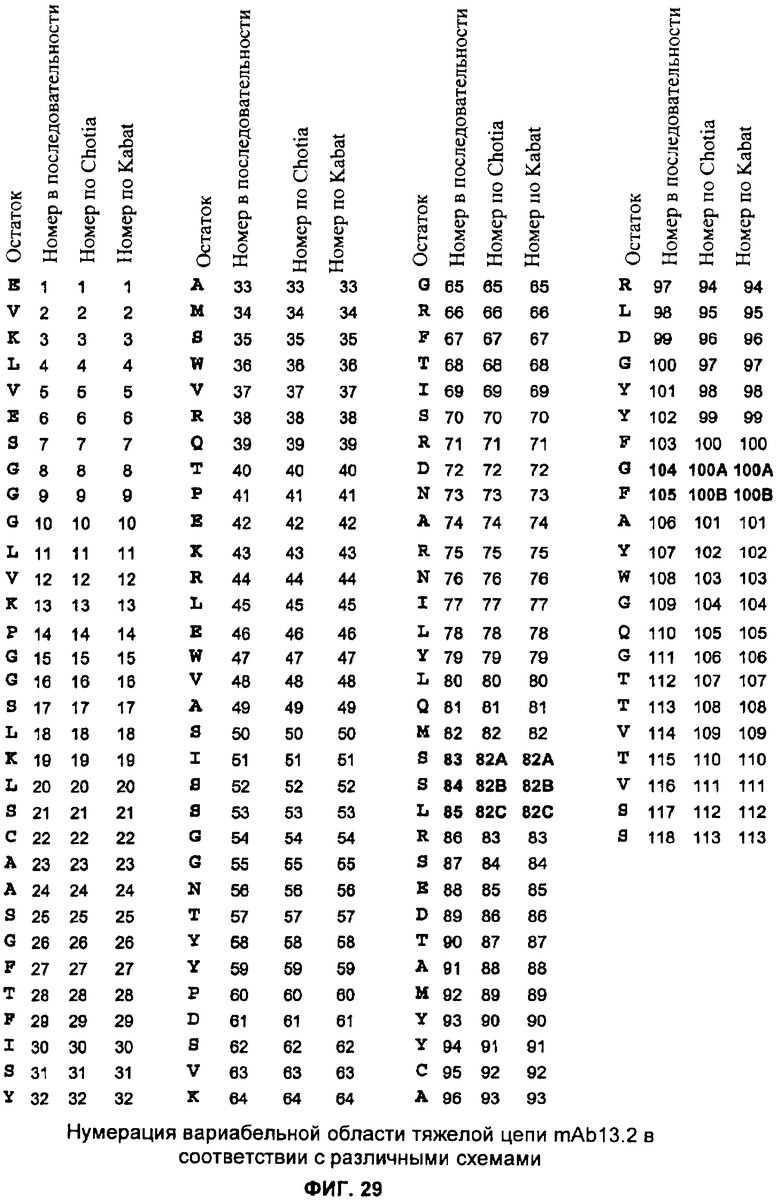
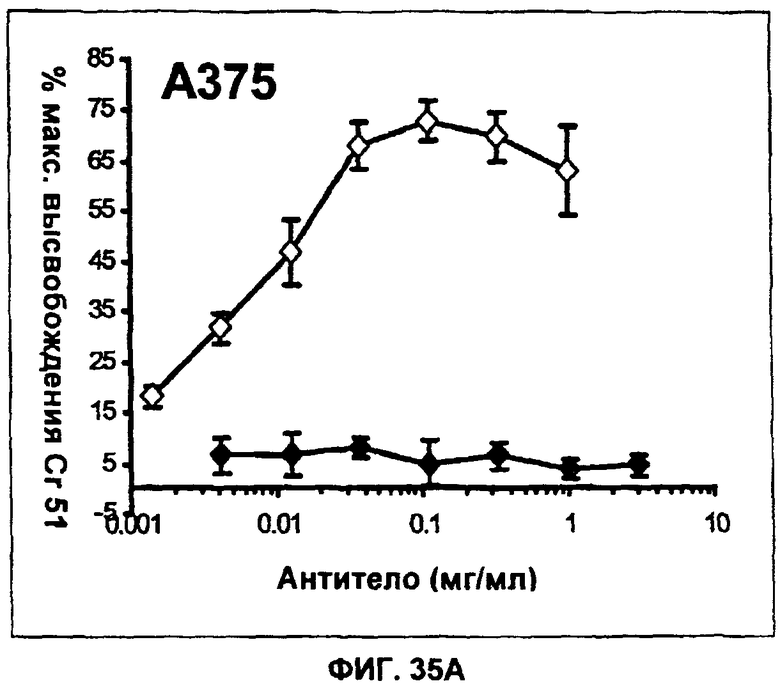
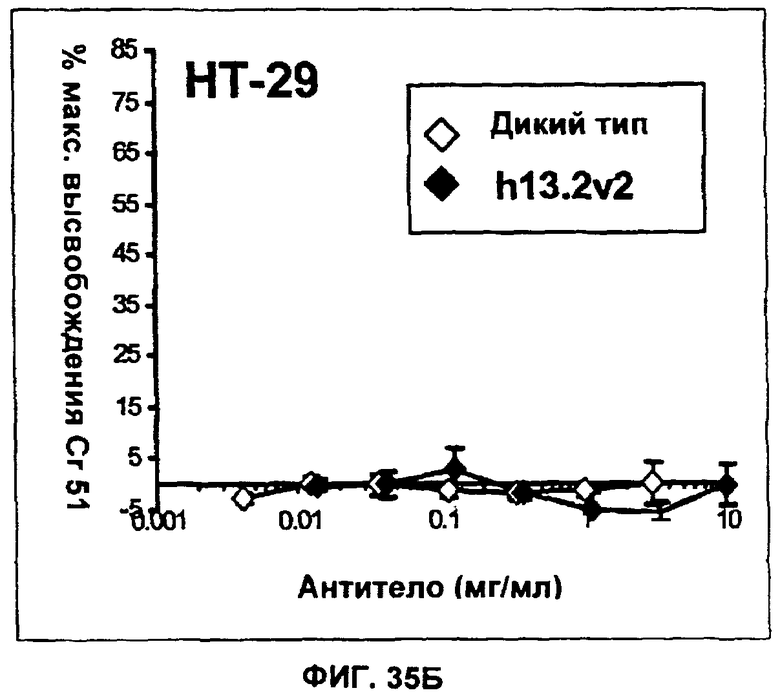
Изобретение относится к иммунологии и биотехнологии. Предложены варианты антител и их антиген-связывающие фрагменты, специфичные к IL-13, а также, в частности, к IL-13 человека. Описаны: фармацевтическая композиция, фармацевтический состав на основе антитела, варианты кодирующих и гибридизующихся нуклеиновых кислот и экспрессионных векторов. Предложены варианты: клеток и способов получения антитела, способов лечения расстройства, связанного с IL-13. Описан способ обнаружения IL-13 в образце. Использование изобретения обеспечивает новые антитела к IL-13 с KD порядка 10-10 М, которые можно использовать для диагностики, предотвращения и/или лечения у субъекта одного или более заболеваний, связанных с IL-13. 24 н. и 63 з.п. ф-лы, 37 ил., 5 табл.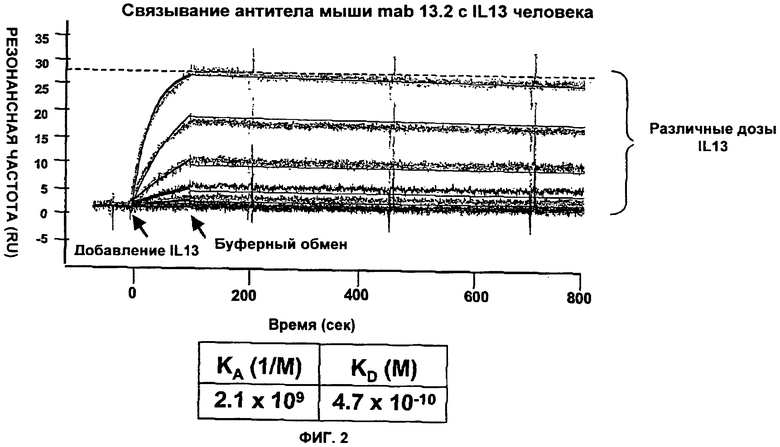
1. Антитело или его антигенсвязывающий фрагмент, которые содержат вариабельную область тяжелой цепи иммуноглобулина и вариабельную область легкой цепи иммуноглобулина, которые связывают IL-13 с KD менее чем 10-7 М, при этом указанная вариабельная область легкой цепи содержит последовательность аминокислот:
(i) KASESVDNYGKSLMH (SEQ ID NO: 19), в CDR1,
(ii) RASNLES (SEQ ID NO: 20), в CDR2, и
(iii) QQSNEDPWT (SEQ ID NO: 21), в CDR3;
а указанная вариабельная область тяжелой цепи содержит последовательность аминокислот:
(i) SYAMS (SEQ ID NO: 22), в CDR1,
(ii) SISSGGNTYYPDSVKG (SEQ ID NO: 23), в CDR2, и
(iii) LDGYYFGFAY (SEQ ID NO: 24), в CDR3,
или последовательность аминокислот, которая отличается менее чем на три консервативных замены аминокислот от последовательности аминокислот, выбранной из SEQ ID NO: 19-24.
2. Антитело или его антигенсвязывающий фрагмент, которые содержат вариабельную область тяжелой цепи иммуноглобулина и вариабельную область легкой цепи иммуноглобулина, которые связывают IL-13 с KD менее чем 10-7 М, при этом указанная вариабельная область легкой цепи содержит последовательность аминокислот:
(i) KASESVDNYGKSLMH (SEQ ID NO: 19), в CDR1,
(ii) RASNLES (SEQ ID NO: 20), в CDR2, и
(iii) QQSNEDPWT (SEQ ID NO: 21), в CDR3;
а указанная вариабельная область тяжелой цепи содержит последовательность аминокислот:
(i) SYAMS (SEQ ID NO: 22), в CDR1,
(ii) SISSGGNTYYPDSVKG (SEQ ID NO: 23), в CDR2, и
(iii) LDGYYFGFAY (SEQ ID NO: 24), в CDR3,
или последовательность аминокислот, которая отличается менее чем на три консервативных замены аминокислот от последовательности аминокислот, выбранной из SEQ ID NO: 19-24,
и при этом антитело или его антигенсвязывающий фрагмент соединены с: другим антителом, токсином, радиоизотопом, цитотоксическим агентом или цитостатическим агентом.
3. Антитело или его антигенсвязывающий фрагмент по п.1, в которых вариабельная область легкой цепи иммуноглобулина по меньшей мере на 95% идентична последовательности SEQ ID NO: 11, 12, или 35.
4. Антитело или его антигенсвязывающий фрагмент по п.1, в которых вариабельная область тяжелой цепи иммуноглобулина содержит последовательность аминокислот SEQ ID NO: 15, 16, или 36.
5. Антитело или его антигенсвязывающий фрагмент по п.1 или 4, в которых вариабельная область легкой цепи иммуноглобулина содержит последовательность аминокислот SEQ ID NO: 11, 12, или 35.
6. Антитело или его антигенсвязывающий фрагмент по п.1, которые дополнительно содержат константную область легкой цепи иммуноглобулина по меньшей мере на 95% идентична последовательности аминокислот SEQ ID NО: 18.
7. Антитело или его антигенсвязывающий фрагмент по п.1, которые дополнительно содержат константную область тяжелой цепи иммуноглобулина, которая содержит последовательность аминокислот SEQ ID NO: 17.
8. Антитело или его антигенсвязывающий фрагмент по п.1 или 7, которые дополнительно содержат константную область легкой цепи иммуноглобулина, которая содержит последовательность аминокислот SEQ ID NO: 18.
9. Антитело или его антигенсвязывающий фрагмент, которые содержат вариабельную область тяжелой цепи иммуноглобулина и вариабельную область легкой цепи иммуноглобулина, которые связывают IL-13 с KD менее чем 10-7 М, при этом вариабельная область легкой цепи содержит последовательность аминокислот:
(i) xxxxxxxNYxKxxxx (SEQ ID NO: 25), в CDR1,
(ii) Rxxxxxx (SEQ ID NO: 26), в CDR2, и
(iii) xxxNxDxWx (SEQ ID NO: 27), в CDR3;
а указанная вариабельная область тяжелой цепи содержит последовательность аминокислот:
(i) SxAMx (SEQ ID NO: 28), в CDR1,
(ii) SxSSxxxxxYxxSVKG (SEQ ID NO: 29), в CDR2, и
(iii) LDGYYFxxxx (SEQ ID NO: 30), в CDR3,
причем х представляет собой аминокислоту, имеющую заряд и гидрофобность, схожие с аминокислотой в соответствующем положении в аминокислотной последовательности SEQ ID NO: 19-24.
10. Антитело или его антигенсвязывающий фрагмент по п.1, которое имеет одно или более из следующих свойств:
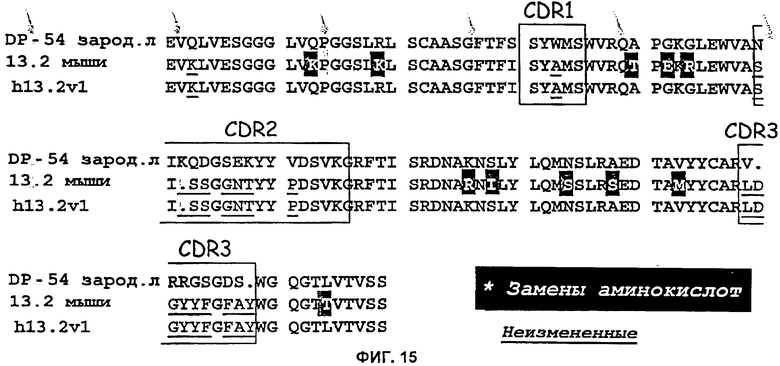
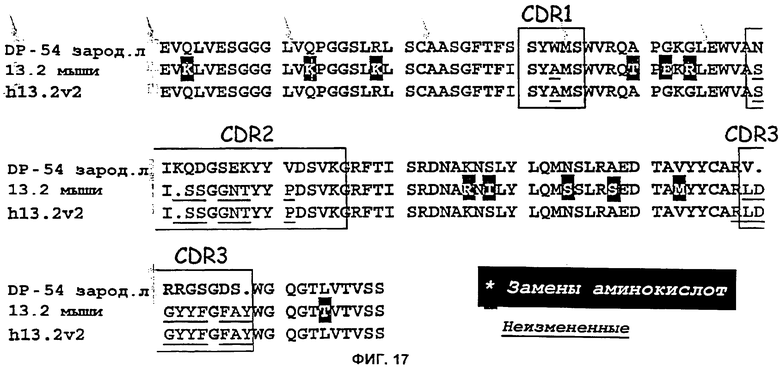
(a) вариабельная область тяжелой цепи иммуноглобулина содержит последовательность CDR3 тяжелой цепи моноклонального антитела mAb 13.2 (SEQ ID NO: 24) или последовательность CDR3 тяжелой цепи, которая отличается менее чем на три консервативных замены аминокислот от соответствующей последовательности CDR3 тяжелой цепи моноклонального антитела mAb 13.2;
(b) вариабельная область легкой цепи иммуноглобулина содержит последовательность CDR1 легкой цепи моноклонального антитела mAb 13.2 (SEQ ID NO: 19) или последовательность CDR1 легкой цепи, которая отличается менее чем на 3 консервативных замены аминокислот от соответствующей последовательности CDR1 легкой цепи моноклонального антитела mAb 13.2;
(c) вариабельная область тяжелой цепи иммуноглобулина содержит последовательность, кодируемую нуклеиновой кислотой, которая гибридизуется в условиях повышенной жесткости с последовательностью, комплементарной последовательности нуклеиновой кислоты, кодирующей вариабельный домен тяжелой цепи h13.2 (SEQ ID NO: 15, 16 или 36);
(d) вариабельная область тяжелой цепи иммуноглобулина содержит последовательность аминокислот, кодируемую нуклеиновой кислотой, которая гибридизуется в условиях повышенной жесткости с нуклеиновой кислотой, которая комплементарна нуклеиновой кислоте, которая содержит последовательность нуклеотидов SEQ ID NO: 7, 8, или 34;
(e) вариабельная область легкой цепи иммуноглобулина содержит последовательность, кодируемую нуклеиновой кислотой, которая гибридизуется в условиях повышенной жесткости с последовательностью, комплементарной последовательности нуклеиновой кислоты, кодирующей вариабельный домен легкой цепи h13.2 (SEQ ID NO: 11,12 или 35);
(f) вариабельная область легкой цепи иммуноглобулина содержит последовательность аминокислот, кодируемую нуклеиновой кислотой, которая гибридизуется в условиях повышенной жесткости с нуклеиновой кислотой, которая комплементарна нуклеиновой кислоте, которая содержит последовательность нуклеотидов SEQ ID NO: 3, 4, или 33;
(g) вариабельная область тяжелой цепи иммуноглобулина по меньшей мере на 90% идентична вариабельному домену тяжелой цепи h13.2 (SEQ ID NO: 15, 16 или 36);
(h) вариабельная область легкой цепи иммуноглобулина по меньшей мере на 90% идентична вариабельному домену легкой цепи h13.2 (SEQ ID NO: 11, 12, или 35);
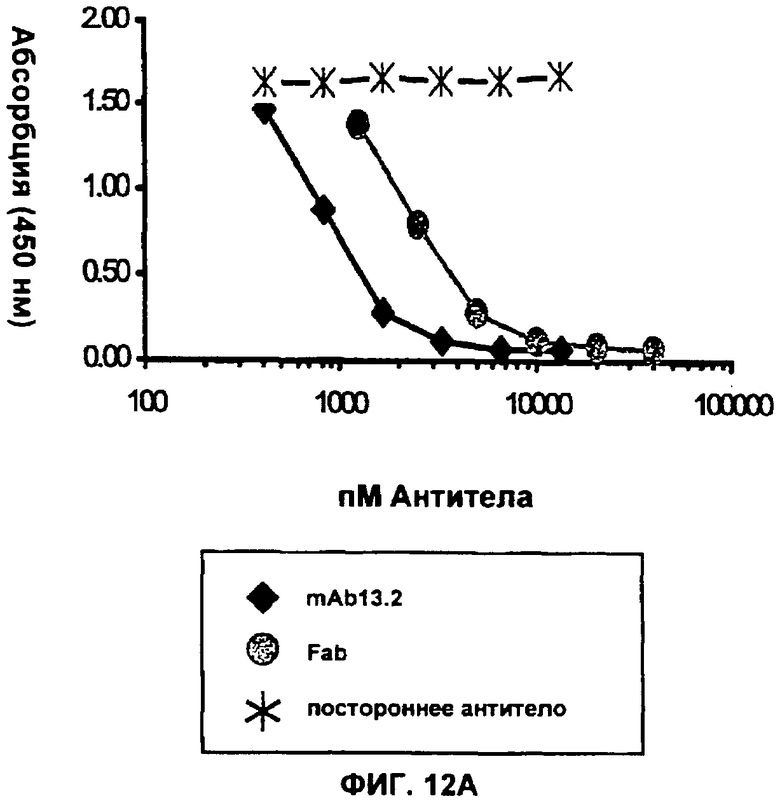
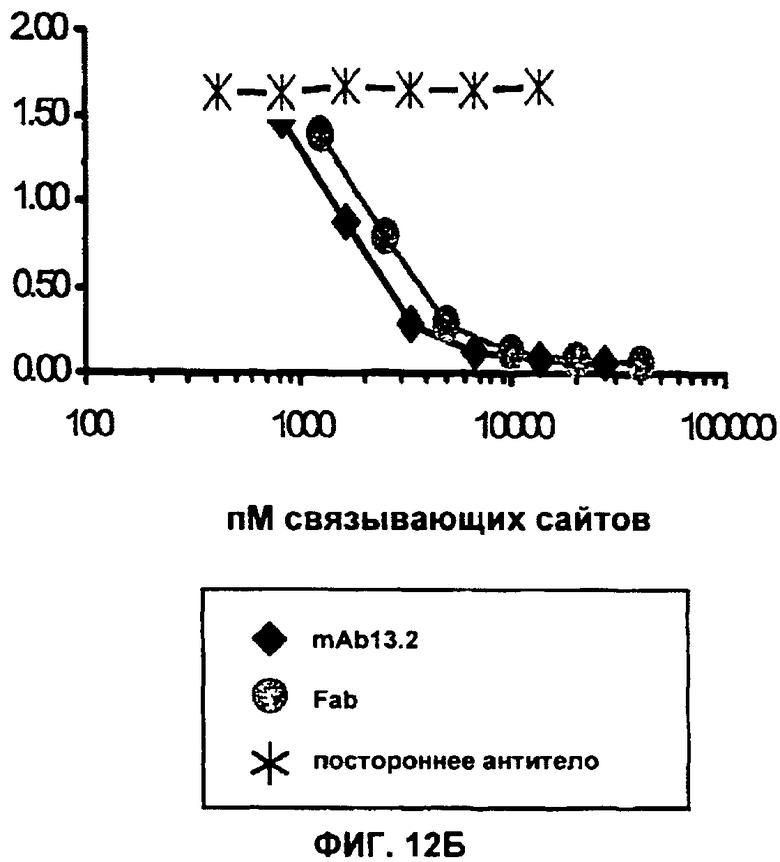
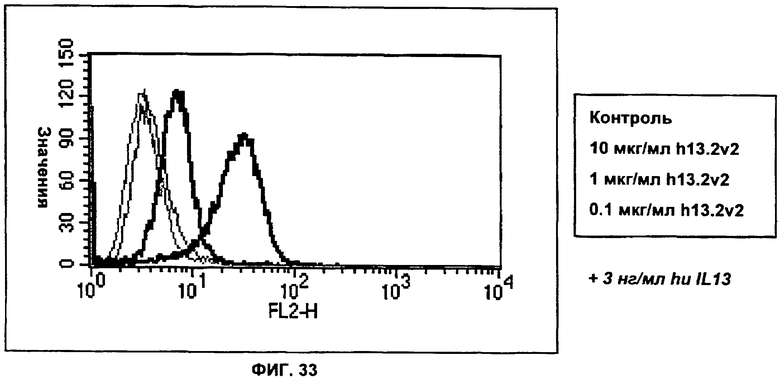
(i) указанное антитело или его антигенсвязывающий фрагмент конкурирует с моноклональным антителом mAb 13.2 за связывание с IL-13 человека;
(j) указанное антитело или его антигенсвязывающий домен контактирует с IL-13, в положениях остатков аминокислот: 68, 72, 88, 91, 92, 93 и 105 последовательности SEQ ID NO: 31;
(k) вариабельная область тяжелой цепи имеет ту же каноническую структуру, что и у моноклонального антитела mAb13.2;
(l) вариабельная область легкой цепи имеет ту же каноническую структуру, что и у монокпонального антитела mAb13.2;
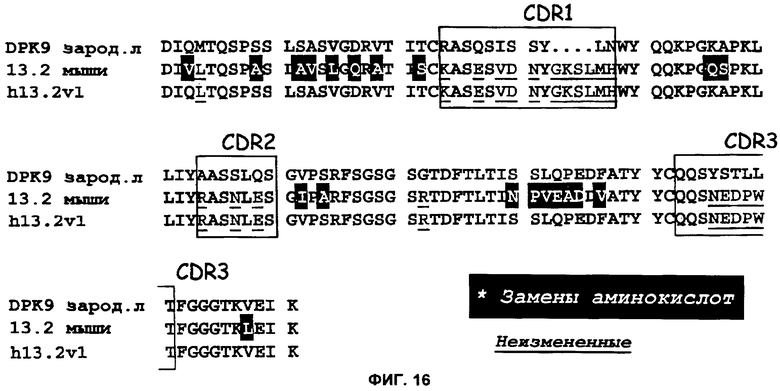
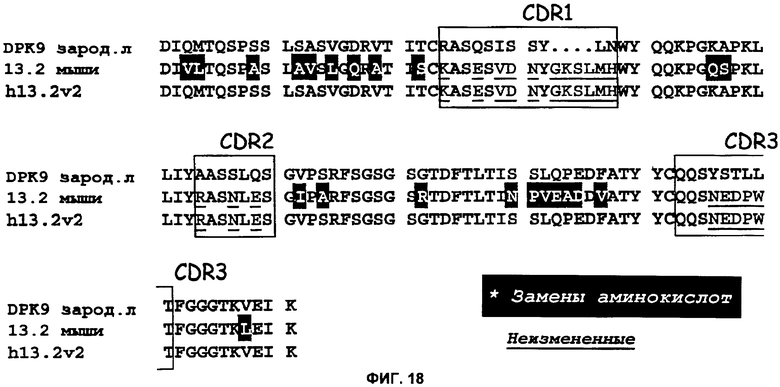
(m) вариабельная область тяжелой цепи и/или вариабельная область легкой цепи имеют каркасные области FR1, FR2 и FR3 из VH сегментов, кодируемых генами зародышевой линии человека DP-54 и DPK-9 соответственно, или последовательность по меньшей мере на 95% идентичную VH сегментам, кодируемым генами зародышевой линии человека DP-54 и DPK-9;
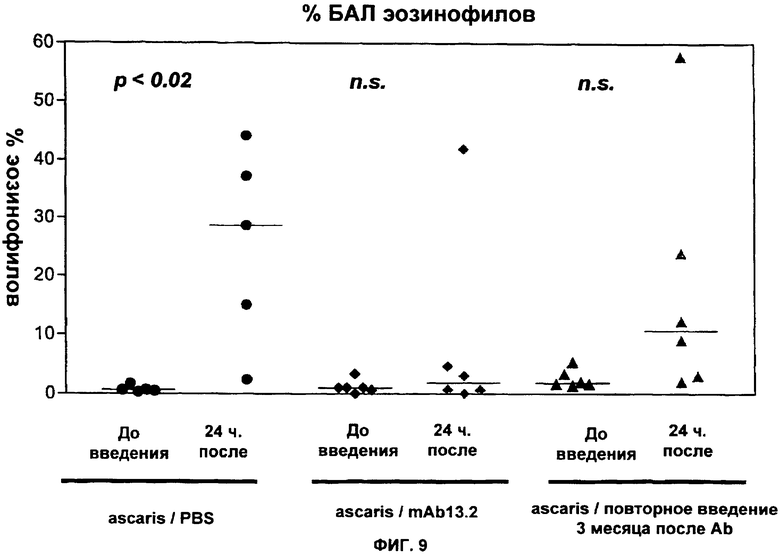
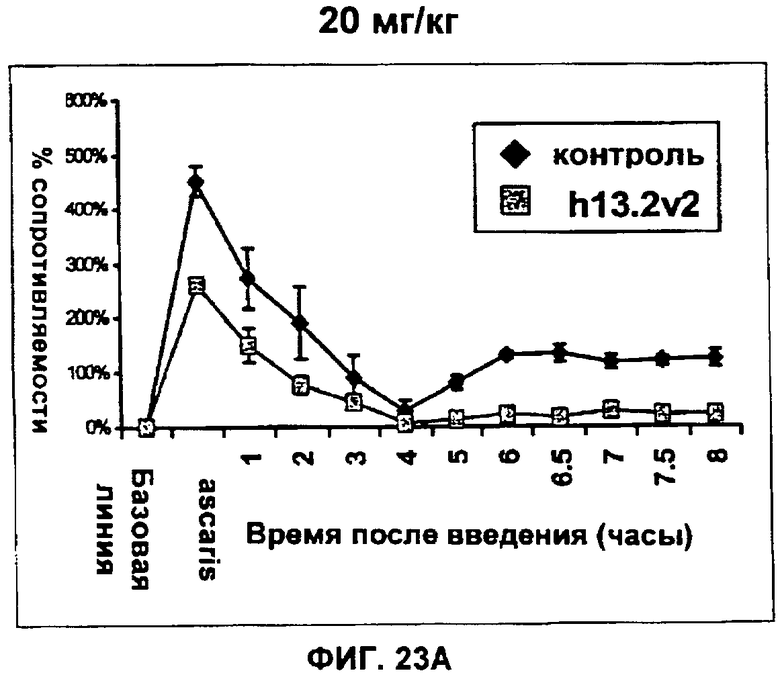
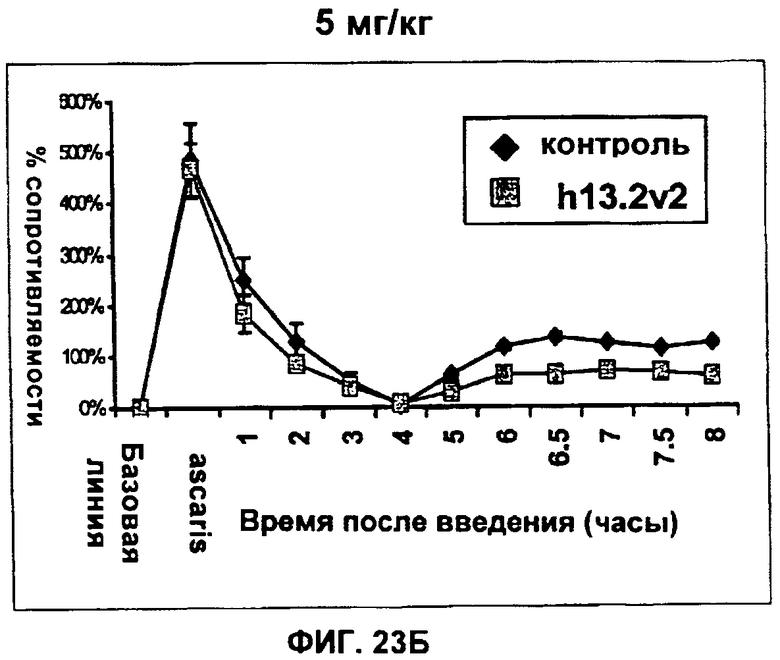
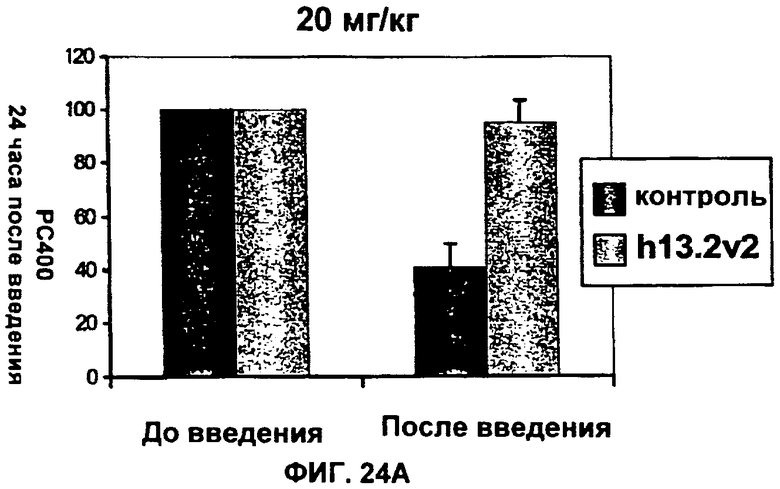
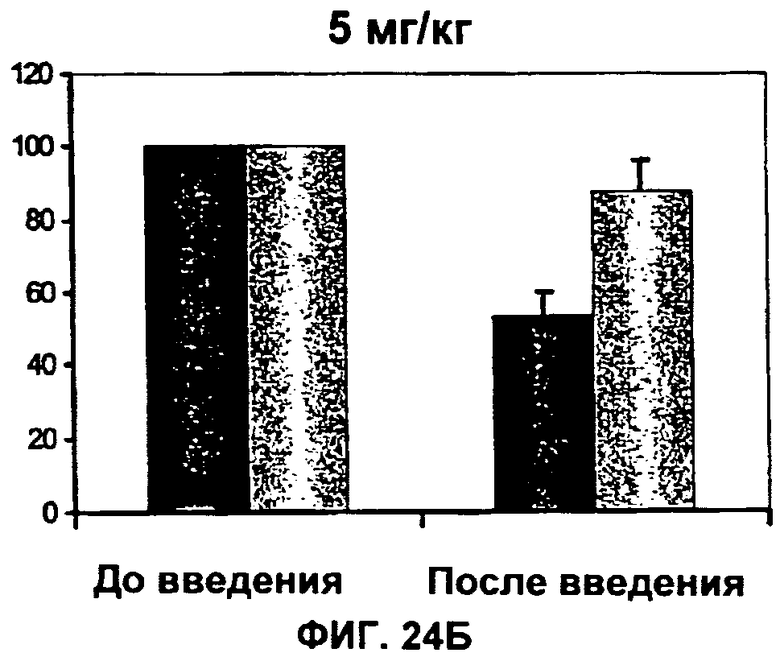
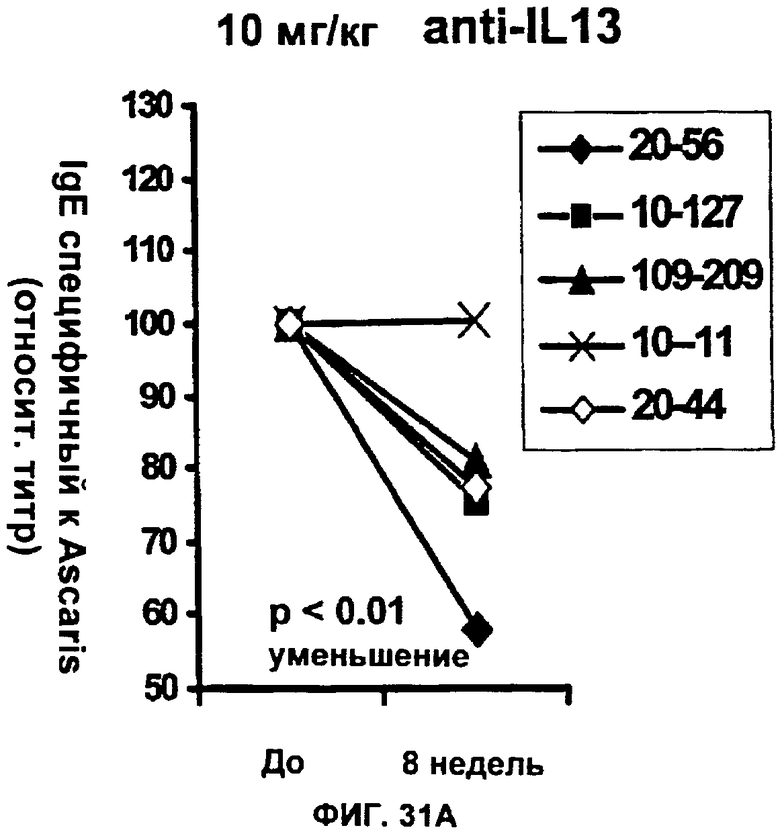
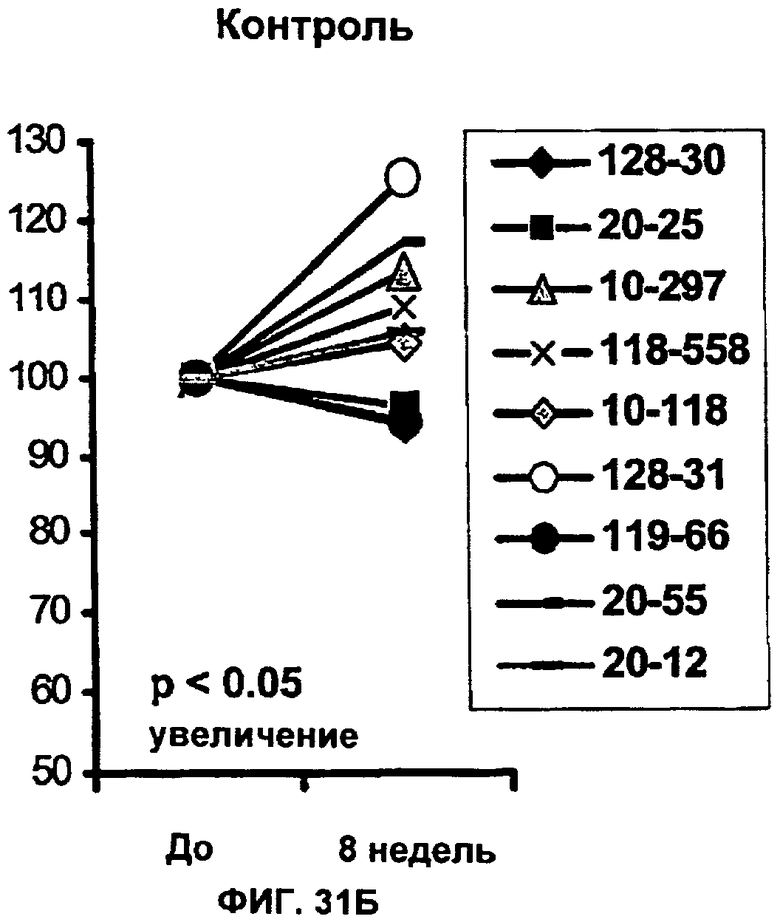
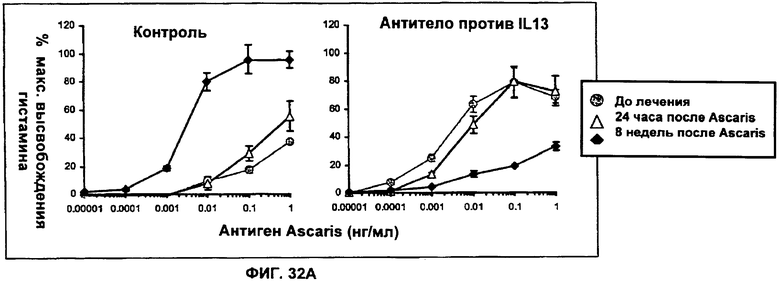
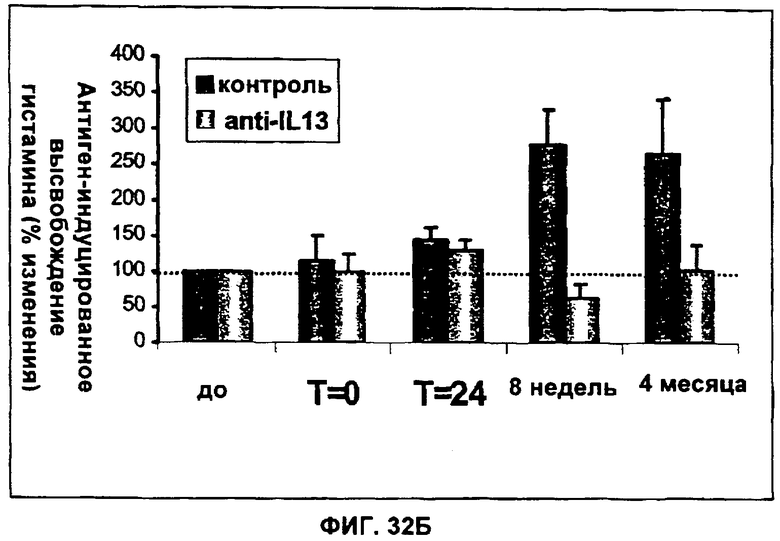
(n) придает пост-инъекционное защитное действие против антигена Аскариды на модели овцы в течение по меньшей мере 6 недель после инъекции.
11. Изолированное рекомбинантное антитело IgG, которое связывает IL-13 и содержит две цепи иммуноглобулинов: легкую цепь, которая содержит последовательность аминокислот, соответствующую SEQ ID NO: 9, 10, 11, 12 или 35 и тяжелую цепь, которая содержит последовательность аминокислот, соответствующую SEQ ID NO: 13, 14, 15, 16 или 36, или последовательность аминокислот по меньшей мере на 95% идентичную SEQ ID NO: 9, 10, 11, 12, 13, 14, 15, 16, 35 или 36.
12. Изолированное рекомбинантное антитело IgG no п.5, в котором тяжелая цепь дополнительно содержит последовательность аминокислот SEQ ID NO: 17, а легкая цепь дополнительно содержит последовательность аминокислот SEQ ID NO: 18 или последовательность аминокислот по меньшей мере на 95% идентичную SEQ ID NO: 17 или 18.
13. Антитело или его антигенсвязывающий фрагмент по п.1, отличающиеся тем, что обладают одним или более из следующих свойств:
(а) специфически связываются с эпитопом, содержащим остатки 81-93 или 114-132 IL-13 человека (SEQ ID NO: 31) или их консервативные аминокислотные замены;
(b) специфично связываются с эпитопом IL-13 человека, содержащим следующие аминокислотные остатки: глутамат в положении 49, аспарагин в положении 53; глицин в положении 69, пролин в положении 72, гистидин в положении 73, лизин в положении 74 и аргинин в положении 86 последовательности SEQ ID NO: 32 или их консервативные аминокислотные замены;
(c) связываются с комплексом IL-13 и IL13Rα1;
(d) препятствуют связывающему взаимодействию между IL-13 и IL-4Rα;
(e) препятствуют связывающему взаимодействию между IL-13/IL-13Rα1 и IL-4Rα; и
(f) специфично связываются с IL-13 человека и конкурентно ингибируют связывание второго антитела с вышеуказанным антигеном человека, причем вышеуказанное второе антитело содержит вариабельную область тяжелой и легкой цепи выбранные из mAbl3.2 (SEQ ID NO: 13 и SEQ ID NO: 9 соответственно), ch13.2 (SEQ ID NO: 14 и SEQ ID NO: 10 соответственно), h13.2v1 (SEQ ID NO: 15 и SEQ ID NO: 14 соответственно), h13.2v2 (SEQ ID NO: 16 и SEQ ID NO: 12 соответственно), или h13.2v3 (SEQ ID NO: 36 и SEQ ID NO: 35 соответственно); и/или
(g) указанное антитело содержит вариабельную область легкой цепи иммуноглобулина с последовательностью SEQ ID NO: 11, 12, или 35, остатки аминокислот которой: ASN31 (CDR1), TYR32 (CDR1), LYS34 (CDR1), ARG54 (CDR2), ASN96 (CDR3), ASP98 (CDR3), и TRP100 (CDR3) контактируют с IL-13; вариабельную область тяжелой цепи иммуноглобулина с последовательностью SEQ ID NO: 15, 16, или 36, остатки аминокислот которой: ILE30, SER31 (CDR1), ALA33 (CDR1), TRP47, SER50 (CDR2), SER52 (CDR2), SER53 (CDR2), TYR58 (CDR2), LEU98 (CDR3), ASP99 (CDR3), GLY100 (CDR3), TYR101 (CDR3), TYR102 (CDR3) и РНЕ103 (CDR3), контактируют с IL-13.
14. Антитело или его антигенсвязывающий фрагмент по п.13, которые соединены с: другим антителом, токсином, радиоизотопом, цитотоксическим агентом или цитостатическим агентом.
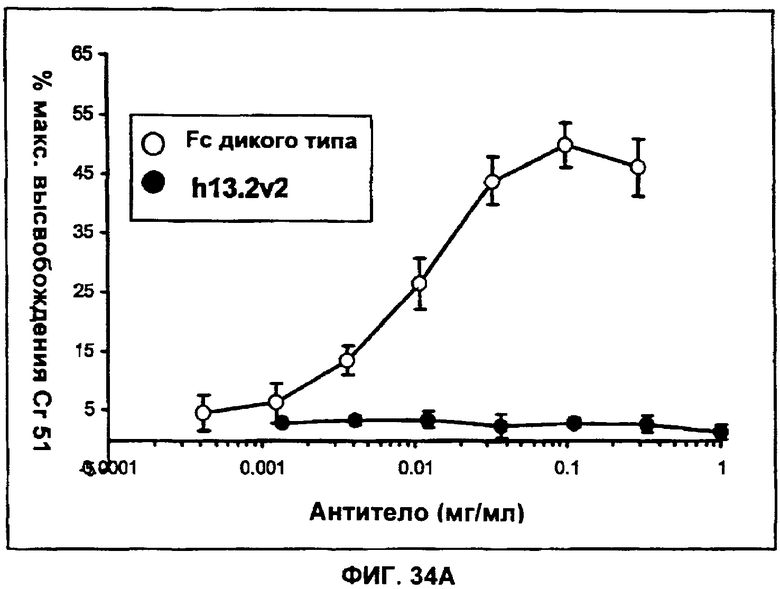
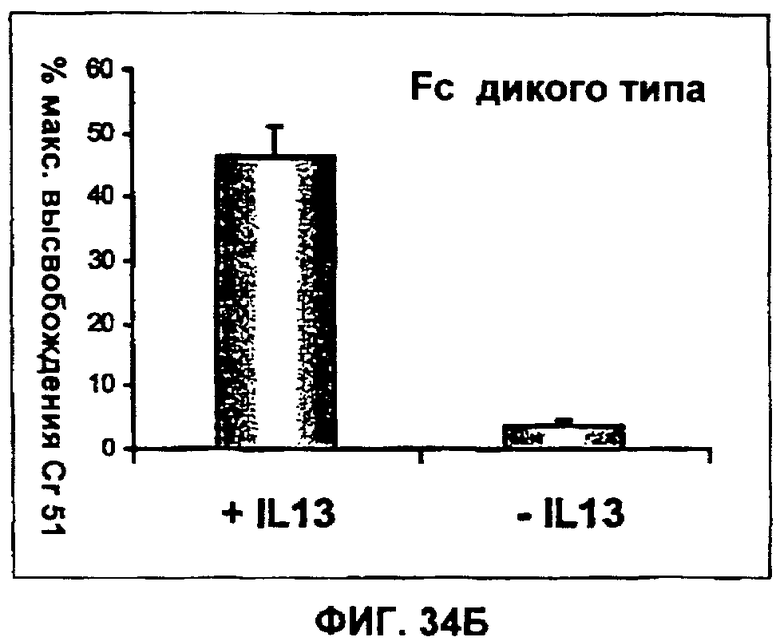
15. Антитело или его антигенсвязывающий фрагмент по п.13, которые содержат константную область, измененную таким образом, чтобы уменьшить: связывание с Fc рецептором, гликозилирование антитела, количество остатков цистеина, функцию эффекторной клетки или функцию комплемента.
16. Антитело или его антигенсвязывающий фрагмент по п.13, которые дополнительно содержат константную область IgG1 человека, в которой изменены один или более остатков 116 и 119 последовательности SEQ ID NO: 17 для уменьшения связывания с Fc рецептором.
17. Антитело или его антигенсвязывающий фрагмент по п.13, которые дополнительно содержат легкую цепь каппа иммуноглобулина человека.
18. Антитело или его антигенсвязывающий фрагмент по п.13, которые содержат по меньше мере одну CDR-область, содержащую аминокислотную последовательность, выбранную из группы, включающей: аминокислотную последовательность SEQ ID NO: 19, аминокислотную последовательность SEQ ID NO: 20, аминокислотную последовательность SEQ ID NO: 21, аминокислотную последовательность SEQ ID NO: 22, аминокислотную последовательность SEQ ID NO: 23 и аминокислотную последовательность SEQ ID NO: 24.
19. Антитело или его антигенсвязывающий фрагмент по п.13, отличающиеся тем, что фрагмент представляет собой фрагмент scFv, Fab, Fd, dAb или F(ab')2.
20. Антитело или его антигенсвязывающий фрагмент по п.13, которые дополнительно содержат легкую цепь, содержащую константную область каппа иммуноглобулина человека, или ее активный фрагмент и тяжелую цепь, содержащую константную область IgG человека или ее активный фрагмент.
21. Антитело или его антигенсвязывающий фрагмент по п.20, в которых константная область каппа вышеуказанной легкой цепи иммуноглобулина человека содержит аминокислотную последовательность SEQ ID NO: 18 или ее активный фрагмент.
22. Антитело или его антигенсвязывающий фрагмент по п.20, в которых константная область вышеуказанной тяжелой цепи IgG человека изменена для уменьшения связывания FcR и комплемента.
23. Антитело или его антигенсвязывающий фрагмент по п.20, в которых измененная константная область вышеуказанной тяжелой цепи IgG человека содержит аминокислотную последовательность SEQ ID NO: 17 или ее активный фрагмент.
24. Антитело или его антигенсвязывающий фрагмент по п.1 или 13, которые содержат вариабельную область тяжелой цепи иммуноглобулина и вариабельную область легкой цепи иммуноглобулина, которые связывают IL-13 с КD менее чем 10-7 М, при этом указанная вариабельная область легкой цепи содержит последовательность аминокислот:
(i) KASESVDNYGKSLMH (SEQ ID NO: 19), в CDR1,
(ii) RASNLES (SEQ ID NO: 20), в CDR2, и
(iii) QQSNEDPWT (SEQ ID NO: 21), в CDR3;
а указанная вариабельная область тяжелой цепи содержит последовательность аминокислот:
(i) SYAMS (SEQ ID NO: 22), в CDR1,
(ii) SISSGGNTYYPDSVKG (SEQ ID NO: 23), в CDR2, и
(iii) LDGYYFGFAY (SEQ ID NO: 24), в CDR3.
25. Антитело или его антигенсвязывающий фрагмент по п.1 или 24, в которых вариабельная область легкой цепи иммуноглобулина содержит последовательность SEQ ID NO: 11, 12, или 35, остатки аминокислот которой: ASN31 (CDR1), TYR32 (CDR1), EYS34 (CDR1), ARG54 (CDR2), ASN96 (CDR3), ASP98 (CDR3), и TRP100 (CDR3) контактируют с IL-13; вариабельную область тяжелой цепи иммуноглобулина с последовательностью SEQ ID NO:15, 16, или 36, остатки аминокислот которой: ILE30, SER31 (CDR1), ALA33 (CDR1), TRP47, SER50 (CDR2), SER52 (CDR2), SER53 (CDR2), TYR58 (CDR2), LEU98 (CDR3), ASP99 (CDR3), GEY100 (CDR3), TYR101 (CDR3), TYR102 (CDR3) и РНЕ103 (CDR3), контактируют с IE-13.
26. Антитело или его антигенсвязывающий фрагмент по п.1, в которых вариабельная область тяжелой цепи иммуноглобулина по меньшей мере на 95% идентична последовательности SEQ IDNO: 15, 16, или 36.
27. Антитело или его антигенсвязывающий фрагмент по п.26, в которых вариабельная область тяжелой цепи иммуноглобулина по меньшей мере на 95% идентична последовательности SEQ ID NO: 11, 12, или 35.
28. Антитело или его антигенсвязывающий фрагмент по п.1, в котором константная область изменена с целью уменьшить одно или более из следующих свойств: связывание с Fc рецептором, гликозилирование антитела, число остатков цистеина, функцию эффекторных клеток или функцию комплемента.
29. Антитело или его антигенсвязывающий фрагмент по п.1, которые дополнительно содержат константную область lgG1 человека, в которой изменен один или более остаток в положении 116 и 119 SEQ ID NO: 17 для уменьшения связывания с Fc рецептором.
30. Антитело или его антигенсвязывающий фрагмент по п.29, которые дополнительно содержат легкую цепь типа каппа иммуноглобулина человека.
31. Антитело или его антигенсвязывающий фрагмент по п.1, которые дополнительно содержат константную область тяжелой цепи иммуноглобулина по меньшей мере на 95% идентична последовательности аминокислот SEQ ID NO: 17.
32. Антитело или его антигенсвязывающий фрагмент по п.30, которые дополнительно содержат константную область легкой цепи иммуноглобулина по меньшей мере на 95% идентична последовательности аминокислот SEQ ID NO: 18.
33. Антитело или его антигенсвязывающий фрагмент по п.1, которые содержат последовательность аминокислот вариабельной области тяжелой цепи, которую кодирует нуклеиновая кислота, гибридизующаяся в условиях повышенной жесткости с нуклеиновой кислотой, которая комплементарна нуклеиновой кислоте, которая кодирует вариабельную область тяжелой цепи, содержащую последовательность аминокислот SEQ ID NO: 15, 16, или 36; или с нуклеиновой кислотой, которая комплементарна нуклеиновой кислоте, которая содержит последовательность нуклеотидов SEQ ID NO: 7, 8, или 34.
34. Антитело или его антигенсвязывающий фрагмент по п.33, которые содержат последовательность аминокислот вариабельной области легкой цепи, которую кодирует нуклеиновая кислота, гибридизующаяся в условиях повышенной жесткости с нуклеиновой кислотой, которая комплементарна нуклеиновой кислоте, которая кодирует вариабельную область легкой цепи, содержащую последовательность аминокислот SEQ ID NO: 11, 12, или 35; или с нуклеиновой кислотой, которая комплементарна нуклеиновой кислоте, которая содержит последовательность нуклеотидов SEQ ID NO: 3, 4, или 33.
35. Антитело или его антигенсвязывающий фрагмент по п.1, вариабельная область тяжелой цепи которых содержит последовательность аминокислот, которую кодирует нуклеиновая кислота, содержащая последовательность SEQ ID NO: 7, 8, или 34.
36. Антитело или его антигенсвязывающий фрагмент по п.35, вариабельная область легкой цепи которых содержит последовательность аминокислот, которую кодирует нуклеиновая кислота, содержащая последовательность SEQ ID NO:3, 4, или 33.
37. Антитело или его антигенсвязывающий фрагмент по п.10, которые соединены с: другим антителом, токсином, радиоизотопом, цитотоксическим агентом или цитостатическим агентом.
38. Антитело или его антигенсвязывающий фрагмент по любому из пп.1, 10, 11, 13, которые являются очищенными или рекомбинантными.
39. Антитело или его антигенсвязывающий фрагмент по любому из пп.1, 10, 11, 13, которые представляют собой рекомбинантный полноразмерный IgG.
40. Антитело или его антигенсвязывающий фрагмент по любому из пп.1, 10, 11, 13, которые представляют собой Fab, F(ab')2, Fd, dAb или scFv.
41. Антитело или его антигенсвязывающий фрагмент по любому из пп.1, 10, 11, 13, которые содержат каркасную область, которая по меньшей мере на 90% идентична каркасной области зародышевой линии человека.
42. Антитело или его антигенсвязывающий фрагмент по любому из пп.1, 10, 11, 13, которые содержат каркасную область антитела человека, Fc область антитела человека, либо обе эти области.
43. Антитело или его антигенсвязывающий фрагмент по любому из пп.1, 10, 11, 13, в которых вариабельная область тяжелой цепи образует водородные связи с IL-13 с участием аминокислот SER50 (CDR2), SER53 (CDR2), TYR101 (CDR3) и TYR102 (CDR3) последовательности SEQ ID NO:15, 16 или 36; и вариабельная область легкой цепи иммуноглобулина образует водородные связи с IL-13 с участием аминокислот ASN31, TYR32 (CDR1), LYS34 (CDR1), ASN96 (CDR3) и ASP98 (CDR3) последовательности SEQ ID NO: 11, 12 или 35.
44. Антитело или его антигенсвязывающий фрагмент по п.43, в которых вариабельная область легкой цепи иммуноглобулина содержит последовательность SEQ ID NO: 11, 12, или 35, остатки аминокислот которой: ASN31 (CDR1), TYR32 (CDR1), LYS34 (CDR1), ARG54 (CDR2), ASN96 (CDR3), ASP98 (CDR3), и TRP100 (CDR3) контактируют через взаимодействия Ван-дер-Ваальса с IL-13;
вариабельную область тяжелой цепи иммуноглобулина с последовательностью SEQ ID NO: 15, 16 или 36, остатки аминокислот которой: ILE30, SER31 (CDR1), ALA33 (CDR1), TRP47, SER50 (CDR2), SER52 (CDR2), SER53 (CDR2), TYR58 (CDR2), LEU98 (CDR3), ASP99 (CDR3), GLY100 (CDR3), TYR101 (CDR3), TYR102 (CDR3) и РНЕ103 (CDR3), контактируют через взаимодействия Ван-дер-Ваальса с IL-13.
45. Антитело или его антигенсвязывающий фрагмент по любому из пп.1, 10, 11, 13, которые связывают IL-13 человека с KD от 90 до 120 пМ.
46. Антитело или его антигенсвязывающий фрагмент по любому из пп.1, 10. 11, 13, которые связывают IL-13 человека с Koff меньше, чем 1×10-4 с-1.
47. Антитело или его антигенсвязывающий фрагмент по любому из пп.1, 10, 11, 13, которые связывают IL-13 человека с Кon от 5×104 до 8×105M-lc-l.
48. Антитело или его антигенсвязывающий фрагмент по любому из пп.1, 10, 11, 13, которые уменьшают способность IL-13 связываться с IL-4Rα.
49. Антитело или его антигенсвязывающий фрагмент по любому из пп.1, 10, 11, 13, которые связываются с IL-13, который находится в комплексе с IL-13Rα1 in vitro.
50. Выделенное рекомбинантное антитело IgG, которое связывает IL-13 и содержит две цепи иммуноглобулина: легкую цепь, содержащую последовательность аминокислот, которую кодирует SEQ ID NO: 1, 2, 3, 4, или 33, или последовательность, которая гибридизуется в условиях повышенной жесткости с последовательностью SEQ ID NO: 1, 2, 3, 4, или 33; и тяжелую цепь, содержащую последовательность аминокислот, которую кодирует SEQ ID NO: 5, 6, 7, 8, или 34, или последовательность, которая гибридизуется в условиях повышенной жесткости с последовательностью SEQ ID NO: 5, 6, 7, 8, или 34.
51. Выделенное рекомбинантное антитело IgG, которое связывает IL-13 и содержит две цепи иммуноглобулина: легкую цепь, содержащую последовательность аминокислот, которую кодирует SEQ ID NO: 4, или последовательность нуклеотидов, которая гибридизуется в условиях повышенной жесткости с последовательностью SEQ ID NO: 4; и тяжелую цепь, содержащую последовательность аминокислот, которую кодирует SEQ ID NO: 8, или последовательность нуклеотидов, которая гибридизуется в условиях повышенной жесткости с последовательностью SEQ ID NO: 8.
52. Выделенное рекомбинантное антитело IgG, которое связывает IL-13 и содержит две цепи иммуноглобулина: легкую цепь, содержащую последовательность аминокислот SEQ ID NO: 12; и тяжелую цепь, содержащую последовательность аминокислот SEQ ID NO: 16.
53. Выделенное рекомбинантное антитело IgG по п.52, в котором указанная тяжелая цепь дополнительно содержит последовательность SEQ ID NO: 17; а указанная легкая цепь дополнительно содержит последовательность SEQ ID NO: 18.
54. Фармацевтическая композиция для связывания IL-13, содержащая антитело или его антигенсвязывающий фрагмент по любому из пп.1-53, которая содержит последовательность вариабельной области тяжелой цепи иммуноглобулина и последовательность вариабельной области легкой цепи иммуноглобулина, которые связывают IL-13 с KD менее чем 10-7 и фармацевтически приемлемый носитель, в комбинации с одним или более дополнительным терапевтическим агентом, выбранным из группы, включающей: ингалируемые стероиды, бета-агонисты, антагонисты лейкотриенов или лейкотриеновых рецепторов, ингибиторы IgE, ингибиторы фосфодиестеразы, ксантины, антихолинергические препараты, агенты, стабилизирующие тучные клетки, ингибиторы IL-4, ингибиторы IL-5, ингибиторы эотаксина/ CCR3, антигистамины, антагонисты TNF, антагонисты TNF фермента, антагонисты TGFα, интерферон гамма, префенидон, хемотерапевтические агенты, нестероидные противовоспалительные вещества, иммуномодуляторы, ингибиторы р38 и ингибиторы NFκB.
55. Фармацевтический состав, предназначенный для связывания IL-13, содержащий эффективное количество антитела или его антигенсвязывающего фрагмента по любому из пп.1-53 и фармацевтически приемлемый носитель.
56. Фармацевтический состав по п.55, который подходит для подкожного введения, ингаляции или местного применения.
57. Нуклеиновая кислота, которая содержит нуклеотидную последовательность, которая:
(i) кодирует полипептид, содержащий вариабельную область тяжелой цепи иммуноглобулина антитела или его антигенсвязывающего фрагмента, которые связывают IL-13, которая:
(a) содержит последовательность аминокислот:
(i) SYAMS (SEQ ID NO: 22), в CDR1, (ii) SISSGGNTYYPDSVKG (SEQ ID NO: 23), в CDR2 и (iii) LDGYYFGFAY (SEQ ID NO: 24), в CDR3,
или последовательность аминокислот, которая отличается менее чем на три консервативных замены аминокислот от последовательности аминокислот, выбранной из: SEQ ID NO: 22-24; или
(b) идентична вариабельному домену тяжелой цепи h13.2 (SEQ ID NO: 15, 16, или 36) по меньшей мере на 90%; или
(ii) гибридизуется в условиях повышенной жесткости с последовательностью, комплементарной последовательности нуклеиновой кислоты (SEQ ID NO: 15, 16, или 36), кодирующей вариабельный домен тяжелой цепи h13.2.
58. Нуклеиновая кислота, которая содержит нуклеиновую последовательность, которая:
(i) кодирует полипептид, содержит вариабельную область тяжелой цепи иммуноглобулина антитела или его антигенсвязывающего фрагмента, которые связывают IL-13, которая:
(a) содержит последовательность аминокислот:
(i) KASESVDNYGKSLMH (SEQ ID NO: 19), в CDR1, (ii) RASNLES (SEQ ID NO: 20), в CDR2, и (iii) QQSNEDPWT (SEQ ID NO: 21), в CDR3;
или последовательность аминокислот, которая отличается менее чем на три консервативных замены аминокислот от последовательности аминокислот, выбранной из: SEQ ID NO: 19-21; или
(b) идентична вариабельному домену легкой цепи h13.2 (SEQ ID NO: 11,12 или 35) по меньшей мере, на 90%; или
(ii) гибридизуется в условиях повышенной жесткости с последовательностью, комплементарной последовательности нуклеиновой кислоты, кодирующей вариабельный домен легкой цепи h13.2 (SEQ ID NO: 11, 12 или 35).
59. Нуклеиновая кислота, содержащая последовательность нуклеотидов, которая гибридизуется в условиях повышенной жесткости с нуклеиновой кислотой, комплементарной нуклеиновой кислоте, которая кодирует вариабельную область тяжелой цепи антитела или его антигенсвязывающего фрагмента, которые связывают IL-13, которая содержит последовательность остатков аминокислот SEQ ID NO: 15, 16 или 36 или с нуклеиновой кислотой комплементарной нуклеиновой кислоте, которая содержит последовательность нуклеотидов SEQ ID NO: 7, 8 или 34.
60. Нуклеиновая кислота по п.59, отличающаяся тем, что указанная последовательность нуклеотидов кодирует вариабельную область тяжелой цепи, которая содержит последовательность остатков аминокислот SEQ ID NO: 15, 16 или 36, или содержит последовательность нуклеотидов SEQ ID NO: 7, 8 или 34.
61. Нуклеиновая кислота по п.60, отличающаяся тем, что указанная последовательность нуклеотидов кодирует вариабельную область тяжелой цепи, которая содержит последовательность остатков аминокислот SEQ ID NO: 16, или содержит последовательность нуклеотидов SEQ ID NO: 8.
62. Нуклеиновая кислота, содержащая последовательность нуклеотидов, которая гибридизуется в условиях повышенной жесткости с нуклеиновой кислотой, комплементарной нуклеиновой кислоте, которая кодирует вариабельную область легкой цепи антитела или его антигенсвязывающего фрагмента, которые связывают IL-13, которая содержит последовательность остатков аминокислот SEQ ID NO: 11, 12 или 35 или с нуклеиновой кислотой комплементарной нуклеиновой кислоте, которая содержит последовательность нуклеотидов SEQ ID NO: 3, 4 или 33.
63. Нуклеиновая кислота по п.62, отличающаяся тем, что указанная последовательность нуклеотидов кодирует вариабельную область легкой цепи, которая содержит последовательность остатков аминокислот SEQ ID NO: 11, 12 или 35, или содержит последовательность нуклеотидов SEQ ID NO: 3, 4 или 33.
64. Нуклеиновая кислота по п.63, отличающаяся тем, что указанная последовательность нуклеотидов кодирует вариабельную область легкой цепи, которая содержит последовательность остатков аминокислот SEQ ID NO: 12, или содержит последовательность нуклеотидов SEQ ID NO: 4.
65. Экспрессионный вектор, который содержит нуклеиновую кислоту по любому из пп.57-64.
66. Экспрессионный вектор, который содержит нуклеиновую кислоту, кодирующую вариабельную область тяжелой цепи и вариабельную область легкой цепи по любому из пп.57-64.
67. Клетка-хозяин для получения антитела, связывающего IL-13 или его антигенсвязывающего фрагмента, отличающаяся тем, что указанная клетка-хозяин содержит нуклеиновую кислоту по любому из пп.57-64.
68. Клетка-хозяин для получения антитела, связывающего IL-13 или его антигенсвязывающего фрагмента, отличающаяся тем, что указанная клетка-хозяин содержит нуклеиновую кислоту, кодирующую вариабельную область тяжелой цепи и вариабельную область легкой цепи по любому из пп.57-64.
69. Клетка-хозяин по п.67, отличающаяся тем, что она представляет собой клетку млекопитающего.
70. Клетка-хозяин по п.68, отличающаяся тем, что она представляет собой клетку млекопитающего.
71. Клетка-хозяин для получения антитела или его антигенсвязывающего фрагмента, которая содержит последовательность нуклеиновой кислоты, кодирующую антитело или его антигенсвязывающий фрагмент по любому из пп.1-53.
72. Способ получения рекомбинантного антитела, связывающего IL-13, включающий: обеспечение клетки-хозяина по п.67 или 68 и поддержание указанной клетки при условиях, при которых осуществляется экспрессия указанного антитела или антигенсвязывающего фрагмента.
73. Способ получения рекомбинантного антитела, связывающего IL-13, включающий:
обеспечение клетки хозяина последовательностью, которая включает последовательность нуклеиновой кислоты, которая кодирует антитело или его антигенсвязывающий фрагмент по любому из пп.1-53, и поддерживание указанной клетки в условиях, при которых происходит экспрессия антитела или его антигенсвязывающего фрагмента.
74. Способ по п.73, который дополнительно включает выделение белка из указанной клетки хозяина или из среды, в которой поддерживали клетку хозяин.
75. Способ по п.74, который дополнительно включает приготовление указанного выделенного белка в виде фармацевтического состава.
76. Способ лечения расстройства, связанного с IL-13, включающий введение млекопитающему с указанным расстройством или с повышенным риском возникновения указанного расстройства эффективного количества антитела или его антигенсвязывающего фрагмента по любому из пп.1-53.
77. Способ по п.76, отличающийся тем, что расстройство, связанное с IL-13, выбрано из группы, включающей: астматическое расстройство, атопическое нарушение, хроническую обструктивную болезнь легких (COPD), состояние, включающее воспаление дыхательных путей, эозинофилию, фиброз и повышенное выделение слизи, воспалительное состояние, аутоиммунное состояние, опухоль или рак, вирусную инфекцию и подавление проявления защитного иммунного ответа 1 типа.
78. Способ по п.76, отличающийся тем, что расстройство представляет собой астматическое нарушение или аллергический ринит.
79. Способ по п.76, отличающийся тем, что расстройство представляет собой воспалительное заболевание кишечника.
80. Способ по п.76, отличающийся тем, что расстройство представляет собой хроническую обструктивную болезнь легких (COPD).
81. Способ по п.76, отличающийся тем, что расстройство представляет собой атопическое расстройство.
82. Способ по п.76, в котором белок вводят подкожно, с помощью ингаляции или местно.
83. Способ по п.79, отличающийся тем, что указанное воспалительное заболевание кишечника представляет собой болезнь Крона или язвенный колит.
84. Способ лечения расстройства, связанного с IL-13, включающий введение млекопитающему эффективного количества антитела или его антигенсвязывающего фрагмента по любому из пп.1-53, причем указанное антитело имеет одно или более из следующих свойств:
(i) придает пост-инъекционное защитное действие против антигена Аскариды на модели овцы по меньшей мере в течение 6 недель после инъекции; или
(ii) препятствует связыванию IL-13 с IL-4Rα, но не препятствует связыванию IL-13cIL-13Rα1.
85. Способ обнаружения присутствия IL-13 в образце, включающий:
(i) приведение в контакт образца и антитела против IL-13 или его фрагмента по любому из пп.1-53; и
(ii) обнаружение образования комплекса между антителом против IL-13 или его фрагментом и образцом, причем образование комплекса в образце указывает на присутствие в нем IL-13 млекопитающего.
86. Способ по п.84, отличающийся тем, что образец получают от млекопитающего.
87. Способ лечения млекопитающего, имеющего симптомы астмы, выбранные из группы, включающей хрип, одышку, бронхостеноз, гиперактивность дыхательных путей, уменьшение объема легких, фиброз, воспаление дыхательных путей и выделение слизи, причем вышеуказанный способ включает этап введения пациенту антитела по любому из пп.1-53, причем антитело связывается с IL-13 и препятствует образованию функционального сигнального комплекса IL-13.
| BOST et al., In vivo treatment with anti-interleukin-13 antibodies significantly reduces the humoral immune response against an oral immunogen in mice, Immunology, 1996 Apr; 87(4):633-41 | |||
| РЕКОМБИНАНТНЫЕ IL4-АНТИТЕЛА, ИСПОЛЬЗУЕМЫЕ ДЛЯ ЛЕЧЕНИЯ НАРУШЕНИЙ, СВЯЗАННЫХ С ДЕЙСТВИЕМ IL4 | 1994 |
|
RU2162711C2 |
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
Авторы
Даты
2011-08-27—Публикация
2005-06-09—Подача