Изобретение относится к медицине, а именно к дерматологии, стоматологии и физиотерапии, в частности к применению фотодинамической терапии при селективном уничтожении патогенных и условно-патогенных микроорганизмов (бактерий и грибковых организмов).
Многочисленные клинические испытания убедительно свидетельствуют о том, что инфракрасное низкоинтенсивное лазерное излучение (ИК НИЛИ) может эффективно использоваться для профилактики и лечения травматических повреждений, сосудистых нарушений, системно-функциональных расстройств, а также дегенеративно-дистрофических заболеваний (Авруцкий М.Я., Катковский Д.Г., Мусихин Л.В., Гусейнов Т.Ю. Влияние низкоинтенсивного лазерного излучения на основные биологические процессы и гомеостаз больных. // Анестезиология и реаниматоогия. - 1991. - №5. - С.74-79; Гладких СП., Алексеев Ю.В., Истомин С.П. Триггерные молекулярные механизмы формирования биологических эффектов при низкоэнергетической лазерной терапии. // Использование лазеров для диагностики и лечения заболеваний. - М.: Изд-во ЛАС, 1996. - С.7-11).
Использование ИК НИЛИ эффективно при лечении различных острых и хронических инфекционных заболеваний, а также при гнойно-септических и гнойно-воспалительных осложнениях (Закревский Г.И., Василевич Н.М. Лазеротерапия при гнойно-воспалительных заболеваниях у детей. // Клин. хирургия. - 1980. - №6. - С.61-62; Karu Т. Photobiological fundamentals of low-power laser therapy. // Laser Health: abstr. of the 1-st international congress. - Limawssol, 1997. - P.207-210).
Терапевтический эффект ИК НИЛИ связан с его фотоактивизирующим и нормализующим (в терапевтических дозах) действием на активность важнейших ферментов метаболизма, биосинтез белков, ДНК, РНК, пролиферацию клеток, регенерацию тканей, активность иммунной системы и системы микроциркуляции крови и лимфы (Hawkins D.H., Abrahamse H. The role of laser influence in cell viability, proliferation, and membrane integrity of wounded human skin fibroblasts following helium-neon laser irradiation. // Lasers in Surgery and Medicine. - 2006. - V.38, №1. - P.74-83.).
Для лазеротерапии чаще всего используют лазерное излучение инфракрасного (λ=800-1200 нм) диапазона, генерируемое в непрерывном или импульсном режимах, при этом особенно выраженный терапевтический эффект наблюдается при использовании длин волн 800-890 нм.
Фотобиологические процессы, вызванные ИК НИЛИ, достаточно разнообразны и специфичны. В основе их лежат фотофизические и фотохимические реакции, возникающие в организме при воздействии лазерного света. Фотофизические реакции обусловлены преимущественно нагреванием объекта до различной степени и распространением тепла в биотканях. Разница температуры более выражена на биологических мембранах, что ведет к оттоку ионов Na+ и К+, раскрытию белковых каналов и увеличению транспорта молекул и ионов. Фотохимические реакции обусловлены возбуждением электронов в атомах поглощающего свет вещества. На молекулярном уровне это выражается в виде фотоионизации вещества, его восстановления или фотоокисления, фотодиссоциации молекул, в их перестройке - фотоизомеризации. В таком состоянии биомолекулярные комплексы приобретают высокую реакционную способность, что позволяет им активно участвовать в разнообразных процессах клеточного метаболизма (Кару Т.Й. Первичные и вторичные клеточные механизмы лазерной терапии. // Низкоинтенсивная лазерная терапия. / Под ред. С.В.Москвина и В.А.Буйлина. - М.: ТОО «Фирма «Техника», 2000. - С.71-94; Бриль Г.Е. Молекулярные аспекты биологического действия низкоинтенсивного лазерного излучения. // Актуальные проблемы патологии. Саратов, из-во Саратовского ун-та, 2001. - С.124-136).
В патенте РФ №2376045, МПК A61N 5/067 описан способ, когда осуществляют многократное сеансовое транскутанное воздействие низкоинтенсивным инфракрасным лазерным излучением арсенид-галлиевой природы с частотой 600 Гц на грудную клетку в области воспалительного инфильтрата с постоянным перемещением излучателя по межреберным промежуткам в пределах зоны.
Данный способ не учитывает особенности воспалительного процесса, чувствительность к воздействию инфекционных агентов, ставших причиной воспаления. Указанные недостатки существенно снижают эффективность лечения пневмонии.
В патенте РФ №2122447, МПК A61N 5/06 раскрывается способ послеоперационного лечения распространенных форм гнойной инфекции брюшной полости, включающий инфракрасную лазеротерапию в терапевтических дозах в сочетании с облучением крови и передней брюшной стенки с шести полей. Производят магнито-лазерное облучение с магнитной индукцией 35 мТл, при этом переднюю брюшную стенку облучают ежедневно по 2 минуты на поле, облучение крови проводят чрескожно над бедренными сосудами при экспозиции 15 минут и чередуют его через день с облучением зоны проекции тимуса при частоте 10 Гц и экспозиции 5 минут при общей длительности курса 5-7 дней.
Недостатком данного способа также является то, что невозможно корректировать параметры воздействия в зависимости от бактериальной природы гнойно-воспалительного заболевания. Поскольку осуществление способа проводят путем облучения кожи, велик риск негативного воздействия на нормальную микрофлору организма пациента.
В патенте РФ №2294223, МПК A61N 5/067 описан способ фотообработки биоткани, который заключается в облучении биоткани световым излучением с длиной волны от 500 нм до 2500 нм с плотностью энергии, достаточной для индуцирования апоптоза клеток части биоткани, содержащей хромофор. Способ позволяет осуществить фотообработку для целей ингибирования роста нежелательных волос, удаления сосудистых дефектов и пигментных пятен кожи, ремоделирования кожи, редукции сальных желез при акне, удаления новообразований, редукции, в т.ч. удаления гипертрофических и келоидных рубцов с индукцией светоиндуцированного апоптоза клеток этих частей биоткани.
У способа присутствуют недостатки, описанные выше: не учитывается реакция воздействия патологической и нормальной микрофлоры.
В качестве одного из типов оптических индикаторов при диагностике заболеваний в медицинской практике широкое применение нашли химические красители. Одним из таких красителей является индоцианин зеленый. Индоцианин зеленый активно используется в самых различных областях медицины: онкологии, офтальмологии, кардиологии, хирургии, дерматологии, тестирования функций печени, в косметологии.
Например, в патенте РФ №2245123, МПК A61F 9/007 описан способ лечения неоваскулярной глаукомы путем хирургического вмешательства. После премедикации, проведения анестезии и акинезии выполняют парацентез роговицы, через который вводят индоцианин зеленый для окрашивания новообразованной базальной мембраны, после окрашивания мембрану удаляют с поверхности радужной оболочки и с поверхности трабекулы при помощи капсульного пинцета, промывают переднюю камеру физиологическим раствором до полного вымывания остатков индоцианина зеленого. Важным является также очень низкая токсичность и быстрое выведение данного красителя из организма (индоцианин зеленый выводится из плазмы почти исключительно паренхиматозными клетками печени и выделяется полностью в желчь). Индоцианин зеленый является перспективным красителем для применения в фотодинамической терапии, поскольку его максимум поглощения находится в пределах от 780 до 850 нм, что соответствует максимуму испускания инфракрасных лазеров.
Фотокаталитические материалы представляют собой полупроводники, в которых под действием света возникает пара электрон-дырка, при этом на поверхности материала образуются свободные радикалы с высокой реакционной активностью. Диоксид титана является именно таким полупроводником. Известно, что диоксид титана можно использовать для удаления природных или промышленных загрязнителей в воздухе и воде при УФ-облучении, при этом кислород воздуха восстанавливается, а примесь окисляется с образованием безвредного конечного продукта (минерализуется). Кроме того, поверхность диоксида титана благодаря поглощению УФ-света становится сверхгидрофильной. На этом основано защитное действие тонкой пленки диоксида титана на зеркалах или оконных стеклах.
Важной особенностью диоксида титана является способность поглощать свет как в синей (405-420 нм), так и в инфракрасной (950-1000 нм) областях спектра, т.е. данные наночастицы могут быть использованы в сочетании с разнообразными источниками излучения: широкополосными лампами, одноволновыми светодиодами или лазерами (Баллюзек Ф.В., Куркаев А.С., Сентле Л. Нанотехнологии в медицине. - СПб: «Сезам», 2007. - 103 с.).
Антимикробный эффект фотодинамической терапии с одновременным использованием как фотокатализатора, так и фотосенсибилизатора в сочетании с излучением соответствующего спектрального состава обеспечивается множественным токсическим действием генерируемых активных радикалов (гидроксидный радикал, супероксидный анион, перекись водорода, сигнглетный кислород).
Использование инфракрасного лазерного излучения способно обеспечить не только фотодинамический эффект за счет генерации активных радикалов, но и фототермические процессы. Локальная подача тепловой энергии широко используется в онкологии и может быть применена при лечении заболеваний микробной природы. Установлены фототермические свойства нанотрубок диоксида титана с использованием инфракрасного (808 нм) лазерного излучения (G.K.Mor, S.Kim, M.Paulose, O.K.Varghese et all. Visible to Near-Infrared Light Harvesting in TiO2 Nanotube Array-РЗНТ Based Heterojunction Solar Cells. // Nano Lett., 2009. - Vol.9, №12. - P.4250-4257).
Индоцианин зеленый также может быть использован для селективного местного фототермического эффекта (W.Baumler, С.Abels, S.Karrer, et al. Photo-oxidative killing of human colonic cancer cells using indocyanine green and infrared light. // British J. Cancer, 1999. - Vol.80, №3/4. - P.360-363; С.Abels, S.Fickweiler, P.Weiderer, W.Baumler, et al., Indocyanine green (ICG) and laser irradiation induce photooxidation. // Arch. Dermatol. Res., 2000. - Vol.292. - P.404-411). При этом локальный нагрев будет происходить только в области, обработанной индоцианином зеленым, и сведет к минимуму тепловые повреждения окружающих неокрашенных тканей.
Наиболее близким к предлагаемому способу является способ, описанный в патенте РФ №2318511, МПК А61К 31/409, А61Р 27/02, для фотодинамической терапии меланомы хориоидеи. Для этого внутривенно вводят фотосенсибилизатор хлоринового ряда в дозе 0,8-1 мг/кг веса, затем облучают новообразование лазером транспупиллярно с длиной волны, соответствующей максимуму поглощения фотосенсибилизатора, проводят от 2 до 4 сеансов внутривенного введения ФС и лазерного облучения поверхности опухоли до достижения полной ее резорбции. Аналогичный метод может быть использован для лечения гнойно-воспалительных заболеваний кожи и слизистых оболочек, возбудителями которых являются различные микроорганизмы.
Однако для фотодинамического воздействия инфракрасного лазерного излучения в качестве фотосенсибилизатора более выгодно использовать индоцианин зеленый, а не сенсибилизаторы хлоринового ряда. Данный краситель является разрешенным лекарственным препаратом и имеет максимум поглощения в ИК-области спектра. Недостатком метода, предложенного в прототипе, также является необходимость нескольких сеансов, тогда как в предлагаемом авторами способе антимикробный эффект может быть достигнут после однократного фотодинамического воздействия.
Задачей настоящего изобретения является разработка способа для эффективной и селективной инактивации патогенных и условно-патогенных микроорганизмов возбудителей инфекционных заболеваний человека и животных.
Технический результат - эффективное средство антимикробной терапии, неспособное негативно повлиять на нормальный микробный состав кожи, полости рта и других полостей организма пациента.
Поставленная задача решается тем, что в способе уничтожения патогенных и условно-патогенных микроорганизмов одновременно обрабатывают область, содержащую микроорганизмы, композицией фотосенсибилизатора и фотокатализатора, выдерживают в течение периода времени, необходимого для эффективного связывания композиции с клетками микроорганизмов; затем воздействуют на указанную область оптическим излучением с длинами волн, соответствующими максимуму поглощения фотосенсибилизатора и фотокатализатора, и плотностью мощности для активации композиции, при этом в качестве фотосенсибилизатора используют индоцианин зеленый, а в качестве фотокатализатора используют наночастицы диоксида титана.
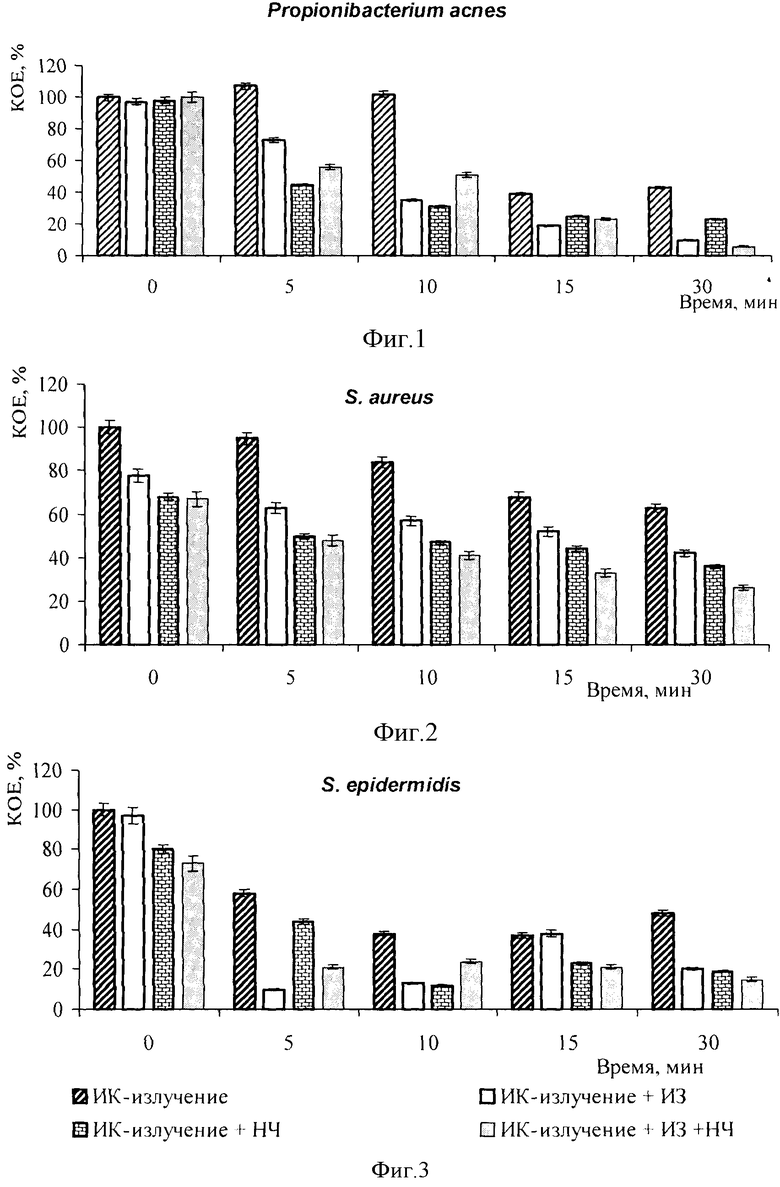
Изобретение поясняется чертежами, где на фиг.1. 2 и 3 показано влияние лазерного инфракрасного излучения (805 нм) на микроорганизмы: фиг.1 - Р.acnes; фиг.2 - S.aureus; фиг.3 - S.Epidermidis; на фиг.4 и 5 показано действие лазерного инфракрасного излучения (810 нм) на колониеобразующую способность микроорганизмов: фиг.4 - Н.ectinomycetemcomitans: фиг.5 - Str.Salivarius.
Настоящее изобретение относится к способу уничтожения патогенных и условно-патогенных микроорганизмов с использованием композиции, содержащей наночастицы диоксида титана и индоцианин зеленый, в сочетании с инфракрасным лазерным излучением.
Предполагается, что при одновременном введении фотокатализатора и фотосенсибилизатора в область, содержащую микроорганизмы, эффективность фотодинамического-фотокаталитического воздействия будет увеличиваться за счет синергетического взаимодействия данных фотохимически активных веществ. Наночастицы диоксида титана имеют пористую разветвленную поверхность, способную сорбировать молекулы фотодинамических красителей, тем самым увеличивая эффективность электронного возбуждения при воздействии света и пленение дополнительных электронов для увеличения эффективности фотокаталитического действия. При облучении такой системы «частица-краситель» количество генерируемых радикалов увеличивается. Присутствие системы «частица-краситель» в микроокружении бактериальной клетки или на поверхности клеточной стенки обеспечит ее разрушение в результате активных окислительных процессов.
В предпочтительном способе композицию, содержащую наночастицы диоксида титана (концентрация от 0.1 до 0.01%) и индоцианин зеленый (концентрация от 0.1 до 0.01%), вводят в область, содержащую патогенные или условно-патогенные микроорганизмы. Выжидают достаточное количество времени (10-20 мин), чтобы композиция веществ успела связаться с клетками микроорганизмов, затем проводят облучение указанной области лазерным инфракрасным излучением с длиной волны 800-1000 нм, плотностью мощности от 40 до 50 мВт/см2 в течение 1-30 мин.
Способ осуществляют по следующей схеме. Для создания асептических условий иммунологический полистирольный 96-луночный планшет помещают в стеклянный или пластиковый корпус. Источник излучения располагают над ячейками планшета. При постановке опытов используют суточную культуру исследуемого штамма. Из разведения микроорганизмов 10000 м.к./мл 0,1 мл взвеси вносят в 0.9 мл раствора фотосенсибилизатора, инкубируют в течение 10-20 мин без доступа света. Из конечного разведения, а также из раствора фотосенсибилизатора бактериальную взвесь в объеме 0.2 мл вносят в ячейки планшета. Воздействие излучения проводят на бактериальные клетки во взвеси, находящейся в соответствующих ячейках, последовательно увеличивая время облучения. После воздействия взвеси бактерий переносят на чашки Петри с плотной питательной средой и равномерно распределяют по поверхности стерильным шпателем. Учет результатов проводят путем подсчета числа колониеобразующих единиц (КОЕ) через 24-72 часа после анаэробной инкубации при 37°С. Контролем служат взвеси бактерий, не обработанные сенсибилизатором и не подвергнутые облучению.
Пример 1. Определение чувствительности микроорганизмов к различным концентрациям фотосенсибилизатора и фотокатализатора после облучения.
В качестве объекта исследования используют патогенные (Propionibacterium acnes) и условно-патогенные (Staphylococcus aureus, S.epidermidis) микроорганизмы. В качестве фотосенсибилизатора используют водный раствор индоцианина зеленого с концентрациями 0,1; 0,05; 0,01%. Фотокатализатором служат суспензии наночастиц диоксида титана (ТiO2) в концентрации 0,1; 0,02; 0,01%. При работе используют лазерный диод с максимумом спектра испускания λ=805±15 нм, плотностью мощности излучения - 50 мВт/см2. Облучение бактериальных взвесей проводят в течение 15 мин.
Используемые концентрации индоцианина зеленого и диоксида титана повышают чувствительность микроорганизмов к действию светодиодного излучения.
Пример 2. Фотодинамическое воздействие на микроорганизмы, возбудители угревой сыпи, сенсибилизированные индоцианином зеленым и наночастицами диоксида титана.
Модельными патогенными микроорганизмами служат виды Propionibacterium acnes и Staphylococcus aureus, которые являются возбудителями кожных гнойно-воспалительных заболеваний у человека, в частности угревой сыпи. Микроорганизмы Р.acnes выращивают в анаэробных условиях в специальном контейнере с газовой смесью CO2:N2=9:1 при температуре 37°С на тиогликолиевой среде. В качестве представителя условно-патогенной флоры, сопутствующей акне, используют вид Staphylococcus epidermidis. Стафилококки выращивают на мясо-пептонном агаре при температуре 37°С.
При работе используют лазерный диод с максимумом спектра испускания λ=805±15 нм, плотностью мощности излучения 50 мВт/см2. Облучение бактериальных взвесей проводят в течение 5, 10, 15, 30 мин.
В качестве фотосенсибилизатора используют 0.01% водный раствор индоцианина зеленого. Фотокатализатором служит суспензия наночастиц диоксида титана (ТiO2) в концентрации 0.02%.
Результаты экспериментов показаны на фиг.1-3.
Фотодинамическое воздействие с использованием комбинации метиленового синего и наночастиц диоксида титана демонстрирует выраженный угнетающий эффект на рост бактериальных клеток.
Пример 3. Влияние лазерного инфракрасного (810 нм) излучения на микроорганизмы, входящие в состав нормальной микрофлоры полости рта человека, сенсибилизированные индоцианином зеленым.
Объектом исследования служат бактерии видов Haemophilus actionomycetemcomitans и Streptococcus salivarius - представители нормальной микрофлоры полости рта человека.
При работе используют лазерный диод с максимумом спектра испускания λ=810±15 нм, плотностью мощности излучения 45 мВт/см2. Облучение бактериальных взвесей проводят в течение 1, 5, 10, 15 мин. В качестве фотосенсибилизатора используют 0.1% водный раствор индоцианина зеленого. Результаты экспериментов представлены на фиг.4-5.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ УНИЧТОЖЕНИЯ ПАТОГЕННЫХ И УСЛОВНО-ПАТОГЕННЫХ МИКРООРГАНИЗМОВ | 2010 |
|
RU2430756C1 |
| СПОСОБ СЕЛЕКТИВНОГО РАЗРУШЕНИЯ РАКОВЫХ КЛЕТОК С ПОМОЩЬЮ МАГНИТНЫХ МИКРОКОНТЕЙНЕРОВ С ФОТОДИНАМИЧЕСКИМИ ИЛИ ФОТОТЕРМИЧЕСКИМИ КРАСИТЕЛЯМИ | 2009 |
|
RU2405600C9 |
| ЭКСПЕРИМЕНТАЛЬНЫЙ СПОСОБ УНИЧТОЖЕНИЯ ПАТОГЕННЫХ И УСЛОВНО-ПАТОГЕННЫХ МИКРООРГАНИЗМОВ | 2012 |
|
RU2500430C1 |
| СПОСОБ ЛАЗЕРНОГО ФОТОТЕРМОЛИЗА РАКОВЫХ КЛЕТОК | 2009 |
|
RU2424831C1 |
| Способ комбинированного лечения местного отграниченного перитонита в эксперименте | 2023 |
|
RU2822708C1 |
| Способ оптимизации фотодинамической терапии гнойных ран (варианты) | 2015 |
|
RU2609735C1 |
| Способ лечения онихомикоза и других заболеваний, вызванных патогенными грибками | 2023 |
|
RU2837352C2 |
| Способ комбинированного лечения гнойного мастита в эксперименте | 2021 |
|
RU2781245C1 |
| СПОСОБ БОРЬБЫ С БАКТЕРИАЛЬНЫМИ БИОПЛЁНКАМИ | 2019 |
|
RU2737417C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОГО ЛЕЧЕНИЯ ОСТРОГО И ХРОНИЧЕСКОГО ГНОЙНОГО ГАЙМОРИТА | 2002 |
|
RU2228775C1 |

Изобретение относится к медицине, а именно к физиотерапии. Способ включает обработку области, содержащей микроорганизмы, композицией фотосенсибилизатора и фотокатализатора. После этого их выдерживают в течение времени, необходимого для эффективного связывания композиции с клетками микроорганизмов. Затем на указанную область воздействуют оптическим излучением с длинами волн, соответствующими максимуму поглощения фотосенсибилизатора и фотокатализатора, и плотностью мощности, необходимой для активации композиции. При этом в качестве фотосенсибилизатора используют индоцианин зеленый. В качестве фотокатализатора используют наночастицы диоксида титана. Способ повышает эффективность инактивации патогенных и условно-патогенных микроорганизмов за счет повышения чувствительности микроорганизмов к излучению. 7 з.п. ф-лы, 5 ил.
1. Способ подавления патогенных и условно-патогенных микроорганизмов, характеризующийся тем, что одновременно обрабатывают область, содержащую микроорганизмы, композицией фотосенсибилизатора и фотокатализатора, выдерживают в течение периода времени, необходимого для эффективного связывания композиции с клетками микроорганизмов; затем воздействуют на указанную область оптическим излучением с длинами волн, соответствующими максимуму поглощения фотосенсибилизатора и фотокатализатора, и плотностью мощности для активации композиции, при этом в качестве фотосенсибилизатора используют индоцианин зеленый, а в качестве фотокатализатора используют наночастицы диоксида титана.
2. Способ по п.1, характеризующийся тем, что воздействуют лазерным инфракрасным излучением.
3. Способ по п.1, характеризующийся тем, что длины волн излучения выбирают в диапазоне от 800 до 10000 нм.
4. Способ по п.1, характеризующийся тем, что плотностью мощности излучения выбирают в диапазоне от 40 до 50 мВт/см2.
5. Способ по п.1, характеризующийся тем, что длительность облучения составляет от 1 до 30 мин.
6. Способ по п.1, характеризующийся тем, что концентрация индоцианина зеленого составляет от 0,01 до 0,1%.
7. Способ по п.1, характеризующийся тем, что концентрация наночастиц диоксида титана составляет от 0,1 до 0,01%.
8. Способ по п.1, характеризующийся тем, что период времени составляет от 10 до 20 мин.
| ТУЧИНА Е.Н | |||
| Оценка фотодинамического воздействия in vitro на бактерии микробоценозов из ротовой полости и кожи человека | |||
| Автореферат кандидатской диссертации | |||
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| RU 2002128389 А, 27.04.2004 | |||
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКОГО ТОНЗИЛЛИТА | 2003 |
|
RU2235568C1 |
| RU 2006116563 A, 27.11.2007 | |||
| US 2009299441 A, 03.12.2009 | |||
| ТУЧИН В.В | |||
| и др | |||
| Фотодинамическая и селективная | |||
Авторы
Даты
2011-10-10—Публикация
2010-03-31—Подача