Текст описания приведен в факсимильном виде.



























































| название | год | авторы | номер документа |
|---|---|---|---|
| СОСТАВ НАЦЕЛЕННЫХ МИКРОВЕЗИКУЛ, НАПОЛНЕННЫХ ГАЗОМ | 2015 |
|
RU2725808C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2014 |
|
RU2690377C2 |
| МИМЕТИКИ АПОЛИПОПРОТЕИНА А-I | 2010 |
|
RU2532222C2 |
| УЛЬТРАЗВУКОВЫЕ КОНТРАСТНЫЕ ВЕЩЕСТВА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2004 |
|
RU2345793C2 |
| КОНФОРМАЦИОННО ОГРАНИЧЕННЫЕ ПЕПТИДЫ | 2020 |
|
RU2838107C2 |
| ПРИМЕНЕНИЕ МЕЛАНОКОРТИНОВ ДЛЯ ЛЕЧЕНИЯ ЧУВСТВИТЕЛЬНОСТИ К ИНСУЛИНУ | 2008 |
|
RU2453328C2 |
| ЛИГАНДЫ РЕЦЕПТОРОВ МЕЛАНОКОРТИНОВ | 2006 |
|
RU2401841C2 |
| АНАЛОГИ ПАРАТИРЕОИДНОГО ГОРМОНА ДЛЯ ЛЕЧЕНИЯ ОСТЕОПОРОЗА | 1997 |
|
RU2203286C2 |
| ЛИГАНДЫ РЕЦЕПТОРОВ МЕЛАНОКОРТИНОВ | 2006 |
|
RU2439079C2 |
| МОДУЛЯЦИЯ АКТИВНОСТИ КОМПЛЕМЕНТА | 2015 |
|
RU2778514C2 |
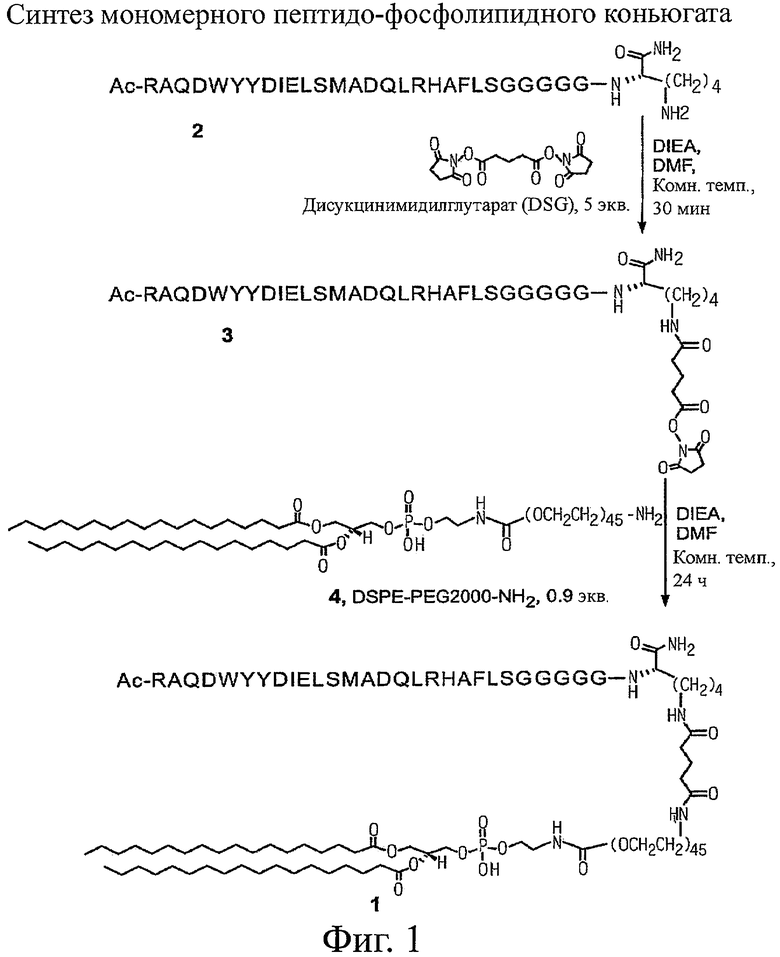
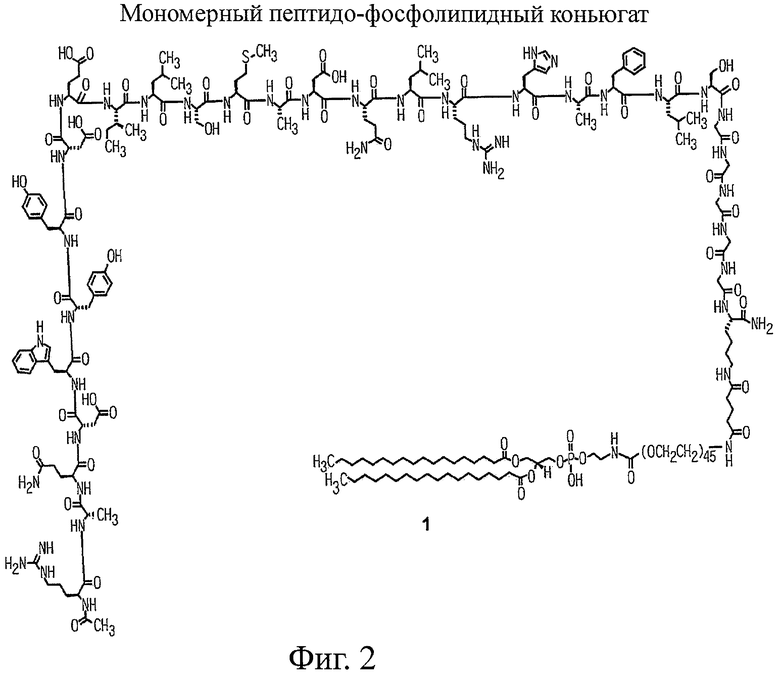
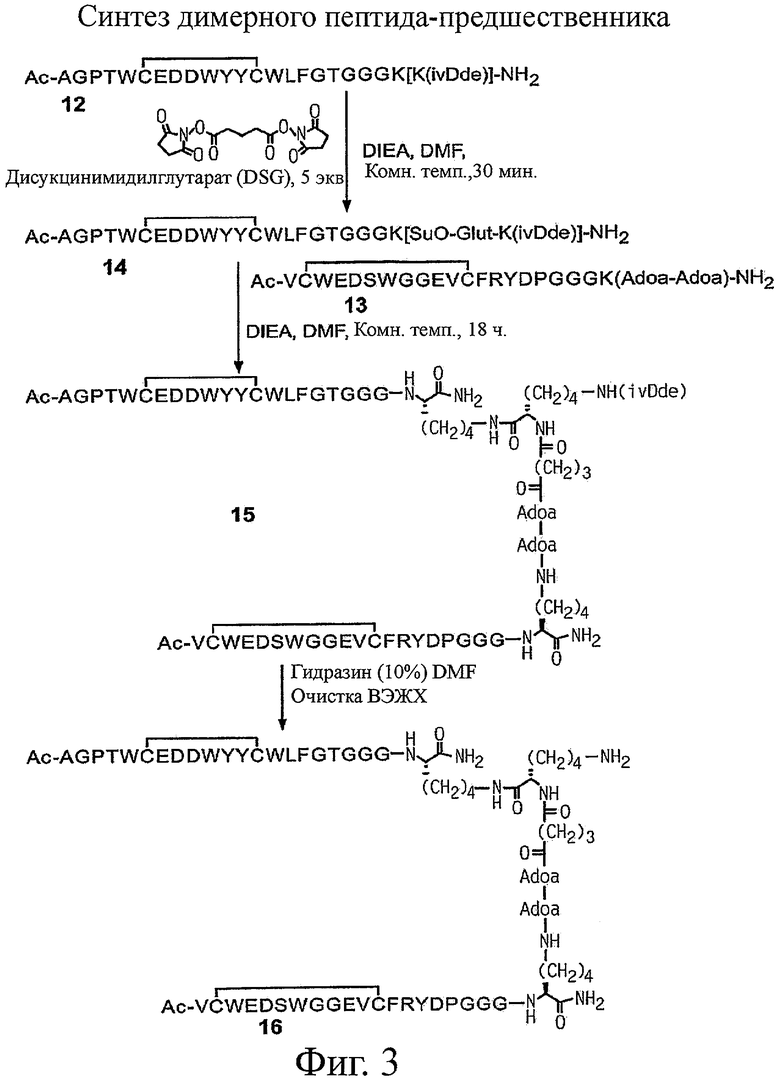
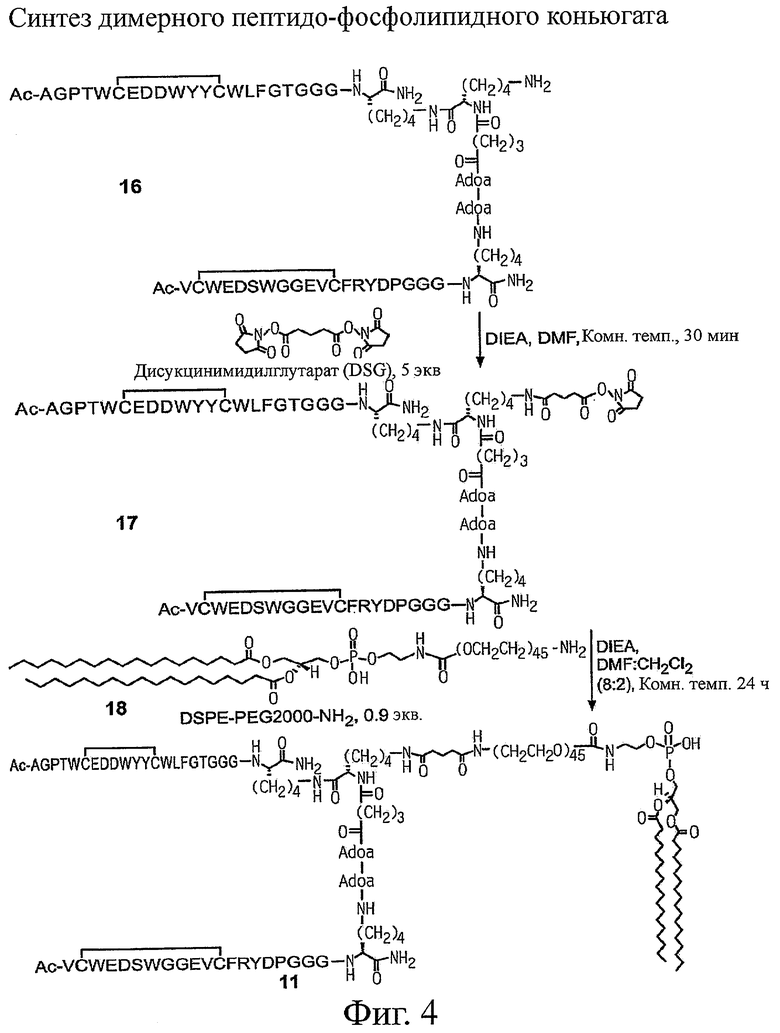
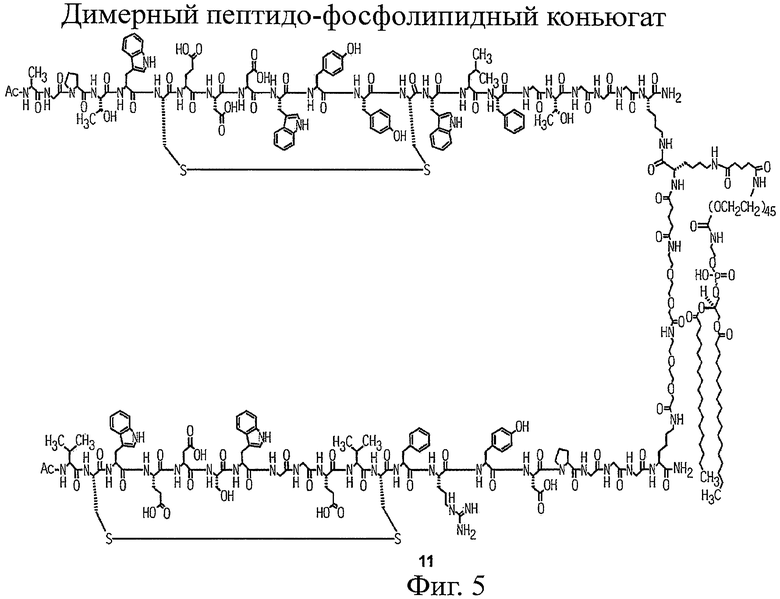
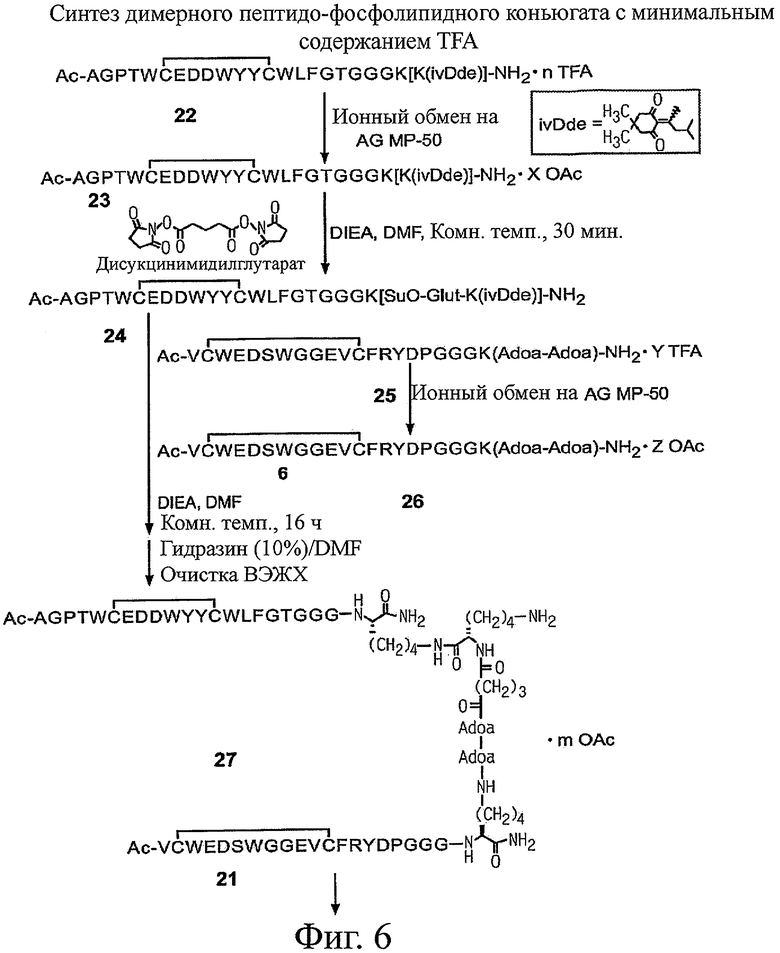
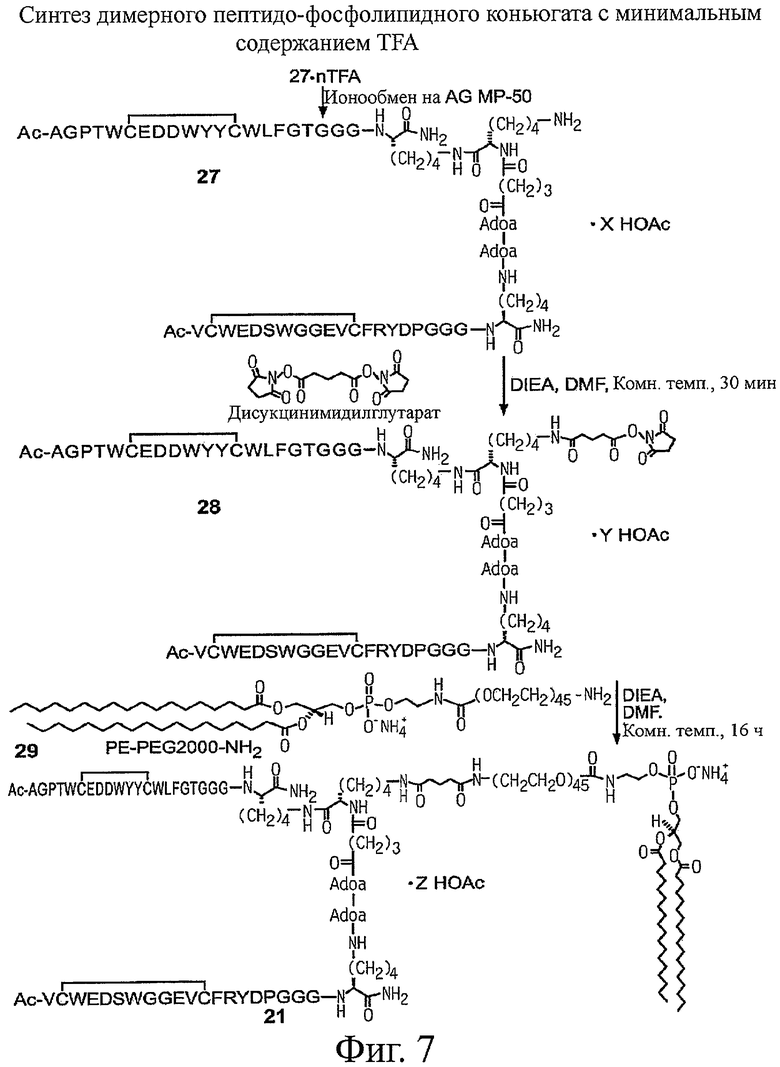
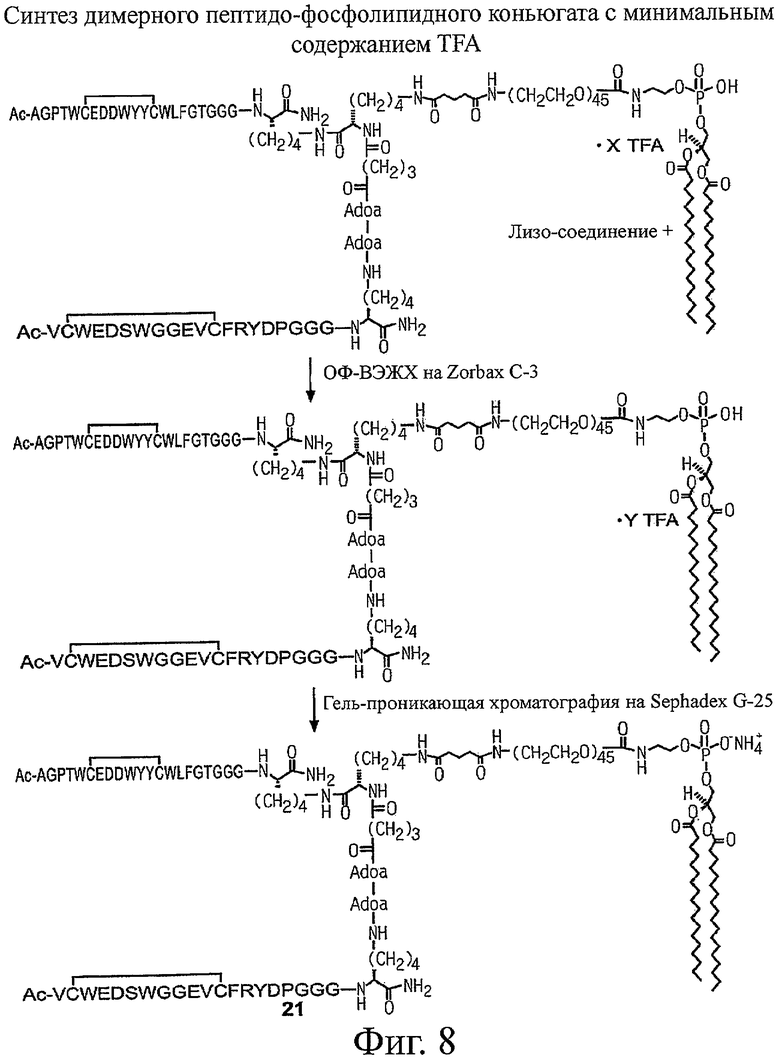
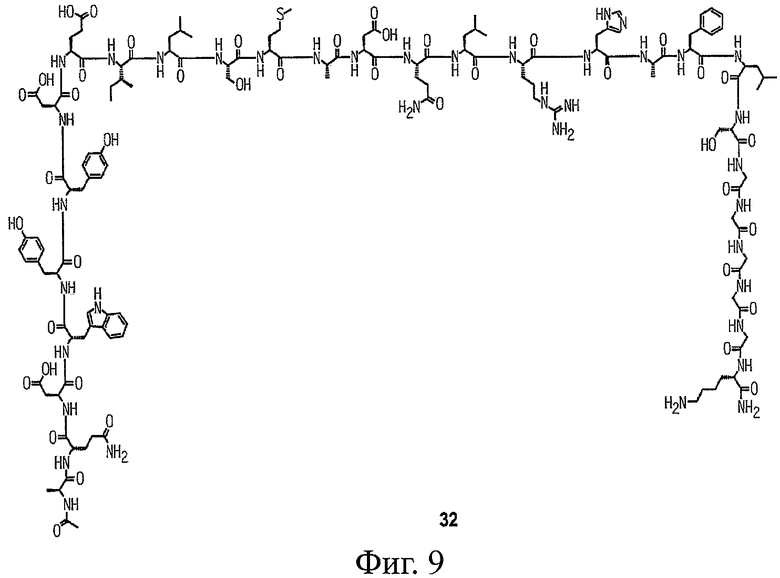
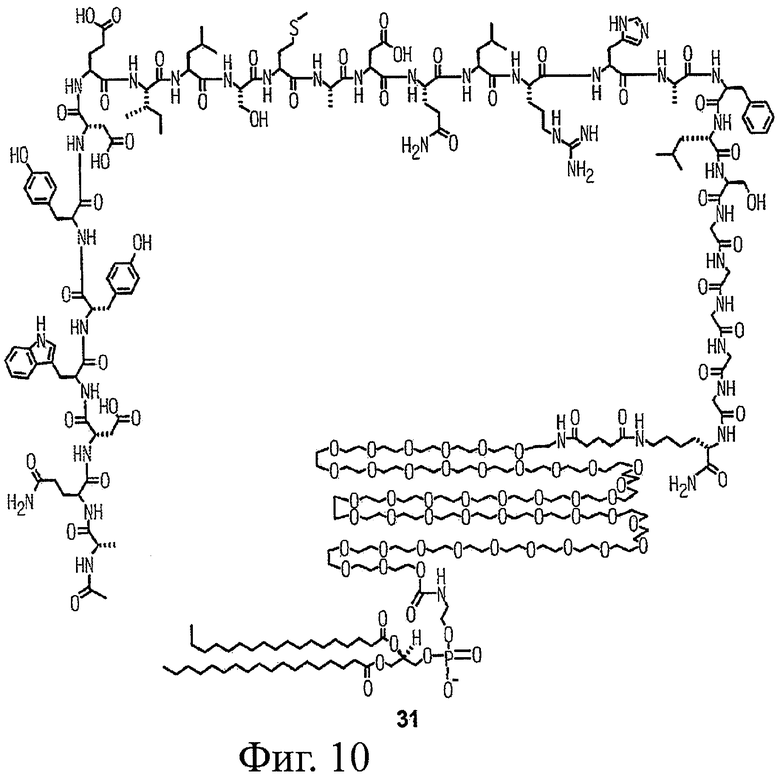






Настоящее изобретение относится к конъюгатам фосфолипидов и направляющих пептидных векторов, связывающихся с KDR с высоким сродством, а также к их способам получения. Такие пептидофосфолипидные конъюгаты могут входить в состав композиций эхоконтрастирующих агентов для УЗИ и особенно ценны в терапевтических и диагностических методах, например для визуализации KDR-содержащих тканей и для оценки и лечения ангиогенных процессов при новообразованиях. 6 н. и 27 з.п. ф-лы, 12 ил., 9 табл.
1. Пептидо-фосфолипидный конъюгат, выбранный из группы, состоящей из
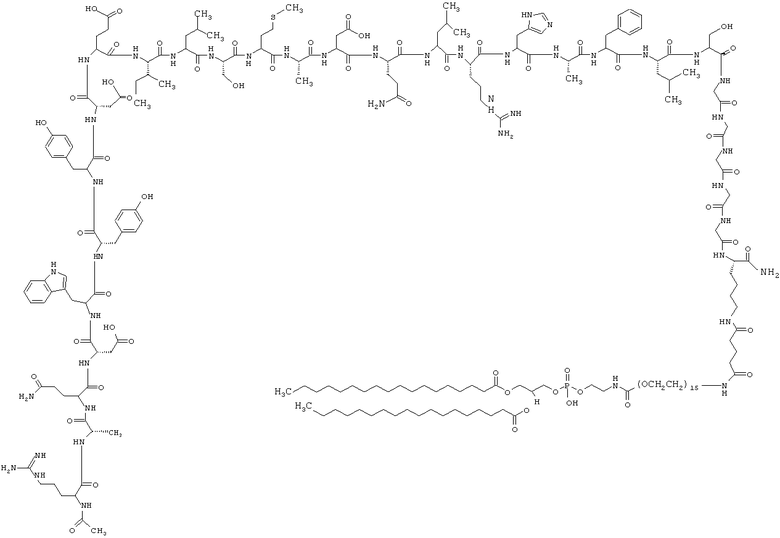
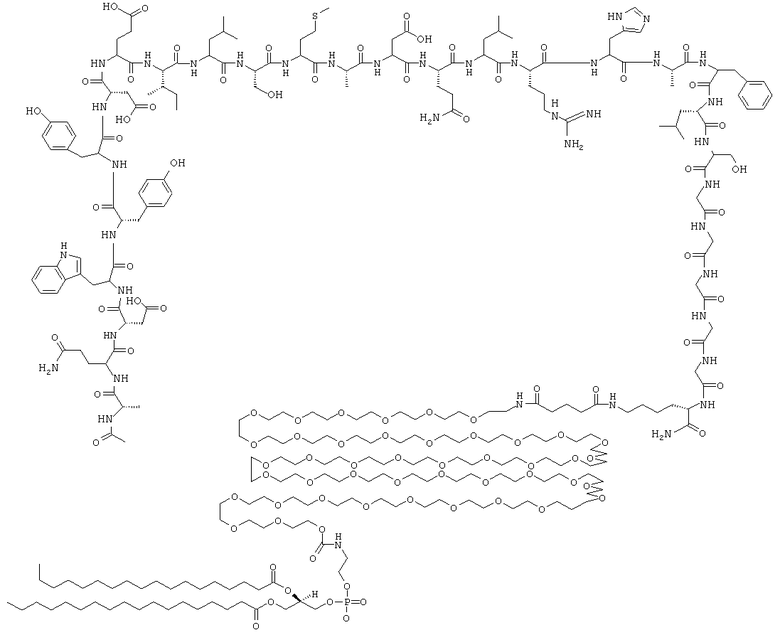
и
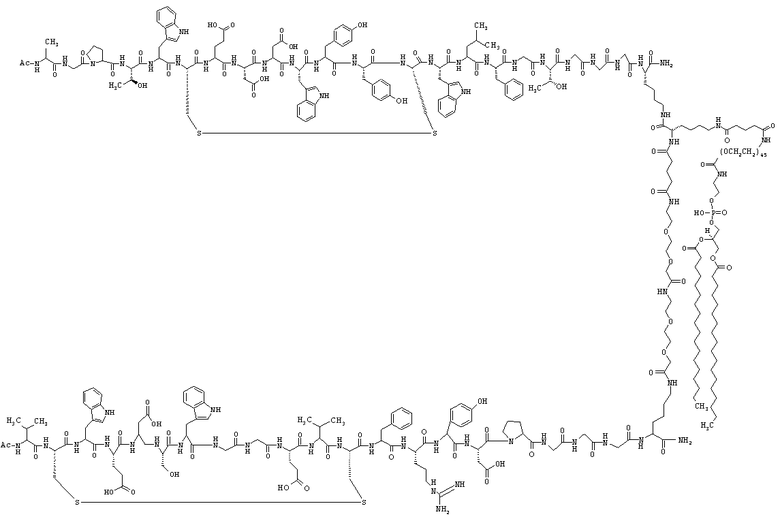
2. Композиция контрастирующего агента для ультразвукового исследования, содержащая конъюгат по п.1.
3. Композиция по п.2, где контрастирующий агент содержит инкапсулированные газовые микропузырьки.
4. Композиция по п.3, где инкапсулированные газовые микропузырьки содержат фосфолипид.
5. Композиция по п.3, где инкапсулированные газовые микропузырьки дополнительно содержат два или более компонентов, выбранных из группы, состоящей из: DSPC, DPPG, DPPA, DSPA, DPPE, DSPE-PEG1000, DSPE-PEG2000, пальмитиновой кислоты и стеариновой кислоты.
6. Композиция по п.5, где конъюгат включает Ас-AGPTWCEDDWYYCWLFGTGGGK{Ac-VCWEDSWGGEVCFRYDP-GGGK[-Adoa-Adoa-Glut-K(DSPE-PEG2000-NH-Glut)]-NH2 циклический (2-12)дисульфид}-NН2 циклический (6-13) дисульфид, и контрастирующий агент дополнительно содержит DSPC и DPPG.
7. Композиция по п.5, где конъюгат включает SEQ ID NO: 4, и контрастирующий агент дополнительно содержит DSPC и DPPG.
8. Композиция по п.5, где конъюгат включает SEQ ID NO: 4, и контрастирующий агент дополнительно содержит DSPE-PEG1000, DPPE и DPPG.
9. Композиция по п.5, где конъюгат включает Ас-AGPTWCEDDWYYCWLFGTGGGK{Ac-VCWEDSWGGEVCFRYDP-GGGK[-Adoa-Adoa-Glut-K(DSPE-PEG2000-NH-Glut)]-NH2 циклический (2-12)дисульфид}-NН2 циклический (6-13) дисульфид, и контрастирующий агент дополнительно содержит DSPE-PEG1000, DPPE и DPPG.
10. Композиция по п.5, где конъюгат включает Ас-AGPTWCEDDWYYCWLFGTGGGK{Ac-VCWEDSWGGEVCFRYDP-GGGK[-Adoa-Adoa-Glut-K(DSPE-PEG2000-NH-Glut)]-NH2 циклический (2-12)дисульфид}-NН2 циклический (6-13) дисульфид, и контрастирующий агент дополнительно содержит DSPE-PEG1000, DSPC и DSPA.
11. Композиция по п.5, где конъюгат включает SEQ ID NO: 1, и контрастирующий агент дополнительно содержит DSPE-PEG2000, DSPC и DSPA.
12. Композиция по п.5, где конъюгат включает SEQ ID NO: 1, и контрастирующий агент дополнительно содержит DSPC и DSPA.
13. Композиция по п.5, где конъюгат включает Ас-AGPTWCEDDWYYCWLFGTGGGK{Ac-VCWEDSWGGEVCFRYDP-GGGK[-Adoa-Adoa-Glut-K(DSPE-PEG2000-NH-Glut)]-NH2 циклический (2-12)дисульфид}-NН2 циклический (6-13) дисульфид, и контрастирующий агент дополнительно содержит DSPE-PEG2000, DSPC и стеарат.
14. Композиция по п.5, где конъюгат включает SEQ ID NO: 1, и контрастирующий агент дополнительно содержит DSPE-PEG2000, DSPC и стеарат.
15. Композиция по п.5, где конъюгат включает Ас-AGPTWCEDDWYYCWLFGTGGGK{Ac-VCWEDSWGGEVCFRYDP-GGGK[-Adoa-Adoa-Glut-K(DSPE-PEG2000-NH-Glut)]-NH2 циклический (2-12)дисульфид}-NН2 циклический (6-13) дисульфид, и контрастирующий агент дополнительно содержит DSPC и стеарат.
16. Композиция по п.5, где конъюгат включает Ас-AGPTWCEDDWYYCWLFGTGGGK{Ac-VCWEDSWGGEVCFRYDP-GGGK[-Adoa-Adoa-Glut-K(DSPE-PEG2000-NH-Glut)]-NH2 циклический (2-12)дисульфид}-NH2 циклический (6-13) дисульфид, и контрастирующий агент дополнительно содержит DSPE-PEG1000, DSPC и стеарат.
17. Композиция по п.5, где конъюгат включает SEQ ID NO: 1, и контрастирующий агент дополнительно содержит DSPE-PEG1000, DSPC и стеарат.
18. Композиция по п.5, дополнительно содержащая компонент, выбранный из группы, состоящей из: сахаров, полисахаридов и полиолов.
19. Композиция по п.18, где упомянутый компонент выбран из группы, состоящей из маннита, декстрана и полиэтиленгликоля.
20. Композиция по п.18, где упомянутый газ включает фторированный газ.
21. Композиция по п.3, где газ включает С3F8, C4F10 или SF6, при необходимости в смеси с воздухом, азотом, кислородом или углекислым газом.
22. Пептид-мономер, содержащий Ac-Arg-Ala-Gln-Asp-Trp-Tyr-Tyr-Asp-Glu-Ile-Leu-Ser-Met-Ala-Asp-Gln-Leu-Arg-His-Ala-Phe-Leu-Ser-Gly-Gly-Gly-Gly-Gly-Lys-NH2.
23. Композиция контрастирующего агента для ультразвукового исследования, включающая липопептид, содержащий один или более
мономеров, выбранных из группы, состоящей из Ac-Arg-Ala-Gln-Asp-Trp-Tyr-Tyr-Asp-Glu-Ile-Leu-Ser-Met-Ala-Asp-Gln-Leu-Arg-His-Ala-Phe-Leu-Ser-Gly-Gly-Gly-Gly-Gly-Lys-NH2, Ac-Ala-Gln-Asp-Trp-Tyr-Tyr-Asp-Glu-Ile-Leu-Ser-Met-Ala-Asp-Gln-Leu-Arg-His-Ala-Phe-Leu-Ser-Gly-Gly-Gly-Gly-Gly-Lys-NH2, Ас-Аlа-Glу-Рrо-Thr-Trp-Суs-Glu-Аsр-Аsр-Trp-Туr-Туr-Cys-Trp-Leu-Phe-Gly-Thr-Gly-Gly-Gly-Lys(ivDde)-NH2 циклический (6-13) дисульфид, Ас-Val-Cys-Trp-Glu-Asp-Ser-Trp-Gly-Gly-Glu-Val-Cys-Рhe-Аrg-Tyr-Asp-Pro-Gly-Gly-Gly-Lys(Adoa-Adoa)-NH2 циклический(2-12) дисульфид.
24. Композиция по п.23, где контрастирующий агент содержит инкапсулированные газовые микропузырьки.
25. Композиция по п.24, где упомянутый газ включает фторированный газ.
26. Композиция по п.25, дополнительно содержащая фосфолипид.
27. Композиция по п.26, дополнительно содержащая два или более компонентов, выбранных из группы, состоящей из DSPC, DPPG, DPPA, DSPA, DPPE, DSPE-PEG1000, DSPE-PEG2000, пальмитиновой кислоты и стеариновой кислоты.
28. Композиция по п.27, где газ включает С3F8, C4F10 или SF6, при необходимости в смеси с воздухом, азотом, кислородом или углекислым газом.
29. Способ получения инкапсулированных газовых микропузырьков, содержащих фосфолипид, который включает следующие стадии:
a) получение водоорганической эмульсии, содержащей i) водную среду, включающую воду, ii) органический растворитель, практически не смешивающийся с водой, iii) фосфолипид, iv) пептидо-фосфолипидный конъюгат по п.1 и v) лиопротектор;
b) лиофилизация упомянутой эмульсии для получения лиофилизованного матрикса, содержащего упомянутый фосфолипид;
c) контактирование упомянутого лиофилизованного матрикса с биосовместимым газом;
d) восстановление упомянутого лиофилизованного матрикса путем растворения его в физиологически приемлемом водном жидком носителе для получения суспензии упомянутых инкапсулированных газовых микропузырьков.
30. Способ по п.29, где стадия а) включает следующие стадии:
a) получение водной суспензии, содержащей PEG-илированный фосфолипид и конъюгат по п.1;
b) получение водоорганической эмульсии, содержащей водную среду, органический растворитель, фосфолипид и лиопротектор;
c) смешивание упомянутой водной суспензии со стадии a1 с эмульсией со стадии а2.
31. Способ получения пептидо-фосфолипидного конъюгата, включающий конъюгирование пептида, выбранного из группы, состоящей из: SEQ ID NO: 2, Ac-AGPTWCEDDWYYCWLFGTGGGK[K(ivDde)]-NH2 циклический(6-13)дисульфид, Ac-VCWEDSWGGEVCFRYDPGGGK(Adoa-Adoa)-NH2 циклический(2-12)дисульфид, SEQ ID NO: 5 и Ac-AGPTWCEDDWYYCWLFGTGGGK[Ac-
VCWEDSWGGEVCFRYDPGGGK(-Adoa-Adoa-Glut-K)-NH2 циклический (2-12)дисульфид]-NН2 циклический (6-13) дисульфид, с фосфолипидом.
32. Способ по п.31, где фосфолипидом является DSPE-PEG2000-NH2.
33. Способ по п.32, где конъюгация включает реакцию между моно-NHS-эфиром пептида со свободной аминогруппой соли фосфолипида.
| US 2005100963 A1, 12.05.2005 | |||
| WO 03074005 А2, 12.09.2003 | |||
| US 2005147555 A1, 07.07.2005 | |||
| WO9640285 Al, 19.12.1996 | |||
| US 2005250700 A1, 10.11.2005 | |||
| RU 2005127634 C2, 20.01.2006. |
Авторы
Даты
2011-11-10—Публикация
2006-12-08—Подача