Описание предшествующего уровня техники
Настоящее изобретение относится к пептидам, которые являются лигандами одного или более рецепторов меланокортинов (MC-R), их фармацевтически приемлемым солям, способам применения таких пептидов для лечения млекопитающих и к полезным фармацевтическим композициям, включающим указанные пептиды.
Меланокортины представляют собой семейство регуляторных пептидов, которые образуются путем посттрансляционной обработки про-гормона про-опиомеланокортина (РОМС; длиной 131 аминокислот). РОМС обрабатывается в 3 класса гормонов: меланокортины, адренокортикотропный гормон и различные эндорфины (например, липотропин) (Cone, et al., Recent Prog. Horm. Res., 51:287-317, (1996); Cone et al., Ann. N.Y. Acad. Sci., 31:342-363, (1993)).
Меланокортины были обнаружены в широком разнообразии нормальных человеческих тканей, включая мозг, надпочечники, кожу, семенники, селезенку, почки, яичники, легкие, щитовидную железу, печень, толстую кишку, тонкую кишку и поджелудочную железу (Tatro, J. B. et al., Endocrinol. 121:1900-1907 (1987); Mountjoy, K. G. et al., Science 257:1248-1251 (1992); Chhajlani, V. et al., FEBS Lett. 309:417-420 (1992); Gantz, I. et al. J. Biol. Chem. 268:8246-8250 (1993) и Gantz, I. et al., J. Biol. Chem. 268:15174-15179 (1993)).
Было показано, что пептиды меланокортинов проявляют широкое разнообразие видов физиологической активности, включая регуляцию поведения и памяти, с воздействием на нейротропные и антипиретические свойства, а также с воздействием на модуляцию иммунной системы. Было также показано, что меланокортины, кроме их хорошо известных воздействий на функции коры надпочечников (адернокортикотропный гормон, АКТГ) и на меланоциты (меланоцит-стимулирующий гормон, МСГ), регулируют сердечно-сосудистую систему, анальгезию, терморегуляцию и высвобождение других нейрогуморальных агентов, включая пролактин, лютеинизирующий гормон и биогенные амины (De Wied, D. et al., Methods Achiev. Exp. Pathol. 15:167-199 (1991); De Wied, D. et al., Physiol. Rev. 62:977-1059 (1982); Guber, K.A. et al., Am. J. Physiol. 257:R681-R694 (1989); Walker J.M. et al., Science 210:1247-1249 (1980); Murphy, M. T. et al., Science 221:192-193 (1983); Ellerkmann, E. et al., Endocrinol. 130:133-138 (1992) и Versteeg, D. H. G. et al., Life Sci. 38:835-840 (1986)).
Было также показано, что участки связывания меланокортинов распределены во многих различных типах тканей, включая слезные и подчелюстные железы, поджелудочную железу, жировую ткань, мочевой пузырь, 12-персную кишку, селезенку, мозг и ткани половых желез, а также в злокачественных меланомных опухолях. К настоящему времени охарактеризованы 5 рецепторов меланокортинов (MC-R). Они включают меланоцит-специфический рецептор (MC1-R), специфичный для коры надпочечников рецептор АКТГ (MC2-R), рецептор меланокортина-3 (MC3-R), меланокортина-4 (MC4-R) и меланокортина-5 (MC5-R). Все рецепторы меланокортина реагируют на класс пептидных гормонов, стимулирующих мелоноциты (MSH) (Cone, R. D. et al., Ann. N.Y. Acad. Sci., 680:342-363 (1993); Cone, R. D. et al., Recent Prog. Horm. Res., 51:287-318 (1996)).
MC1-R, известный в данной области как рецептор гормона, стимулирующего меланоциты (MSH-R), рецептор меланотропина или рецептор меланокортина-1, представляет собой трансмембранный белок из 315 аминокислот, относящийся к семейству рецепторов, связанных с G-белком. MC1-R представляет собой рецептор и для MSH, и для АКТГ. Активность MC1-R опосредована G-белками, которые активируют аденилатциклазу. Рецепторы MC1-R обнаруживаются в меланоцитах и ткани коры надпочечников, а также в различных других тканях, таких как надпочечники, лейкоциты, легкие, лимфоузлы, яичники, семенники, гипофиз, плацента, селезенка и матка. MC2-R, также называемый рецептором адренокортикотропного гормона (ACTH-R), представляет собой трансмембранный белок из 297 аминокислот, обнаруживаемый в меланоцитах и ткани коры надпочечников. MC2-R опосредует кортикотропный эффект АКТГ. У людей MC3-R представляет собой белок из 360 аминокислот, обнаруживаемый в мозговой ткани; у мышей и крыс MC3-R представляет собой белок из 323 аминокислот. MC4-R представляет собой трансмембранный белок из 332 аминокислот, который также экспрессирован в мозге, а также в тканях плаценты и кишечника. MC5-R представляет собой трансмембранный белок из 325 аминокислот, экспрессированный в надпочечниках, желудке, легких и селезенке и на очень низких уровнях в мозге. MC5-R также экспрессирован в трех слоях коры надпочечников, преимущественно в клетках гломерулезной зоны, продуцирующих альдостерон.
Однако пять известных рецепторов меланокортина различаются по функциям. Например, MC1-R представляет собой G-белок, который регулирует пигментацию в ответ на α-MSH, мощный агонист MC1-R. Агонизм рецептора MC1-R приводит к стимуляции меланоцитов, что вызывает образование эумеланина и увеличивает риск рака кожи. Агонизм MC1-R может также оказывать неврологические эффекты. Стимуляция активности MC2-R может привести к карциноме ткани надпочечников. Недавнее фармакологическое подтверждение установило, что центральные рецепторы MC4-R представляют собой первичные медиаторы анорексических и орексигенических воздействий, о которых сообщалось в отношении соответственно агонистов и антагонистов меланокортина. Эффекты агонизма MC3-R и MC5-R еще не известны.
Проявлялся большой интерес к рецепторам меланокортина (MC-R) как мишеням для разработки новых терапевтических средств для лечения расстройств массы тела, таких как ожирение и кахексия. И генетические, и фармакологические доказательства указывают на центральные рецепторы MC4-R как основную мишень (Giraudo, S. Q. et al., Brain Res., 809:302-306 (1998); Farooqi, I. S. et al., NE J Med., 348:1085-1095 (2003); MacNeil, D. J. et al., Eu. J. Pharm., 44:141-157 (2002); MacNeil, D. J. et al., Eu. J. Pharm., 450:93-109 (2002); Kask, A. et al., NeuroReport, 10:707-711 (1999)). Современные достижения в разработке селективных в отношении рецепторов агонистов и антагонистов свидетельствует о терапевтическом потенциале активации рецепторов меланокортина, в частности MC4-R.
Агонистические, анатагонистические или другие лигандные соединения, активирующие один или более рецептор меланокортина, могли бы использоваться для лечения широкого разнообразия показаний у субъекта, нуждающегося в них, или с риском их развития, включая острые и хронические воспалительные заболевания, такие как общее воспаление (U.S. Patent No. 6613874; Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), воспалительное заболевание кишечника (патент США №6713487; Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), энцефалит (Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), сепсис (патент США №6613874; патент США №6713487; Catania, A. et al., Pharm. Rev., 56:1-29 (2004)) и септический шок (патент США №6613874; Catania, A. et al., Pharm. Rev., 56:1-29 (2004)); заболевания с аутоиммунным компонентом, такие как ревматоидный артрит (патент США №6713487; Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), подагрический артрит (Catania, A. et al., Pharm. Rev., 56:1-29 (2004), Getting, S. J. et al., Curr. Opin. Investig. Drugs, 2:1064-1069 (2001)) и рассеянный склероз (патент США №6713487); метаболические заболевания и медицинские состояния, сопровождающиеся прибавкой массы тела, такие как ожирение (патент США №6613874; патент США №6600015; Fehm, H. L. et al., J. Clin. Endo. & Metab., 86:1144-1148 (2001); Hansen, M. J. et al., Brain Res., 1039:137-145 (2005); Ye, Z. et al., Peptides, 26:2017-2025 (2005); Farooqi, I. S. et al., NE J Med., 348:1085-1095 (2003); MacNeil, D. J. et al., Eu. J. Pharm., 44:141-157 (2002); MacNeil, D. J. et al., Eu. J. Pharm., 450:93-109 (2002); Kask, A. et al., NeuroReport, 10:707-711 (1999); Schwartz, A. W., J. Clin. Invest., 108:963-964 (2001), Gura, Т., Science, 287:1738-1740 (2000), Raffin-Sanson, M. L., Eu. J. Endo., 144:207-208 (2001), Hamilton, B. S. et al., Obesity Res. 10:182-187 (2002)), feeding disorders (патент США No. 6720324; Fehm, H. L. et al., J. Clin. Endo. & Metab., 86:1144-1148 (2001); Pontillo, J. et al., Bioorganic & Med. Chem. Ltrs., 15:2541-2546 (2005)) и Prader-Willi Syndrome (GE, Y. et al., Brain Research, 957:42-45 (2002)); метаболические заболевания и медицинские состояния, сопровождающиеся потерей массы тела, такие как анорексия (патент США №6613874; Wisse, B.R. et al., Endo., 142:3292-3301 (2001)), булимия (патент США №6720324), истощение при СПИДе (Marsilje, T. H. et al., Bioorg. Med. Chem. Lett., 14:3721-3725 (2004); Markison, S. et al., Endocrinology, 146:2766-2773 (2005)), кахексия (патент США №6613874; Lechan, R. M. et al., Endo., 142:3288-3291 (2001); Pontillo, J. et al., Bioorganic & Med. Chem. Ltrs., 15:2541-2546 (2005)), раковая кахексия (патент США №6639123) и алиментарная дистрофия у истощенных пожилых лиц (патент США №6639123); диабет (патент США №6713487) и связанные с диабетом состояния и осложнения диабета, такие как ретинопатия (патент США №6525019); неопластическая пролиферация (патент США №6713487), такая как рак кожи (Sturm, R.A., Melanoma Res., 12:405-416 (2002); Bastiens, M. T. et al., Am. J. Hum. Genet., 68:884-894 (2001)), и рак предстательной железы (Luscombe, C.J. et al., British J. Cancer, 85:1504-1509 (2001); репродуктивные или половые медицинские состояния, такие как эндометриоз (патент США №6713487), и маточное кровотечение у женщин (патент США №6613874), половая дисфункция (патент США №6720324; Van der Ploeg, L. H. T. et al., PNAS, 99:11381-11386 (2002), Molinoff, P. B. et al., Ann. N.Y. Acad. Sci., 994:96-102 (2003), Hopps, С. V. et al., BJU International, 92:534-538 (2003)), эректильная дисфункция (патент США №6613874; Diamond, L. E. et al., Urology, 5:755-759 (2005), Wessells, H. et al., Int. J. Impotence Res., 12:S74-S79 (2000), Andersson, K-E. et al., Int. J. Impotence Res., 14:S82-S92 (2002), Bertolini, A. et. al., Sexual Behavior: Pharmacology and Biochemistry, Raven Press, NY, p 247-257 (1975); Wessells, H. et al, Neuroscience, 118:755-762 (2003), Wessells, H. et al., Urology, 56:641-646 (2000), Shadiack, A. M. et al., Society for Neuroscience Abstract, (2003); Wessells, H. et al., J. Urology, 160:389-393 (1998), Rosen, R. С et al., Int. J. Impotence Res., 16:135-142 (2004), Wessells, H. et al., Peptides, 26:1972-1977 (2005)) и сниженная сексуальная реакция у женщин (патент США №6713487; Fourcroy, J.L., Drugs, 63:1445-1457 (2003)); заболевания или состояния, возникающие в результате лечения или повреждающего воздействия на организм, такого как отторжение органного трансплантата (патент США №6713487; Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), ишемическое и реперфузионное повреждение (Mioni, C. et al., Eu. J. Pharm. 477:227-234 (2003); Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), лечение травм спинного мозга и для ускорения заживления ран (Sharma H. S. et al., Acta. Nerochir. Suppl., 86:399-405 (2003); Sharma H. S., Ann. N.Y. Acad. Sci. 1053: 407-421 (2005); патент США №6525019), а также потеря массы тела, вызванная химиотерапией, лучевой терапией, временной или постоянной иммобилизацией (Harris, R. B. et al., Physiol. Behav., 73:599-608 (2001)) или диализом; сердечно-сосудистые заболевания или состояния, такие как геморрагической шок (Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), кардиогенный шок (патент США №6613874), гиповолемический шок (патент США №6613874), сердечно-сосудистые расстройства (патент США №6613874) и сердечная кахексия (Markison, S. et al., Endocrinology, 146:2766-2773 (2005); легочные заболевания или состояния, такие как острый респираторный дистресс-синдром (патент США №6350430; Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), хроническое обструктивное легочное заболевание (патент США №6713487), астма (патент США №6713487) и пневмофиброз; для усиления иммунной толерантности (Luger, T. A. et al., Pathobiology, 67:319-321 (1999)) и для борьбы с атаками на иммунную систему, такими как воздействия, связанные с определенными видами аллергии (патент США №6713487) или отторжением органных трансплантатов (патент США №6713487; Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), лечение дерматологических заболеваний и состояний, таких как псориаз (патент США №6713487), истощение пигментации кожи (патент США №6713487; Ye, Z. et al., Peptides, 26:2017-2025 (2005), угри (Hatta, N. et al., J. Invest. Dermatol., 116:564-570 (2001); Bohm, M. et al., J. Invest. Dermatol., 118:533-539 (2002)), образование келоидов (патент США №6525019) и рак кожи (Sturm, R.A., Melanoma Res., 12:405-416 (2002); Bastiens, M. T. et al., Am. J. Hum. Genet., 68:884-894 (2001)); поведенческие расстройства и состояния и расстройства центральной нервной системы, такие как тревога (патент США №6720324; Pontillo, J. et al., Bioorganic & Med. Chem. Ltrs., 15:2541-2546 (2005)), депрессия (Chaki, S. et al., Peptides, 26:1952-1964 (2005), Bednarek, M. A. et al., Expert Opinion Ther. Patents, 14:327-336 (2004); патент США №6720324), расстройства и дисфункция памяти (патент США №6613874; Voisey, J. et al., Curr. Drug Targets, 4:586-597 (2003)), модуляция восприятия боли (патент США №6613874; Bertolini, A. et al., J. Endocrinol. Invest, 4:241-251 (1981); Vrinten, D. et al., J. Neuroscience, 20:8131-8137 (2000)) и лечение нейропатической боли (Pontillo, J. Et al., Bioorganic & Med. Chem. Ltrs., 15:2541-2546 (2005)); состояния и заболевания, связанные с употреблением алкоголя, злоупотреблением алкоголем и/или алкоголизмом (WO 05/060985; Navarro, M. et al., Alcohol Clin. Exp. Res., 29:949-957 (2005)); и почечные состояния или заболевания, такие как лечение почечной кахексии (Markison, S. Et al., Endocrinology, 146:2766-2773 (2005) или натриурез (патент США №6613874).
Лигандные соединения, активирующие один или более рецепторов меланокортина, были бы полезны для моделирования широкого разнообразия нормализующей или гомеостатической активности у нуждающегося в них субъекта, что включает высвобождение тироксина (патент США №6613874), синтез и высвобождение альдостерона (патент США №6613874), температуру тела (патент США №6613874), артериальное давление (патент США №6613874), частоту сердечных сокращений (патент США №6613874), сосудистый тонус (патент США №6613874), мозговой кровоток (патент США №6613874), уровни глюкозы в крови (патент США №6613874), костный метаболизм, образование или развитие костной ткани (Dumont, L. M. et al., Peptides, 26:1929-1935 (2005), массу яичников (патент США №6613874), развитие плаценты (патент США №6613874), секрецию пролактина и ФСГ (патент США №6613874), внутриматочный рост плода (патент США №6613874), роды (патент США №6613874), сперматогенез (патент США №6613874), секрецию сала и феромонов (патент США №6613874), нейропротекцию (патент США №6639123) и рост нервов (патент США №6613874), а также модуляцию мотивации (патент США №6613874), обучение (патент США №6613874) и другие виды поведения (патент США №6613874).
Поэтому целью настоящего изобретения является предоставление лигандов для рецепторов меланокортина, которые проявляют большую устойчивость и селективность к рецепторам меланокорнина, чем нативные лиганды рецепторов меланокортина.
Краткое описание сущности изобретения
В одном аспекте, настоящее изобретение направлено на соединение в соответствии с формулой (I):
(R2R3)-A1-c(A2-A3-A4-A5-A6-A7-A8-A9)-A10-R1,
где:
А1 представляет собой Асс, HN-(CH2)m-C(O), L- или D-аминокислоту или подвергнут делеции;
А2 представляет собой Cys, D-Cys, hCys, D-hCys, Pen, D-Pen, Asp или Glu;
А3 представляет собой Gly, Ala, β-Ala, Gaba, Aib, D-аминокислоту или подвергнут делеции;
А4 представляет собой His, 2-Pal, 3-Pal, 4-Pal, Taz, 2-Thi, 3-Thi или (X1,X2,X3,X4,X5)Phe;
А5 представляет собой D-Phe, D-1-Nal, D-2-Nal, D-Trp, D-Bal, D-(X1,X2,X3,X4,X5)Phe, L-Phe или D-(Et)Tyr;
А6 представляет собой Arg, hArg, Dab, Dap, Lys, Orn, или HN-CH((CH2)n-N(R4R5))-C(O);
А7 представляет собой Trp, 1-Nal, 2-Nal, Bal, Bip, D-Trp, D-1-Nal, D-2-Nal, D-Bal или D-Bip;
А8 представляет собой Gly, D-Ala, Acc, Ala, β-Ala, Gaba, Apn, Ahx, Aha, HN-(CH2)s-C(O) или подвергнут делеции;
А9 представляет собой Cys, D-Cys, hCys, D-hCys, Pen, D-Pen, Dab, Dap, Orn или Lys;
А10 представляет собой Асс, HN-(CH2)t-C(O), L- или D-аминокислоту или подвергнут делеции;
R1 представляет собой -OH или NH2;
каждый из R2 и R3 независимо для каждого случая выбран из группы, состоящей из Н, (С1-С30)алкила, (С1-С30)гетероалкила, (С1-С30)ацила, (С2-С30)алкенила, (С2-С30)алкинила, арил(С1-С30)алкила, арил(С1-С30)ацила, замещенного (С1-С30)алкила, замещенного (С1-С30)гетероалкила, замещенного (С1-С30)ацила, замещенного (С2-С30)алкенила, замещенного (С2-С30)алкинила, замещенного арил(С1-С30)алкила и замещенного арил(С1-С30)ацила;
каждый из R4 и R5 независимо для каждого случая представляет собой Н, (С1-С40)алкил, (С1-С40)гетероалкил, (С1-С40)ацил, (С2-С40)алкенил, (С2-С40)алкинил, арил(С1-С40)алкил, арил(С1-С40)ацил, замещенный (С1-С40)алкил, замещенный (С1-С40)гетероалкил, замещенный (С1-С40)ацил, замещенный (С2-С40)алкенил, замещенный (С2-С40)алкинил, замещенный арил(С1-С40)алкил, замещенный арил(С1-С40)ацил, (С1-С40)алкилсульфонил или -C(NH)-NH2;
m независимо для каждого случая = 1, 2, 3, 4, 5, 6 или 7;
n независимо для каждого случая = 1, 2, 3, 4 или 5;
s независимо для каждого случая = 1, 2, 3, 4, 5, 6 или 7;
t независимо для каждого случая = 1, 2, 3, 4, 5, 6 или 7;
каждый из X1, X2, X3, X4 и X5 независимо для каждого случая представляет собой H, F, Cl, Br, I, (С1-С10)алкил, замещенный (С1-С10)алкил, (С2-С10)алкенил, замещенный (С2-С10)алкенил, (С2-С10)алкинил, замещенный (С2-С10)алкинил, арил, замещенный арил, OH, NH2, NO2 или CN;
при условии, что
(I) когда R4 представляет собой (С1-С40)ацил, арил(С1-С40)ацил, замещенный (С1-С40)ацил, замещенный арил(С1-С40)ацил, (С1-С40)алкилсульфонил или -C(NH)-NH2, тогда R5 представляет собой (С1-С40)алкил, (С1-С40)гетероалкил, (С2-С40)алкенил, (С2-С40)алкинил, арил(С1-С40)алкил, замещенный (С1-С40)алкил, замещенный (С1-С40)гетероалкил, замещенный (С2-С40)алкенил, замещенный (С2-С40)алкинил или замещенный арил(С1-С40)алкил;
(II) когда R2 представляет собой (С1-С30)ацил, арил(С1-С30)ацил, замещенный (С1-С30)ацил, или замещенный арил(С1-С30)ацил, тогда R3 представляет собой Н, (С1-С30)алкил, (С1-С30)гетероалкил, (С2-С30)алкенил, (С2-С30)алкинил, арил(С1-С30)алкил, замещенный (С1-С30)алкил, замещенный (С1-С30)гетероалкил, замещенный (С2-С30)алкенил, замещенный (С2-С30)алкинил или замещенный арил(С1-С30)алкил;
(III) любой из А3 и А8 или они оба должны присутствовать в указанном соединении;
(IV) когда А2 представляет собой Cys, D-Cys, hCys, D-hCys, Pen, или D-Pen, тогда А9 представляет собой Cys, D-Cys, hCys, D-hCys, Pen, или D-Pen;
(V) когда А2 представляет собой Asp или Glu, тогда А9 представляет собой Dab, Dap, Orn или Lys;
(VI) когда А8 представляет собой Ala или Gly, тогда А1 не представляет собой Nle; и
(VII) когда А1 подвергнут делеции, тогда R2 и R3 не могут оба представлять собой Н;
или его фармацевтически приемлемую соль.
Предпочтительная группа соединений непосредственно выше представленной формулы представляет собой ту, в которой А1 представляет собой A6c, Gaba, Nle, Met, Phe, D-Phe, D-2-Nal, hPhe, Chg, D-Chg, Cha, hCha, hPro, hLeu, Nip, β-hMet, или Oic;
А2 представляет собой Cys, D-Cys, hCys, D-hCys, Pen, D-Pen, Asp или Glu;
А3 представляет собой Gly, Ala, D-Ala, D-Glu, β-Ala, Gaba, Aib или подвергнут делеции;
А4 представляет собой His;
А5 представляет собой D-Phe, D-1-Nal, D-2-Nal, D-Trp, D-Bal, или D-(Et)Tyr;
А6 представляет собой Arg или hArg;
А7 представляет собой Trp, Bip, D-Trp, 1-Nal или 2-Nal;
А8 представляет собой A6c, Ala, β-Ala, Gaba, Apn или Ahx;
А9 представляет собой Cys, D-Cys, hCys, D-hCys, Pen, D-Pen или Lys;
А10 представляет собой Thr или подвергнут делеции,
или его фармацевтически приемлемую соль.
Предпочтительная группа соединений непосредственно выше представленной формулы представляет собой ту, в которой каждый из R2 и R3 независимо представляет собой Н, ацил, н-пропаноил или н-бутаноил или его фармацевтически приемлемую соль.
Более предпочтительное соединение формулы (I) представляет собой то, где указанное соединение имеет формулу:
А1 представляет собой Асс, Arg, D-Arg, Cha, D-Cha, hCha, Chg, D-Chg, Gaba, Ile, Leu, hLeu, β-hMet, 2-Nal, D-2-Nal, Nip, Nle, Oic, Phe, D-Phe, hPhe, hPro, Val или подвергнут делеции;
А2 представляет собой Cys, D-Cys, Pen или Asp;
А3 представляет собой Gly, Ala, β-Ala, Gaba, Aib, D-Ala, D-Abu, D-Cha, D-Ile, D-Leu, D-Tle, D-Val или подвергнут делеции;
А4 представляет собой His или 3-Pal;
А5 представляет собой D-Phe, D-2-Nal или D-(Et)Tyr;
А6 представляет собой Arg или hArg;
А7 представляет собой Trp, 1-Nal, 2-Nal, Bal, Bip или D-Trp;
А8 представляет собой Gly, D-Ala, Acc, Ala, β-Ala, Gaba, Apn, Ahx, Aha или подвергнут делеции;
А9 представляет собой Cys, D-Cys, Pen или Lys;
А10 представляет собой Thr или подвергнут делеции;
где, по меньшей мере, один из А3 или А8 подвергнут делеции, но не оба,
или его фармацевтически приемлемую соль.
Более предпочтительное соединение представленной непосредственно выше группы соединений представляет собой соединение, имеющее формулу:
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-β-Ala-Lys)-NH2; SEQ ID NO:1
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-A6c-Lys)-NH2; SEQ ID NO:1
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Ahx-Cys)-NH2; SEQ ID NO:2
D-Phe-c(Cys-His-D-Phe-Arg-Trp-Ala-D-Cys)-Thr-NH2; SEQ ID NO:3
D-Phe-c(Cys-His-D-Phe-Arg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:3
D-Phe-c(Cys-His-D-Phe-Arg-Trp-Gaba-D-Cys)-Thr-NH2; SEQ ID NO:3
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Apn-Cys)-NH2; SEQ ID NO:2
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-Apn-Lys)-NH2; SEQ ID NO:4
Ac-A6c-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:5
Ac-D-2-Nal-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:6
Ac-Cha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:6
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:6
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:7
Ac-Nle-c(Cys-β-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:7
Ac-Nle-c(Cys-Gaba-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:7
Ac-Nle-c(Cys-Aib-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:7
Ac-Nle-c(Cys-Gly-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:7
Ac-Nle-c(D-Cys-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:8
Ac-Nle-c(D-Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:8
Ac-Nle-c(D-Cys-β-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:8
Ac-Nle-c(D-Cys-Gaba-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:8
Ac-Nle-c(D-Cys-Aib-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:8
Ac-Nle-c(D-Cys-Gly-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:8
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:9
Ac-Nle-c(Cys-β-Ala-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:9
Ac-Nle-c(Cys-Gaba-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:9
Ac-Nle-c(Cys-Aib-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:9
Ac-Nle-c(Cys-Gly-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:9
Ac-Nle-c(D-Cys-Ala-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:10
Ac-Nle-c(D-Cys-D-Ala-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:10
Ac-Nle-c(D-Cys-β-Ala-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:10
Ac-Nle-c(D-Cys-Gaba-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:10
Ac-Nle-c(D-Cys-Aib-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:10
Ac-Oic-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-Chg-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-hCha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-D-Cha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-Nip-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-hPro-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-hLeu-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-hCha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-Phe-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-D-Phe-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-D-Chg-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
н-бутаноил-Cha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:12
Ac-hPhe-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-β-hMet-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-Gaba-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-Cha-c(Asp-His-D-Phe-Arg-D-Trp-Ala-Lys)-NH2; SEQ ID NO:13
Ac-hCha-c(Asp-His-D-Phe-Arg-D-Trp-Ala-Lys)-NH2; SEQ ID NO:13
Ac-Leu-c(Asp-His-D-Phe-Arg-D-Trp-Ala-Lys)-NH2; SEQ ID NO:13
Ac-hLeu-c(Asp-His-D-Phe-Arg-D-Trp-Ala-Lys)-NH2; SEQ ID NO:13
Ac-Phe-c(Asp-His-D-Phe-Arg-D-Trp-Ala-Lys)-NH2; SEQ ID NO:13
Ac-Nle-c(Asp-His-D-Phe-Arg-D-Trp-D-Ala-Lys)-NH2; SEQ ID NO:14
Ac-Nle-c(Asp-His-D-Phe-Arg-D-Trp-β-Ala-Lys)-NH2; SEQ ID NO:14
Ac-Nle-c(Asp-His-D-Phe-Arg-D-Trp-Gaba-Lys)-NH2; SEQ ID NO:14
Ac-Nle-c(Asp-His-D-Phe-Arg-D-Trp-Aha-Lys)-NH2; SEQ ID NO:14
Ac-Nle-c(Asp-His-D-Phe-Arg-D-Trp-Apn-Lys)-NH2; SEQ ID NO:14
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-Apn-Cys)-NH2; SEQ ID NO:15
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-Gaba-Cys)-NH2; SEQ ID NO:15
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-Ahx-Cys)-NH2; SEQ ID NO:15
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-β-Ala-Cys)-NH2; SEQ ID NO:15
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-D-Ala-Cys)-NH2; SEQ ID NO:15
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; SEQ ID NO:16
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-2-Nal-Cys)-NH2; SEQ ID NO:16
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-1-Nal-Cys)-NH2; SEQ ID NO:16
н-бутаноил-Nle-c(Cys-D-Ala-His-D-Phe-Arg-2-Nal-Cys)-NH2; SEQ ID NO:17
н-бутаноил-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:17
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-2-Nal-Cys)-NH2; SEQ ID NO:18
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-1-Nal-Cys)-NH2; SEQ ID NO:18
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Bal-Cys)-NH2; SEQ ID NO:18
Ac-Nle-c(Cys-D-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:61
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-D-Ala-Lys)-NH2; SEQ ID NO:19
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-Bal-Cys)-NH2; SEQ ID NO:20
Ac-Nle-c(Pen-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:21
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO:22
Ac-Nle-c(Pen-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO:22
D-Phe-c(Cys-His-D-Phe-hArg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:23
D-Phe-c(Cys-His-D-(Et)Tyr-Arg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:24
D-Phe-c(Cys-His-D-Phe-Arg-Bip-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:25
D-Phe-c(Cys-His-D-(Et)Tyr-hArg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:24
D-Phe-c(Cys-His-D-Phe-hArg-Bip-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:26
D-Phe-c(Cys-His-D-(Et)Tyr-hArg-Bip-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:26
Nle-c(Cys-His-D-Phe-Arg-Trp-Apn-Cys)-NH2; SEQ ID NO:27
Ac-Nle-c(Asp-D-Ala-His-D-Phe-Arg-Trp-Lys)-NH2; SEQ ID NO:28
Ac-Nle-c(Asp-D-Ala-His-D-Phe-Arg-Bal-Lys)-NH2; SEQ ID NO:28
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-OH; SEQ ID NO:29
Ac-Nle-c(Cys-D-Abu-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:30
Ac-Nle-c(Cys-D-Val-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:30
Ac-Nle-c(Cys-D-Ile-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:30
Ac-Nle-c(Cys-D-Leu-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:30
Ac-Nle-c(Cys-D-Tle-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:30
Ac-Nle-c(Cys-D-Cha-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:30
Ac-Nle-c(Pen-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:31
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO:32
Ac-Nle-c(Pen-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO:32
Ac-Leu-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:33
Ac-Cha-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:33
Ac-Ile-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:33
Ac-Phe-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:33
Ac-Val-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:33
Ac-2-Nal-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:33
Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:34
Phe-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:34
Ac-Nle-c(Cys-3-Pal-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:35
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-OH; SEQ ID NO:36
Ac-Nle-c(Cys-His-Phe-Arg-D-Trp-Gaba-Cys)-NH2; SEQ ID NO:37
Ac-Nle-c(Asp-His-D-2-Nal-Arg-Trp-Ala-Lys)-NH2; SEQ ID NO:38
Ac-Nle-c(Asp-His-D-2-Nal-Arg-Trp-β-Ala-Lys)-NH2; SEQ ID NO:38
Ac-Nle-c(Cys-His-D-2-Nal-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:39
Ac-Nle-c(Cys-His-D-2-Nal-Arg-Trp-Ahx-Cys)-NH2; SEQ ID NO:39
Ac-hPhe-c(Asp-His-D-2-Nal-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:40
Ac-Cha-c(Asp-His-D-2-Nal-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:40
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-β-Ala-Lys)-OH; SEQ ID NO:41
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Ahx-Cys)-OH; SEQ ID NO:42
D-Phe-c(Cys-His-D-Phe-Arg-Trp-Ala-D-Cys)-Thr-OH; SEQ ID NO:43
D-Phe-c(Cys-His-D-Phe-Arg-Trp-β-Ala-D-Cys)-Thr-OH; SEQ ID NO:43
D-Phe-c(Cys-His-D-Phe-Arg-Trp-Gaba-D-Cys)-Thr-OH; SEQ ID NO:43
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Apn-Cys)-OH; SEQ ID NO:42
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-Apn-Lys)-OH; SEQ ID NO:41
Ac-Cha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO:44
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO:44
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-OH; SEQ ID NO:29
Ac-Chg-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO:44
Ac-D-Cha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO:44
Ac-hCha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO:44
Ac-D-Chg-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO:44
Ac-hPhe-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO:44
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-Gaba-Cys)-OH; SEQ ID NO:45
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-Ahx-Cys)-OH; SEQ ID NO:45
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-β-Ala-Cys)-OH; SEQ ID NO:45
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-D-Ala-Cys)-OH; SEQ ID NO:45
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-OH; SEQ ID NO:46
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-2-Nal-Cys)-OH; SEQ ID NO:46
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-1-Nal-Cys)-OH; SEQ ID NO:46
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-Bal-Cys)-OH; SEQ ID NO:46
Ac-Nle-c(Pen-D-Ala-His-D-Phe-Arg-Trp-Cys)-OH; SEQ ID NO:47
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-OH; SEQ ID NO:29
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-OH; SEQ ID NO:48 или
Ac-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; SEQ ID NO:49
или его фармацевтически приемлемую соль.
Более предпочтительное соединение представленной непосредственно выше группы соединений представляет собой соединение, имеющее формулу:
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:7
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO:22
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO:32
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-OH; SEQ ID NO:29
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-OH; SEQ ID NO:29 или
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-OH; SEQ ID NO:48
или его фармацевтически приемлемую соль.
Более предпочтительное соединение формулы (I) представляет собой соединение, имеющее формулу:
А1 представляет собой Arg, D-Arg, Cha, hCha, Chg, D-Chg, Ile, Leu, 2-Nal, Nle, Phe, D-Phe, hPhe, Val или подвергнут делеции;
А2 представляет собой Cys, Pen или Asp;
А3 представляет собой D-Ala, D-Abu, D-Cha, D-Ile, D-Leu, D-Tle, D-Val или подвергнут делеции;
А4 представляет собой His или 3-Pal;
А5 представляет собой D-Phe, D-2-Nal или D-(Et)Tyr;
А6 представляет собой Arg или hArg;
А7 представляет собой Trp, 2-Nal, Bal, Bip или D-Trp;
А8 представляет собой Gly, Ala, β-Ala, Gaba, Apn, Ahx или подвергнут делеции;
А9 представляет собой Cys, D-Cys, Pen или Lys;
А10 представляет собой Thr или подвергнут делеции;
каждый из R2 и R3 независимо выбран из группы, состоящей из Н или ацила;
или его фармацевтически приемлемую соль.
Более предпочтительное соединение представленной непосредственно выше группы соединений представляет собой соединение формулы:
Ac-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:50
Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:50
Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO:51
Ac-D-Arg-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO:52
Ac-Arg-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO:52
Ac-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO:51
Ac-D-Arg-c(Asp-His-D-Phe-Arg-Trp-Ala-Lys)-NH2; SEQ ID NO:53
Ac-Arg-c(Asp-His-D-Phe-Arg-Trp-Ala-Lys)-NH2; SEQ ID NO:53
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:7
D-Phe-c(Cys-His-D-(Et)Tyr-Arg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:24
Nle-c(Cys-His-D-Phe-Arg-Trp-Apn-Cys)-NH2; SEQ ID NO:27
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO:32
Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:34
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-β-Ala-Lys)-NH2; SEQ ID NO:1
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Ahx-Cys)-NH2; SEQ ID NO:2
D-Phe-c(Cys-His-D-Phe-Arg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:3
D-Phe-c(Cys-His-D-Phe-Arg-Trp-Gaba-D-Cys)-Thr-NH2; SEQ ID NO:3
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Apn-Cys)-NH2; SEQ ID NO:2
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-Apn-Lys)-NH2; SEQ ID NO:4
Ac-Cha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:6
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:6
Ac-Chg-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-hCha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-D-Chg-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-hPhe-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-β-Ala-Cys)-NH2; SEQ ID NO:15
Ac-Nle-c(Pen-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:21
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO:22
D-Phe-c(Cys-His-D-Phe-hArg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:23
D-Phe-c(Cys-His-D-Phe-Arg-Bip-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:25
D-Phe-c(Cys-His-D-(Et)Tyr-hArg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:24
D-Phe-c(Cys-His-D-Phe-hArg-Bip-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:26
D-Phe-c(Cys-His-D-(Et)Tyr-hArg-Bip-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:26
Ac-Nle-c(Asp-D-Ala-His-D-Phe-Arg-Trp-Lys)-NH2; SEQ ID NO:28
Ac-Nle-c(Asp-D-Ala-His-D-Phe-Arg-Bal-Lys)-NH2; SEQ ID NO:28
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-OH; SEQ ID NO:29
Ac-Nle-c(Cys-D-Abu-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:30
Ac-Nle-c(Cys-D-Val-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:30
Ac-Nle-c(Cys-D-Ile-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:30
Ac-Nle-c(Cys-D-Leu-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:30
Ac-Nle-c(Cys-D-Tle-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:30
Ac-Nle-c(Cys-D-Cha-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:30
Ac-Nle-c(Pen-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:31
Ac-Nle-c(Pen-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO:32
Ac-Leu-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:33
Ac-Cha-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:33
Ac-Ile-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:33
Ac-Phe-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:33
Ac-Val-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:33
Ac-2-Nal-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:33
Phe-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:34
Ac-Nle-c(Cys-3Pal-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:35
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-OH; SEQ ID NO:36
Ac-Nle-c(Cys-His-Phe-Arg-D-Trp-Gaba-Cys)-NH2; SEQ ID NO:37
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; SEQ ID NO:16
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-2-Nal-Cys)-NH2; SEQ ID NO:16
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-Bal-Cys)-NH2; SEQ ID NO:20
Ac-Nle-c(Asp-His-D-2-Nal-Arg-Trp-Ala-Lys)-NH2; SEQ ID NO:38
Ac-Nle-c(Asp-His-D-2-Nal-Arg-Trp-β-Ala-Lys)-NH2; SEQ ID NO:38
Ac-Nle-c(Cys-His-D-2-Nal-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:39
Ac-Nle-c(Cys-His-D-2-Nal-Arg-Trp-Ahx-Cys)-NH2; SEQ ID NO:39
Ac-hPhe-c(Asp-His-D-2-Nal-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:40
Ac-Cha-c(Asp-His-D-2-Nal-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:40 или
Ac-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; SEQ ID NO:49
или его фармацевтически приемлемую соль.
Более предпочтительное соединение формулы (I) представляет собой то, где указанное соединение имеет формулу:
А1 представляет собой Arg, D-Arg, hArg, или D-hArg;
или его фармацевтически приемлемую соль.
Более предпочтительное соединение непосредственно выше представленной группы соединений представляет собой соединение, имеющее формулу:
А2 представляет собой Cys, D-Cys, hCys, D-hCys, Pen, D-Pen, Asp или Glu;
А3 представляет собой Gly, Ala, D-Ala, D-Glu, β-Ala, Gaba, Aib или подвергнут делеции;
А4 представляет собой His;
А5 представляет собой D-Phe, D-1-Nal, D-2-Nal, D-Trp, D-Bal, или D-(Et)Tyr;
А6 представляет собой Arg или hArg;
А7 представляет собой Trp, Bip, D-Trp, 1-Nal или 2-Nal;
А8 представляет собой A6c, Ala, β-Ala, Gaba, Apn или Ahx;
А9 представляет собой Cys, D-Cys, hCys, D-hCys, Pen, D-Pen, или Lys;
А10 представляет собой Thr или подвергнут делеции;
или его фармацевтически приемлемую соль.
Более предпочтительное соединение представленной непосредственно выше группы соединений представляет собой то, в котором каждый из R2 и R3 независимо представляет собой Н, ацил, н-пропаноил или н-бутаноил или его фармацевтически приемлемую соль.
Более предпочтительное соединение представленной непосредственно выше группы соединений представляет собой то, в котором указанное соединение имеет формулу:
А2 представляет собой Cys или Asp;
А3 представляет собой D-Ala или подвергнут делеции;
А4 представляет собой His;
А5 представляет собой D-Phe или D-2-Nal;
А6 представляет собой Arg;
А7 представляет собой Trp;
А8 представляет собой Ala, Gaba или подвергнут делеции;
А9 представляет собой Cys, Pen, или Lys;
А10 подвергнут делеции;
или его фармацевтически приемлемую соль.
Более предпочтительное соединение представленной непосредственно выше группы соединений представляет собой то, в котором каждый из R2 и R3 независимо представляет собой Н или ацил; или его фармацевтически приемлемую соль.
Более предпочтительное соединение представленной непосредственно выше группы соединений представляет собой соединение формулы:
Ac-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:50
Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:50
Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO:51
Ac-D-Arg-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO:52
Ac-Arg-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO:52
Ac-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO:51
Ac-D-Arg-c(Asp-His-D-Phe-Arg-Trp-Ala-Lys)-NH2; SEQ ID NO:53
Ac-Arg-c(Asp-His-D-Phe-Arg-Trp-Ala-Lys)-NH2; SEQ ID NO:53 или
Ac-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; SEQ ID NO:49
или его фармацевтически приемлемые соли.
Более предпочтительное соединение представленной непосредственно выше группы соединений представляет собой соединение формулы:
Ac-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:50
Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO:51 или
Ac-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; SEQ ID NO:49
или его фармацевтически приемлемую соль.
Более предпочтительное соединение представленной непосредственно выше группы соединений представляет собой соединение формулы:
Ac-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:50
или его фармацевтически приемлемую соль.
Более предпочтительное соединение представленной непосредственно выше группы соединений представляет собой соединение формулы:
Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO:51
или его фармацевтически приемлемую соль.
Более предпочтительное соединение представленной непосредственно выше группы соединений представляет собой соединение формулы:
Ac-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; SEQ ID NO:49
или его фармацевтически приемлемую соль.
В одном аспекте настоящее изобретение направлено на соединение в соответствии с формулой (II):
(R2R3)-A1-c(A2-A3-A4-A5-A6-A7-A8-A9)-NH2,
где:
А1 представляет собой Nle или подвергнут делеции;
А2 представляет собой Cys или Asp;
А3 представляет собой Glu или D-Ala;
А4 представляет собой His;
А5 представляет собой D-Phe;
А6 представляет собой Arg;
А7 представляет собой Trp, 2-Nal или Bal;
А8 представляет собой Gly, D-Ala, β-Ala, Gaba или Apn;
А9 представляет собой Cys или Lys;
каждый из R2 и R3 независимо выбран из группы, состоящей из Н или (С1-С6)ацила;
при условии, что
(I) когда R2 представляет собой (С1-С6)ацил, то R3 представляет собой Н; и
(II) когда A2 представляет собой Cys, то A9 представляет собой Cys,
или его фармацевтически приемлемую соль.
Более предпочтительное соединение представленной непосредственно выше группы соединений представляет собой соединение формулы:
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Gly-Cys)-NH2; SEQ ID NO:54
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-D-Ala-Cys)-NH2; SEQ ID NO:54
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-β-Ala-Cys)-NH2; SEQ ID NO:54
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:54
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Apn-Cys)-NH2; SEQ ID NO:54
Ac-c(Cys-Glu-His-D-Phe-Arg-Trp-Ala-Cys)-NH2; SEQ ID NO:55
Ac-c(Cys-Glu-His-D-Phe-Arg-2-Nal-Ala-Cys)-NH2; SEQ ID NO:55
Ac-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Ala-Cys)-NH2; SEQ ID NO:56
Ac-c(Cys-D-Ala-His-D-Phe-Arg-2-Nal-Ala-Cys)-NH2; SEQ ID NO:56
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Ala-Cys)-NH2; SEQ ID NO:57
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-β-Ala-Cys)-NH2; SEQ ID NO:57
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:57 или
Ac-Nle-c(Asp-D-Ala-His-D-Phe-Arg-Bal-Ala-Lys)-NH2; SEQ ID NO:58
или его фармацевтически приемлемую соль.
Другое более предпочтительное соединение формулы (I) или формулы (II) представляет собой каждое из соединений, которые определенным образом пронумерованы ниже в разделе «Примеры» настоящего описания, или их фармацевтически приемлемую соль.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли и фармацевтически приемлемый носитель или разбавитель.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, где указанное соединение представляет собой селективный агонист рецепторов меланокортина-4.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, где указанное соединение представляет собой селективный агонист рецептора меланокортина-4 с функциональной активностью, характеризуемой ЕС50, по меньшей мере, в 15 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-1, человеческому рецептору меланокортина-3 и человеческому рецептору меланокортина-5.
В еще одном аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, где указанное соединение представляет собой селективный агонист рецептора меланокортина-4 с функциональной активностью, характеризуемой ЕС50, по меньшей мере, в 17 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-3, ЕС50, по меньшей мере, в 90 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-3, ЕС50, по меньшей мере, в 200 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-5, или ЕС50, по меньшей мере, в 3000 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-5.
В еще одном аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, используемую для лечения острого или хронического воспалительного заболевания или медицинского состояния, такого как общее воспаление, воспалительное заболевание кишечника, энцефалит, сепсис и септический шок.
В еще одном аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, используемую для лечения заболевания или медицинского состояния с аутоиммунным компонентом, такого как ревматоидный артрит, подагрический артрит и рассеянный склероз.
В еще одном аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, используемую для лечения метаболического заболевания или медицинского состояния, сопровождающегося прибавкой массы тела, такого как ожирение, расстройства питания и синдром Prader-Willi. В еще одном аспекте подвергаемое лечению заболевание или состояние представляет собой ожирение. В еще одном аспекте подвергаемое лечению заболевание или состояние представляет собой расстройство питания.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, используемую для уменьшения потребления пищи, для снижения массы тела или их комбинации. В предпочтительном варианте осуществления настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединение формулы (I), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, которую можно использовать для уменьшения потребления пищи, снижения массы тела или их комбинации, где активный ингредиент представляет собой один или более из следующих соединений: Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2 SEQ ID NO:32, Ac-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2 SEQ ID NO:50, Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2 SEQ ID NO:50, Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2 SEQ ID NO:51, Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2 SEQ ID NO:7, D-Phe-c(Cys-His-D-(Et)Tyr-Arg-Trp-β-Ala-D-Cys)-Thr-NH2 SEQ ID NO:24, Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2 SEQ ID NO:22 или Ac-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2 SEQ ID NO:49. В еще одном предпочтительном варианте осуществления настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединение формулы (I), как определено выше в настоящем описании, или его фармацевтически приемлемой соли, вместе с фармацевтически приемлемым носителем или разбавителем, которую можно использовать для уменьшения потребления пищи, снижения массы тела или их комбинации, где активный ингредиент представляет собой: Ac-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2 SEQ ID NO:50. В еще одном предпочтительном варианте осуществления настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I), как определено выше в настоящем описании, или его фармацевтически приемлемой соли, вместе с фармацевтически приемлемым носителем или разбавителем, которую можно использовать для уменьшения потребления пищи, снижения массы тела или их комбинации, где активный ингредиент представляет собой: Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2 SEQ ID NO:51. В еще одном предпочтительном варианте осуществления настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I), как определено выше в настоящем описании, или его фармацевтически приемлемой соли, вместе с фармацевтически приемлемым носителем или разбавителем, которую можно использовать для уменьшения потребления пищи, снижения массы тела или их комбинации, где активный ингредиент представляет собой: Ac-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2 SEQ ID NO:49.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, применяемую для снижения аппетита без нарушения массы тела. В еще одном аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, применяемую для уменьшения потребления пищи, в то же самое время увеличивая массу тела.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, применяемую для лечения метаболического заболевания или медицинского состояния, сопровождающегося потерей массы тела, такого как анорексия, булимия, истощение при СПИДе, кахексия, раковая кахексия и алиментарная дистрофия у истощенных пожилых лиц. В еще одном аспекте подвергаемое лечению заболевание или состояние представляет собой анорексию. В еще одном аспекте подвергаемое лечению заболевание или состояние представляет собой булимию. В еще одном аспекте подвергаемое лечению заболевание или состояние представляет собой истощение при СПИДе или алиментарную дистрофию у истощенных пожилых лиц. В еще одном аспекте подвергаемое лечению заболевание или состояние представляет собой кахексию или раковую кахексию.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, применяемую для лечения неопластического заболевания или медицинского состояния, такого как рак кожи и раковая кахексия.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, применяемую для лечения репродуктивного или полового медицинского состояния, такого как эндометриоз, маточное кровотечение, сексуальная дисфункция, эректильная дисфункция и сниженная сексуальная реакция у женщин.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, применяемую для лечения заболевания или медицинского состояния, возникающего в результате повреждающего воздействия на организм, такого как отторжение органного трансплантата, ишемическое и реперфузионное повреждение, ранение и травма спинного мозга и потеря массы тела вследствие медицинской процедуры, выбранной из группы, состоящей из химиотерапии, лучевой терапии, временной или постоянной иммобилизации и диализа.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, применяемую для лечения сердечно-сосудистого заболевания или медицинского состояния, такого как геморрагический шок, кардиогенный шок, гиповолемический шок, сердечно-сосудистые расстройства и сердечная кахексия.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, применяемую для лечения легочного заболевания или медицинского состояния, такого как острый респираторный дистресс-синдром, пневмофиброз, хроническое обструктивное легочное заболевание и астма.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, применяемую для усиления иммунной толерантности и для лечения аллергических состояний.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, применяемую для лечения дерматологического заболевания или медицинского состояния, такого как псориаз, истощение пигментации кожи, угри и образование келоида.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, применяемую для лечения поведенческих расстройств или заболевания или медицинского состояния центральной нервной системы, такого как тревога, депрессия, дисфункция памяти и нейропатическая боль.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, применяемую для лечения почечного заболевания или медицинского состояния, такого как почечная кахексия и натриурез.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, применяемую для модулирования массы яичников, развития плаценты, секреции пролактина, секреции ФСГ, внутриматочного роста плода, родов, сперматогенеза, высвобождения тироксина, синтеза и высвобождения альдостерона, температуры тела, артериального давления, частоты сердечных сокращений, сосудистого тонуса, мозгового кровотока, уровней глюкозы крови, секреции сала, секреции феромонов, мотивации, обучения и поведения, восприятия боли, нейропротекции и роста нервов.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, применяемую для модулирования костного метаболизма, образования костной ткани и развития костей.
В другом аспекте настоящее изобретение предоставляет фармацевтическую композицию, включающую эффективное количество соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли вместе с фармацевтически приемлемым носителем или разбавителем, применяемую для ингибирования употребления алкоголя, для снижения употребления алкоголя, для лечения алкоголизма или для лечения злоупотребления алкоголем. В еще одном аспекте соединение композиции, применяемой для ингибирования употребления алкоголя, для снижения употребления алкоголя, для лечения алкоголизма или для лечения злоупотребления алкоголем, представляет собой селективный агонист рецептора меланокортина-4. В еще одном аспекте соединение композиции, применяемой для ингибирования употребления алкоголя, представляет собой селективный агонист рецептора меланокортина-4 или его фармацевтически приемлемую соль с функциональной активностью, характеризуемой ЕС50, по меньшей мере, в 15 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-1, человеческому рецептору меланокортина-3 и человеческому рецептору меланокортина-5. В еще одном аспекте соединение композиции, применяемое для ингибирования употребления алкоголя, представляет собой селективный агонист рецептора меланокортина-4 или его фармацевтически приемлемую соль с функциональной активностью, характеризуемой ЕС50, по меньшей мере, в 17 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-3, ЕС50, по меньшей мере, в 90 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-3, ЕС50, по меньшей мере, в 200 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-5, или, по меньшей мере, в 3000 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-5.
В другом аспекте настоящее изобретение предоставляет применение терапевтически эффективного количества агониста рецептора меланокортина-4 соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли, для изготовления лекарственного препарата для лечения алкоголизма или для лечения злоупотребления алкоголем у нуждающегося в таком лечении субъекта.
В еще одном аспекте настоящее изобретение предоставляет способ вызова агонистического или антагонистического эффекта от рецептора меланокортина у нуждающегося в нем субъекта, который включает введение указанному субъекту эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение предоставляет способ вызова агонистического или антагонистического эффекта от рецептора меланокортина у нуждающегося в нем субъекта, который включает введение указанному субъекту эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли, где указанное соединение представляет собой селективный агонист рецептора меланокортина-4.
В другом аспекте настоящее изобретение предоставляет способ вызова агонистического или антагонистического эффекта от рецептора меланокортина у нуждающегося в нем субъекта, который включает введение указанному субъекту эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли, где указанное соединение представляет собой селективный агонист рецептора меланокортина-4 с функциональной активностью, характеризуемой ЕС50, по меньшей мере, в 15 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-1, к человеческому рецептору меланокортина-3 и к человеческому рецептору меланокортина-5.
В другом аспекте настоящее изобретение предоставляет способ вызова агонистического или антагонистического эффекта от рецептора меланокортина у нуждающегося в нем субъекта, который включает введение указанному субъекту эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли, где указанное соединение представляет собой селективный агонист рецептора меланокортина-4 с функциональной активностью, характеризуемой ЕС50, в 17 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-3, ЕС50, по меньшей мере, в 90 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-3, ЕС50, по меньшей мере, в 200 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-5, или, по меньшей мере, в 3000 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-5.
В другом аспекте настоящее изобретение предоставляет способ лечения острого или хронического воспалительного заболевания или медицинского состояния, такого как общее воспаление, воспалительное заболевание кишечника, энцефалит, сепсис и септический шок, путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение предоставляет способ лечения заболевания или медицинского состояния с аутоиммунным компонентом, такого как ревматоидный артрит, подагрический артрит и рассеянный склероз, путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение предоставляет способ лечения заболевания или медицинского состояния, сопровождающегося прибавкой массы тела, такого как ожирение, расстройства питания и синдром Prader-Willi, путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли. В еще одном аспекте описанного выше способа подвергаемое лечению заболевание или состояние представляет собой ожирение. В еще одном аспекте описанного выше способа подвергаемое лечению заболевание или состояние представляет собой расстройство питания.
В другом аспекте настоящее изобретение предоставляет способ снижения потребления пищи, уменьшения массы тела или их комбинации путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли. В предпочтительном варианте осуществления настоящее изобретение предоставляет способ снижения потребления пищи, уменьшения массы тела или их комбинации путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли, где указанное соединение представляет собой Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2 SEQ ID NO:32, Ac-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2 SEQ ID NO:50, Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2 SEQ ID NO:50, Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2 SEQ ID NO:51, Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2 SEQ ID NO:7, D-Phe-c(Cys-His-D-(Et)Tyr-Arg-Trp-β-Ala-D-Cys)-Thr-NH2 SEQ ID NO:24, Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2 SEQ ID NO:22, или Ac-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2 SEQ ID NO:49. В другом предпочтительном варианте осуществления настоящее изобретение предоставляет способ снижения потребления пищи, уменьшения массы тела или их комбинации путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли, где указанное соединение представляет собой Ac-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2 SEQ ID NO:50. В другом предпочтительном варианте осуществления, настоящее изобретение предоставляет способ снижения потребления пищи, уменьшения массы тела или их комбинации путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли, где указанное соединение представляет собой Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2 SEQ ID NO:51. В другом предпочтительном варианте осуществления настоящее изобретение предоставляет способ снижения потребления пищи, уменьшения массы тела или их комбинации путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли, где указанное соединение представляет собой Ac-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2 SEQ ID NO:49.
В другом аспекте настоящее изобретение предоставляет способ снижения аппетита без нарушения массы тела введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли. В другом аспекте настоящее изобретение предоставляет способ снижения потребления пищи с одновременным увеличением массы тела введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение предоставляет способ лечения метаболического заболевания или медицинского состояния, сопровождающегося потерей массы тела, такого как анорексия, булимия, истощение при СПИДе, кахексия, раковая кахексия и алиментарная дистрофия у истощенных пожилых лиц путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли. В еще одном аспекте описанный выше способ применяется для лечения анорексии. В еще одном аспекте описанный выше способ применяется для лечения булимии. В еще одном аспекте описанный выше способ применяется для лечения истощения при СПИДе или алиментарной дистрофии у истощенных пожилых лиц. В еще одном аспекте описанный выше способ применяется для лечения кахексии или раковой кахексии.
В другом аспекте настоящее изобретение предоставляет способ лечения неопластического заболевания или медицинского состояния, такого как рак кожи и раковая кахексия, путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение предоставляет способ лечения репродуктивного или полового медицинского состояния, такого как эндометриоз, маточное кровотечение, сексуальная дисфункция, эректильная дисфункция и сниженная сексуальная реакция у женщин, путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение предоставляет способ лечения заболевания или медицинского состояния, возникающего в результате повреждающего воздействия на организм, такого как отторжение органного трансплантата, ишемическое и реперфузионное повреждение, ранение и травма спинного мозга и потеря массы тела вследствие медицинской процедуры, выбранной из группы, состоящей из химиотерапии, лучевой терапии, временной или постоянной иммобилизации и диализа, путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение предоставляет способ лечения сердечно-сосудистого заболевания или медицинского состояния, такого как геморрагический шок, кардиогенный шок, гиповолемический шок, сердечно-сосудистые расстройства и сердечная кахексия, путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение предоставляет способ лечения легочного заболевания или медицинского состояния, такого как острый респираторный дистресс-синдром, пневмофиброз, хроническое обструктивное легочное заболевание и астма, путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение предоставляет способ усиления иммунной толерантности или лечения аллергических состояний путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение предоставляет способ лечения дерматологического заболевания или медицинского состояния, такого как псориаз, истощение пигментации кожи, угри и образование келоида, путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение предоставляет способ лечения поведенческих расстройств или заболевания или медицинского состояния центральной нервной системы, такого как тревога, депрессия, дисфункция памяти и нейропатическая боль, путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение предоставляет способ лечения почечного заболевания или медицинского состояния, такого как почечная кахексия и натриурез, путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение предоставляет способ модулирования нормализующей или гомеостатической активности, такой как массы яичников, развития плаценты, секреции пролактина, секреции ФСГ, внутриматочного роста плода, родов, сперматогенеза, высвобождения тироксина, синтеза и высвобождения альдостерона, температуры тела, артериального давления, частоты сердечных сокращений, сосудистого тонуса, мозгового кровотока, уровней глюкозы крови, секреции сала, секреции феромонов, мотивации, обучения и поведения, восприятия боли, нейропротекции и роста нервов, путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение предоставляет способ модулирования нормализующей или гомеостатической активности, такой как костный метаболизм, образование костной ткани и развитие костей, путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение предоставляет способ ингибирования употребления алкоголя, для снижения употребления алкоголя, для лечения алкоголизма или для лечения злоупотребления алкоголем путем вызова агонистического или антагонистического эффекта от рецептора меланокортина введением эффективного количества соединения формулы (I) или формулы (II), как определено выше в настоящем описании, или его фармацевтически приемлемой соли. В еще одном аспекте описанного выше способа соединение представляет собой селективный агонист рецептора меланокортина-4. В еще одном аспекте представленного непосредственно выше способа соединение композиции, используемой для ингибирования потребления алкоголя, представляет собой селективный агонист рецептора меланокортина-4 или его фармацевтически приемлемую соль, с функциональной активностью, характеризуемой ЕС50, по меньшей мере, в 15 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-1, к человеческому рецептору меланокортина-3 и к человеческому рецептору меланокортина-5. В еще одном аспекте представленного непосредственно выше способа соединение композиции, используемой для ингибирования потребления алкоголя, представляет собой селективный агонист рецептора меланокортина-4 или его фармацевтически приемлемую соль, с функциональной активностью, характеризуемой ЕС50, по меньшей мере, в 17 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-3, ЕС50, по меньшей мере, в 90 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-3, ЕС50, по меньшей мере, в 200 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-5, или, ЕС50, по меньшей мере, в 3000 раз более селективной к человеческому рецептору меланокортина-4, чем к человеческому рецептору меланокортина-5.
В еще одном аспекте настоящее изобретение предоставляет применение терапевтически эффективного количества агониста или антагониста рецептора меланокортина-4 в соответствии с формулой (I) или формулой (II), как определено выше, или его фармацевтически приемлемой соли для изготовления лекарственного препарата, используемого для лечения заболевания и/или медицинского острого состояния, выбранного из группы, состоящей из острых и хронических воспалительных заболеваний, таких как общее воспаление, воспалительное заболевание кишечника, энцефалит, сепсис и септический шок; заболеваний с аутоиммунным компонентом, таких как ревматоидный артрит, подагрический артрит и рассеянный склероз; метаболических заболеваний и медицинских расстройств, сопровождающихся прибавкой массы тела, таких как ожирение, расстройства питания и синдром Prader-Willi; метаболических заболеваний и медицинских расстройств, сопровождающихся потерей массы тела, таких как анорексия, булимия, истощение при СПИДе, кахексия, раковая кахексия и алиментарная дистрофия у истощенных пожилых лиц; диабета и связанных с диабетом состояний и осложнений диабета, таких как ретинопатия; неопластической пролиферации, такой как рак кожи, и рак предстательной железы; репродуктивных или половых медицинских состояний, таких как эндометриоз и маточное кровотечение у женщин, половая дисфункция, эректильная дисфункция и сниженная сексуальная реакция у женщин; заболеваний или состояний, возникающих в результате лечения или повреждающего воздействия на организм, такого как отторжение органного трансплантата, ишемическое и реперфузионное повреждение, травм, ранений спинного мозга, а также потери массы тела, вызванной химиотерапией, лучевой терапией, временной или постоянной иммобилизацией или диализом; сердечно-сосудистых заболеваний или состояний, таких как геморрагической шок, кардиогенный шок, гиповолемический шок, и сердечно-сосудистых расстройств и сердечной кахексии; легочных заболеваний или состояний, таких как острый респираторный дистресс-синдром, хроническое обструктивное легочное заболевание, астма и пневмофиброз; для усиления иммунной толерантности и для борьбы с атаками на иммунную систему, такими как воздействия, связанные с определенными видами аллергии или отторжением органных трансплантатов; дерматологических заболеваний и состояний, таких как псориаз, истощение пигментации кожи, угри, образование келоидов и рак кожи; поведенческих расстройств, расстройств центральной нервной системы и нейрогенных расстройств, таких как тревога, депрессия, дисфункция памяти и нейропатическая боль; и почечных состояний или заболеваний, таких как почечная кахексия и натриуерез.
В еще одном аспекте настоящее изобретение предоставляет применение терапевтически эффективного количества агониста или антагониста рецептора меланокортина-4 в соответствии с формулой (I) или формулой (II), как определено выше, или его фармацевтически приемлемой соли для изготовления лекарственного препарата, используемого для модулирования нормализующей или гомеостатической активности, такой как масса яичников, развитие плаценты, секреция пролактина, секреция ФСГ, внутриматочный рост плода, роды, сперматогенез, высвобождение тироксина, синтез и высвобождение альдостерона, температура тела, артериальное давление, частота сердечных сокращений, сосудистый тонус, мозговой кровоток, уровни глюкозы в крови, секреция сала, секреция феромонов, мотивация, обучение и поведение, восприятие боли, нейропротекция, рост нервов, костный метаболизм, образование костной ткани и развитие костей.
Следует понимать, что также предусмотрены терапевтические вмешательства, направленные и на нормальные физиологические, и на патофизиологические процессы, в которых используются рецепторы меланокортина.
Дополнительные цели, преимущества и признаки настоящего изобретения станут очевидными из следующего описания и прилагаемой формулы изобретения, взятых в сочетании с сопровождающими чертежами.
Соединения формул (I) или (II) представляют собой лиганды, по меньшей мере, для одного из рецепторов меланокортина (MC1-R, MC2-R, MC3-R, MC4-R и MC5-R), и их выбор испытывали на их способность действовать в качестве лиганда в описанном ниже анализе in vitro.
Краткое описание чертежей
Фиг.1А: Средняя разность потребления пищи из носителя голодавшими крысами через 6 ч после введения 100 нмоль/кг выбранных соединений.
Фиг.1В. Средняя разность потребления пищи из носителя голодавшими крысами через 6 ч после введения 500 нмоль/кг выбранных соединений.
Фиг.2А. Кумулятивная разность среднего потребления пищи из носителя у крыс после введения различных концентраций соединения А.
Фиг.2В. Кумулятивная разность средней массы тела из носителя у крыс после введения различных концентраций соединения А.
Фиг.3А. Кумулятивная разность среднего потребления пищи из носителя у крыс после введения выбранных соединений.
Фиг.3В. Кумулятивная разность средней массы тела из носителя у крыс после введения выбранных соединений.
Фиг.4А. Кумулятивная разность среднего потребления пищи из носителя у крыс после введения выбранных соединений.
Фиг.4В. Кумулятивная разность средней массы тела из носителя у крыс после введения выбранных соединений.
Подробное описание изобретения
Номенклатура, используемая для определения пептидов, представляет собой ту, которая обычно используется в данной области, где аминогруппа N-конца появляется слева, а карбоксильная группа на С-конце появляется справа. Когда аминокислота имеет изомерные формы, то, пока нет других ясных указаний, она представлена L-формой. Пока нет других определений, все использованные в настоящем описании технические и научные термины имеют такое же значение, которое обычно понимает средний специалист в области, к которой относится настоящее изобретение. Также все публикации, патентные заявки, патенты и другие ссылки, указанные в настоящем описании, включены в качестве ссылки.
Номенклатура и аббревиатуры
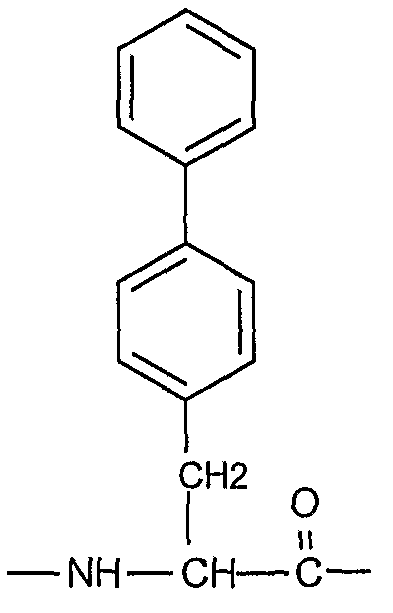

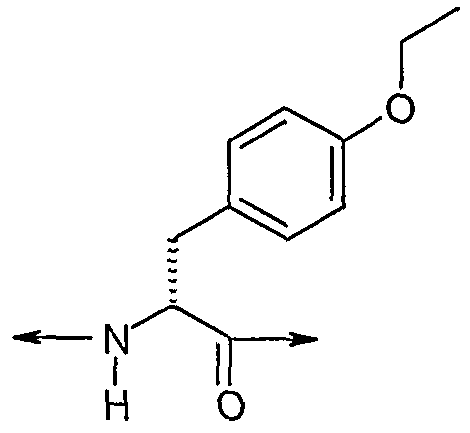
Некоторые другие аббревиатуры, использованные в настоящем описании, определены ниже:
Пока нет других указаний, все аббревиатуры (например, Ala) аминокислот, за исключением N-концевой аминокислоты, в настоящем описании обозначают структуру -NH-C(R)(R')-CO-, где каждый R и R' независимо представляет собой водород или боковую цепь аминокислоты (например, R=CH3 и R'=H для Ala), или R и R' могут быть соединены для образования кольцевой системы.
Для N-концевой аминокислоты аббревиатура обозначает структуру:
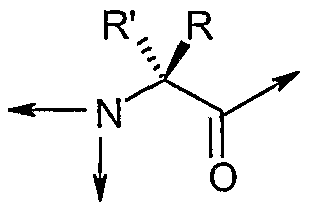
Обозначение “NH2”, например, в Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2 указывает на то, что С-конец пептида амидирован. Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys) или, альтернативно, Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-OH указывает на то, что С-конец представляет собой свободную кислоту.
“-c(Cys-Cys)-“ или “цикло(Cys-Cys)-“ обозначает структуру:

“-c(Cys-Pen)-“ или “цикло(Cys-Pen)-“ обозначает структуру:

“-c(Asp-Lys)-“ или “цикло(Asp-Lys)-“ обозначает структуру:
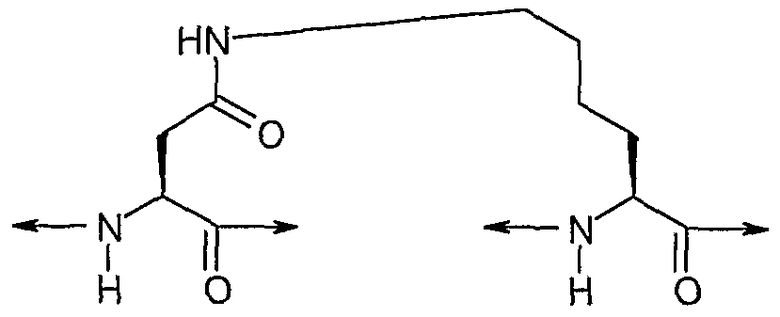
«Ацил» относится к R”-C(O)-, где R” представляет собой Н, алкил, замещенный алкил, гетероалкил, замещенный гетероалкил, алкенил, замещенный алкенил, арил, алкиларил или замещенный алкиларил и указан в общей формуле определенного варианта осуществления как “Ac”.
«Алкил» относится к углеводородной группе, состоящей из одного или нескольких атомов углерода, где множественные атомы углерода, если присутствуют, соединены одиночными связями. Алкильная углеводородная группа может быть прямоцепочечной или содержать одну или несколько ветвей или циклических групп.
«Гидроксиалкил» относится к алкильной группе, где один или несколько атомов водорода углеводородной группы замещены одним или несколькими гидрокси радикалами, такими как гидроксиметил, гидроксиэтил, гидроксипропил, гидроксибутил, гидроксипентил, гидроксигексил, и им подобными.
«Замещенный алкил» относится к алкилу, где один или несколько атомов водорода углеводородной группы замещены одним или несколькими заместителями, выбранными из группы, состоящей из галогена (т.е. фтора, хлора, брома и йода), -ОН, -CN, -SH, -NH2, -NHCH3, -NO2 и С1-20 алкил, где указанный С1-20 алкил необязательно может быть замещен одним или несколькими заместителями, независимо выбранными для каждого случая из группы, состоящей из -CF3, -OCH3, -OCF3 и -(CH2)0-20-COOH. В различных вариантах осуществления присутствуют 1, 2, 3 или 4 заместителя. Присутствие -(CH2)0-20-COOH приводит к продукции алкиловой кислоты. Не ограничивающие примеры алкиловых кислот, содержащих -(CH2)0-20-COOH, включают 2-норборнануксусную кислоту, трет-масляная кислота, 3-циклопентилпропионовую кислоту и им подобные.
Термин «галоид» охватывает фтор-, хлор-, бром- и йод-.
«Гетероалкил» относится к алкилу, где один или несколько атомов углерода в углеводородной группе замещены одной или несколькими из следующих групп: амино, амидо, -О-, -S- или карбонил. В различных вариантах осуществления присутствуют 1 или 2 гетероатома.
«Замещенный гетероалкил» относится к гетероалкилу, где один или несколько атомов водорода углеводородной группы замещены одним или несколькими заместителями, выбранными из группы, состоящей из галогена (т.е. фтора, хлора, брома и йода), -OH, -CN, -SH, -NH2, -NHCH3, -NO2 и С1-20 алкила, где указанный С1-20 алкил необязательно может быть замещен одним или несколькими заместителями, выбранными независимо для каждого случая из группы, состоящей из галогенов, -CF3, -OCH3, -OCF3 и -(CH2)0-20-COOH. В различных вариантах осуществления присутствуют 1, 2, 3 или 4 заместителя.
«Алкенил» относится к углеводородной группе, составленной из двух или более углеродов, где присутствуют одна или несколько межуглеродные двойные связи. Алкенильная углеводородная группа может быть прямоцепочечной или содержать одну или несколько ветвей или циклических групп.
«Замещенный алкенил» относится к алкенилу, где один или несколько водородов замещены одним или несколькими заместителями, выбранными из группы, состоящей из группы, состоящей из галогена (т.е. фтора, хлора, брома и йода), -ОН, -CN, -SH, -NH2, -NHCH3, -NO2 и С1-20 алкила, где указанный С1-20 алкил необязательно может быть замещен одним или несколькими заместителями, независимо выбранными для каждого случая из группы, состоящей из -CF3, -OCH3, -OCF3 и -(CH2)0-20-COOH. В различных вариантах осуществления присутствуют 1, 2, 3 или 4 заместителя.
«Арил» относится к необязательно замещенной ароматической группе, по меньшей мере, с одним кольцом, имеющим сопряженно связанную pi-электронную систему, содержащую до трех сопряженно связанных или конденсированных кольцевых систем. Арил включает карбоциклическую арильную, гетероциклическую арильную и биарильную группы. Предпочтительно арил представляет собой 5- или 6-членное кольцо. Предпочтительные атомы для гетероциклического арила представляют собой один или несколько из серы, кислорода и/или азота. Не ограничивающие примеры арила включают фенил, 1-нафтил, 2-нафтил, индол, хинолин, 2-имидазол, 9-антрацен и им подобные. Арильные заместители выбраны из группы, состоящей из С1-20 алкила, С1-20 алкокси, галогена (т.е. фтора, хлора, брома и йода), -ОН, -CN, -SH, -NH2, -NO2, -С1-20 алкила, замещенного галогеном, -CF3, -OCF3 и -(CH2)0-20-COOH. В различных вариантах осуществления присутствуют 1, 2, 3 или 4 заместителя.
«Алкиларил» относится к «алкилу», соединенному с «арилом».
Термин «(С1-12)углеводородная часть» охватывает алкил, алкенил и алкинил и в случае алкенила и алкинила имеется С2-12.
Используемый в настоящем описании термин «нормализующие» функции или виды активности относится к тем типам функций, которые можно считать участвующими в нормальной функции или гомеостазе организма. Такие функции включают без ограничения виды активности и функции, воздействующие на температуру тела, артериальное давление, частоту сердечных сокращений, сосудистый тонус, мозговой кровоток, уровни глюкозы в крови, и им подобные.
Используемые в настоящем описании соединения, которые считаются «селективными» к определенному рецептору меланокортина, представляют собой соединения, обладающие функциональной активностью, характеризуемой ЕС50, по меньшей мере, примерно в 2 раза, по меньшей мере, примерно в 5 раз, по меньшей мере, примерно в 10 раз, по меньшей мере, примерно в 15 раз, по меньшей мере, примерно в 17 раз, по меньшей мере, примерно в 90 раз, по меньшей мере, примерно в 200 раз, по меньшей мере, примерно в 3000 раз, или, по меньшей мере, примерно в 10000 раз, или даже большую селективность в отношении любого рецептора меланокортина по сравнению с любым другим рецептором меланокортина. Например, селективный агонист рецептора меланокортина-4 по изобретению проявляет функциональную активность, характеризуемую ЕС50, по меньшей мере, в 15 раз более селективную в отношении человеческого рецептора меланокортина-4, чем в отношении человеческого рецептора меланокортина-1, человеческого рецептора меланокортина-3 и человеческого рецептора меланокортина-5. Также, например, селективный агонист рецептора меланокортина-4 по изобретению проявляет функциональную активность, характеризуемую ЕС50, по меньшей мере, в 17 раз более селективную в отношении человеческого рецептора меланокортина-4, чем в отношении человеческого рецептора меланокортина-3.
Синтез
Пептиды по изобретению можно получить стандартным твердофазным пептидным синтезом. См., например, Stewart, J.M., et al., Solid Phase Synthesis (Pierce Chemical Co., 2d ed. 1984). Заместители R2 и R3 указанной выше генерической формулы могут быть присоединены к свободному амину N-концевой аминокислоты стандартными способами, известными в данной области. Например, алкильные группы, такие как (С1-30)алкил, могут быть присоединены с использованием восстановительного алкилирования. Гидроксиалкильные группы, например (С1-30)гидроксиалкил, также могут быть присоединены с использованием восстановительного алкилирования, где свободная гидроксильная группа защищена сложным трет-бутиловым эфиром. Ацильные группы, например СОЕ1, могут быть присоединены связью свободной кислоты, например Е1СООН, со свободным амином N-концевой аминокислоты смешиванием полной смолы с 3 молярными эквивалентными и свободной кислоты, и диизопропилкарбодиимида в метиленхлориде в течение 1 ч. Если свободная кислота содержит свободную гидроксильную группу, например п-гидроксифенилпропионовую кислоту, затем соединение следует производить с дополнительными 3 молярными эквивалентами HOBt.
Когда R1 представляет собой -NH2, синтез пептида начинается с Fmoc-аминокислоты, которая соединяется с МВНА смолой амида Rink. Если R1 представляет собой -ОН, синтез пептида начинается с Fmoc-аминокислоты, которая соединяется со смолой Wang.
При синтезе пептида по настоящему изобретению, содержащему A6c и/или Aib, время соединения составляет 2 ч для этих остатков и остатка, непосредственно следующего за ними.
Следующие примеры описывают способы синтеза для получения пептидов по настоящему изобретению, причем эти способы хорошо известны специалистам в данной области. Другие способы также известны специалистам в данной области. Примеры представлены с целью иллюстрации и никоим образом не предназначены для ограничения объема настоящего изобретения.
ПРИМЕРЫ
Пример 1: Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH 2 SEQ ID NO:7
Указанный в заголовке пептид был синтезирован на множественном пептидном синтезаторе Advanced ChemTech (Louisville, KY 40228) модели 396® с использованием фторфенилметилоксикарбонильного (Fmoc) химии. Использовали 4-метилбензилгидриламиновую (МВНА) смолу амида Rink (Novabiochem®, San Diego, CA) с замещением 0,58 ммоль/г. Использованные Fmoc аминокислоты (Novabiochem®, CA и Chem-Impex®, IL) представляли собой Fmoc-Nle-OH, Fmoc-Cys(Trt)-OH, Fmoc-D-Ala-OH, Fmoc-His(Trt)-OH, Fmoc-D-Phe-OH, Fmoc-Arg(Pbf)-OH и Fmoc-Trp(Boc)-OH. Синтез проводили в масштабе 0,035 ммоль. Группы Fmoc удаляли обработкой 25% пиперидином в N,N-диметилформамиде (DMF) в течение 30 мин. На каждой стадии соединения Fmoc аминокислоту (10 экв., 0,35 ммоль), N,N-диизопропилкарбодиимид (DIC) (10 экв., 0,35 ммоль) и 1-гидроксибензотриазол (HOBt) (10 экв., 0,35 ммоль) использовали в DMF (1,4 мл). После промывания DMF выполняли двойное соединение с Fmoc-аминокислотой (10 экв., 0,35 ммоль), гексафторфосфатом 2-(1-Н-бензотриазол-1-ил)-1,1,2,3-тетраметилурония (HBTU) (8 экв., 0,28 ммоль), HOBT (10 экв., 0,35 ммоль) и диизопропилэтиламином (DIEA) (20 экв., 0,7 ммоль) в DMF (1,26 мл). Множественный пептидный синтезатор АСТ 396® был запрограммирован для выполнения следующего цикла реакции: (1) промывание DMF, (2) удаление защитной группы Fmoc 25% пиперидином в DMF, (4) соединение с Fmoc аминокислотой в присутствии DIC и HOBt в течение 1 ч, (5) промывание DMF, (6) двойное связывание с той же с Fmoc аминокислотой, что на стадии 4, в присутствии HBTU, HOBt и DIEA в течение 1 ч. Смолу соединяли последовательно в соответствии с последовательностью указанного в заголовке пептида. После сборки пептидной цепи и удаления последней Fmoc-защитной группы смолу полностью промывали путем использования DMF и дихлорметана (DCM).
Для расщепления указанного в заголовке пептида смолу обрабатывали раствором (1,5 мл) TFA, H2O и триизопропилсилана (TIS) (об./об./об.: 90/6,2/3,8) в течение 2 ч при комнатной температуре. Смолу отфильтровывали и фильтрат выливали в 30 мл простого эфира. Осадок собирали центрифугированием. Этот неочищенный продукт растворяли в воде (~7 мл) и рН водного раствора доводили до ~7,5 добавлением 2N NH4HCO3. Раствор открывали для доступа воздуха на 72 ч при комнатной температуре. Полученный неочищенный продукт очищали на системе препаративной ВЭЖХ в обращенной фазе колонкой (4×43 см) C18 DYNAMAX-100® A0 (Varian®, Walnut Creek, CA). Колонку элюировали в течение приблизительно 1 ч, используя линейный градиент 85% А:15% В до 30% А:70% В, где А представлял собой 0,1% TFA в воде, а В представлял собой 0,1% TFA в ацетонитриле. Фракции проверяли аналитической ВЭЖХ, и те, которые содержали чистый продукт, объединяли и лиофилизировали до сухости для получения 10,3 мг (выход 27%) белого твердого вещества. Чистоту анализировали с использованием ВЭЖХ и обнаружили, что она составляла приблизительно 88%. Анализ электрораспылительной ионизацией масс - спектрометрией (ESI-MS) дал молекулярную массу на уровне 1073,6 (что согласуется с рассчитанной молекулярной массой 1074,3).
Пример 2: Ac-Cha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH 2 SEQ ID NO:6
Указанный в заголовке пептид был синтезирован на пептидном синтезаторе Applied Biosystems® (Foster City, CA) модели 430А, который был модифицирован для проведения ускоренного твердофазного пептидного синтеза с использованием Boc-химии. См. Schnolzer, et al., Int. J. Peptide Protein Res., 40:180 (1992). Использовали 4-метилбензгидриламиновую (МВНА) смолу (Peninsula®, Belmont, CA) с замещением 0,91 ммоль/г. Использованные следующие Вос аминокислоты (Novabiochem®, San Diego, CA и Chem-Impex®, Wood Dale, IL): Boc-Cha-OH, Boc-Asp(OFm)-OH, Boc-His(DNP)-OH, Boc-D-Phe-OH, Boc-Arg(Tos)-OH, Boc-Trp(For)-OH, Boc-Gaba-OH и Boc-Lys(Fmoc)-OH. Синтез проводили в масштабе 0,20 ммоль. Группы Boc удаляли обработкой 100% TFA в течение 2×1 мин. Вос аминокислоты (2,5 ммоль) предварительно активировали HBTU (2,0 ммоль) и DIEA (1,0 мл) в 4 мл DMF и соединяли без предварительной нейтрализации соли TFA пептида-смолы. Продолжительность соединения составляла 5 мин.
В конце сборки Boc-Asp(OFm)-His(DNP)-D-Phe-Arg(Tos)-Trp(For)-Gaba-Lys(Fmoc)-MBHA пептид-смолу переносили в реакционный сосуд на вибростенде. Смолу обрабатывали дважды 25% пиперидином в DMF в течение 15 мин за процедуру, промывали DMF и встряхивали с гексафторфосфатом бром-трис-пирролидинфосфония (PyBrOP) (6 экв., 0,3 ммоль), DIEA (1 мл) и 4-(диметиламино)пиридином (DMAP) (24 мг) в DMF (2 мл) в течение 12 ч. После промывания DMF смолу обрабатывали дважды 100% TFA в течение 2 мин на обработку, промывали DMF и DCM и затем сушили под пониженным давлением. Одну четвертую часть пептида-смолы (0,05 ммоль) использовали для следующего соединения с Boc-Cha-OH (10 экв., 0,5 ммоль) в присутствии HBTU (9 экв., 0,45 ммоль) и DIEA (0,25 мл) в DMF в течение 10 мин. После снятия защиты 100% TFA двумя приемами, длящимися приблизительно по 2 мин каждый, пептид-смолу затем промывают DMF. Конечную стадию кэппинга проводили встряхиванием смолы с уксусным ангидридом (40 экв., 2,0 ммоль) и DIEA (20 экв., 1,0 ммоль) в DMF в течение 1 ч. После промывания DMF смолу обрабатывали дважды раствором 20% меркаптоэтанола/10% DIEA в DMF, причем каждая обработка продолжалась приблизительно 30 мин, для удаления группы DNP на гистидиновой боковой цепи. Формильную группу на боковой цепи триптофана удаляли встряхиванием с раствором 15% этаноламина/15% воды/70% DMF дважды в течение 30 мин на встряхивание. Петид-смолу промывали DMF и DCM и сушили при пониженном давлении. Окончательное расщепление проводили перемешиванием пептида-смолы в 10 мл HF, содержащих 1 мл анисола и дитиотреитола (30 мг), при 0°С в течение 75 мин. HF удаляли потоком азота. Остаток промывали простым эфиром (6×10 мл) и экстрагировали 4N HOAc (6×10 мл).
Пептидную смесь в водном экстракте очищали на препаративной высокоэффективной жидкостной хроматографии (ВЭЖХ) в обращенной фазе с использованием обращеннофазовой колонки VYDAC® C18 (Nest Group®, Southborough, MA). Колонку элюировали линейным градиентом (с 10% до 50% раствора В в течение 40 мин) при скорости потока 10 мл/мин (раствор А = вода, содержащая 0,1% TFA; Раствор В = ацетонитрил, содержащий 0,1% TFA). Фракции собирали и проверяли на аналитической ВЭЖХ. Фракции, содержащие продукт, объединяли и лиофилизировали до сухости. Получали 5,1 мг белого твердого вещества. Выход составил 8,9%. Чистота составила 94,5% на основании анализа аналитической ВЭЖХ. Анализ электрораспылительным масс - спектрометром (MS(ES))S дал молекулярную массу на уровне 1148,5 (что согласуется с рассчитанной молекулярной массой 1148,3).
Другие пептиды по изобретению средний специалист в данной области может получить, используя синтетические процедуры, аналогичные тем, которые в целом описаны выше в настоящем описании, и/или тем, раскрытым, в частности, в приведенных выше примерах, как и соединения, изображенные в таблицах 1А и 1В.
Следующие примеры можно получить в соответствии с целесообразными процедурами, описанными выше:
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-β-Ala-Lys)-NH2; SEQ ID NO:1
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-A6c-Lys)-NH2; SEQ ID NO:1
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Ahx-Cys)-NH2; SEQ ID NO:2
D-Phe-c(Cys-His-D-Phe-Arg-Trp-Ala-D-Cys)-Thr-NH2; SEQ ID NO:3
D-Phe-c(Cys-His-D-Phe-Arg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:3
D-Phe-c(Cys-His-D-Phe-Arg-Trp-Gaba-D-Cys)-Thr-NH2; SEQ ID NO:3
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Apn-Cys)-NH2; SEQ ID NO:2
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-Apn-Lys)-NH2; SEQ ID NO:4
Ac-A6c-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:5
Ac-D-2-Nal-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:6
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:6
Ac-Nle-c(Cys-β-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:7
Ac-Nle-c(Cys-Gaba-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:7
Ac-Nle-c(Cys-Aib-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:7
Ac-Nle-c(Cys-Gly-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:7
Ac-Nle-c(D-Cys-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:8
Ac-Nle-c(D-Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:8
Ac-Nle-c(D-Cys-β-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:8
Ac-Nle-c(D-Cys-Gaba-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:8
Ac-Nle-c(D-Cys-Aib-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:8
Ac-Nle-c(D-Cys-Gly-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:8
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:9
Ac-Nle-c(Cys-β-Ala-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:9
Ac-Nle-c(Cys-Gaba-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:9
Ac-Nle-c(Cys-Aib-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:9
Ac-Nle-c(Cys-Gly-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:9
Ac-Nle-c(D-Cys-Ala-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:10
Ac-Nle-c(D-Cys-D-Ala-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:10
Ac-Nle-c(D-Cys-β-Ala-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:10
Ac-Nle-c(D-Cys-Gaba-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:10
Ac-Nle-c(D-Cys-Aib-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO:10
Ac-Oic-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-Chg-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-hCha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-D-Cha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-Nip-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-hPro-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-hLeu-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-hCha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-Phe-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-D-Phe-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-D-Chg-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
н-бутаноил-Cha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:12
Ac-hPhe-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-β-hMet-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-Gaba-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:11
Ac-Cha-c(Asp-His-D-Phe-Arg-D-Trp-Ala-Lys)-NH2; SEQ ID NO:13
Ac-hCha-c(Asp-His-D-Phe-Arg-D-Trp-Ala-Lys)-NH2; SEQ ID NO:13
Ac-Leu-c(Asp-His-D-Phe-Arg-D-Trp-Ala-Lys)-NH2; SEQ ID NO:13
Ac-hLeu-c(Asp-His-D-Phe-Arg-D-Trp-Ala-Lys)-NH2; SEQ ID NO:13
Ac-Phe-c(Asp-His-D-Phe-Arg-D-Trp-Ala-Lys)-NH2; SEQ ID NO:13
Ac-Nle-c(Asp-His-D-Phe-Arg-D-Trp-D-Ala-Lys)-NH2; SEQ ID NO:14
Ac-Nle-c(Asp-His-D-Phe-Arg-D-Trp-β-Ala-Lys)-NH2; SEQ ID NO:14
Ac-Nle-c(Asp-His-D-Phe-Arg-D-Trp-Gaba-Lys)-NH2; SEQ ID NO:14
Ac-Nle-c(Asp-His-D-Phe-Arg-D-Trp-Aha-Lys)-NH2; SEQ ID NO:14
Ac-Nle-c(Asp-His-D-Phe-Arg-D-Trp-Apn-Lys)-NH2; SEQ ID NO:14
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-Apn-Cys)-NH2; SEQ ID NO:15
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-Gaba-Cys)-NH2; SEQ ID NO:15
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-Ahx-Cys)-NH2; SEQ ID NO:15
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-β-Ala-Cys)-NH2; SEQ ID NO:15
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-D-Ala-Cys)-NH2; SEQ ID NO:15
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; SEQ ID NO:16
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-2-Nal-Cys)-NH2; SEQ ID NO:16
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-1-Nal-Cys)-NH2; SEQ ID NO:16
н-бутаноил-Nle-c(Cys-D-Ala-His-D-Phe-Arg-2-Nal-Cys)-NH2; SEQ ID NO:17
н-бутаноил-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:17
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-2-Nal-Cys)-NH2; SEQ ID NO:18
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-1-Nal-Cys)-NH2; SEQ ID NO:18
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Bal-Cys)-NH2; SEQ ID NO:18
Ac-Nle-c(Cys-D-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:61
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-D-Ala-Lys)-NH2; SEQ ID NO:19
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-Bal-Cys)-NH2; SEQ ID NO:20
Ac-Nle-c(Pen-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:21
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO:22
Ac-Nle-c(Pen-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO:22
D-Phe-c(Cys-His-D-Phe-hArg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:23
D-Phe-c(Cys-His-D-(Et)Tyr-Arg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:24
D-Phe-c(Cys-His-D-Phe-Arg-Bip-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:25
D-Phe-c(Cys-His-D-(Et)Tyr-hArg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:24
D-Phe-c(Cys-His-D-Phe-hArg-Bip-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:26
D-Phe-c(Cys-His-D-(Et)Tyr-hArg-Bip-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO:26
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Gly-Cys)-NH2; SEQ ID NO:54
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-D-Ala-Cys)-NH2; SEQ ID NO:54
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-β-Ala-Cys)-NH2; SEQ ID NO:54
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:54
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Apn-Cys)-NH2; SEQ ID NO:54
Nle-c(Cys-His-D-Phe-Arg-Trp-Apn-Cys)-NH2; SEQ ID NO:27
Ac-Nle-c(Asp-D-Ala-His-D-Phe-Arg-Trp-Lys)-NH2; SEQ ID NO:28
Ac-Nle-c(Asp-D-Ala-His-D-Phe-Arg-Bal-Lys)-NH2; SEQ ID NO:28
Ac-c(Cys-Glu-His-D-Phe-Arg-Trp-Ala-Cys)-NH2; SEQ ID NO:55
Ac-c(Cys-Glu-His-D-Phe-Arg-2-Nal-Ala-Cys)-NH2; SEQ ID NO:55
Ac-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Ala-Cys)-NH2; SEQ ID NO:56
Ac-c(Cys-D-Ala-His-D-Phe-Arg-2-Nal-Ala-Cys)-NH2; SEQ ID NO:56
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Ala-Cys)-NH2; SEQ ID NO:57
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-β-Ala-Cys)-NH2; SEQ ID NO:57
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:57
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-OH; SEQ ID NO:29
Ac-Nle-c(Cys-D-Abu-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:30
Ac-Nle-c(Cys-D-Val-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:30
Ac-Nle-c(Cys-D-Ile-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:30
Ac-Nle-c(Cys-D-Leu-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:30
Ac-Nle-c(Cys-D-Tle-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:30
Ac-Nle-c(Cys-D-Cha-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:30
Ac-Nle-c(Pen-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:31
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO:32
Ac-Nle-c(Pen-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO:32
Ac-Leu-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:33
Ac-Cha-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:33
Ac-Ile-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:33
Ac-Phe-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:33
Ac-Val-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:33
Ac-2-Nal-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:33
Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:34
Phe-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:34
Ac-Nle-c(Cys-3-Pal-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:35
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-OH; SEQ ID NO:36
Ac-Nle-c(Cys-His-Phe-Arg-D-Trp-Gaba-Cys)-NH2; SEQ ID NO:37
Ac-Nle-c(Asp-D-Ala-His-D-Phe-Arg-Bal-Ala-Lys)-NH2; SEQ ID NO:58
Ac-Nle-c(Asp-His-D-2-Nal-Arg-Trp-Ala-Lys)-NH2; SEQ ID NO:38
Ac-Nle-c(Asp-His-D-2-Nal-Arg-Trp-β-Ala-Lys)-NH2; SEQ ID NO:38
Ac-Nle-c(Cys-His-D-2-Nal-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO:39
Ac-Nle-c(Cys-His-D-2-Nal-Arg-Trp-Ahx-Cys)-NH2; SEQ ID NO:39
Ac-hPhe-c(Asp-His-D-2-Nal-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:40
Ac-Cha-c(Asp-His-D-2-Nal-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO:40
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-β-Ala-Lys)-OH; SEQ ID NO:41
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Ahx-Cys)-OH; SEQ ID NO:42
D-Phe-c(Cys-His-D-Phe-Arg-Trp-Ala-D-Cys)-Thr-OH; SEQ ID NO:43
D-Phe-c(Cys-His-D-Phe-Arg-Trp-β-Ala-D-Cys)-Thr-OH; SEQ ID NO:43
D-Phe-c(Cys-His-D-Phe-Arg-Trp-Gaba-D-Cys)-Thr-OH; SEQ ID NO:43
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Apn-Cys)-OH; SEQ ID NO:42
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-Apn-Lys)-OH; SEQ ID NO:41
Ac-Cha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO:44
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO:44
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-OH; SEQ ID NO:29
Ac-Chg-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO:44
Ac-D-Cha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO:44
Ac-hCha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO:44
Ac-D-Chg-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO:44
Ac-hPhe-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO:44
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-Gaba-Cys)-OH; SEQ ID NO:45
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-Ahx-Cys)-OH; SEQ ID NO:45
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-β-Ala-Cys)-OH; SEQ ID NO:45
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-D-Ala-Cys)-OH; SEQ ID NO:45
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-OH; SEQ ID NO:46
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-2-Nal-Cys)-OH; SEQ ID NO:46
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-1-Nal-Cys)-OH; SEQ ID NO:46
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-Bal-Cys)-OH; SEQ ID NO:46
Ac-Nle-c(Pen-D-Ala-His-D-Phe-Arg-Trp-Cys)-OH; SEQ ID NO:47
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-OH; SEQ ID NO:29
Ac-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:50
Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO:50
Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO:51
Ac-D-Arg-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO:52
Ac-Arg-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO:52
Ac-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO:51
Ac-D-Arg-c(Asp-His-D-Phe-Arg-Trp-Ala-Lys)-NH2; SEQ ID NO:53
Ac-Arg-c(Asp-His-D-Phe-Arg-Trp-Ala-Lys)-NH2; SEQ ID NO:53
Ac-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; SEQ ID NO:49 и
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-OH SEQ ID NO:48.
Другие пептиды по изобретению средний специалист в данной области может получить, используя синтетические процедуры, аналогичные тем, которые в целом описаны выше в настоящем описании, и/или тем, раскрытым, в частности, в приведенных выше примерах, как и соединения, изображенные в таблицах 1А и 1В.
Таблицы 1А и 1В - Молекулярная масса и чистота выбранных вариантов осуществления
Пример 3: Исследования in vitro
Соединения по настоящему изобретению могут и были испытаны на наличие активности в качестве лигандов одного или нескольких рецепторов меланокортина в соответствии со следующими процедурами. Специалисту в данной области было бы известно, что процедуры, аналогичные тем, которые описаны в настоящем описании, можно использовать для анализа активности связывания соединений по изобретению с молекулами рецепторов меланокортина.
Анализы связывания лигандов, меченных радиоактивным изотопом
Клеточные мембраны, использованные для анализов связывания in vitro, получали из трансгенных клеток СНО-К1, устойчиво экспрессирующих желаемый подтип 1, 3, 4 или 5 рецептора hMC-R. Клетки СНО-K1 обрабатывали ультразвуком (Branson®, установка 7, приблизительно 30 с) в ледяной 50 мМ Tris-HCl при рН 7,4 и затем центрифугировали при 30000 g в течение 10 мин приблизительно при 4°С. Гранулы повторно суспендировали в этом же буфере и центрифугировали при 50000 g в течение 10 мин приблизительно при 4°С. Промытые гранулы, содержащие клеточные мембраны, хранили приблизительно при -80ºС.
Конкурентное ингибирование [125I](Tyr2)-(Nle4-D-Phe7)α-MSH ([125I]-NDP-α-MSH, Amersham Biosciences®) связывания проводили в полипропиленовых 96-луночных планшетах. Клеточные мембраны (1-10 мкг белка/лунку), полученные, как описано выше, инкубировали в 50 мМ Tris-HCl при рН 7,4, содержащем 0,2% бычий сывороточный альбумин (BSA), 5 мМ MgCl2, 1 мМ CaCl2 и 0,1 мг/мл бацитрацина с увеличивающимися концентрациями испытуемого соединения и 0,1-0,3 нМ [125I]-NDP-α-MSH в течение приблизительно 90-120 мин приблизительно при 37°С. Связанный лиганд [125I]-NDP-α-MSH отделяли от свободного [125I]-NDP-α-MSH фильтрацией через стекловолоконные фильтровальные пластины GF/C (Unifiller®; Packard), предварительно пропитанные 0,1% (мас./об.) полиэтиленимином (PEI), используя сборщик клеток Packard Filtermate®. Фильтры промывали 3 раза 50 мМ Tris-HCl при рН 7,4 при температуре приблизительно 0-4°С и затем анализировали на радиоактивность с использованием сцинтилляционного счетчика Packard Topcount®. Данные связывания анализировали нелинейным регрессионным анализом с помощью компьютера (подбор XL; IDBS).
Выбор предпочтительных вариантов осуществления испытывали с использованием обсужденного выше анализа и констант связывания (Ki в нМ) представлены в таблицах 2А, 2В и 2С.
Таблицы 2А, 2В и 2С - Данные анализа связывания лигандов, меченных радиоактивным изотопом, по выбранным соединениям
hMC1-R
hMC3-R
hMC4-R
hMC5-R
hMC1-R/
MC4-R
hMC1-R
hMC3-R
hMC4-R
hMC5-R
hMC1-R
/MC4-R
/MC4-R
Биологический анализ циклического АМФ
Уровни внутриклеточного циклического АМФ (цАМФ) определяли анализом электрохемилюминесценции (ECL) (Meso Scale Discovery®, Gaithersburg, MD; далее именуемый MSD). Клетки СНО-К1, устойчиво экспрессирующие подтипы рецепторов hMC, суспендировали в аналитическом буфере RMPI 1640® (буфер RMPI 1640 содержит 0,5 мМ изобутилметилксантина (IBMX) и 0,2% белковую смесь (блокатор А MSD)). Трансгенные клетки СНО-К1, устойчиво экспрессирующие подтипы 1, 3, 4 или 5 рецептора hMC, подавали при плотности приблизительно 7000 клеток/лунку в 384-луночные планшеты Multi-Array® (MSD), содержащие интегрированные углеродные электроды и покрытые антителом против цАМФ. Добавляли увеличивающиеся концентрации испытуемых соединений и клетки инкубировали в течение приблизительно 40 мин приблизительно при 37°С. После этой инкубации добавляли лизисный буфер (забуференный HEPES солевой раствор с MgCl2 и Triton X-100® при рН 7,3), содержащий 0,2% белковую смесь и 2,5 нМ TAG™ меченного рутением цАМФ (MSD), и клетки инкубировали в течение приблизительно 90 мин при комнатной температуре. В конце второго периода инкубации добавляли буфер считывания (забуференный Tris раствор, содержащий совместный реагент ECL и Triton X-100 при рН 7,8) и сразу определяли уровни цАМФ в клеточных лизатах выявлением ECL считывающим устройством Sector Imager 6000 reader® (MSD). Данные анализировали, используя нелинейный регрессионный анализ с помощью компьютера (подбор XL; IDBS) и представляли в виде или величины ЕС50 или величины Kb.
ЕС50 представляет концентрацию соединения агониста, требуемую для получения 50% максимальной реакции, например 50% максимального уровня цАМФ, по данным определения с использованием описанного выше анализа. Величина Kb отражает активность антагониста и определяется анализом Schild. Вкратце, кривые зависимости реакции от концентрации для агониста получают в присутствии возрастающих концентраций антагониста. Величина Kb представляет собой концентрацию антагониста, которая бы вызвала двукратный сдвиг кривой зависимости реакции от концентрации для агониста. Она рассчитывается экстраполированием линии на графике Schild до нуля на у-оси.
Отбор соединений испытывали, используя обсужденные выше анализы, и результаты представлены в таблицах 3А, 3В и 3D.
Таблицы 3А, 3В, 3С и 3D - Данные биологического анализа цАМФ для отобранных соединений
hMC1-R
hMC3-R
hMC4-R
hMC5-R
hMC1-R
/MC4-R
Таблица 3В
hMC1-R
hMC3-R
hMC4-R
hMC5-R
hMC1-R
/MC4-R
Таблица 3D
Пример 4: Исследования in vivo
Соединения по настоящему изобретению могут и были испытаны на наличие влияния на потребление пищи и/или массу тела в соответствии со следующими процедурами. Специалисту в данной области должно быть известно, что для анализа влияния соединений по изобретению на потребление пищи и/или массу тела можно использовать процедуры, аналогичные тем, которые описаны в настоящем описании.
Ниже приведены соединения лигандов, активирующие рецепторы меланокортина, испытанные в исследованиях in vivo (таблица 4):
Эксперименты по острому кормлению (после голодания)
Самцов крыс Sprague Dawley (250 г) содержали в отдельных клетках и поддерживали чередование света и темноты по 12 ч. Крысы голодали в течение 18 ч перед началом эксперимента при доступе к воде без ограничения. Во время 0 крысам подкожно (п/к) инъецировали выбранные соединения в дозах или 500, или 100 нмоль/кг, или носитель и им давали корм. Индивидуальное потребление корма измеряли примерно через 1, 2, 3, 4, 5 и 6 ч после инъекции. Данные по отобранным соединениям по изобретению представлены на фиг.1А и 1В.
Эксперименты по острому кормлению (без голодания)
Самцов крыс Sprague Dawley (250 г) содержали в отдельных клетках и поддерживали чередование света и темноты по 12 ч. Корм и вода были доступны без ограничения в течение всего эксперимента. Во время 0 крысам п/к инъецировали соединение в дозах или 500, или 100 нмоль/кг, или носитель. Индивидуальное потребление корма измеряли примерно через 1, 2, 3, 4, 5 и 6 ч после инъекции.
Эксперименты по хроническому кормлению
Самцов крыс Sprague Dawley (250 г) содержали в отдельных клетках и поддерживали чередование света и темноты по 12 ч при доступе к пище и воде без ограничения. Крысам п/к 3х/д (приблизительно в 08:00 ч, 12:00 ч и в 16:00 ч) инъецировали соединение в различных дозах или носитель в течение 7 д. Ежедневно измеряли индивидуальную массу тела и потребление пищи. Данные по отобранным соединениям по изобретению представлены на фиг.2А и 2В, фиг.3А и 3В и фиг.4А и 4В.
Введение и применение
Пептиды по настоящему изобретению можно получить в форме фармацевтически приемлемых солей. Примеры таких солей включают без ограничения соли, образованные с органическими кислотами (например, уксусной, молочной, малеиновой, лимонной, яблочной, аскорбиновой, янтарной, бензойной, метансульфоновой, толуолсульфоновой или памоевой кислотой), неорганическими кислотами (например, хлористоводородной кислотой, серной кислотой или фосфорной кислотой) и полимерными кислотами (например, дубильной кислотой, карбоксиметилцеллюлозой, полимолочной, полигликолевой или сополимерами полимолочной-гликолевой кислот). Типичный способ получения соли пептида по настоящему изобретению хорошо известен в данной области и может быть осуществлен стандартными способами солевого обмена. Соответственно, соль TFA пептида по настоящему изобретению (соль TFA получается в результате очистки пептида путем использования препаративной ВЭЖХ, элюирования TFA, содержащей буферные растворы) можно превратить в другую соль, такую как ацетат, растворением пептида в небольшом количестве 0,25 N водного раствора уксусной кислоты. Полученный раствор наносится на колонку полупрепаративной ВЭЖХ (Zorbax®, 300 SB, C-8). Колонку элюировали: (1) 0,1N водным раствором ацетата аммония в течение 0,5 ч; (2) 0,25N водным раствором уксусной кислоты в течение 0,5 ч; и (3) линейным градиентом (от 20% до 100% раствора В в течение 30 мин) при скорости потока 4 мл/мин (раствор А представляет собой 0,25N водный раствор уксусной кислоты; раствор В представляет собой 0,25N раствор уксусной кислоты в ацетонитриле/воде, 80:20). Фракции, содержащие пептид, собирают и лиофилизируют до сухости.
Как хорошо известно специалистам в данной области, известные и потенциальные виды применения пептидов с активностью агониста или антагониста рецепторов меланокортина (MC-R) разнообразны и многочисленны; таким образом, введение соединений по настоящему изобретению с целью вызова эффекта агониста может иметь такие же эффекты и виды применения, как сам меланокортин.
Соответственно, настоящее изобретение включает в свой объем фармацевтические композиции, включающие в качестве активного ингредиента, по меньшей мере, одно из соединений формулы (I) в ассоциации с фармацевтически приемлемым носителем.
Дозировка активного ингредиента в композициях по настоящему изобретению может варьироваться; однако необходимо, чтобы количество активного ингредиента было таким, чтобы была получена подходящая дозировка. Выбранная дозировка зависит от желаемого терапевтического эффекта, от пути введения и от длительности лечения. В целом, эффективная дозировка для видов активности по настоящему изобретению находится в диапазоне от 1×10-7 до 200 мг/кг/д, предпочтительно от 1×10-4 до 100 мг/кг/д, которые можно вводить в виде одной дозы или разделенной на множественные дозы.
Соединения по настоящему изобретению можно вводить пероральным, парентеральным (например, внутримышечной, внутрибрюшинной, внутривенной или подкожной инъекцией или имплантатом), интраназальным, вагинальным, ректальным, сублингвальным или местным путями введения и могут составляться с фармацевтически приемлемыми носителями для предоставления лекарственных форм, целесообразных для каждого пути введения.
Твердые лекарственные формы для перорального введения включают капсулы, таблетки, пилюли, порошки и гранулы. В таких твердых лекарственных формах активное соединение смешано, по меньшей мере, с одним инертным фармацевтически приемлемым носителем, таким как сахароза, лактоза или крахмал. Такие лекарственные формы могут также включать, как в обычной практике, дополнительные вещества, отличные от таких инертных разбавителей, например смазывающие агенты, такие как стеарат магния. В случае капсул, таблеток и пилюль лекарственные формы могут также включать забуферивающие агенты. Таблетки и пилюли можно дополнительно получить с энтеросолюбильным покрытием.
Жидкие лекарственные формы для перорального введения включают фармакологически приемлемые эмульсии, растворы, суспензии, сиропы, эликсиры, содержащие инертные разбавители, обычно используемые в настоящей области, такие как вода. Кроме таких инертных разбавителей, композиции могут также включать адъюванты, такие как смачивающие агенты, эмульгирующие и суспендирующие агенты, и подслащивающие, придающие приятный вкус и запах агенты.
Препараты в соответствии с настоящим изобретением для парентерального введения включают стерильные водные или неводные растворы, суспензии или эмульсии. Примерами неводных растворителей или носителей являются пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло и кукурузное масло, желатин и инъецируемые сложные органические эфиры, такие как этилолеат. Такие лекарственные формы могут также содержать адъюванты, такие как консервирующие, смачивающие, эмульгирующие и диспергирующие агенты. Препараты можно стерилизовать, например, фильтрацией через удерживающий бактерии фильтр, включением стерилизующих агентов в композиции, облучением композиций или нагреванием композиций. Препараты можно также изготовить в форме стерильных твердых композиций, которые можно растворить в стерильной воде или какой-либо другой стерильной инъецируемой среде непосредственно перед применением.
Композиции для ректального или вагинального введения представляют собой предпочтительно суппозитории, которые могут содержать, в дополнение к активному веществу, эксципиенты, такие как масло какао или воск суппозиторий.
Композиции для интраназального или сублингвального введения также получают со стандартными эксципиентами, хорошо известными в данной области.
Кроме того, соединение по настоящему изобретению можно вводить в композиции длительного высвобождения, такие как композиции, описанные в следующих патентах и патентных заявках. В патенте США №5672659 речь идет о композициях длительного высвобождения, включающих биологически активный агент и сложный полиэфир. В патенте США №5595760 речь идет о композициях длительного высвобождения, включающих биологически активный агент в образующей гель форме. В патенте США №5821221 речь идет о полимерных композициях с длительным высвобождением, включающих биологически активный агент и хитозан. В патенте США №5916883 речь идет о композициях длительного высвобождения, включающих биологически активный агент и циклодекстрин. Положения указанных выше патентов и заявок включены в настоящее описание в качестве ссылки.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛИГАНДЫ РЕЦЕПТОРОВ МЕЛАНОКОРТИНОВ | 2006 |
|
RU2380372C2 |
| ЛИГАНДЫ РЕЦЕПТОРОВ МЕЛАНОКОРТИНОВ | 2006 |
|
RU2401841C2 |
| ПРИМЕНЕНИЕ МЕЛАНОКОРТИНОВ ДЛЯ ЛЕЧЕНИЯ ЧУВСТВИТЕЛЬНОСТИ К ИНСУЛИНУ | 2008 |
|
RU2453328C2 |
| СПОСОБ ЛЕЧЕНИЯ НАРУШЕНИЙ, АССОЦИИРОВАННЫХ С ПУТЕМ РЕЦЕПТОРА МЕЛАНОКОРТИНА 4 | 2016 |
|
RU2785889C1 |
| ЛИГАНДЫ МЕЛАНОКОРТИНОВЫХ РЕЦЕПТОРОВ, МОДИФИЦИРОВАННЫЕ ГИДАНТОИНОМ | 2008 |
|
RU2450017C2 |
| АГОНИСТЫ РЕЦЕПТОРОВ НЕЙРОМЕДИНА В И СОМАТОСТАТИНА | 2000 |
|
RU2263680C2 |
| ПЕПТИДНЫЕ КОМПОЗИЦИИ | 2014 |
|
RU2725150C2 |
| АНАЛОГИ АЛЬФА- и ГАММА-MSH | 2013 |
|
RU2668791C2 |
| АНАЛОГИ ГПП-1 | 1999 |
|
RU2208015C2 |
| ПЕПТИДНЫЕ ВЕКТОРЫ | 2004 |
|
RU2361876C2 |








































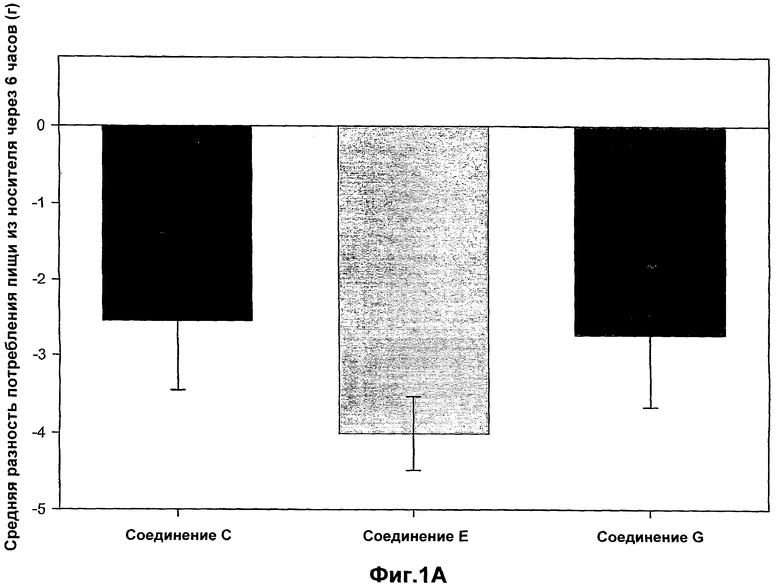
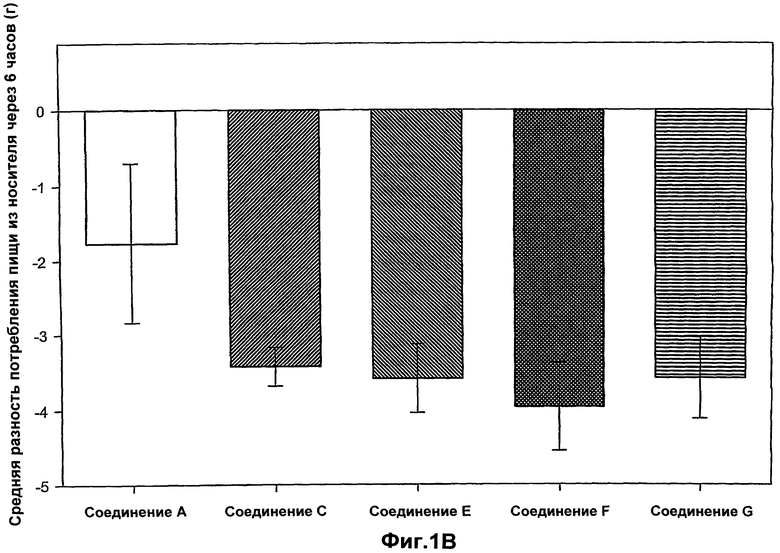

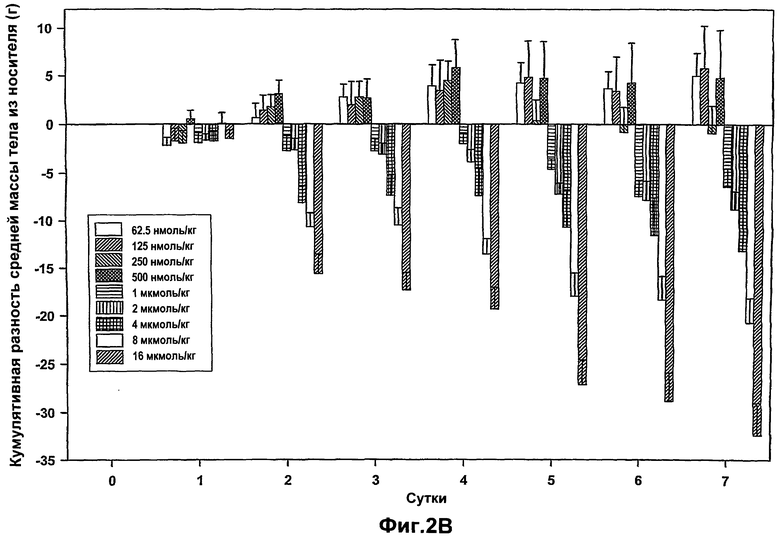
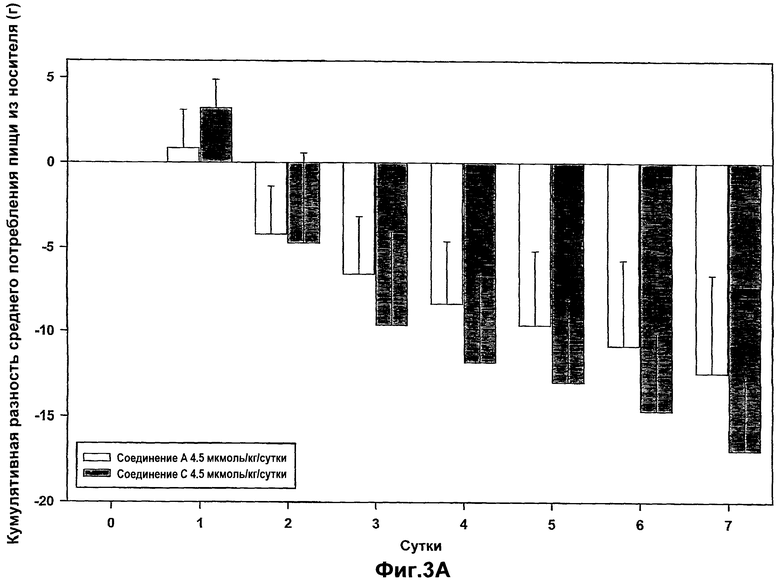
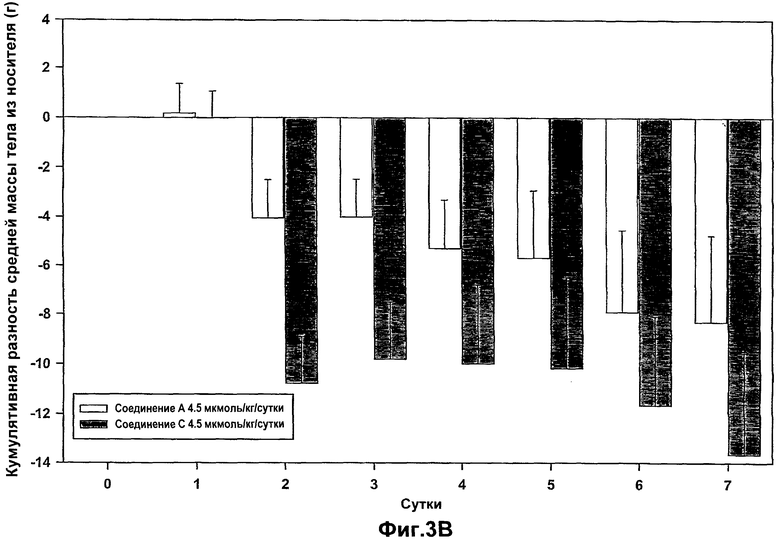

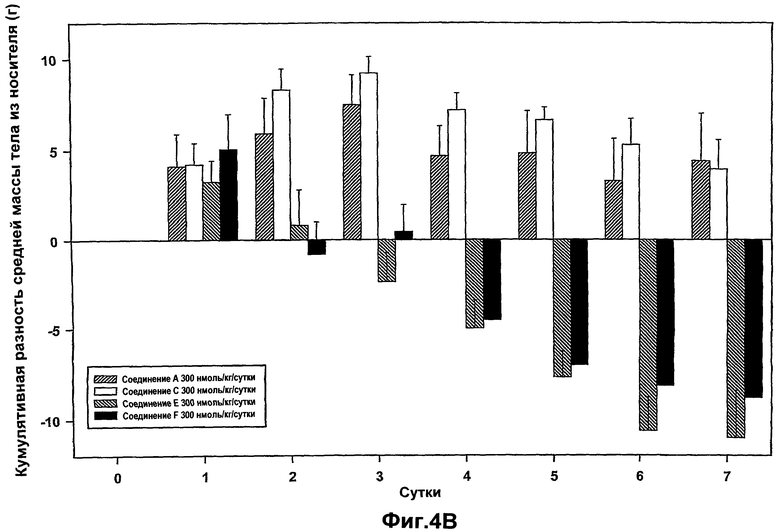
Настоящее изобретение относится к соединениям в соответствии с формулой (R2R3)-А1-c(А2-А3-А4-А5-A6-A7-A8-A9)-А10-R1 и их фармацевтически приемлемым солям, которые действуют в качестве лигандов для одного или более рецепторов меланокортина, к способам применения таких соединений для лечения млекопитающих и к фармацевтическим композициям, включающим указанные соединения. 4 н. и 25 з.п. ф-лы, 8 ил., 10 табл.
1. Соединение формулы (I):
(R2R3)-А1-c(А2-А3-А4-А5-A6-A7-A8-A9)-А10-R1,
где А1 представляет собой Асс, Arg, D-Arg, Cha, D-Cha, hCha, Chg, D-Chg, Gaba, Ile, Leu, hLeu, β-hMet, 2-Nal, D-2-Nal, Nip, Nle, Oic, Phe, D-Phe, hPhe, hPro, Val, HN-(CH2)m-C(O) или удален;
А2 представляет собой Cys, D-Cys, Pen или Asp;
А3 представляет собой β-Ala, Gaba, Aib, D-Ala, D-Glu, D-Abu, D-Val, D-Ile, D-Leu, D-Tle, D-Cha или удален;
А4 представляет собой His, 3-Pal или Phe;
А5 представляет собой D-Phe, D-2-Nal, Phe или D-(Et)Tyr;
А6 представляет собой Arg или hArg;
А7 представляет собой Trp, 1-Nal, 2-Nal, Bal, Bip или D-Trp;
А8 представляет собой Gly, D-Ala, Acc, Ala, β-Ala, Gaba, Apn, Ahx, Aha, HN-(CH2)s-C(O) или удален;
А9 представляет собой Cys, D-Cys, Pen или Lys;
А10 представляет собой Асс, HN-(CH2)t-C(O), Thr или удален;
R1 представляет собой -ОН или -NH2;
R2 и R3 независимо для каждого случая представляют собой Н или (С1-С6)ацил;
m независимо для каждого случая равно 1, 2, 3, 4, 5, 6 или 7;
s независимо для каждого случая равно 1, 2, 3, 4, 5, 6 или 7;
t независимо для каждого случая равно 1, 2, 3, 4, 5, 6 или 7;
при условии, что
(I) когда R2 представляет собой (С1-С6)ацил;
(II) или А3, или А8, или они оба должны присутствовать в указанном соединении;
(III) когда А2 представляет собой Cys, D-Cys или Pen, тогда А9 представляет собой Cys, D-Cys или Pen;
(IV) когда А2 представляет собой Asp, то А9 представляет собой Dab, Dap, Orn или Lys;
(V) когда А8 представляет собой Ala или Gly, то А1 не является Nle;
(VI) когда А1 удален, то R2 и R3 не могут оба представлять собой Н; и
(VII) указанное соединение не является соединением Ac-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2 (SEQ ID NO: 50),
или его фармацевтически приемлемая соль.
2. Соединение по п.1, где
А1 представляет собой А6с, Gaba, Nle, Met, Phe, D-Phe, D-2-Nal, hPhe, Chg, D-Chg, Cha, hCha, hPro, hLeu, Nip, β-hMet или Oic;
А2 представляет собой Cys, D-Cys, Pen или Asp;
А3 представляет собой D-Ala, D-Glu, β-Ala, Gaba, Aib или удален;
А4 представляет собой His;
А5 представляет собой D-Phe, D-2-Nal или D-(Et)Tyr;
А6 представляет собой Arg или hArg;
А7 представляет собой Trp, Bip, D-Trp, 1-Nal или 2-Nal;
А8 представляет собой А6с, Ala, β-Ala, Gaba, Apn или Ahx;
А9 представляет собой Cys, D-Cys, Pen или Lys; и
А10 представляет собой Thr или удален,
или его фармацевтически приемлемая соль.
3. Соединение по п.2, где
R2 и R3 независимо для каждого случая представляют собой Н, ацил, н-пропаноил или н-бутаноил,
или его фармацевтически приемлемая соль.
4. Соединение по п.1, где
А1 представляет собой Асс, Arg, D-Arg, Cha, D-Cha, hCha, Chg, D-Chg, Gaba, Ile, Leu, hLeu, β-hMet, 2-Nal, D-2-Nal, Nip, Nle, Oic, Phe, D-Phe, hPhe, hPro, Val или удален;
А2 представляет собой Cys, D-Cys, Pen или Asp;
А3 представляет собой β-Ala, Gaba, Aib, D-Ala, D-Abu, D-Cha, D-Ile, D-Leu, D-Tle, D-Val или удален;
А4 представляет собой His или 3-Pal;
А5 представляет собой D-Phe, D-2-Nal или D-(Et)Tyr;
А6 представляет собой Arg или hArg;
А7 представляет собой Trp, 1-Nal, 2-Nal, Bal, Bip или D-Trp;
А8 представляет собой Gly, D-Ala, Acc, Ala, β-Ala, Gaba, Apn, Ahx, Aha или удален;
А9 представляет собой Cys, D-Cys, Pen или Lys; и
А10 представляет собой Thr или удален;
при условии, что или А3, или А8 удален, но не оба;
или его фармацевтически приемлемая соль.
5. Соединение по п.4, где указанное соединение представляет собой:
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-β-Ala-Lys)-NH2; SEQ ID NO: 1
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-A6c-Lys)-NH2; SEQ ID NO: 1
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Ahx-Cys)-NH2; SEQ ID NO: 2
D-Phe-c(Cys-His-D-Phe-Arg-Trp-Ala-D-Cys)-Thr-NH2; SEQ ID NO: 3
D-Phe-c(Cys-His-D-Phe-Arg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO: 3
D-Phe-c(Cys-His-D-Phe-Arg-Trp-Gaba-D-Cys)-Thr-NH2; SEQ ID NO: 3
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Apn-Cys)-NH2; SEQ ID NO: 2
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-Apn-Lys)-NH2; SEQ ID NO: 4
Ac-A6c-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 5
Ac-D-2-Nal-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 6
Ac-Cha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 6
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 6
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 7
Ac-Nle-c(Cys-β-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 7
Ac-Nle-c(Cys-Gaba-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 7
Ac-Nle-c(Cys-Aib-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 7
Ac-Nle-c(D-Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 8
Ac-Nle-c(D-Cys-β-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 8
Ac-Nle-c(D-Cys-Gaba-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 8
Ac-Nle-c(D-Cys-Aib-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 8
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO: 9
Ac-Nle-c(Cys-β-Ala-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO: 9
Ac-Nle-c(Cys-Gaba-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO: 9
Ac-Nle-c(Cys-Aib-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO: 9
Ac-Nle-c(Cys-Gly-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO: 9
Ac-Nle-c(D-Cys-Ala-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO: 10
Ac-Nle-c(D-Cys-D-Ala-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO: 10
Ac-Nle-c(D-Cys-β-Ala-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO: 10
Ac-Nle-c(D-Cys-Gaba-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO: 10
Ac-Nle-c(D-Cys-Aib-His-D-Phe-Arg-Trp-D-Cys)-NH2; SEQ ID NO: 10
Ac-Oic-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 11
Ac-Chg-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 11
Ac-hCha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 11
Ac-D-Cha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 11
Ac-Nip-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 11
Ac-hPro-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 11
Ac-hLeu-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 11
Ac-hCha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 11
Ac-Phe-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 11
Ac-D-Phe-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 11
Ac-D-Chg-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 11
H-бутаноил-Cha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 12
Ac-hPhe-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 11
Ac-β-hMet-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 11
Ac-Gaba-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 11
Ac-Cha-c(Asp-His-D-Phe-Arg-D-Trp-Ala-Lys)-NH2; SEQ ID NO: 13
Ac-hCha-c(Asp-His-D-Phe-Arg-D-Trp-Ala-Lys)-NH2; SEQ ID NO: 13
Ac-Leu-c(Asp-His-D-Phe-Arg-D-Trp-Ala-Lys)-NH2; SEQ ID NO: 13
Ac-hLeu-c(Asp-His-D-Phe-Arg-D-Trp-Ala-Lys)-NH2; SEQ ID NO: 13
Ac-Phe-c(Asp-His-D-Phe-Arg-D-Trp-Ala-Lys)-NH2; SEQ ID NO: 13
Ac-Nle-c(Asp-His-D-Phe-Arg-D-Trp-D-Ala-Lys)-NH2; SEQ ID NO: 14
Ac-Nle-c(Asp-His-D-Phe-Arg-D-Trp-β-Ala-Lys)-NH2; SEQ ID NO: 14
Ac-Nle-c(Asp-His-D-Phe-Arg-D-Trp-Gaba-Lys)-NH2; SEQ ID NO: 14
Ac-Nle-c(Asp-His-D-Phe-Arg-D-Trp-Aha-Lys)-NH2; SEQ ID NO: 14
Ac-Nle-c(Asp-His-D-Phe-Arg-D-Trp-Apn-Lys)-NH2; SEQ ID NO: 14
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-Apn-Cys)-NH2; SEQ ID NO: 15
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-Gaba-Cys)-NH2; SEQ ID NO: 15
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-Ahx-Cys)-NH2; SEQ ID NO: 15
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-β-Ala-Cys)-NH2; SEQ ID NO: 15
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-D-Ala-Cys)-NH2; SEQ ID NO: 15
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; SEQ ID NO: 16
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-2-Nal-Cys)-NH2; SEQ ID NO: 16
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-l-Nal-Cys)-NH2; SEQ ID NO: 16
н-бутаноил-Nle-c(Cys-D-Ala-His-D-Phe-Arg-2-Nal-Cys)-NH2; SEQ ID NO: 17
н-бутаноил-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 17
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-2-Nal-Cys)-NH2; SEQ ID NO: 18
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-l-Nal-Cys)-NH2; SEQ ID NO: 18
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Bal-Cys)-NH2; SEQ ID NO: 18
Ac-Nle-c(Cys-D-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 61
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-D-Ala-Lys)-NH2; SEQ ID NO: 19
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-Bal-Cys)-NH2; SEQ ID NO: 20
Ac-Nle-c(Pen-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 21
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO: 22
Ac-Nle-c(Pen-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO: 22
D-Phe-c(Cys-His-D-Phe-hArg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO: 23
D-Phe-c(Cys-His-D-(Et)Tyr-Arg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO: 24
D-Phe-c(Cys-His-D-Phe-Arg-Bip-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO: 25
D-Phe-c(Cys-His-D(Et)Tyr-hArg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO: 24
D-Phe-c(Cys-His-D-Phe-hArg-Bip-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO: 26
D-Phe-c(Cys-His-D-(Et)Tyr-hArg-Bip-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO: 26
Nle-c(Cys-His-D-Phe-Arg-Trp-Apn-Cys)-NH2; SEQ ID NO: 27
Ac-Nle-c(Asp-D-Ala-His-D-Phe-Arg-Trp-Lys)-NH2; SEQ ID NO: 28
Ac-Nle-c(Asp-D-Ala-His-D-Phe-Arg-Bal-Lys)-NH2; SEQ ID NO: 28
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-OH; SEQ ID NO: 29
Ac-Nle-c(Cys-D-Abu-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 30
Ac-Nle-c(Cys-D-Val-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 30
Ac-Nle-c(Cys-D-Ile-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 30
Ac-Nle-c(Cys-D-Leu-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 30
Ac-Nle-c(Cys-D-Tle-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 30
Ac-Nle-c(Cys-D-Cha-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 30
Ac-Nle-c(Pen-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 31
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO: 32
Ac-Nle-c(Pen-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO: 32
Ac-Leu-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 33
Ac-Cha-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 33
Ac-Ile-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 33
Ac-Phe-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 33
Ac-Val-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 33
Ac-2-Nal-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 33
Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 34
Phe-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 34
Ac-Nle-c(Cys-3-Pal-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 35
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-OH; SEQ ID NO: 36
Ac-Nle-c(Cys-His-Phe-Arg-D-Trp-Gaba-Cys)-NH2; SEQ ID NO: 37
Ac-Nle-c(Asp-His-D-2-Nal-Arg-Trp-β-Ala-Lys)-NH2; SEQ ID NO: 38
Ac-Nle-c(Cys-His-D-2-Nal-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 39
Ac-Nle-c(Cys-His-D-2-Nal-Arg-Trp-Ahx-Cys)-NH2; SEQ ID NO: 39
Ac-hPhe-c(Asp-His-D-2-Nal-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 40
Ac-Cha-c(Asp-His-D-2-Nal-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 40
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-β-Ala-Lys)-OH; SEQ ID NO: 41
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Ahx-Cys)-OH; SEQ ID NO: 42
D-Phe-c(Cys-His-D-Phe-Arg-Trp-Ala-D-Cys)-Thr-OH; SEQ ID NO: 43
D-Phe-c(Cys-His-D-Phe-Arg-Trp-β-Ala-D-Cys)-Thr-OH; SEQ ID NO: 43
D-Phe-c(Cys-His-D-Phe-Arg-Trp-Gaba-D-Cys)-Thr-OH; SEQ ID NO: 43
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Apn-Cys)-OH; SEQ ID NO: 42
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-Apn-Lys)-OH; SEQ ID NO: 41
Ac-Cha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO: 44
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO: 44
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-OH; SEQ ID NO: 29
Ac-Chg-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO: 44
Ac-D-Cha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO: 44
Ac-hCha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO: 44
Ac-D-Chg-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO: 44
Ac-hPhe-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-OH; SEQ ID NO: 44
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-Gaba-Cys)-OH; SEQ ID NO: 45
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-Ahx-Cys)-OH; SEQ ID NO: 45
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-β-Ala-Cys)-OH; SEQ ID NO: 45
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-D-Ala-Cys)-OH; SEQ ID NO: 45
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-OH; SEQ ID NO: 46
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-2-Nal-Cys)-OH; SEQ ID NO: 46
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-1-Nal-Cys)-OH; SEQ ID NO: 46
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-Bal-Cys)-OH; SEQ ID NO: 46
Ac-Nle-c(Pen-D-Ala-His-D-Phe-Arg-Trp-Cys)-OH; SEQ ID NO: 47
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-OH; SEQ ID NO: 29
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-OH; SEQ ID NO: 48
или
Ac-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; SEQ ID NO: 49
или его фармацевтически приемлемая соль.
6. Соединение по п.5, где указанное соединение представляет собой:
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 7
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO: 22
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO: 32
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-OH; SEQ ID NO: 29
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-OH; SEQ ID NO: 29
или
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-OH; SEQ ID NO: 48,
или его фармацевтически приемлемая соль.
7. Соединение по п.1, где
А1 представляет собой Arg, D-Arg, Cha, hCha, Chg, D-Chg, Ile, Leu, 2-Nal, Nle, Phe, D-Phe, hPhe, Val или удален;
А2 представляет собой Cys, Pen или Asp;
А3 необязательно удален;
А4 представляет собой His или 3-Pal;
А5 представляет собой D-Phe, D-2-Nal или D-(Et)Tyr;
А6 представляет собой Arg или hArg;
А7 представляет собой Trp, 2-Nal, Bal, Bip или D-Trp;
А8 представляет собой Gly, Ala, β-Ala, Gaba, Apn, Ahx или удален;
А9 представляет собой Cys, D-Cys, Pen или Lys;
А10 представляет собой Thr или удален и
R2 и R3 представляют собой независимо для каждого случая Н или ацил,
или его фармацевтически приемлемая соль.
8. Соединение по п.7, где указанное соединение представляет собой:
Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 50
Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO: 51
Ac-D-Arg-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO: 52
Ac-Arg-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO: 52
Ac-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO: 51
Ac-D-Arg-c(Asp-His-D-Phe-Arg-Trp-Ala-Lys)-NH2; SEQ ID NO: 53
Ac-Arg-c(Asp-His-D-Phe-Arg-Trp-Ala-Lys)-NH2; SEQ ID NO: 53
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 7
D-Phe-c(Cys-His-D-(Et)Tyr-Arg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO: 24
Nle-c(Cys-His-D-Phe-Arg-Trp-Apn-Cys)-NH2; SEQ ID NO: 27
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO: 32
Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 34
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-p-Ala-Lys)-NH2; SEQ ID NO: 1
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Ahx-Cys)-NH2; SEQ ID NO: 2
D-Phe-c(Cys-His-D-Phe-Arg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO: 3
D-Phe-c(Cys-His-D-Phe-Arg-Trp-Gaba-D-Cys)-Thr-NH2; SEQ ID NO: 3
Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Apn-Cys)-NH2; SEQ ID NO: 2
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-Apn-Lys)-NH2; SEQ ID NO: 4
Ac-Cha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 6
Ac-Nle-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 6
Ac-Chg-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 11
Ac-hCha-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 11
Ac-D-Chg-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 11
Ac-hPhe-c(Asp-His-D-Phe-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 11
Ac-Nle-c(Cys-His-D-Phe-Arg-D-Trp-β-Ala-Cys)-NH2; SEQ ID NO: 15
Ac-Nle-c(Pen-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 21
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO: 22
D-Phe-c(Cys-His-D-Phe-hArg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO: 23
D-Phe-c(Cys-His-D-Phe-Arg-Bip-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO: 25
D-Phe-c(Cys-His-D-(Et)Tyr-hArg-Trp-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO: 24
D-Phe-c(Cys-His-D-Phe-hArg-Bip-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO: 26
D-Phe-c(Cys-His-D-(Et)Tyr-hArg-Bip-β-Ala-D-Cys)-Thr-NH2; SEQ ID NO: 26
Ac-Nle-c(Asp-D-Ala-His-D-Phe-Arg-Trp-Lys)-NH2; SEQ ID NO: 28
Ac-Nle-c(Asp-D-Ala-His-D-Phe-Arg-Bal-Lys)-NH2; SEQ ID NO: 28
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-OH; SEQ ID NO: 29
Ac-Nle-c(Cys-D-Abu-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 30
Ac-Nle-c(Cys-D-Val-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 30
Ac-Nle-c(Cys-D-Ile-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 30
Ac-Nle-c(Cys-D-Leu-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 30
Ac-Nle-c(Cys-D-Tle-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 30
Ac-Nle-c(Cys-D-Cha-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 30
Ac-Nle-c(Pen-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 31
Ac-Nle-c(Pen-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO: 32
Ac-Leu-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 33
Ac-Cha-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 33
Ac-Ile-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 33
Ac-Phe-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 33
Ac-Val-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 33
Ac-2-Nal-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 33
Phe-c(Cys-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 34
Ac-Nle-c(Cys-3-Pal-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 35
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-OH; SEQ ID NO: 36
Ac-Nle-c(Cys-His-Phe-Arg-D-Trp-Gaba-Cys)-NH2; SEQ ID NO: 37
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; SEQ ID NO: 16
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-2-Nal-Cys)-NH2; SEQ ID NO: 16
Ac-Nle-c(Cys-D-Ala-His-D-2-Nal-Arg-Bal-Cys)-NH2; SEQ ID NO: 20
Ac-Nle-c(Asp-His-D-2-Nal-Arg-Trp-p-Ala-Lys)-NH2; SEQ ID NO: 38
Ac-Nle-c(Cys-His-D-2-Nal-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 39
Ac-Nle-c(Cys-His-D-2-Nal-Arg-Trp-Ahx-Cys)-NH2; SEQ ID NO: 39
Ac-hPhe-c(Asp-His-D-2-Nal-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 40
Ac-Cha-c(Asp-His-D-2-Nal-Arg-Trp-Gaba-Lys)-NH2; SEQ ID NO: 40
или
Ac-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; SEQ ID NO: 49,
или его фармацевтически приемлемая соль.
9. Соединение по п.1, где
А1 представляет собой Arg или D-Arg,
или его фармацевтически приемлемая соль.
10. Соединение по п.9, где
А2 представляет собой Cys, D-Cys, Pen или Asp;
А3 представляет собой D-Ala, D-Glu, β-Ala, Gaba, Aib или удален;
А4 представляет собой His;
А5 представляет собой D-Phe, D-l-Nal, D-2-Nal, D-Trp, D-Bal или D-(Et)Tyr;
А6 представляет собой Arg или hArg;
А7 представляет собой Trp, Bip, D-Trp, 1-Nal или 2-Nal;
А8 представляет собой A6c, Ala, β-Ala, Gaba, Apn, Ahx или удален;
А9 представляет собой Cys, D-Cys, Pen или Lys;
А10 представляет собой Thr или удален, или его фармацевтически приемлемая соль.
11. Соединение по п.10, где:
R2 и R3 представляют собой независимо для каждого случая Н, ацил, н-пропаноил или н-бутаноил;
или его фармацевтически приемлемая соль.
12. Соединение по п.11, где:
А2 представляет собой Cys или Asp;
А3 представляет собой D-Ala или удален;
А4 представляет собой His;
А5 представляет собой D-Phe или D-2-Nal;
А6 представляет собой Arg;
А7 представляет собой Trp;
А8 представляет собой Ala, Gaba или удален;
А9 представляет собой Cys, Pen или Lys;
А10 удален,
или его фармацевтически приемлемая соль.
13. Соединение по п.12, где:
R2 и R3 независимо для каждого случая представляют собой Н или ацил,
или его фармацевтически приемлемая соль.
14. Соединение по п.13, где указанное соединение представляет собой:
Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; SEQ ID NO: 50
Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO: 51
Ac-D-Arg-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO: 52
Ac-Arg-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2; SEQ ID NO: 52
Ac-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO: 51
Ac-D-Arg-c(Asp-His-D-Phe-Arg-Trp-Ala-Lys)-NH2; SEQ ID NO: 53
Ac-Arg-c(Asp-His-D-Phe-Arg-Trp-Ala-Lys)-NH2; SEQ ID NO: 53
или
Ac-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; SEQ ID NO: 49,
или его фармацевтически приемлемые соли.
15. Соединение по п.14, где соединение представляет собой
Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO: 51 или
Ac-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; SEQ ID NO: 49,
или его фармацевтически приемлемая соль.
16. Соединение по п.15, где указанное соединение представляет собой
Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; SEQ ID NO: 51,
или его фармацевтически приемлемая соль.
17. Соединение по п.15, где указанное соединение представляет собой
Ac-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; SEQ ID NO: 49,
или его фармацевтически приемлемая соль.
18. Фармацевтическая композиция, пригодная для уменьшения потребления пищи, или пригодная для снижения веса, или пригодная для уменьшения потребления пищи и снижения веса, содержащая терапевтически эффективное количество соединения по любому из пп.1-17 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель или разбавитель.
19. Фармацевтическая композиция, пригодная для уменьшения потребления пищи, или пригодная для снижения веса, или пригодная для уменьшения потребления пищи и снижения веса, по п.18, где указанное соединение выбрано из группы, состоящей из Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2 SEQ ID NO: 32, Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2 SEQ ID NO: 50, Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2 SEQ ID NO: 51, Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2 SEQ ID NO: 7, D-Phe-c(Cys-His-D-(Et)Tyr-Arg-Trp-β-Ala-D-Cys)-Thr-NH2 SEQ ID NO: 24, Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2 SEQ ID NO: 22 и Ac-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2 SEQ ID NO: 49 или его фармацевтически приемлемой соли.
20. Фармацевтическая композиция по п.19, предназначенная для уменьшения потребления пищи, где указанное соединение представляет собой Ac-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2 SEQ ID NO: 49 или его фармацевтически приемлемую соль.
21. Фармацевтическая композиция по п.19, предназначенная для уменьшения потребления пищи, где указанное соединение представляет собой Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2 SEQ ID NO: 51 или его фармацевтически приемлемую соль.
22. Соединение по любому из пп.1-17 для снижения потребления пищи, или для уменьшения веса, или для уменьшения потребления пищи и уменьшения веса.
23. Соединение, пригодное для уменьшения потребления пищи, или пригодное для снижения веса, или пригодное для уменьшения потребления пищи и снижения веса, по п.22, где указанное соединение представляет собой Ac-Nle-c(Cys-His-D-Phe-Arg-Trp-Gaba-Pen)-NH2 SEQ ID NO: 32, Ас-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2 SEQ ID NO: 50, Ac-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2 SEQ ID NO: 51, Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2 SEQ ID NO: 7, D-Phe-c(Cys-His-D-(Et)Tyr-Arg-Trp-P-Ala-D-Cys)-Thr-NH2 SEQ ID NO: 24, Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2 SEQ ID NO: 22 и Ac-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2 SEQ ID NO: 49 или его фармацевтически приемлемую соль.
24. Соединение по п.23, где указанное соединение представляет собой Ас-Arg-c(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2 SEQ ID NO: 49 или его фармацевтически приемлемую соль.
25. Соединение по п.23, где указанное соединение представляет собой Ас-D-Arg-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2 SEQ ID NO: 51 или его фармацевтически приемлемую соль.
26. Соединение по формуле (II)
(R2R3)-А1-c(А2-А3-А4-А5-A6-A7-A8-A9)-NH2,
где А1 представляет собой Nie или удален;
А2 представляет собой Cys или Asp;
А3 представляет собой Glu или D-Ala;
А4 представляет собой His;
А5 представляет собой D-Phe;
А6 представляет собой Arg;
А7 представляет собой Trp, 2-Nal или Bal;
А8 представляет собой Gly, Ala, D-Ala, β-Ala, Gaba или Арп;
А9 представляет собой Cys или Lys;
каждый из R2 и R3 независимо выбран из группы, состоящей из Н или (C1-С6)ацила;
при условии, что
(I) когда R2 представляет собой (С1-С6)ацил, то R3 представляет собой Н;
и
(II) когда А2 представляет собой Cys, то А9 представляет собой Cys,
или его фармацевтически приемлемая соль.
27. Соединение по п.26, где указанное соединение представляет собой:
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Gly-Cys)-NH2; SEQ ID NO: 54
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-D-Ala-Cys)-NH2; SEQ ID NO: 54
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-β-Ala-Cys)-NH2; SEQ ID NO: 54
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 54
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Apn-Cys)-NH2; SEQ ID NO: 54
Ac-c(Cys-Glu-His-D-Phe-Arg-Trp-Ala-Cys)-NH2; SEQ ID NO: 55
Ac-c(Cys-Glu-His-D-Phe-Arg-2-Nal-Ala-Cys)-NH2; SEQ ID NO: 55
Ac-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Ala-Cys)-NH2; SEQ ID NO: 56
Ac-c(Cys-D-Ala-His-D-Phe-Arg-2-Nal-Ala-Cys)-NH2; SEQ ID NO: 56
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Ala-Cys)-NH2; SEQ ID NO: 57
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-β-Ala-Cys)-NH2; SEQ ID NO: 57
Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Gaba-Cys)-NH2; SEQ ID NO: 57 или
Ac-Nle-c(Asp-D-Ala-His-D-Phe-Arg-Bal-Ala-Lys)-NH2; SEQ ID NO: 58,
или его фармацевтически приемлемая соль.
28. Фармацевтическая композиция, пригодная для уменьшения потребления пищи, или пригодная для снижения веса, или пригодная для уменьшения потребления пищи и снижения веса, содержащая терапевтически эффективное количество соединения по п.26 или 27 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель или разбавитель.
29. Соединение по п.26 или 27 для снижения потребления пищи, или для уменьшения веса, или для уменьшения потребления пищи и уменьшения веса.
| WO 2005000339 А2, 06.01.2005 | |||
| US 6613874 B1, 02.09.2003 | |||
| US 2004138136 A1, 15.07.2004 | |||
| US 2003212002 A1, 13.11.2003 | |||
| US 6127381 А, 03.10.2000 | |||
| ЛИГАНДЫ МЕЛАНОКОРТИНОВЫХ РЕЦЕПТОРОВ | 2000 |
|
RU2213098C2 |
Авторы
Даты
2012-01-10—Публикация
2006-07-10—Подача