Настоящее изобретение относится к соединениям, применимым в качестве ингибиторов киназ Janus (JAK). Настоящее изобретение также относится к фармацевтически приемлемым композициям, содержащим соединения по настоящему изобретению, и к способам применения композиций для лечения различных нарушений.
Киназы Janus (JAK) представляют собой семейство тирозинкиназ, состоящее из киназ JAK1, JAK2, JAK3 и TYK2. Киназы JAK играют ключевую роль в цитокинзависимой передаче сигнала. Субстраты, расположенные в каскаде передачи сигнала ниже киназ семейства JAK, включают белки передачи сигнала и активации транскрипции (STAT). Передача сигнала в каскаде JAK/STAT опосредует многие аномальные виды иммунного ответа, такие как аллергии, астма, аутоиммунные заболевания, такие как отторжение трансплантата, ревматоидный артрит, боковой амиотрофический склероз и рассеянный склероз, а также вовлечена в развитие солидных опухолей и злокачественных опухолей крови, таких как лейкозы и лимфомы. Киназа JAK2 также принимает участие в миелопролиферативных нарушениях, которые включают истинную полицетемию, эссенциальную тромбоцитемию, хронический идиопатический миелофиброз, миелоидную метаплазию с миелофиброзом, хронический миелолейкоз, хронический миеломоноцитарный лейкоз, хронический эозинофильный лейкоз, гиперэозинофильный синдром и системный мастоцитоз.
Ассоциированные с Rho и образующие двойную спираль сериновые/треониновые протеинкиназы (семейство ROCK) представляют собой эффекторы Ras-зависимой малой ГТФазы Rho. Семейство ROCK включает p160ROCK (ROCK-1), ROCKα/Rho-киназа/ROCK-II, протеинкиназу PKN и цитрон, и цитронкиназу. Семейство ROCK вовлечено в развитие различных заболеваний и нарушений, включая гипертензию, хроническое обструктивное заболевание легких, церебральный вазоспазм, коронарный вазоспазм, бронхиальную астму, эректильную дисфункцию, глаукому, пролиферацию гладкомышечных клеток сосудов, гипертрофию миокарда, малигному, индуцированное ишемией/реперфузией повреждение, эндотелиальную дисфункцию, болезнь Крона и колит, разрастание нейритов, болезнь Рейно, стенокардию, болезнь Альцгеймера, атеросклероз и гипертрофию сердца и периваскулярный фиброз.
Протеинкиназа A (PKA, также известная как цАМФ-зависимая протеинкиназа) представляет собой тетрамерный голофермент, который содержит две каталитические субъединицы, связанные с гомодимерной регулирующей субъединицей (которая действует в качестве ингибитора каталитических субъединиц). При связывании с цАМФ (активация фермента) каталитические субъединицы отделяются от регуляторных субъединиц с получением активной серин/треонин протеинкиназы. На настоящее время сообщалось о трех изоформах каталитической субъединицы (C-α, C-β и C-γ), причем субъединица C-α является наиболее полно изученной, главным образом, вследствие ее повышенной экспрессии в первичных и метастазирующих меланомах. Было показано, что PKA регулирует многие жизненные функции, включая энергетический обмен, транскрипцию гена, пролиферацию, дифференциацию, репродуктивную функцию, секрецию, нейрональную активность, память, сократительную способность и двигательную способность.
Соответственно, существует острая потребность в разработке соединений, применимых в качестве ингибиторов протеинкиназ, включая киназы семейств JAK, ROCK и PKA. В особенности была бы желательной разработка соединений, применимых в качестве ингибиторов JAK2 и JAK3.
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Было обнаружено, что соединения по настоящему изобретению и их фармацевтически приемлемые композиции эффективны в качестве ингибиторов протеинкиназ, в особенности киназ семейства JAK. В определенных примерах осуществления указанные соединения эффективны в качестве ингибиторов протеинкиназы JAK3. Указанные соединения представляют собой соединения общей формулы I:

или являются их фармацевтически приемлемой солью, где значения R1, R2, Z1, Z2 и Z3 определены ниже.
Указанные соединения и их фармацевтически приемлемые композиции применимы для лечения и ослабления тяжести различных нарушений, включая аллергические заболевания, такие как астма и атопический дерматит, аутоиммунные заболевания, такие как системная красная волчанка и псориаз, состояния, ассоциированные с трансплантацией органов, миелопролиферативные нарушения, гипертензию, хроническое обструктивное заболевание легких и пролиферативные нарушения, такие как меланома.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Соединения и определения
Соединения по настоящему изобретению включают соединения, описанные в общих чертах выше, и дополнительно проиллюстрированы раскрытыми в этом документе классами, подклассами и видами. Используемые в этом документе следующие определения должны применяться, если иное не указано особо. Для целей настоящего изобретения химические элементы указаны в соответствии с Periodic Table of the Elements, CAS version, Handbook of Chemistry and Physics, 75th Ed. Кроме того, общие принципы органической химии описаны по "Organic Chemistry", Thomas Sorrell, University Science Books, Sausalito: 1999, и в "March's Advanced Organic Chemistry", 5th Ed., Ed.: Smith, M.B. and March, J., John Wiley & Sons, New York: 2001, полное содержание которых включено в этот документ посредством ссылки.
Как описано в этом документе, соединения по настоящему изобретению могут быть необязательно замещены одним или несколькими заместителями, такими как проиллюстрированные в общих чертах выше или представленные в качестве примера определенными классами, подклассами и видами по настоящему изобретению. Следует учитывать, что выражение «необязательно замещенный» используется взаимозаменяемо с выражением «замещенный или незамещенный». Термин «замещенный», с предшествующим ему термином «необязательно» или без него, как правило, относится к замене радикалов водорода в данной структуре радикалом определенного заместителя. Если иное не указано особо, необязательно замещенная группа может содержать заместитель в каждом возможном для замещения положении группы и, если более чем одно положение в любой данной структуре может быть замещено более чем одним заместителем, выбранным из определенной группы, то в каждом положении заместитель может быть либо одинаковым, либо разным.
Как описано в этом документе, если термин «необязательно замещенный» предшествует перечню, то упомянутый термин относится ко всем из последующих в этом перечне групп, возможных для замещения. Например, если X представляет собой галоген; необязательно замещенный C1-3алкил или фенил; то X может представлять собой или необязательно замещенный алкил, или необязательно замещенный фенил. Сходным образом, если термин «необязательно замещенный» следует за перечнем, то упомянутый термин также относится ко всем предшествующим в перечне группам, подходящим для замещения, если иное особо не указано. Например, если X представляет собой галоген, C1-3алкил или фенил, где X необязательно замещен JX, то C1-3алкил и фенил могут быть оба замещены JX. Как очевидно любому среднему специалисту в данной области техники, такие группы, как H, галоген, NO2, CN, NH2, OH или OCF3, не могут быть включены, поскольку они не являются возможными для замещения группами.
Сочетания заместителей, предусматриваемые настоящим изобретением, предпочтительно являются такими, которые приводят к образованию стабильных или химически возможных соединений. Используемый в этом документе термин «стабильный» относится к соединениям, которые остаются по существу неизменными в условиях их получения, обнаружения и предпочтительно их извлечения и очистки и использования для одной или нескольких из целей, раскрытых в этом документе. В некоторых примерах осуществления стабильное соединение или химически возможное соединение представляет собой соединение, которое остается по существу неизменным при температуре 40°C или менее в отсутствие влаги или других химически реакционноспособных условий в течение, по крайней мере, недели.
Как описано в этом документе, связь, начерченная от заместителя к центру одного кольца в составе полициклической кольцевой системы (как представлено ниже), представляет собой замещение заместителя в любом возможном для замещения положении в любом из колец из состава полициклической кольцевой системы. Например, на фигуре a указано возможное замещение в любом из положений, как представлено на фигуре b.

Это также применимо к полициклическим кольцевым системам, конденсированным с необязательными кольцевыми системами (которые должны быть представлены пунктирными линиями). Например, на фигуре c X представляет собой необязательный заместитель и для кольца A, и для кольца B.
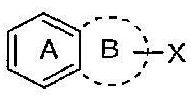
Фигура с
Однако если каждое из двух колец в составе полициклической кольцевой системы содержит различные заместители, начерченные от центра каждого кольца, то каждый заместитель представляет собой замещение лишь того кольца, к которому он присоединен, если иное не определено особо. Например, на фигуре d Y представляет собой необязательный заместитель только для кольца A и X представляет собой необязательный заместитель только для кольца B.
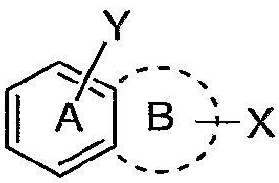
Фигура d
Используемый в этом документе термин «алифатический» или «алифатическая группа» означает неразветвленную (т.е. с прямой цепью) или разветвленную, замещенную или незамещенную углеводородную цепь, которая является полностью насыщенной или которая содержит один или несколько центров ненасыщенности. Если иное не указано особо, алифатические группы содержат 1-20 алифатических атомов углерода. В некоторых примерах осуществления алифатические группы содержат 1-10 алифатических атомов углерода. В других примерах осуществления алифатические группы содержат 1-8 алифатических атомов углерода. В еще одних примерах осуществления алифатические группы содержат 1-6 алифатических атомов углерода, и в других примерах осуществления алифатические группы содержат 1-4 алифатических атомов углерода. Подходящие алифатические группы включают без ограничения неразветвленные или разветвленные, замещенные или незамещенные алкильные, алкенильные или алкинильные группы. Дополнительные примеры алифатических групп включают метил, этил, пропил, бутил, изопропил, изобутил, винил и втор-бутил.
Термин «циклоалифатическая группа» (или «карбоцикл», или «циклоалкил») относится к моноциклическому C3-C8углеводороду или бициклическому C8-C12углеводороду, который является полностью насыщенным или который содержит один или несколько центров ненасыщенности, но не является ароматическим, который имеет одну точку присоединения к оставшейся части молекулы, где любое отдельное кольцо в упомянутой бициклической кольцевой системе содержит 3-7 кольцевых атомов. Подходящие циклоалифатические группы включают без ограничения циклоалкил, циклоалкенил и циклоалкинил. Дополнительные примеры алифатических групп включают циклопентил, циклопентенил, циклогексил, циклогексенил, циклогептил и циклогептенил.
Используемый в этом документе термин «гетероцикл», «гетероциклил», «гетероциклоалифатическая группа» или «гетероциклическая группа» означает неароматические, моноциклические, бициклические или трициклические кольцевые системы, в которых один или несколько атомов в кольце представляют собой независимо выбранный гетероатом. В некоторых примерах осуществления «гетероцикл», «гетероциклил» «гетероциклоалифатическая» или «гетероциклическая» группа содержит 3-14 кольцевых атомов, один или несколько из которых представляют собой гетероатом, независимо выбранный из кислорода, серы, азота или фосфора, и каждое кольцо в системе содержит от 3 до 7 кольцевых атомов.
Дополнительные примеры гетероциклических колец включают без ограничения следующие моноциклы: 2-тетрагидрофуранил, 3-тетрагидрофуранил, 2-тетрагидротиофенил, 3-тетрагидротиофенил, 2-морфолино, 3-морфолино, 4-морфолино, 2-тиоморфолино, 3-тиоморфолино, 4-тиоморфолино, 1-пирролидинил, 2-пирролидинил, 3-пирролидинил, 1-тетрагидропиперазинил, 2-тетрагидропиперазинил, 3-тетрагидропиперазинил, 1-пиперидинил, 2-пиперидинил, 3-пиперидинил, 1-пиразолинил, 3-пиразолинил, 4-пиразолинил, 5-пиразолинил, 1-пиперидинил, 2-пиперидинил, 3-пиперидинил, 4-пиперидинил, 2-тиазолидинил, 3-тиазолидинил, 4-тиазолидинил, 1-имидазолидинил, 2-имидазолидинил, 4-имидазолидинил, 5-имидазолидинил, и следующие бициклы: 3-1H-бензимидазол-2-он, 3-(1-алкил)бензимидазол-2-он, индолинил, тетрагидрохинолинил, тетрагидроизохинолинил, бензотиолан, бензодитиан и 1,3-дигидроимидазол-2-он.
Термин «гетероатом» означает один или несколько из атомов кислорода, серы, азота, фосфора или кремния (включая любую окисленную форму азота, серы, фосфора или кремния; кватернизованную форму любого основного азота; или возможный для замещения атом азота в гетероциклическом кольце, например N (как в 3,4-дигидро-2H-пирролиле), NH (как в пирролидиниле) или NR+ (как в N-замещенном пирролидиниле)).
Используемый в этом документе термин «ненасыщенный» означает, что радикал содержит один или несколько центров ненасыщенности.
Используемый в этом документе термин «алкокси» или «тиоалкил» относится к определенной ранее алкильной группе, присоединенной к основной углеродной цепи через атом кислорода («алкокси») или серы («тиоалкил»).
Термины «галогеналкил», «галогеналкенил» и «галогеналкокси» означают алкил, алкенил или алкокси, соответственно замещенные одним или несколькими атомами галогена. Термин «галоген» означает F, Cl, Br или I.
Термин «арил», используемый отдельно или как часть более крупного радикала, такого как «аралкил», «аралкокси» или «арилоксиалкил», относится к моноциклическим, бициклическим и трициклическим кольцевым системам, содержащим всего 5-14 кольцевых атомов, в которых, по крайней мере, одно кольцо в системе является ароматическим и в которых каждое кольцо в системе содержит 3-7 кольцевых атомов. Термин «арил» может использоваться взаимозаменяемо с термином «арильное кольцо». Термин «арил» также относится к гетероарильным кольцевым системам, описанным в этом документе ниже. Примеры арильных колец могут включать фенил, нафтил и гетероарильные группы, перечисленные ниже.
Термин «гетероарил», используемый отдельно или как часть более крупного радикала, такого как «гетероаралкил» или «гетероарилалкокси», относится к моноциклическим, бициклическим и трициклическим кольцевым системам, содержащим всего 5-14 кольцевых атомов, в которых, по крайней мере, одно кольцо в системе является ароматическим, по крайней мере, одно кольцо в системе содержит один или несколько гетероатомов и каждое кольцо в системе содержит 3-7 кольцевых атомов. Термин «гетероарил» может использоваться взаимозаменяемо с термином «гетероарильное кольцо» или с термином «гетероароматическая группа».
Дополнительные примеры гетероарильных колец включают следующие моноциклы: 2-фуранил, 3-фуранил, N-имидазолил, 2-имидазолил, 4-имидазолил, 5-имидазолил, 3-изоксазолил, 4-изоксазолил, 5-изоксазолил, 2-оксазолил, 4-оксазолил, 5-оксазолил, N-пирролил, 2-пирролил, 3-пирролил, 2-пиридил, 3-пиридил, 4-пиридил, 2-пиримидинил, 4-пиримидинил, 5-пиримидинил, пиридазинил (например, 3-пиридазинил), 2-тиазолил, 4-тиазолил, 5-тиазолил, тетразолил (например, 5-тетразолил), триазолил (например, 2-триазолил и 5-триазолил), 2-тиенил, 3-тиенил, пиразолил (например, 2-пиразолил), изотиазолил, 1,2,3-оксадиазолил, 1,2,5-оксадиазолил, 1,2,4-оксадиазолил, 1,2,3-триазолил, 1,2,3-тиадиазолил, 1,3,4-тиадиазолил, 1,2,5-тиадиазолил, пиразинил, 1,3,5-триазинил, и следующие бициклы: бензимидазолил, бензофурил, бензотиофенил, индолил (например, 2-индолил), пуринил, хинолинил (например, 2-хинолинил, 3-хинолинил, 4-хинолинил) и изохинолинил (например, 1-изохинолинил, 3-изохинолинил или 4-изохинолинил).
Арильная (включая аралкил, аралкокси, арилоксиалкил и тому подобное) или гетероарильная (включая гетероаралкил и гетероарилалкокси и тому подобное) группа может содержать один или несколько заместителей. Подходящие заместители ненасыщенного атома углерода арильной или гетероарильной группы выбирают из заместителей, перечисленных выше в определении JX, JQ, JR; галогена; -R°; -OR°; -SR°; 1,2-метилендиокси; 1,2-этилендиокси; фенила (Ph), необязательно замещенного R°; -O(Ph), необязательно замещенной R°; -(CH2)1-2(Ph), необязательно замещенной R°; -CH=CH(Ph), необязательно замещенной R°; -NO2; -CN; -N(R°)2; -NR°C(O)R°; -NR°C(S)R°; -NR°C(O)N(R°)2; -NR°C(S)N(R°)2; -NR°CO2R°; -NR°NR°C(O)R°; -NR°NR°C(O)N(R°)2; -NR°NR°CO2R°; -C(O)C(O)R°; -C(O)CH2C(O)R°; -CO2R°; -C(O)R°; -C(S)R°; -C(O)N(R°)2; -C(S)N(R°)2; -OC(O)N(R°)2; -OC(O)R°; -C(O)N(OR°)R°; -C(NOR°)R°; -S(O)2R°; -S(O)3R°; -SO2N(R°)2; -S(O)R°; -NR°SO2N(R°)2; -NR°SO2R°; -N(OR°)R°; -C(=NH)-N(R°)2; или -(CH2)0-2NHC(O)R°, где в каждом независимом случае R° выбирают из водорода, необязательно замещенной C1-6алифатической группы, незамещенного 5-6-членного гетероарильного или гетероциклического кольца, фенила, -O(Ph) или -CH2(Ph), или несмотря на приведенное выше определение две независимые R° на одном заместителе или на разных заместителях образуют вместе с атомом (атомами), к которому присоединена каждая группа R°, 5-8-членное гетероциклическое, арильное или гетероарильное кольцо или 3-8-членное циклоалкильное кольцо, содержащее 0-3 гетероатома, независимо выбранных из азота, кислорода или серы. Необязательные заместители алифатической группы R° выбирают из NH2, NH(C1-4алифатическая группа), N(C1-4алифатическая группа)2, галогена, C1-4алифатической группы, OH, O(C1-4алифатическая группа), NO2, CN, CO2H, CO2(C1-4алифатическая группа), O(галогенC1-4алифатическая группа) или галогенC1-4алифатической группы, где каждая из упомянутых C1-4алифатических групп R° является незамещенной.
Алифатическая или гетероалифатическая группа или неароматическое гетероциклическое кольцо, может содержать один или несколько заместителей. Подходящие заместители насыщенного атома углерода алифатической или гетероалифатической группы или неароматического гетероциклического кольца, выбирают из заместителей, перечисленных выше для ненасыщенного атома углерода арильной и гетероарильной группы, и дополнительно включают следующие: =O, =S, =NNHR*, =NN(R*)2, =NNHC(O)R*, =NNHCO2(алкил), =NNHSO2(алкил) или =NR*, где каждый R* независимо выбирают из водорода или необязательно замещенной C1-6алифатической группы. Необязательные заместители алифатической группы R* выбирают из NH2, NH(C1-4алифатическая группа), N(C1-4алифатическая группа)2, галогена, C1-4алифатической группы, OH, O(C1-4алифатическая группа), NO2, CN, CO2H, CO2(C1-4алифатическая группа), O(галогенC1-4алифатическая группа) или галоген(C1-4алифатическая группа), где каждая из упомянутых C1-4алифатических групп R* является незамещенной.
Необязательные заместители азота в неароматическом гетероциклическом кольце включают заместители, перечисленные в этом документе в определении JQ и R7; -R+, -N(R+)2, -C(O)R+, -CO2R+, -C(O)C(O)R+, -C(O)CH2C(O)R+, -SO2R+, -SO2N(R+)2, -C(=S)N(R+)2, -C(=NH)-N(R+)2 или -NR+SO2R+; где R+ представляет собой водород, необязательно замещенную C1-6алифатическую группу, необязательно замещенный фенил, необязательно замещенную -O(Ph), необязательно замещенную -CH2(Ph), необязательно замещенную -(CH2)1-2(Ph); необязательно замещенную -CH=CH(Ph); или незамещенное 5-6-членное гетероарильное или гетероциклическое кольцо, содержащее 1-4 гетероатома, независимо выбранных из азота, кислорода или серы, или несмотря на приведенное выше определение две независимые R+ на одном заместителе или на разных заместителях образуют вместе с атомом (атомами), к которому присоединена каждая группа R+, 5-8-членное гетероциклическое, арильное или гетероарильное кольцо или 3-8-членное циклоалкильное кольцо, содержащее 0-3 гетероатома, независимо выбранных из азота, кислорода или серы. Необязательные заместители алифатической группы или фенильного кольца R+ выбирают из NH2, NH(C1-4алифатическая группа), N(C1-4алифатическая группа)2, галогена, C1-4алифатической группы, OH, O(C1-4алифатическая группа), NO2, CN, CO2H, CO2(C1-4алифатическая группа), O(галогенC1-4алифатическая группа) или галоген(C1-4алифатическая группа), где каждая из упомянутых C1-4алифатических групп R+ является незамещенной.
Как детально рассмотрено выше, в некоторых примерах осуществления две независимые R° (или R+, или любые другие переменные группы, сходным образом определенные в этом документе) образуют вместе с атомом (атомами), к которому присоединена каждая переменная группа, 5-8-членное гетероциклическое, арильное или гетероарильное кольцо или 3-8-членное циклоалкильное кольцо, содержащее 0-3 гетероатома, независимо выбранных из азота, кислорода или серы. Примеры колец, которые образуются в том случае, когда a) две независимые R° (или R+, или любые другие переменные группы, сходным образом определенные в этом документе) образуют вместе с атомом (атомами), к которому присоединена каждая переменная группа, R+, или любые другие переменные группы, сходным образом определенные в этом документе), связанные с одним атомом и образующие вместе с этим атомом кольцо, например, N(R°)2, где обе независимых R° образуют вместе с атомом азота пиперидин-1-ильную, пиперазин-1-ильную или морфолин-4-ильную группу; и b) две независимые R° (или R+, или любые другие переменные группы, сходным образом определенные в этом документе), связанные с разными атомами и образующие вместе с этими атомами кольцо, например, если фенильная группа замещена двумя OR°  ,
,
то эти две R° образуют вместе с атомами кислорода, к которым они присоединены, конденсированное 6-членное кислородсодержащее кольцо:  . Следует учитывать, что в том случае, когда две независимые R° (или R+, или любые другие переменные группы, сходным образом определенные в этом документе) образуют вместе с атомом (атомами), к которому присоединена каждая переменная группа, целый ряд других колец, рассмотренные выше примеры не подразумеваются в качестве ограничивающих.
. Следует учитывать, что в том случае, когда две независимые R° (или R+, или любые другие переменные группы, сходным образом определенные в этом документе) образуют вместе с атомом (атомами), к которому присоединена каждая переменная группа, целый ряд других колец, рассмотренные выше примеры не подразумеваются в качестве ограничивающих.
Алкильная или алифатическая цепь могут быть необязательно прерваны другим атомом или группой. Это означает, что метиленовое звено алкильной или алифатической цепи необязательно заменено упомянутым другим атомом или группой. Примеры таких атомов или групп могут включать без ограничения -NR-, -O-, -S-, -CO2-, -OC(O)-, -C(O)CO-, -C(O)-, -C(O)NR-, -C(=N-CN), -NRCO-, -NRC(O)O-, -SO2NR-, -NRSO2-, -NRC(O)NR-, -OC(O)NR-, -NRSO2NR-, -SO- или -SO2-, где значение R определено в этом документе. Если иное не определено особо, необязательные замены приводят к образованию химически стабильного соединения. Необязательные разрывы могут происходить как внутри цепи, так и на концах цепи; как в точке присоединения, так и на конце. Две необязательные замены могут также быть смежными по отношению друг к другу внутри цепи. Если иное не определено особо, в случае концевой замены или разрыва заменяемый атом связан с концевым H. Например, если -CH2CH2CH3 необязательно прерывается -O-, то полученное соединение может представлять собой -OCH2CH3, -CH2OCH3 или -CH2CH2OH.
Если иное не указано особо, подразумевается, что описанные в этом документе структуры включают все изомерные (например, энантиомерные, диастереоизомерные и геометрические (или конформационные)) формы структуры; например R- и S-конфигурации для каждого асимметрического центра, (Z)- и (E)-изомеры по двойной связи и (Z)- и (E)-конформационные изомеры. Поэтому отдельные стереохимические изомеры, а также энантиомерные, диастереоизомерные и геометрические (или конформационные) смеси соединений по настоящему изобретению включены в объем настоящего изобретения.
Если иное не указано особо, все таутомерные формы соединений по настоящему изобретению включены в объем настоящего изобретения. Кроме того, если иное не указано особо, то также подразумевается, что описанные в этом документе структуры включают соединения, которые различаются лишь содержанием одного или нескольких изотопно обогащенных атомов. Например, соединения, имеющие структуру по настоящему изобретению, за исключением замены водорода дейтерием или тритием, или замены углерода 13C- или 14C-обогащенным углеродом, включены в объем настоящего изобретения. Такие соединения применимы, например, в качестве аналитических средств или зондов в биологических методах анализа.
Настоящее соединение относится к соединению формулы I:

или к его фармацевтически приемлемой соли, в которой
R1 представляет собой H, -NO2, -CN, -OCF3, галоген или амино; или C1-6алифатическую группу, C3-7циклоалифатическую группу, C1-6алкокси или C1-4галогеналкил, необязательно замещенные 0-10 группами JR;
R2 представляет собой H, -NO2, -CN, -OCF3, галоген или амино; или C1-6алифатическую группу, C3-7циклоалифатическую группу, C1-6алкокси или C1-4галогеналкил, необязательно замещенные 0-10 группами JR;
Z1 представляет собой C1-6алифатическую группу или C3-10циклоалифатическую группу, необязательно замещенные 0-10 группами JZ; если связь между Z1 и C является двойной, то Z1 может также представлять собой =O, =NR или =C(R)2;
Z2 представляет собой H или галоген; или C1-10галогеналкил, C1-4галогеналкокси, Y, -(Vn)-CN, -(Vn)-NO2, -(Vn)-OH, -(Vn)-(C1-6алифатическая группа), -(Vn)-(C3-12гетероциклил), -(Vn)-(C6-10арил), -(Vn)-(5-10-членный гетероарил) или -(Vn)-(C3-10циклоалифатическая группа), необязательно замещенные 0-10 группами JZ; или
Z1 и Z2 образуют вместе с атомом углерода, к которому они присоединены, кольцо Q;
Z3 представляет собой H или C1-6алкил, необязательно замещенный 0-3 группами JZ; или
Z1, Z2 и Z3 образуют вместе с атомом углерода, к которому они присоединены, 6-14-членное насыщенное, частично насыщенное или ненасыщенное бициклическое кольцо, содержащее 0-3 гетероатома; где
если связь между Z1 и C является тройной, то Z2 отсутствует; и
если связь между Z1 и C является двойной или тройной, то Z3 отсутствует;
Q представляет собой 3-8-членное насыщенное или частично насыщенное моноциклическое кольцо, содержащее 0-3 гетероатома, выбранных из азота, кислорода или серы, где упомянутое Q необязательно и независимо конденсировано с Q1 или Q2; или и с Q1 и с Q2; где упомянутое Q необязательно замещено 0-4 группами JQ;
Q1 представляет собой 3-8-членное насыщенное, частично насыщенное или ненасыщенное моноциклическое кольцо, содержащее 0-3 гетероатома, выбранных из азота, кислорода или серы, где упомянутая группа Q1 необязательно замещена 0-4 группами JQ;
Q2 представляет собой 3-8-членное насыщенное, частично насыщенное или ненасыщенное моноциклическое кольцо, содержащее 0-3 гетероатома, выбранных из азота, кислорода или серы, где упомянутая группа Q2 необязательно замещена 0-4 группами JQ;
R представляет собой H, необязательно замещенные C1-6алифатическую группу, C3-10циклоалифатическую группу, C6-10арил, 5-14-членный гетероарил или 5-14-членный гетероциклил; или две группы R, на одном заместителе или на разных заместителях, образуют вместе с атомом (атомами), к которому присоединена каждая группа R, необязательно замещенное 3-14-членное насыщенное, частично ненасыщенное или полностью ненасыщенное моноциклическое, бициклическое или трициклическое кольцо, содержащее 0-4 гетероатома, независимо выбранных из азота, кислорода или серы, где упомянутая R необязательно замещена 0-10 группами JR;
каждый заместитель JQ и JZ на ненасыщенном атоме углерода независимо выбирают из водорода, -OCF3, C1-6галогеналкила, N(R)2, OR, галогена, Y, -(Vn)-CN, -(Vn)-NO2, -(Vn)-OH, -(Vn)-(C1-6алифатическая группа), -(C3-10циклоалифатическая группа)-C(O)R, -(C3-10циклоалифатическая группа)-(C3-12гетероциклил); -(Vn)-(C3-12гетероциклил), -(Vn)-(C6-10арил), -(Vn)-(5-10-членный гетероарил), -(Vn)-(C3-10циклоалифатическая группа); где каждый JQ и JZ необязательно замещен до 10 группами JR;
каждый заместитель JQ и JZ на насыщенном атоме углерода выбирают из заместителей, перечисленных выше для ненасыщенного атома углерода, а также из следующих заместителей: =O, =NN(Ra)2, =NNHC(O)Ra, =NNHCO2(C1-4алкил), =NNHSO2(C1-4алкил) и =NRa, где каждый JQ и JZ необязательно замещен до 10 группами JR;
каждый заместитель JQ и JZ на атоме азота независимо выбирают из водорода, Y, -(Vn)-CN, -(Vn)-NO2, -(Vn)-OH, -(Vn)-(C1-6алифатическая группа), -(C3-10циклоалифатическая группа)-C(O)R, -(C3-10циклоалифатическая группа)-(C3-12гетероциклил), -(Vn)-(C3-12гетероциклил), -(Vn)-(C6-10арил), -(Vn)-(5-10-членный гетероарил), -(Vn)-(C3-10циклоалифатическая группа); где две группы JZ на одном заместителе или на разных заместителях могут необязательно образовывать вместе с атомом (атомами), к которому присоединена каждая группа JZ, необязательно замещенное 3-14-членное насыщенное, частично ненасыщенное или полностью ненасыщенное моноциклическое, бициклическое или трициклическое кольцо, содержащее 0-4 гетероатома, независимо выбранных из азота, кислорода или серы; где каждый JQ и JZ необязательно замещен до 10 группами JR;
JR выбирают из галогена, -N(Rb)2, SRb, ORb, оксо, C1-4галогеналкокси, C1-4галогеналкила, L, -(Ln)-(C1-6алкил), -(Ln)-(C3-12гетероциклил), -(Ln)-(C6-10арил), -(Ln)-(5-10-членный гетероарил), -(Ln)-(C3-10циклоалифатическая группа), -(Ln)-NO2, -(Ln)-CN, -(Ln)-OH, -CO2Rb, -CORb, -OC(O)Rb, -NC(O)Rb;
L представляет собой C1-10алкил, в котором до трех метиленовых звеньев заменены -NRb-, -O-, -S-, - CO2-, -OC(O)-, -C(O)CO-, -C(O)-, -C(O)NRb-, -C(=N-CN), -NRbCO-, -NRbC(O)O-, -SO2NRb-, -NRbSO2-, -NRbC(O)NR-, -OC(O)NRb-, -NRbSO2NRb-, -SO- или -SO2-;
V представляет собой C1-10алифатическую группу, в которой до трех метиленовых звеньев заменены GV, где GV выбирают из -NR-, -O-, -S-, -CO2-, -OC(O)-, -C(O)CO-, -C(O)-, -C(O)NR-, -C(=N-CN), -NRCO-, -NRC(O)O-, -SO2NR-, -NRSO2-, -NRC(O)NR-, -OC(O)NR-, -NRSO2NR-, -SO- или -SO2-;
Y представляет собой C1-10алифатическую группу, в которой до трех метиленовых звеньев заменены GY, где GY выбирают из -NR-, -O-, -S-, -CO2-, -OC(O)-, -C(O)CO-, -C(O)-, -C(O)NR-, -C(=N-CN), -NRCO-, -NRC(O)O-, -SO2NR-, -NRSO2-, -NRC(O)NR-, -OC(O)NR-, -NRSO2NR-, -SO- или -SO2-;
Ra представляет собой водород или C1-6алифатическую группу, необязательно замещенную 0-3 группами JR;
Rb представляет собой водород или незамещенную C1-6алифатическую группу;
n равно 0 или 1;
при условии, что:
если R1 и R2 представляют собой H, и Z2 и Z3 представляют собой H, то Z1 не является метилом;
если R1 представляет собой CH3, и R2 представляет собой H, то все Z1, Z2 и Z3 не являются H;
если R1 и R2 представляют собой H, и Z2 и Z3 представляют собой H, то Z1 не является незамещенным фенилом, 4-пиридилом или одной из структур, представленных ниже:
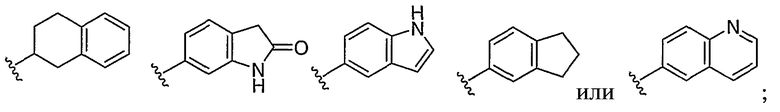
и
если R1 и R2 представляют собой H, то Z1 и Z2 вместе не являются -C≡C-CH2CH2COOH.
В соответствии с одним примером осуществления настоящего изобретения Z1, Z2 и Z3 образуют вместе с атомом углерода, к которому они присоединены, бициклическое кольцо, представленное на формуле II:
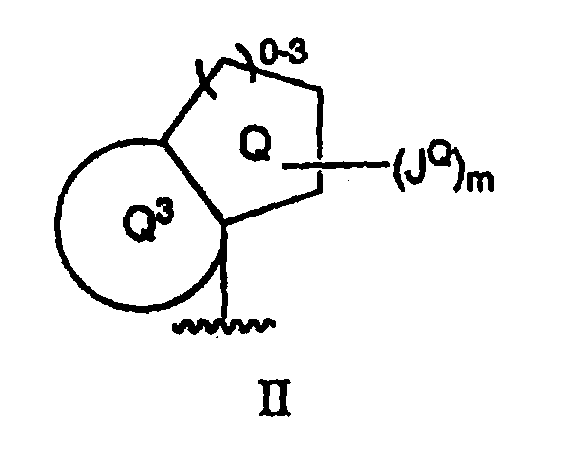
в которой
Q3 представляет собой 3-8-членное насыщенное, ненасыщенное или частично насыщенное моно циклическое кольцо;
каждый Q и Q3 необязательно и независимо замещен 0-4 группами JQ.
В одном примере осуществления Q3 представляет собой циклопропильную группу, необязательно замещенную 0-2 группами JQ, как представлено на формуле III:

В соответствии с другим примером осуществления настоящего изобретения Z1 и Z2 образуют вместе с атомом углерода, к которому они присоединены, моноциклическое, бициклическое или трициклическое кольцо, как представлено на формуле IV:

в которой
Z11 выбирают из С, N, О или S;
Z12 выбирают из С, N, О или S;
Q представляет собой 3-8-членное насыщенное или частично насыщенное моноциклическое кольцо, необязательно конденсированное с Q1 или Q2;
каждый Q1 и Q2 независимо представляет собой 3-8-членное насыщенное, ненасыщенное или частично насыщенное моноциклическое кольцо;
каждый Q, Q1 и Q2 независимо содержит до трех гетероатомов, выбранных из О, N или S;
m равно 0-4 и выбирается независимо для Q, Q1 и Q2; и
Z3 представляет собой Н; или если связь между С и Z11 является двойной, то Z3 отсутствует.
В некоторых примерах осуществления каждый Z11 и Z12 независимо представляет собой углерод.
В одном примере осуществления Q представляет собой С3-7 моноцикл, а Q1 и Q2 отсутствуют.
В другом примере осуществления Q и Q1 образуют вместе конденсированное 6-14-членное бициклическое кольцо, и Q2 отсутствует.
В еще одном примере осуществления Q, Q1 и Q2 образуют вместе конденсированное 8-20-членное трициклическое кольцо.
В одном примере осуществления настоящего изобретения Z12 представляет собой углерод, a Q, Q1 и необязательно Q2 образуют конденсированное кольцо, как представлено на формуле V:
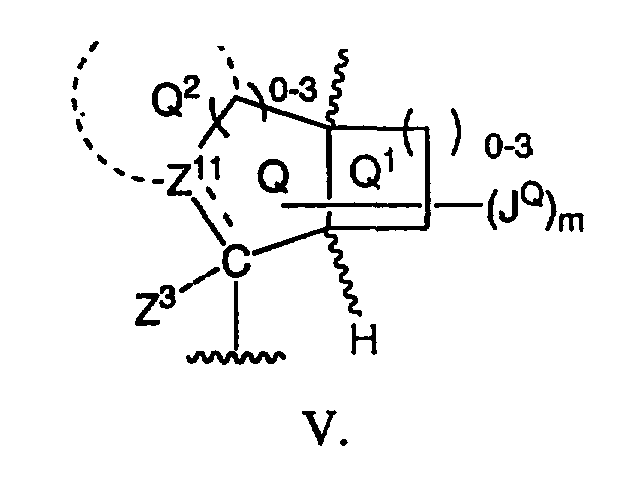
в которой каждый Q, Q1 и Q2 независимо и необязательно содержит
a) 0-2 гетероатома, выбранных из О, N или S; и
b) 0-4 заместителя JQ.
В одном примере осуществления атомы водорода в точке конденсации кольца Q и кольца Q1 находятся в цис-конформации, как представлено в формуле VI:

В другом примере осуществления атомы водорода в точке конденсации кольца Q и кольца Q1 находятся в транс-конформации.
В одном примере осуществления C-Z11 представляет собой одинарную связь.
В другом примере осуществления C=Z11 представляет собой двойную связь.
двух гетероатомов. В других примерах осуществления кольцо Q содержит один гетероатом; и в еще одних примерах осуществления кольцо Q не содержит гетероатомов.
В одном примере осуществления Q содержит два гетероатома, и каждый из упомянутых гетероатомов независимо выбирают из азота, серы или кислорода; предпочтительно из азота или серы; более предпочтительно из азота. В некоторых примерах осуществления оба гетероатома представляют собой азот. В других примерах осуществления один гетероатом представляет собой азот, а другой гетероатом представляет собой серу. В некоторых примерах осуществления один гетероатом представляет собой азот, а другой гетероатом представляет собой кислород. В еще одних примерах осуществления один гетероатом представляет собой азот, а другой гетероатом представляет собой серу.
В другом примере осуществления Q содержит один гетероатом, выбранный из O, N или S. В некоторых примерах осуществления гетероатом представляет собой кислород; в других примерах осуществления гетероатом представляет собой азот; в еще одних примерах осуществления гетероатом представляет собой серу. В некоторых примерах осуществления сера необязательно замещена 0, 1 или 2 оксогруппами.
Примеры гетероциклических групп включают пиперидин, пиперазин, морфолин, тиоморфолин и пирролидин.
В некоторых примерах осуществления кольцо Q представляет собой 5-7-членную циклоалифатическую группу. Примеры циклоалифатических групп включают циклогексан, циклопентан, циклогексен и циклопентен.
В других примерах осуществления Q1 представляет собой 6-членное арильное или 5-6-членное гетероарильное кольцо. Примеры арильных или гетероарильных колец включают фенил, пиридин, пиримидин, тиофен, тиазол, тетразол, триазол, пиррол, фуран и пиразол.
В некоторых примерах осуществления Q1 представляет собой 3-7-членное циклоалифатическое кольцо. Примеры циклоалифатических колец включают циклогексан, циклопентан, циклогексен, циклопентен, циклогептен, циклогептан, циклопропан, циклобутан, циклопропен и циклобутен.
В другом примере осуществления Q1 представляет собой 3-7-членное гетероциклическое кольцо. Примеры гетероциклических групп включают пиперидин, пиперазин, морфолин, тиоморфолин, пирролидин, гомопиперидин и гомопиперазин.
В одном примере осуществления Q или Q-Q1 представлены следующими структурами:


в которых каждый R7 и JQ независимо выбирают из водорода, Y, -(Vn)-CN, -(Vn)-NO2, -(Vn)-OH, -(Vn)-(C1-6алифатическая группа), -(Vn)-(C3-12гетероциклил), -(Vn)-(C6-10арил), -(Vn)-(5-10-членный гетероарил), -(Vn)-(C3-10циклоалифатическая группа) и -(C3-10циклоалифатическая группа)-(C3-12гетероциклил);
где для каждого Q и Q1 m независимо равно 0-3; и
каждый R7 и JQ необязательно и независимо замещен 0-10 группами JR.
В одном примере осуществления m равно 0, 1 или 2. В другом примере осуществления m равно 1 или 2. В некоторых примерах осуществления m равен 0; в других примерах осуществления m равен 1; в еще одних примерах осуществления m равно 2.
В некоторых примерах осуществления JQ представляет собой Y, -(V1 n)-CN, -(V1 n)-NO2, -(V1 n)-OH, -(V1 n)-(C1-6алифатическая группа), -(V1 n)-(C3-12гетероциклил), -(V1 n)-(C6-10арил), -(V1 n)-(5-10-членный гетероарил), -(V1 n)-(C3-10циклоалифатическая группа) или -(C3-10циклоалифатическая группа)-(C3-12гетероциклил); где
V1 представляет собой -GV-(X)p, где X представляет собой C1-9алифатическую группу, в которой до двух метиленовых звеньев заменены -NR-, -O-, -S-, -CO2-, -OC(O)-, -C(O)CO-, -C(O)-, -C(O)NR-, -C(=N-CN), -NRCO-, -NRC(O)O-, -SO2NR-, -NRSO2-, -NRC(O)NR-, -OC(O)NR-, -NRSO2NR-, -SO- или -SO2-;
p равно 0 или 1;
n равно 0 или 1;
GV выбирают из C=O, C(=O)NR, S(O)2 или S(O); и
упомянутая JQ необязательно замещена 0-10 группами JR.
В одном примере осуществления X представляет собой необязательно замещенную C1-4алифатическую группу. В некоторых примерах осуществления X представляет собой необязательно замещенный C1-4алкил. В некоторых примерах осуществления X представляет собой необязательно замещенный C1-2алкил.
В некоторых примерах осуществления n равно 0. В других примерах осуществления n равно 1. В определенных примерах осуществления p равно 0. В других примерах осуществления p равно 1.
В некоторых примерах осуществления JQ необязательно замещена 0-10 группами JR; в некоторых примерах осуществления 0-5 группами JR; в других примерах осуществления 0-3 группами JR; и в еще одних примерах осуществления 0-2 группами JR; в некоторых примерах осуществления одной группой JR и в определенных примерах осуществления не замещена группами JR.
В одном примере осуществления GV представляет собой C=O.
В другом примере осуществления настоящего изобретения каждый R1 и R2 независимо представляет собой H, галоген, C1-4алкил или C1-4алкокси. В одном примере осуществления каждый R1 и R2 независимо представляет собой H.
В некоторых примерах осуществления R7 независимо выбирают из Y, -(V1 n)-CN, -(V1 n)-NO2, -(V1 n)-OH, -(V1 n)-(C1-6алифатическая группа), -(V1 n)-(C3-12гетероциклил), -(V1 n)-(C6-10арил), -(V1 n)-(5-10-членный гетероарил), -(V1 n)-(C3-10циклоалифатическая группа) или -(C3-10циклоалифатическая группа)-(C3-12гетероциклил); где
V1 представляет собой -GV-(X)p, где X представляет собой C1-9алифатическую группу, в которой до двух метиленовых звеньев заменены -NR-, -O-, -S-, -CO2-, -OC(O)-, -C(O)CO-, -C(O)-, -C(O)NR-, -C(=N-CN), -NRCO-, -NRC(O)O-, -SO2NR-, -NRSO2-, -NRC(O)NR-, -OC(O)NR-, -NRSO2NR-, -SO- или -SO2-;
p равно 0 или 1;
n равно 0 или 1;
GV выбирают из C=O, C(=O)NR, S(O)2 или S(O).
Типичные примеры соединений формулы I представлены ниже в таблице 1.

Формула VI
в которой A выбирают из 
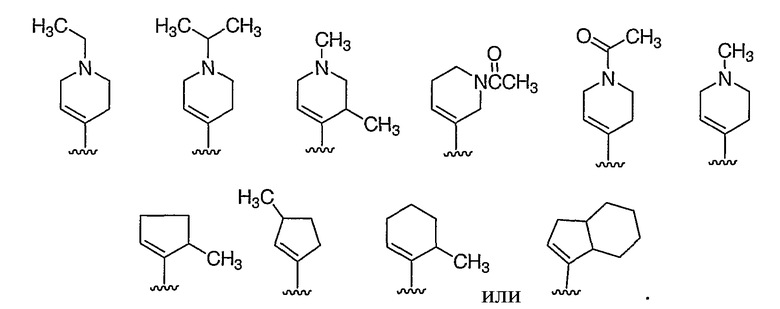
В другом примере осуществления настоящего изобретения Z1 и Z2 не объединены с образованием кольца и Z3 представляет собой H или отсутствует.
В одном примере осуществления Z1 представляет собой H или C1-6алифатическую группу, необязательно замещенную 0-3 группами JZ. В некоторых примерах осуществления Z представляет собой H.
В определенных примерах осуществления C≡Z1 представляет собой тройную связь, а Z2 и Z3 отсутствуют.
В других примерах осуществления C=Z1 представляет собой двойную связь и Z3 отсутствует.
В определенных примерах осуществления Z1 представляет собой O; в других примерах осуществления Z1 представляет собой CH2.
В определенных примерах осуществления Z2 представляет собой необязательно замещенную Y, -(Vn)-(C1-6алифатическая группа), -(Vn)-(C3-12гетероциклил), -(Vn)-(C6-10арил), -(Vn)-(5-10-членный гетероарил) или -(Vn)-(C3-10циклоалифатическая группа). В некоторых примерах осуществления n равно 0; в других примерах осуществления n равно 1.
В других примерах осуществления Z2 представляет собой необязательно замещенный 5-7-членный моноцикл, выбранный из гетероциклила, циклоалифатической группы, арила или гетероарила; предпочтительно 5-7-членный полностью или частично насыщенный моноцикл, выбранный из гетероциклила или циклоалифатической группы; более предпочтительно 6-членный моноцикл с 0-2 атомами азота. В одном предпочтительном примере осуществления настоящего изобретения Z2 представляет собой пиперидин, необязательно замещенный 0-3 группами JZ.
В некоторых примерах осуществления Z2 представляет собой необязательно замещенную -(Vn)-(C3-10циклоалифатическая группа), где n равен 0. В одном примере осуществления Z2 представляет собой бициклооктановое кольцо. В другом примере осуществления Z2 представляет собой C5-7циклоалифатическую группу. В еще одном примере осуществления Z2 представляет собой C5-7циклоалкил.
В одном примере осуществления Jz представляет собой галоген, CF3, необязательно замещенный C1-4галогеналкил, -(V1 n)-CN, -(V1 n)-NO2, -(V1 n)-OH, Y, -(V1 n)-(C3-12гетероциклил), -(V1 n)-(C6-10арил), -(V1 n)-(5-10-членный гетероарил), -(V1 n)-(C3-10циклоалифатическая группа) или -(C3-10циклоалифатическая группа)-(C3-12гетероциклил); где
V1 представляет собой -GV-(X)p, где X представляет собой C1-9алифатическую группу, в которой до двух метиленовых звеньев заменены -NR-, -O-, -S-, -CO2-, -OC(O)-, -C(O)CO-, -C(O)-, -C(O)NR-, -C(=N-CN), -NRCO-, -NRC(O)O-, -SO2NR-, -NRSO2-, -NRC(O)NR-, -OC(O)NR-, -NRSO2NR-, -SO- или -SO2-;
p равно 0 или 1; и
GV выбирают из C=O, C(=O)NR, S(O)2 или S(O).
В некоторых примерах осуществления X представляет собой C1-5алифатическую группу. В некоторых примерах осуществления X представляет собой C1-5алкил. В других предпочтительных примерах осуществления X представляет собой C1-2алкил.
В некоторых примерах осуществления GV выбирают из C=O, C(=O)NR, S(O)2 или S(O). В определенных примерах осуществления GV представляет собой C=O. В других примерах осуществления GV представляет собой C(=O)NR. В еще одних примерах осуществления GV представляет собой S(O)2 или S(O).
В некоторых примерах осуществления JZ представляет собой галоген, CF3, CN, необязательно замещенную C1-6алифатическую группу, C1-4галогеналкил, -(C1-6алкил)n-RJ, -(C1-6алкил)n-C(=O)RJ, -(C1-6алкил)n-CON(Rb)RJ, -(C1-6алкил)n-N(Rb)RJ, -(C1-6алкил)n-ORJ, -(C1-6алкил)n-OCON(Rb)RJ, -(C1-6алифатическая группа)n-S(O)N(Rb)RJ, -(C1-6алифатическая группа)n-S(O)RJ или -(C1-6алифатическая группа)n-NHC(O)RJ; где
RJ представляет собой C1-6алифатичекую группу, C3-12гетероциклил, C6-10арил, 5-10-членный гетероарил или C3-10циклоалифатическую группу; и
n равно 0 или 1.
В других примерах осуществления JZ представляет собой галоген, ORJ, N(Rb)2, CF3, CN, необязательно замещенный C1-6алкил, -(C1-6алкил)n-RJ, -C(=O)(C1-6алкил), -CON(Rb)(C1-6алкил), -OCON(Rb)(C1-6алкил), -S(O)N(Rb)(C1-6алкил), -S(O)(C1-6алкил), -NHC(O)C1-6алкил, -(C1-6алкил)-CONH, -(C1-6алкил)-N(Rb)2, -(C1-6алкил)-OCON(Rb)RJ, -(C1-6алифатическая группа)-S(O)N(Rb)(C6-10арил), -N(Rb)C(O)N(Rb)RJ или -N(Rb)C(O)Rb.
В других примерах осуществления JZ представляет собой галоген, OR, N(Rb)2, CF3, CN, необязательно замещенный C1-6алкил, -(C1-6алкил)n-RJ, C(=O)(C1-6алкил), CONH, -(C1-6алкил)-CONH, -(C1-6алкил)-N(Rb)2, -(C1-6алкил)-OCON(Rb)RJ, -(C1-6алифатическая группа)-S(O)N(Rb)(C6-10арил), -N(Rb)C(O)N(Rb)2 или -N(Rb)C(O)Rb.
В определенных примерах осуществления RJ представляет собой C6-10арил или 5-10-членный гетероарил. В других примерах осуществления RJ представляет собой C1-6алифатическую группу или C3-10циклоалифатическую группу. В некоторых примерах осуществления RJ представляет собой C1-6алифатическую группу. В других примерах осуществления RJ представляет собой C3-10циклоалифатическую группу.
В некоторых примерах осуществления n равно 1. В других примерах осуществления n равно 0.
В определенных примерах осуществления JZ представляет собой необязательно замещенный -C(=O)(C1-6алкил), -C(=O)CH2CN или C1-6алкил.
Типичные примеры соединений формулы I представлены ниже в таблице 2.
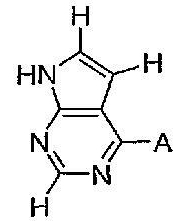
Формула VII
в которой A выбирают из


Типичные примеры соединений формулы I представлены ниже в таблице 3:
Таблица 3
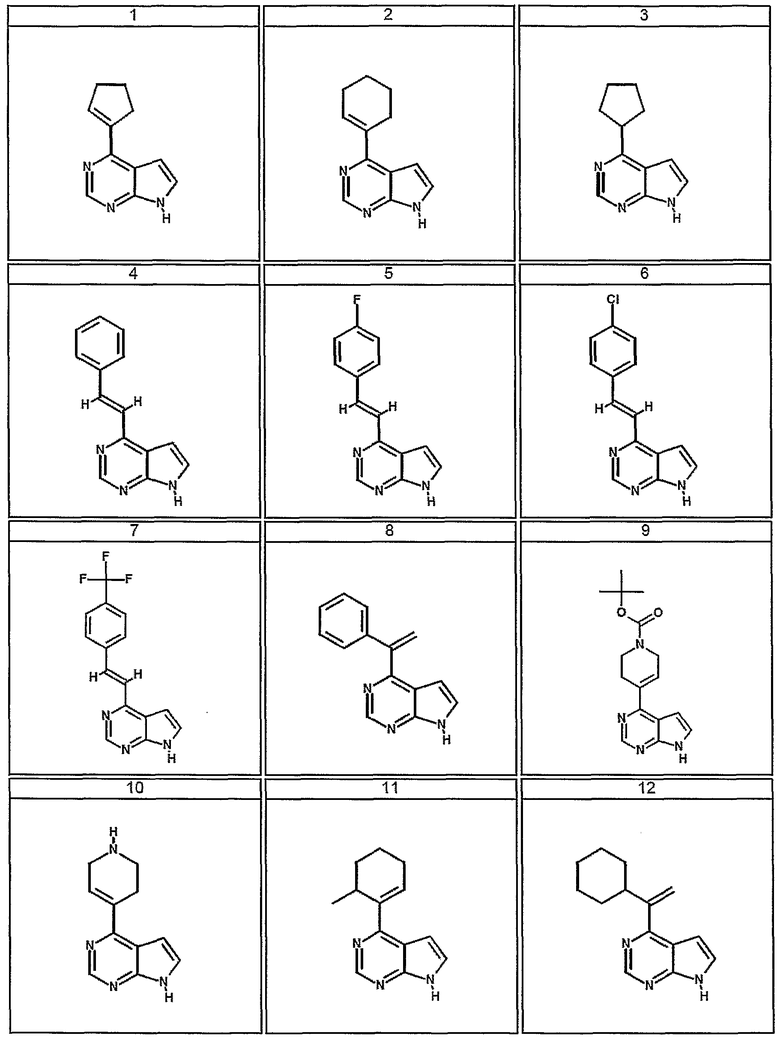


Общая методика синтеза
Соединения по настоящему изобретению могут быть, в целом, получены способами, известными специалистам в данной области техники для аналогичных соединений, или способами, представленными в приведенных ниже примерах. В общем, в примере 1 представлено несколько способов получения функционализированных хиноксалинов.
Хотя в этом документе в качестве примеров представлены и описаны определенные примеры осуществления, следует учитывать, что соединения по настоящему изобретению могут быть получены в соответствии со способами, описанными в общих чертах выше, с использованием подходящих исходных материалов, способами, как правило, доступными среднему специалисту в данной области техники.
Все ссылки, приведенные в схемах синтеза и примерах, включены в этот документ посредством ссылки. Все используемые в этом документе сокращения, символы и условные обозначения соответствуют таковым, используемым в современной научной литературе (см., например, Janet S. Dodd, ed., The ACS Style Guide: A Manual for Authors and Editors, 2nd Ed., Washington, D.C: American Chemical Society, 1997, включенный в этот документ во всей своей полноте посредством ссылки). Кроме того, следующие определения описывают термины и сокращения, используемые в этом документе:
(Ts-Cl - пара-толуолсульфонилхлорид (тозилхлорид);
DMF - диметилформамид;
Tf - трифлат;
LiHMDS - гексаметилдисилазид лития;
dppf - 1,1'-бис(дифенилфосфино)ферроцен;
Ac - ацетил;
DME - 1,2-диметоксиэтан;
atm -атм;
EDCI - гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида;
DIEA - диизопропилэтиламин;
LiHMDS - гексаметилдисилазан лития;
THF - тетрагидрофуран;
HEPES - 4-(2-гидроксиэтил)-1-пиперазинэтансульфоновая кислота;
Glu - глутамат;
Tyr - тирозин;
ATP - аденозинтрифосфат;
Ph - фенил;
Me - метил;
BSA - бычий сывороточный альбумин;
DTT - дитиотреитол)
Схема 1
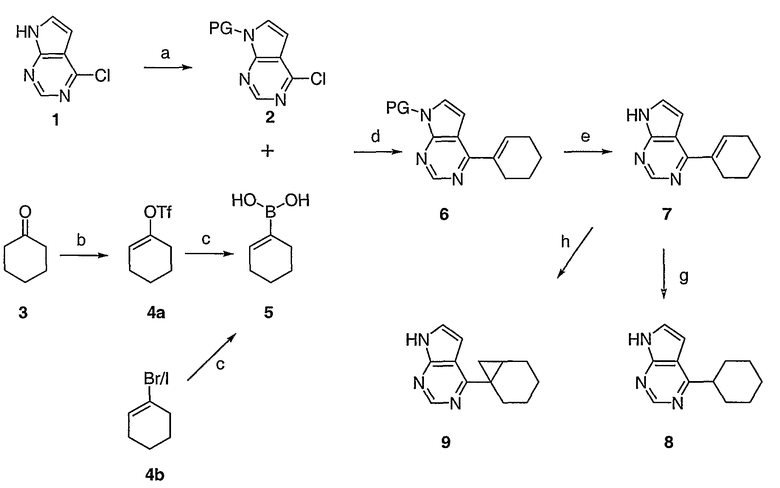
Условия: (a) Ts-Cl, K2CO3, DMF; (b) Tf2O, лутидин или LiHMDS, PhNTf2 от -78°C до комнатной температуры; (c) бис(пинаколято)боран, Pd(dppf)2Cl2, KOAc, затем вода; (d) Pd(PPh3)4, KOAc, диоксан или DME, 100-180°C; (f) LiOH или NaOMe; (g) Pd-C, атмосфера H2
Схема 1 представляет собой характерную схему получения соединений по настоящему изобретению. Соединение 1, которое является коммерчески доступным, может быть защищено подходящей защитной группой (например, тозилом), как описано в T.W. Greene & P.G.M Wutz, "Protective Groups in Organic Synthesis", 3rd Edition, John Wiley & Sons, Inc. (1999)), с получением соединения 2. Бороновые кислоты/сложные эфиры (5) могут быть получены из соответствующих винилгалогенидов (4b) или винилтрифлатов (4a), как описано в Comins, D.L.; Dehghani, A. Tetrahedron Lett. 1992, 33, 6299-6302; McMurry, J.E.; Scott, W.J. Tetrahedron Lett, 1983, 24, 979; Stang, P.J.; Fisk, P.J. Synthesis, 1980, 283; Stang, P.J.; Fisk, P.J. Synthesis, 1979, 438; Takagi, J.; Takahashi, K.; Ishiyama, T.; Miyaura, N. J. Am. Chem. Soc, 2002, 124, 8001 и в приведенных в них ссылках. Путем катализируемого Pd кросс-сочетания N-защищенного галогенида (например, хлорида) (2) и бороновой кислоты (3) в присутствии подходящего основания, такого как KOAc или Na2CO3, получают соединения типа (6), как описано в A. Suzuki, H.C. Brown "Organic Synthesis Via Boranes; Volume 3: Suzuki Coupling" Aldrich Chemical Company: Milwaukee, WI, 2003 и в приведенных в ней ссылках. Путем снятия защиты в щелочных условиях (например, водный LiOH или NaOMe) получают (7). Путем гидрирования с Pd-C в атмосфере H2 получают (8). Путем циклопропанирования (7), как описано в Reiser, Oliver "Cyclopropanation and other reactions of palladium-carbene (and carbyne) complexes" Handbook of Organopalladium Chemistry for Organic Synthesis (2002), 1 1561-1577, получают (9).
Схема 2

Условия: (a) i: HCl-HNMeOMe, EDCI, DIEA; ii: MeMgBr; (b) LiHMDS, PhNTf2, THF, -78°C; (c) бис(пинаколято)боран, Pd(dppf)2Cl2, KOAc, затем вода; (d) Pd(PPh3)4, KOAc, диоксан или DME, 100-180°C; (e) i: LiOH или NaOMe, ii: HCl,; (f) R'COCl, R'OCOCl или R'NCO; DIEA или R'OOH; EDCI; и DIEA (где R'COCl, R'OCOCl и R'NCO относится к подходящим хлорангидридам, оксалилхлоридам и изоцианатам, которые либо являются коммерчески доступными, либо могут быть получены из коммерчески доступных исходных материалов).
На схеме 2 представлены дополнительные способы получения соединений по настоящему изобретению. В дополнение к хлорангидридам, изоцианатам и оксалилхлоридам, другие взаимодействующие с аминами соединения могут использоваться для осуществления P1-замещений. Примеры включают без ограничения R'-галоген, R'-тозил, R'-мезилат, R'S(O)2Cl, R'NS(O)2Cl, R'OH, R'COOH и R'CH2-галоген. Содержащие -C=CH2 соединения могут быть необязательно преобразованные в содержащие -C=O соединения путем озонолиза (g).
Схема 3
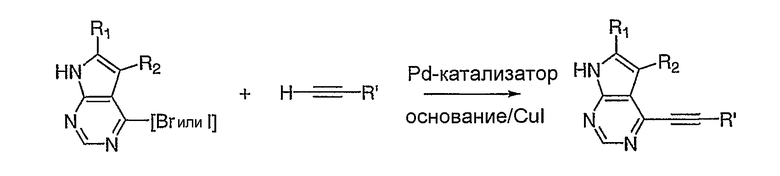
На схеме 3 представлен дополнительный способ получения соединений по настоящему изобретению. Может быть осуществлено сочетание арилбромида или арилйодида с замещенными терминальными алкинами в присутствии палладиевого катализатора и CuI в условиях проведения сочетания по Sonogashira (Sonogashira, Kenkichi. "Palladium-catalyzed alkynylation" Editor(s): Negishi, Ei-ichi. Handbook of Organopalladium Chemistry for Organic Synthesis (2002), 1: 493-529. Publisher: John Wiley & Sons, Inc., Hoboken, N.J.) с получением представленного продукта. Обозначение  относится к подходящим терминальным алкинам, которые либо являются коммерчески доступными, либо могут быть получены из коммерчески доступных исходных материалов.
относится к подходящим терминальным алкинам, которые либо являются коммерчески доступными, либо могут быть получены из коммерчески доступных исходных материалов.
Хотя в описании в качестве примеров представлены и описаны определенные примеры осуществления, следует учитывать, что соединения по настоящему изобретению могут быть получены в соответствии со способами, описанными в общих чертах выше, с использованием подходящих исходных материалов способами, как правило, доступными среднему специалисту в данной области техники.
Применения, составы и введение
Как обсуждалось ранее, настоящее изобретение относится к соединениям, которые представляют собой ингибиторы протеинкиназ, включая киназы семейств JAK, ROCK и PKA, в частности киназы JAK2 и JAK3, а потому соединения по настоящему изобретению применимы для лечения заболеваний, нарушений или состояний, включая без ограничения иммунодефицитные нарушения, воспалительные заболевания, аллергические заболевания, аутоиммунные заболевания, пролиферативные нарушения, иммунологически опосредованные заболевания, респираторные нарушения. Соответственно, в другом аспекте настоящее изобретение относится к фармацевтически приемлемым композициям, причем указанные композиции содержат любое из описанных в этом документе соединений и необязательно содержит фармацевтически приемлемый носитель, адъювант или растворитель. В определенных примерах осуществления указанные композиции необязательно дополнительно содержат одно или несколько дополнительных терапевтических средств.
Также следует понимать, что предназначенные для лечения определенные соединения по настоящему изобретению могут существовать в свободной форме или, когда это целесообразно, в виде его фармацевтически приемлемого производного. В соответствии с настоящим изобретением фармацевтически приемлемое производное включает без ограничения фармацевтически приемлемые соли, сложные эфиры, соли сложных эфиров или любой другой аддукт или производное, которые при введении нуждающемуся в этом пациенту способны являться источником, прямо или опосредованно, описанного в этом изобретении соединения или его метаболита или остатка.
Используемый в этом документе термин «фармацевтически приемлемая соль» относится к тем солям, которые, с точки зрения лечащего врача, подходят для применения в контакте с тканями человека и низших животных без возникновения нежелательной токсичности, раздражения, аллергической реакции и тому подобное и соответствуют приемлемому соотношению между эффектом и степенью риска. Термин «фармацевтически приемлемая соль» означает любую нетоксичную соль соединения по настоящему изобретению.
Фармацевтически приемлемые соли хорошо известны в данной области техники. Например, S.M. Berge et al. подробно описывают фармацевтически приемлемые соли в Pharmaceutical Sciences, 1977, 66, 1-19, включенной в этот документ посредством ссылки. Фармацевтически приемлемые соли по настоящему изобретению включают соли, полученные из подходящих неорганических и органических кислот и оснований. Примерами фармацевтически приемлемых нетоксичных солей добавления кислоты являются соли аминогруппы, образованные с неорганическими кислотами, такими как соляная кислота, бромистоводородная кислота, фосфорная кислота, серная кислота и перхлорная кислота, или с органическими кислотами, такими как уксусная кислота, щавелевая кислота, малеиновая кислота, винная кислота, лимонная кислота, янтарная кислота или малоновая кислота, или с использованием других способов, применяемых в данной области техники, таких как ионообмен. Другие фармацевтически приемлемые соли включают адипаты, альгинаты, аскорбаты, аспартаты, бензолсульфонаты, бензоаты, бисульфаты, бораты, бутираты, камфораты, камфорсульфонаты, цитраты, циклопентанпропионаты, диглюконаты, додецилсульфаты, этансульфонаты, формиаты, фумараты, глюкогептонаты, глицерофосфаты, глюконаты, гемисульфаты, гептаноаты, гексаноаты, гидройодиды, 2-гидроксиэтансульфонаты, лактобионаты, лактаты, лаураты, лаурилсульфаты, малаты, малеаты, малонаты, метансульфонаты, 2-нафталинсульфонаты, никотинаты, нитраты, олеаты, оксалаты, пальмитаты, памоаты, пектинаты, персульфаты, 3-фенилпропионаты, фосфаты, пикраты, пивалаты, пропионаты, стеараты, сукцинаты, сульфаты, тартраты, тиоцианаты, пара-толуолсульфонаты, ундеканоаты, валераты, и тому подобное. Соли, полученные из подходящих оснований, включают соли щелочных металлов, щелочноземельных металлов, аммония и N+(C1-4алкил)4. Настоящее изобретение также предусматривает кватернизацию любых основных азотсодержащих групп соединений, раскрытых в этом документе. Путем такой кватернизации могут быть получены растворимые в воде или жирорастворимые или диспергируемые продукты. Примеры солей щелочных или щелочноземельных металлов включают соли натрия, лития, калия, кальция, магния, и тому подобное. Дополнительные фармацевтически приемлемые соли включают, когда это целесообразно, нетоксичные катионы аммония, четвертичного аммония и амина, образованные с использованием противоионов, таких как галогенид, гидроксид, карбоксилат, сульфат, фосфат, нитрат, (низший алкил)сульфонат или арилсульфонат.
Как описано выше, фармацевтически приемлемые композиции по настоящему изобретению дополнительно содержат фармацевтически приемлемый носитель, адъювант или растворитель, который, как используется в этом документе, включает все без исключения растворители, разбавители или другой жидкий растворитель, вспомогательные диспергирующие или суспендирующие средства, поверхностно-активные вещества, придающие изотоничность вещества, загустители или эмульгаторы, консерванты, твердые связующие вещества, смазки, и тому подобное, пригодные для конкретно требуемой дозированной формы. В работе Remington's Pharmaceutical Sciences, Sixteenth Edition, E.W. Martin (Mack Publishing Co., Easton, Pa., 1980) раскрыты различные носители, используемые в составлении фармацевтически приемлемых композиций и известные методики их приготовления. За исключением тех случаев, когда любая традиционно используемая среда несовместима с соединениями по настоящему изобретению, например, вызывая нежелательный биологический эффект или иначе неблагоприятно взаимодействуя с другой компонентой (компонентами) фармацевтически приемлемой композиции, предполагается, что ее применение подпадает под объем настоящего изобретения. Некоторые примеры веществ, которые могут служить в качестве фармацевтически приемлемых носителей, включают без ограничения ионообменники, окись алюминия, стеарат алюминия, лецитин, сывороточные белки, такие как сывороточный альбумин человека, буферные вещества, такие как фосфаты, глицин, сорбиновая кислота или сорбат калия, смеси неполных глицеридов насыщенных растительных жирных кислот, воду, соли или электролиты, такие как сульфат протамина, двузамещенный фосфорнокислый натрий, гидрофосфат калия, хлорид натрия, соли цинка, коллоидный кремнезем, трисиликат магния, поливинилпирролидон, полиакрилаты, воски, блок-сополимеры полиэтилена/полипропилена, ланолин, сахара, такие как лактоза, глюкоза и сахароза; крахмалы, такие как кукурузный крахмал и картофельный крахмал; целлюлозу и ее производные, такие как карбоксиметилцеллюлоза, этилцеллюлоза и ацетатцеллюлоза натрия; порошкообразный трагакант; солод; желатин; тальк; наполнители, такие как какао-масло и воски для суппозиториев; масла, такие как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; гликоли, такие как пропиленгликоль или полиэтиленгликоль; сложные эфиры, такие как этилолеат и этиллаурат; агар; буферные вещества, такие как гидроксид магния и гидроксид алюминия; альгиновую кислоту; апирогенную воду; изотонический солевой раствор; раствор Рингера; этиловый спирт и фосфатные буферные растворы; а также другие нетоксичные совместимые смазки, такие как лаурилсульфат натрия и стеарат магния, а также красители, антиадгезивы, глазировочные средства, подслащивающие вещества, вкусовые и ароматизирующие добавки, консерванты и антиоксиданты могут также содержаться в композиции по решению составителя смеси.
В еще одном аспекте настоящее изобретение относится к способу лечения или ослабления тяжести пролиферативного нарушения, нарушения сердечной деятельности, нейродегенеративного нарушения, аутоиммунного нарушения, состояния, связанного с пересадкой органа, воспалительного нарушения или иммунологически опосредованного нарушения, включающему введение эффективного количества соединения или содержащей соединение фармацевтически приемлемой композиции нуждающемуся в этом пациенту. В определенных примерах осуществления настоящего изобретения «эффективное количество» соединения или фармацевтически приемлемой композиции представляет собой такое количество, которое эффективно для лечения или ослабления тяжести пролиферативного нарушения, нарушения сердечной деятельности, нейродегенеративного нарушения, аутоиммунного нарушения, состояния, связанного с пересадкой органа, воспалительного нарушения, психотического нарушения, вирусного заболевания, заболевания костей или иммунологически опосредованного нарушения. В соответствии со способом по настоящему изобретению соединения и композиции могут вводиться с использованием любого количества и любого пути введения, эффективного для лечения или ослабления тяжести пролиферативного нарушения, нарушения сердечной деятельности, нейродегенеративного нарушения, аутоиммунного нарушения, состояния, связанного с пересадкой органа, воспалительного нарушения, психотического нарушения, вирусного заболевания, заболевания костей или иммунологически опосредованного нарушения. Точное требуемое количество может варьировать от субъекта к субъекту в зависимости от вида, возраста и общего состояния субъекта, тяжести инфекции, конкретного средства, его способа введения, и тому подобное. Соединения по настоящему изобретению предпочтительно включают в состав дозированной формы для облегчения введения и равномерности дозировки. Используемое в этом документе выражение «дозированная форма» относится к физически дискретной единице средства, подходящей для подвергаемого лечению пациенту. Однако следует понимать, что общая суточная дозировка соединений и композиций по настоящему изобретению определяется по обоснованному суждению лечащего врача. Конкретная эффективная дозировка для любого конкретного пациента или организма может зависеть от различных факторов, включая подвергаемое лечению нарушение и тяжесть нарушения; активность конкретно применяемого соединения; конкретно применяемую композицию; возраст, массу тела, общее состояние здоровья, пол и рацион питания пациента; время введения, путь введения и скорость выведения конкретно применяемого соединения; продолжительность лечения; лекарственные средства, применяемые в сочетании или совместно с конкретно применяемым соединением, и сходные факторы, хорошо известные в области медицины. Используемый в этом документе термин «пациент» означает животное, предпочтительно млекопитающее и наиболее предпочтительно человека.
Фармацевтически приемлемые композиции по настоящему изобретению могут вводиться человеку и другим животным перорально, ректально, парентерально, интрацистернально, интравагинально, интраперитонеально, местно (то есть в виде порошков, мазей или капель), буккально, в виде перорального или назального спрея, и тому подобное, в зависимости от тяжести подвергаемой лечению инфекции. В определенных примерах осуществления для получения требуемого терапевтического эффекта соединения по настоящему изобретению могут один или несколько раз в сутки водиться перорально или парентерально в дозировках от приблизительно 0,01 мг/кг до приблизительно 50 мг/кг и предпочтительно от приблизительно 1 мг/кг до приблизительно 25 мг/кг массы тела субъекта в сутки.
Жидкие дозированные формы для перорального введения включают без ограничения фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. В дополнение к активным соединениям жидкие дозированные формы могут содержать обычно используемые в данной области техники инертные разбавители, такие как, например, воду и другие растворители, солюбилизаторы и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, масла (в частности, хлопковое, арахисовое, кукурузное, зародышевое, оливковое, касторовое и кунжутное масла), глицерин, тетрагидрофурфуриловый спирт, полиэтиленгликоли и сложные жирнокислые эфиры сорбитана и их смеси. Помимо инертных разбавителей пероральные композиции могут также содержать адъюванты, такие как смачивающие средства, эмульгаторы и суспендирующие средства, подслащивающие вещества, вкусовые и ароматические добавки.
Инъецируемые препараты, например стерильные инъецируемые водные или масляные суспензии, могут быть составлены в соответствии с известным уровнем техники с использованием подходящих диспергирующих или смачивающих средств и суспендирующих средств. Стерильный инъецируемый препарат может также представлять собой стерильный инъецируемый раствор, суспензию или эмульсию в нетоксичном приемлемом для парентерального введения разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. Среди приемлемых основ и растворителей, которые могут применяться, могут быть названы вода, раствор Рингера, U.S.P. и изотонический раствор хлорида натрия. Кроме того, в качестве растворителя или суспендирующей среды могут традиционно применяться стерильные нелетучие масла. Для этих целей может применяться любое легкое нелетучее масло, включая синтетические моноглицериды и диглицериды. Кроме того, в инъецируемых препаратах применяются жирные кислоты, такие как олеиновая кислота.
Инъецируемые препараты могут быть стерилизованы, например, путем фильтрации через удерживающий бактерии фильтр или путем включения в состав стерилизующих агентов в форме стерильных твердых композиций, которые перед применением могут быть растворены или диспергированы в стерильной воде или в другой стерильной среде для инъекций.
Для того чтобы продлить эффект соединения по настоящему изобретению, часто желательно замедлить всасывание соединения из подкожных или внутримышечных инъекций. Это может быть достигнуто путем использования жидкой суспензии кристаллического или аморфного материала, плохо растворимого в воде. Скорость всасывания соединения тогда зависит от скорости его растворения, что, в свою очередь, может зависеть от размера кристаллов и кристаллической формы. В качестве альтернативы, замедленное всасывание парентерально вводимого соединения достигается путем растворения или суспендирования соединения в масляной основе. Инъецируемые формы с замедленным высвобождением получают путем формирования микроинкапсулированных матриц соединения в биоразрушаемых полимерах, таких как полилактид/полигликолид. В зависимости от соотношения соединения и полимера и природы конкретно используемого полимера может регулироваться скорость высвобождения соединения. Примеры других биоразрушаемых полимеров включают поли(ортоэфиры) и поли(ангидриды). Инъецируемые составы с замедленным высвобождением также получают путем захватывания соединения липосомами или микроэмульсиями, совместимыми с тканями тела.
Композиции для ректального или вагинального введения предпочтительно представляют собой суппозитории, которые могут быть получены путем смешивания соединений по настоящему изобретению с подходящими не вызывающими раздражение наполнителями или носителями, такими как какао-масло, полиэтиленгликоль или воск для суппозиториев, которые являются твердыми при температуре окружающей среды, но жидкими при температуре тела, а потому плавятся в прямой кишке или вагине и высвобождают активное соединение.
Твердые дозированные формы для перорального введения включают капсулы, таблетки, пилюли, порошки и гранулы. В таких твердых дозированных формах активное соединение смешивают, по крайней мере, с одним инертным фармацевтически приемлемым наполнителем или носителем, таким как цитрат натрия или дикальцийфосфат и/или: a) наполнители или разбавляющие добавки, такие как крахмалы, лактоза, сахароза, глюкоза, маннит или кремниевая кислота, b) связующие вещества, такие как, например, карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидон, сахароза и аравийская камедь, c) увлажнители, такие как глицерин, d) разрыхлители, такие как агар-агар, карбонат кальция, картофельный крахмал или тапиоковый крахмал, альгиновая кислота, определенные силикаты и карбонат натрия, e) замедляющие растворение агенты, такие как парафин, f) ускорители всасывания, такие как четвертичные соединения аммония, g) смачивающие агенты, такие как, например, цетиловый спирт и моностеарат глицерина, h) абсорбенты, такие как каолин и бентонитовая глина, и i) смазки, такие как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия, и их смеси. В случае капсул, таблеток и пилюль дозированная форма может также содержать буферные вещества.
Твердые композиции сходного типа могут также применяться в качестве наполнителя мягких и твердых желатиновых капсул с использованием таких наполнителей, как лактоза или молочный сахар, а также высокомолекулярных полиэтиленгликолей, и тому подобное. Твердые дозированные формы в виде таблеток, драже, капсул пилюль и гранул могут быть приготовлены с использованием покрытий и оболочек, таких как энтеросолюбильные покрытия и другие покрытия, хорошо известные в области фармацевтики. Они могут необязательно содержать контрастные вещества, а также могут быть частью композиции, которая высвобождает активный ингредиент (ингредиенты) исключительно или предпочтительно в определенной части желудочно-кишечного тракта, необязательно замедленным путем. Примеры возможных для применения композиций для имплантации могут включать полимерные вещества и воски. Твердые композиции сходного типа могут также применяться в качестве наполнителя мягких и твердых желатиновых капсул с использованием таких наполнителей, как лактоза или молочный сахар, а также высокомолекулярных полиэтиленгликолей, и тому подобное.
Активные соединения могут также находиться в микроинкапсулированной форме с одним или несколькими наполнителями, как отмечено выше. Твердые дозированные формы в виде таблеток, драже, капсул, пилюль и гранул могут быть приготовлены с использованием покрытий и оболочек, таких как энтеросолюбильные покрытия, регулирующие высвобождение покрытия, и другие покрытия, хорошо известные в области фармацевтики. В таких твердых дозированных формах активное соединение может быть смешано, по крайней мере, с одним инертным разбавителем, таким как сахароза, лактоза или крахмал. Такие дозированные формы могут также содержать, как и в обычной практике, дополнительные вещества, отличные от инертных разбавителей, например смазки для таблетирования и другие вспомогательные средства для таблетирования, такие как стеарат магния и микрокристаллическая целлюлоза. В случае капсул, таблеток и пилюль дозированные формы могут также содержать буферные вещества. Они могут необязательно содержать контрастные вещества, а также могут быть частью композиции, которая высвобождает активный ингредиент (ингредиенты) исключительно или предпочтительно в определенной части желудочно-кишечного тракта, необязательно, замедленным путем. Примеры возможных для применения композиций для имплантации включают полимерные вещества и воски.
Дозированные формы для местного или чрескожного введения соединения по настоящему изобретению включают мази, пасты, кремы, лосьоны, гели, порошки, растворы, спреи, ингаляторы или пластыри. Активный компонент смешивают в стерильных условиях с фармацевтически приемлемым носителем и любыми необходимыми консервантами или буферными веществами, которые могут понадобиться. Подразумевается, что офтальмический состав, ушные капли и глазные капли включены в объем настоящего изобретения. Кроме того, настоящим изобретением предусматривается применение пластырей для чрескожного введения, которые обладают дополнительным преимуществом регулируемого введения соединения в организм. Такие дозированные формы могут быть получены путем растворения или диспергирования соединения в подходящей среде. Для увеличения скорости потока соединения через кожу также могут использоваться усилители всасывания. Скорость может регулироваться либо путем оснащения контролирующей скорость мембраной, либо путем диспергирования соединения в полимерной матрице или геле.
Как в общих чертах описано выше, соединения по настоящему изобретению применимы в качестве ингибиторов протеинкиназ, в частности киназ семейства JAK, ROCK и PKA. В конкретном примере осуществления соединения и композиции по настоящему изобретению являются ингибиторами JAK2 и JAK3. Соединения и композиции применимы для лечения или ослабления тяжести заболевания, состояния или нарушения, где в развитие заболевания, состояния или нарушения вовлечена активация киназы семейства JAK, ROCK и/или PKA. В особенном примере осуществления соединения и композиции применимы для лечения или ослабления тяжести заболевания, состояния или нарушения, где в развитие заболевания, состояния или нарушения вовлечена активация JAK2 или JAK3. Если в развитие конкретного заболевания, состояния или нарушения вовлечена активация JAK2, JAK3, ROCK или PKA, то заболевание, состояние или нарушение может также называться «JAK2-опосредованным заболеванием», «JAK3-опосредованным заболеванием», «ROCK-опосредованным заболеванием» или «PKA-опосредованным заболеванием» соответственно. Следовательно, в другом аспекте настоящее изобретение относится к способу лечения или ослабления тяжести заболевания, состояния или нарушения, где в развитие болезненного состояния вовлечена активация киназы семейства JAK, ROCK или PKA, в особенности JAK2 или JAK3.
Активность соединения, используемого в настоящем изобретении в качестве ингибитора киназы семейства JAK, ROCK или PKA, в особенности JAK2 или JAK3, может быть проанализирована in vitro, in vivo или на клеточной линии. Методы анализа in vitro включают методы, в которых определяется либо фосфорилирующая активность, либо АТФазная активность активированной JAK2, JAK3, ROCK или PKA. В альтернативных методах анализа in vitro количественно оценивается способность ингибитора связываться с JAK2, JAK3, ROCK или PKA. Связывание ингибитора может быть измерено путем радиоактивного мечения ингибитора перед связыванием, выделения комплекса ингибитор/киназа и определения количества связанной радиоактивной метки. В качестве альтернативы, связывание ингибитора может быть определено путем проведения эксперимента с конкурентным связыванием, где новые ингибиторы инкубируют с представляющей интерес киназой, связанной с известными радиоактивными лигандами.
Используемый в этом документе термин «явно ингибировать» означает определяемое изменение активности JAK2, JAK3, ROCK или PKA в образце, содержащем упомянутую композицию и JAK2, JAK3, ROCK или PKA, по сравнению с эквивалентным образцом, содержащим JAK2, JAK3, ROCK или PKA соответственно, в отсутствие упомянутой композиции.
Используемый в этом документе термин «JAK3-опосредованное заболевание» или «JAK3-опосредованное состояние» означает любое заболевание или другое вредное состояние, в котором, как известно, играет роль JAK3. JAK3-опосредованное состояние или заболевание также означает такие заболевания или состояния, которые смягчаются путем лечения ингибитором JAK3. Такие состояния включают без ограничения иммунные реакции, такие как аллергические реакции или реакции гиперчувствительности I типа, астма, аутоиммунные заболевания, такие как отторжение трансплантата, реакция «трансплантат против хозяина», ревматоидный артрит, латеральный амиотрофический склероз и рассеянный склероз, нейродегенеративные нарушения, такие как семейный латеральный амиотрофический склероз (FALS), а также злокачественные солидные опухоли и опухоли крови, такие как лейкозы и лимфомы.
Используемый в этом документе термин «JAK2-опосредованное заболевание» или «JAK2-опосредованное состояние» означает любое заболевание или другое вредное состояние, в котором, как известно, играет роль JAK2. JAK2-опосредованное состояние или заболевание также означает такие заболевания или состояния, которые смягчаются путем лечения ингибитором JAK2. Такие состояния включают, без ограничения, миелопролиферативные нарушения, включая истинную полицитемию, эссенциальную тромбоцитемию, хронический идиопатический миелофиброз, миелоидную метаплазию с миелофиброзом, хронический миелолейкоз, хронический миеломоноцитарный лейкоз, хронический эозинофильный лейкоз, гиперэозинофильный синдром и системный клеточный мастоцитоз.
Используемый в этом документе термин «ROCK-опосредованное заболевание» или «ROCK-опосредованное состояние» означает любое заболевание или другое вредное состояние, в котором, как известно, играет роль ROCK. ROCK-опосредованное состояние или заболевание также означает такие заболевания или состояния, которые смягчаются путем лечения ингибитором ROCK. Такие состояния включают, без ограничения, гипертензию, стенокардию, грудную жабу, цереброваскулярное сокращение, астму, нарушение периферического кровообращения, преждевременные роды, рак, эректильную дисфункцию, артериосклероз, спазм (церебральный вазоспазм или коронароспазм), ретинопатию (например, глаукома), воспалительные нарушения, аутоиммунные нарушения, СПИД, остеопороз, гипертрофию миокарда, вызванное ишемией/реперфузией повреждение, эндотелиальную дисфункцию, болезнь Альцгеймера или доброкачественную гиперплазию предстательной железы. В других примерах осуществления такие состояния, в которых, как известно, играет роль ROCK, включают, без ограничения, гипертензию, церебральный вазоспазм, коронарный вазоспазм, бронхиальную астму, преждевременные роды, эректильную дисфункцию, глаукому, пролиферацию гладкомышечных клеток сосудов, гипертрофию миокарда, малигному, вызванное ишемией/реперфузией повреждение, эндотелиальную дисфункцию, болезнь Крона и колит, разрастание нейритов, болезнь Рейно, стенокардию, болезнь Альцгеймера, доброкачественную гиперплазию предстательной железы или атеросклероз.
Используемый в этом документе термин «PKA-опосредованное заболевание» или «PKA-опосредованное состояние» означает любое заболевание или другое вредное состояние, в котором, как известно, играет роль PKA. Термин «RKА-опосредованное заболевание или состояние» также означает такие состояния или заболевания, которые смягчаются путем лечения ингибитором PKA. PKA-опосредованные заболевания или состояния включают, без ограничения, пролиферативные нарушения и рак.
Следует также понимать, что соединения и фармацевтически приемлемые композиции по настоящему изобретению могут применяться в комбинированных видах терапии, т.е. соединения и фармацевтически приемлемые композиции могут вводиться одновременно с одним или несколькими другими желаемыми терапевтическими средствами или медицинскими процедурами, перед ними или после них. При конкретном сочетании видов лечения (терапевтических средств или процедур) для проведения комбинированного лечения необходимо принимать во внимание совместимость желаемых терапевтических средств и/или процедур и требуемого терапевтического эффекта, который необходимо достичь. Следует также понимать, что использование выбранных видов лечения позволяет достичь требуемого эффекта для одного и того же нарушения (например, соединение по настоящему изобретению может вводиться одновременно с другим средством, используемым для лечения того же заболевания), или они могут достигать различных эффектов (например, регулирование любых нежелательных эффектов). Дополнительные терапевтические средства, которые обычно вводят для лечения или предупреждения конкретного заболевания или состояния, известны в этом документе как «соответствующие подвергаемому лечению заболеванию или состоянию».
Количество дополнительного терапевтического средства, содержащегося в композициях по настоящему изобретению, не может быть большим, чем количество, обычно вводимое в композиции, содержащей указанное терапевтическое средство в качестве единственного активного ингредиента. Предпочтительно количество дополнительного терапевтического средства в раскрытых в настоящем изобретении композициях может варьировать от приблизительно 50% до 100% от количества, обычно содержащегося в композиции, содержащей указанное средство в качестве единственного терапевтически активного ингредиента.
Соединения по настоящему изобретению или содержащие их фармацевтически приемлемые композиции могут также входить в состав композиций для покрытия имплантируемых медицинских устройств, таких как протезы, искусственные клапаны, сосудистые трансплантаты, стенты и катетеры. Соответственно, в другом аспекте настоящее изобретение относится к композиции для покрытия имплантируемого устройства, содержащего соединение по настоящему изобретению, описанное в общих чертах выше, и его классах и подклассах, и носитель, подходящий для покрытия упомянутого имплантируемого устройства. В еще одном аспекте настоящее изобретение относится к имплантируемому устройству, покрытому композицией, содержащей соединение по настоящему изобретению, описанное в общих чертах выше, и его классах и подклассах, и носитель, подходящий для покрытия упомянутого имплантируемого устройства.
Сосудистые стенты, например, использовались для преодоления рестеноза (повторного сужения сосудистой стенки после повреждения). Однако у пациентов со стентами или другими имплантируемыми устройствами существует риск образования тромба или активации тромбоцитов. Эти нежелательные эффекты могут быть предупреждены или ослаблены путем предварительного покрытия устройства фармацевтически приемлемой композицией, содержащей ингибитор киназ. Подходящие покрытия и общее получение покрытых имплантируемых устройств описаны в патентах США № 6099562, 5886026 и 5304121. Покрытия обычно представляют собой биосовместимые полимерные материалы, такие как гидрогельполимер, полиметилдисилоксан, поликапролактон, полиэтиленгликоль, полимолочная кислота, этиленвинилацетат и их смеси. Для придания композиции характеристик регулируемого высвобождения на покрытия может быть необязательно нанесено подходящее поверхностное покрытие из фторсиликона, полисахаридов, полиэтиленгликоля, фосфолипидов или их комбинаций.
Другой аспект настоящего изобретения относится к способу ингибирования активности JAK2, JAK3, ROCK или PKA в биологическом образце, который включает приведение упомянутого биологического образца в контакт с соединением формулы I или с композицией, содержащей упомянутое соединение. Используемый в этом документе термин «биологический образец» представляет собой ex vivo или in vitro образец, и включает, без ограничения, клеточные культуры или их экстракты; полученный от млекопитающего биоптат или его экстракты; и кровь, слюну, мочу, кал, семенную жидкость, слезы или другие жидкости организма или их экстракты.
Ингибирование активности киназы JAK2, JAK3, ROCK или PKA в биологическом образце применимо для различных целей, известных специалисту в данной области техники. Примеры таких целей включают, без ограничения, переливание крови, трансплантацию органов, хранение биологического образца и биологические методы анализа.
ПРИМЕРЫ
В примерах 1-7 1H-ЯМР-спектры записывали на 500 МГц с использованием прибора Bruker AMX 500. Масс-спектрометрию образцов и их анализ проводили на масс-спектрометре MicroMass ZQ или Quattro II в режиме измерения МС с ионизацией электрораспылением. Образцы вводили в масс-спектрометр при помощи проточного инжектора (FIA) или хроматографии. Подвижная фаза для проведения масс-спектрометрического анализа всех проб состояла из смесей ацетонитрил/вода с добавлением 0,2% муравьиной кислоты в качестве модификатора. Используемый в этом документе термин «Rt» относится ко времени удерживания при проведении ВЭЖХ-анализа (в минутах) для каждого соединения.
Пример 1
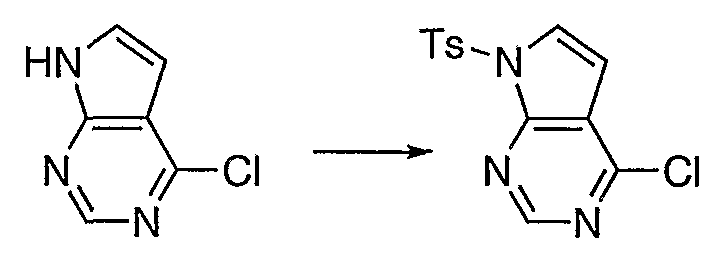
4-Хлор-7-тозил-7H-пирроло[2,3-d]пиримидин
Взвесь 1 (307 мг, 2,00 ммоль), тозилхлорида (418 мг, 2,20 ммоль) и свежеизмельченного K2CO3 (1,1 г, 8,0 ммоль) в DMF (5,0 мл) перемешивали при комнатной температуре в течение 2 час. Смесь распределяли между водой и EtOAc, органическую фазу промывали насыщенным солевым раствором (2×), сушили (Na2SO4), фильтровали и концентрировали с получением указанного в заголовке соединения (583 мг, 1,89 ммоль, выход 95%) в виде белого твердого вещества.

4-Циклопентенил-7-тозил-7H-пирроло[2,3-d]пиримидин
Смесь 4-хлор-7-тозил-7H-пирроло[2,3-d]пиримидина (62 мг, 0,20 ммоль), циклопентенбороновой кислоты (27 мг, 0,24 ммоль), KOAc (78 мг, 0,80 ммоль) и Pd(PPh3)4 (11 мг, 0,010 ммоль) в диоксане (0,6 мл) нагревали до 150°C (MW, 600 с) в герметично закрытой пробирке. Реакционную смесь подвергали флэш-хроматографии (SiO2, градиент 0-50% EtOAc/гексаны) с получением указанного в заголовке соединения (55 мг, 0,16 ммоль, выход 81%) в виде белого твердого вещества.
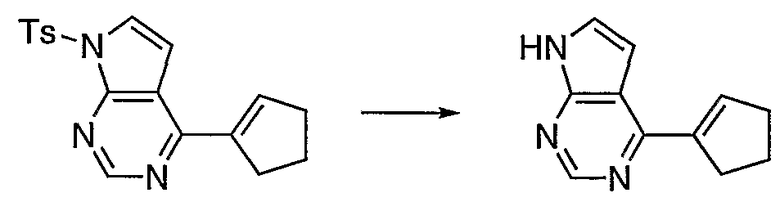
4-Циклопентенил-7H-пирроло[2,3-d]пиримидин (соединение 1)
Смесь 4-циклопентенил-7-тозил-7H-пирроло[2,3-d]пиримидина (55 мг, 0,16 ммоль) в метаноле (0,5 мл) обрабатывали NaOMe (0,5н, 0,25 мл) и нагревали до 60°C в течение 25 мин. Реакционную смесь разбавляли, гасили TFA (трифторуксусная кислота), концентрировали и подвергали флэш-хроматографии с получением указанного в заголовке соединения (19 мг) в виде белого твердого вещества.
ЖХ-МС время удерживания = 1,57 мин, (M+H+) 186,00
1H ЯМР (500 МГц, CDCl3) 9,30 (ушир.с, 1H), 8,86 (с, 1H), 7,33 (дд, 1H), 6,98 (дд, 1H), 6,79 (дд, 1H), 3,06 (м, 2H), 2,70 (м, 2H), 2,13 (кв, 2H)
Пример 2
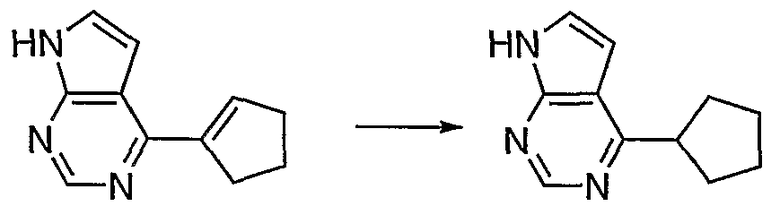
4-Циклопентил-7H-пирроло[2,3-d]пиримидин (соединение 3)
Смесь 4-циклопентенил-7H-пирроло[2,3-d]пиримидин (11 мг, 0,060 ммоль) и Pd-C (10% на угле, 22 мг) в EtOAc (1 мл) перемешивали в атмосфере H2 (баллон) в течение 5 час. Смесь фильтровали и концентрировали с получением указанного в заголовке соединения (10 мг) в виде белого твердого вещества.
ЖХ-МС время удерживания = 1,37 мин, (M+H+) 188,10
1H ЯМР (500 МГц, CDCl3) 9,00 (ушир.с, 1H), 8,80 (с, 1H), 7,24 (частично перекрытый дд, 1H), 6,63 (дд, 1H), 3,56 (кв, 2H), 2,13 (м, 2H), 2,05 (м, 2H), 1,92 (м, 2H), 1,75 (м, 2H)
Соединения примеров 3-7 получали в соответствии со схемой II.
Пример 3

4-(1-Фенилвинил)-7H-пирроло[2,3-d]пиримидин (соединение 8)
ЖХ-МС Время удерживания = 2 мин, (M+H+) 221
1H ЯМР: 500 МГц; ДМСО-d6: 12,6 (ушир.м, 1Н), 8,85 (с, 1Н), 7,53 (м, 1Н), 7,4 (м, 5H), 6,03 (м, 3H)
Пример 4
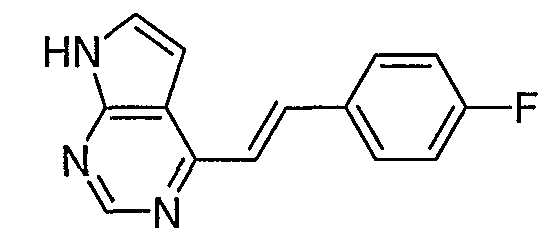
4-(4-Фторстирил)-7H-пирроло[2,3-d]пиримидин (соединение 5)
ЖХ-МС время удерживания = 2 мин, (M+H+) 239
1H ЯМР: 500 МГц; ДМСО-d6: 13,8 (ушир.м, 1Н), 8,93 (с, 1Н), 8,14 (д, 1Н), 7,92 (дд, 2H), 7,83 (м, 1Н), 7,71 (д, 1Н), 7,35 (дд, 2H), 7,27 (м, 1Н)
Пример 5

4-(4-хлорстирил)-7H-пирроло[2,3-d]пиримидин (соединение 6)
ЖХ-МС время удерживания = 2,3 мин, (M+H+) 255
1H ЯМР: 500 МГц; ДМСО-d6: 12,7 (ушир.м, 1Н), 8,90 (с, 1Н), 8,10 (д, 1Н), 7,90 (д, 2H), 7,79 (м, 2H), 7,54 (д, 2H), 7,22 (м, 1Н)
Пример 6

4-(4-(Трифторметил)стирил)-7H-пирроло[2,3-d]пиримидин (соединение 7)
ЖХ-МС Время удерживания = 2,7 мин, (M+H^) 289
1H ЯМР: 500 МГц; ДМСО-d6: 12,5 (ушир.м, 1Н), 8,88 (с, 1Н), 8,15 (д, 1Н), 8,07 (д, 2H), 7,90 (д, 1Н), 7,85 (д, 2H), 7,75 (м, 1Н), 7,45 (м, 1Н), 7,17 (м, 1Н)
Пример 7

4-Стирил-7H-пирроло[2,3-d]пиримидин (соединение 4)
ЖХ-МС время удерживания = 2 мин, (M+H+) 221
1H ЯМР: 500 МГц; ДМСО-d6: 12,8 (ушир.м, 1Н), 8,93 (с, 1Н), 8,14 (д, 2H), 7,85 (д, 2H), 7,83 (м, 1Н), 7,75 (д, 1Н), 7,51 (д, 2H), 7,47 (м, 1Н), 7,28 (м, 1Н)
Пример 8
Схема III

Стадия 1: Соединение A (1-(трет-бутоксикарбонил)-3-пиперидинкарбоновую кислоту) (4,60 г, 20,0 ммоль) суспендировали в 40 мл CH2Cl2. Добавляли EDCI (4,60 г, 24,0 ммоль), затем N,O-диметиламин (HCl) (2,34 г, 24,0 ммоль) и каталитическое количество DMAP. Полученную смесь оставляли перемешиваться при комнатной температуре в течение ночи. Все летучие вещества удаляли при пониженном давлении. Остаток растворяли в насыщенном водном растворе NaHCO3 и EtOAc. Слои разделяли и органический слой промывали насыщенным солевым раствором, сушили над MgSO4, фильтровали и упаривали досуха. Материал использовали, как есть, без дополнительной очистки. Выход: 4,7 г, приблизительно 86%.
1H ЯМР (500 МГц, CDCl3) 3,73 (с, 3H), 3,18 (с, 3H), 2,87-2,81 (м, 4H), 1,94 (с, H), 1,73-1,65 (м, 4H), 1,49-1,46 (м,9H).
Стадия 2: К раствору соединения B (4,7 г, 17,2 ммоль) в 70 мл THF при 0°C (в атмосфере N2) добавляли 3,0 M (11,5 мл, 34,5 ммоль) раствора метилмагнийбромида в THF. После завершения добавления охлаждающую баню удаляли, полученной смеси позволяли достичь комнатной температуры и оставляли ее перемешиваться в течение ночи. Полученную смесь гасили насыщенным водным раствором KHSO4 и разбавляли EtOAc. Органическую фазу промывали насыщенным солевым раствором, сушили над MgSO4, фильтровали и упаривали досуха. Неочищенный остаток пропускали через слой силигагеля и элюировали 5-20% EtOAc/гексаном. Выход: 2,37 г, приблизительно 60%.
1H ЯМР (500 МГц, CDCl3) 4,10 (д, J=12,0 Гц, H), 3,92 (с, H), 2,94 (дд, J=10,3, 13,3 Гц, H), 2,82-2,77 (м, H), 2,52-2,48 (м, H), 2,18 (с, 3H), 1,98 (дд, J=3,6, 12,9 Гц, H), 1,73 -1,69 (м, H), 1,56-1,44 (м, 11H).
Стадия 3: Соединение C (2,37 г, 10,4 ммоль) растворяли в 5,0 мл THF и добавляли (в атмосфере N2) к раствору LiHMDS (13,0 мл, 13,0 ммоль) при -78°C (баня с IPA/сухим льдом). Через 30 мин добавляли 2-[N,N-бис(трифторметилсульфонил)амино]пиридин (4,11 г, 11,5 ммоль), и через 10 мин удаляли охлаждающую баню. Полученной смеси позволяли постепенно достичь комнатной температуры и оставляли ее перемешиваться в течение ночи. Полученную смесь гасили насыщенным водным раствором KHSO4 и разбавляли EtOAc. Слои разделяли, органический слой промывали насыщенным солевым раствором, сушили над MgSO4, фильтровали и упаривали досуха. Неочищенный остаток пропускали через слой силигагеля и элюировали 10% EtOAc/гексаном. Выход: 2,93 г, приблизительно 79%.
1H ЯМР (500 МГц, CDCl3) 5,19 (д, J=4,1 Гц, H), 5,01 (дд, J=1,0, 4,1 Гц, H), 4,14-4,11 (м, H), 2,84 (дд, J=9,7, 13,2 Гц, 3H), 2,41 (с, H), 2,04-2,00 (м, H), 1,72 (т, J=3,4 Гц, H), 1,52-1,46 (м, 11H).
Стадия 4: Соединение D (2,93 г, 8,2 ммоль) растворяли в 30 мл толуола. Добавляли бис(пинаколято)диборон (2,07 г, 8,2 ммоль), а затем трифенилфосфин (117,3 мг, 0,44 ммоль) и феноксид калия (1,48 г, 11,2 ммоль). Реакционную смесь дегазировали Ar в течение 5 мин. Добавляли транс-дихлорбис(трифенилфосфин)палладий (II) (157,0 мг, 0,22 ммоль) и оставляли полученную смесь перемешиваться при 55°C в течение 3 часов. Полученной смеси позволяли охладиться до комнатной температуры и оставляли ее перемешиваться в течение ночи. Полученную смесь разбавляли насыщенным водным раствором NaHCO3 и EtOAc. Слои разделяли, органический слой промывали насыщенным солевым раствором, сушили над MgSO4, фильтровали и упаривали досуха. Неочищенный остаток пропускали через слой силигагеля и элюировали 5-15% EtOAc/гексаном. По-прежнему отмечалось содержание фенола, поэтому материал растворяли в Et2O и промывали 1н. раствором NaOH. Органическую фазу сушили над MgSO4, фильтровали и упаривали досуха. Выход: 2,01 г, приблизительно 73%.
1H ЯМР (500 МГц, CDCl3) 5,83 (д, J=2,6 Гц, H), 5,65 (с, H), 4,07 (дд, J=1,6, 12,8 Гц, 2H), 2,64-2,58 (м, 2H), 2,26 (т, J=11,2 Гц, H), 1,82-1,79 (м, H), 1,67-1,64 (м, H), 1,50 (т, J=3,7 Гц, 11H), 1,29-1,19 (м, 12H).
Стадия 5: Соединение E (45,7 мг, 0,14 ммоль) растворяли в 1,0 мл DME. Добавляли 4-хлор-7H-пирроло[2,3-d]пиримидин (20,8 мг, 0,14 ммоль), а затем 2,0M раствор Na2CO3 (200 мкл, 0,4 ммоль). Полученную смесь дегазировали Ar в течение 5 мин и добавляли каталитическое количество тетракис(трифенилфосфин)палладия(0). Полученную смесь нагревали до 160°C путем микроволновой обработки. Через 10 мин полученную смесь охлаждали до комнатной температуры. Полученную смесь разбавляли H2O и EtOAc. Слои разделяли, органический слой промывали насыщенным солевым раствором, сушили над MgSO4, фильтровали и упаривали досуха. Неочищенный остаток подвергали хроматографии на слое силикагеля и элюировали 10-30% EtOAc/гексаном. Выход: 7,1 мг соединения 22.
Пример 9
Схема IV
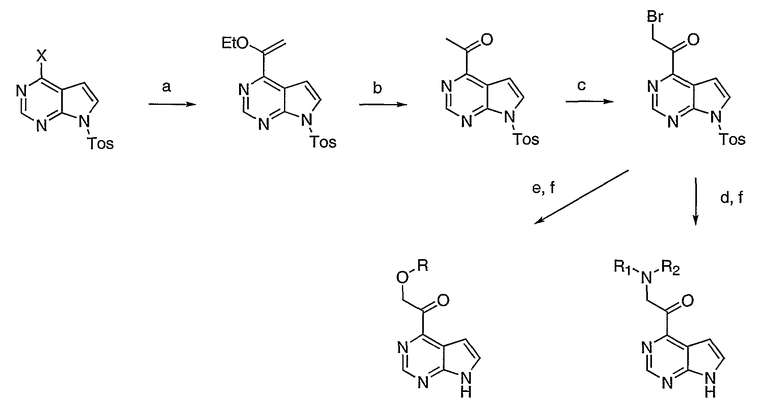
Условия: (a) три-н-бутил(1-этоксивинил)олово, Pd(PPh3)2Cl2, толуол, 90°C; (b) 6н HCl, MeOH, THF; (c) HBr, HOAc; (d) HNR1R2, Et3N; (e) NaOR или HOR, Et3N; (f) LiOH или NaOMe

4-Йод-7-(толуол-4-сульфонил)-7H-пирроло[2,3-d]пиримидин: К 100 мл холодной 47% стабилизированной йодистоводородной кислоты при перемешивании при 0°C малыми порциями добавляли 4-хлор-7-(толуол-4-сульфонил)-7H-пирроло[2,3-d]пиримидин (5 г, 16,2 ммоль; описанный в примере 1) и перемешивали в течение 1 час; затем температуре позволяли достичь температуры окружающей среды и дополнительно перемешивали в течение 5 час. Реакционную смесь разбавляли водой, твердое вещество выделяли путем фильтрования с отсасыванием и дополнительно промывали твердое вещество водой. Неочищенное твердое вещество растворяли в дихлорметане, дважды промывали насыщенным раствором гидрокарбоната натрия, промывали насыщенным солевым раствором, сушили (Na2SO4), удаляли растворитель при пониженном давлении и растирали со смесью гексанов/MTBE (2/1) с получением 5,7 г белого вещества (88%).
1Н-ЯМР: 500 МГц, в CDCl3 δ 8,61 (с, 1Н), 8,06 (д, 2Н, J=8,5 Гц), 7,75 (д, 1Н, J=4,1 Гц), 7,32 (д, 2Н, J=8,5 Гц), 6,45 (д, 1Н, J=4,1 Гц), 2,4 (с, 3Н).

Стадия a: 4-(1-Этоксивинил)-7-(толуол-4-сульфонил)-7H-пирроло[2,3-d]пиримидин: 4-Йод-7-(толуол-4-сульфонил)-7H-пирроло[2,3-d]пиримидин (10 г, 25 ммоль; описанный выше) растворяли/суспендировали в 200 мл безводного толуола вместе с дихлоридом бис(трифенилфосфин)палладия(II) [2,0 г, 2,85 ммоль]. Смесь продували газообразным азотом в течение ~5 мин, после чего смесь нагревали до 90°C на масляной бане в атмосфере газообразного азота. Медленно по каплям в течение 2 час добавляли три-н-бутил(1-этоксивинил)олово [12,66 мл, 13,54 г, 37,5 ммоль] в 100 мл безводного толуола. После завершения добавления смесь дополнительно нагревали в течение 6 час в атмосфере азота. Реакционную смесь охлаждали до температуры окружающей среды и удаляли растворитель при пониженном давлении до тех пор, пока оставшийся объем не составлял 1/5 от начального объема. К этой взвеси добавляли 160 мл петролейного эфира, смесь перемешивали в течение 1 час, твердое вещество выделяли путем фильтрования с отсасыванием и промывали петролейным эфиром. Влажное твердое вещество суспендировали в ацетонитриле, перемешивали в течение 1 час, твердое вещество повторно выделяли путем фильтрования с отсасыванием и сушили на воздухе. Полученное бледно-желтое твердое вещество (7,2 г, что соответствует выходу 82%) использовали без дополнительной очистки.
1H ЯМР: 500 МГц в CDCl3 δ 8,9 (с, 1Н), 8,07 (д, 2H, J=8,5 Гц), 7,7 (д, 1H, J=4,1 Гц), 7,28 (д, 2H, J=8,5 Гц), 7,04 (д, 1Н, J=4,1 Гц), 5,7 (д, 1Н, J=2 Гц), 4,58 (д, 1Н, J=2 Гц), 4,0 (кварт., 2H), 2,4 (с, 3H), 1,5 (т, 3H).
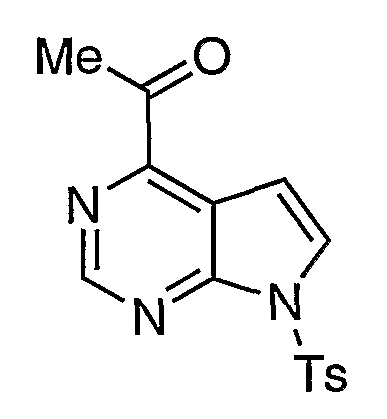
Стадия b: 1-[7-(Толуол-4-сульфонил)-7H-пирроло[2,3-d]пиримидин-4-ил]этанон: 4-(1-Этоксивинил)-7-(толуол-4-сульфонил)-7H-пирроло[2,3-d]пиримидин [7,25 г, 21,12 ммоль] растворяли в метаноле и THF (по 50 мл каждого) и перемешивали с 10 мл 6н HCl в течение 4,0 час при температуре окружающей среды. Растворители удаляли при пониженном давлении и распределяли остаток между дихлорметаном и насыщенным раствором гидрокарбоната натрия. Органическую фракцию промывали насыщенным солевым раствором, сушили над безводным сульфатом натрия и удаляли растворитель при пониженном давлении. Неочищенный материал растирали со смесью MTBE и петролейного эфира (1/4) в течение нескольких часов, твердое вещество окончательно выделяли путем фильтрования с отсасыванием и сушили на воздухе. Бледно-желтое вещество (5,95 г, что соответствует выходу 89%) использовали без дополнительной очистки.
1H ЯМР: 500 МГц CDCl3 δ 9,0 (с, 1Н), 8,08 (д, 2H, J=8,4 Гц), 7,87 (д, 1H, J=4,1 Гц), 7,3 (м, 3H), 2,8 (с, 3H), 2,4 (с, 3H).

Стадия c: 2-Бром-1-[7-(толуол-4-сульфонил)-7H-пирроло[2,3-d]пиримидин-4-ил]этанон: 1-[7-(Толуол-4-сульфонил)-7H-пирроло[2,3-d]пиримидин-4-ил]этанон [5,95 г, 18,88 ммоль] растворяли/суспендировали в 90 мл ледяной уксусной кислоты и 30% бромоводороде [7,53 мл, 10,197 г, 37,76 ммоль] в уксусной кислоте. К этой смеси при перемешивании при температуре окружающей среды в течение 1,0 час добавляли бром [0,970 мл, 3,02 г, 18,88 ммоль] в 10 мл ледяной уксусной кислоты. Реакционную смесь дополнительно перемешивали в течение 4,0 час при температуре окружающей среды, в процессе чего образовывался желтый осадок. Растворитель удаляли при пониженном давлении и распределяли остаток между дихлорметаном и насыщенным раствором гидрокарбоната натрия. Органическую фазу промывали водой, насыщенным солевым раствором, сушили над безводным сульфатом натрия и удаляли растворитель при пониженном давлении. Неочищенное твердое вещество растирали/перемешивали с MTBE в течение ночи, твердое вещество выделяли путем фильтрования с отсасыванием и сушили на воздухе с получением 4,2 г бледно-желтого твердого веществ, (выход 56,6%).
1Н ЯМР: 500 МГц в CDCl3 δ 9,1 (с, 1Н), 8,09 (д, 2H, J=8,5 Гц), 7,93 (д, 1Н, J=4,0 Гц), 7,33 (д, 2H, J=8,5 Гц), 7,29 (д, 1Н, J=4,0 Гц), 4,83 (с, 2H), 2,4 (с, 3H).
Стадии d, e: Преобразование бромида может быть осуществлено путем нуклеофильного замещения первичными или вторичными аминами (т.е. стадия d) или путем обработки спиртом (т.е. стадия e) в щелочных условиях.
Стадия f: С соединения снимают защитные группы, как описано для соединения 1.
Пример 10
Схема V

Условия: (a) Алкилцинкгалогенид, THF, от комнатной температуры до 100°C; (b) LiOH/THF или NaOMe/MeOH

Условия: (a) Алкилцинкгалогенид, THF, от комнатной температуры до 80°C; (b) NaOMe/MeOH
Стадии a, b: 4-Бицикло[2.2.1]гепт-2-ил-7H-пирроло[2,3-d]пиримидин: К раствору N-тозил-4-хлордеазапурина (40 мг, 0,13 ммоль) в безводном THF (0,5 мл) добавляли соответствующий алкилцинкгалогенид (например, экзо-2-норборнилцинкбромид [0,40 мл, 0,5M]) и перемешивали смесь в течение ночи при комнатной температуре. Затем смесь дополнительно нагревали до 80°C в течение 1,5 час и охлаждали до комнатной температуры. Реакционную смесь обрабатывали NaOMe (200 мкл, 0,5M) в MeOH при 50°C в течение 1,5 ч перед исследованием. Добавляли виннокислый калий-натрий и несколько раз экстрагировали смесь EtOAc. Органический слой фильтровали и концентрировали. Неочищенный остаток очищали по методу ВЭЖХ с получением соединения 26.
ЖХ-МС время удерживания = 1,86 мин, (M+H) = 214,2
1Н ЯМР (ДМСО) 12,42 (м, 2H), 8,78 (с, 1H), 8,74 (с, 1H), 7,62 (ушир.с, 2H), 6,82 (с, 1H), 6,77 (с, 1H), 3,76 (м, 1H), 3,31 (с, 1H), 2,75 (м, 1H), 2,46 (м, 1H), 2,37 (м, 2H), 2,14 (м, 2H), 1,90 (м, 1H), 1,72 (м, 1H), 1,67 (д, 2H), 1,59 (м, 2H), 1,55-1,42 (комплекс м, 3H), 1,33 (м, 2H), 1,23 (м, 1H), 1,17 (д, 1H), 0,99 (м, 1H).
Соединения 23, 24, 25, 27, 28, 29, 30 и 31 получали описанным выше способом.
В представленной ниже таблице 4 показаны примеры результатов 1H-ЯМР-спектроскопии (NMR) и жидкостной хроматографии/масс-спектрометрии, представленные в виде массы с протоном (M+H), определенной по методу электрораспыления, и времени удерживания (RT) для определенных соединений по настоящему изобретению, где номера соединений в таблице 4 соответствуют соединениям, представленным в таблице 3 (пустые клетки означают, что тест не проводился).
Пример 11: Метод анализа ингибирования JAK3
Скрининг способности соединений ингибировать JAK проводили с использованием метода, описанного ниже. Реакции проводили в киназном буферном растворе, содержащем 100 мМ HEPES (pH 7,4), 1 мМ DTT, 10 мМ MgCl2, 25 мМ NaCl и 0,01% BSA.
Концентрации субстрата в процессе анализа составляли 5 мкМ ATP (200 мкКи/мкМ ATP) и 1 мкМ поли(Glu)4Tyr. Реакции проводили при 25°C и в присутствии 1 нМ JAK3.
В каждую лунку 96-луночного поликарбонатного микропланшета добавляли 1,5 мкл предполагаемого ингибитора JAK3 вместе с 50 мкл киназного буферного раствора, содержащего 2 мкМ поли(Glu)4Tyr и 10 мкМ ATP. Затем смесь перемешивали и добавляли 50 мкл киназного буферного раствора, содержащего 2 нМ фермента JAK3, для инициирования реакции. Через 20 мин реакции при комнатной температуре (25°C) реакцию останавливали добавлением 50 мкл 20% трихлоруксусной кислоты (TCA), также содержащей 0,4 мМ ATP. Затем полное содержимое каждой лунки переносили в 96-луночный микропланшет со стекловолоконным фильтром с использованием TomTek Cell Harvester. После промывки добавляли 60 мкл сцинтилляционной жидкости и определяли встраивание 33P на счетчике Perkin Elmer TopCount.
Пример 12: Метод анализа ингибирования JAK2
Анализ проводили, как описано в примере 11, за исключением того, что использовали фермент JAK-2, конечная концентрация поли(Glu)4Tyr составляла 15 мкМ и конечная концентрация ATP составляла 12 мкМ.
Пример 13: Методы анализа ингибирования ROCK
Скрининг способности соединений ингибировать активность ROCK I (AA 6-553) проводили с использованием стандартной сопряженной ферментной системы (Fox et al. Protein Sci. 7: 2249, 1998). Реакции проводили в растворах, содержащих 100 мМ HEPES (pH 7,5), 10 мМ MgCl2, 25 мМ NaCl, 2 мМ DTT и 1,5% ДМСО. Конечные концентрации субстрата в процессе анализа составляли 45 мкМ ATP (Sigma Chemicals, St. Louis, MO) и 200 мкМ пептида (American Peptide, Sunnyvale, CA). Реакции проводили при 30°C и в присутствии 45 нМ ROCK I. Конечные концентрации компонентов сопряженной ферментной системы составляли 2,5 мМ фосфоенолпирувата, 350 мкМ NADH, 30 мкг/мл пируваткиназы и 10 мкг/мл лактатдегидрогеназы.
Скрининг способности соединений ингибировать активность ROCK проводили с использованием стандартного радиоферментного анализа. Анализ проводили в растворах, содержащих 100 мМ HEPES (pH 7,5), 10 мМ MgCl2, 25 мМ NaCl, 2 мМ DTT и 1,5% ДМСО. Конечные концентрации субстрата в процессе анализа составляли 13 мкМ [γ-33P] ATP (25 мКи 33P ATP/ммоль ATP, Perkin Elmer, Cambridge, MA/Sigma Chemicals, St. Louis, MO) и 27 мкМ основного миелинового белка (MBP). Конечная концентрация субстрата в процессе анализа составляла 5 нМ ROCK. Анализ проводили при комнатной температуре. В 96-луночный микропланшет помещали 1,5 мкл маточного раствора в ДМСО, содержащего последовательные разведения соединения по настоящему изобретению (концентрации варьировали от 10 мкМ до 2,6 нм). В микропланшет добавляли 50 мкл раствора 1 (100 мМ HEPES (pH 7,5), 10 мМ MgCl2, 26 мМ [γ-33P] ATP). Реакцию инициировали добавлением 50 мкл раствора 2 (100 мМ HEPES (pH 7,5), 10 мМ MgCl2, 4 мМ DTT, 54 мМ MBP и 10 нМ ROCK). Через 2 час реакцию гасили добавлением 50 мкл 30% трихлоруксусной кислоты (TCA, Fisher), содержащей 9 мМ ATP. В микропланшет со стекловолоконным фильтром (Corning, Cat.  No. 3511) переносили 140 мкл гашеной реакционной смеси, а затем трижды промывали 5% TCA. Добавляли 50 мкл сцинтилляционной жидкости Optima Gold (Perkin Elmer) и проводили подсчет в микропланшете на счетчике Top Count (Perkin Elmer). Из полученных во всех измерительных точках данных вычитали средние фоновые значения и спрямляли полученные данные с применением программного обеспечения Prism с получением Ki (приблизительно).
No. 3511) переносили 140 мкл гашеной реакционной смеси, а затем трижды промывали 5% TCA. Добавляли 50 мкл сцинтилляционной жидкости Optima Gold (Perkin Elmer) и проводили подсчет в микропланшете на счетчике Top Count (Perkin Elmer). Из полученных во всех измерительных точках данных вычитали средние фоновые значения и спрямляли полученные данные с применением программного обеспечения Prism с получением Ki (приблизительно).
Пример 14: Метод анализа ингибирования PKA
Скрининг способности соединений ингибировать активность PKA проводили с использованием стандартной сопряженной ферментной системы (Fox et al., Protein Sci, 1998, 7, 2249). Анализ проводили в смеси 100 мМ HEPES (pH 7,5), 10 мМ MgCl2, 25 мМ NaCl, 1 мМ DTT и 3% ДМСО. Конечные концентрации субстрата в процессе анализа составляли 50 мкМ ATP (Sigma Chemicals) и 80 мкМ пептида (Kemptide, American Peptide, Sunnyvale, CA). Анализ проводили при 30°C и в присутствии 18 нМ PKA. Конечные концентрации компонент сопряженной ферментной системы составляли 2,5 мМ фосфоенолпирувата, 300 мкМ NADH, 30 мкг/мл пируваткиназы и 10 мкг/мл лактатдегидрогеназы.
Маточный буферный раствор для анализа приготавливали из всех перечисленных выше реактивов за исключением ATP и тестируемого соединения по настоящему изобретению. В 96-луночный микропланшет помещали 55 мкл маточного раствора, а затем добавляли 2 мкл маточного раствора в ДМСО, содержащего последовательные разведения тестируемого соединения по настоящему изобретению (обычно начиная с конечной концентрации 5 мкМ). Микропланшет предварительно инкубировали в течение 10 мин при 30°C и инициировали реакцию добавлением 5 мкл ATP (конечная концентрация 50 мкМ). Начальные скорости реакции определяли при помощи микропланшетного ридера Molecular Devices SpectraMax Plus в течение 15-минутных интервалов времени. Значения IC50 и Ki рассчитывали путем нелинейного регрессионного анализа с использованием пакета программного обеспечения Prism (версия 3.0a GraphPad Prism для Macintosh, GraphPad Software, San Diego California, USA).
В таблице 5 представлены данные ингибирования ферментов (Ki) для определенных примеров соединений. Номера соединений в таблице 5 соответствуют номерам соединений, представленных в таблице 3. В таблице 5 «A» означает значения Ki менее 0,5 мкМ, «B» означает значения Ki от 0,5 до 5,0 мкМ, и «C» означает значения Ki более 5,0 мкМ.
| название | год | авторы | номер документа |
|---|---|---|---|
| ТРИАЗОЛЫ, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗ | 2005 |
|
RU2393155C2 |
| ПИРРОЛОПИРИДИНЫ, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗЫ | 2006 |
|
RU2435769C2 |
| ПИРАЗОЛО[1,5-a]ПИРИМИДИНЫ, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗ | 2005 |
|
RU2417996C2 |
| АЗАИНДОЛЫ, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ JAK И ДРУГИХ ПРОТЕИНКИНАЗ | 2005 |
|
RU2403252C2 |
| БЕНЗИМИДАЗОЛЫ, ПРИМЕНИМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНКИНАЗ | 2006 |
|
RU2415853C2 |
| КОМПОЗИЦИИ, ПОЛЕЗНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПОТЕНЦИАЛЗАВИСИМЫХ НАТРИЕВЫХ КАНАЛОВ | 2007 |
|
RU2470012C2 |
| ПРОИЗВОДНЫЕ ПИРАЗИНА, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ ATR | 2009 |
|
RU2604066C2 |
| ДИАМИНОТРИАЗОЛЬНЫЕ СОЕДИНЕНИЯ, ПРИМЕНЯЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ ПРОТЕИНОВОЙ КИНАЗЫ | 2005 |
|
RU2443700C2 |
| СПОСОБ СИНТЕЗА ИНГИБИТОРОВ Е1-АКТИВИРУЮЩЕГО ФЕРМЕНТА | 2008 |
|
RU2553476C2 |
| ПРОИЗВОДНЫЕ 2-УРЕИДО-6-ГЕТЕРОАРИЛ-3Н-БЕНЗИМИДАЗОЛ-6-КАРБОНОВОЙ КИСЛОТЫ И РОДСТВЕННЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ ГИРАЗЫ И/ИЛИ ТОПОИЗОМЕРАЗЫ IV ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2003 |
|
RU2333208C2 |
Настоящее изобретение относится к новым пирролопиримидинам общей формулы (I) или их фармацевтически приемлемым солям, обладающим свойствами ингибиторов протеинкиназ семейства JANUS: JAK2, JAK3, протеинкиназы А (РКА), семейства серин/треонин протеинкиназы ROCK. Соединения могут найти применение для лечения таких заболеваний, как аллергия, астма, атопический дерматит и др. В структурной
формуле (I):
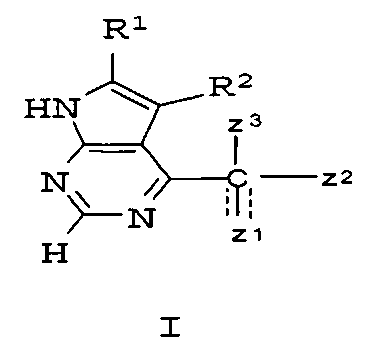
R1 представляет собой H; R2 представляет собой H; Z1 представляет собой С1-6алифатическую группу или С5-7циклоалифатическую группу, необязательно замещенные 0-1 группами JZ; если связь между Z1 и С является двойной, то Z1 может также представлять собой =O или =C(R)2; Z2 представляет собой Н; или С1-10алогеналкил, -(Vn)-CN, (Vn)-(гетероциклил), где гетероциклил представляет собой 6-членное кольцо, содержащее атом азота или два атома кислорода в качестве гетероатомов, -(Vn)-(фенил) или -(Vn)-(С3-10циклоалифатическая группа), необязательно замещенные 0-1 группами JZ; или Z1 и Z2 образуют вместе с атомом углерода, к которому они присоединены, кольцо Q; Z3 представляет собой Н или С1-6алкил, необязательно замещенный 0-1 группами JZ; или Z1, Z2 и Z3 образуют вместе с атомом углерода, к которому они присоединены, 6-8-членное насыщенное бициклическое кольцо Q; где если связь между Z1 и С является тройной, то Z2 и Z3 отсутствуют; если связь между Z1 и С является двойной или тройной, то Z3 отсутствует или Z2 и Z3 отсутствуют; Q представляет собой 3-8-членное насыщенное или частично насыщенное моноциклическое кольцо, содержащее 0-2 гетероатома, выбранных из азота, кислорода или серы, где упомянутое Q необязательно и независимо конденсировано с Q1; где упомянутое Q необязательно замещено 0-4 группами JQ. Значения других радикалов указаны в формуле изобретения. 9 н. и 26 з. п. ф-лы, 5 табл.
1. Соединение формулы (I):
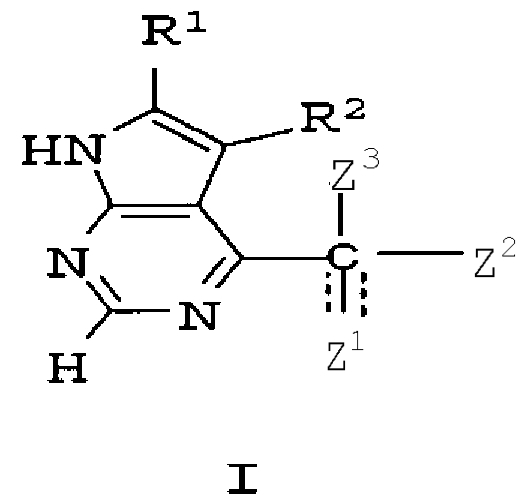
или его фармацевтически приемлемая соль, где
R1 представляет собой Н;
R2 представляет собой Н;
Z1 представляет собой С1-6алифатическую группу или
С5-7циклоалифатическую группу, необязательно замещенные 0-1 группами JZ; если связь между Z1 и С является двойной, то Z1 может также представлять собой =O или =C(R)2;
Z2 представляет собой Н; или С1-10галогеналкил, -(Vn)-CN, (Vn)-(гетероциклил), где гетероциклил представляет собой 6-членное кольцо, содержащее атом азота или два атома кислорода в качестве гетероатомов, -(Vn)-(фенил) или
-(Vn)-(С3-10циклоалифатическая группа), необязательно замещенные 0-1 группами JZ; или
Z1 и Z2 образуют вместе с атомом углерода, к которому они присоединены, кольцо Q;
Z3 представляет собой Н или С1-6алкил, необязательно замещенный 0-1 группами JZ;
или
Z1, Z2 и Z3 образуют вместе с атомом углерода, к которому они присоединены, 6-8-членное насыщенное бициклическое кольцо;
где если связь между Z1 и С является тройной, то Z2 и Z3 отсутствует;
если связь между Z1 и С является двойной или тройной, то Z3 отсутствует или Z2 и Z3 отсутствует;
Q представляет собой 3-8-членное насыщенное или частично насыщенное моноциклическое кольцо, содержащее 0-2 гетероатома, выбранных из азота, кислорода или серы, где упомянутое Q необязательно и независимо конденсировано с Q1; где упомянутое Q необязательно замещено 0-4 группами JQ;
Q1 представляет собой 5-6-членное насыщенное или частично насыщенное моноциклическое кольцо, содержащее 0-2 гетероатома, выбранных из азота, где упомянутая группа Q1 необязательно замещена 0-4 группами JQ,
R представляет собой Н;
каждый заместитель JQ и JZ на ненасыщенном атоме углерода независимо выбирают из водорода, C1-6галогеналкила, галогена, Y, -(Vn)-CN, -(Vn)-(С1-6алкил),
-(Vn)-(фенил); где каждый JQ и JZ необязательно замещен одной группой JR;
каждый заместитель JQ и JZ на атоме азота независимо выбирают из водорода, Y, -(Vn)-CN, -(Vn)-(С1-6алифатическая группа); где каждый JQ и JZ необязательно замещен 1 группой JR;
JR выбирают из ORb, L, -(Ln)-(С1-6алкил), -(Ln)-CN, -CO2Rb, -CORb;
L представляет собой С1-10алкил, в котором до трех метиленовых звеньев заменены -NRb-, -ОС(О)-, -С(О)-, -C(O)NRb- или -SO2-;
V представляет собой С1-10алифатическую группу;
Y представляет собой С1-10алифатическую группу, в которой до трех метиленовых звеньев заменены GY, где GY выбирают из -NR-, ОС (О)-, -С(О)-, -C(O)NR- или -SO2-;
Ra представляет собой водород или С1-6алифатическую группу, необязательно замещенную 0-3 группами JR;
Rb представляет собой водород или незамещенную C1-6алкильную группу;
n равно 0 или 1;
при условии, что
если R1 и R2 представляют собой Н, и Z2 и Z3 представляют собой Н, то Z1 не является метилом;
если R1 представляет собой СН3, и R2 представляет собой Н, то все Z1, Z2 и Z3 не являются Н;
если R1 и R2 представляют собой Н, и Z2 и Z3 представляют собой Н, то Z1 не является незамещенным фенилом, 4-пиридилом или одной из структур, представленных ниже:
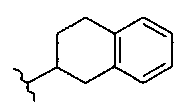


 или
или  ;
;
и
если R1 и R2 представляют собой Н, то Z1 и Z2 вместе не являются -С≡С-СН2СН2СООН.
2. Соединение по п.1, в котором Z1, Z2 и Z3 образуют вместе с атомом углерода, к которому они присоединены, бициклическое кольцо, представленное в формуле II:
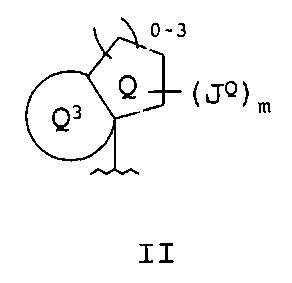
в которой Q3 представляет собой 3-4-членное насыщенное моноциклическое кольцо;
каждый Q и Q3 необязательно и независимо замещен 0-4 группами JQ.
3. Соединение по п.2, в котором Q3 представляет собой циклопропильную группу, и каждый из Q и Q3 необязательно замещен 0-2 группами JQ, как представлено на формуле III:

4. Соединение по любому из пп.2 или 3, в котором кольцо Q содержит два гетероатома.
5. Соединение по любому из пп.2 или 3, в котором кольцо Q содержит один гетероатом.
6. Соединение по любому из пп.2 или 3, в котором кольцо Q не содержит гетероатомов.
7. Соединение по п.4, в котором каждый из упомянутых гетероатомов независимо выбирают из азота или серы.
8. Соединение по п.4, в котором оба гетероатома представляют собой азот.
9. Соединение по п.5, в котором гетероатом представляет собой азот.
10. Соединение по п.6, в котором кольцо Q представляет собой 5-7-членную циклоалифатическую группу.
11. Соединение по п.1, в котором Q или Q-Q1 выбирают из

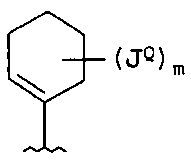

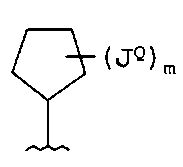

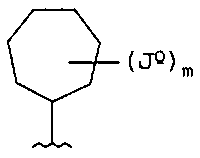



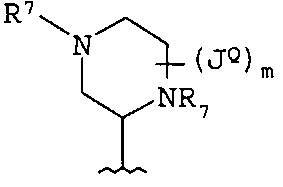


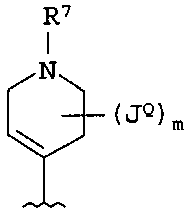


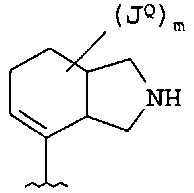




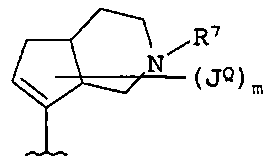


в которых каждый R7 и JQ независимо выбирают из водорода, Y, -(Vn)-CN, -(Vn)-(С1-6алкил), -(Vn)-(фенил);
для каждого Q и Q1 m независимо равно 0-3; и
каждый R7 и JQ необязательно и независимо замещен 1 группой JR.
12. Соединение по п.11, в котором m равно 0.
13. Соединение по п.11, в котором m равно 1 или 2.
14. Соединение формулы VII:
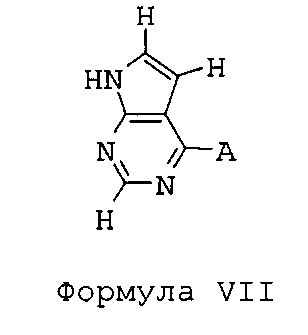
в которой А выбирают из
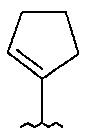






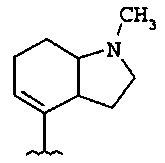




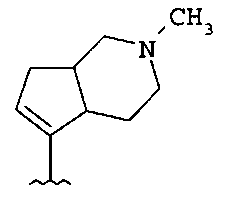
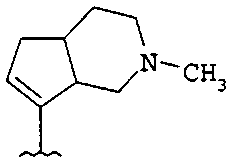


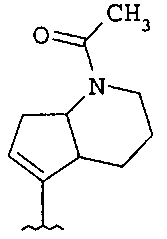

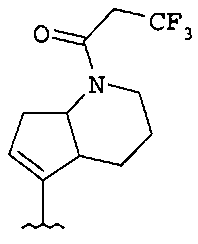


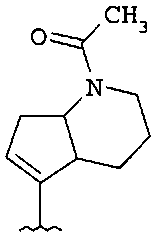





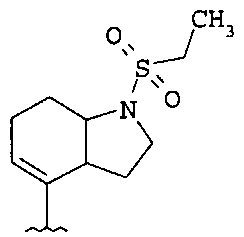







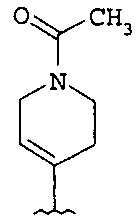



 или
или 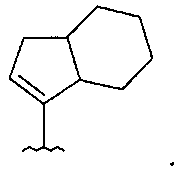
15. Соединение по п.1, в котором Z1 и Z2 не объединены с образованием кольца, и Z3 представляет собой Н или отсутствует.
16. Соединение по п.15, в котором Z1 представляет собой Н или С1-6алифатическую группу, необязательно замещенную 0-1 группами JZ.
17. Соединение по п.15, в котором Z1 представляет собой Н.
18. Соединение по п.15, в котором C≡Z1 представляет собой тройную связь, a Z2 и Z3 отсутствуют.
19. Соединение по п.15, в котором C=Z1 представляет собой двойную связь, и Z3 отсутствует.
20. Соединение по п.19, в котором Z1 представляет собой О.
21. Соединение по п.19, в котором Z1 представляет собой СН2.
22. Соединение по любому из пп.15-21, в котором Z2 представляет собой необязательно замещенный -(Vn)-(гетероциклил), где гетероциклил представляет собой 6-членное кольцо, содержащее атом азота или два атома кислорода в качестве гетероатомов, -(Vn)-(фенил) или -(Vn)-(С3-10циклоалифатическая группа); где n равно 0.
23. Соединение по п.22, в котором Z2 представляет собой необязательно замещенный 5-7-членный моноцикл, выбранный из циклоалифатической группы, 6-членный гетероциклил или фенил.
24. Соединение по п.23, в котором Z2 представляет собой необязательно замещенный 5-7-членный полностью или частично насыщенный моноцикл, выбранный из циклоалифатической группы, или 6-членный гетероциклил.
25. Соединение по п.23, в котором Z2 представляет собой необязательно замещенный 6-членный моноцикл с 0-1 атомами азота.
26. Соединение по п.23, в котором Z2 представляет собой пиперидин, необязательно замещенный 0-1 группой JZ.
27. Соединение по п.22, в котором Z2 представляет собой необязательно замещенную С3-10циклоалифатическую группу.
28. Соединение по п.27, в котором Z2 представляет собой бициклооктановое кольцо.
29. Соединение формулы VIII:

в которой А выбирают из

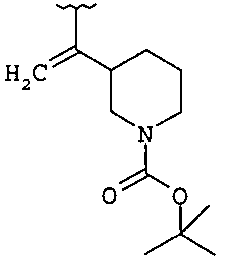

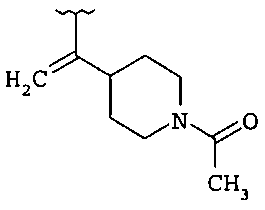





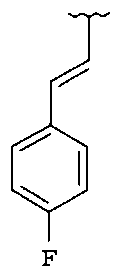

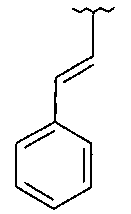
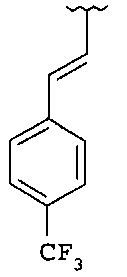



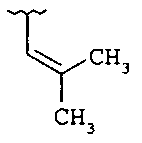 или
или

30. Соединение, выбранное из






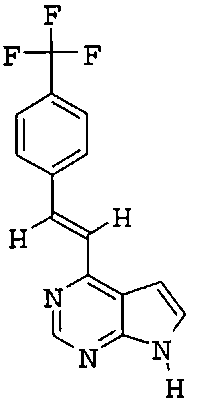

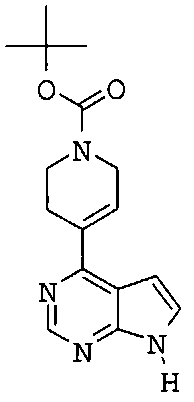

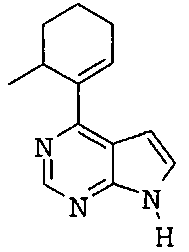

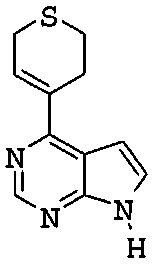



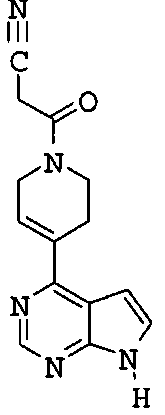



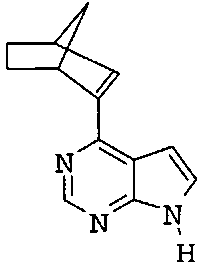

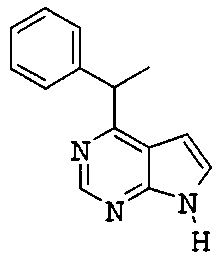
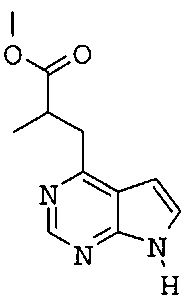





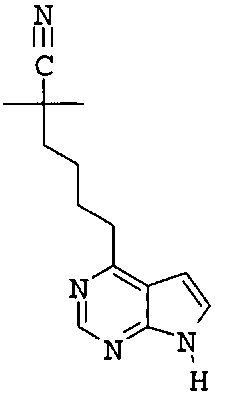

31. Фармацевтическая композиция, обладающая свойствами ингибитора семейства тирозинкиназ JANUS: JAK2, JAK3, протеинкиназы А (РКА), семейства серин/треонин протеинкиназы ROCK, содержащая эффективное количество соединения по п.1 или 31 и фармацевтически приемлемый носитель или адъювант.
32. Способ ингибирования активности киназы JAK3, включающий введение соединения по п.1 или композиции по п.31, содержащей упомянутое соединение.
33. Способ ингибирования активности киназы JAK2, включающий введение соединения по п.1 или композиции по п.31, содержащей упомянутое соединение.
34. Способ ингибирования активности киназы ROCK, включающий введение соединения по п.1 или композиции по п.31, содержащей упомянутое соединение.
35. Способ ингибирования активности киназы РКА, включающий введение соединения по п.1 или композиции по п.31, содержащей упомянутое соединение.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Online!: Chem Abstr., KHACHATRYAN et al | |||
| "Synthesis and mass spectra of some furo-, thieno-, and pyrrolo[2,3-d]pyrimidines", 1989:135185, CAS RN119707-35-6, abstracs | |||
| АЗОТСОДЕРЖАЩИЕ АРОМАТИЧЕСКИЕ ПРОИЗВОДНЫЕ, ИХ ПРИМЕНЕНИЕ, ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ИХ ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ | 2001 |
|
RU2264389C2 |
| СКОНДЕНСИРОВАННЫЕ С ГЕТЕРОЦИКЛИЧЕСКИМ КОЛЬЦОМ ПРОИЗВОДНЫЕ ПИРИМИДИНА | 1996 |
|
RU2136683C1 |
Авторы
Даты
2011-11-27—Публикация
2006-02-02—Подача