Изобретение относится к области химии, в частности к новым производным монометоксиполиэтиленгликоля, содержащим ароматическую диазогруппу, и может быть использовано при создании новых конъюгатов биологически активных соединений.
Монометоксиполиэтиленгликоль (далее - мПЭГ) представляет собой нейтральный полиэфир с различной молекулярной массой, который применяется для модификации разнообразных полипептидов [Никитин И.Г. Пегилированные препараты: современное состояние проблемы и перспективы / И.Г.Никитин, Г.И.Сторожаков // Вирусные гепатиты, достижения перспективы. - 2001. - №3(13). - С 3-8].
Сам мПЭГ непосредственно с полипептидами не взаимодействует, поэтому к его молекуле «прикрепляют» различные функциональные группы, которые позволяют полимеру связываться с белком [Kozlowski A. Development of Pegylated hiterferons for the Treatment of Chronic Hepatitis С / A.Kozlowski, S.A. Charles, J. M.Harris // BioDrugs - 2001. - №15 (7). P 419-429].
К таким производным мПЭГ относятся мПЭГ-альдегиды [US 5990237], мПЭГ-карбонаты [US 5324844], активированные эфиры [US 5932462] и другие. Как правило, данные пегилирующие агенты взаимодействуют со свободными аминогруппами полипептидов, в результате чего образуется смесь позиционных изомеров, число которых равно количеству свободных аминогрупп в протеине [Блохин Н.П. Особенности фармакологической динамики и кинетики пегилированного α-интерферона (40 kDa) «Пегасис»: новые возможности терапии хронического гепатита C /Н.П.Блохин, И.Г.Никитин // Материалы VII Российской конференции «Гепатология сегодня» РЖГГК, - 2002. - 6].
Поскольку позиционные изомеры протеинов имеют различную биологическую активность [Foser S. Isolation, structural characterization, and antiviral activity of positional isomers of monopegylated interferon alpha-2a (PEGASYS) / S.Foser, A.Schacher A, K.A.Weyer, D.Brugger, E.Dietel, S.Marti, T.Schreitmuller // Protein Expr Purif. - 2003 Jul; - 30 (1), - P.78-87], весьма актуальным становится расширение арсенала пегилирующих агентов, не затрагивающих аминогруппы полипептидов, что позволяет не только изменить места и способы прикрепления полимера к белку, а следовательно, получить новые конъюгаты, но и изменить количество и соотношение позиционных изомеров.
Наиболее близким аналогом изобретения по данной заявке являются пегилирующие агенты по патенту RU 2288212 (C07C 47/12, 2003), которые представляют собой альдегидные производные полиэтиленгликоля. Указанные пегилирующие агенты взаимодействуют с аминогруппами полипептидов.
Задачей данного изобретения является создание новых пегилирующих агентов, взаимодействующих с полипептидами преимущественно по аминокислотным остаткам тирозина и гистидина.
Целью изобретения являются пегилирующие агенты, содержащие ароматическую диазогруппу.
Указанная цель достигается использованием в качестве пегилирующих агентов предварительно диазотированных мПЭГ-эфиров или мПЭГ-амидов аминобензойных кислот с молекулярной массой от 20000 до 50000 Д и общей структурой:
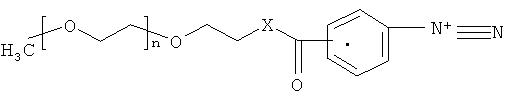 ,
,
где X - O или NH;
n - целое число в интервале от 455 до 1140.
Предложенные пегилирующие агенты взаимодействуют в слабощелочных средах преимущественно с тирозиновыми и гистидиновыми аминокислотными фрагментами полипептидов с образованием азогруппы. В результате образуется хромофор, поглощающий в видимой и ближней УФ-области электронного спектра и сообщающий окраску целевому конъюгату.
Пример 1. Диазотирование ароматической аминогруппы
Соответствующий мПЭГ-эфир или мПЭГ-амид аминобензойной кислоты с молекулярной массой от 20000 до 50000 Д растворяли при охлаждении в разбавленной HBr и приливали избыток раствора NaNO2. По завершении диазотирования, избыток нитрита удаляли мочевиной и полученный бесцветный раствор мПЭГ-диазония ex tempore использовали для модификации пептидов.
Характеристика мПЭГ-диазония
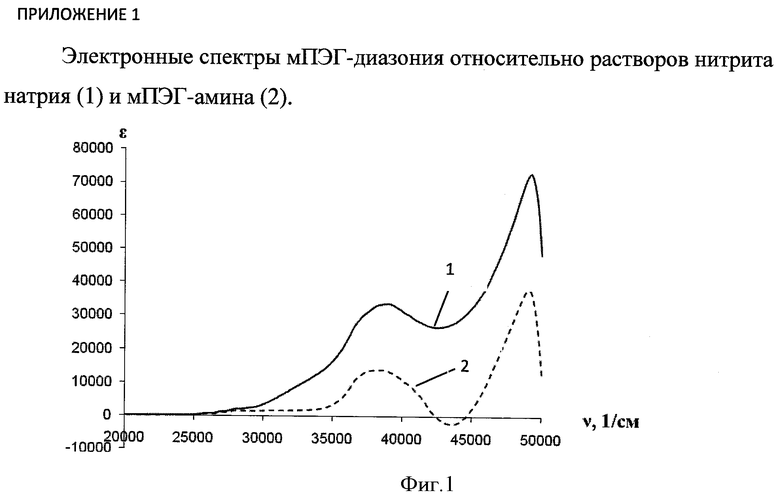
А) Электронные спектры мПЭГ-диазония в 0,1 М растворе HCl относительно растворов нитрита натрия (1) и недиазотированного ПЭГ-амина (2) в 0,1 М HCl приведены на фиг.1.
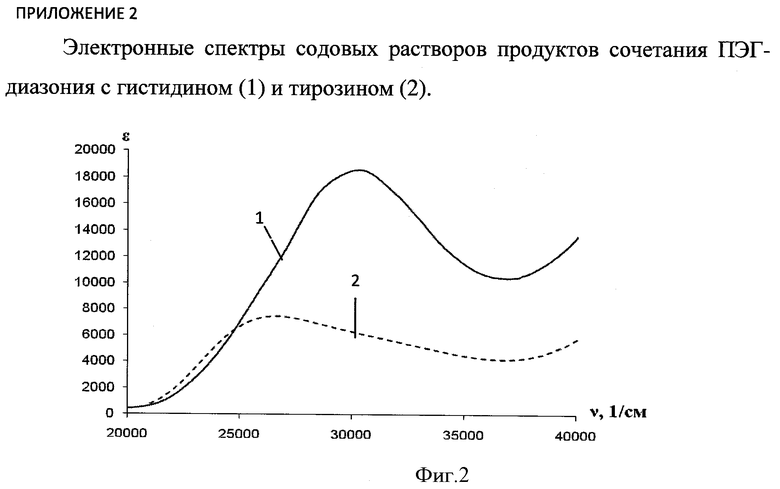
Б) мПЭГ-диазоний взаимодействует в щелочной среде с гистидином (желтое окрашивание) и тирозином (красное окрашивание, переходящее при подкислении в желто-оранжевое) с образованием окрашенных соединений. На фиг.2 приведены электронные спектры продуктов азосочетания мПЭГ-диазония с гистидином (1) и тирозином (2) в 0,1 М Na2CO3.
Таким образом, мПЭГ-диазоний взаимодействует с гистидином и тирозином с образованием окрашенных азосоединений.
Пример 2. Пегилирование полипептидов на примере интерферона α-2b.
К охлажденному раствору интерферона α-2b в боратном буфере приливали избыток пегилирующего агента. Процесс пегилирования контролируют обращенно-фазовой ВЭЖХ.
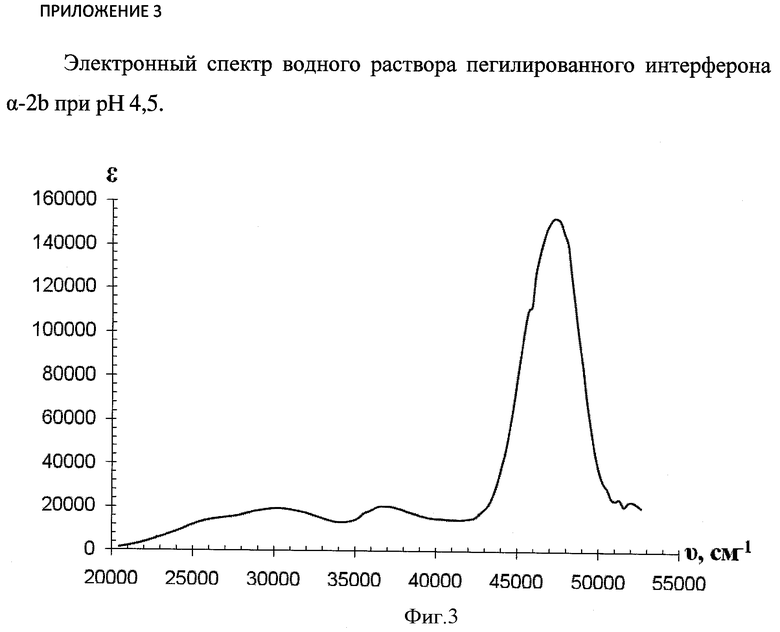
Пегилирование останавливали добавлением избытка тирозина, после чего немодифицированный интерферон и интерфероны с разной степенью пегилирования разделяли с помощью ионообменной или гель-фильтрационной хроматографии. Электронный спектр пегилированного интерферона приведен на фиг.3.
Из указанного спектра видно, что полученный конъюгат мПЭГ с интерфероном содержал:
- хромофор, образовавшийся в результате азосочетания мПЭГ-диазония с полипептидом и поглощавщий в видимой и ближней УФ-области электронного спектра (20000-34000 см-1);
- ароматические фрагменты (35000-40000 см-1), в том числе аминокислотные остатки триптофана, фенилаланина и тирозина, принадлежавщие белковой части конъюгата;
- полиэфирные и полипептидные связи, совместно поглощающие в области 45000-50000 см-1 и, соответственно, принадлежавщие полимерному и белковому фрагментам конъюгата.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭРИТРОПОЭТИН, КОНЪЮГИРОВАННЫЙ С ПОЛИЭТИЛЕНГЛИКОЛЕМ | 2010 |
|
RU2433134C1 |
| ИНТЕРФЕРОН, КОНЪЮГИРОВАННЫЙ С ПОЛИЭТИЛЕНГЛИКОЛЕМ | 2010 |
|
RU2433135C1 |
| СПОСОБ РЕГУЛИРОВАНИЯ УСЛОВИЙ ДЛЯ САЙТ-СПЕЦИФИЧЕСКОГО СВЯЗЫВАНИЯ ПОЛИПЕПТИДА И НЕПЕПТИДИЛЬНОГО ПОЛИМЕРА | 2010 |
|
RU2495881C2 |
| НОВЫЙ ФУНКЦИОНАЛЬНО АКТИВНЫЙ ВЫСОКООЧИЩЕННЫЙ СТАБИЛЬНЫЙ КОНЪЮГАТ ИНТЕРФЕРОНА α С ПОЛИЭТИЛЕНГЛИКОЛЕМ, ПРЕДСТАВЛЕННЫЙ ОДНИМ ПОЗИЦИОННЫМ ИЗОМЕРОМ ПЭГ-NH-ИФН, С УМЕНЬШЕННОЙ ИММУНОГЕННОСТЬЮ, С ПРОЛОНГИРОВАННЫМ БИОЛОГИЧЕСКИМ ДЕЙСТВИЕМ, ПРИГОДНЫЙ ДЛЯ МЕДИЦИНСКОГО ПРИМЕНЕНИЯ, И ИММУНОБИОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ | 2010 |
|
RU2447083C1 |
| КОВАЛЕНТНОЕ МОДИФИЦИРОВАНИЕ ПОЛИПЕПТИДОВ ПОЛИЭТИЛЕНГЛИКОЛЯМИ | 1992 |
|
RU2148586C1 |
| НОВЫЙ ФУНКЦИОНАЛЬНО АКТИВНЫЙ, ВЫСОКООЧИЩЕННЫЙ СТАБИЛЬНЫЙ КОНЪЮГАТ ГРАНУЛОЦИТАРНОГО КОЛОНИЕСТИМУЛИРУЮЩЕГО ФАКТОРА (Г-КСФ) С ПОЛИЭТИЛЕНГЛИКОЛЕМ С ПРОЛОНГИРОВАННЫМ БИОЛОГИЧЕСКИМ ДЕЙСТВИЕМ, ПРИГОДНЫЙ ДЛЯ МЕДИЦИНСКОГО ПРИМЕНЕНИЯ, И ИММУНОБИОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ | 2010 |
|
RU2446173C1 |
| ОЧИСТКА ПЕГИЛИРОВАННЫХ ПОЛИПЕПТИДОВ | 2008 |
|
RU2476439C2 |
| ХРОМАТОГРАФИЧЕСКИЕ СПОСОБЫ | 2008 |
|
RU2464066C2 |
| ПЕГИЛИРОВАННЫЙ КОНЪЮГАТ ВАРИАНТА РЕКОМБИНАНТНОГО КОНСЕНСУСНОГО ИНТЕРФЕРОНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ, И ПРИМЕНЕНИЕ | 2011 |
|
RU2575796C9 |
| КОНЪЮГАТЫ БЕЛКОВ СВЕРТЫВАНИЯ КРОВИ | 2010 |
|
RU2595442C2 |
Изобретение относится к пегилирующему агенту, содержащему ароматическую диазогруппу и имеющему следующую общую структуру:
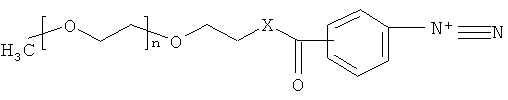 ,
,
где Х - О или NH; n - целое число в интервале от 455 до 1140. Технический результат: получен новый пегилирующий агент, который связывается с полипептидами посредством азогруппы, в результате чего образуется ковалентный конъюгат, поглощающий в видимой и ближней УФ-области электронного спектра. 3 ил.
Пегилирующие агенты, содержащие ароматическую диазогруппу, представляющие собой диазотированные метоксиполиэтиленгликолевые эфиры или амиды аминобензойных кислот с молекулярной массой от 20000 до 50000 Да и с общей формулой
 ,
,
где Х - О или NH;
n - целое число от 455 до 1140.
| ПРОИЗВОДНЫЕ АЛЬДЕГИДА ПОЛИЭТИЛЕНГЛИКОЛЯ | 2003 |
|
RU2288212C2 |
| US 5932462 A, 03.08.1999 | |||
| СПОСОБ ПОЛУЧЕНИЯ ДИАЗОСОЕДИНЕНИЙ ТРУДНОДИАЗОТИРУЕМЫХ АМИНОВBlJt:(JU!<33h'A'S'ПАти17ес-,.:;:^::":г:йзE'^S.':;-!0 /НА ' | 0 |
|
SU365355A1 |
| US 5324844 A, 28.01.1994. | |||
Авторы
Даты
2012-01-10—Публикация
2010-10-06—Подача