Область изобретения
Изобретение относится к фармацевтической композиции для инъекционного, особенно целенаправленного местного применения, дающего возможность внесения активного соединения непосредственно в место локализации опухоли.
Предпосылки создания изобретения
Комплексы платины широко известны как эффективные вещества, имеющие широкий спектр противоопухолевого действия и использующиеся таким образом, при лечении ряда опухолевых заболеваний. До настоящего времени в терапевтической практике используются только комплексы двухвалентной платины, главным образом цисплатин, карбоплатин или оксалиплатин. Однако комплексы двухвалентной платины являются нестабильными в желудочно-кишечном тракте, и/или они очень плохо всасываются. Это делает невозможным использование комплексов двухвалентной платины в пероральных дозированных формах, которые в других случаях являются наиболее благоприятными для пациента. Было найдено, что некоторые комплексы четырехвалентной платины не имеют этого недостатка и сохраняют свою противоопухолевую активность даже при пероральном введении. Эти комплексы четырехвалентной платины были описаны как новые химические соединения для перорального введения в ЕР 0328274, ЕР 0423707 и PCT/CZ 99/00015.
Однако комплексы четырехвалентной платины весьма ограничено растворимы в воде (около 0,03 г/100 мл) имеют низкую насыпную плотность (около 0,2 г/мл), низкую насыпную плотность после уплотнения постукиванием (около 0,4 г/мл) и высокий электростатический заряд. Упомянутые физические свойства представляют серьезную проблему при приготовлении твердой пероральной лекарственной формы. Кроме того, комплексы четырехвалентной платины являются химически нестабильными в контакте с металлами или со многими используемыми в настоящее время эксципиентами. Эти проблемы были с частичным успехом разрешены в PCT/CZ 99/00015, где описано приготовление твердых пероральных лекарственных форм конкретных комплексов четырехвалентной платины в форме комплексов включения циклодекстринов с указанными комплексами четырехвалентной платины. Согласно упомянутому патентному документу эти комплексы включения получают реакцией циклодекстринов с комплексами четырехвалентной платины в органическом растворителе и последующей лиофилизацией, и используют для перорального применения. Однако применяемое количество циклодекстрина заметно ограничивает содержание комплекса четырехвалентной платины, присутствующего в пероральной лекарственной форме, что является недостатком. Полученная таким образом пероральная лекарственная форма имеет относительно большой объем и ее трудно глотать, что делает невозможным пероральный прием дозированных единиц с более высокой дозой комплекса четырехвалентной платины.
Этот недостаток пероральных форм комплексов четырехвалентной платины может быть устранен предоставлением инъекционной формы с достаточным содержанием комплексов четырехвалентной платины. Из состояния данной области очевидно, что до настоящего времени задача приготовления такой инъекционной формы не была удовлетворительно решена. Поэтому задача настоящего изобретения - предоставить фармацевтическую композицию для инъекционного введения, которая могла бы содержать достаточное терапевтически эффективное количество комплексов четырехвалентной платины.
Раскрытие изобретения
В рамках работы над изобретением было неожиданно найдено, что определенные ниже комплексы четырехвалентной платины, содержащиеся в фармацевтической композиции согласно изобретению, могут быть использованы не только при системном, но также и при местном применении, что делает возможным введение комплекса четырехвалентной платины непосредственно в место локализации опухоли. Благодаря кумуляции комплекса четырехвалентной платины в месте локализации опухоли, могут быть использованы более низкие терапевтические дозы комплекса по сравнению с системно применяемыми дозами с таким же терапевтическим эффектом. Кроме того, комплекс четырехвалентной платины оказывается, таким образом, защищенным от длительной циркуляции в кровотоке и от химического и ферментативного разложения, происходящего при контакте с биологическими защитными системами, присутствующими в биологических жидкостях, в частности в пищеварительных соках и в крови, или при проходе через печень. В дополнение, использование фармацевтической композиции согласно изобретению делает возможным достижение длительного воздействия комплекса четырехвалентной платины.
Данное изобретение таким образом относится к фармацевтической композиции для инъекционного, в частности, целенаправленного местного применения, характеризующейся тем, что она включает стерильную суспензию платинового комплекса общей формулы I:
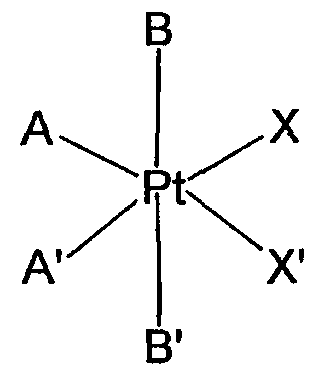
в которой:
A и A' независимо друг от друга представляют NH3-группу или амино- или диаминогруппу, имеющую от 1 до 18 атомов углерода;
B и B' независимо друг от друга представляют атом галогена или гидроксигруппу, или являются группами -O-C(O)-R или -O-C(O)-R', где R и R' независимо друг от друга представляют атом водорода, алкильную, алкенильную, арильную, аралкильную, алкиламино или алкоксигруппу, где указанные группы содержат от 1 до 10 атомов углерода, или функциональные производные этих групп;
X и X' независимо друг от друга представляют атом галогена или монокарбоксилатную группу, содержащую от 1 до 20 атомов углерода, или X и X' вместе образуют дикарбоксилатную группу, содержащую от 2 до 20 атомов углерода,
в фармацевтически приемлемой гидрофильной или гидрофобной инъекционной жидкой фазе, где 100% частиц платинового комплекса общей формулы I имеют размер меньше чем 250 мкм.
Предпочтительно 90% частиц платинового комплекса общей формулы I имеют размер меньше чем 40 мкм, предпочтительно меньше чем 10 мкм.
Предпочтительно, массовое отношение платинового комплекса общей формулы I к жидкой фазе составляет от 1:100 до 30:100, более предпочтительно от 5:100 до 10:100.
Предпочтительно, в качестве жидкой фазы фармацевтическая композиция содержит гидрофильную жидкую фазу, выбранную из группы, состоящей из воды, глицерина и пропиленгликоля.
Предпочтительно, жидкая фаза содержит по меньшей мере один стабилизатор, в частности пептизатор, и/или модификатор вязкости.
Предпочтительно, в качестве пептизатора жидкая фаза содержит полиспиртовое соединение, преимущественно выбранное из группы, состоящей из лактозы, фруктозы, маннита и сорбита.
Предпочтительно, массовое отношение полиспиртового соединения к платиновому комплексу общей формулы I составляет от 0,1:1 до 10:1.
Предпочтительно, в качестве модификатора вязкости жидкая фаза содержит гидрофильный полимер, преимущественно выбранный из группы, состоящей из поливинилпирролидона, поливинилацетата, гидроксипропилцеллюлозы и гидроксипропилметилцеллюлозы.
Предпочтительно, фармацевтическая композиция содержит от 0,1 до 10 мас.% по меньшей мере одного модификатора вязкости в расчете на общую массу композиции.
Предпочтительно, в качестве жидкой фазы фармацевтическая композиция содержит гидрофильную жидкую фазу, которая является водным буфером с рН от 4 до 8.
Предпочтительно, в качестве жидкой фазы фармацевтическая композиция содержит гидрофобную жидкую фазу, которая является олеофильной средой, выбранной, в частности, из группы, состоящей из масла для инъекций, оливкового масла и масла подсолнечника.
Изобретение также относится к вышеупомянутой фармацевтической композиции в качестве лекарства для лечения злокачественных опухолей.
В следующей части изобретение будет объяснено более подробно с использованием конкретных примеров осуществления, которые имеют только иллюстративное значение и никоим образом не ограничивают объем изобретения, который однозначно определен прилагаемой формулой изобретения.
В этих примерах в качестве конкретного представителя комплексов платины общей формулы I использован комплекс (ОС-6-43)-бис(ацетато)-(1-адамантиламино)аммин-дихлорплатины (IV) с кодовым названием LA-12 и формулы II:
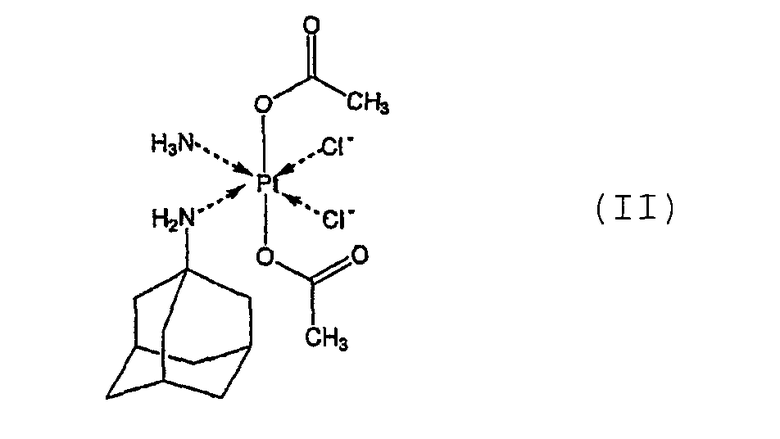
В примерах этот конкретный платиновый комплекс обозначен своим кодовым названием.
Примеры
Пример 1
Приготовление гидрофильной суспензионной инъекционной формы платинового комплекса LA-12
Маннит (5 мас. частей) и гидроксипропилметилцеллюлозу (1 мас. часть) растворяли в водном буфере с рН 4 (85 мас. частей), и раствор стерилизовали в автоклаве. В полученном таким образом стерилизованном растворе асептически суспендировали платиновый комплекс LA-12 (100% частиц меньше 250 мкм). Полученную суспензию заливали в стерильные флаконы.
Пример 2
Приготовление гидрофобной инъекционной формы платинового комплекса LA-12
Платиновый комплекс LA-12, 100% частиц которого имели размер меньше 250 мкм, (5 мас. частей) асептически суспендировали в масле для инъекций (95 мас. частей). Полученную суспензию асептически заливали в стерильные флаконы.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ | 2007 |
|
RU2430718C2 |
| КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ ПЛАТИНЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1999 |
|
RU2200164C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ВВЕДЕНИЯ ИНЪЕКЦИЕЙ | 2007 |
|
RU2443432C2 |
| КОМПЛЕКСЫ ПЛАТИНЫ (IV) С ПОВЫШЕННОЙ ПРОТИВОРАКОВОЙ ЭФФЕКТИВНОСТЬЮ | 2014 |
|
RU2666898C1 |
| НОВЫЕ КОМПЛЕКСЫ ПЛАТИНЫ IV С ПО СУЩЕСТВУ ПОВЫШЕННОЙ ПРОТИВООПУХОЛЕВОЙ ЭФФЕКТИВНОСТЬЮ | 2019 |
|
RU2802514C1 |
| КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ ПЛАТИНЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1999 |
|
RU2203901C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ КОМПЛЕКС ПЛАТИНЫ В КАЧЕСТВЕ АКТИВНОГО ВЕЩЕСТВА, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2004 |
|
RU2343913C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ИНГАЛЯЦИОННОГО ВВЕДЕНИЯ | 2010 |
|
RU2445119C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИС-ДИАММОНИЙДИХЛОРДИГИДРОКСОПЛАТИНЫ (IV) И ЕЕ ПРИМЕНЕНИЕ | 2004 |
|
RU2345086C2 |
| СУСПЕНЗИОННЫЕ КОМПОЗИЦИИ ВЫСОКОНЦЕНТРИРОВАННЫХ ДИСПЕРСИЙ | 2019 |
|
RU2804658C2 |
Изобретение относится к фармацевтической композиции для инъекционного целенаправленного местного применения, которая включает стерильную суспензию платинового комплекса (ОС-6-43)-бис(ацетато)-(1-адамантиламино)аммин-дихлорплатины (IV) (LA-12) в фармацевтически приемлемой гидрофильной или гидрофобной инъекционной жидкой фазе, при этом 100% частиц платинового комплекса размер менее 250 мкм. Изобретение обеспечивает получение стерильной пригодной для инъекционного использования суспензии платинового комплекса LA-12, которая содержит достаточное терапевтически эффективное количество комплекса. 12 з.п. ф-лы.
1. Фармацевтическая композиция для инъекционного в особенности целенаправленного местного применения, характеризующаяся тем, что она включает стерильную суспензию комплекса (ОС-6-43)-бис(ацетато)-(1-адамантиламино)аммин-дихлорплатины (IV) структурной формулы II:
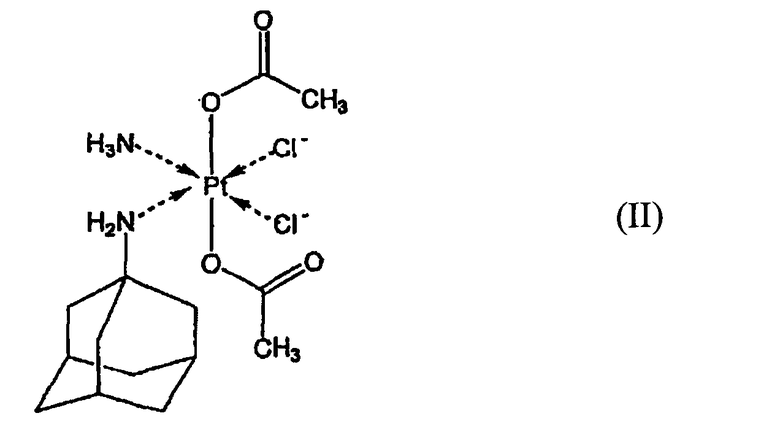
в фармацевтически приемлемой гидрофильной или гидрофобной инъекционной жидкой фазе, где 100% частиц платинового комплекса структурной формулы II имеют размер меньше чем 250 мкм.
2. Фармацевтическая композиция по п.1, характеризующаяся тем, что 90% частиц комплекса структурной формулы II имеют размер меньше чем 40 мкм, предпочтительно меньше чем 10 мкм.
3. Фармацевтическая композиция по п.1, характеризующаяся тем, что массовое отношение комплекса структурной формулы II к жидкой фазе составляет от 1:100 до 30:100.
4. Фармацевтическая композиция по п.3, характеризующаяся тем, что массовое отношение комплекса структурной формулы II к жидкой фазе составляет от 5:100 до 10:100.
5. Фармацевтическая композиция по п.1, характеризующаяся тем, что в качестве жидкой фазы она включает гидрофильную жидкую фазу, выбранную из группы, включающей воду, глицерин и пропиленгликоль.
6. Фармацевтическая композиция по п.1, характеризующаяся тем, что жидкая фаза включает по меньшей мере один стабилизатор, предпочтительно пептизатор, и/или модификатор вязкости.
7. Фармацевтическая композиция по п.6, характеризующаяся тем, что в качестве пептизатора жидкая фаза содержит полиспиртовое соединение, предпочтительно выбранное из группы, включающей лактозу, фруктозу, маннит и сорбит.
8. Фармацевтическая композиция по п.7, характеризующаяся тем, что массовое отношение полиспиртового соединения к платиновому комплексу структурной формулы II составляет от 0,1:1 до 10:1.
9. Фармацевтическая композиция по п.6, характеризующаяся тем, что в качестве модификатора вязкости жидкая фаза содержит гидрофильный полимер, предпочтительно выбранный из группы, включающей поливинилпирролидон, поливинилацетат, гидроксипропилцеллюлозу и гидроксипропилметилцеллюлозу.
10. Фармацевтическая композиция по п.9, отличающаяся тем, что она содержит от 0,1 до 10 мас.% по меньшей мере одного модификатора вязкости в расчете на общую массу композиции.
11. Фармацевтическая композиция по п.1, отличающаяся тем, что в качестве жидкой фазы она содержит гидрофильную жидкую фазу, состоящую из водного буфера с рН от 4 до 8.
12. Фармацевтическая композиция по п.1, отличающаяся тем, что в качестве жидкой фазы она содержит гидрофобную жидкую фазу, состоящую из олеофильной среды, предпочтительно выбранной из группы, состоящей из масла для инъекций, оливкового масла и масла подсолнечника.
13. Фармацевтическая композиция по любому из пп.1-12 в качестве лекарства для лечения злокачественных опухолей.
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ ПЛАТИНЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1999 |
|
RU2200164C2 |
Авторы
Даты
2012-01-20—Публикация
2007-06-20—Подача