УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Воспалительный процесс активирует нервную систему, вызывая боль при воспалении и нарушение моторной функции. Раздражение чувствительных нервов становится причиной расширения кровеносных сосудов и экстравазации плазмы, приводящих к нейрогенному воспалению и раздражению, вызывающему сенсорное возбуждение, гиперчувствительность и боль.
Нейрогенное воспаление вызывается активацией ноцицептивных и термочувствительных окончаний в тканях и может вызываться врожденными состояниями, такими как аутоиммунные заболевания, включающими в себя аллергию, вирусную инфекцию, а также и травмой. Нейрогенное воспаление при данных состояниях может влиять на соматосенсорную систему, которая состоит из различных сенсорных рецепторов, ответственных за ощущения, такие как давление, прикосновение, температура, боль, зуд, щекотка, покалывание и онемение. Активированные нервы могут бесконечно поддерживать хроническое воспаление, индуцируя выделение цитокинов, активируя моноциты и хемотаксис.
Белки, активные при нейрогенном воспалении, могут служить мишенями для терапевтических подходов в диагностике и лечении заболеваний.
Примером лекарственного средства, применяемого для лечения боли, является нейронтин (габапентин), который применяют для лечения диабетической периферийной невропатии, а также постгерпетической невралгии. Таким образом, существует потребность в дополнительном лекарственном препарате для лечения невропатической боли.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Следующие ниже определения предназначены для того, чтобы облегчить понимание описанных в настоящем описании изобретений.
Термин «антитело» или «пептид(ы) антитела» означает интактное антитело или его связывающий фрагмент, который конкурирует с интактным антителом за специфическое связывание и включает в себя химерные, гуманизированные, полностью человеческие и биспецифические антитела. В определенных вариантах осуществления связывающие фрагменты получены технологиями рекомбинантных ДНК. В дополнительных вариантах осуществления связывающие фрагменты получены ферментативным или химическим расщеплением интактных антител. Связывающие фрагменты включают в себя, в качестве неограничивающих примеров, Fab, Fab', F(ab').sub.2, Fv и одноцепочечные антитела.
Термин «выделенное антитело» означает антитело, которое идентифицировали и отделили и/или извлекли из компонента его естественного окружения. Загрязняющие компоненты его естественного окружения представляют собой вещества, которые могли бы помешать диагностическому или терапевтическому применению антитела и которые могут включать в себя ферменты, гормоны и другие белковые или небелковые растворы. В вариантах осуществления антитело будет очищено (1) до более 95% по массе антитела, как определено по способу Лоури, и включая более 99% по массе, (2) до степени, достаточной для получения по меньшей мере 15 остатков N-концевой или внутренней аминокислотной последовательности при помощи секвенатора с вращающимся стаканом, или (3) до однородности при SDS-PAGE в восстанавливающих и невосстанавливающих условиях, применяя окрашивание кумасси голубым или, предпочтительно, серебром. Выделенное антитело включает в себя антитело in situ в рекомбинантных клетках, поскольку не будет присутствовать по меньшей мере один компонент естественного окружения антитела. Как правило, тем не менее, выделенное антитело получают посредством по меньшей мере одной стадии очистки.
«Вариант» антитела против IL-31 означает в настоящем описании молекулу, которая отличается по аминокислотной последовательности от «исходной» аминокислотной последовательности антитела против IL-31 вследствие добавления, удаления и/или замены одного или более аминокислотных остатков в исходной последовательности антитела. При осуществлении вариант содержит одну или более аминокислотных замен в одном или более гипервариабельных участках исходного антитела. Например, вариант может содержать по меньшей мере одну, например, от приблизительно одной до приблизительно десяти и от приблизительно двух до приблизительно пяти замен в одном или более гипервариабельных участках исходного антитела. Как правило, вариант будет содержать аминокислотную последовательность, обладающую по меньшей мере 75% идентичности аминокислотной последовательности с последовательностями вариабельных доменов тяжелой или легкой цепи исходного антитела, более предпочтительно по меньшей мере 80%, более предпочтительно по меньшей мере 85%, более предпочтительно по меньшей мере 90% и наиболее предпочтительно по меньшей мере 95%. Идентичность или гомология в отношении данной последовательности определена в настоящем описании в качестве процента аминокислотных остатков в последовательности-кандидате, которые идентичны остаткам исходного антитела, после выравнивания последовательностей и внесения пропусков, если это необходимо, для достижения максимального процента идентичности последовательности. Ни одно из N-концевых, C-концевых или внутренних удлинений, делеций или вставок в последовательность антитела не следует рассматривать в качестве влияющих на идентичность последовательности или гомологию. Вариант сохраняет способность связывать IL-31 человека и предпочтительно обладает свойствами, которые превосходят свойства исходного антитела. Например, вариант может обладать более высокой аффинностью связывания, повышенной способностью ингибировать вызванную IL-31 стимуляцию иммунных клеток. Для анализа таких свойств следует сравнивать Fab-форму варианта с Fab-формой исходного антитела или полноразмерную форму варианта с полноразмерной формой исходного антитела, например, поскольку было обнаружено, что структура антитела против IL-31 воздействует на его активность в описанных в настоящем описании тестах на биологическую активность. Особенно интересный в настоящем описании вариант антитела представляет собой вариант, который демонстрирует увеличение биологической активности при сравнении с исходным антителом по меньшей мере приблизительно в 10 раз, предпочтительно по меньшей мере приблизительно в 20 раз и наиболее предпочтительно по меньшей мере приблизительно в 50 раз.
Применяемый в настоящем описании термин «исходное антитело» означает антитело, которое кодируется аминокислотной последовательностью, применяемой для получения варианта. Предпочтительно, исходное антитело содержит человеческий каркасный участок и, если присутствует, содержит константную область антитела человека. Например, исходное антитело может представлять собой гуманизированное или человеческое антитело.
Термин «агонист» означает любое соединение, включающее в себя белок, полипептид, пептид, антитело, фрагмент антитела, большую молекулу или небольшую молекулу (менее 10 кДа), которое увеличивает активность, активацию или функцию другой молекулы. Агонисты IL-31 вызывают, например: стимуляцию NK-клеток, субпопуляции T-клеток и субпопуляции B-клеток и дендритных клеток.
Термин «антагонист» означает любое соединение, включающее в себя белок, полипептид, пептид, антитело, фрагмент антитела, большую молекулу или небольшую молекулу (менее 10 кДа), которое снижает активность, активацию или функцию другой молекулы. Антагонисты IL-31 вызывают: снижение иммунной функции NK-клеток, субпопуляции T-клеток и субпопуляции B-клеток и дендритных клеток; связывание IL-31 такое, что взаимодействие белка IL-31 блокируется, ингибируется, снижается, оказывается обратное действие или нейтрализуется.
«Бивалентное антитело», отличающееся от «мультиспецифического» или «мультифункционального» антитела, в определенных вариантах осуществления, как предполагают, содержит участки связывания, обладающие идентичной антигенной специфичностью.
«Биспецифическое» или «бифункциональное» антитело представляет собой гибридное антитело, содержащее две различные пары тяжелой/легкой цепи и два различных участка связывания. Биспецифические антитела можно получить различными способами, включающими в себя в качестве неограничивающих примеров слияние гибридом или сшивки Fab'-фрагментов. Смотрите, например, Songsivilai & Lachmann, Clin. Exp. Immunol. 79: 315-321 (1990); Kostelny et al., J. Immunol. 148: 1547-1553 (1992).
Термин «химерное антитело» или «химерные антитела» означает антитела, чьи гены легких и тяжелый цепей сконструированы, обычно посредством генной инженерии, из генов вариабельной и константной областей иммуноглобулина, принадлежащих к различным видам. Например, вариабельные сегменты генов из моноклонального антитела мыши можно объединить с человеческими константными сегментами, такими как гамма 1 и гамма 3. Типичное терапевтическое химерное антитело, таким образом, представляет собой гибридный белок, составленный из вариабельного или антигенсвязывающего домена из антитела мыши и константный домен из антитела человека, хотя могут применяться и другие виды млекопитающих.
Термин «эпитоп» включает в себя любую белковую детерминанту, способную к специфическому связыванию с иммуноглобулином или рецептором T-клетки. Эпитопные детерминанты обычно состоят из химически активных поверхностных группировок молекул, таких как аминокислоты или боковые цепи сахаров, и обычно обладают определенными трехмерными структурными характеристиками, а также и определенными зарядными характеристиками. Конкретнее, применяемый в настоящем описании термин «эпитоп IL-31» означает части полипептида IL-31, обладающие антигенной или иммуногенной активностью у животного, предпочтительно у млекопитающего и наиболее предпочтительно у мыши или человека. Эпитоп, обладающий иммуногенной активностью, представляет собой часть полипептида IL-31, которая вызывает иммунный ответ у животного. Эпитоп, обладающий антигенной активностью, представляет собой часть полипептида IL-31, с которой антитело связывается иммуноспецифически, как определено любым способом, хорошо известным в данной области, например иммуноанализами. Антигенные эпитопы не обязательно должны быть иммуногенными.
Применяемый в настоящем описании термин «меченый эпитоп» означает антитело против IL-31, соединенное с «меткой эпитопа». Полипептид метки эпитопа содержит достаточное количество остатков, чтобы обеспечить присутствие эпитопа, против которого можно получить антитело, все же достаточно короткий, такой, что он не влияет на активность антитела к IL-31. Метка эпитопа предпочтительно достаточно уникальна так, чтобы антитело по существу не реагировало перекрестно с другими эпитопами. Подходящие полипептиды метки в общем случае содержат по меньшей мере 6 аминокислотных остатков и обычно в диапазоне приблизительно 8-50 аминокислотных остатков (предпочтительно в диапазоне приблизительно 9-30 остатков). Примеры включают в себя полипептид метки НА гриппа и его антитело 12CA5 (Field et al. Mol. Cell. Biol. 8: 2159-2165 (1988)); метку c-myc и ее антитела 8F9, 3C7, 6E10, G4, B7 и 9E10 (Evan et al., Mol. Cell. Biol. 5(12): 3610-3616 (1985)); и метку гликопротеина D (gD) вируса простого герпеса и ее антитело (Paborsky et al., Protein Engineering 3(6): 547-553 (1990)). В определенных вариантах осуществления метка эпитопа представляет собой «сохраняющий связывающийся с рецептором эпитоп». Применяемый в настоящем описании термин «сохраняющий связывающийся с рецептором эпитоп» означает эпитоп Fc-области молекулы IgG (например, IgG1, IgG2, IgG3 или IgG4), которая ответственна за увеличение периода полувыведения молекулы IgG из сыворотки крови in vivo.
Применяемый в настоящем описании термин «фрагмент» означает пептид или полипептид, содержащий аминокислотную последовательность по меньшей мере из 5 следующих друг за другом аминокислотных остатков, по меньшей мере из 10 следующих друг за другом аминокислотных остатков, по меньшей мере из 15 следующих друг за другом аминокислотных остатков, по меньшей мере из 20 следующих друг за другом аминокислотных остатков, по меньшей мере из 25 следующих друг за другом аминокислотных остатков, по меньшей мере из 40 следующих друг за другом аминокислотных остатков, по меньшей мере из 50 следующих друг за другом аминокислотных остатков, по меньшей мере из 60 следующих друг за другом аминокислотных остатков, по меньшей мере из 70 следующих друг за другом аминокислотных остатков, по меньшей мере из 80 следующих друг за другом аминокислотных остатков, по меньшей мере из 90 следующих друг за другом аминокислотных остатков, по меньшей мере из 100 следующих друг за другом аминокислотных остатков, по меньшей мере из 125 следующих друг за другом аминокислотных остатков, по меньшей мере из 150 следующих друг за другом аминокислотных остатков аминокислотной последовательности полипептида IL-31 или антитела, которое иммуноспецифически связывается с полипептидом IL-31.
Применяемый в настоящем описании термин «иммуноглобулин» означает белок, состоящий из одного или более полипептидов, по существу кодируемых генами иммуноглобулина. Одна конфигурация иммуноглобулина составляет основную структурную единицу антитела. Данная конфигурация представляет собой тетрамер и состоит из двух идентичных пар цепей иммуноглобулина, причем каждая пара содержит одну легкую и одну тяжелую цепь. В каждой паре вариабельные области легкой и тяжелой цепей совместно ответственны за связывание антигена и константные области ответственны за эффекторные функции антитела.
Полноразмерные «легкие цепи» иммуноглобулина кодируются геном вариабельной области на NH2-конце и геном каппа или лямбда константной области на COOH-конце. Полноразмерные «тяжелые цепи» иммуноглобулина сходным образом кодируются геном вариабельной области и одним из других упомянутых выше генов константной области (приблизительно 330 аминокислот). Тяжелые цепи классифицируются как гамма, мю, альфа, дельта или эпсилон и определяют изотип антитела как IgG (включающего в себя IgG1, IgG4), IgM, IgA, IgD и IgE, соответственно. В легких и тяжелых цепях вариабельные и константные области соединяются с областью «J» из приблизительно 12 или более аминокислот, с тяжелой цепью, также включающей область «D» приблизительно из 10 дополнительных аминокислот. (В общем смотрите Fundamental Immunology (Paul, W., ed., 2nd ed. Raven Press, N. Y., 1989), Ch. 7 (полностью включенную в качестве ссылки).)
Вариабельная область легкой или тяжелой цепи иммуноглобулина состоит из «каркасного участка», прерываемого тремя гипервариабельными участками. Таким образом, термин «гипервариабельный участок» означает аминокислотные остатки антитела, которые ответственны за связывание антигена. Гипервариабельный участок содержит аминокислотные остатки из «определяющей комплементарность области» или «CDR» (смотрите Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, Md. (1991) и Chothia and Lesk, 1987, J. Mol. Biol. 196: 901-917) (обе из которых включены в настоящее описание в качестве ссылки). Остатки «каркасного участка» или «FR» представляют собой такие остатки вариабельного домена, за исключением остатков гипервариабельного участка, как определено в настоящем описании. Последовательности каркасных участков различных легких или тяжелых цепей относительно консервативны среди видов. Таким образом, «человеческий каркасный участок» представляет собой каркасный участок, который по существу идентичен (приблизительно на 85% или более, обычно на 90-95% или более) каркасному участку встречающегося в природе иммуноглобулина человека. Каркасный участок антитела, который объединен с каркасными участками составляющих легких и тяжелых цепей, служит для позиционирования и выравнивания CDR. CDR прежде всего ответственны за связывание с эпитопом антигена.
Соответственно, термин «гуманизированный» иммуноглобулин означает иммуноглобулин, содержащий человеческий каркасный участок и одну или более CDR из нечеловеческого (обычно мышиного или крысиного) иммуноглобулина. Нечеловеческий иммуноглобулин, дающий CDR, называют «донором», и иммуноглобулин человека, дающий каркас, называют «акцептором». Константные области не должны присутствовать, но если есть, они должны быть по существу идентичны константным областям иммуноглобулина человека, то есть идентичными по меньшей мере приблизительно на 85-90%, предпочтительно приблизительно на 95% или более. Следовательно, все части гуманизированного иммуноглобулина, кроме, возможно, CDR, по существу идентичны соответствующим частям природных последовательностей иммуноглобулина человека. «Гуманизированное антитело» представляет собой антитело, содержащее гуманизированную легкую цепь и гуманизированную тяжелую цепь иммуноглобулина. Например, гуманизированное антитело не охватывало бы типичное химерное антитело, как определено выше, например, поскольку вся вариабельная область химерного антитела является нечеловеческой.
Применяемый в настоящем описании термин «человеческое антитело» включает в себя и антитело, которое содержит аминокислотную последовательность иммуноглобулина человека и включает в себя антитела, выделенные из библиотек иммуноглобулинов человека или из животных, трансгенных в отношении одного или более иммуноглобулинов человека, и которые не экспрессируют эндогенных иммуноглобулинов, как описано, например, Kucherlapati et al. в патенте США №5939598.
Термин «генетически измененные антитела» означает антитела, в которых аминокислотные последовательности отличаются от последовательности нативного антитела. Из-за применимости технологий рекомбинантных ДНК при получении антител не следует ограничиваться аминокислотными последовательностями, обнаруженными в природных антителах; антитела можно переконструировать, чтобы получить необходимые характеристики. Возможные изменения представляют собой множество изменений и находятся в диапазоне от изменения только одной или нескольких аминокислот до полной реконструкции, например, вариабельной или константной области. Изменения в константной области будут, в общем случае, предприняты для того, чтобы улучшить или изменить характеристики, такие как фиксация, взаимодействие с мембранами и другие эффекторные функции. Изменения в вариабельной области будут предприняты для того, чтобы улучшить характеристики связывания антигена.
В добавление к антителам иммуноглобулины могут присутствовать во множестве других конфигураций, включающих в себя, например, одноцепоченые или Fv, Fab и (Fab')2, а также и диатела, линейные антитела, мультивалентные или мультиспецифические антитела (как описано выше и более подробно в: Lanzavecchia et al., Eur. J. Immunol. 17, 105 (1987)) и в одноцепочечных формах (например, Huston et al., Proc. Natl. Acad. Sci. U.S.A. 85 5879-5883 (1988) и Bird et al., Science. 242: 423-426 (1988), которые включены в настоящее описание в качестве ссылки). (Смотрите, в общем, Hood et al., "Immunology", Benjamin, N.Y., 2nd ed. (1984) и Hunkapiller and Hood, Nature, 323: 15-16 (1986), которые включены в настоящее описание в качестве ссылки).
Применяемые в настоящем описании термины «одноцепочечный Fv», «одноцепочечное антитело», «Fv» или «scFv» означает фрагменты антител, которые содержат области как из тяжелых, так и из легких цепей, но не содержат константные области, но в одной единственной полипептидной цепи. В общем случае, одноцепочечное антитело дополнительно содержит полипептидный линкер между VH и VL доменами, который позволяет ему сформировать необходимую структуру, которая позволила бы осуществлять связывание антигена. Одноцепочечные антитела подробно обсуждаются Pluckthun в The Pharmacology of Monoclonal Antibodies, vol.113, Rosenburg and Moore eds. Springer-Verlag, New York, pp.269-315 (1994); смотрите также публикацию заявки на международный патент № WO 88/01649 и патенты США №№4946778 и 5260203, описания которых включены в качестве ссылок с любой целью. В определенных вариантах осуществления одноцепочечные антитела могут также быть биспецифическими или гуманизированными.
«Fab-фрагмент» состоит из одной легкой цепи и CH1 и вариаблельных областей одной тяжелой цепи. Тяжелая цепь Fab-молекулы не может образовать дисульфидную связь с другой молекулой тяжелой цепи.
«Fab'-фрагмент» содержит одну легкую цепь и одну тяжелую цепь, которая содержит большую константную область, между доменами CH1 и CH2, таким образом, что межцепочечная дисульфидная связь может образоваться между двумя тяжелыми цепями с получением F(ab')2-молекулы.
«F(ab')2-фрагмент» содержат две легкие цепи и две тяжелые цепи, содержащие часть константной области между доменами CH1 и CH2, таким образом, что межцепочечная дисульфидная связь образуется между двумя тяжелыми цепями.
Термин «диатела» означает небольшие фрагменты антител с двумя антигенсвязывающими участками, в которых фрагменты содержат вариабельный домен тяжелой цепи (VH), связанный с вариабельным доменом легкой цепи (VL) в одной и той же полипептидной цепи (VH-VL). Применяя линкер, который является слишком коротким, чтобы осуществить объединение двух доменов в одной и той же цепи, домены принуждают к объединению с комплементарными доменами другой цепи и созданию двух антигенсвязывающих участков. Более полно диатела описаны, например, в ЕР 404097; WO 93/11161 и Hollinger et al., Proc. Natl. Acad. Sci. USA, 90: 6444-6448 (1993).
Термин «линейные антитела» означает антитела, описанные Zapata et al. Protein Eng. 8(10): 1057-1062 (1995). Вкратце, данные антитела содержат пару тандемных Fd-сегментов (VH-CH1-VH-CH1), которые образуют пару антигенсвязывающих участков. Линейные антитела могут быть биспецифическими или моноспецифическими.
Применяемый в настоящем описании термин «иммунологически функциональный фрагмент иммуноглобулина» означает фрагмент полипептида, который содержит по меньшей мере вариабельные домены тяжелых и легких цепей иммуноглобулина. Иммунологически функциональный фрагмент иммуноглобулина по изобретению способен связывать лиганд, предотвращать связывание лиганда с его рецептором, прерывать биологический ответ, являющийся результатом связывания лиганда с рецептором, или осуществлять любую их комбинацию.
Термин «моноклональное антитело» означает антитело, которое происходит из одного клона, включающего в себя эукариотический, прокариотический или фаговый клон, а не способ, которым оно получено.
Настоящее изобретение частично базируется на открытии, что субъединицы гетеродимерного рецептора, который связывает IL-31, например IL-31Ra и OSMRb, экспрессируются в нервных клетках, таких как клетки ганглия заднего корешка. Таким образом, настоящее изобретение охватывает применение антагонистов IL-31 при ингибировании боли и воспаления и симптомов воспалительных заболеваний кишечника, болезни Крона, зуда и нейрогенной боли и повышенной чувствительности. Настоящее изобретение также охватывает применение агонистов IL-31 для улучшения чувствительности посредством стимуляции клеток ганглия заднего корешка.
IL-31 представляет собой наименование в HUGO для цитокина, который ранее был описан как Zcytor17lig в опубликованной заявке на патент США (смотрите опубликованную заявку на патент США номер 20030224487, заявку на патент США порядковый номер 10/352554, поданную 21 января 2003 г., в настоящее время выданный патент США номер 7064186; Sprecher, Cindy et al., 2003, включенные в настоящее описание в качестве ссылок). Гетеродимерный рецептор IL-31 содержит гетеродимер, образованный IL-31Ra и рецептором онкостатина M бета (OSMRb). IL-31Ra представляет собой наименование в HUGO для белка, называемого zcytorl7 в находящейся в общедоступной опубликованной заявке на патент США номер 20030215838, в заявке на патент США порядковый номер 10/351157, поданной 21 января 2003 г., включенных в настоящее описание в качестве ссылки. Полинуклеотидная и полипептидная последовательности IL-31 человека указаны в SEQ ID NO: 1 и 2, соответственно. Полинуклеотидная и полипептидная последовательности мышиного IL-31 указаны в SEQ ID NO: 3 и 4, соответственно. Применяемый в настоящем описании термин IL-31 означает zcytor17lig, как применяется в публикации патента США номер 20030224487, как указано выше. IL-31Ra ранее был описан в находящейся в общедоступной заявке на патент США порядковый номер 09/892949, поданной 26 июня 2001 г., которая включена в настоящее описание в качестве ссылки.
Аминокислотная последовательность рецепторов OSMR и IL-31RA указывает, что кодируемые рецепторы принадлежат к подсемейству рецепторов цитокинов класса I, которые включают в себя в качестве неограничивающих примеров рецепторы IL-2, IL-4, IL-7, Lif, IL-12, IL-15, EPO, TPO, GM-CSF и G-CSF (для обзора смотрите Cosman, "The Hematopoietin Receptor Superfamily" in Cytokine 5(2): 95-106, 1993). Рецептор zcytorl7 подробно описан в находящейся в общественной заявке на патент PCT № US 01/20484 (публикация WIPO № WO 02/00721; включенной в настоящее описание в качестве ссылки).
Настоящее изобретение включает в себя применение агентов против IL-31, включающих в себя антагонисты, антитела, связывающие белки, варианты и фрагменты, обладающие активностью против IL-31. Изобретение включает в себя введение субъекту молекулы против IL-31 и предполагает терапевтическое применение и для человека, и в ветеринарии. Иллюстративные ветеринарные субъекты включают в себя субъекты млекопитающих, такие как сельскохозяйственные животные и домашние животные.
Нативные полинуклеотидные и полипептидные последовательности для «длинной» формы IL-31RA указаны в SEQ ID NO: 5 и 6, соответственно. Нативные полинуклеотидные и полипептидные последовательности для «короткой» формы IL-31RA указаны в SEQ ID NO: 7 и 8, соответственно. Дополнительные укороченные формы полипептида IL-31RA, по-видимому, экспрессируются естественным образом. Обе формы кодируют растворимые рецепторы IL-31RA. «Длинные» полинуклеотидные и полипептидные последовательности растворимого IL-31RA указаны в SEQ ID NO: 9 и 10, соответственно. «Короткие» полинуклеотидные и полипептидные последовательности растворимого IL-31RA указаны в SEQ ID NO: 11 и 12, соответственно. Нативные полинуклеотидные и полипептидные последовательности для IL-31RA мыши указаны в SEQ ID NO: 13 и 14, соответственно. Нативные полинуклеотидные и полипептидные последовательности для OSMR-бета человека указаны в SEQ ID NO: 15 и 16, соответственно. Смотрите заявки PCT WO 02/00721 и WO 04/003140, которые обе включены в настоящее описание в качестве ссылок.
Антагонисты IL-31 включают в себя молекулы против IL-31, такие как антитела, которые связываются с IL-31, включающие в себя их варианты, фрагменты или производные, и которые ингибируют, ограничивают, уменьшают, сводят к минимуму, предотвращают или нейтрализуют действие IL-31, которое он оказывает при связывании с его родственным рецептором.
Анализ экспрессии in situ выявил, что IL-31RA и OSMR-бета экспрессируются в спинном мозге и клетках ганглия заднего корешка у людей. Смотрите пример 1. Следовательно, молекулы IL-31, их агонисты или антагонисты играют роль в обеспечении жизнедеятельности нейронов и в нейрогенном воспалении и возбуждении. Это указывает на то, что агонисты, антагонисты IL-31 можно применять для лечения различных нейродегенеративных заболеваний, таких как боковой амиотрофический склероз (ALS), болезнь Альцгеймера, болезнь Хантингтона, болезнь Паркинсона, периферические невропатии и демиелинизирующие заболевания, включающие в себя множественный склероз. Тканевая специфичность IL-31RA и OSMRb предполагает, что IL-31 может быть фактором роста и/или обеспечения жизнедеятельности в спинном мозге и головном мозге, который можно применять для лечения спинного мозга, головного мозга или повреждений периферической нервной системы.
Способы измерения способности IL-31 стимулировать боль известны специалистам в данной области. Например, клетки ганглия заднего корешка можно выделить и культивировать. Смотрите Voilley, N. et al., J. Neurosci. 27(20): 8026-8033. 2001. Например, клетки ганглия заднего корешка получали из самцов взрослых крыс Wistar (5-7 недель) и новорожденных крыс диссоциацией в 0,1% коллагеназе и помещая на покрытые коллагеном чашки P35 в DMEM с добавлением 5% фетальной телячьей сыворотки. Похожие способы выделения клеток ганглия заднего корешка описаны Steinhoff, M. et al. (Смотрите Steinhoff, M. et al., Nature Medicine. 6(2): 151-157. 2000). Вкратце, клетки ганглия заднего корешка измельчают в холодной модифицированной по способу Дульбекко среде Игла (DMEM) и инкубируют в DMEM, содержащей 0,05 мг/мл трипсина, 1 мг/мл коллагеназы и 0,01 мг/мл ДНКазы I в течение 45-60 минут при 37 градусах C. SBTI добавляют для того, чтобы нейтрализовать трипсин, и суспензию центрифугируют приблизительно при 1000 g в течение 1 мин. Нейроны в осадке суспендируют в DMEM, содержащей 10% фетальной бычьей сыворотки, 5 нг/мл фактора роста нервов, 2 мМ глутамина, 1 мг/мл смеси пенициллин/стрептомицин и ДНКазу I, и помещают на покровное стекло, покрытое Matrigel. Нейроны культивируют в течение 3-5 дней перед применением. Экспрессию IL-31RA в цитоплазматических мембранах подтверждают иммунофлюоресценцией с применением антитела.
Для того, чтобы определить воздействие IL-31 на стимуляцию ганглия заднего корешка, внутриклеточную концентрацию ионов кальция измеряют в культивируемых нейронах, как описано выше Steinhoff et al. Нейроны инкубируют в сбалансированном солевом растворе Хенкса, 20 мМ HEPES, pH 7,4, содержащей 5 мкМ Fura-2/AM (Molecular Probes, Юджин, Штат Орегон) в течение 1 ч при 37 градусах C. Покровные стекла моют, устанавливают в камеру (объемом 1 мл) инвертированного микроскопа Zeiss 100 TV и рассматривают, применяя объектив Fluar Zeiss x40. Флуоресценцию измеряют при 340 нм и 380 нм, чтобы осуществить определение кальция. Клетки подвергали воздействию IL-31 с применением и без применения других повышающих чувствительность веществ и определяли ингибирование в присутствии антагонистов IL-31.
Для того, чтобы определить способность антагониста IL-31 влиять на связывание IL-31 с его родственным гетеродимерным рецептором в ганглии заднего корешка, или вообще нервных клетках, на боль, можно измерять несколько медиаторов боли, таких как, например, в качестве неограничивающих примеров простагландины, вещество P, CGRP, галанин, нейропептид Y, гистамин, брадикинин, каннабиноиды и медиаторы пути метаболизма арахидоновой кислоты.
В дополнение к указанным выше способам определения способности антагонистов IL-31 действовать в отношении вызывающего боль воздействия IL-31 на нервные клетки, можно также применять некоторые модели in vivo. Смотрите, например, Honore, P. et al., Neuroscience, 98(3): 585-598, 2000. В данной статье описаны некоторые модели боли при воспалении, невропатической боли и боли при раке. Например, в одной модели определяют эффект антагониста IL-31, такой как подкожная инъекция IL-31 в подошвенную поверхность задней лапы мыши с применением и без молекулы антагониста. Мышь подвергали эвтаназии через 3 дня после инъекции и измеряли периферический отек. Определяли ингибирующее, ограничивающее, сводящее к минимуму, уменьшающее, предотвращающее или нейтрализующее отек действие антагониста IL-31. Дополнительные модели in vivo представляют собой лигирование спинномозговых нервов, рассечение седалищного нерва, вызванную саркомой раковую опухоль кости, анализ поведения и эффекты морфина.
Другая мышиная модель боли представляет собой механическую аллодинию. Смотрите, например, Sweitzer, S. M. et al., J. Neuroimm., 125: 82-93. 2002. Вкратце, крыс или мышей тестируют в отношении механической аллодинии с применением 2- и/или 12-g волокон Фрея. Сначала животные привыкают к процедуре, и предпринимают измерение исходного уровня. IL-31 вводят в различных количествах. Аллодинию описывают в качестве интенсивности отдергивания лапы на не являющиеся вредоносными стимулами в ответ на введение IL-31. Сравнение проводят при введении и без введения молекул антагонистов IL-31.
Провоспалительный нейропептид, вещество P (SP), продуцируется спинными ганглиями и затем передается на периферию ноцицептивными нервами А и С (15). SP может вызывать зуд при высвобождении гистамина из гранул тучных клеток. На коже SP может также вызывать эритему, отек и нейрогенное воспаление, высвобождающее гистамин, IL-1, простагландины и лизосомальные ферменты, но он быстро деградирует в дерме (16). Предшествующее пероральное введение антигистаминовых средств ингибирует зуд, вызванный SP. Капсаицин, получаемый из острого перца, применяемый местно, уменьшает количество SP в кожных нервах и, таким образом, уменьшает зуд. Поскольку субъединицы рецептора для IL-31 экспрессируются в клетках ганглия заднего корешка, введение молекул антагонистов IL-31 может уменьшить стимуляцию данных клеток и может снизить количество вещества P, появление которого может индуцироваться введением IL-31.
Связывание IL-31 с его рецептором, то есть с IL-31RA и OSMR-бета, в клетках ганглия заднего корешка может стимулировать соматосенсорную систему, которая состоит из различных сенсорных рецепторов, ответственных за ощущения, такие как давление, прикосновение, температура, боль, зуд, щекотка, покалывание и онемение. Связывание IL-31 с его родственным рецептором может привести к нейрогенному воспалению и стимуляции, которая может привести к высвобождению дополнительных факторов, которые индуцируют нейрогенный стимул. Одна группа факторов, которые опосредуют возникновение боли, представляет собой простагландины, которые также способствуют локальному воспалению. Таким образом, антагонист IL-31 может оказать полезное воздействие на боль при остром воспалении, которое обычно лечат НПВС, таком как миалгия, головная боль, сочетанные боли при острых повреждениях, и на хроническую боль, такую как боль, вызываемую остеоартритом. Такой нейрогенный стимул может представлять собой результат воспаления, вызванного, например, аутоиммунными реакциями, такими как аллергия, вирусной инфекцией, такой как ветряная оспа, и повреждением, таким как ожог или травма. Таким образом, антагонисты, которые влияют на трансдукцию сигнала, вызванную связыванием лиганда IL-31 с его родственным рецептором, можно применять для уменьшения, ограничения, предотвращения или снижения до минимума нейрогенного воспаления и стимуляции соматосенсорной системы. Как таковые, антагонисты вызванной IL-31 трансдукции сигнала в клетках ганглия заднего корешка можно применять для лечения боли, зуда, покалывания, вызванного аутоиммунными заболеваниями, вирусной инфекцией и травмой. Более того, поскольку нейрогенное воспаление может приводить к повышенной чувствительности нерва после первичного кровоизлияния, антагонисты IL-31 могут представлять собой эффективное лечение симптомов. Например, некоторые пациенты с опоясывающим лишаем испытывают сенсорные симптомы боли и/или зуда намного позже после того, как вирусная инфекция прошла или уменьшилась до минимума. Невралгия, которая сопровождает острый опоясывающий лишай, и постгерпетическая невралгия происходят, вероятно, вследствие воспаления ганглиев заднего корешка и ганглиев тройничного нерва, где вирусные антигены притягивают T-клетки и другие клетки воспаления. Длительная боль может происходить в результате постоянного воспаления дерматома после сильной противовирусной реакции. Следовательно, уровень или стадия вирусной инфекции, возможно, не являются показательными для сенсорного восприятия у субъекта. Таким образом, благоприятное воздействие противодействия вызванной IL-31 трансдукции сигнала может выходить за пределы текущего состояния вирусной инфекции или травмы.
Нейропатия и сенсорная недостаточность влекут за собой боль и потерю чувствительности и могут быть связаны с такими заболеваниями, как атопия, диабет, рассеянный склероз и гипертония, например. Поскольку IL-31RA и OSBR-бета представляют собой белки, которые экспрессируются в спинном мозге и клетках ганглия заднего корешка, антагонисты IL-31 можно применять при лечении боли и сенсорных недостаточностей. Например, антагонисты IL-31 можно предоставлять местно, подкожно, центрально или систематично для лечения диабетической периферийной невропатии, постгерпетической периферийной невропатии, а также и боли, в общем случае, включающей в себя боль в качестве симптома у пациентов с ожогом.
Ожоговые повреждения вызывают интенсивную и длительную боль, которая усиливается, когда меняют раневую повязку. Частые замены повязки необходимы для предотвращения инфицирования и способствуют заживлению. Количество боли, испытываемой пациентами во время обработки раны, остается международной проблемой для жертв ожогов, а также и множества других популяций пациентов. Когда пациенты находятся в состоянии покоя, боль, связанную с ожогом, можно лечить опиатами, которые обладают некоторыми нежелательными эффектами. Тем не менее, во время обработки раны, такой как ежедневная смена повязки, очищение раны, удаления волокон и так далее, опиатов становится недостаточно, причем большинство пациентов с ожогами сообщают о сильной до мучительной боли во время обработки раны.
Поскольку оба элемента гетеродимера для IL-31, то есть IL-31RA и OSMR-бета, экспрессируются в клетках ганглия заднего корешка, антагонист к IL-31, такой как нейтрализующее антитело, применим для предотвращения, снижения до минимума, ограничения и/или лечения боли, включающей боль, связанную с ожогом или невропатией. Модели in vivo, имитирующие ожоги, известны специалисту в данной области.
Постоянная боль может вызвать гиперплазию, так что меньший чем исходный стимул может вызвать усиленную боль, также называемую аллодиния. Поскольку обе субъединицы IL-31RA и OSMR-бета экспрессируются в клетках ганглия заднего корешка, антагонист вызванной IL-31 трансдукции сигнала в нейронных клетках, несущих данные субъединицы, может способствовать смягчению симптомов аллодинии.
Полипептиды по настоящему изобретению, такие как IL-31, а также и агонисты, их фрагменты, варианты и/или химеры, можно также применять для повышения чувствительности у млекопитающих. Например, полипептиды IL-31 по настоящему изобретению, включающие в себя агонисты, можно применять для повышения чувствительности (боль, высокая температура или механическая чувствительность) при локальной или местной, систематической или центральной доставке, и определять в любых моделях или экспериментах, известных специалисту в данной области и/или описанных в настоящем описании. Также полипептиды по настоящему изобретению можно вводить для увеличения чувствительности спинальных и нейронных клеток для того, чтобы улучшить функционирование сохранивших работоспособность нейронов в отношении медиаторов и поэтому могли бы быть эффективны при болезни Паркинсона или Альцгеймера, а также параличе.
Схожим образом, когда у пациента повышенная чувствительность к боли, антагонисты IL-31 можно применять для того, чтобы уменьшить ощущение боли у пациента с невропатией. Например, для пациента с диабетической невропатией и постгерпетической невропатией, с хронической, усиленной болью, может быть применим антагонист IL-31 для ограничения, предотвращения или уменьшения боли.
В качестве рецептора для белка, который является провоспалительным, присутствие IL-31RA и OSMR-бета в спинном мозге и клетках ганглия заднего корешка указывает на то, что антагонисты IL-31 можно применять для уменьшения воспаления в данных тканях. Таким образом, на состояния, такие как менингит, может оказать благотворное влияние введение антагонистов, включающих в себя антитела.
Заболевания, которые влекут за собой нейрогенное воспаление и стимуляцию и на которые может оказать благотворное влияние противодействие вызванной IL-31 боли в нейронных тканях, включая сюда клетки ганглия заднего корешка, включают в себя: хроническую боль, мигрень, артрит, остеоартрит, ревматоидный артрит, полиневропатию, диабетическую периферийную невропатию, боль, являющуюся результатом разрыва нерва (например, боль после хирургической операции), воспалительные состояния, которые вовлекают в процесс нейрогенный продуцирующий боль компонент, такие как воспалительные заболевания кишечника, нефрит, некоторые метастатические карциномы и воспаление кровяных сосудов. Данные заболевания можно также лечить антагонистом вызванной IL-31 трансдукции сигнала. В дополнение, кожные состояния, включая сюда радиационное раздражение и ожоги, химические ожоги, множественную химическую чувствительность, потницу, ринит, тепловые ожоги, солнечные ожоги, покраснения кожи и вызванные химическими веществами повреждения, и острые аллергические реакции, такие как острый приступ астмы и воспаление легких, вызванные воздействием химических веществ, и крапивницу, а также конъюнктивиты и воспаление десен можно лечить антагонистами IL-31. Дополнительно, лопаточно-перонеальные синдромы представляют собой гетерогенные нейромышечные нарушения, которые характеризуются недостатком в распределении мускулатуры плечевого пояса и в малоберцовой области. Были описаны как нейрогенные (лопаточно-перонеальная спинальная мышечная атрофия, SPSMA), так и миопатические (лопаточно-перонеальная мышечная дистрофия, SPMD) лопаточно-перониальные синдромы. Хромосомное местоположение гена SPMD было недавно приписано хромосоме 12q, которая представляет собой тот же самый локус для IL-31. Таким образом, антагонисты IL-31 можно применять для лечения данных заболеваний.
В Соединенных Штатах приблизительно 500000 человек страдают от воспалительных заболеваний кишечника, которые могут затрагивать либо одно из двух, либо как тонкую кишку, так и толстый кишечник. Язвенный колит и болезнь Крона являются наиболее известными формами воспалительных заболеваний кишечника, и оба отнесены к «идиопатическим» воспалительным заболеваниям кишечника, поскольку этиология для них неизвестна.
Болезнь Крона может затронуть любую часть желудочно-кишечного тракта, но наиболее часто затрагивает дистальную тонкую кишку и толстую кишку. Воспаление может привести к появлению чего-либо от небольшой язвы на лимфоидном фолликуле до глубокой разрывающейся язвы до трансмурального рубца и хронического воспаления. Хотя этиология неизвестна, были предположены инфекционные и иммунологические механизмы. Симптомы переменчивы и могут включать в себя диарею, лихорадку и боль, а также внекишечные проявления артрита, увеита, узловатой эритемы и анкилозирующий спондилоартрит.
Традиционный подход для лечения воспалительных заболеваний кишечника представляет собой иммуносуппрессию азатиоприном (смотрите, например, Rutgeerts, J. Gastroenterol. Hepatol. 17 (Suppl.): S176-85 (2002)). Совсем недавно химерное моноклональное антитело против фактора некроза опухоли, инфликсимаб, было применено для ориентации на определенные патогенные механизмы заболевания, и оно позволяет получить полное подавление развития заболевания и заживление кишки в долгосрочной перспективе. Тем не менее, такая терапия связана с проблемами иммуногенности. Образование антител к инфликсимабу влияет на эффективность и связано с реакциями на инфузию.
Синдром раздраженного кишечника (IBS) представляет собой хроническое функциональное желудочно-кишечное нарушение. Оно представляет собой гетерогенное состояние, характеризующееся различными кишечными симптомами, включающими в себя брюшную боль и вздутие, которые обычно ассоциированы с изменением ритма дефекации (Collins et al., 2001). Предполагают, что от 12 до 20% американского населения страдает от данного состояния. Для того, чтобы определить IBS, были предложены различные критерии, включающие в себя критерии Маннинга (Manning et al., 1978), Римские критерии (Thompson et al., 1992) и совсем недавно Римские критерии II (Thompson et al., 1999). В сообщениях о научно-исследовательской работе по IBS часто классифицируют пациентов с IBS на два подтипа с преобладающим запором (CON) и с преобладающей диареей (DIA) и иногда добавляют третий подтип переменного типа (ALT).
Молекулы против IL-31, антагонисты, антитела, связывающие белки, варианты и фрагменты применимы для лечения, определения боли, связанной с воспалительными заболеваниями кишечника (IBD) и с синдромом раздраженного кишечника (IBS).
Воспалительное заболевание кишечника (IBD) может поражать толстую и/или прямую кишку (язвенный колит) или тонкий и толстый кишечник (болезнь Крона). Патогенез данных заболеваний неясен, но они влекут за собой хроническое воспаление пораженных тканей. Потенциальные терапевтические средства включают в себя молекулы против IL-31, включающие в себя антитела против IL-31, другие связывающие белки, варианты, фрагменты, химеры и другие антагонисты IL-31. Данные молекулы могли бы служить в качестве чрезвычайно полезного терапевтического средства для уменьшения воспаления и патологических эффектов при IBD и родственных заболеваниях.
Язвенный колит (UC) представляет собой воспалительное заболевание толстого кишечника, обычно называемого толстой кишкой, характеризующееся воспалением и изъязвлением слизистой оболочки или глубоко лежащей выстилки толстой кишки. Такое воспаление вызывает частое опустошение толстой кишки, приводя к диарее. Симптомы включают в себя ослабление стула и связанные с этим брюшные спазмы, лихорадку и потерю веса. Хотя точная причина UC неизвестна, недавнее исследование предполагает, что естественные защитные реакции организма работают против белков организма, которые организм считает чужеродными («аутоиммунная реакция»). Возможно, потому, что они напоминают бактериальные белки в кишечнике, данные белки могут либо провоцировать, либо стимулировать воспалительный процесс, который начинает разрушать выстилку толстой кишки. Поскольку выстилка толстой кишки разрушается, образуются язвы, выпускающие слизь, гной и кровь. Заболевание обычно начинается в ректальной области и может, в конечном счете, распространяться по всему толстому кишечнику. Повторные эпизоды воспаления приводят к утолщению стенки кишечника и прямой кишки тканью шрама. Разрушение ткани толстой кишки или сепсис может иметь место при тяжелом заболевании. Симптомы язвенного колита меняются по степени тяжести, и их появление может быть постепенным или внезапным. Обострения могут быть вызваны множеством факторов, включающими в себя дыхательные инфекции или стресс. Таким образом, молекулы против IL-31 по настоящему изобретению можно применять для лечения или обнаружения UC.
Хотя не существует в настоящий момент никакого доступного лечения UC, терапия сосредоточена на подавлении неправильного воспалительного процесса в выстилке толстой кишки. Терапия, включающая в себя иммуносупрессивные кортикостероиды (например, азатиоприн, меркаптопурин и метотрексат) и аминосалицилаты, доступна для лечения заболевания. Однако долговременное применение иммуносупрессивных средств, таких как кортикостероиды и азатиоприн, может привести к тяжелым побочным эффектам, включающим в себя истончение костей, катаракт, инфекции и воздействия на печень и костный мозг. Для пациентов, у которых доступные в настоящее время способы лечения не имеют успеха, хирургическая операция является выбором. Хирургическая операция приводит к удалению всей толстой и прямой кишки.
Существует несколько моделей на животных, которые могут частично воспроизводить хронический язвенный колит. Наиболее широко применяемая модель представляет собой модель вызванного 2,4,6-тринитробензолсульфоновой кислотой/этанолом (TNBS) колита, которая индуцирует хроническое воспаление и изъязвление толстой кишки. Когда TNBS вводят в толстую кишку восприимчивых мышей посредством внутриректальной инстилляции, это индуцирует опосредованную T-клетками иммунную реакцию в слизистой оболочке толстой кишки, в данном случае приводя к масштабному воспалению слизистой оболочки, характеризующемуся плотной инфильтрацией T-клеток и макрофагов по всей стенке толстого кишечника. Кроме того, такая гистопатологическая картина сопровождается клинической картиной нарастающей потери веса (истощение), кровавого поноса, ректального пролапса и утолщением стенок толстого кишечника кишки (Neurath et al. Intern. Rev. Immunol. 19: 51-62, 2000).
В других моделях колитов применяют декстрансульфат натрия (DSS), который вызывает острый колит, проявляющийся кровавым поносом, потерей веса, укорочением толстой кишки и изъязвлением слизистой оболочки с инфильтрацией нейтрофилами. Вызванный DSS колит гистологически характеризуется инфильтрацией воспалительных клеток в собственную пластинку слизистой оболочки, с лимфатической гипреплазией, очаговым повреждением крипт и эпителиальным изъязвлением. Данные изменения, как думают, развиваются из-за токсичного действия DSS на эпителий и посредством фагоцитоза клеток собственной пластинки слизистой оболочки и продукции TNF-альфа и IFN-гамма. DSS расценивают в качестве независимой от T-клеток модели, поскольку наблюдают ее у животных с дефицитом T-клеток, таких как мыши SCID.
Введение антагонистов IL-31 или связывающих партнеров в такие модели TNBS или DSS можно применять для определения смягчения симптомов и изменения динамики желудочно-кишечного заболевания. IL-31 может играть роль в воспалительной реакции и боли, связанной с колитом, и нейтрализация активности IL-31 при введении антагонистов представляет собой потенциальный терапевтический подход для лечения IBD.
Синдром раздраженного кишечника представляет собой одно из наиболее распространенных состояний в желудочно-кишечной клинике. Пока еще диагностика и лечение IBS остаются ограниченными. Для экспрессии IL-31 и IL-31RA1 установили корреляцию с повышенной регуляцией при болезни Крона (смотрите пример 5). Антагонисты IL-31, включая антитела против IL-31, другие связывающие белки, варианты, фрагменты, химеры и другие антагонисты IL-31, применимы для уменьшения симптомов и лечения заболевания.
Введение антагонистов IL-31 или связывающих партнеров пациентам с IBD или IBS можно применять для смягчения симптомов и изменения динамики желудочно-кишечного заболевания. IL-31 может играть роль в воспалительной реакции при колите, и нейтрализация активности IL-31 при введении антагонистов представляет собой потенциальный терапевтический подход для лечения IBD и/или IBS.
Для нарушений, связанных с IBS и IBD, клинические признаки улучшенного функционирования включают в себя в качестве неограничивающих примеров снижение боли, спазмов и чувствительности, уменьшение диареи и улучшенную консистенцию стула, уменьшенное вздутие живота и увеличенное прохождение содержимого через кишечник. Улучшение можно также определить по уменьшению индекса активности болезни Крона (CDAI). Смотрите Best. W. et al., Gasttoenterology 70: 439-44, 1976. Дополнительно, улучшенное функционирование можно определить в соответствии с оценкой качества жизни, как описано Irvine et al. (Irvine, E. et al., Gasttoenterology 106: 287-96, 1994).
Модели на животных синдрома раздраженного кишечника описаны Mayer and Collins. Gastroenterol. 122: 2032-2048 (2002). Данные модели можно разделить на модели, которые опосредуются, прежде всего, направленными на ЦНС механизмами (модели «стрессовой памяти») и модели с первоначально направленной на кишечник этиологий (модели «память боли» и «иммунная память»). В одной модели животных подготавливают хирургическим путем с применением электродов, вживленных в проксимальную часть толстой кишки и поперечнополосатые мышцы, и катетеров, вживленных в боковые желудочки мозга. Ректальное вздутие выполняют при помощи наполнения ректально введенного надувного баллона, и измеряют давление, выявляющее характеристики висцеромоторного ответа. Исследуемое соединение, такое как антагонист IL-31 и/или варианты или антагонисты, вводят посредством соответствующего способа введения (п/о, в/б, п/к, в/в или в/м) и в соответствующее время (то есть ~20 минут при в/б или в/к) перед растяжением. Исследуемое соединение оценивают по его способности воздействовать на перистальтику толстой кишки, брюшные сокращения и висцеральную боль.
Дополнительно, нарушения, связанные с воспалением кишечника, можно лечить описанными в настоящем описании антагонистами IL-31, такими как фрагменты, их агонисты и антагонисты. Например, синдром раздраженного кишечника (IBS) характеризуется очень широким спектром симптомов (боль; приступы диареи и/или запора; нарушенная желудочно-кишечная перистальтика). Точно определить этиологию трудно, и она может охватывать компоненты, связанные со стрессом, генетикой и/или воспалением. Схожим образом, молекулы против IL-31 по настоящему изобретению, включающие в себя антитела и связывающие партнеры, можно применять для лечения воспалительных заболеваний кишечника (включающих в себя колит и болезнь Крона). IBD является более тяжелым, чем IBS, и характеризуется диареей, болью и недоеданием. У пациентов с IBD часто имеет место повышенный риск возникновения желудочно-кишечного рака.
Желудочно-кишечную моторную активность можно определить в модели на собаке следующим образом: собак обезболивают и вскрывают им брюшную полость. Экстраполостные динамометрические датчики (датчик для измерения сокращения) зашивают в пяти (5) участках, то есть в полости желудка, 3 см ближе к пилорическому кольцу, в двенадцатиперстной кишке, 5 см дальше от пилорического кольца, в тощей кишке, 70 см дальше от пилорического кольца, в подвздошной кишке, 5 см ближе к соединению толстой кишки и подвздошной кишки, и в толстой кишке, 5 см дальше от соединения толстой кишки и подвздошной кишки. Ведущие провода данных динамометрических датчиков извлекают из брюшной полости и затем выводят через сделанный между лопатками разрез кожи, в котором устанавливают соединитель. После операции на собаку надевают защитный жакет, чтобы защитить соединитель. Измерение желудочно-кишечной моторной активности начинают через две недели после операции. Для неограниченного измерения телеметрическое устройство (электроволновой преобразователь данных) соединено с соединителем для того, чтобы определить сокращающую подвижность на каждом участке желудочно-кишечного тракта. Данные сохраняют в компьютере через телеметрическое устройство для анализа. Исследуемое соединение, такое как антагонист IL-31, вводят посредством соответствующего способа введения (п/о, в/в, в/б, п/к, в/м) в соответствующее время, чтобы оценить его способность воздействовать на желудочно-кишечную моторную активность. Такую процедуру можно выполнить на нормальных собаках или собаках, у которых вызвали парез желудка/непроходимость кишечника. Упомянутый выше способ представляет собой модификацию способов Yoshida and Ito. J. Pharmacol. Experiment. Therap. 257, 781-787 (1991) и Furuta et al. Biol. Pharm. Bull. 25: 103-1071 (2002).
IL-31 может представлять собой пусковой механизм для повторной активации неинфекционных вирусных инфекций, таких как инфицирование ветряной оспой. При первичном инфицировании вирусом ветряной оспы (VZV) T-клетки, наиболее вероятно, инфицированные вирусом ветряной оспы, представляют собой CD4-положительные T-клетки памяти, экспрессирующие CLA и CCR4. Существуют мигрирующие в кожу T-клетки, которые могут увеличивать ассоциированную с клетками вирусемию и перенос инфекционного вируса в кожу и DRG. Данные клетки также являются исходными продуцентами IL-31. Таким образом, IL-31 при первичном инфицировании VZV может способствовать появлению зуда/боли, являющегося следствием повреждения кожи. Повторная активация неинфекционного вируса в DRG вызывает опосредованные VZV ответы T-клеток, которые вносят свой вклад в нейрогенное воспаление. Мигрирующие в кожу T-клетки наиболее легко заражаются VZV, и наблюдали передачу вируса in vivo от T-клеток к DRG. Постгерпетическая невралгия представляет собой одно из основных осложнений опоясывающего лишая, вызванное повторной активацией вируса ветряной оспы, и характеризуется сильной болью. Смотрите Sato-Takeda, M. et al., Anesthesiology. 2006 104(5): 1063-9, включенную в настоящее описание в качестве ссылки. В данной ссылке также сообщают о мышиной модели постгерпетической боли, которая соответствует постгерпетической невралгии. Вкратце, мыши BALB/c (гаплотип MHC: H-2), мыши C57BL/6 (гаплотип MHC: H-2) и мыши BALB/b, конгенный BALB/c штамм с H-2, заражают через кожу на задней лапе вирусом простого герпеса типа I. Вызывают одностороннее напоминающее опоясывающий лишай повреждение кожи и связанные с болью реакции (острая герпетическая боль), и некоторые мыши демонстрируют связанные с болью реакции (постгерпетическая боль) после лечения повреждений кожи. Антиген вируса простого герпеса типа I и CD3-положительные клетки окрашивали с применением иммунной метки в ганглиях заднего корешка в острой фазе. Смотрите также Argoff, C.E., et al., J Pain Symptom Manage. 2004 Oct; 28(4): 396-411, включенную в настоящее описание в качестве ссылки. Таким образом, антагонисты IL-31 можно применять для ограничения или предотвращения повторной активации вирусных инфекций при ветряной оспе.
Модели мыши для экспериментального аллергического энцефаломиелита (EAE) применяли в качестве инструмента для исследования как механизмов опосредованных иммунной системой заболеваний, так и способов потенциального терапевтического вмешательства. Модель напоминает рассеянный склероз человека и становится причиной демиелинизации в результате активации T-клеток к нейробелкам, таким как основной миелиновый белок (MBP) или протеолипидный белок (PLP). Заражение антигеном приводит к индукции CD4+, рестриктированных по антигенам МНС класса II T-клеток (Th1). Изменения в протоколе для EAE могут позволить получить острый, хронически рецидивирующий или с пассивным переносом варианты модели (Weinberg et al., J. Immunol. 162: 1818-26, 1999; Mijaba et al., Cell. Immunol. 186: 94-102, 1999; и Glabinski, Meth. Enzym. 288: 182-90, 1997). Введение антагонистов IL-31 или других растворимых и слитых белков можно применять для смягчения симптомов и изменения динамики заболевания.
Антагонист для вызванной IL-31 трансдукции сигнала в клетках ганглия заднего корешка можно применять для лечения уремического зуда; зуда от гепатита, печеночной недостаточности или застоя желчи; от чесотки или эпидермофитии стопы; от зуда, связанного с беременностью; от зуда у пациентов на диализе; и от зуда при анестезии и психологических нарушений следующим образом.
Уремический зуд или ренальный зуд часто является невыносимым симптомом хронической почечной недостаточности (Blachley JD, Blankenship DM, Menter A et al. Uremic pruritus: skin divalent ion content and response to ultraviolet phototherapy. Am J Kidney Dis 1985; 5: 237-41), имеющим место приблизительно в 13% случаев; можно наблюдать вторичные повреждения кожи из-за расчесывания. Такой процесс еще более обычен для пациентов, подвергающихся перитонеальному диализу или гемодиализу (Murphy M, Carmichael AJ. Renal itch. Clin Exp Dermatol 2000; 25: 103-6.); он может быть локализованным или генерализованным. Зуд не имеет места при острой почечной недостаточности. Лечение почечного зуда основано на интенсивном и эффективном диализе для того, чтобы удалить приводящие к зуду вещества из крови, и на применении неактивирующих комплемент мембран. Можно также применять УФ-терапию, смягчающие мази, активированный уголь, холестирамин (4 грамма два раза в день), связывающие фосфат средства. Иногда необходимо удаление паращитовидных желез.
Боль противодействует зуду. Смотрите, например, Ward, L. et al., Pain 64: 129-138. 1996. Также медиатор боли, такой как антагонист IL-31, можно применять для лечения боли, связанной с зудом, таким образом облегчая не только зуд, или состояние расчесывания, но также и ассоциированную боль.
Зуд представляет собой хорошо распознаваемое проявление среди пациентов с болезнями печени и с внутрипеченочным или постпеченочным застоем желчи. Печеночные заболевания, приводящие к зуду, включают в себя первичный биллиарный цирроз, вирусный гепатит B и C, первичный склерозирующий холангит, карциному желчных протоков, алкогольный цирроз печени, аутоиммунный гепатит и другие. Зуд генерализован и более интенсивен на руках, ногах и вокруг плотно облегающей одежды, в то время как лицо, шея и генитальная область затрагиваются редко.
Генерализованный зуд имеет место у 1-8% беременных женщин. Зуд беременных можно отличить от дерматозного зуда при беременности, такого как гестозный пемфигоид (герпес беременных), папулезный и зудящий дерматоз беременности и другие. Зуд беременных проявляется без какой-либо сыпи, главным образом, в третий триместр беременности, но он может также появиться в более ранние сроки, сначала на животе и затем становится генерализованным. Данный симптом обычно имеет тенденцию усиливаться ночью и исчезает после родов (в течение 1-4 недель). Вероятно, это связано с внутрипеченочным застоем желчи, поскольку имеет место увеличение GT-гамма и щелочной фосфатазы и иногда также непосредственного уровня билирубина у данных пациенток. Зуд более часто встречается при многоплодных беременностях и может повторяться при последующих беременностях или во время применения пероральных противозачаточных средств. Дополнительно, зудящие уртикарные папулы и бляшки беременных (PUPP), наиболее общий дерматоз, ассоциированный с беременностью, не реагирует на антигистаминные препараты и часто сохраняется после родов.
Некоторые гематологические нарушения, как известно, ассоциированы c зудом. При настоящей стойкой красной полицитемии с повышенной продукцией всех трех кроветворных линий клеток пациенты типично испытывают сильный зуд, локализованный на торсе и умеренный на лице, руках и ногах, через несколько минут после контакта с теплой водой. Вызванный водой зуд (аквагеннный зуд, или зуд после ванны) может иметь место у 70% пациентов. Зуд может длиться в течение от приблизительно 15 минут до одного часа, и может быть настолько сильным, что пациенты отказываются от купания. В последние десятилетия зуд описали у пациентов с реакцией трансплантата в отношении хозяина после пересадки костного мозга.
Хроническая выработка IL-31 вызывает зуд и облысение у мышей, за которыми следует развитие повреждений кожи, напоминающих дерматит, предполагающий, что IL-31 может вызвать зуд. Смотрите Dillon S.R., et al., Nat Immunol: 5, 752 (2004). Причастность IL-31 была проверена при индукции реакции зуда двумя способами, как показано в примере 2: (i) лечение капсаицином подвергшихся действию IL-31 мышей и (ii) лечение IL-31 нокаутных мышей Tac 1, которые значительно уменьшили ноцицептивные реакции на боль из-за недостаточной экспрессии нейропептидов. В дополнение, в примере 2 было проверено, может ли нейтрализация IL-31 у получавших IL-31 мышей предотвратить зуд и облысение.
У мышей NC/Nga спонтанно развиваются AD-подобные повреждения, которые соответствуют AD человека во многих аспектах, включающих в себя клинические динамику и признаки, гистопаталогию и иммунопатологию, когда их помещают в содержащие особые патогены (non-SPF) условия в возрасте приблизительно 6-8 недель. В отличие от этого, у мышей NC/Nga, содержащихся в условиях SPF, не развиваются повреждения кожи. Тем не менее, начало спонтанных повреждений кожи и состояния расчесывания можно синхронизировать у мышей NC/Nga, помещенных в условия SPF, еженедельной внутрикожной инъекцией неочищенного антигена пылевого клеща. Смотрите Matsuoka H., et al., Allergy: 58, 139 (2003). Следовательно, развитие AD у NC/Nga является применимой моделью для оценки новых терапевтических средств для лечения AD.
В дополнение к модели NC/Nga спонтанного AD накожное повышение чувствительности у мышей при применении OVA можно также применять в качестве модели для того, чтобы вызвать зависимое от антигена эпидермальное и дермальное утолщение мононуклеарным инфильтратом в коже сенсибилизированных мышей. Данный процесс обычно совпадает с повышенными уровнями общего и специфического IgE в сыворотке, однако в данной модели, как правило, не имеет место нарушение функции кожного барьера или зуд. Смотрите Spergel J.M., et al., J Clin Invest, 101: 1614, (1998). Данный протокол можно модифицировать для того, чтобы индуцировать нарушение регуляции кожного барьера и зуд, сенсибилизируя трансгенных мышей DO11.10 OVA TCR при помощи OVA. Увеличивая количество антигенспецифических T-клеток, которые могли бы распознать сенсибилизирующий антиген, можно увеличить уровень воспаления в коже, чтобы индуцировать видимое состояние расчесывания и лихенизацию/образование чешуек на коже.
Как модель NC/Nga спонтанного AD, так и накожную модель DO11.10 с OVA можно применять для определения экспрессии IL-31 и IL-31RA при AD, а также способности описанных в настоящем описании антагонистов ингибировать, уменьшать или нейтрализовать воздействия IL-31. Описанные в настоящем описании антагонисты применимы для ингибирования расчесывания, ассоциированного с дерматитом и зудящими заболеваниями, включающими в себя атопический дерматит, узелковую почесуху и экзему. При AD состояние расчесывания вызвано сильным зудом кожи, что, как полагают, осложняет заболевание, нарушая функции кожного барьера и активируя кератиноциты, приводя к продукции хемокина и увеличенному воспалению. Многие клиницисты рассматривают AD в качестве самораспространяющегося цикла, так как повреждения, образующиеся при частом расчесывании, подвергаются воздействию инфекции и дальнейшей стимуляции антигена. Факт, что у пациентов с поражением почти полной площади поверхности тела можно наблюдать непораженную кожу в областях, которые трудно расцарапать, что придает правдоподобность данной гипотезе. Посредством предотвращения зуда введение антагонистов IL-31 или его рецептора может быть эффективным при лечении зудящих заболеваний, уменьшая вызванную IL-31 активацию кератиноцитов и неврологическую стимуляцию, таким образом нарушая связь между воспалением и зудом. Снижение зуда могло бы также уменьшить секрецию факторов нейростимуляции и уменьшить воспаление и экскориацию, связанные с постоянным расчесыванием, приводя к улучшению оценки заболевания и/или более продолжительному периоду между вспышками заболевания. В дополнение, ингибирование, уменьшение или предотвращение расчесывания само по себе может быть эффективным при лечении зудящих заболеваний, включающих в себя в качестве неограничивающих примеров атопический дерматит, узелковую почесуху и экзему, поскольку прекращение расчесывания остановит прогрессирование дерматита, развитие которого зависит от расчесывания.
Применяемый в настоящем описании термин «антитела» включает в себя поликлональные антитела, аффинно-очищенные поликлональные антитела, моноклональные антитела и антигенсвязывающие фрагменты, такие как протеолитические фрагменты F(ab')2 и Fab. Также сюда включены генетически сконструированные интактные антитела или фрагменты, такие как химерные антитела, Fv-фрагменты, одноцепочечные антитела и тому подобное, а также синтетические антигенсвязывающие пептиды и полипепиды. Нечеловеческие антитела можно гуманизировать, перенося нечеловеческие CDR в человеческие каркасный участок и константную область или встраивая все нечеловеческие вариабельные области (необязательно «маскируя» их под подобный человеческому вид посредством замены экспонированных остатков, где результатом является «облицованное» антитело). В некоторых случаях гуманизированные антитела могут сохранить нечеловеческие остатки внутри человеческих каркасных доменов вариабельных областей, чтобы усилить надлежащие характеристики связывания. Посредством гуманизированных антител можно увеличить биологический период полувыведения, и возможность появления побочных иммунных реакций при введении людям уменьшается. Кроме того, человеческие антитела можно получать в трансгенных животных помимо человека, которые сконструированы так, чтобы содержать гены иммуноглобулина человека, как описано в публикации WIPO № WO 98/24893. Предпочтительно, что эндогенные гены иммуноглобулина у таких животных инактивированы или удалены так, как при гомологичной рекомбинации.
Антитела, как полагают, специфически связываются, если 1) они проявляют пороговый уровень связывающей активности и 2) они не реагируют перекрестно в значительной степени с родственными полипептидными молекулами. Пороговый уровень связывания определяют, если антитела против IL-31 связываются при этом с полипептидом IL-31, пептидом или эпитопом с аффинностью по меньшей мере в 10 раз большей, чем аффинность связывания с контрольным полипептидом (не IL-31). Предпочтительно, чтобы антитела демонстрировали аффинность связывания (Ka) 106 M-1 или выше, предпочтительно 107 M-1 или выше, более предпочтительно 108 M-1 или выше и наиболее предпочтительно 109 M-1 или выше. Аффинность связывания может легко определить обычный специалист в данной области, например, посредством анализа Скэтчарда (Scatchard, G., Ann. NY Acad. Sci. 51: 660-672, 1949).
Не реагируют ли перекрестно в значительной степени антитела против IL-31 с родственными полипептидными молекулами, показано, например, при помощи антитела, определяющего полипептид IL-31, но не известные родственные полипептиды, применяя стандартный анализ вестерн-блотом (Ausubel et al., там же). Примеры известных родственных полипептидов, такие как известные ортологи и паралоги и сходные известные члены белкового семейства, описаны на известном уровне техники. Скрининг можно также провести, применяя нечеловеческий IL-31 и мутантный полипептид IL-31. Кроме того, антитела можно «отобрать против» известных родственных полипептидов, чтобы выделить популяцию, которая специфически связывается с полипептидами IL-31. Например, антитела, появляющиеся к IL-31, адсорбируются родственными полипептидами, прикрепленными к нерастворимой матрице; специфичные для IL-31 антитела будут протекать через матрицу при надлежащих буферных условиях. Скрининг позволяет выделить поликлональные или моноклональные антитела, не реагирующие перекрестно с известными близкородственными полипептидами (Antibodies: A Laboratory Manual, Harlow and Lane (eds.), Cold Spring Harbor Laboratory Press, 1988; Current Protocols in Immunology, Cooligan, et al. (eds.), National Institutes of Health, John Wiley and Sons, Inc., 1995). Скрининг и выделение специфических антител хорошо известны в данной области. Смотрите Fundamental Immunology, Paul (eds.), Raven Press, 1993; Getzoff et al., Adv. in Immunol. 43: 1-98, 1988; Monoclonal Antibodies: Principles and Practice, Goding, J.W. (eds.), Academic Press Ltd., 1996; Benjamin et al., Ann. Rev. Immunol. 2: 67-101, 1984. Специфически связывающиеся антитела против IL-31 можно определить большим количеством способов в данной области, и они описаны ниже.
Получение моноклональных антител хорошо известно специалисту в данной области. Очищенный зрелый рекомбинантный полипептид IL-31 человека (аминокислотные остатки с 27 (Leu) до 167 (Thr) SEQ ID NO:2) или мышиный ортолог можно применять для получения моноклональных антител.
Эффект введения антагонистов опосредованной IL-31 сигнальной трансдукции можно определить in vivo по уменьшению, ингибированию, предотвращению, снижению до минимума, нейтрализации воспаления, кожного или дермального утолщения, увеличения количества лимфоцитов и акантоза, например, и других симптомов или комбинаций симптомов, таких как индекса распространенности и тяжести экземы (EASI), которые очевидны для специалиста в данной области. Дополнительные эффекты могли бы включать в себя изменение или уменьшение продукции цитокинов или хемокинов поврежденной кожей, снижение оценки при кожной пробе на атопию и снижение высвобождения растворимых факторов, таких как цитокины, хемокины или нейропептиды, как определяется внутрикожным микродиализом или другими способами. Оценку степени зуда или боли можно определить, применяя клинически одобренный инструментарий или средства, такие как визуальная аналоговая шкала. Частоту расчесывания можно проверить счетчиками движения конечности, пьезоэлектрическими устройствами преобразователей, прикрепленными к ногтям, или при помощи замедленной инфракрасной фотографии или видеографии ночного расчесывания у пациентов. Другие способы оценки уменьшения боли или зуда очевидны для специалиста в данной области.
Моноклональные антитела, очищенные от среды культивирования ткани, характеризуют по их эффективности в ELISA для количественного определения рекомбинантного и нативного IL-31 человека. Антитела отбирают и проводят количественный анализ.
Моноклональные антитела, очищенные от среды культивирования ткани, характеризуют по их способности блокировать или уменьшать активность связывания с рецептором («анализ нейтрализации») очищенного рекомбинантного huIL-31 в нервных клетках, экспрессирующих IL-31Ra и OSMRb. Большое количество «нейтрализующих» моноклональных антител идентифицировано таким образом. Гибридомы, экспрессирующие описанные нейтрализующие моноклональные антитела против IL-31 человека, можно затем поместить в патентный депозитарий американской коллекции типовых культур тканей (ATCC; Манассас, Вирджиния) в качестве первоначальных депонирований по условиям Будапештского договора.
Пять крысиных гибридом против мыши были получены подобным способом и им дали следующие ниже обозначения клонов: клон 271.9.4.2.6, клон 271.26.6.6.1, клон 271.33.1.2.2, клон 271.33.3.2.1 и клон 271.39.4.6.5. Моноклональные антитела, продуцируемые данными клонами, характеризовали множеством способов, включающих в себя связывание (то есть определение, могло ли каждое антитело ингибировать связывание любого другого связывания), относительную аффинность и нейтрализацию. Моноклональные антитела, по-видимому, попадают в две отдельные группы, причем клон 271.33.3.2.1 связывается с особым эпитопом, чем другие четыре.
Моноклональные антитела в среде культивирования ткани характеризуют по их способности блокировать или уменьшать связывание с рецептором, когда они растут в присутствии очищенных рекомбинантных белков IL-31 человека.
Аффинность связывания моноклональных антител можно вычислить. Козье специфическое антитело IgG-Fc-гамма против белка крысы (Jackson) иммобилизируют на чипе CM5 Biacore. Анализ оптимизируют для связывания каждого mAb на поверхности захвата против белка крысы, и затем ряд концентрации IL-31 вводят сквозь mAb, чтобы наблюдать ассоциацию (Ka) и диссоциацию (Kd). После каждой партии поверхность снова восстанавливают до антитела против крысы при помощи 2 инъекций 20 мМ HCl. Данные получали для каждой партии и программное обеспечение для анализа (программное обеспечение BIAevaluation, версия 3.2, Pharmacia BIAcore, Упсала, Швеция) применяли, чтобы оценить кинетику связывания антитела против IL-31 с белком IL-31.
Биохимическое подтверждение, что молекула-мишень, распознаваемая предполагаемыми mAb против IL-31, является действительно IL-31, проводят по стандартному способу иммунной преципитации, после чего следует анализ SDS-PAGE или методики вестерн-блоттинга, и тот и другие применяющиеся для растворимых мембранных препаратов из трансфецированных IL-31 по сравнению с нетрансфецированными Baf3-клетками. mAb проверяют на их способность специфически образовывать иммунопреципитат или вестерн-блоттинг с растворимым белком IL-31-muFc.
Моноклональные антитела к IL-31 описаны в находящейся в общедоступной заявке на патент США 11/430066, поданной 8 мая 2006 г., опубликованной заявке на патент США номер 2006-0275296. Данные моноклональные антитела очищали от среды культивирования ткани, характеризовали по их способности блокировать или ингибировать способность IL-31 связаться с его рецептором в анализе нейтрализации. Двадцать «нейтрализующих» моноклональных антител идентифицировали таким образом. Моноклональные антитела, продуцируемые данными клонами, характеризовали большим количеством способов, включающих в себя связывание (то есть определение, могло ли каждое антитело ингибировать связывание любого другого связывания), относительную аффинность и нейтрализацию. Десять хороших нейтрализующих антител, по-видимому, находятся в одной и той же группе с другими моноклональными антителами, группирующимися на три отдельных группы. При этом восемь из хороших нейтрализующих антител представляют собой изотип IgG1, и два другие представляют собой изотип IgG2a. Такие моноклональные антитела могут представлять собой IgG1 или IgG4, чтобы минимизировать связывание комплемента и активность ADCC.
Гибридомы, экспрессирующие описанные выше нейтрализующие моноклональные антитела к IL-31 человека, поместили в патентный депозитарий Американской Коллекции Типовых Культур Тканей (ATCC; Манассас, Вирджиния) в качестве первоначальных депонирований по условиям Будапештского договора, и им были даны следующие ниже инвентарные номера: обозначение патентного депонирования в ATCC PTA-6815, депонированный 29 июня 2005 года; обозначение патентного депонирования в ATCC PTA-6816, депонированный 29 июня 2005 года; обозначение патентного депонирования в ATCC PTA-6829, депонированный 6 июля 2005 года; обозначение патентного депонирования в ATCC PTA-6830, депонированный 6 июля 2005 года; обозначение патентного депонирования в ATCC PTA-6831, депонированный 6 июля 2005 года; обозначение патентного депонирования в ATCC PTA-6871, депонированный 19 июля 2005 года; обозначение патентного депонирования в ATCC PTA-6872, депонированный 19 июля 2005 года; обозначение патентного депонирования в ATCC PTA-6875, депонированный 19 июля 2005 года; и обозначение патентного депонирования в ATCC PTA-6873, депонированный 19 июля 2005 года.
Гибридому, экспрессирующую описанные выше нейтрализующие моноклональные антитела к IL-31 мыши, поместили в патентный депозитарий Американской Коллекции Типовых Культур Тканей (ATCC; Манассас, Вирджиния) в качестве первоначальных депонирований по условиям Будапештского договора, и ей был присвоен следующий ниже инвентарный номер: обозначение патентного депонирования в ATCC PTA-6874, депонированный 19 июля 2005 года. Моноклональные антитела, продуцируемые клонами данной гибридомы, можно культивировать в питательной среде из 90% среды Дульбекко, модифицированной по способу Исков, с 2 мМ L-глутамина, 100 мкг/мл пенициллина и 100 мкг/мл сульфата стрептомицина и 10% фетальной сыворотки клона I (Hyclone Laboratories). Клоны можно размножить из исходных культур при концентрации 2×105 клеток/мл и поддерживая концентрацию в диапазоне от 1×105 до 5×105 клеток/мл при 37°C и 5-6% CO. Клетки можно адаптировать к бессывороточным условиям при последующих переносах. Клетки, которые замораживают, хранят в 90% сыворотке, 10% ДМСО и хранят в газовой фазе в аппарате с замораживанием погружением в жидкий азот.
Антагонисты IL-31, полученные описанными в настоящем описании способами, можно проверить в отношении нейтрализации, ингибирования, уменьшения, антагонистического действия различными способами. В дополнение, нейтрализацию можно исследовать, определяя уменьшение продукции провоспалительных хемокинов, таких как TARC и MDC, культурами кератиноцитов в присутствии лиганда и моноклонального антитела. Другие биомаркеры, такие как MCP-1, MIP1a, TARC, MCP-1, MDC, IL-6, IL-8, I-309, SCYA19, MPIF-1, TECK, MIP-1b, SCYB13, GROa/MGSA, CTACK, SCCA1/серпин B3, TSLP и NT-4, можно также применять. Нейтрализацию можно также определить в описанных в настоящем описании моделях in vivo.
Биоактивные антагонисты или конъюгаты антител, описанные в настоящем описании, можно доставлять внутривенно, внутриартериально или внутрипротоково, подкожно, местно или их можно вводить местно в намеченный участок действия.
Для антагонистов по настоящему изобретению можно определить их способность связывать лиганд IL-31, как определено в любой из описанных в настоящем описании модели in vivo, включающих в себя в качестве неограничивающих примеров модель NcNga, модель накожного Ova, модель хронической гиперчувствительности, хроническую гаптеновую модель, модель потока кальция, модель аллодинии.
Дополнительные модели для определения ингибиторных эффектов антител против IL-31 известны специалисту в данной области и описаны в настоящем описании и описаны Umeuchi, H. et al., European Journal of Pharmacology, 518: 133-139, 2005 и Yoo, J. et al., J. Experimental Medicine, 202: 541-549, 2005.
Мышиные модели для определения нейрогенного воспаления известны в данной области. Смотрите, например, Sweitzer, S. M., et al., J. Neuroimmunology 125: 82-93; 2002 и Honore, P., et al., Neuroscience, (98): 585-598, 2000. Также смотрите, Yonehara, N. and Yoshimura M., Pain, 2001 (92/1-2): pp. 259-265).
В рамках аспектов изобретения, в изобретении предлагаются способы лечения воспаления в нейронной ткани млекопитающих; способы лечения боли у млекопитающих; способы противодействия вызванной IL-31 сигнальной трансдукции в клетках ганглия заднего корешка; способы лечения симптомов, ассоциированных с ожогом; способы лечения симптомов, ассоциированных с вирусной инфекцией и для того, чтобы предотвратить повторную активацию вирусной инфекции; и способы лечения боли, ассоциированной с воспалительными заболеваниями кишечника. В варианте осуществления воспалительное заболевание кишечника представляет собой болезнь Крона.
В вариантах осуществления данных аспектов в изобретении предлагается способ, включающий в себя добавление антагониста IL-31 в нейронную ткань, где воспаление, боль, сигнальная трансдукция в ганглии заднего корешка, вирусная инфекция или ее повторная активация или боль в ткани после ожога или боль, ассоциированная с воспалительными заболеваниями кишечника, уменьшается, ограничивается, предотвращается, сводится до минимума или нейтрализуется.
В других вариантах осуществления антагонист IL-31 связывается с полипептидом, содержащим аминокислотную последовательность, как указано в SEQ ID NO: 2 с 27 остатка по 164 остаток. В других вариантах осуществления антагонист выбран из антиидиотипических антител; фрагментов антител; химерных антител и гуманизированных антител. В другом варианте осуществления антагонист представляет собой антитело. В других вариантах осуществления антитело представляет собой моноклональное антитело. В других вариантах осуществления антитело специфически связывается с полипептидом, содержащим аминокислотную последовательность SEQ ID NO: 2, и где полипептид способен связываться с моноклональным антителом, продуцируемым гибридомой, выбранной из группы, состоящей из: a) обозначение патентного депонирования в ATCC PTA-6815; b) обозначение патентного депонирования в ATCC PTA-6816; c) обозначение патентного депонирования в ATCC PTA-6829; d) обозначение патентного депонирования в ATCC PTA-6830; e) обозначение патентного депонирования в ATCC PTA-6831; f) обозначение патентного депонирования в ATCC PTA-6871; g) обозначение патентного депонирования в ATCC PTA-6872; h) обозначение патентного депонирования в ATCC PTA-6875 и i) обозначение патентного депонирования в ATCC PTA-6873. В другом варианте осуществления моноклональное антитело выбрано из группы антител, где гибридома, продуцирующая антитело, выбрана из: a) обозначение патентного депонирования в ATCC PTA-6815; b) обозначение патентного депонирования в ATCC PTA-6829; c) обозначение патентного депонирования в ATCC PTA-6816; d) обозначение патентного депонирования в ATCC PTA-6871 и e) обозначение патентного депонирования в ATCC PTA-6830. В другом варианте осуществления моноклональное антитело выбрано из группы антител, где гибридома, продуцирующая антитело, выбрана из: a) обозначение патентного депонирования в ATCC PTA-6872; b) обозначение патентного депонирования в ATCC PTA-6873; c) обозначение патентного депонирования в ATCC PTA-6875 и d) обозначение патентного депонирования в ATCC PTA-6831.
В других вариантах осуществления нейронная ткань включает в себя ганглий заднего корешка или ткань спинного мозга.
ПРИМЕРЫ
Пример 1
Гибридизация in situ IL-31RA, IL-31 и pOSMRb в нейронных тканях
Пять человеческих образцов ткани головного мозга и образец спинного мозга, все из одного и того же индивидуума, и ганглии заднего корешка (DRG) из другого пациента анализировали в данном исследовании.
Применяемыми зондами являлись зонды для IL-31RA, IL-31 и OSMR-бета.
Результаты показаны в таблице 1:
Результаты анализа ISH
Срезы головного мозга: Не наблюдали никакого обнаружимого количества сигнала во всех областях головного мозга для всех трех зондов. Имело место необоснованное окрашивание pOSMRb в субпопуляции нейронов в гипоталамусе. Необоснованность может быть вызвана очень низким уровнем экспрессии pOSMRb, который находится около уровня обнаружения.
Спинной мозг: Имело место положительное окрашивание в одной области спинного мозга. Информация о возможной локализации или ориентации среза спинного мозга недоступна. Сигнал, по-видимому, находится в передней (вентральной) части спинного мозга. Противоположная сторона/область (также передняя) была отрицательна. Положительный сигнал, по-видимому, заключен в субпопуляции более крупных нейронов. Как IL-31RA, так и pOSMRb показали схожие типы экспрессии в данной области. IL-31 оказался отрицателен.
Ганглий заднего корешка (DRG): Субпопуляция униполярных нейронов в DRG оказалась положительной и в отношении IL-31RA, и в отношении pOSMRb. Небольшие амфициты оказались отрицательными. IL-31 отсутствовал во всех клетках, включая нейроны.
Таким образом, антагонист IL-31 можно применять для облегчения симптомов, ассоциированных с нейрогенной стимуляцией. Также антагонисты IL-31 можно применять для лечения воспаления и боли, вызванных нервной стимуляцией клетки, такой как стимуляция ганглия заднего корешка, и можно определить как уменьшение, ограничение, сведения к минимуму, предотвращение или нейтрализация боли и воспаления.
Пример 2
Участие IL-31 в индукции ответа в виде зуда
A. Способы I (Лечение капсаицином мышей, подвергаемых воздействию IL-31)
Животных BALB/c в возрасте десяти недель обезболивали и вводили им болеутоляющее средство длительного действия, гидрохлорид бупранорфина, подкожно в количестве 0,1 мг/кг до инъекции 0,25 мл 4 мг/мл раствора капсаицина в смеси 10% этанол + 10% Tween-80 в солевом растворе подкожно в заднюю часть шеи. Животным сохраняли обезболивание в течение по меньшей мере 30 минут после введения нейротоксина. Через сорок восемь часов подкожно имплантировали осмотические насосы, рассчитанные на работу в течение 14 дней, для непрерывного введения 20 мкг/день IL-31 в течение 14 дней. Мышей проверяли ежедневно в течение 6 дней в отношении облысения и зуда, применяя следующие ниже критерии: 0 = нет расчесывания, животное кажется нормальным, 1 = утончение шерстного покрова на небольших участках, замечено расчесывание, 2 = незначительное выпадение волос (небольшие участки), расчесывание, 3 = умеренное выпадение волос, расчесывание и 4 = сильное выпадение волос, повышенное расчесывание.
Результаты показывают, что в то время, как для не получавших капсаицин мышей показана средняя оценка расчесывания/выпадения волос 2,625 через три дня введения IL-31, для получавших капсаицин мышей показана значительно более низкая оценка 1. Таким образом, мыши, получавшие капсаицин до введения IL-31, показали и задержку в частоте расчесывания, и выпадения волос, и более низкую оценку по интенсивности расчесывания и выпадения волос за шесть дней эксперимента. Такие данные позволяют предположить, что IL-31 действительно индуцирует какой-то нейронный компонент, который вносит вклад в облысение и зуд, вызванный IL-31. Следовательно, нейтрализация IL-31 может уменьшить частоту возникновения и интенсивность зуда, и, следовательно, дерматит у пациентов, страдающих от кожных воспалений, которые влекут за собой зуд.
B. Способы II
Мыши, которые являются гомозиготными по отсутствию гена Tac1, не экспрессируют никакого обнаружимого количества вещества P или нейрокинина A. У таких мышей в значительной степени уменьшены ноцицептивные болевые реакции на стимулы от умеренных до интенсивных, и следовательно, они являются применимым средством для изучения вклада тахикининовых пептидов в появление боли/зуда и состояния воспалительных заболеваний. Нокаутным по Tac1 мышам в возрасте двенадцати недель имплантировали осмотические насосы, рассчитанные на работу в течение 14 дней, подающих 1 мкг/день белка IL-31, и ежедневно наблюдали за облысением и зудом, применяя следующие ниже критерии: 0 = нет расчесывания, животное кажется нормальным, 1 = утончение шерстного покрова на небольших участках, замечено расчесывание, 2 = незначительное выпадение волос (небольшие участки), расчесывание, 3 = умеренное выпадение волос, расчесывание и 4 = сильное выпадение волос, повышенное расчесывание.
Результаты данного анализа показывают, что мыши с дефицитом Tac1 были менее восприимчивы к вызванному IL-31 расчесыванию/выпадению волос по сравнению с контрольными мышами дикого типа. В то время, как у 100% мышей дикого типа (10/10) обнаруживали признаки расчесывания и выпадения волос при 6-дневном введении IL-31, только 33,3% (2/6) мышей с дефицитом Tac1 показывали признаки расчесывания и выпадения волос за тот же самый период времени. Такие данные показывают, что IL-31 индуцирует нейронный компонент, который вносит вклад в появление фенотипа с расчесыванием/выпадением волос у мышей, получавших IL-31, и нейтрализация IL-31 может уменьшить частоту возникновения и интенсивность расчесывания в отношении дерматита.
C. Способы III (Введение нейтрализующего IL-31 антитела)
Нормальным самкам мышей BALB/c (CRL) в возрасте от приблизительно 8 до 12 недель подкожно имплантировали осмотические насосы (Alzet, #2002), рассчитанные на работу в течение 14 дней, подающие 1 мкг/день mIL-31. Группам мышей вводили внутрибрюшинные (в/б) инъекции крысиного моноклонального антитела против IL-31 мыши в количестве 10 мг/кг (200 мкг/мышь) дважды в неделю, начиная с 1 недели до подачи IL-31. Контрольным группам мышей вводили в/б инъекции носителя (PBS/0,1% BSA) с идентичными режимами дозирования. Мышей оценивали в отношении облысения и зуда, применяя следующие ниже критерии: 0 = нет расчесывания, животное кажется нормальным, 1 = утончение шерстного покрова на небольших участках, замечено расчесывание, 2 = незначительное выпадение волос (небольшие участки), расчесывание, 3 = умеренное выпадение волос, расчесывание и 4 = сильное выпадение волос, повышенное расчесывание.
Во всех экспериментах мыши, получившие крысиное mAb против mIL-31, показывали замедление начала развития симптомов от приблизительно 5 до 7 дней и более низкую общую оценку степени облысения и зуда. Во всех группах получившие mAb мыши (независимо от частоты введения дозы или концентрации), с появившимся облысением и зудом, сходны с контрольными мышами на 13 день исследования. Такие данные предполагают, что нейтрализация IL-31 может задерживать начало развития реакции расчесывание/выпадение волос, вызванное IL-31.
Пример 3
Люциферазный анализ рецептора IL-31RA/OSMR-бета
Плазмиду KZ134 конструировали с применением комплементарных олигонуклеотидов, которые содержали связывающий элемент фактора транскрипции STAT из 4 генов, которые включали в себя индуцируемый Sis элемент c-fos (m67SIE или hSIE) (Sadowski, H. et al., Science 261: 1739-1744, 1993), p21 SIE1 из гена p21 WAF1 (Chin, Y. et al., Science 272: 719-722, 1996), элемент реакции молочной железы гена β-казеина (Schmitt-Ney, M. et al., Mol. Cell. Biol. 11: 3745-3755, 1991) и индуцируемый STAT элемент из гена Fcg RI (Seidel, H. et al., Proc. Natl. Acad. Sci. 92: 3041-3045, 1995). Данные олигонуклеотиды содержат совместимые Asp718-XhoI концы, и их замыкали, применяя стандартные способы, в люциферазный репортерный вектор светлячка-реципиента с промотором c-fos (Poulsen, L.K. et al., J. Biol. Chem. 273: 6229-6232, 1998), расщепленный теми же самыми ферментами и содержащий селектируемый маркер в отношении неомицина. Плазмиду KZ134 применяли в стабильно трансфецируемых клетках BaF3, применяя стандартные способы трансфекции и селекции, чтобы получить клеточную линию BaF3/KZ134.
Сконструировали стабильную индикаторную клеточную линию BaF3/KZ134, экспрессирующую полноразмерный рецептор IL-31RA или IL-31RA/OSMR-бета. Клоны разбавляли, высевали и отбирали, применяя стандартные методики. Проводили скрининг клонов посредством люциферазного анализа (смотрите B, ниже), применяя кондиционированную среду IL-31 человека или очищенный белок IL-31 в качестве индуктора. Отбирали клоны с наиболее высокой люциферазной реакцией (посредством STAT люциферазы) и наиболее низким уровнем фона. Отбирали стабильные трансфецированные клеточные линии. Клеточные линии называли BaF3/KZ134/IL-31RA или BaF3/KZ134/IL-31RA/OSMR-бета в зависимости от трансфецированных в клеточную линию рецепторов.
Сходным образом, клеточные линии BHK также конструировали, применяя описанный в настоящем описании способ, и применяли в описанном в настоящем описании люциферазном анализе. Клеточные линии называли BHK/KZ134/IL-31RA или BHK/KZ134/IL-31RA/OSMR-бета в зависимости от трансфецированных в клеточную линию рецепторов.
Клетки BaF3/KZ134/IL-31RA и BaF3/KZ134/IL-31RA/OSMR-бета центрифугировали и промывали несодержащей mIL-3 средой. Клетки центрифугировали и промывали 3 раза, чтобы гарантировать удаление mIL-3. Затем клетки подсчитывали в гемоцитометре. Клетки помещали в планшеты 96-луночного формата в количестве приблизительно 30000 клеток на лунку в объеме 100 мкл на лунку, применяя несодержащую mIL-3 среду. Ту же самую процедуру применяли для нетрансфецированных клеток BaF3/KZ134 для применения в качестве контроля в последующем анализе. Клетки BHK/KZ134/IL-31RA или BHK/KZ134/IL-31RA/OSMR-бета помещали в планшеты 96-луночного формата в количестве 15000 клеток на лунку в 100 мкл среды. Исходные клетки BHK/KZ134 применяли в качестве контроля.
Активацию STAT клеток BaF3/KZ134/IL-31RA, BaF3/KZ134/IL-31RA/OSMR-бета, BHK/KZ134/IL-31RA или BHK/KZ134/IL-31RA/OSMR-бета оценивают, применяя кондиционированную среду или очищенный белок. Сто микролитров разбавленной кондиционированной среды или белка добавляют к клеткам BaF3/KZ134/IL-31RA, BaF3/KZ134/IL-31RA/OSMR-бета, BHK/KZ134/IL-31RA или BHK/KZ134/IL-31RA/OSMR-бета. Анализ, применяя кондиционированную среду, проводят параллельно на нетрансфецированных клетках BaF3/KZ134 или BHK/KZ134 в качестве контроля. Объем для полного анализа составляет 200 мкл. Анализируемые планшеты инкубируют при 37°C, 5% CO2 в течение 24 часов, после чего клетки BaF3 осаждают центрифугированием при 2000 об./мин в течение 10 мин, и среду отсасывают и добавляют 25 мкл лизирующего буфера (Promega). Для клеточных линий BHK стадия центрифугирования не является обязательной, поскольку клетки склеены. Через 10 минут при комнатной температуре планшеты анализируют в отношении активации репортерной конструкции STAT, считывая их в люминометре (Labsystems Luminoskan, модель RS), в котором добавлено 40 мкл субстрата для люциферазного анализа (Promega) при пятисекундной интеграции.
Пример 4
Люциферазный анализ трансформированных эпителиальных клеточных линий человека посредством транзиторного инфицирования аденовирусным репортерным геном STAT/SRE
Ингибирование, уменьшение и/или нейтрализацию активности IL-31 можно определить посредством люциферазного анализа. Например, трансформированную клеточную линию человека можно высевать в 96-луночные планшеты с плоским дном в количестве 10000 клеток/лунку в стандартной питательной среде, как определено для каждого типа клеток. На следующий день клетки инфицируют аденовирусной репортерной конструкцией KZ136 при множественности заражения 5000. Репортер KZ136 содержит элементы STAT в дополнение к элементу реакции на сыворотку. Полный объем составляет 100 мкл/лунку, применяя DMEM, дополненную 2 мМ L-глутамином (GibcoBRL), 1 мМ пируватом натрия (GibcoBRL) и 1× добавкой инсулин-трансферрин-селен (GibcoBRL) (далее обозначаемые как бессывороточные среды). Клетки культивируют в течение ночи.
На следующий день среду удаляют и заменяют 100 мкл индукционной среды. Индукционная среда представляет собой IL-31 человека, разведенный в бессывороточных средах при концентрациях 100 нг/мл, 50 нг/мл, 25 нг/мл, 12,5 нг/мл, 6,25 нг/мл, 3,125 нг/мл и 1,56 нг/мл. Применяли положительный контроль 20% FBS для подтверждения достоверности анализа и для гарантии, что заражение аденовирусом проходит благополучно. Клетки индуцируют в течение 5 часов, после чего среду отсасывают. Затем клетки промывают PBS в количестве 50 мкл/лунку и впоследствии лизируют в 1× буфере для лизиса клеток в количестве 30 мкл/лунку (Promega). Через 10 минут инкубирования при комнатной температуре лизат в количестве 25 мкл/лунку переносят в непрозрачные белые 96-луночные планшеты. Планшеты затем считывают в люминометре, применяя 5-секундную интеграцию с применением инъекции люциферазного субстрата в количестве 40 мкл/лунку (Promega).
Пример 5
Анализ IL-31 в тканях толстой кишки при воспалительных заболеваниях кишечника
A) Иммуногистохимия IL-31
Поликлональное антитело (кроличье против IL-31 человека CEE, аффинно очищенное до 1,0 мг/мл) применяли для обнаружения IL-31 человека в желудочно-кишечных тканях от пациентов с воспалительными заболеваниями кишечника посредством системы определения основанной на ABC-elite. Нормальную сыворотку кролика, протеин A, очищенный до 1,66 мг/мл, применяли в качестве отрицательного контроля, применяя один и тот же протокол и концентрации антител.
Протокол был следующим: ABC-HRP Elite (Vector Laboratories, PK-6100); восстановление мишени (ph 9) в течение 20' выпаривания, 20' охлаждения для RT; блокада белка в течение 30'; первичное Ab (1:1000 - 2500) в течение 60'; вторичное Ab (Bi:ant-Rabbit) в течение 45'; комплекс ABC-HRP в течение 45' и субстрат DAB, как рекомендовано.
В данном исследовании всего 19 индивидуальных ЖК тканей анализировали при помощи кроличьего поликлонального антитела против IL-31 человека. В данной группе находилось пять образцов толстой кишки из нормальной ткани, соседствующей с IBD или раковыми тканями. В девяти образцах диагностировали болезнь Крона и в пяти - язвенный колит. В целом, кажется, что существует больше клеток, положительных в образцах с болезнью Крона, чем в нормальных тканях, соседствующих с IBD или раковыми тканями или тканях с язвенным колитом. Преобладающее количество клеток с сигналом в образцах с болезнью Крона расположены в собственной пластинке слизистой и подслизистой оболочке, причем инфильтрирующие клетки показывают сигнал между пучками гладких мышц. В гранулемах, множество более крупных клеток в центре узелкового утолщения положительны, однако кортикальный слой данных узелков и пейеровы бляшки кажутся отрицательными. Эпителий кишечных желез иногда положителен. В образцах с язвенным колитом существует небольшое количество рассеянных клеток в подслизистой оболочке, и инфильтрирующие клетки между пучками гладких мышц положительны. Процент положительных клеток в образцах с язвенным колитом меньше процента положительных клеток в образцах с болезнью Крона, но похож или немного выше процента положительных клеток из «нормальных» образцов. Клетки в собственной пластинке слизистой при язвенном колите в основном отрицательны. В заключение, данное исследование показывает, IL-31 обладает повышенной регуляцией в ЖК образцах с болезнью Крона. По-видимому, в данном исследовании, IL-31 показывает сходные профили экспрессии в образцах с язвенным колитом и «нормальных» контрольных образцах.
B) Гибридизация IL-31 in situ
Подгруппу тканей также анализировали, применяя гибридизацию in situ (ISH). При ISH мРНК IL-31 обнаруживали в нескольких инфильтрирующих клетках в подслизистой оболочке и жировых тканях. Применяя IHC, авторы изобретения заметили, что белок IL-31 положительно окрашен в упомянутой раннее популяции клеток, а также и в клетках собственной пластинки слизистой и центрах гранулем. Различие между данными двумя исследованиями можно было бы объяснить чувствительностью анализа.
Пример 6
Анализ IL-31RA в тканях толстой кишки при воспалительных заболеваниях кишечника
A) Иммуногистохимия IL-31RA
Поликлональное антитело (кроличье CEE против IL-31RA человека (версия 4), аффинно очищенное до 1,33 мг/мл) применяли для обнаружения IL-31RA человека в желудочно-кишечных тканях пациентов с воспалительными заболеваниями кишечника посредством системы определения основанной на ABC-elite. Нормальную сыворотку кролика, протеин A, очищенный до 1,66 мг/мл, применяли в качестве отрицательного контроля, применяя один и тот же протокол и концентрации антител. Кроличье антитело против IL-31RA человека (версия 4) применяли в соотношении 1:2000 (665 нг/мл).
Протокол был следующим: ABC-HRP Elite (Vector Laboratories, PK-6100); восстановление мишени (ph 9) в течение 20' выпаривания, 20' охлаждения для RT; блокада белка в течение 30'; первичное Ab (1:2000) в течение 60'; вторичное Ab в течение 45'; комплекс ABC-HRP в течение 45'; и DAB + Dako Cytomation в течение 10'.
В данном исследовании всего 19 индивидуальных ЖК тканей анализировали при помощи кроличьего антитела СЕЕ против IL-31RA человека (версия 4). В данной группе находилось приблизительно пять образцов толстой кишки из нормальной ткани, соседствующей с IBD или раковыми тканями. В девяти образцах диагностировали болезнь Крона и в пяти - язвенный колит. В целом, кажется, что существует больше клеток, положительных в образцах с болезнью Крона, чем в нормальных тканях, соседствующих с IBD или раковыми тканями или тканях с язвенным колитом. Положительные клетки в образцах с болезнью Крона, в основном, расположены в соединительной ткани подслизистой оболочки. Узелки гранулемы отрицательны. Иногда присутствует слабый эпителиальный сигнал в образцах с болезнью Крона. Не было никакого определяемого сигнала в образцах с язвенным колитом (UC). Несколько клеток в подслизистой оболочке окрашивались положительно при IHC в отношении белка IL-31RA.
B) Гибридизация IL-31RA in situ
В предыдущем исследовании, применяя ISH, изучали пять тканей, три из которых представляли собой толстую кишку с болезнью Крона. В данных тканях с болезнью Крона мРНК IL-31RA в значительной степени обладала повышенной регуляцией по сравнению с их нормальными аналогами, и сигнал локализован в кортикальной части узлов гранулемы и во множестве инфильтрирующих клеток в соединительной ткани подслизистой оболочки и областях жировой ткани. Возможные причины несоответствия между IHC и анализом in situ включают в себя изменяющуюся экспрессию мРНК, продолжительность процессирования белка, стабильность IL-31RA и/или различия в чувствительности между двумя анализами.
Пример 7
Исследования вызванного DSS-колита у трансгенных мышей EµLck IL-31
Трансгенных EµLck IL-31 и нетрансгенных однопометных контрольных мышей проверяли в вызванной декстрансульфатом натрия (DSS) модели воспаления слизистой оболочки, чтобы обнаружить возможные различия в восприимчивости к заболеванию и его тяжести. У нормальных мышей, получавших 2-3% DSS в питьевой воде, проявлялись симптомы и патология, которая воспроизводила воспалительное заболевание кишечника человека (Смотрите Strober, Fuss and Blumberg, Annu. Rev. Immunol. 2002). Механистически, DSS разрушает эпителиальный барьер слизистой оболочки толстого кишечника, что вызывает последующее воспаление. В результате такого воспаления получавшие DSS мыши теряют массу тела, и у них развивается диарея. За мышами наблюдали в отношении тяжести колита, применяя индекс активности заболевания (DAI), который является совокупной оценкой, основанной на массе тела, консистенции стула и присутствия крови в стуле. DSS можно применять для того, чтобы вызвать острые или хронические формы колита. Острый колит вызывают посредством ведения DSS (2% или 3% в исследовании авторов изобретения) с питьевой водой в период от 0 дня до 7 дня, в то время как хронический колит вызывают посредством ведения DSS с питьевой водой в течение 5 дней, после чего следует фаза выздоровления от 7 до 12 дней перед повторным введением DSS.
Проводили четыре исследования трансгенных мышей EµLck IL-31. Независимо от того, применяли ли острую или хроническую модель DSS, трансгенные мыши EµLck IL-31 быстрее теряли больше массы тела по сравнению с однопометными контрольными мышами. Фактически, в 3 из 4 исследованиях трансгенные мыши IL-31 продемонстрировали значительно бóльшую потерю веса по сравнению с контролями (p<0,001, p=0,011). Дополнительно, трансгенные мыши обладали значительно более короткими толстыми кишками по сравнению с контролями дикого типа (p<0,05). Оценка DAI была значительно выше для трансгенных по IL-31 мышей по сравнению с нетрансгенными контролями в исследовании хронического колита (p<0,001).
Для того, чтобы определить, могло ли системное введение IL-31 влиять на развитие вызванного DSS колита у нормальных нетрансгенных мышей, авторы изобретения имплантировали животным осмотические насосы, подающие ежедневную дозу IL-31 или носителя (PBS, 0,1% BSA) до введения DSS. В одном исследовании поколение N3, нетрансгенным мышам (B6C3F2 × C57BL/6) подкожно имплантировали насосы, которые подавали либо 20 мкг/день IL-31, либо носитель во время курса введения DSS. Не было никаких различий в потере веса, оценке DAI или длине толстой кишки между получавшими IL-31 мышами по сравнению с мышами, получавшими носитель. Подобное исследование подачи насосом также проводили на нормальных мышах C57BL/6; мышам имплантировали насосы, которые подавали 10 мкг/день IL-31 или носителя, и давали им 2% DSS в остром режиме. Снова не было никаких различий между мышами по любому из параметров DSS-колита, имплантировали ли насос, подающий IL-31, или носитель. В заключение, исследование острого колита с 2% DSS проводили на мышах с дефицитом IL-31RA (IL-31RA-/-). Снова не было никаких различий в потере веса, оценке DAI или длине толстой кишки между мышами с дефицитом IL-31RA и контролями дикого типа.
В заключение IL-31, по-видимому, непосредственно не влияет на воспаление слизистой оболочки, вызванное DSS, так как системное введение IL-31 нормальным мышам в исследованиях острого колита не обладало никаким воздействием на последствие заболевания. Трансгенные по IL-31 животные, возможно, более восприимчивы к вызванному DSS колиту в результате стресса, вызванного трансгенным фенотипом. Тем не менее, трансгенные мыши EμLck IL-31 характеризуются увеличенным количеством активизированных CD4+ и CD8+ T-клеток в периферических лимфатических узлах (Dillon, et al., 2004), и повышенная восприимчивость к вызванному DSS колиту, наблюдаемая у трансгенных мышей EμLck IL-31, может являться следствием наличия данных активизированных лимфоцитов.
Пример 8
Эффекты терапии против IL-31 при получении образцов дермальной межклеточной жидкости при помощи микродиализа
Микродиализ можно применять для молекул по настоящему изобретению для меры непосредственного анализа биодоступности и распределения антител в коже. Микродиализ применяют для сбора и анализа межклеточной жидкости. Антитело в межклеточной жидкости можно определить, применяя видоспецифичные перекрестносшитые с гранулами фирмы Люминекс антитела против IgG. Далее оценку свободных от связывающих IgG IL-31 проводят, применяя в качестве вторичного антитела антитело против IL-31, а не против IgG. 2. Оценивают провоспалительные цитокины и хемокины, продуцируемые при активации IL-31 кератиноцитов и/или ганглия заднего корешка. Смотрите British J. Dermatology 142(6); 1114-1120, (2000); J. Neurol. Neurosurg. Psychiatry 73; 299-302, (2002); Am J. Physiol Heart Circ. Physiol 286; 108-112, (2004); Neuroscience Letters 230; 117-120, (1997); и AAPS J. 7(3); E686-E692, (2005). Смотрите также Steinhoff, M., et al., J. Neuroscience, 23 (15): 6176-6180, 2003.
Катетеры для микродиализа поставляются TSE Systems (Мидленд, Мичиган). Катетер T-образный и состоит из мембраны с порами 3000 кДа 0,3 мм OD длиной 4 мм, прикрепленной к 15 мм основанию. Входное и выходное отверстия соединены с 0,12 мм ID считывающей системой трубок. Анализ ex vivo проводили, применяя длины трубок, идентичные длинам трубки, применяемым для анализа in vivo. Катетеры HMWCO функционирует вместе с системой двухтактной накачки, чтобы минимизировать внешний (внутрь межклеточного пространства) поток. Тем не менее, также применяют только нагнетание (Harvard PHD 2000). Потерю жидкости в результате Δp и ΔΠ определяют при разных скоростях потока. Эффективность (Ed) мембраны определяют при разных скоростях потока, применяя известные количества IgG в смесительной камере, чтобы убрать немембранную (наружную) диффузию. Ed IgG мыши и гемоглобина мыши определяют и применяют их в качестве контролей in vivo. Количественный анализ проводят при помощи козьего антитела против IgG крысы, связанного с гранулами фирмы Лиминекс, и захват описывают с применением кроличьего или ослиного биотинилированного антитела против IgG крысы, чтобы снизить неспецифическую реакционную способность. Анализы в отношении IgG и гемоглобина мыши проводят для контролей в исследованиях in vivo. Связывание с гранулами проводят, применяя стандартный набор и протокол.
Применяют введение цитокинов мышам и крысам при помощи осмотического насоса, интрадермально или через волокно для микродиализа. Антитело вводят внутривенно. Катетер стерилизуют УФ. Катетер для микродиализа имплантируют и собирают образцы крови и анализируемые вещества. Количественный анализ транспорта IgG из циркуляции в потоке в кожу проводят, применяя мембранные параметры, определенные ex vivo, оценивают проницаемость для антитела и скорость перфузии.
Следующие ниже стадии проводят, применяя один момент времени на пару животных и достаточное количество моментов времени, чтобы оценить циркулирующие уровни антитела и диффузию в кожу/эпидермис в течение продолжительного времени: i) мембрану для микродиализа имплантируют в кожу и пробный образец забирают при скорости, определенной анализом ex vivo. Данный контрольный образец определяет базовую реакционную способность жидкости для проникновения; 2) крысиные антитела против IL-31 вводят посредством внутривенной инъекции в хвост, и в предварительно определенные моменты времени интраорбитальный образец крови забирают, чтобы определить уровни циркулирующего антитела; 3) образец после микродиализа достаточного для анализа объема забирают при скорости потока по протоколу; 4) в конце забора образов исследуемых веществ забирают другой интраорбитальный образец, чтобы определить уровни циркулирующего антитела против IL-31.
Мультиплексный анализ исследуемого вещества и плазмы проводят посредством Luminex и количественного анализа в отношении 1) антитела против IL-31, 2) антитела против IgG мыши в качестве контроля истощения/диффузии и 3) антитела против гемоглобина мыши для контроля травмы при микродиализном имплантировании и повреждения кровеносных сосудов. Применяя определенные ex vivo параметры мембраны и определенной скорости притока антитела против IL-31 в исследуемый образец при данной концентрации циркулирующего антитела, проводят оценку скорости диффузии в кожу. Концентрацию IgG мыши в исследуемом образце применяют для оценки локального истощения белков вблизи катетера. Возможно, необходимо изобрести формулу для компенсации локального истощения при анализе диффузии.
Из указанного выше будет оценено, что, хотя определенные варианты осуществления изобретения описаны в настоящем описании в иллюстративных целях, можно осуществить различные модификации, не отклоняясь от сущности и объема изобретения. Соответственно, изобретение не ограничено ничем, кроме как приложенной формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ЛЕЧЕНИЯ ВОСПАЛЕНИЯ В НЕЙРОННОЙ ТКАНИ С ПРИМЕНЕНИЕМ МОНОКЛОНАЛЬНОГО АНТИТЕЛА ИЛИ ЕГО СВЯЗЫВАЮЩЕГО ФРАГМЕНТА | 2007 |
|
RU2565391C2 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА ПРОТИВ IL-31 И СПОСОБЫ ПРИМЕНЕНИЯ | 2006 |
|
RU2444528C2 |
| ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО ОТ ЗУДА | 2008 |
|
RU2541780C2 |
| ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО ОТ ЗУДА | 2008 |
|
RU2596397C2 |
| НОВЫЙ ЛИГАНД РЕЦЕПТОРА ЦИТОКИНА ZCYTOR17 | 2003 |
|
RU2490276C2 |
| ПРОФИЛАКТИЧЕСКОЕ ИЛИ ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ВОСПАЛИТЕЛЬНОГО ЗАБОЛЕВАНИЯ | 2007 |
|
RU2511406C2 |
| ПРОДУЦИРУЮЩИЕ ГИСТАМИН БАКТЕРИАЛЬНЫЕ ШТАММЫ И ИХ ПРИМЕНЕНИЕ ПРИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЯХ | 2016 |
|
RU2747390C2 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА ПРОТИВ IL-21 ЧЕЛОВЕКА | 2008 |
|
RU2504552C2 |
| СОСТАВЫ И СПОСОБЫ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ И НАРУШЕНИЙ, СВЯЗАННЫХ С ПЕРЕДАЧЕЙ СИГНАЛОВ ЦИТОКИНАМИ | 2006 |
|
RU2426742C2 |
| ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ БАКТЕРИАЛЬНОГО ГИСТАМИНА | 2012 |
|
RU2628536C2 |











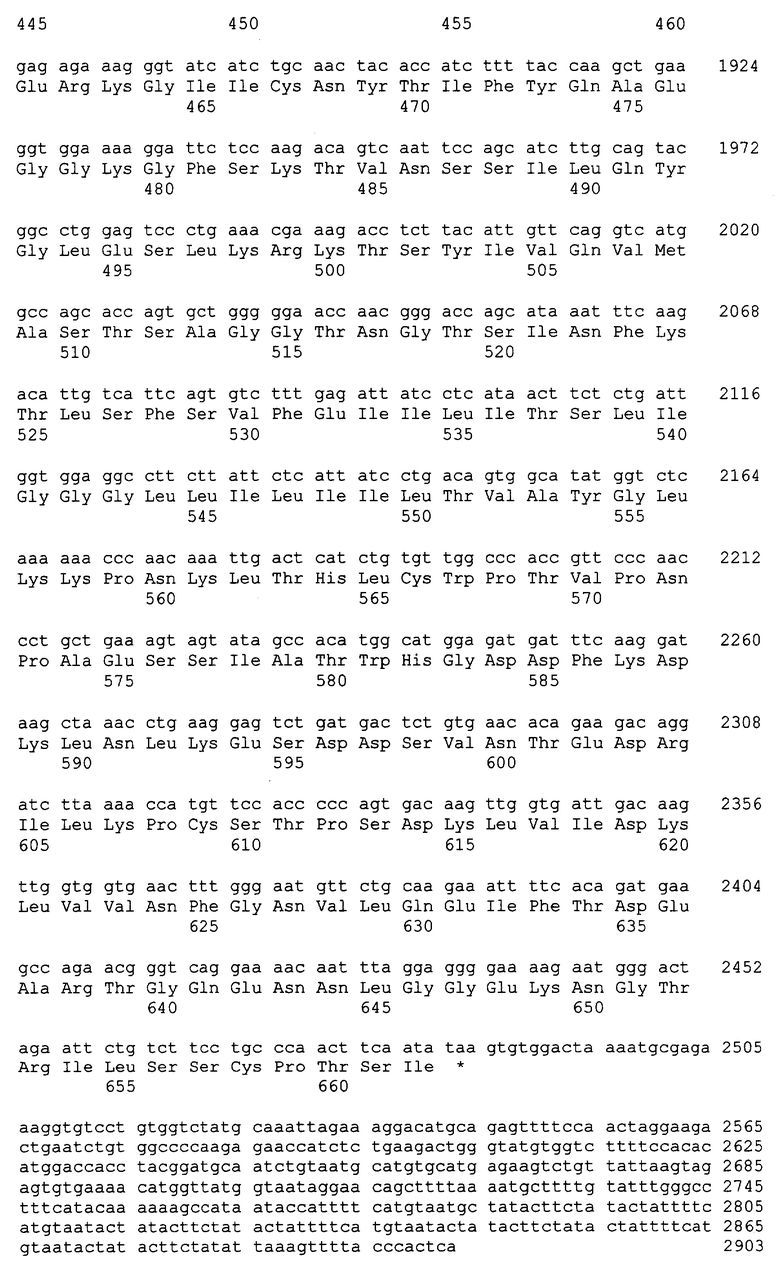

















Изобретение относится к области медицины. Способ включает применение антагониста IL-31 для ингибирования сигнальной трансдукции индуцированной IL-31 в клетках ганглия заднего корешка. Антагонист IL-31 ингибирует связывание полипептида IL-31, включающего аминокислотные остатки 27-164 SEQ ID NO: 2, с его гетеродимерным рецептором, включающим IL-31RA и OSMR-бета. Антагонист представляет собой гуманизированное моноклональное антитело или химерное антитело. Использование способа эффективно уменьшает воспаление, боль и зуд. 8 з.п. ф-лы, 1 табл.
1. Применение антагониста IL-31 для ингибирования сигнальной трансдукции индуцированной IL-31 в клетках ганглия заднего корешка, где антагонист IL-31 ингибирует связывание полипептида IL-31, включающего аминокислотные остатки 27-164 SEQ ID NO: 2 с его гетеродимерным рецептором, включающим IL-31RA и OSMR-бета.
2. Применение по п.1, где антагонист представляет собой антитело.
3. Применение по п.2, где антитело представляет собой моноклональное антитело.
4. Применение по п.2 или 3, где антитело является гуманизированным.
5. Применение по любому из пп.2-4, где антитело является химерным антителом.
6. Применение по любому из пп.2-5, где антитело представляет собой одноцепочечное антитело, фрагмент Fab, фрагмента Fab' или фрагмент F(ab')2.
7. Применение по п.2, где антитело продуцируется гибридомой, выбранной из группы, состоящей из а) гибридомы, имеющей номер патентного депонирования в АТСС РТА-6815; b) гибридомы, имеющей номер патентного депонирования в АТСС РТА-6816; с) гибридомы, имеющей номер патентного депонирования в АТСС РТА-6829; d) гибридомы, имеющей номер патентного депонирования в АТСС РТА-6830; е) гибридомы, имеющей номер патентного депонирования в АТСС РТА-6831, f) гибридомы, имеющей номер патентного депонирования в АТСС РТА-6871; g) гибридомы, имеющей номер патентного депонирования в АТСС РТА-6872; h) гибридомы, имеющей номер патентного депонирования в АТСС РТА-6875 и i) гибридомы, имеющей номер патентного депонирования в АТСС РТА-6873.
8. Применение по п.7, где антитело IL-31 является гуманизированным.
9. Применение по любому из предшествующих пунктов, где ингибирование сигнальной трансдукции индуцированной IL-31 уменьшает боль.
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
Авторы
Даты
2012-01-20—Публикация
2007-01-10—Подача