УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
1. Область техники, к которой относится изобретение
Изобретение относится к способу преобразования растительного волокнистого материала для получения сахарида.
2. Описание предшествующего уровня техники
Сахарид эффективно используют в качестве пищевого продукта или горючего, причем под сахаридом, главным образом, подразумевается глюкоза и ксилоза, производимые из целлюлозы или гемицеллюлозы посредством преобразования растительного волокнистого материала, например выжатых остатков сахарного тростника (жмыха) или древесной щепы. В особенности, обращает на себя внимание технология получения энергии из биомассы, в которой сахарид, полученный посредством преобразования растительного волокнистого материала, подвергают сбраживанию для получения спирта, например этанола, используемого в качестве горючего. Например, различные способы получения сахарида, в частности глюкозы, предложены в публикации японской патентной заявки №8-299000 (JP-A-8-299000), в публикации японской патентной заявки №2006-149343 (JP-A-2006-149343), в публикации японской патентной заявки №2006-129735 (JP-A-2006-129735) и в публикации японской патентной заявки №2002-59118 (JP-A-2002-59118). Документ JP-A-8-299000 раскрывает способ гидролиза целлюлозы с применением соляной или серной кислот (разбавленной серной кислоты или концентрированной серной кислоты). Также доступны способ с применением целлюлозы (JP-A-2006-149343), способ с применением твердого катализатора, такого как активированный уголь или цеолит (JP-A-2006-129735), и способ с применением горячей воды под давлением (JP-A-2002-59118).
Однако в случае применения способа, в котором целлюлозу преобразуют с использованием кислоты, например серной кислоты, бывает трудно разделить кислоту и сахарид. Это связано с тем, что и кислота, и глюкоза, которая является основным ингредиентом продукта преобразования, растворимы в воде. Удаление кислоты нейтрализацией или ионным обменом не только затруднительно и дорого, но также связано с трудностями полного удаления кислоты потому, что кислота может оставаться в реакционной смеси в процессе сбраживания сахарида для получения этанола. В результате этого, даже тогда, когда рН оптимизируется ввиду активности дрожжей в процессе сбраживания для получения этанола, концентрация соли становится высокой, что приводит к снижению активности дрожжей, а это, в свою очередь, приводит к снижению эффективности сбраживания.
В особенности трудно и очень энергоемко удаление серной кислоты без инактивации дрожжей в том случае, если используется концентрированная серная кислота. С другой стороны, если используется разбавленная серная кислота, то удаление серной кислоты происходит относительно просто. Однако необходимо преобразовывать целлюлозу в условиях высокой температуры, что связано со значительной энергоемкостью. В дополнение к этому, кислоту, например серную кислоту и соляную кислоту, очень трудно отделить, собрать и повторно использовать. Таким образом, применение этих кислот в качестве катализатора для получения глюкозы является причиной повышения себестоимости биоэтанола.
В случае применения способа, в котором используется горячая вода под давлением, трудно отрегулировать условия реакции и, следовательно, трудно обеспечить получение глюкозы со стабильным выходом продукта. В дополнение к этому, в соответствии с вышеуказанным способом, равномерное преобразование исходного сырья в глюкозу приводит к уменьшению выхода глюкозы, и, кроме того, вследствие накопления продукта преобразования снижается активность дрожжей, что может привести к подавлению процесса брожения. Кроме того, реактор (сверхкритическое обрабатывающее устройство) довольно дорог и подвержен быстрому износу, вследствие чего этот способ также проблематичен в экономическом аспекте.
В то же время широко применяемые катализаторы включают кластерный кислотный катализатор типа гетерополикислоты. Например, в публикации японской патентной заявки №2006-206579 (JP-A-2006-206579) описан способ производства левулината сложного эфира, в котором углевод и спирт реагируют в присутствии гетерополикислоты. В способе, описанном в документе WO 95/26438, в процессе удаления лигнина из древесной пульпы и в процессе отбеливания древесной пульпы применяется кластерный кислотный катализатор в виде водного раствора от 0,001 до 0,20 М.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Изобретение предлагает способ преобразования растительного волокнистого материала, в котором катализатор для ускорения гидролиза целлюлозы или гемицеллюлозы и сахарид, получаемый в результате гидролиза целлюлозы и т.п. сырья, достаточно просто разделяются, причем сепарированный катализатор можно использовать повторно. В дополнение к этому, изобретение предлагает способ преобразования растительного волокнистого материала, который обладает превосходными характеристиками в плане энергетической эффективности.
Способ преобразования растительного волокнистого материала в соответствии с первым аспектом изобретения включает гидролиз целлюлозы, содержащейся в растительном волокнистом материале, с применением в качестве катализатора псевдожидкой кластерной кислоты, и получение сахарида, который в наибольшей степени представлен глюкозой.
В первом аспекте изобретения кластерная кислота, используемая в качестве катализатора для гидролиза целлюлозы, в целом, обладает более сильной кислотностью, чем серная кислота и, следовательно, проявляет достаточную каталитическую активность даже в условиях низких температур, что делает возможным получение из целлюлозы такого сахарида, как глюкоза, с высокой энергетической эффективностью. Кроме того, поскольку псевдожидкая кластерная кислота также способна действовать в реакции как растворитель, можно существенно уменьшить количество растворителя, используемого в реакции, по сравнению с процессами гидролиза, в которых применяются другие катализаторы. В результате этого становится возможным сепарировать и собирать кластерную кислоту более эффективно и с меньшими затратами энергии.
Стадия гидролиза может быть проведена при температуре 140°С или ниже и при атмосферном давлении порядка 1 МПа.
Гидролиз целлюлозы может быть проведен при температуре 120°С или ниже.
Гидролиз целлюлозы может быть проведен при температуре 100°С или ниже.
Соотношение между растительным волокнистым материалом и кластерной кислотой может находиться в диапазоне от 1:1 до 1:4.
Когда кластерную кислоту приводят в псевдожидкое состояние, она проявляет каталитическую активность в отношении гидролиза целлюлозы или гемицеллюлозы. Поскольку псевдожидкое состояние кластерной кислоты меняется в зависимости от температуры и количества кристаллизационной воды, содержащейся в кластерной кислоте, при переведении кластерной кислоты в псевдожидкое состояние необходимо контролировать количество кристаллизационной воды в кластерной кислоте и температуру реакции. В то же время вода необходима для гидролиза целлюлозы, представляющей собой полимер, в котором молекулы глюкозы соединены β-1,4-гликозидными связями, образуя такие сахариды как глюкоза или ксилоза.
Ввиду этого факта, количество воды в гидролизной реакционной системе может быть равным или превышать сумму i) количества кристаллизационной воды, необходимого для переведения всей кластерной кислоты в гидролизной реакционной системе в псевдожидкое состояние в температурных условиях, способствующих гидролизу, и ii) количества воды, необходимого для гидролиза всей целлюлозы в гидролизной реакционной системе в глюкозу.
Кластерная кислота может представлять собой гетерополикислоту.
Гетерополикислота может быть выбрана из группы, состоящей из фосфорновольфрамовой кислоты, кремневольфрамовой кислоты и фосфорномолибденовой кислоты.
Гетерополикислота может иметь структуру Кеггина.
Гетерополикислота может иметь структуру Доусона.
Далее, способ преобразования растительного волокнистого материала может включать стадию сепарации после получения глюкозы, причем на этой стадии сахарид осаждают при помощи органического растворителя, а сахарид, содержащий затвердевший в процессе гидролиза и осажденный сахарид, отделяют от остатков сырья и кластерной кислоты.
Если в качестве катализатора для гидролиза целлюлозы применяют кластерную кислоту и при этом используют органический растворитель, хорошо растворяющий кластерную кислоту, но плохо растворяющий сахарид, который, в основном, представлен глюкозой как продуктом, то можно осадить сахарид и без затруднений разделить кластерную кислоту и сахарид.
Растворимость сахарида в органическом растворителе может составлять 0,6 г/100 мл или менее.
Растворимость сахарида в органическом растворителе может составлять 0,06 г/100 мл или менее.
Растворимость кластерной кислоты в органическом растворителе может составлять 20 г/100 мл или более.
Растворимость кластерной кислоты в органическом растворителе может составлять 40 г/100 мл или более.
В качестве органического растворителя можно применять, по меньшей мере, один из растворителей, выбранных из числа эфирных и спиртовых растворителей.
Органическим растворителем может быть этанол.
Органическим растворителем может быть диэтиловый эфир.
На стадии сепарации количество воды в реакционной смеси, в которой проводится сепарация, можно контролировать таким образом, чтобы вся кластерная кислота в реакционной системе, в которой осуществляется сепарация сахарида, содержала кристаллизационную воду в таком количестве, которое равно нормальному количеству кристаллизационной воды или несколько меньше него. Если кластерная кислота содержит кристаллизационную воду в таком количестве, которое превышает нормальное количество кристаллизационной воды на стадии сепарации, то молекулы воды, которые не координированы относительно кластерной кислоты, смешиваются с органическим растворителем, а сахарид растворяется в смешанной воде, что приводит к смешению сахарида с органической фазой растворителя, в которой растворена кластерная кислота. Контролируя количество кристаллизационной воды в кластерной кислоте на стадии сепарации, как это описано выше, можно свести к минимуму растворение сахарида в воде, смешанной с органической фазой растворителя, как это описано выше, следовательно, можно улучшить выход сахарида.
Когда сахарид перемещается в органическую фазу растворителя, кластерную кислоту можно обезводить после стадии сепарации с тем расчетом, чтобы вся кластерная кислота в органическом растворителе содержала кристаллизационную воду в таком количестве, которое равно нормальному количеству кристаллизационной воды или несколько меньше него. Обезвоживая кластерную кислоту в органическом растворителе для уменьшения количества кристаллизационной воды, можно осадить и собрать сахарид, растворенный в воде, которая не координирована относительно кластерной кислоты и смешана с органической фазой растворителя.
В качестве осушающего средства для обезвоживания кластерной кислоты можно использовать кластерную кислоту, содержащую кристаллизационную воду в таком количестве, которое равно нормальному количеству кристаллизационной воды или несколько меньше него.
Уровень содержания кристаллизационной воды в кластерной кислоте, используемой в качестве осушающего средства, составляет 70% или менее.
Уровень содержания кристаллизационной воды в кластерной кислоте, используемой в качестве осушающего средства, составляет 30% или менее.
Кластерную кислоту, растворенную в органическом растворителе, можно отделить от органического растворителя. Выделенную кластерную кислоту можно использовать повторно в качестве катализатора для гидролиза целлюлозы или гемицеллюлозы, содержащейся в растительном волокнистом материале.
Растительным волокнистым материалом может быть биомасса на основе целлюлозы.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Описанные выше и ниже признаки и полезные эффекты изобретения будут очевидны из приведенного в последующем тексте описания иллюстративных вариантов осуществления изобретения со ссылками на сопровождающие чертежи, в которых цифровые обозначения используются для обозначения соответствующих элементов и в которых
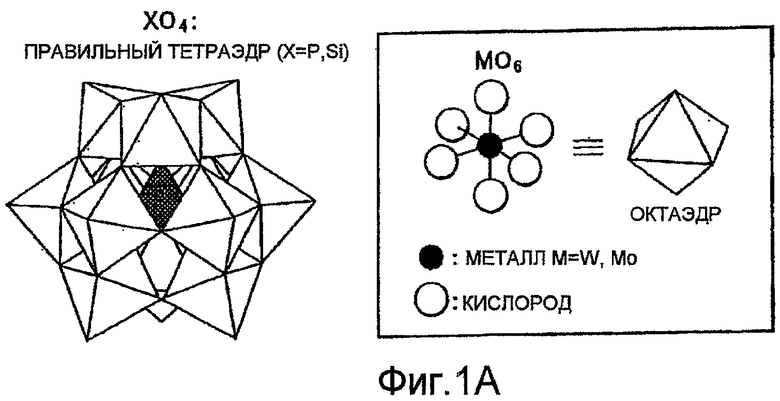
ФИГ.1А показывает структуру Кеггина гетерополикислоты;
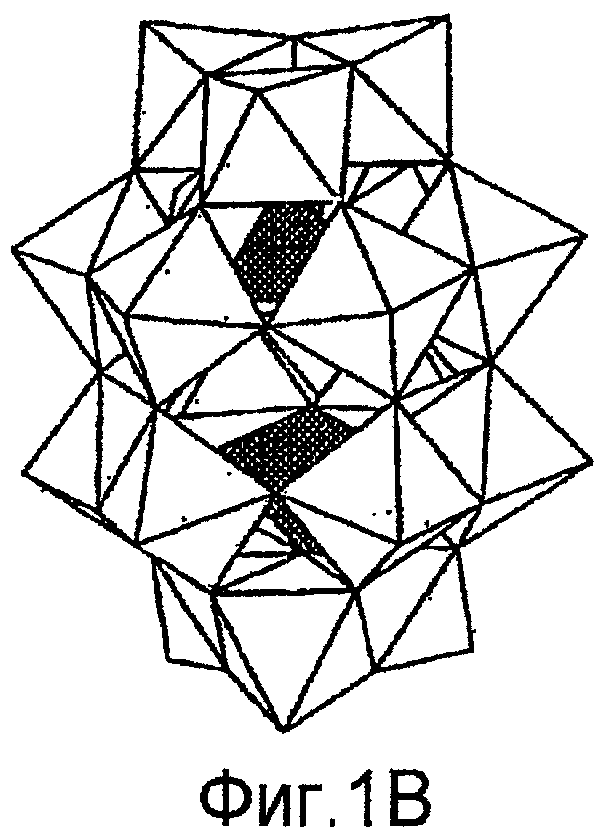
ФИГ.1В показывает структуру Доусона гетерополикислоты;
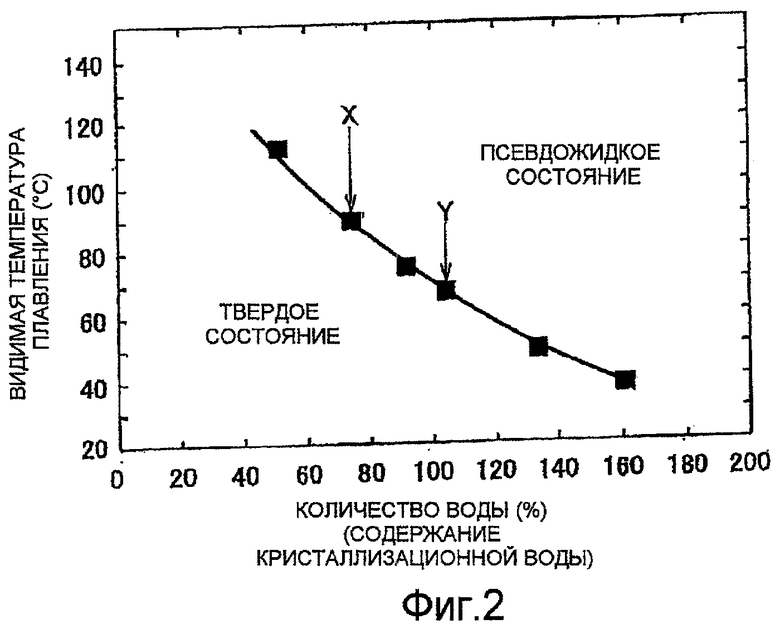
ФИГ.2 представляет собой график, демонстрирующий связь между содержанием кристаллизационной воды в катализаторе типа кластерной кислоты и видимой температурой плавления;
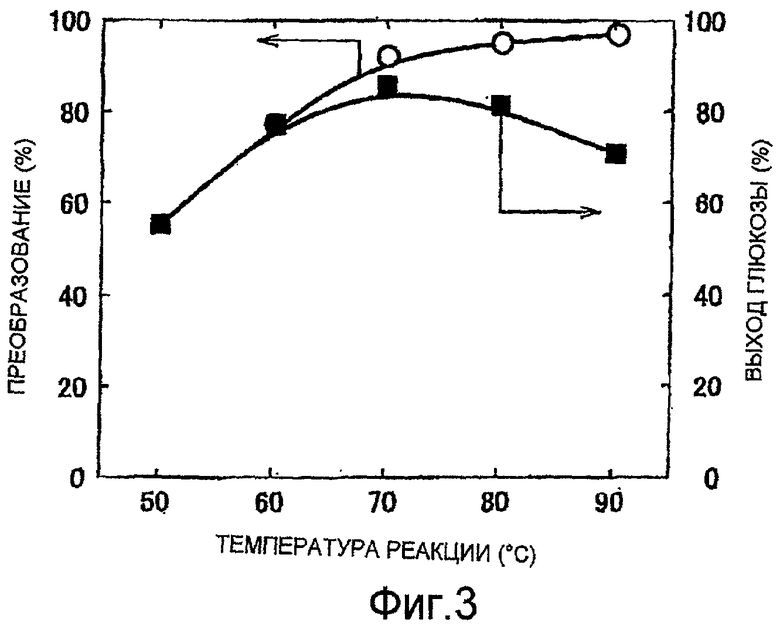
ФИГ.3 представляет собой график, демонстрирующий связь между преобразованием целлюлозы (R), выходом глюкозы (η) и температурой реакции гидролиза;
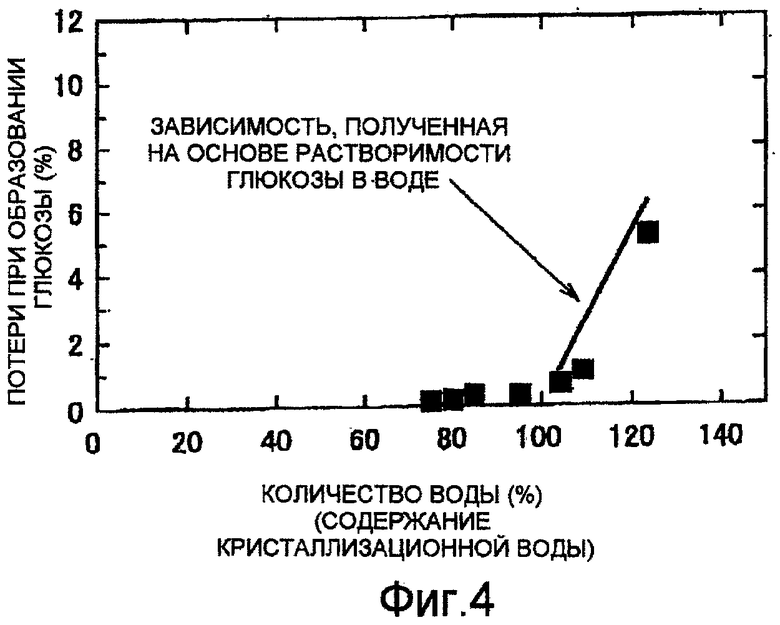
ФИГ.4 представляет собой график, демонстрирующий зависимость между содержанием кристаллизационной воды и потерей глюкозы вследствие растворения при сборе катализирующей кластерной кислоты, и
ФИГ.5 представляет собой блок-схему, описывающую стадии от гидролиза целлюлозы до сбора сахарида и гетерополикислоты в примере 9.
ПОДРОБНОЕ ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Первый вариант осуществления изобретения, который относится к способу преобразования растительного волокнистого материала, будет описан ниже со ссылками на чертежи.
Авторы настоящего изобретения обнаружили, что псевдожидкая кластерная кислота действует как катализатор гидролиза целлюлозы или гемицеллюлозы для получения сахарида, в основном представленного глюкозой. Термин "кластерная кислота" при использовании здесь означает кислоту, в которой конденсировано множество оксокислот, то есть так называемую поликислоту. Во многих случаях поликислота находится в таком состоянии, когда множество атомов кислорода соединены с центральным элементом, который вследствие этого окислен до максимальной степени окисления, в результате чего поликислота проявляет блестящие свойства катализатора окисления. Кроме того, известно, что многие поликислоты являются сильными кислотами. Например, кислотность фосфорновольфрамовой кислоты (рКа=-13,16), которая является гетерополикислотой, превышает кислотность серной кислоты (рКа=-11,93). Таким образом, даже при мягких условиях, например при температуре 50°С, можно преобразовывать целлюлозу или гемицеллюлозу для получения таких сахаридов, как глюкоза или ксилоза.
Кластерная кислота, применяемая в изобретении, может представлять собой либо изополикислоту, либо гетерополикислоту. Предпочтительной кластерной кислотой является гетерополикислота, поскольку она обладает высокой окислительной способностью и сильной кислотностью. Не существует конкретных ограничений в отношении разновидности используемой гетерополикислоты. Например, гетерополикислота может иметь общую структуру [HwAxByOz], где А представляет гетероатом, такой как фосфор, кремний, германий, мышьяк или бор, который способен образовывать гетерополикислоту, В представляет полиатом, такой как вольфрам, молибден, ванадий или ниобий, который способен образовывать поликислоту, и w, х, y и z означают содержание компонентов Н, А, В и О соответственно. Число разновидностей полиатомов и гетероатомов, которые содержатся в одной молекуле гетерополикислоты, может составлять одну или более.
В особенности применимы фосфорновольфрамовая кислота H3[PW12O40] или кремневольфрамовая кислота Н4[SiW12O40], которые являются вольфраматами, ввиду сбалансированных величин кислотности и окислительной способности. В альтернативном варианте можно применять фосфорномолибденовую кислоту Н3[PMo12O40], которая является молибдатом.
Например, структура гетерополикислоты типа Кеггина (фосфорновольфрамовой кислоты) [Xn+M12O40: Х=Р, Si, Ge, As и т.д., М=Мо, W и т.д.] показана на фиг.1А. В центре многогранников, каждый из которых является октаэдром МО6, представлен тетраэдр XO4, а вокруг этой структуры имеется много кристаллизационной воды. Следует отметить, что не существует особых ограничений в отношении структуры кластерной кислоты. Например, гетерополикислота может представлять собой гетерополикислоту типа Доусона, как это показано на фиг.1В. Хотя катализирующая кластерная кислота по своей сути не является кристаллической, термин "кристаллизационная вода" при использовании здесь относится к воде, координированной относительно катализирующей кластерной кислоты в определенном соотношении. Хотя, в целом, кристаллизационная вода представляет собой воду, содержащуюся в катализирующей кластерной кислоте, когда указанная катализирующая кластерная кислота находится в кристаллическом состоянии, к кристаллизационной воде также относятся молекулы воды, координированные относительно катализирующей кластерной кислоты, когда указанная катализирующая кластерная кислота находится в псевдожидком состоянии, в котором все молекулы катализирующей кластерной кислоты отделены друг от друга, или катализирующая кластерная кислота растворена в этаноле (более точно, катализирующая кластерная кислота не растворена в этаноле, а суспендирована в нем в коллоидном состоянии).
Как описано выше, катализирующая кластерная кислота при комнатной температуре находится в твердом состоянии. Когда катализирующую кластерную кислоту нагревают, она переходит в псевдожидкое состояние и проявляет каталитическую активность при гидролизе целлюлозы или гемицеллюлозы. Понятие псевдожидкое состояние при использовании здесь означает такое состояние, в котором кластерная кислота, несомненно, расплавлена, но не полностью перешла в жидкое состояние, псевдожидкое состояние похоже на коллоидное (золевое) состояние, когда кластерная кислота диспергирована в растворе, и является таким состоянием, пребывая в котором кластерная кислота демонстрирует текучесть. Следует заметить, что в этом состоянии кластерная кислота обладает высокой вязкостью и высокой плотностью. Можно определить, находится ли кластерная кислота в псевдожидком состоянии, пользуясь визуальным контролем или, в случае гомогенной системы, например, дифференциальным сканирующим калориметром (DSC).
Кластерная кислота проявляет высокую каталитическую активность при гидролизе целлюлозы в условиях низких температур, благодаря своей сильной кислотности, как это описано выше. Поскольку диаметр молекулы кластерной кислоты составляет приблизительно 2 нм, кластерная кислота легко смешивается с растительным волокнистым материалом, который является сырьевым материалом, и, следовательно, эффективно стимулирует гидролиз целлюлозы. Таким образом, становится возможным проводить гидролиз целлюлозы в мягких условиях, что обеспечивает высокую энергетическую эффективность и небольшую нагрузку на окружающую среду. В дополнение к этому, в отличие от гидролиза целлюлозы с применением, например, серной кислоты, гидролиз целлюлозы с применением в качестве катализатора кластерной кислоты в соответствии с настоящим изобретением позволяет достичь высокоэффективного разделения сахарида и катализатора, следовательно, делает возможным легкое разделение сахарида и катализатора, благодаря чему количество катализатора, остающегося в сахариде, сводится к минимуму, а процесс гидролиза в этом варианте осуществления изобретения также выгодно отличается в аспекте сбраживания сырья.
В дополнение к этому следует упомянуть, что, поскольку кластерная кислота твердеет в зависимости от температуры, становится возможным отделить кластерную кислоту от сахарида, который является продуктом процесса. Таким образом, можно собирать и повторно использовать выделенную кластерную кислоту. Кроме того, поскольку псевдожидкая катализирующая кластерная кислота также действует в реакции как растворитель, можно существенно уменьшить количество растворителя, используемого в реакции, по сравнению с другими процессами гидролиза. Это означает, что можно достичь высокой эффективности при разделении кластерной кислоты и сахарида, являющегося продуктом процесса, и при сборе выделенной кластерной кислоты. Особо следует упомянуть, что изобретение, в котором кластерная кислота использована в качестве катализатора при гидролизе целлюлозы, снижает экономические затраты и в то же время не оказывает вредного воздействия на окружающую среду.
Стадия гидролиза целлюлозы, включенная в процесс преобразования растительного волокнистого материала в соответствии с настоящим изобретением, будет подробно описана ниже. Хотя в заявке, в основном, описана стадия, в ходе которой из целлюлозы образуется глюкоза, растительный волокнистый материал, в дополнение к целлюлозе, включает гемицеллюлозу, а продукт процесса, в дополнение к глюкозе, включает ксилозу, и эти случаи также попадают в объем притязаний изобретения. Растительный волокнистый материал не имеет специальных ограничений, как и содержание в нем целлюлозы и гемицеллюлозы, то есть включает такие виды биомассы на основе целлюлозы, как древесину лиственных пород, бамбук, хвойную древесину, кенаф, отходы древесины из фурнитуры, рисовую солому, пшеничную солому, рисовую шелуху и выжатые остатки сахарного тростника (жмых). Растительным волокнистым материалом может быть целлюлоза или гемицеллюлоза, которые выделены из вышеуказанных видов биомассы либо искусственно синтезированы.
В общем, применительно к волокнистому материалу такого рода предпочтительно его использование в измельченном состоянии ввиду характеристик дисперсии в реакционной системе. Способ измельчения волокнистого материала может представлять собой широко применяемый способ. В связи с улучшением и упрощением смешивания с катализирующей кластерной кислотой, а также с увеличением вероятности удачной реакции, растительный волокнистый материал можно измельчать до порошка с диаметром частиц приблизительно от нескольких микронов до 200 микронов.
Катализирующую кластерную кислоту и растительный волокнистый материал можно смешивать и взбалтывать еще до нагревания. Как описано выше, на стадии гидролиза катализирующая кластерная кислота переходит в псевдожидкое состояние и действует в реакции, как растворитель. Таким образом, в этом варианте осуществления изобретения, хотя он и зависит, например, от вида растительного волокнистого материала (от размера и состояния волокон), а также от соотношения в смеси и по объему между катализирующей кластерной кислотой и растительным волокнистым материалом, отпадает необходимость в использовании воды, органических растворителей и т.д. в качестве растворителей для реакции. По этой причине, если необходимо обеспечить контакт между кластерной кислотой и растительным волокнистым материалом, то можно до некоторой степени смешивать катализирующую кластерную кислоту и растительный волокнистый материал прежде, чем катализирующая кластерная кислота перейдет в псевдожидкое состояние.
Псевдожидкое состояние кластерной кислоты варьируется в зависимости от температуры и количества кристаллизационной воды, содержащейся в катализирующей кластерной кислоте (см. фиг.2). В особенности необходимо отметить обнаруженный авторами настоящего изобретения факт, что если количественное содержание кристаллизационной воды увеличивается, то снижается температура, при которой фосфорновольфрамовая кислота, которая является кластерной кислотой, переходит в псевдожидкое состояние. То есть катализирующая кластерная кислота, содержащая относительно большое количество кристаллизационной воды, проявляет каталитическое действие при гидролизе целлюлозы в условиях пониженной температуры по сравнению с тем случаем, когда катализирующая кластерная кислота содержит кристаллизационную воду в меньшем количестве.
Фиг.2 показывает связь между содержанием кристаллизационной воды в гетерополикислоте (фосфорновольфрамовой кислоте), которая является типичной катализирующей кластерной кислотой, и температурой (очевидной температурой плавления), при которой кислота переходит в псевдожидкое состояние. На фиг.2 катализирующая кластерная кислота находится в твердом состоянии в области под кривой и в псевдожидком состоянии в области над кривой. В дополнение к этому, на фиг.2 количество воды (содержание кристаллизационной воды) (%) определяется при том допущении, что содержание воды составляет 100%, если количество кристаллизационной воды в кластерной кислоте (фосфорновольфрамовой кислоте) равно нормальному количеству n кристаллизационной воды (n=30). Поскольку ни один из компонентов катализирующей кластерной кислоты не подвергается термическому распаду и не испаряется даже при высокой температуре, например, при 800°С, можно определять количество кристаллизационной воды пиролитическими способами, например, методом термогравиметрии (TG).
Нормальным количеством кристаллизационной воды является такое количество (число молекул) кристаллизационной воды, которое содержится в молекуле кластерной кислоты в твердом кристаллическом состоянии при комнатной температуре, причем это количество варьируется в зависимости от разновидности кластерной кислоты. Например, нормальное количество кристаллизационной воды составляет приблизительно 30 для фосфорновольфрамовой кислоты (H3[PW12O40]·nH2O (n≈30)), приблизительно 24 для кремнефольфрамовой кислоты (H4[SiW12O40]·nH2O (n≈24)) и приблизительно 30 для фосфорномолибденовой кислоты (Н3[PMo12O40]·nH2O (n≈30)).
Контролируя количество кристаллизационной воды, содержащейся в катализирующей кластерной кислоте, в реакционной системе гидролиза на основе взаимосвязи между количеством кристаллизационной воды и видимой температурой плавления, можно перевести катализирующую кластерную кислоту в псевдожидкое состояние при температуре реакции гидролиза. Например, если в качестве катализирующей кластерной кислоты используется фосфорновольфрамовая кислота, то можно контролировать температуру реакции гидролиза в диапазоне от 40°С до 110°С, изменяя количество кристаллизационной воды в кластерной кислоте (см. фиг.2).
Количество кристаллизационной воды в катализирующей кластерной кислоте можно регулировать, контролируя количество воды, присутствующей в реакционной системе гидролиза. В особенности, если желательно увеличить количество кристаллизационной воды, содержащейся в катализирующей кластерной кислоте, то есть снизить температуру реакции, можно предпринять такую меру, как добавление воды к реакционной системе гидролиза, например, добавив воду к смеси, содержащей растительный волокнистый материал и катализирующую кластерную кислоту, или повысив относительную влажность атмосферы, окружающей реакционную систему. В результате кластерная кислота присоединяет добавочную воду как кристаллизационную воду, а видимая температура плавления катализирующей кластерной кислоты снижается.
С другой стороны, если желательно уменьшить количество кристаллизационной воды, содержащейся в катализирующей кластерной кислоте, можно предпринять такую меру, как удаление воды из реакционной системы гидролиза, например, нагреванием реакционной системы для испарения воды или добавлением осушающего средства к смеси, содержащей растительный волокнистый материал и катализирующую кластерную кислоту. В результате видимая температура плавления катализирующей кластерной кислоты повышается. Как описано выше, можно достаточно просто контролировать количество кристаллизационной воды, содержащейся в кластерной кислоте, а также достаточно просто регулировать температуру реакции, при которой происходит гидролиз целлюлозы, управляя количеством кристаллизационной воды.
Снижение температуры реакции на стадии гидролиза выгодно тем, что позволяет повысить энергетическую эффективность. В дополнение к этому авторы настоящего изобретения обнаружили, что избирательность, с которой образуется глюкоза при гидролизе целлюлозы, содержащейся в растительном волокнистом материале, варьируется в зависимости от температуры реакции гидролиза (см. фиг.3). Как показано на фиг.3, имеет место такой общий факт, что чем выше температура реакции, тем интенсивнее происходит превращение; при гидролизе целлюлозы с применением фосфорновольфрамовой кислоты, в которой содержание кристаллизационной воды составляет 160% (видимая температура плавления около 40°С, см. фиг.2), превращение R в температурном диапазоне от 50°С до 90°С увеличивается по мере увеличения температуры, и почти вся целлюлоза реагирует при температуре приблизительно 80°С.
С другой стороны, хотя в случае преобразования целлюлозы выход η глюкозы увеличивается в диапазоне от 50°С до 60 и достигает максимума при 70°С, а затем снижается по мере увеличения температуры. Более конкретно, глюкоза образуется с высокой избирательностью в диапазоне температур от 50°С до 60°С, тогда как в диапазоне температур от 70°С до 90°С протекают другие реакции, нежели получение глюкозы, включая, например, образование других сахаридов, в частности, ксилозы, а также трансформация. Следует отметить, что R-преобразование целлюлозы и выход η глюкозы можно определить расчетным способом на основе следующих выражений:
R={(QCt-QCr)/QCt}×100
η=R×(QG/QGt),
где QCt означает количество подготовленной целлюлозы, QCr - количество непрореагировавшей целлюлозы, QG - количество образованной глюкозы в случае гидролиза всей подготовленной целлюлозы и QGt - фактическое количество собранной целлюлозы.
Как описано выше, температура реакции гидролиза является важным фактором, оказывающим влияние на химическое превращение целлюлозы и избирательность применительно к образованию глюкозы. Хотя, исходя из соображений энергетической эффективности, предпочтительно, чтобы температура реакции гидролиза была низкой, эту температуру можно определить, принимая во внимание химическое превращение целлюлозы, избирательность образования глюкозы и т.д. Следует отметить, что избирательность образования сахарида, получаемого посредством гидролиза целлюлозы, может демонстрировать поведение, отличающееся от показанного на фиг.3, в зависимости от условий реакции и т.д.
Как описано выше, можно управлять системой таким образом, чтобы катализирующая кластерная кислота переходила в псевдожидкое состояние при желательной температуре реакции гидролиза, что осуществляется посредством добавления воды в реакционную систему гидролиза или удаления воды из реакционной системы гидролиза описанным выше способом (по мере надобности).
Однако на стадии гидролиза целлюлозы необходима одна молекула воды на одну молекулу глюкозы. Таким образом, в том случае, если количество воды, присутствующей в реакционной системе, меньше, чем сумма количества воды, равная количеству кристаллизационной воды, необходимой для приведения катализирующей кластерной кислоты в псевдожидкое состояние при температуре реакции, и количеству воды, необходимой для гидролиза всей имеющейся целлюлозы в глюкозу, когда кристаллизационная вода, содержащаяся в катализирующей кластерной кислоте используется для гидролиза целлюлозы, то содержание кристаллизационной воды в катализирующей кластерной кислоте уменьшается, и, следовательно, кластерная кислота переходит в твердое состояние. В соответствии с этим каталитическое воздействие кластерной кислоты на гидролиз целлюлозы ослабевает, и, в дополнение к этому, повышается вязкость смеси растительного волокнистого материала и катализирующей кластерной кислоты, что может привести к недостаточному перемешиванию компонентов смеси.
Если намечено поддерживать активность катализатора и функцию катализирующей кластерной кислоты в качестве растворителя реакции при температуре реакции на стадии гидролиза (то есть поддерживать катализирующую кластерную кислоту на стадии гидролиза в псевдожидком состоянии), то количество воды в реакционной системе устанавливают так, как это описано ниже. Более конкретно, количество воды в реакционной системе устанавливают так, чтобы оно было равно сумме количества кристаллизационной воды, необходимого для приведения всей катализирующей кластерной кислоты, присутствующей в реакционной системе, в псевдожидкое состояние при температуре реакции на стадии гидролиза, и количества воды, необходимого для гидролиза всей целлюлозы, присутствующей в реакционной системе, в глюкозу, либо превышало эту сумму.
Кристаллизационная вода, необходимая для приведения всей катализирующей кластерной кислоты в псевдожидкое состояние, здесь соответствует такому случаю, когда часть молекул воды находится за пределами кристаллической решетки, а также такому случаю, когда кристаллизационная вода, необходимая для приведения всей катализирующей кластерной кислоты в псевдожидкое состояние при температуре гидролиза, находится внутри кристаллической решетки. Хотя можно определить нижний предел количества воды, присутствующей в реакционной системе на стадии гидролиза, основываясь на приведенном выше описании, верхний предел этого количества определить довольно трудно, поскольку верхний предел варьируется в зависимости от различных условий на стадии гидролиза. Поскольку избыточное количество воды может вызвать увеличение количества энергии, необходимой для поддержания температуры реакционной системы, то есть с высокой вероятностью ухудшить реакцию между целлюлозой и катализирующей кластерной кислотой и т.д., то, чем меньше количество воды на стадии гидролиза, тем лучше.
Следует отметить, что препараты можно делать так, чтобы даже при падении относительной влажности вокруг реакционной системы в результате нагревания сохранялось нужное количество кристаллизационной воды, содержащейся в катализирующей кластерной кислоте. Более конкретно, например, можно применить способ, в котором для насыщения атмосферы, окружающей реакционную систему, водяными парами при заранее определенной температуре реакции внутреннее содержимое закрытого реакционного контейнера насыщают водяными парами при температуре реакции гидролиза, затем температуру в закрытом реакционном контейнере снижают, чтобы конденсировать водяные пары, в результате чего сконденсированная вода добавляется в растительный волокнистый материал и катализирующую кластерную кислоту. Когда применяется растительный волокнистый материал, количество воды, присутствующей в растительном волокнистом материале, принимается во внимание как количество воды, присутствующей в реакционной системе, хотя при использовании высушенного растительного волокнистого материала это не надо принимать во внимание.
На стадии гидролиза, когда количество воды в реакционной системе и, следовательно, количество кристаллизационной воды, содержащейся в катализирующей кластерной кислоте, снижается, и, следовательно, катализирующая кластерная кислота переходит в твердое состояние со снижением каталитической активности, этого снижения каталитической активности катализирующей кластерной кислоты можно избежать, например, повысив температуру реакции гидролиза, чтобы катализирующая кластерная кислота перешла в псевдожидкое состояние.
Температуру на стадии гидролиза можно соответствующим образом определить, принимая во внимания несколько указанных выше факторов, таких как избирательность реакции, энергетическая эффективность и преобразование целлюлозы. Принимая во внимание баланс между энергетической эффективностью, преобразованием целлюлозы и выходом глюкозы, температуру можно установить на уровне 140°С или ниже, предпочтительнее на уровне 120°С или ниже. В зависимости от вида растительного волокнистого материала можно использовать низкотемпературные условия, например 100°С или ниже. Особенно следует отметить, что в этом случае можно получать глюкозу с высокой энергетической эффективностью.
Не существует особых ограничений в отношении давления на стадии гидролиза. Поскольку каталитическая активность катализирующей кластерной кислоты в отношении гидролиза целлюлозы высока, можно активировать эффективный гидролиз целлюлозы даже при мягких условиях давления, например при нормальном (атмосферном) давлении порядка 10 МПа.
Соотношение между растительным волокнистым материалом и катализирующей кластерной кислотой варьируется, например, в зависимости от таких характеристик, используемых на стадии гидролиза, как размер используемого волокнистого материала, способ перемешивания, способ взбалтывания и т.д. Таким образом, это соотношение можно соответствующим образом определить, принимая во внимание практические условия. Например, соотношение (весовое) между катализирующей кластерной кислотой и растительным волокнистым материалом может находиться в диапазоне от 1:1 до 1:4, в типичном случае, 1:1.
Не существует особых ограничений в отношении длительности стадии гидролиза. Эту длительность можно соответствующим образом задать, принимая во внимание вид используемого растительного волокнистого материала, соотношение между растительным волокнистым материалом и катализирующей кластерной кислотой, каталитическую производительность катализирующей кластерной кислоты, температуру реакции, давление в реакции и т.д. На стадии гидролиза вязкость смеси, содержащей катализирующую кластерную кислоту и растительный волокнистый материал, высока, и, следовательно, предпочтительным способом перемешивания/взбалтывания является такой способ, в котором используется, например, нагретая шаровая мельница. Однако вполне можно применять и обыкновенную мешалку.
Далее будет описан второй вариант осуществления изобретения, который связан со способом разделения сахарида, полученного на стадии гидролиза, который в большей степени представлен глюкозой, и катализирующей кластерной кислоты. Более конкретно, будет описан способ, при котором растительный волокнистый материал, содержащий целлюлозу или гемицеллюлозу, подвергается гидролизу с применением катализирующей кластерной кислоты для получения сахарида, в большей степени представленного глюкозой, после чего полученный сахарид и катализирующая кластерная кислота сепарируются.
Поскольку и катализирующая кластерная кислота, и образованный сахарид растворимы в воде, то при наличии достаточного количества воды результирующая смесь, полученная после стадии гидролиза, находится в таком состоянии, когда остатки растительного волокнистого материала (непрореагировавшая целлюлоза и т.п.) включены в качестве твердого ингредиента, а катализирующая кластерная кислота и сахарид растворены. Часть сахарида, образованного в процессе гидролиза, осаждена в виде твердого вещества.
Исследования, проведенные авторами настоящего изобретения, показали, что катализирующая кластерная кислота проявляет растворимость в органическом растворителе, в котором с трудом растворяется или вообще не растворяется сахарид, в большей степени представленный глюкозой. Таким образом, можно сепарировать сахарид и катализирующую кластерную кислоту с применением органического растворителя, который является плохим растворителем для сахарида и хорошим растворителем для катализирующей кластерной кислоты. Например, сахарид осаждается при добавлении достаточного количества вышеуказанного органического растворителя к смеси катализирующей кластерной кислоты, сахарида и остатков сырья после стадии гидролиза (далее обозначаемой здесь также как "гидролизная смесь"), то есть при введении органического растворителя и гидролизной смеси в контакт друг с другом, посредством чего сахарид и остаток растительного волокнистого материала, включая непрореагировавшую целлюлозу, отделяются в виде твердого вещества. Тем временем катализирующая кластерная кислота переходит в состояние раствора, то есть растворяется в органическом растворителе. Хотя большая часть сахарида, образованного в процессе гидролиза, осаждена в виде твердого вещества, часть сахарида находится в растворенном состоянии. Осаждая растворенный сахарид с применением органического растворителя, можно выделить растворенный сахарид, наряду с сахаридом, осажденным в процессе гидролиза, из смеси, следовательно, можно улучшить выход сахарида.
В отношении указанного выше органического растворителя не существует особых ограничений до тех пор, пока органический растворитель имеет такие растворяющие свойства, что он является хорошим растворителем для катализирующей кластерной кислоты и плохим растворителем для сахарида. Для того чтобы можно было эффективно осаждать сахарид, растворимость сахарида в органическом растворителе должна быть равной 0,6 г/100 мл или менее, предпочтительно 0,06 г/100 мл или менее. Для эффективного осаждения только сахарида растворимость кластерной кислоты в органическом растворителе должна быть равной 20 г/100 мл или более, предпочтительно 40 г/100 мл или более.
Более конкретно, указанные органические растворители включают, например, спирты, такие как этанол, метанол или н-пропанол, эфиры, такие как диэтиловый эфир или диизопропиловый эфир. Применительно к спиртам и эфирам, среди прочих, можно использовать этанол и диэтиловый эфир. Диэтиловый эфир является оптимальным растворителем для сепарации сахарида и катализирующей кластерной кислоты, поскольку сахарид, в частности глюкоза, нерастворим в диэтиловом эфире, а кластерная кислота высоко растворима в диэтиловом эфире. В то же время другим оптимальным растворителем является этанол, поскольку сахарид, в частности глюкоза, с трудом растворим в этаноле, а катализирующая кластерная кислота высоко растворима в этаноле. Принимая во внимание перегонку, диэтиловый эфир предпочтителен по сравнению с этанолом. Преимущество этанола заключается в том, что он более доступен по сравнению с диэтиловым эфиром.
Количество используемого органического растворителя варьируется в зависимости от растворяющих характеристик указанного растворителя в отношении сахарида и катализирующей кластерной кислоты, а также от количества воды, содержащегося в гидролизной смеси. Так, например, количество используемого органического растворителя можно определить соответствующим образом, чтобы было возможно эффективно осадить образованный сахарид без потерь, эффективно собрать кластерную кислоту и растворить катализирующую кластерную кислоту, содержащуюся в части отвердевшего сахарида, посредством измельчения отвердевшего сахарида.
Температура на стадии сепарации может находиться в диапазоне от комнатной температуры до 60°С, причем она зависит от точки кипения органического растворителя. На стадии сепарации не существует особых ограничений в отношении того, каким образом гидролизная смесь и органический растворитель вводятся в контакт друг с другом, более конкретно, в отношении способа добавления органического растворителя к гидролизной смеси и способа перемешивания гидролизной смеси с органическим растворителем, например, можно применить какой-либо традиционный способ. С учетом эффективности сбора кластерной кислоты предпочтителен такой способ перемешивания, в котором перемешивание и/или измельчение осуществляются с применением шаровой мельницы или подобного устройства.
В дополнение к этому авторы настоящего изобретения обнаружили, что если катализирующая кластерная кислота на стадии сепарации содержит большое количество кристаллизационной воды (например, количество кристаллизационной воды больше ее нормального количества), то избыточное количество воды не координировано относительно кластерной кислоты, вступая в смесь с органическим растворителем и сахаридом (продуктом реакции), то есть растворяется в воде, смешанной с органическим растворителем. Если вода смешивается с органическим растворителем, в котором растворена катализирующая кластерная кислота, а в этой воде растворен сахарид, то выход сахарида уменьшается.
Таким образом, для того чтобы свести к минимуму потери выхода сахарида, общее количество кристаллизационной воды, содержащееся во всей катализирующей кластерной кислоте, присутствующей в реакционной системе, должно соответствовать нормальному количеству кристаллизационной воды на вышеописанной стадии сепарации или быть меньше него. В экспериментах, проведенных авторами изобретения, было подтверждено, что сахарид, в большей степени представленный глюкозой, защищен от растворения в воде, которая не координирована относительно кластерной кислоты и смешана с органическим растворителем, если количество кристаллизационной воды, содержащееся в катализирующей кластерной кислоте, присутствующей в реакционной системе, равно нормальному количеству кристаллизационной воды или меньше него (см. фиг.4). В этом тексте термин "количество кристаллизационной воды, содержащейся в катализирующей кластерной кислоте, присутствующей в реакционной системе, равно нормальному количеству кристаллизационной воды или меньше него" означает, что количество кристаллизационной воды, содержащееся в катализирующей кластерной кислоте, равно нормальному количеству кристаллизационной воды или меньше него, если вода, присутствующая в реакционной системе на стадии сепарации, равномерно воспринята всей катализирующей кластерной кислотой как кристаллизационная вода.
Примеры способа управления количеством воды, присутствующей в реакционной системе на стадии сепарации, включают способ, в котором вода, присутствующая в гидролизной смеси, выпаривается за счет разблокирования закрытого состояния реакционной системы и нагревания реакционной системы, а также способ, в котором к гидролизной смеси добавляется осушающее или подобное ему средство для удаления воды из гидролизной смеси. Когда применяется вышеописанный способ выпаривания, можно использовать остаточное тепло вследствие температуры реакции на стадии гидролиза, что приводит к блестящей энергетической эффективности, и, кроме того, стадия сепарации осушающего или подобного ему средства не нужна.
Таким образом, чем меньше количество кристаллизационной воды, содержащейся в катализирующей кластерной кислоте на стадии сепарации, тем лучше, причем оптимальное количество кристаллизационной воды может отличаться от такового на стадии гидролиза, когда требуется принимать во внимание температуру реакции гидролиза, преобразование, избирательность в отношении продукта и т.д. В соответствии с этим количество кристаллизационной воды, содержащееся в катализирующей кластерной кислоте, можно отрегулировать перед стадией гидролиза, принимая во внимание эффективность разделения сахарида и катализирующей кластерной кислоты на стадии сепарации, либо количество кристаллизационной воды, содержащееся в катализирующей кластерной кислоте, можно контролировать по мере необходимости между стадиями гидролиза и сепарации, как это описано выше.
На стадии сепарации осадок сахарида получают в виде твердого вещества наряду с остатками растительного волокнистого материала и т.д., в то же время получая раствор в органическом растворителе, содержащий растворенную катализирующую кластерную кислоту. Сепарацию твердых веществ и раствора в органическом растворителе осуществляют определенным способом, например фильтрацией. Твердые вещества, содержащие сахарид, можно сепарировать далее, разделяя их на водный раствор сахарида и твердые остатки сырья, при добавлении воды, то есть применяя способ, в котором используется растворимость сахарида в воде и нерастворимость остатков сырья в воде. С другой стороны, раствор в органическом растворителе, содержащий катализирующую кластерную кислоту, можно сепарировать на катализирующую кластерную кислоту и органический растворитель, применяя общепринятый способ сепарации, например выпаривание. Таким образом, катализирующую кластерную кислоту после ее применения в качестве катализатора гидролиза целлюлозы можно отделить от продукта, остатков сырья и т.д. и собрать, кроме того, также возможно повторно использовать катализирующую кластерную кислоту в качестве катализатора при гидролизе растительного волокнистого материала, содержащего целлюлозу.
Допустим, что на стадии сепарации избыточное количество кристаллизационной воды, содержащейся в катализирующей кластерной кислоте, смешивается с органическим растворителем, а сахарид, растворенный в этой воде, переносится в органическую фазу растворителя наряду с катализирующей кластерной кислотой. В таком случае можно осадить сахарид, присутствующий в органическом растворителе, понизив в этом растворе количество воды, в которой растворена катализирующая кластерная кислота. Более конкретно, катализирующую кластерную кислоту можно обезводить с тем расчетом, чтобы вся катализирующая кластерная кислота, растворенная в органическом растворителе, содержала кристаллизационную воду в таком количестве, которое равно нормальному количеству кристаллизационной воды или меньше него. Это делается потому, что можно предохранить сахарид, по большей части представленный глюкозой, от растворения в воде, которая включает молекулы воды, не имеющие возможности скоординироваться относительно катализирующей кластерной кислоты, то есть смешивающиеся с органическим растворителем (это осуществимо в том случае, если количество кристаллизационной воды, содержащееся в катализирующей кластерной кислоте, равно нормальному количеству кристаллизационной воды или меньше него, как описано выше).
Не существует особых ограничений в отношении способа обезвоживания катализирующей кластерной кислоты, растворенной в органическом растворителе, и примеры таких способов включают способ, в котором к органическому раствору добавляют соответствующее количество осушающего средства, например безводного хлорида кальция или силикагеля. Однако, если используется такое осушающее средство, то требуется еще одна стадия - удаление этого осушающего средства.
В качестве другого примера можно привести такой способ, когда в качестве осушающего средства используется катализирующая кластерная кислота, в которой долевое содержание кристаллизационной воды ((фактическое количество кристаллизационной воды)/(нормальное количество кристаллизационной воды)×100%) равно 70% или менее, предпочтительнее равно 30% или менее. Можно уменьшить количество кристаллизационной воды, содержащейся в катализирующей кластерной кислоте до уровня менее нормального количества кристаллизационной воды, добавив катализирующую кластерную кислоту в сухом состоянии, то есть увеличив количественное содержание катализирующей кластерной кислоты в растворе органического растворителя. В дополнение к этому, катализирующую кластерную кислоту, используемую в качестве осушающего средства, можно сепарировать и собрать наряду с катализирующей кластерной кислотой, используемой в качестве катализатора гидролиза. Сахарид, осажденный из раствора органического растворителя посредством обезвоживания, можно выделить из него и собрать, используя общепринятый способ, например декантацию или фильтрование.
В качестве примера способа разделения катализирующей кластерной кислоты и сахарида чаще всего приводится способ, основанный на различии между катализирующей кластерной кислотой и сахаридом по растворимости в растворителях. Однако, поскольку имеется различие по размеру молекул (гетерополикислота, которая является показательным примером катализирующих кластерных кислот, имеет диаметр молекулы приблизительно 2 нм, а глюкоза имеет диаметр молекулы приблизительно 0,7 нм), также можно использовать эффекты молекулярного просеивания через пористые материалы, такие как MFI-цеолит и β-цеолит, которые имеют десятичленные кольца с кислородом, а также морденит, который имеет двенадцатичленные кольца с кислородом.
В экспериментах, описанных ниже, измерение D-(+)-глюкозы и D-(-)-глюкозы проводили способом флуоресцентного выявления после внесения метки с применением жидкостной хроматографии высокого разрешения (HPCL).
Далее будет описан эксперимент по исследованию взаимосвязи между видимой температурой плавления и содержанием кристаллизационной воды в кластерной кислоте (гетерополикислоте). Видимая температура плавления фосфорновольфрамовой кислоты (Н3[PW12O40]·nH2O), которая содержала разное количество кристаллизационной воды, была визуально исследована при нагревании. Результаты показаны на фиг.2. Содержание кристаллизационной воды в фосфорновольфрамовой кислоте регулировали высушиванием (X (долевое содержание кристаллизационной воды 75%) и Y (долевое содержание кристаллизационной воды 100%)) при нагревании этих материалов или закапыванием в них воды. Процентное содержание кристаллизационной воды допускается равным 100%, если число молекул кристаллизационной воды составляет 30 (n=30). Как показано на фиг.2, было обнаружено, что, чем выше содержание кристаллизационной воды в гетерополикислоте, тем ниже видимая температура плавления (температура псевдоплавления) гетерополикислоты.
Пример 1. Как описано ниже, преобразование целлюлозы и избирательность образования глюкозы измеряли при одинаковой температуре реакции гидролиза (температуре псевдожидкого материала: 50°С, 60°С, 70°С, 80°С, 90°С). Вначале смешивали 1 кг фосфорновольфрамовой кислоты (процентное содержание кристаллизационной воды 160%, диаметр молекулы приблизительно 2 нм) и 0,5 кг целлюлозы (сухой вес), помещали смесь в закрытый контейнер, расположенный на плоской нагреваемой поверхности, и нагревали. Фосфорновольфрамовая кислота переходила в псевдожидкое регулируемое состояние при температуре приблизительно 40°С. Затем смесь нагревали до соответствующей температуры (50°С, 60°С, 70°С, 80°С, 90°С), перемешивали взбалтыванием и подвергали реакции гидролиза в течение трех часов.
После снижения температуры смеси до комнатной температуры к указанной смеси добавляли 3 литра этанола. После этого в закрытом контейнере смесь фосфорновольфрамовой кислоты, которая перешла из псевдожидкого состояния в твердое состояние, сахарида, в большей степени представленного глюкозой, полученной в процессе гидролиза целлюлозы, и волокна (включая такой трансформированный материал), такого как лигнин, перемешивали в течение 30 минут. Хотя фосфорновольфрамовая кислота была растворена в добавленном этаноле, сахарид не растворялся в этаноле и был получен в виде осадка наряду с волокном.
Осажденный сахарид и волокно фильтровали для отделения от раствора в этаноле и осаждали (сахарид и волокно). Затем к осадку добавляли 1,5 литра дистиллированной воды и перемешивали в течение 30 минут для растворения сахарида, а полученный раствор еще раз фильтровали для разделения водного раствора сахарида, в котором сахарид был растворен, и волокна (непрореагировавшей целлюлозы). С другой стороны, раствор этанола подвергали перегонке для разделения этанола и фосфорновольфрамовой кислоты.
Преобразование R и выход глюкозы η при соответствующих температурах реакции гидролиза показаны на фиг.3. Как можно увидеть на фиг.3, преобразование целлюлозы усиливается с увеличением температуры реакции. С другой стороны, хотя в случае преобразования целлюлозы выход глюкозы увеличивается в диапазоне от 50°С до 60°С, он достигает максимума при 70°С, а затем снижается с увеличением температуры. Таким образом, в условиях этого эксперимента было обнаружено, что глюкоза с высокой избирательностью образуется при температуре от 50°С до 60°С, тогда как в диапазоне температур от 70°С до 90°С протекают другие реакции, не связанные с образованием глюкозы. Вполне вероятно, что этот результат может варьироваться в зависимости от вида реактора, путей процесса и т.д., то есть можно сказать, что для получения высокого выхода продукта и повышения избирательности также важна оптимизация используемой аппаратуры.
Пример 2. Жмых сахарного сырья измельчали при помощи мельницы тонкого помола в порошок с размером частиц приблизительно десять с лишним микронов, после чего 0,3 кг этого порошка (сухой вес) и 1 кг фосфорновольфрамовой кислоты (содержание кристаллизационной воды неизвестно; диаметр молекул составляет приблизительно 2 нм) перемешивали, помещали в закрытый контейнер и нагревали. Фосфорновольфрамовая кислота переходила в псевдожидкое регулируемое состояние при температуре приблизительно 40°С. Смесь нагревали приблизительно до 50°С и перемешивали еще в течение трех часов.
После снижения температуры смеси до комнатной температуры к указанной смеси А добавляли 3 литра этанола, после этого в закрытом контейнере смесь А фосфорновольфрамовой кислоты, которая перешла из псевдожидкого состояния в твердое состояние, сахарида, в большей степени представленного глюкозой, полученной в процессе гидролиза целлюлозы, и волокна (включая такой трансформированный материал как лигнин) перемешивали в течение 30 минут. Хотя фосфорновольфрамовая кислота была растворена в добавленном этаноле, сахарид не растворялся в этаноле и был получен в виде осадка наряду с волокном.
Осажденный сахарид и волокно фильтровали для отделения от раствора в этаноле и осаждали (сахарид и волокно). Затем к осадку добавляли 1 литр дистиллированной воды и перемешивали в течение 30 минут для растворения сахарида, а полученный раствор еще раз фильтровали для разделения водного раствора сахарида, в котором был растворен, и волокна (непрореагировавшей целлюлозы). С другой стороны, раствор этанола подвергали перегонке для разделения этанола и фосфорновольфрамовой кислоты. Выход глюкозы составил 0,20 кг, а выход ксилозы составил 0,06 кг.
Пример 3. Древесную щепу дробили, в течение двух часов обрабатывали паром, а затем измельчали при помощи мельницы тонкого помола в порошок с размером частиц приблизительно десять с лишним микронов, после чего 0,3 кг этого порошка (сухой вес) и приблизительно 1 кг фосфорновольфрамовой кислоты (содержание кристаллизационной воды неизвестно) перемешивали, помещали в закрытый контейнер и нагревали. Фосфорновольфрамовая кислота переходила в псевдожидкое регулируемое состояние при температуре приблизительно 40°С. Смесь нагревали приблизительно до 70°С и перемешивали еще в течение трех часов. После этого собирали фосфорновольфрамовую кислоту, применяя способ, аналогичный описанному в примере 2, а полученный сахарид и непрореагировавшую целлюлозу сепарировали. Выход глюкозы составил 0,21 кг, а выход ксилозы составил 0,07 кг.
Пример 4. Как и в случае, описанном в японской патентной заявке №2001-240411 (JP-A-2001-240411), был приготовлен цилиндр из пористого глинозема с мембраной из морденита на внешней стороне. Смесь А, полученную способом, сходным с описанным в примере 2, разбавляли 1 литром дистиллированной воды, переносили в цилиндр и выдерживали в течение часа под давлением 2 МПа, приложенным к содержимому цилиндра. Во время выполнения этих действий цилиндр был погружен в 1 литр дистиллированной воды.
Часом позже отбирали пробу воды, в которую был погружен цилиндр, и подвергали образец анализу методом жидкостной хроматографии высокого разрешения (HPLC). В результате было подтверждено, что в воде содержались D-(+)-глюкоза и D-(+)-ксилоза. Одновременно проводили отбор образца жидкости внутри цилиндра и анализировали этот образец методом HPLC. В результате было подтверждено, что концентрация сахарида упала. Когда концентрация сахарида (глюкозы и ксилозы) в жидкости внутри цилиндра падала до одной десятой начальной концентрации, вышеописанный процесс повторяли. В то же время фосфорновольфрамовую кислоту, оставшуюся в воде внутри цилиндра, собирали как твердую фосфорновольфрамовую кислоту.
Пример 5. Прежде всего были приготовлены смеси, в которых были перемешаны фосфорновольфрамовая кислота с различным содержанием кристаллизационной воды (см. фиг.4) и глюкозы в соотношении 2:1 ((фосфорновольфрамовая кислота):(глюкоза) (весовое соотношение)). Для фосфорновольфрамовой кислоты с процентным содержанием кристаллизационной воды 100% или более содержание кристаллизационной воды в фосфорновольфрамовой кислоте регулировали, при необходимости добавляя к смеси соответствующее количество воды с тем расчетом, чтобы фосфорновольфрамовая кислота в смеси после перемешивания фосфорновольфрамовой кислоты с глюкозой содержала желательное количество воды. С другой стороны, для фосфорновольфрамовой кислоты с процентным содержанием кристаллизационной воды менее 100% фосфорновольфрамовую кислоту заблаговременно нагревали и обезвоживали. Количество воды, содержащейся в фосфорновольфрамовой кислоте после обезвоживания измеряли способом TGA (термогравиметрического анализа). Затем к смеси фосфорновольфрамовой кислоты и глюкозы добавляли обезвоженный этанол в весовом соотношении этанола и фосфорновольфрамовой кислоты 100/30. После хорошего перемешивания и взбалтывания смеси сепарировали твердые вещества, включая осажденную глюкозу, для получения раствора этанола. Количество глюкозы в этом растворе этанола анализировали и измеряли флуоресцентным выявлением после внесения метки, используя HPCL, чтобы расчетным способом определить потерю глюкозы, которая указывает на относительное количество глюкозы, оставшейся в растворе этанола и не поддающейся сепарации. Результаты показаны на фиг.4.
Фиг.4 показывает, что если процентное содержание кристаллизационной воды в фосфорновольфрамовой кислоте составляет 100% или менее, то относительная потеря глюкозы по отношению к фосфорновольфрамовой кислоте почти равна нулю. Более конкретно, доводя количественное содержание кристаллизационной воды в кластерной кислоте до нормального количества кристаллизационной воды или менее, можно свести к минимуму потери выхода сахарида, которые обусловлены растворением сахарида в воде, не координированной относительно кластерной кислоты и смешанной с органическим растворителем на том этапе, когда кластерную кислоту и сахарид сепарируют, осаждая сахарид при помощи органического растворителя.
Пример 6. В закрывающийся контейнер заблаговременно наливали дистиллированную воду, после чего температуру дистиллированной воды поднимали до заранее определенной температуры реакции (60°С) для насыщения внутреннего содержимого контейнера парами воды и инициации контакта водяного пара с внутренними стенками контейнера. Затем перемешивали 1 кг фосфорновольфрамовой кислоты с заранее измеренным количественным содержанием кристаллизационной воды и 0,5 кг целлюлозы (сухой вес), помещая смесь в закрывающийся контейнер. В дополнение к этому добавляли дистиллированную воду (55,6 г), количество которой было равно тому количеству, в котором вода, присутствующая в реакционной системе, приближается к сумме количества воды (158 г), которое требуется для приведения фосфорновольфрамовой кислоты в псевдожидкое состояние при температуре реакции 60°С, и количества воды (55,6 г), которое требуется для гидролиза целлюлозы в глюкозу.
Если затем закрытый контейнер нагревали, то фосфорновольфрамовая кислота переходила в псевдожидкое состояние, начиная с температуры приблизительно 40°С, и переходила в такое состояние, которое позволяло перемешивать и взбалтывать смесь в контейнере, при температуре приблизительно 50°С. Смесь дополнительно нагревали до 60°С и перемешивали в течение 1,5 часа при 60°С. Затем нагревание прекращали, охлаждая смесь приблизительно до 40°С. После этого добавляли 6 литров этанола, смесь перемешивали в течение 60 минут для растворения фосфорновольфрамовой кислоты в этаноле и сахарид осаждали вместе с остаточным волокном (непрореагировавшей целлюлозой).
Затем осадок фильтровали, к сепарированному осадку добавляли 1 литр дистиллированной воды и смесь перемешивали в течение 15 минут для растворения сахарида. Смесь снова фильтровали для сепарирования водного раствора сахарида и волокна. С другой стороны, раствор этанола подвергали перегонке для разделения этанола и фосфорновольфрамовой кислоты. Преобразование R составило 67%, а выход глюкозы η составил 60%.
Пример 7. В закрытом контейнере перемешивали 1 кг фосфорновольфрамовой кислоты с содержанием кристаллизационной воды 100% (показано точкой Y на фиг.2) и 0,5 кг целлюлозы (сухой вес), добавляя к смеси дистиллированную воду (55,6 г) с тем расчетом, чтобы обеспечить количество воды, необходимое для гидролиза 0,5 кг целлюлозы в глюкозу. Когда эту смесь нагревали, фосфорновольфрамовая кислота переходила в псевдожидкое состояние при температуре приблизительно 50°С, а при температуре приблизительно 60°С она переходила в такое состояние, которое позволяло эффективно перемешивать смесь. Смесь продолжали перемешивать в течение 1,5 часа, поддерживая ее температуру на уровне 60°С.
После этого собирали фосфорновольфрамовую кислоту, применяя способ, аналогичный описанному в примере 6, а полученный сахарид и непрореагировавшую целлюлозу сепарировали. Преобразование R составило 68%, а выход глюкозы η составил 63%.
Пример 8. В закрытом контейнере перемешивали 1 кг фосфорновольфрамовой кислоты с содержанием кристаллизационной воды 75% (показано точкой Х на фиг.2) и 0,5 кг целлюлозы (сухой вес), добавляя к смеси дистиллированную воду (55,6 г) с тем расчетом, чтобы имелось количество воды, необходимое для гидролиза 0,5 кг целлюлозы в глюкозу. Когда эту смесь нагревали, фосфорновольфрамовая кислота не переходила в псевдожидкое состояние даже при нагревании до 50°С. Смесь постепенно переходила в псевдожидкое состояние при температуре приблизительно 80°С, а в состояние, когда ее можно было эффективно перемешивать, - при температуре приблизительно 90°С. Смесь продолжали перемешивать в течение 1,5 часа, поддерживая ее температуру на уровне 90°С.
После этого собирали фосфорновольфрамовую кислоту, применяя способ, аналогичный описанному в примере 6, а полученный сахарид и непрореагировавшую целлюлозу сепарировали. Преобразование R составило 96%, а выход глюкозы η составил 72%. Расчетный результат выхода ксилозы составил 7%. Хотя имело место очень высокое преобразование 96%, потери при получении глюкозы, которая была желательным веществом, составили 28%. Этот результат показывает, что количественное содержание кристаллизационной воды в фосфорновольфрамовой кислоте, использованной в примере 8, было меньше, чем в фосфорновольфрамовой кислоте, использованной в примере 7, а для переведения фосфорновольфрамовой кислоты в псевдожидкое состояние требовалась более высокая температура реакции, чем в примере 5; хотя превращение было высоким, избирательность образования глюкозы посредством гидролиза снижалась, а количество других побочных продуктов увеличивалось.
Пример 9. Был проведен эксперимент в соответствии с блок-схемой, показанной на фиг.5. Более конкретно, способом, аналогичным примеру 6, была приготовлена смесь перемешиванием целлюлозы, фосфорновольфрамовой кислоты и дистиллированной воды в закрытом контейнере при 60°С в течение 1,5 часа. После этого закрытый контейнер открывали, поддерживая в нем температуру 60°С, для отгонки воды из контейнера. Температуру поддерживали на уровне 60°С какое-то время и после затвердения жидкости в контейнере, а затем наагревание прекращали. После этого собирали фосфорновольфрамовую кислоту, применяя способ, аналогичный описанному в примере 6, а полученный сахарид и непрореагировавшую целлюлозу сепарировали. Преобразование R составило 67%, а выход глюкозы η составил 67%. То есть было собрано почти 100% полученной глюкозы.
Этот результат показывает, что можно предотвратить растворение глюкозы в воде, которая не координирована относительно фосфорновольфрамовой кислоты и смешана с этанолом, то есть улучшить выход глюкозы за счет удаления воды из реакционной системы (уменьшения количественного содержания кристаллизационной воды в фосфорновольфрамовой кислоте до ниже нормального количества кристаллизационной воды до стадии сепарации фосфорновольфрамовой кислоты от сахарида и волокна при добавлении этанола).
Пример 10. Аналогичным примеру 4 способом была приготовлена смесь посредством перемешивания в закрытом контейнере целлюлозы, фосфорновольфрамовой кислоты и дистиллированной воды при температуре 60°С в течение 1,5 часа. После этого к смеси добавляли заранее определенное количество (3 литра) этанола, поддерживая температуру на уровне 60°С, и перемешивали смесь еще 30 минут. Затем температуру смеси понижали приблизительно до уровня комнатной температуры и добавляли осушающее средство, упакованное в мешочек (частицы безводного хлорида кальция) для удаления воды из содержимого контейнера. Порошок глюкозы осаждали, а фосфорновольфрамовую кислоту растворяли в этаноле. Способом, аналогичным примеру 6, проводили сепарацию фосфорновольфрамовой кислоты и сахарида. Преобразование R составило 67%, а выход глюкозы составил 67%. Было собрано почти 100% полученной глюкозы.
Как и в том случае, который описан выше в примере 9, этот результат показывает, что можно предотвратить растворение глюкозы в воде, которая не координирована относительно фосфорновольфрамовой кислоты и смешана с этанолом, то есть улучшить выход глюкозы за счет удаления воды из реакционной системы (уменьшения количественного содержания кристаллизационной воды в фосфорновольфрамовой кислоте до ниже нормального количества кристаллизационной воды до стадии сепарации фосфорновольфрамовой кислоты от сахарида и волокна при добавлении этанола). В описанном выше примере 9 воду, присутствующую в реакционной системе, выпаривали, применяя остаточное тепло вследствие гидролиза целлюлозы, а в примере 10 количество воды в реакционной системе регулировали, добавляя осушающее средство, которому давали возможность абсорбировать воду.
Несмотря на то, что изобретение было описано со ссылками на показательные варианты его осуществления, необходимо понимать, что изобретение не ограничивается описанными вариантами осуществления или толкованиями. Помимо описанных примеров изобретение охватывает различные модификации и эквиваленты. В дополнение к этому следует отметить, что помимо различных элементов иллюстративных примеров осуществления изобретения, показанных в различных комбинациях и конфигурациях, возможны другие комбинации и конфигурации, включающие большее или меньшее число элементов либо только один элемент, которые также соответствуют сущности и объему изобретения.
Изобретение относится к переработке волокнистого материала растительного происхождения. Согласно изобретению целлюлозу, содержащуюся в растительном волокнистом материале, гидролизуют с использованием в качестве катализатора псевдожидкой кластерной кислоты с получением моносахарида, который в наибольшей степени представлен глюкозой. После получения моносахарида его осаждают с применением органического растворителя, затем сепарируют от остатков сырья и от кластерной кислоты. Изобретение позволяет снизить энергоемкость способа. 25 з.п. ф-лы, 6 ил.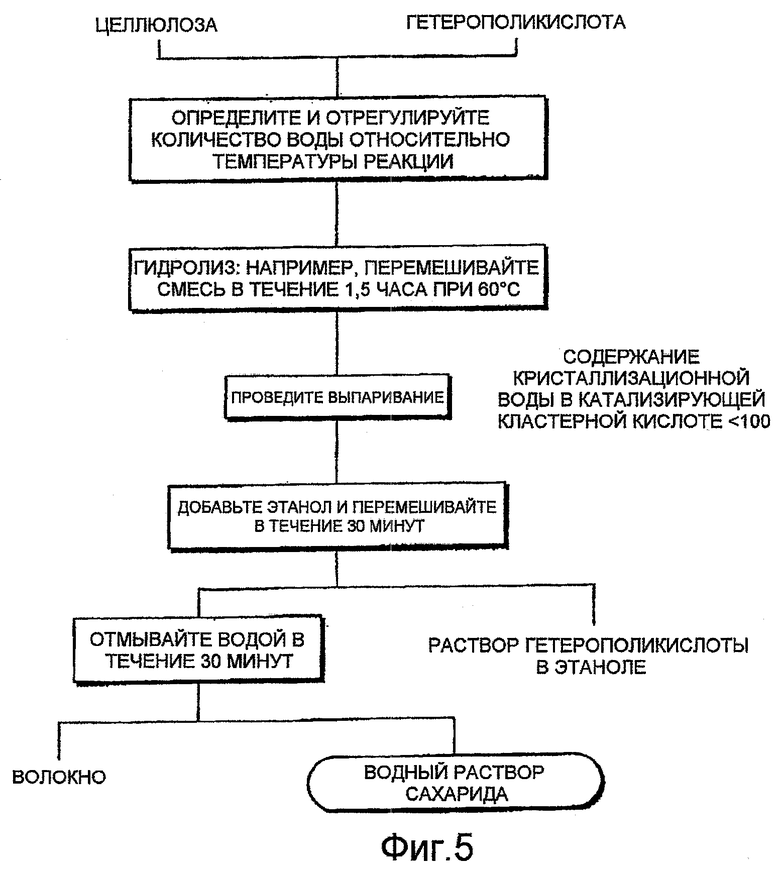
1. Способ получения моносахаридов, большей частью представленных глюкозой, включающий гидролиз целлюлозы, содержащейся в растительном волокнистом материале, отличающийся тем, что в качестве катализатора для гидролиза целлюлозы применяется псевдожидкая кластерная кислота.
2. Способ по п.1, в котором гидролиз целлюлозы осуществляется при температуре 140°С или ниже и при давлении от атмосферного до 1 МПа.
3. Способ по п.2, в котором гидролиз целлюлозы осуществляется при температуре 120°С или ниже.
4. Способ по п.3, в котором гидролиз целлюлозы осуществляется при температуре 100°С или ниже.
5. Способ по п.1, в котором массовое соотношение между растительным волокнистым материалом и кластерной кислотой находится от 1:1 до 1:4.
6. Способ по любому одному из пп.1-5, в котором количество воды в гидролизной реакционной системе равно или превышает сумму i) количества кристаллизационной воды, необходимого для переведения всей кластерной кислоты в гидролизной реакционной системе в псевдожидкое состояние в температурных условиях, способствующих гидролизу, и ii) количества воды, необходимого для гидролиза всей целлюлозы в гидролизной реакционной системе в глюкозу.
7. Способ по п.1, в котором кластерная кислота представляет собой гетерополикислоту.
8. Способ по п.7, в котором гетерополикислота выбрана из группы, состоящей из фосфорновольфрамовой кислоты, кремневольфрамовой кислоты и фосфорномолибденовой кислоты.
9. Способ по п.7 или 8, в котором гетерополикислота имеет структуру Кеггина.
10. Способ по п.7 или 8, в котором гетерополикислота имеет структуру Доусона.
11. Способ по п.1, дополнительно включающий:
осаждение моносахарида с применением органического растворителя после образования глюкозы и
сепарирование моносахарида, включая моносахарид, отвердевший во время гидролиза, и осажденный сахарид, от остатков сырья и от кластерной кислоты.
12. Способ по п.11, в котором растворимость моносахарида в органическом растворителе равна 0,6 г/100 мл или менее.
13. Способ по п.12, в котором растворимость моносахарида в органическом растворителе равна 0,06 г/100 мл или менее.
14. Способ по п.12, в котором растворимость кластерной кислоты в органическом растворителе равна 20 г/100 мл или более.
15. Способ по п.14, в котором растворимость кластерной кислоты в органическом растворителе равна 40 г/100 мл или более.
16. Способ п.11, в котором в качестве органического растворителя используется, по меньшей мере, один растворитель, выбранный из эфирных растворителей и спиртовых растворителей.
17. Способ по п.16, в котором органическим растворителем является этанол.
18. Способ по п.16, в котором органическим растворителем является диэтиловый эфир.
19. Способ по любому одному из пп.11-18, в котором количество воды в реакционной системе для сепарации моносахарида регулируется таким образом, что вся кластерная кислота в реакционной системе для сепарации моносахарида содержит кристаллизационную воду в количестве, равном нормальному количеству кристаллизационной воды или менее.
20. Способ по п.11, в котором после сепарации моносахарида кластерную кислоту обезвоживают так, что вся кластерная кислота в органическом растворителе содержит кристаллизационную воду в количестве, равном нормальному количеству кристаллизационной воды или менее.
21. Способ по п.20, в котором кластерная кислота, содержащая кристаллизационную воду в количестве, равном нормальному количеству кристаллизационной воды или менее, применяется в качестве осушающего средства для обезвоживания кластерной кислоты.
22. Способ по п.21, в котором содержание кристаллизационной воды в кластерной кислоте, используемой в качестве осушающего средства, равно 70% или менее.
23. Способ по п.22, в котором содержание кристаллизационной воды в кластерной кислоте, используемой в качестве осушающего средства, равно 30% или менее.
24. Способ по п.11, дополнительно включающий выделение кластерной кислоты, растворенной в органическом растворителе, из органического растворителя.
25. Способ по п.24, в котором кластерную кислоту, выделенную из органического растворителя, повторно применяют в качестве катализатора для гидролиза целлюлозы, содержащейся в растительном волокнистом материале.
26. Способ по любому одному из пп.1-5, 11-18 и 20-25, в котором растительный волокнистый материал представляет собой биомассу на основе целлюлозы.
| JP 11343301 A, 14.12.1999 | |||
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| JP 03093755 A, 18.04.1991 | |||
| Способ получения сахаров | 1983 |
|
SU1142510A1 |
| Способ получения сахара из целлюлозусодержащего растительного сырья | 1980 |
|
SU949002A1 |
| СПОСОБ ПРОИЗВОДСТВА ЭТАНОЛА ИЗ ЦЕЛЛЮЛОЗОСОДЕРЖАЩИХ ОТХОДОВ (ВАРИАНТЫ) И СПОСОБ ПОЛУЧЕНИЯ ГЛЮКОЗЫ ИЗ ЦЕЛЛЮЛОЗОСОДЕРЖАЩИХ ОТХОДОВ | 1994 |
|
RU2159816C2 |
| СПОСОБ ПРОИЗВОДСТВА САХАРОВ ИЗ МАТЕРИАЛОВ, СОДЕРЖАЩИХ ЦЕЛЛЮЛОЗУ И ГЕМИЦЕЛЛЮЛОЗУ, СПОСОБ ОТДЕЛЕНИЯ КИСЛОТЫ И САХАРОВ ОТ ЖИДКОСТЕЙ, ПОЛУЧЕННЫХ ЭТИМ СПОСОБОМ ПРОИЗВОДСТВА, СПОСОБ СБРАЖИВАНИЯ САХАРОВ, ПОЛУЧЕННЫХ ЭТИМ СПОСОБОМ ПРОИЗВОДСТВА, И СПОСОБ ПЕРЕРАБОТКИ ТВЕРДЫХ ВЕЩЕСТВ, ПОЛУЧЕННЫХ ЭТИМ СПОСОБОМ ПРОИЗВОДСТВА | 1994 |
|
RU2144087C1 |
Авторы
Даты
2012-01-20—Публикация
2008-04-25—Подача