Изобретение относится к области фармации, медицины и ветеринарии, а именно к новым лекарственным средствам для лечения воспалительных и аллергических заболеваний.
Съедобные морские ежи, помимо промыслового объекта для пищевой промышленности, являются богатым источником уникальных биологически активных веществ. К таким веществам относятся полигидроксинафтохиноновые пигменты панцирей и игл морских ежей - спинохромы. В отличие от эндогенных антиоксидантов, таких как витамин Е и убихинон, нафтохиноны способны нейтрализовать действие основных инициаторов неферментативного процесса окисления мембранных липидов - катионов железа, накапливающихся в зоне ишемического повреждения ткани. Такие особенности механизма действия выделяют спинохромы из ряда известных биоантиоксидантов и открывают перспективу для создания на их основе лекарственных препаратов нового поколения.
Известна композиция, содержащая производные природных или синтетических полигидроксинафтохинонов (алкил-, гидроксиалкил-, ацил-, нитро-, амино- или галогенпроизводные) с фунги-, альго-, герби- и бактерицидными свойствами (Pat. Appl. GB2159056A, publ.27.11.1985).
Известна фармацевтическая композиция, содержащая в качестве активного ингредиента этилацетатный экстракт панцирей морских ежей, обладающая антитромботическим действием и рекомендованная при гипертензии и заболеваниях сердечно-сосудистой системы, связанных с повышенным тромбообразованием, таких как инфаркт миокарда, инсульт и пр. (Pat. Appl. KR20020091909A, опубл. 11.12.2002).
Ацетоновый экстракт панцирей морских ежей Strongylocentrotus nudus входит в состав фармацевтической композиции, применение которой рекомендовано для снижения уровня общего холестерина при гипертонии, заболеваниях сердечно-сосудистой системы и нарушениях мозгового кровообращения (Pat. Appl. KR 20020085543 А, опубл. 16.11.2002).
Известна биологически активная добавка (БАД) к пище, обладающая гиполипидимическим и антиоксидантным действием, содержащая в своем составе экстракт плоских морских ежей, содержащий 0,75-0,85% эхинохрома A (Pat. RU 2340216 С1, опубл. 10.12.2008).
Известна композиция, содержащая экстракт гонад, кишок или панцирей морских ежей (Anthocidaris crassispina, Hemicentrotus pulcherrimus, Pseudocentrotus depressus или Strongylocentrotus internmedius} для профилактики и лечения заболеваний печени, обладающая антиоксидантным и детоксифицирующим действием (Pat. Appl. KR20110001251 A, publ. 06.01.2011).
Спиртовой раствор, содержащий эхинохром А в комплексе с хитозаном, аскорбиновой, липоевой, лимонной и янтарной кислотами используется для коррекции патологических нарушений углеводного, липидного и антиоксидантного статуса организма(Pat RU2360683 С1, опубл. 16.04.2008).
Наиболее близким к настоящему изобретению является препарат Гистохром, применяемый для лечения воспалительных заболеваний сетчатки и роговицы глаз, представляющий собой 0,02% изотонический раствор ди- и тринатриевых солей пигмента из группы спинохромов - эхинохрома A (Pat. RU 2134107 С1, опубл. 10.08.1999).
Задачей изобретения является создание средства, содержащего в качестве активного компонента биологически активный комплекс, получаемый из панцирей и игл зеленых морских ежей Strongylocentrotus droebachiensis, содержащий в своем составе от 0,02% до 10% пигментного комплекса, содержащего спинохромы В и D, а так же димерные полигидроксинафтохиноны и от 7,5% до 20% минеральной составляющей панциря морских ежей (кальций, магний, фосфор, натрий, калий) в виде водорастворимых солей, для местного применения в форме глазных капель, интраназальных капель и спрея, оказывающего противовоспалительное и противоаллергическое действие, не токсичное, удобное в использовании и стабильное при хранении.
Поставленная задача решается созданием средства при следующем содержании компонентов в г на 100 г:
Пигментно-минеральный комплекс - 0,05-2,0;
Сорастворитель - 0,01-10;
Консервант - 0,01-0,2
Антиоксидант - 0,01-0,2
Регулятор кислотности -до рН раствора 6,0-8,0
Вода -до 100.
Способ получения средства реализуется следующим образом: консервант смешивают с водой для инъекций при температуре 80-90°С и перемешивают до полного растворения. После охлаждения до температуры 35-40°С к раствору добавляют рассчитанное количество сорастворителя, антиоксиданта и перемешивают до получения прозрачного раствора. Затем в раствор вводят пигментно-минеральный комплекс и доводят рН раствора до 6,0-8,0 с помощью регулятора кислотности. Раствор фильтруют и разливают во флаконы. При необходимости проводят стерилизацию.
В частности для стерилизации могут быть использованы стерильная фильтрация или термическая стерилизация паром под давлением.
Нами установлено, что порядок смешивания ингредиентов имеет существенное значение для обеспечения стабильности пигментно-минерального комплекса. Он имеет высокий окислительно-восстановительный потенциал и легко окисляется. Для обеспечения фармакологической активности пигментно-минерального комплекса, такой как ингибирование свободнорадикального окисления липидов клеточных мембран, модулирование синтеза простагландинов, повышения активности антиоксидантных ферментов организма и т.п., необходима его защита от окисления в процессе приготовления, хранения. Опытным путем установлено, что существенным фактором для обеспечения стабильности композиции при хранении является введение в ее состав антиоксиданта, в качестве которого предлагаются натрия метабисульфит, натрия сульфит, натрия тиосульфат или аскорбиновая кислота.
Использование в составе композиции пигментно-минерального комплекса в концентрации 0,05-2,0 мас.% обеспечивает терапевтическую активность и хорошую переносимость препарата. Увеличение его концентрации свыше указанного предела нежелательно и приводит к изменению изотоничности и изогидричности раствора, а также экономически не оправдано.
Опытным путем нами установлено, что введение в состав средства консерванта необходимо для создания стабильной в течение длительного срока (не менее 2 лет) композиции пигментно-минерального комплекса в виде раствора, а также с учетом многократного их использования после вскрытия упаковки, способствующего микробной контаминации. В качестве консерванта могут быть использованы фармацевтически приемлемые консерванты такие как п-гидроксибензоаты низших алкилов (например, нипагин, нипазол), хлоргексидин в форме ацетата или глюконата и фармацевтически применимые четвертичные соединения аммония (хлорид бензалкония и/или бензагексония).
В состав средства введен сорастворитель, который позволяет повысить при необходимости концентрацию пигментно-минерального комплекса в составе средства, улучшает биологическую доступность действующего вещества. В качестве сорастворителя могут быть использованы фармацевтически приемлемые растворители, такие как спирт этиловый, полисорбат 80, полиэтиленгликоль, пропиленгликоль, глицерин, полиоксиэтилен-40-глицерол-гидроксистеарат, моноэтиловый эфир диэтиленгликоля, поливинилпирролидон, поливиниловый спирт.
Введение регулятора кислотности осуществлено с целью создания комфортной для клеток среды, не вызывающей их повреждения или чувства жжения. Используются натриевые соли угольной кислоты, этилендиаминтетрауксусная кислота в виде три-, тетранатриевых солей, гидроксид натрия, как наиболее соответствующие жидким средам организма.
Технический результат, обеспечиваемый настоящим изобретением, заключается в применении пигментно-минерального комплекса, полученного из панцирей и игл морских ежей, в качестве средства, которое оказывает противовоспалительное и противоаллергическое действие путем блокирования Н1 гистаминовых рецепторов.
Приведенная совокупность отличительных признаков заявляемого способа в литературе не описана, а их влияние на достижение технического результата не следует из известного уровня знаний в области технологии производства лекарственных препаратов.
Технический результат изобретения заключается также в получении безопасного средства на основе пигментно-минерального комплекса в виде готовой лекарственной формы для местного применения (капли или спрей) с выраженным терапевтическим эффектом. Новое свойство пигментно-минерального комплекса из панцирей и игл морских ежей установлено авторами впервые экспериментально.
Состав пигментно-минерального комплекса находится в прямой зависимости от способа получения (Pat. RU №2441661 (С1), опубл. 10.02.2012).
Таким образом, предлагаемое техническое решение соответствует критериям изобретения, а именно «новизна», «изобретательский уровень» и «промышленная применимость».
Возможность реализации заявляемого изобретения показана, но не ограничена, в примерах конкретного выполнения.
Пример 1. Глазные капли (в г на 100 г). В подходящем сосуде с мешалкой, термостатируемом при 80-90°С, в 91,9 мл воды для инъекций растворяют 0,1 г нипагина. Полученный раствор охлаждают до температуры 35°С, добавляют 0,1 г аскорбиновой кислоты, перемешивают, добавляют 3,5 г спирта этилового, перемешивают до получения прозрачного раствора. В раствор вводят 0,05 г пигментно-минерального комплекса и корректируют уровень рН добавлением 4,35 г гидрокарбоната натрия. После фильтрования получают раствор с рН около 6,2. Проводят розлив в стеклянные флаконы объемом 5 мл с последующей стерилизацией в автоклаве при температуре 100°С в течение 30 минут. Получают 19 флаконов (с учетом потерь) по 5 мл глазных капель, содержащих 0,05% пигментно-минерального комплекса.
Пример 2. Капли назальные, спрей (в г на 100 г). В подходящем сосуде с мешалкой, термостатируемом при 80-90°С, в 93,4 мл воды для инъекций растворяют 0,05 г хлорида бензалкония. Полученный раствор охлаждают до температуры 35°С, добавляют 0,15 г натрия метабисульфит, 2,5 г поливинилпирролидона, перемешивают до получения прозрачного раствора. В полученный раствор вносят 1,0 г пигментно-минерального комплекса и корректируют уровень рН полученного раствора до 7,0 добавлением 2,9 г этилендиаминтетрауксусной кислоты в виде дигидрата двунатриевой соли. После фильтрования получают раствор с рН около 7. Готовый раствор фильтруют, подвергают стерилизующей фильтрации в токе азота и затем разливают и укупоривают в асептических условиях в пенициллиновые флаконы темного стекла, снабженные дозаторами-капельницами или распылительной насадкой для спрея, объемом 5 мл. Получают 19 флаконов (с учетом потерь) по 5 мл, содержащих 1,0% пигментно-минерального комплекса.
Пример 3. Противоаллергическая активность in vivo на модели аллергического конъюнктивита.
Аллергический конъюнктивит (АК) индуцировали путем местного нанесения 0,1 мл раствора «Compound 48/80» (10 мг/мл) на конъюнктиву глаза кролика (серая шиншилла). Средство по примеру 1 с содержанием пигментно-минерального комплекса в количестве 0,05% и препараты сравнения Опатанол (0,1% раствор олопатадина гидрохлорида) и Гистохром вводили интраконъюнктивально по 0,05 мл по лечебно-профилактической схеме: 1 раз в день в течение 3 дней до индукции патологии и через 10, 30, 45 и 100 минут после индукции патологии.
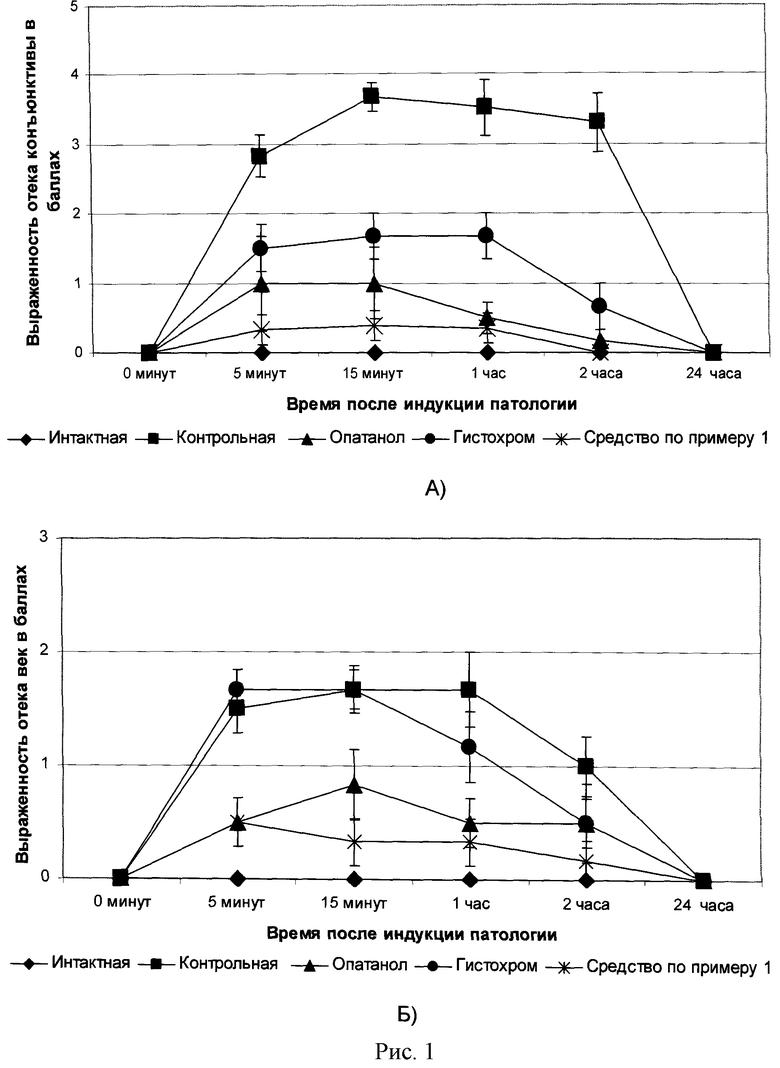
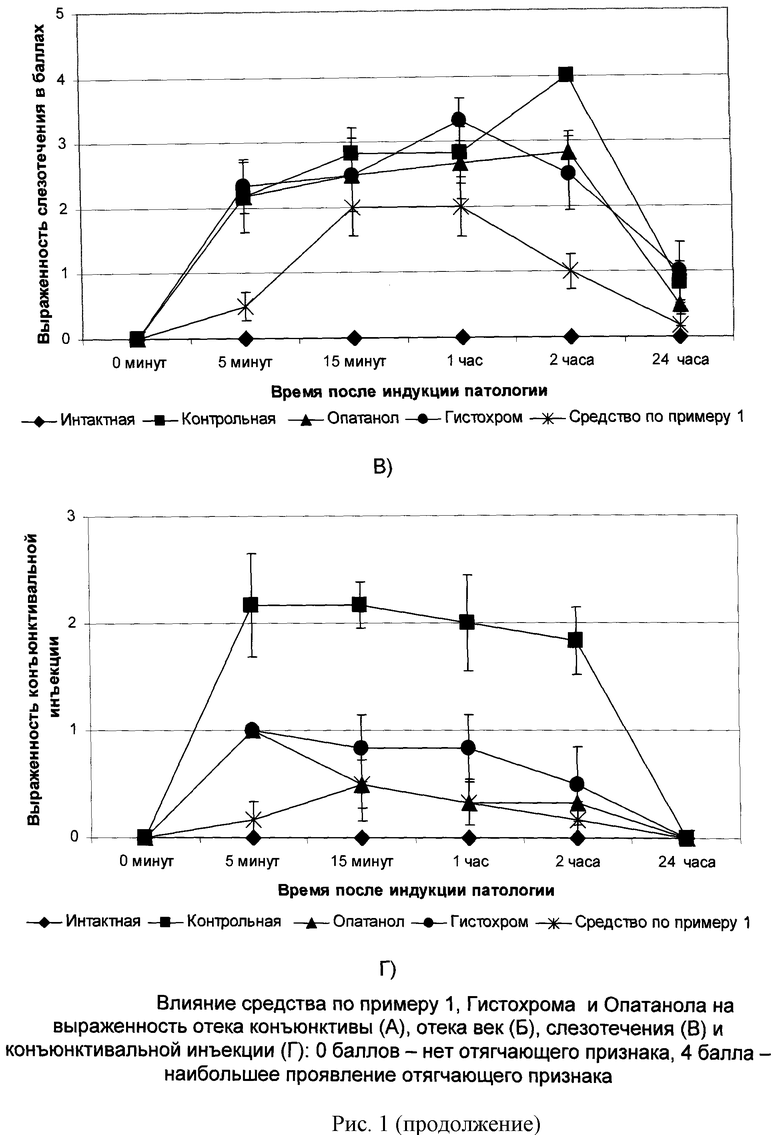
Состояние поверхностных структур и переднего отдела глаза оценивали по балльной системе (Miyazaki et at. Conjunctival mast cell as a mediator of eosinophilic response in ocular allergy // Mol. Vis. 2008. 14. 1525-1532) по показателям: отек конъюнктивы, отек век, слезотечение, конъюнктивальная инъекция до нанесения и через 5, 15 минут, 1, 2 и 24 часа после нанесения раствора Compound 48/80 (рисунок 1).
Противоаллергическая активность средства по примеру 1 по всем исследованным показателям превосходила активность препаратов сравнения. При суммарной оценке баллов за весь период наблюдения установили, что Противоаллергическая активность средства по примеру 1 в отношении внешних признаков проявления аллергического конъюнктивита практически в 3 раза выше, чем у Гистохрома и на 50% превосходит противоаллергическую активность Опатанола.
Пример 4. Влияние средства на чувствительность H1-гистаминовых рецепторов ех vivo
Эксперименты с изолированными тканями позволяют получать полноценные и точные данные о направленности и механизме действия тех или иных медиаторов непосредственно на рецепторный аппарат тканей и органов.
Способность средства по примеру 1 с содержанием пигментно-минерального комплекса в количестве 0,05% связываться с H1-гистаминовыми рецепторами оценивали методом гистамин-индуцированного сокращения подвздошной кишки морской свинки.
Подвздошную кишку извлекали из брюшной полости наркотизированных животных и помещали в емкость с охлажденным до+4°С буфером Кребса-Хенселейта (БКХ). Затем подвздошную кишку разрезали на фрагменты около 1 см длиной, фрагменты закрепляли в проточных камерах и перфузировали оксигенированным БКХ при температуре +30°С в течение 60 минут, после этого проточные камеры заполняли 80 mM KCl, что вызывало сильное сокращение сегментов кишки. Полученные результаты в дальнейшем принимались за 100% сокращения.
Возобновляли перфузию оксигенированным БКХ при температуре +30°С для отмывки тканей и восстановления их способности к сокращению. Через 60 минут отмывки проводили перфузию раствором средства по примеру 1 в БКХ. Концентрация средства по примеру 1 в конечном растворе составляла от 1 до 10 мкл/мл. В качестве препарата сравнения использовали пириламина малеат (10 мкМ). После тридцатиминутного инкубационного периода, растворы сливали, а проточные камеры заполняли водным раствором гистамина (1 мкМ). В течение 10 минут осуществляли регистрацию силы сокращения, оценивали амплитуду и время наступления максимального ответа (таблица 1).
Средство по примеру 1 во всех предложенных концентрациях блокировало H1-гистаминовые рецепторы сарколеммы гладких мышц подвздошной кишки. Эффективная доза (ЭД50) средства по примеру 1 составила 2,97 мкл/мл.
Таким образом, средство по примеру 1, является эффективным блокатором H1-гистаминовых рецепторов.
Пример 5. Противовоспалительная активность in vivo на модели острого риносинусита (ОРС) у крыс.
Эксперимент проводили на крысах-самцах линии Wistar массой тела 220-270 грамм, содержавшихся на стандартном рационе питания. Индукцию патологии осуществляли интраназальным введением 7,5% формалина по 20 мкл в каждый носовой ход. Патология характеризовалась полнокровием, гиперплазией и очаговым некрозом слизистой оболочки носовых ходов, увеличением количества бокаловидных клеток, инфильтрацией монононуклеарами и лейкоцитами, гиперпродукцией слизи железами подслизистой оболочки.
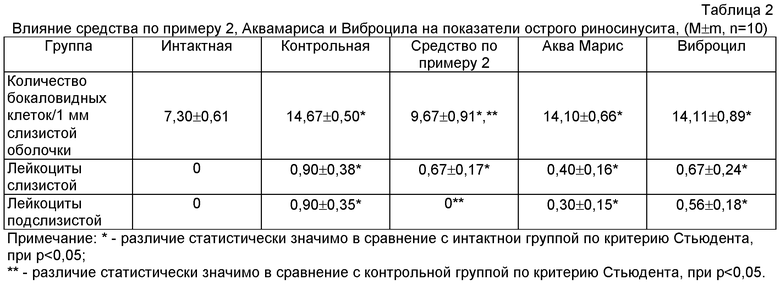
Средство по примеру 2 с содержанием пигментно-минерального комплекса 1% вводили по лечебной схеме в течение 7 дней один раз в сутки, интраназально в дозе 0,025 мл в каждый носовой ход. Препараты сравнения Виброцил и Аква Марис вводили по такой же схеме в дозах 0,1 мл в каждый носовой ход. На 8-ой день после индукции патологии животных подвергали эвтаназии и проводили сравнительные макроскопические и морфологические исследования слизистой и подслизистой оболочек носовых ходов (таблица 2).
Патология, вызванная интраназальным введением 7,5% формалина, характеризовалась катаральной формой риносинусита. При применении средства по примеру 2 наблюдали излечение 30% экспериментальных животных. Препараты сравнения в данной модели были не эффективны и на фоне их применения развивался серозный риносинусит у 70-80% животных и серозно-гнойный риносинусит у 20% животных. Применение средства по примеру 2 препятствовало развитию тяжелых форм воспаления слизистой оболочки носовых ходов.
На фоне применения средства по примеру 2 достоверно снижалось количество бокаловидных клеток на 1 мм слизистой оболочки носовых ходов, а лейкоцитарная инфильтрация подслизистой оболочки была на уровне интактной группы животных.
Таким образом, фармакологическая активность средства по примеру 2 на модели острого риносинусита превышает активность как местного противовоспалительного средства Аква Марис, так и антиконгестивного, сосудосуживающего и противоаллергического средства Виброцил.
Пример 6. Антиоксидантная активность
Известно, что при аллергических процессах увеличивается скорость свободнорадикального окисления (Симонян А.В. Антиоксиданты в современном здравоохранении. // Медицинский вестник. - 2008. - №16. - 443). Таким образом, антиоксидантное действие противоаллергического лекарственного средства является его дополнительным преимуществом, обеспечивающим системность действия препарата.
Влияние средства по примеру 2 на антиоксидантный статус организма исследовали на модели стрептозотоцин-индуцированного диабета 2 типа.
Эксперимент проводили на аутбредных мышах-самцах. Индукцию патологии осуществляли однократным введением стрептозотоцина (60 мг/кг). В период с 11 по 20 день осуществляли внутрибрюшинное введение средства по примеру 2 с содержанием пигментно-минерального комплекса 1% в количестве, обеспечивающем введение комплекса в количестве 1,8 мг/кг, что соответствует дозе 10 мг для человека. Влияние средства по примеру 2 на состояние антиоксидантного статуса организма оценивали по изменению концентрации восстановленного глутатиона и малонового диальдегида в периферической крови (таблица 3).
Увеличение концентрации малонового диальдегида и снижение концентрации восстановленного глутатиона в периферической крови экспериментальных животных контрольной группы свидетельствует о развитии окислительного стресса на фоне введения стрептозотоцина.
Средство по примеру 2 оказывало выраженный антиоксидантный эффект, заключающийся в увеличении концентрации восстановленного глутатиона и снижении концентрации малонового диальдегида и восстановлении их до уровня интактных животных.
Таким образом, средства по примеру 1 и 2 расширяют ассортимент эффективных, безопасных противовоспалительных и противоаллергических средств из природных источников.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПИГМЕНТНОГО КОМПЛЕКСА БИСНАФТАЗАРИНОВ | 2014 |
|
RU2545692C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3,6,7-ТЕТРАГИДРОКСИНАФТАЗАРИНА | 2009 |
|
RU2411939C1 |
| СПОСОБ ПОЛУЧЕНИЯ СПИНОХРОМА А И БЕЛКА МОРСКИХ ЕЖЕЙ, ВЗАИМОДЕЙСТВУЮЩЕГО С ПОЛИГИДРОКСИНАФТОХИНОНОМ | 2008 |
|
RU2362573C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3,7-ТРИОКСИЮГЛОНА (СПИНОХРОМА В) | 2014 |
|
RU2568604C1 |
| СПОСОБ ПЕРЕРАБОТКИ ПАНЦИРЯ МОРСКИХ ЕЖЕЙ | 2010 |
|
RU2441661C1 |
| СРЕДСТВО НА ОСНОВЕ БИСНАФТАЗАРИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2016 |
|
RU2669374C2 |
| Композиция ингредиентов для функциональных пищевых продуктов | 2016 |
|
RU2644957C1 |
| Способ получения кальцийсодержащей композиции из панциря морских ежей | 2015 |
|
RU2611847C1 |
| Способ получения нафтохинонов из морских ежей | 2016 |
|
RU2645077C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОВОСПАЛИТЕЛЬНЫМ ДЕЙСТВИЕМ | 2011 |
|
RU2483741C1 |
Изобретение относится к области фармации, медицины и ветеринарии, а именно к новым лекарственным средствам для лечения воспалительных и аллергических заболеваний. Поставленная задача получения в форме глазных капель, интраназальных капель и спрея не токсичного, удобного в использовании и стабильного при хранении средства, оказывающего противовоспалительное и противоаллергическое действие, решается созданием композиции, содержащей пигментно-минеральный комплекс панцирей морских ежей (0,05-2,0%), включающий спинохромы В, D, димерные полигидроксинафтохиноны и минеральную составляющую (кальций, магний, фосфор, натрий, калий) в виде водорастворимых солей, сорастворитель (0,01-10%), консервант (0,01-0,2%), антиоксидант (0,01-0,2%), регулятор кислотности (до рН 6,0-8,0) и воду (до 100%). Описывается экспериментально подобранный способ получения средства согласно изобретению, исключающий окисление пигментно-минерального комплекса уже на этапе приготовления. 2 н. и 1 з.п. ф-лы, 3 табл., 1 ил., 6 пр.
1. Средство, обладающее противовоспалительным и противоаллергическим действием, в форме глазных капель, интраназальных капель или спрея, содержащее активное вещество, сорастворитель, консервант, регулятор кислотности и воду, отличающееся тем, что дополнительно содержит антиоксидант, выбранный из группы натрия метабисульфит, натрия сульфит, натрия тиосульфат или аскорбиновая кислота, сорастворитель, выбранный из группы спирт этиловый, полисорбат 80, полиэтиленгликоль, пропиленгликоль, глицерин, полиоксиэтилен-40-глицерол-гидроксистеарат, моноэтиловый эфир диэтиленгликоля, поливинилпирролидон, поливиниловый спирт, в качестве активного вещества содержит пигментный комплекс панцирей морских ежей Strongylocentrotus droebachiensis (0,02-10%), содержащий спинохромы В и D, а также димерные полигидроксинафтохиноны, и минеральную составляющую панциря морских ежей (кальций, магний, фосфор, натрий, калий) в виде водорастворимых солей, и регулятор кислотности при следующем соотношении компонентов, г на 100 г:
2. Способ получения средства по п.1, отличающийся тем, что включает в
себя следующие стадии:
а) приготовление раствора консерванта в воде при температуре 80-90°С, охлаждение полученного раствора до 35-40°С;
б) растворение в охлажденном растворе сорастворителя и антиоксиданта до получения прозрачного раствора;
в) введение пигментно-минерального комплекса в полученный раствор вспомогательных веществ при постоянном перемешивании;
г) введение регулятора кислотности и доведение рН раствора до 6,0-8,0;
д) фильтрование полученного раствора и розлив во флаконы.
3. Способ получения по п.2, отличающийся тем, что для стерилизации могут быть использованы стерильная фильтрация или термическая стерилизация паром под давлением.
| ПРЕПАРАТ "ГИСТОХРОМ" ДЛЯ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ СЕТЧАТКИ И РОГОВИЦЫ ГЛАЗ | 1998 |
|
RU2134107C1 |
| СПОСОБ ЛЕЧЕНИЯ ОЖОГОВ ГЛАЗ | 1990 |
|
RU2038088C1 |
| ГЕРОДИЕТИЧЕСКИЙ ПРОДУКТ | 1999 |
|
RU2159056C1 |
| KR 20020091909 A, 11.12.2002. | |||
Авторы
Даты
2013-07-27—Публикация
2012-06-08—Подача