Изобретение относится к области энергетики и технологии основного органического синтеза, а именно к технологии производства этилена и его производных, и может быть использовано в энергетике и химической промышленности.
Современные процессы производства многих крупнотоннажных продуктов основного органического синтеза сопровождаются как большими затратами энергии, так и интенсивным энерговыделением, и часто базируются на том же углеводородном сырье, которое используется для производства электроэнергии. Поэтому все большее распространение получают комбинированные (интегрированные) энергохимические процессы производства (когенерации) химических продуктов и энергии.
Известен процесс одновременного производства (когенерации) метанола и электроэнергии, включающий получение синтез-газа, состоящего из H2, CO, CO2 и небольших количеств метана, на установке риформинга путем подачи низших углеводородов, в т.ч. природного газа, и пара на установку риформинга, разделение синтез-газа на два потока, один из которых используется в качестве сырья для одной или нескольких реакций синтеза метанола, и/или диметилового эфира, и/или других оксигенатов, в то время как другой поток подается в один или более реакторов для проведения реакции конверсии водяного газа, в результате которой образуется поток газа, состоящий в основном из H2 и CO2, подвергающийся затем сепарации на два потока, состоящие из H2 и CO2, соответственно, причем по крайней мере 5% содержащего Н2 потока подается в реактор синтеза метанола, а остальная часть содержащего Н2 потока - на одну или более установок генерации тепла или другие потребляющие Н2 процессы. (Патент США №6809121, МПК C07C 29/151; C10G 2/00, опубл. 26.10.2004 г.)
Известен комбинированный способ производства электроэнергии и жидкого синтетического топлива с использованием газотурбинных и парогазовых установок.
Способ включает частичное окисление углеводородного топлива в потоке сжатого воздуха, отбираемого за компрессором высокого давления газотурбинной установки с последующим дожиманием, получение синтез-газа, его охлаждение и экологическую очистку, подачу полученного синтез-газа в однопроходной реактор синтеза жидкого синтетического топлива с частичным превращением синтез-газа в жидкое топливо. Оставшийся в реакторе синтеза жидкого синтетического топлива энергетический газ выводят в камеру сгорания газотурбинной установки, при этом степень превращения синтез-газа выбирают из условия поддержания температуры рабочего тела на входе в газовую турбину в зависимости от типа газотурбинной установки, используемой для производства электроэнергии, а последующее дожимание воздуха, отбираемого за компрессором высокого давления газотурбинной установки, осуществляют с помощью детандера, приводимого в действие энергетическим газом, подогреваемым за счет охлаждения синтез-газа перед реактором синтеза. (Патент РФ №2250872, МПК C01B 3/32, C10L 3/10, F01K 23/10, опубл. 27.04.2005 г.)
Недостатком известных способов является сложность получения и дальнейшей подготовки синтез-газа и связанная с этим высокая технологическая сложность всего процесса, исключающая возможность его применения для малотоннажных производств и в составе энергоустановок средней и малой мощности.
Известен комбинированный способ производства электроэнергии и синтетического жидкого топлива в составе парогазовой установки.
Способ включает сжатие воздуха в основном и дожимном компрессорах, частичное окисление углеводородсодержащего топлива в реакторе, охлаждение реакционной смеси, получение метанола, расширение продуктов неполного окисления с подачей их в камеру сгорания газовой турбины. При этом углеводородсодержащее топливо проходит последовательное окисление при температуре 380-450°C и давлении 4,5-10 МПа с последующим охлаждением реакционной смеси в холодильнике-конденсаторе конденсатом паротурбинной установки. Отделение метанола от жидких продуктов окисления осуществляют в ректификационной колонне. Обеспечение заданной температуры газа на входе в газовую турбину осуществляется принимаемым числом реакторных установок синтеза метанола либо подмешиванием исходного углеводородсодержащего топлива в камеру сгорания газовой турбины. (Патент РФ №2356877, МПК C07C 27/12, C07C 31/04, опубл. 27.05.2009 г.)
Недостатком известного способа является низкая степень превращения исходных углеводородов в целевой продукт - метанол, которая не превышает 1-2% при селективности выше 70%. При более глубоких степенях превращения селективность по метанолу снижается до нуля.
Известен интегрированный процесс производства жидких продуктов Фишера-Тропша (синтетических жидких углеводородов) и производства электроэнергии с низким уровнем выбросов CO2. Установка, реализующая известный способ, включает получение синтез-газа, разделение воздуха, синтез продуктов Фишера-Тропша, извлечение CO и генерацию электроэнергии на основе комбинированного парогазового цикла (Патент США №6976362, МПК C01B 3/32, опубл. 20.12.2005 г.).
Недостатком известного процесса является большое число стадий, связанных с получением и дальнейшей подготовкой синтез-газа, и, как следствие, его высокая металлоемкость и технологическая сложность, исключающая возможность применения для малотоннажных производств и энергоустановок средней и малой мощности. Кроме того, продукты синтеза Фишера-Тропша фактически являются синтетическим аналогом сырой нефти и требуют дальнейшей переработки в топлива или химические продукты. При наличии более дешевых природных нефтепродуктов их производство, даже с учетом их более высоких экологических характеристик, может быть экономически оправдано только в отдельных случаях.
Более перспективным является интегрированное производство электроэнергии и таких универсальных и энергоемких продуктов, как этилен и продукты его переработки (жидкие углеводороды, этиловый спирт, полиэтилен). Этилен входит в число основных крупнотоннажных продуктов органического синтеза и является основой производства большинства продуктов основного и тонкого органического синтеза. Кроме того, с использованием процесса олигомеризации этилен может быть переработан в синтетическое топливо и масла, аналогичные традиционным ГСМ, получаемым из нефти, и "синтетическую нефть" - смесь жидких продуктов, легко транспортируемую традиционными способами (наливной транспорт, трубопроводы) и перерабатываемую на обычных нефтеперерабатывающих предприятиях. Этиловый спирт (этанол) сам является жидким горючим продуктом и рассматривается в качестве перспективного энергоносителя для различных применений. Полимеры на основе этилена (например, различные виды и марки полиэтилена, сополимеры с другими мономерами) являются основными видами пластиков, используемых повсеместно. По этим причинам создание высокоэффективных и экономичных технологий получения этилена и продуктов его переработки является одной из главных задач современной химической промышленности.
По существующим и реализованным в промышленности технологиям этилен получается главным образом пиролизом различного углеводородного сырья (нафта, пропан-бутановая фракция, этан и др.). Это резко ограничивает сырьевую базу производства этилена. Кроме того, эти процессы являются эндотермическими, т.е. требуют для своего осуществления подвода значительного количества энергии, что дополнительно понижает их эффективность и делает их малоэффективными при небольших объемах производства.
В настоящее время большой интерес вызывают прямые, минуя стадию получения синтез-газа, процессы получения различных продуктов из природного газа (метана), основанные на его окислительных превращениях. Такие процессы имеют ряд преимуществ: простота технологической схемы, отсутствие химических стадий, протекающих с поглощением энергии, возможность одновременной с производством целевого продукта генерации тепла.
В частности, известен процесс получения этилена по реакции окислительной конденсации метана (ОКМ), протекающей в присутствии оксидных катализаторов при температурах 700-900°C с подачей кислорода (воздуха) ниже стехиометрического соотношения (0,1-0,3 объема O2 на 1 объем метана). Этот процесс является экзотермическим, т.е. протекает с выделением энергии, и не требует для осуществления основной реакции металлоемкого оборудования. (B.C.Арутюнов, О.В.Крылов. Окислительные превращения метана, М.: Наука, 1998 г., 361 стр.)
Основным недостатком данного процесса является относительно низкий выход целевого продукта - этилена - за один проход реакционной смеси (не выше 14-15%) и высокий расход сырья (природного газа) на получение целевого продукта.
Технической задачей, на решение которой направлено заявляемое изобретение, является создание высокоэффективного и экономичного способа получения этилена и продуктов его переработки путем совмещения их производства методом прямого газофазного окисления природного газа с выработкой электро- и тепловой энергии на энергоустановке.
Поставленная техническая задача решается тем, что в способе производства этилена и электроэнергии из природного газа путем прямого окисления природного газа с последующей подачей отходящего газа на энергоустановку, заключающемся в том, что исходный поток природного газа направляют на стадию синтеза этилена по реакции окислительной конденсации метана, которую осуществляют в присутствии оксидных катализаторов при температуре от 700°C до 950°C, давлении от 1 атм до 10 атм и мольном соотношении метана к кислороду в интервале от 2:1 до 10:1, далее выделяют из реакционной смеси этилен, остальную часть газового потока, включающего не прореагировавший метан, и горючие продукты водород и CO направляют на энергоустановку, в которой осуществляют выработку электроэнергии и тепла; энергию, выделяющуюся в процессе получения этилена по реакции окислительной конденсации метана в виде теплосодержания пара и других теплоносителей, утилизируют совместно с энергией, вырабатываемой энергоустановкой, которая питается природным газом метаном, не прореагировавшим в реакторе синтеза этилена.
Кроме того, осуществляют выделение этана и высших углеводородов из потока горючих газов, который направляют на энергоустановку, где осуществляют выработку электроэнергии и тепла; выделенные этан и высшие углеводороды направляют на стадию синтеза этилена по реакции окислительной конденсации метана.
Кроме того, оксидный катализатор выбирают из группы: оксиды щелочноземельных элементов Mg, Ca, Sr, Ba, оксиды редкоземельных элементов La, Ce, Nd, Sm или их смеси, промотированные добавками щелочных элементов (Li, Na, K, Rb, Cs), Sb, Bi и/или Pb, нанесенные на носители Al2O3, SiO2, TiO2, ZrO2, HfO2, алюминаты, силикаты щелочноземельных элементов, силикаты редкоземельных элементов.
Кроме того, состав оксидного катализатора выбирают в соответствии с эмпирической формулой
M1 aM2 bM3 2O3+m, где
M1 - щелочноземельный элемент, выбранный из группы Mg, Ca, Sr, Ba (или их комбинация);
M2 - щелочной элемент, выбранный из группы Li, Na, K, Rb, Cs (или их комбинация);
M3 - редкоземельный элемент, выбранный из группы La, Ce, Nd, Sm (или их комбинация);
a - грамм-атомный показатель элемента, значение которого выбирают от 0,005 до 250;
b - грамм-атомный показатель элемента, значение которого выбирают от 0 до 20;
m - стехиометрический коэффициент, определяемый соотношением компонентов M1, M2 и M3.
Кроме того, состав оксидного катализатора выбирают в соответствии с эмпирической формулой
NaXWYMZSiO2+n, где
M - химический элемент Mn или Ce,
X, Y, Z - грамм-атомные соотношения элементов, из которых значение X выбирают от 0,01 до 0,4; значение Y выбирают от 0,005 до 0,2; значение Z выбирают от 0,005 до 0,4.
Технический результат, достижение которого обеспечивается реализацией всей заявляемой совокупности существенных признаков, заключается
- в совмещении производства ценных соединений методом прямого газофазного окисления природного газа с выработкой электро- и тепловой энергии на энергоустановке,
- в снижении удельного расхода природного газа на производство этилена и его производных.
Также с учетом того, что отходящий газ процесса получения этилена и его производных полностью используется для выработки энергии, а вырабатываемый в экзотермических реакциях окисления пар утилизируется вместе с паром, вырабатываемом самой энергоустановкой, суммарная эффективность полезного использования углеводородного сырья в таком интегрированном энергохимическом процессе будет близка к максимально возможной.
Заявляемое изобретение поясняется рисунком, где на фиг.1 представлен пример работающей на природном газе энергоустановки, на которой может быть реализован заявляемый способ. Представленный пример не ограничивает использование иного оборудования, предназначенного для тех же целей, на котором может быть реализован способ.
Фиг.1 содержит следующие позиции:
1 - реактор окислительной конденсации метана (ОКМ);
2 - закалочно-испарительный теплообменный аппарат (генератор пара высокого давления);
3 - теплообменный аппарат, в котором газовая смесь охлаждается до ~30°C с конденсацией основной части реакционной воды;
4 - компрессор реакционного газа;
5 - узел этаноламиновой очистки;
6 - узел щелочной промывки, осушки и охлаждения до минус 100°C с помощью пропиленового и этиленового холодильных циклов;
7 - турбодетандер;
8 - колонна низкотемпературной ректификации (выделения этан-этиленовой фракции);
9 - колонна низкотемпературной ректификации (выделения этилена-сырца);
10 - колонна низкотемпературной ректификации (выделения метана);
11 - рекуперативный теплообменный аппарат «газ-газ».
Заявляемый способ осуществляется следующим образом.
Природный газ из газопровода, содержащий 98% метана и поступающий на электростанцию в объеме 60 тыс. м3/ч, нагревают в рекуперативном теплообменнике «газ-газ» 11 теплом отходящих из реактора 1 газов до 450°C и подают на вход реактора 1, в котором происходит превращение части метана в этилен и другие продукты за счет протекания каталитической реакции окислительной конденсации метана с выделением тепла.
Для повышения эффективности использования тепла реакционных газов исходный природный газ подается в трубное пространство теплообменника 11, а горячие реакционные газы - противотоком в межтрубное пространство того же теплообменника.
Реакцию окислительной конденсации метана в реакторе 1 проводят в присутствии оксидных катализаторов при температуре от 700°C до 950°C, предпочтительно от 750°C до 900°C, давлении от 1 атм до 10 атм, предпочтительно от 1 атм до 3 атм, и мольном соотношении метана к кислороду в интервале от 2:1 до 10:1.
Оксидный катализатор выбирают из группы: оксиды щелочноземельных элементов Mg, Ca, Sr, Ba, оксиды редкоземельных элементов La, Ce, Nd, Sm или их смеси, промотированные добавками щелочных элементов (Li, Na, K, Rb, Cs), Sb, Bi и/или Pb, нанесенные на носители Al2O3, SiO2, TiO2, ZrO2, HfO2, алюминаты, силикаты щелочноземельных элементов, силикаты редкоземельных элементов.
При этом состав оксидного катализатора выбирают в соответствии с эмпирической формулой:
M1 aM1 bM3 2O3+m, где
M1 - щелочноземельный элемент, выбранный из группы Mg, Ca, Sr, Ba (или их комбинация);
M2 - щелочной элемент, выбранный из группы Li, Na, K, Rb, Cs (или их комбинация);
M3 - редкоземельный элемент, выбранный из группы La, Ce, Nd, Sm (или их комбинация);
a - грамм-атомный показатель элемента, значение которого выбирают от 0,005 до 250;
b - грамм-атомный показатель элемента, значение которого выбирают от 0 до 20;
m - стехиометрический коэффициент, определяемый соотношением компонентов M1, M2 и M3.
Кроме того, состав оксидного катализатора выбирают в соответствии с эмпирической формулой
NaXWYMZSiO2+n, где
M - химический элемент Mn или Ce,
X, Y, Z - грамм-атомные соотношения элементов, из которых значение X выбирают от 0,01 до 0,4; значение Y выбирают от 0,005 до 0,2; значение Z выбирают от 0,005 до 0,4.
Катализаторы процесса окислительной конденсации метана с получением этилена являются известными из предыдущего уровня техники, в частности публикации B.C.Арутюнов, О.В.Крылов. Окислительные превращения метана, М.: Наука, 1998 г., 361 стр., где описаны каталитические свойства смешанных оксидов, содержащих в различных соотношениях катионы редкоземельных, щелочноземельных и щелочных металлов, и дана подробная библиография (ссылки на патенты и научные публикации). Совокупность этих данных показывает, что наиболее эффективны системы, содержащие первые члены ряда лантаноидов (La, Nd, Sm и в определенных комбинациях - также Ce и Pr). Лучшие показатели по выходу продуктов ОКМ на катализаторах этого семейства (подтвержденные независимо многими авторами) достигают 18-19% при селективности выше 60%. На стр. 245 той же монографии описаны оксидные катализаторы, соответствующие эмпирической формуле NaXWYMnZSiO2+n и впервые предложенные в работе [Fang X.P., Li S.B., Lin J.Z. J. Mol. Catal. (China), v.6, 1992, p.225]. Эти катализаторы (например, состава 20%Na2WO4+5%Mn/SiO2) позволяют получить наиболее высокий подтвержденный выход продуктов ОКМ (20-22%), но при более высокой температуре (850-900°C по сравнению с оптимумом для систем, содержащих лантаноиды - 750-850°C).
Все интервалы параметров предложенного способа указаны в предельно допустимых значениях, выбор параметров способа за пределами заявленных интервалов значений не обеспечивает достижения указанного технического результата.
Выходящий из реактора 1 газовый поток, обладающий высоким теплосодержанием и содержащий целевой продукт химического превращения - этилен, подвергают охлаждению и разделению, причем выделяющееся в процессе охлаждение тепло используют для подогрева исходного метана в аппарате 11 и генерации высокопотенциального пара в закалочно-испарительном теплообменном аппарате (генератор пара высокого давления) 2. Теплосодержание пара, образующегося в закалочно-испарительном теплообменном аппарате 2, утилизируют в энергоустановке совместно с теплом, получаемым при сгорании непрореагировавшего метана и горючих газов, образовавшихся при окислении части метана в реакторе 1 окислительной конденсации метана (ОКМ). Прошедший закалочно-испарительный теплообменный аппарат 2 поток реакционных газов поступает в теплообменный аппарат 3, в котором осуществляют охлаждение и отделение основного количества реакционной воды в виде конденсата. После охлаждения до 30°C реакционную смесь через компрессор 4 реакционного газа подают в узел 5 этаноламиновой очистки, где отделяется основное количество CO2. В узле 6 осуществляют доочистку потока щелочной промывкой, осушку и охлаждение до температуры минус 100°C с помощью пропиленового и этиленового холодильных циклов. В узле 6 происходит выделение топливного газа, в который уходят водород, оксид углерода, азот, остатки кислорода и небольшая часть метана. Этот поток дросселируется до давления 0.3-0.5 МПа через турбодетандер 7 и подается на энергоустановку. В колонне 8 низкотемпературной ректификации выделяют основную часть непрореагировавшего метана, который также подают на энергоустановку.
Из куба колонны 8 выводится фракция C2+, которая поступает в колонну 9. Кубовый остаток из этой колонны, который состоит в основном из этана и углеводородов С3+, возвращают в реактор 1. Из верхней части колонны 9 выводится газ, содержащий в основном этилен и остаточный метан. Эта смесь разделяется в колонне 10 на этилен-сырец, поступающий на узел переработки, и метан, который подается на энергоустановку.
Процесс генерации электроэнергии на установках различных типов с использованием метана (главного компоненты природного газа) является известным. В качестве энергоустановки в заявляемом интегрированном процессе может быть использован любой известный тип энергоустановки, производящий тепло и/или электроэнергию из природного газа (см., например, С.В.Цанев, В.Д.Буров, А.Н.Ремезов. Газотурбинные и парогазовые установки тепловых электростанций. Под ред. Цанева С.В. Издательство МЭИ, 2002 г., 579 стр.).
Узел переработки этилена может представлять собой совокупность аппаратов, в которых происходит его тонкая очистка и доведение до товарной кондиции, либо реактор, в котором осуществляется превращение этилена в иные целевые продукты (жидкие углеводороды, этанол и др.), и аппараты выделения и очистки этих продуктов.
При осуществлении дальнейшей химической переработки этилена в продукты его олигомеризации ("синтетическая нефть", жидкое топливо, базовые масла), или полимеризации и сополимеризации (полимеры и пластики), или гидратации (этанол), или алкилирования (стирол, другие мономеры; присадки к топливам), энергию, выделяющуюся в процессе химической переработки этилена в виде теплосодержания пара и других теплоносителей утилизируют совместно с энергией, вырабатываемой энергоустановкой, которая питается природным газом метаном, не прореагировавшим в реакторе синтеза этилена, и энергией, полученной на стадии синтеза этилена по реакции окислительной конденсации метана.
Стадии выделения/разделения, реализуемые в приведенном примере в аппаратах 5, 6, 8, 9, 10, могут осуществляться методами химической, криогенной, адсорбционной, абсорбционной обработки и/или с использованием мембранных устройств.
Отличие предложенного способа от известных процессов заключается в том, что
(а) производство этилена, как первичного продукта, включается в схему подготовки газа для энергоустановки;
(б) не прореагировавший в реакторе синтеза этилена метан не подвергается рециркуляции, сбросу или сжиганию на факеле, а направляется в энергоблок (энергоустановку) для производства тепла и электроэнергии;
(в) тепловая энергия (в виде теплосодержания пара и других теплоносителей), выделяющаяся в процессе получения этилена по реакции окислительной конденсации метана и в процессах последовательной переработки этилена в его производные (олиго- или полимеризация, гидратация в этанол), утилизируется совместно с энергией, вырабатываемой энергоустановкой, которая питается природным газом (метаном), не прореагировавшим в реакторе синтеза этилена.
Заявляемый способ производства этилена и его производных в интегрированном процессе на основе прямого парциального окисления природного газа с последующей подачей отходящего газа на энергоустановку позволяет получить существенные экономические и технологические преимущества по сравнению с известными технологическими процессами их производства.
Снижение удельного расхода природного газа на производство этилена и его производных достигается за счет использования на стадии получения и выделения этилена и его производных тепловой и электрической энергии, полученной на энергоустановке. Это исключает необходимость включения в технологическую схему маломощных тепло- и электрогенераторов, имеющих более низкую удельную энергоэффективность.
Кроме того, ввиду исключения из схемы стадии рециркуляции непрореагировавшего метана и возможности ведения окисления исходного сырья воздухом, а не кислородом, снижается общее энергопотребление на стадии получения этилена, что также приводит к повышению удельной эффективности процесса в пересчете на исходный природный газ (метан), который в данном процессе может рассматриваться как сырье и энергоноситель одновременно.
Совмещение производства ценных соединений с высокой добавленной стоимостью с выработкой электро- и тепловой энергии на энергоустановке позволяет практически полностью устранить негативное влияние на экономические показатели процессов получения этилена и его производных прямым окислением природного газа его главных недостатков - высокого расхода метана на производство целевого продукта и низкую экономическую эффективность процесса. При этом полностью сохраняются такие их привлекательные качества, как технологическая простота, низкие капитальные и операционные затраты и возможность использования воздуха в качестве окислителя. Включение производства химических продуктов (этилена и его производных) в технологическую схему энергоустановки позволяет получить значительный экономический эффект.
В отличие от известных технологий, требующих создания крупных энергохимических комплексов на базе мощных электростанций, интегрированный процесс производства химических продуктов (этилена и его производных) методом прямого окисления и электроэнергии может быть реализован на десятках энергоустановок средней и малой мощности, работающих на природном газе. По технико-экономическим оценкам себестоимость получаемого этилена и его производных и удельные капитальные затраты будут заметно ниже тех величин, которые характеризуют специализированные заводы по производству указанных химических продуктов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ХИМИЧЕСКОЙ ПЕРЕРАБОТКИ СМЕСЕЙ ГАЗООБРАЗНЫХ УГЛЕВОДОРОДОВ (АЛКАНОВ) C-C В ОЛЕФИНЫ C-C (ЭТИЛЕН И ПРОПИЛЕН) | 2010 |
|
RU2435830C1 |
| КАТАЛИЗАТОР ДЛЯ ПОЛУЧЕНИЯ ЭТИЛЕНА И СПОСОБ ПОЛУЧЕНИЯ ЭТИЛЕНА С ИСПОЛЬЗОВАНИЕМ ЭТОГО КАТАЛИЗАТОРА | 2013 |
|
RU2523013C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭТИЛЕНА | 2013 |
|
RU2528829C1 |
| СПОСОБ ОКИСЛИТЕЛЬНОГО ГАЛОГЕНИРОВАНИЯ C УГЛЕВОДОРОДОВ ДО ГАЛОГЕНИРОВАННЫХ C УГЛЕВОДОРОДОВ И СВЯЗАННЫЕ С НИМ ИНТЕГРИРОВАННЫЕ СПОСОБЫ | 2002 |
|
RU2286329C2 |
| КАТАЛИЗАТОР (ВАРИАНТЫ), СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ (ВАРИАНТЫ) И СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2003 |
|
RU2248932C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ДЛЯ ОКИСЛИТЕЛЬНОЙ КОНДЕНСАЦИИ МЕТАНА, КАТАЛИЗАТОР, ПРИГОТОВЛЕННЫЙ ПО ЭТОМУ СПОСОБУ, И СПОСОБ ОКИСЛИТЕЛЬНОЙ КОНДЕНСАЦИИ МЕТАНА С ИСПОЛЬЗОВАНИЕМ ПОЛУЧЕННОГО КАТАЛИЗАТОРА | 2013 |
|
RU2515497C1 |
| МНОГОСЛОЙНЫЙ СМЕШАННЫЙ ОКСИДНЫЙ КАТАЛИЗАТОР, НАНЕСЕННЫЙ НА НОСИТЕЛЬ, ДЛЯ ОКИСЛИТЕЛЬНОЙ КОНДЕНСАЦИИ МЕТАНА | 2020 |
|
RU2783516C1 |
| КАТАЛИЗАТОР, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2005 |
|
RU2292237C1 |
| СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2024 |
|
RU2834479C1 |
| СПОСОБ ПОДГОТОВКИ ПОПУТНЫХ И ПРИРОДНЫХ ГАЗОВ ДЛЯ ИСПОЛЬЗОВАНИЯ В ПОРШНЕВЫХ ДВИГАТЕЛЯХ ВНУТРЕННЕГО СГОРАНИЯ | 2008 |
|
RU2385897C1 |
Изобретение относится к способу производства этилена и электроэнергии из природного газа путем прямого окисления природного газа с последующей подачей отходящего газа на энергоустановку. Способ заключается в том, что исходный поток природного газа направляют на стадию синтеза этилена по реакции окислительной конденсации метана, которую осуществляют в присутствии оксидных катализаторов при температуре от 700°C до 950°C, давлении от 1 атм до 10 атм и мольном соотношении метана к кислороду в интервале от 2:1 до 10:1. Далее выделяют из реакционной смеси этилен, остальную часть газового потока, включающего не прореагировавший метан и горючие продукты водород и CO направляют на энергоустановку, в которой осуществляют выработку электроэнергии и тепла. Энергию, выделяющуюся в процессе получения этилена по реакции окислительной конденсации метана в виде теплосодержания пара и других теплоносителей, утилизируют совместно с энергией, вырабатываемой энергоустановкой, которая питается природным газом метаном, не прореагировавшим в реакторе синтеза этилена. Заявляемый способ позволяет получить существенные экономические и технологические преимущества по сравнению с известными технологическими процессами их производства. 4 з.п. ф-лы, 1 фиг.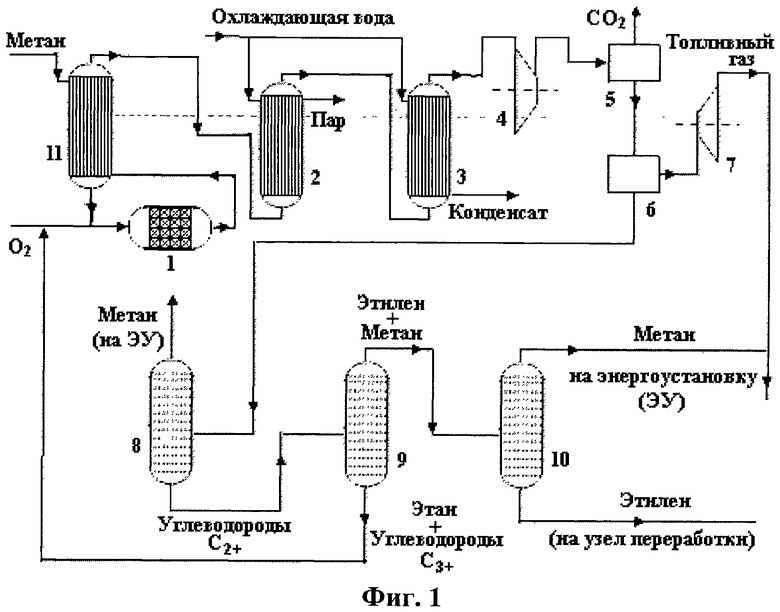
1. Способ производства этилена и электроэнергии из природного газа путем прямого окисления природного газа с последующей подачей отходящего газа на энергоустановку, заключающийся в том, что исходный поток природного газа направляют на стадию синтеза этилена по реакции окислительной конденсации метана, которую осуществляют в присутствии оксидных катализаторов при температуре от 700°C до 950°C, давлении от 1 атм до 10 атм и мольном соотношении метана к кислороду в интервале от 2:1 до 10:1, далее выделяют из реакционной смеси этилен, остальную часть газового потока, включающего не прореагировавший метан и горючие продукты водород и CO направляют на энергоустановку, в которой осуществляют выработку электроэнергии и тепла; энергию, выделяющуюся в процессе получения этилена по реакции окислительной конденсации метана в виде теплосодержания пара и других теплоносителей, утилизируют совместно с энергией, вырабатываемой энергоустановкой, которая питается природным газом метаном, не прореагировавшим в реакторе синтеза этилена.
2. Способ по п.1, отличающийся тем, что осуществляют выделение этана и высших углеводородов из потока горючих газов, который направляют на энергоустановку, где осуществляют выработку электроэнергии и тепла; выделенные этан и высшие углеводороды направляют на стадию синтеза этилена по реакции окислительной конденсации метана.
3. Способ по п.1, отличающийся тем, что оксидный катализатор выбирают из группы: оксиды щелочноземельных элементов Mg, Ca, Sr, Ba, оксиды редкоземельных элементов La, Ce, Nd, Sm или их смеси, промотированные добавками щелочных элементов (Li, Na, K, Rb, Cs), Sb, Bi и/или Pb, нанесенные на носители Al2O3, SiO2, TiO2, ZrO2, HfO2, алюминаты, силикаты щелочноземельных элементов, силикаты редкоземельных элементов.
4. Способ по п.1, отличающийся тем, что состав оксидного катализатора выбирают в соответствии с эмпирической формулой
M1 aM1 bM3 2O3+m,
где M1 - щелочноземельный элемент, выбранный из группы Mg, Ca, Sr, Ba (или их комбинация);
M2 - щелочной элемент, выбранный из группы Li, Na, K, Rb, Cs (или их комбинация);
M3 - редкоземельный элемент, выбранный из группы La, Ce, Nd, Sm (или их комбинация);
a - грамм-атомный показатель элемента, значение которого выбирают от 0,005 до 250;
b - грамм-атомный показатель элемента, значение которого выбирают от 0 до 20;
m - стехиометрический коэффициент, определяемый соотношением компонентов M1, M2 и M3.
5. Способ по п.1, отличающийся тем, что состав оксидного катализатора выбирают в соответствии с эмпирической формулой
NaXWYMZSiO2+n,
где M - химический элемент Mn или Ce,
X, Y, Z - грамм-атомные соотношения элементов, из которых значение X выбирают от 0,01 до 0,4; значение Y выбирают от 0,005 до 0,2; значение Z выбирают от 0,005 до 0,4.
| US 5012028 A, 30.04.1991 | |||
| СПОСОБ ПОЛУЧЕНИЯ ЭТИЛЕНА | 1994 |
|
RU2065429C1 |
| US 4822944 A, 18.04.1989. | |||
Авторы
Даты
2012-04-10—Публикация
2010-10-14—Подача