Данное изобретение относится к синтезу богатой бензиновой фракции из оксигенатов. Более конкретно, изобретение относится к улучшенному способу конверсии органических кислородсодержащих соединений с получением в качестве продукта углеводородов, которые можно использовать в качестве компонентов высококачественного бензина.
Под общепринятое определение термина "бензин" подпадает любой продукт нефтеперерабатывающей и нефтехимической промышленности, который содержит в качестве базовой фракции углеводороды, выкипающие в диапазоне кипения бензина, и который характеризуется также октановым числом, определяющим качество топлива, используемого в карбюраторных двигателях (двигателях внутреннего сгорания). Для придания некоторых дополнительных свойств бензиновому продукту в такие углеводороды можно вводить ряд других добавок. Хорошо известно, что бензиновые продукты с низкими октановыми числами можно смешивать с высокооктановыми бензиновыми продуктами, что дает удовлетворяющее требованиям общее октановое число смешения.
Используемый здесь термин "бензин" подразумевает широкий диапазон углеводородных продуктов, выкипающих в интервале кипения бензиновых фракций, тем самым поддерживается требуемое качество бензина, либо по отдельности, либо в смеси с другими источниками бензина. Бензин обычно включает в свой состав разнообразные соединения углеводородов, содержащие алканы, олефины и нафтены и ароматические углеводороды с числом углеродных атомов от 5 до 12 (С5-12) на молекулу и точкой кипения ниже 200°С.
Нефтеперерабатывающее производство является доминирующим поставщиком высокооктанового бензина для транспортного сектора. Однако по мере того как истощаются запасы сырой нефти или со временем становятся менее доступными, вполне вероятно, что это неизбежно вызовет рост цен на сырье и тем самым чрезмерное удорожание продукции бензина, если не применять более дешевого альтернативного сырья в производстве бензина.
Уже несколько десятилетий известна технология получения ценных бензиновых продуктов из синтез-газа (см., например, C.D.Chang, Catal. Rev., 15 (1983), 1). Эти общеизвестные технологии включают в себя стадии 1) синтеза оксигенатов из синтез-газа, причем эти оксигенаты содержат такие компоненты, как метанол, простой диметиловый эфир, этанол, пропанол, бутанол, ацетон, другие высшие спирты и простые эфиры, и 2) синтеза бензинового продукта из указанных оксигенатов. В соответствии с этой так называемой МТG-технологией (метанол в бензин), метанол-сырец превращают в смесь промежуточных продуктов метанола, простого диметилового эфира (ДМЭ) и воды, которая затем полностью поступает в реактор синтеза бензина, где указанная смесь, содержащая оксигенаты, превращается в бензиновый продукт в соответствии со способом, который описывает S. Yurchak в журнале Stud. Surf. Sci. Catal., 36 (1988), 251. Метанол-сырец можно получить из синтез-газа с применением стандартной технологии синтеза метанола. Общая схема реакционного процесса может быть представлена в следующем виде:
Синтез-газ → Метанол-сырец + теплота реакции
Метанол-сырец → Метанол/ДМЭ/Вода → Бензин + теплота реакции
Наряду с последовательным синтезом, описанным выше, включающим в себя стадии конверсии синтез-газа в метанол, который сначала отделяют, например, в виде метанола-сырца, после чего его повторно сгущают и превращают в бензин, альтернативный способ осуществляют с применением технологической схемы объединенного способа синтеза, в котором весь оксигенатный продукт, полученный на первой стадии, включая непрореагировавшую часть синтез-газа, проходит через вторую стадию синтеза по методике, описанной Topp-Jorgensen в журнале Stud. Surf. Sci. Catal. 36 (1988), 293. В соответствии с технологической схемой указанного объединенного процесса синтеза полная реакция может быть представлена в следующем виде:
Синтез-газ → Метанол/ДМЭ/Вода → Бензин + теплота реакции
Синтез-газ, являющийся базовым сырьем для обоих процессов, описанных выше, может быть получен из различных источников углеводородов с применением традиционных технологий риформинга и газификации.
На стадии синтеза оксигенатов процесс синтеза первичного метанола может протекать с высокой селективностью. Метанол синтезируют из синтез-газа согласно следующим реакциям:
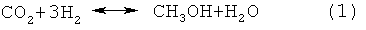
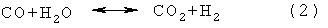
которые могут быть совмещены непосредственно при проведении синтеза или, проводится поочередно, со стадией синтеза простого диметилового эфира (ДМЭ) из метанола согласно следующей реакции:
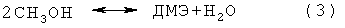
В зависимости от рабочего режима процесса и используемого катализатора образуется большее или меньшее количество сопутствующего продукта (обычно менее 1000 ч./млн в расчете на массу) и, главным образом, небольшие количества высших спиртов (главным образом этанола), кетонов, альдегидов и кислот.
Конверсия синтез-газа, однако, может сопровождаться также совместным образованием значительного количества оксигенатов и углеводородов, иных, чем метанол.
Объединенный процесс синтеза метанола и/или простого диметилового эфира является предпочтительным, ввиду того что последующая стадия превращения метанола в диметиловый эфир позволяет повысить степень конверсии за один цикл в секции синтеза оксигенатов и снизить количество теплоты, выделившееся в секции синтеза бензина, за счет чего, в свою очередь, обеспечивается более высокий выход бензинового продукта и/или удешевление процесса синтеза. Аналогичного результата можно достигнуть за счет совместного образования высших спиртов, возможно, в комбинации с образованием простых эфиров. Метанол и простой диметиловый эфир находят широкое распространение в качестве эквивалентов, а также компонентов перерабатываемого сырья в синтезе бензина, поскольку дегидратация метанола с образованием простого диметилового эфира и воды происходит чрезвычайно быстро на цеолитном катализаторе.
Следовательно, чем большее количество синтез-газа превращается в оксигенат на стадии синтеза оксигенатов, который можно использовать в качестве сырья для синтеза бензина, тем достигается более высокая степень конверсии за проход, в результате чего снижается количество поступающего на рециркулирование непрореагировавшего синтез-газа на стадии синтеза оксигената. Кроме того, чем большее количество высокомолекулярных кислородсодержащих органических соединений образуется на стадии синтеза оксигенатов, тем меньше выделяется тепла на моль бензинового продукта, получаемого на стадии синтеза бензина.
Рабочий режим проведения синтеза оксигенатов влияет на глубину конверсии через кинетику и равновесие. Температурный режим процесса синтеза обычно варьирует в диапазоне 200-350°С, причем образование высших спиртов особенно ускоряется при температурах выше 250°С. Давление имеет особое значение, поскольку оно оказывает существенное влияние на степень конверсии за проход. Процесс синтеза оксигенатов обычно проводят при давлении в интервале от 25 до 150 бар, предпочтительно от около 30 бар.
Катализаторы, способствующие конверсии синтез-газа в метанол, метанол в комбинации с простым диметиловым эфиром и смесью высших спиртов, являются коммерчески доступными или их можно получить известными из литературы методами. Катализаторы, например, на основе цеолитов, гамма-алюмооксидный, силикатный и алюмосиликатный, которые способны обеспечивать конверсию метанола в простой диметиловый эфир, также обладают активностью с получением простых эфиров высших спиртов в случае, когда присутствуют высшие спирты. Такие простые эфиры высших спиртов с таким же успехом конвертируются на стадии синтеза бензина. Пригодные катализаторы для синтеза метанола содержат оксид цинка, Cu или оксид меди или смесь Cu/ZnO, содержащую, необязательно, активаторы катализатора и оксид алюминия.
Кроме того, известно также применение катализаторов на основе железа, кобальта и никеля, возможно, активированных щелочью для получения смеси оксигенатов и углеводородов из синтез-газа в вышеуказанном рабочем режиме.
На стадии синтеза бензина оксигенат превращается сначала во фракцию углеводородов, имеющую точку кипения, характерную диапазону кипения фракции бензина. Бензиновая фракция содержит углеводороды с нормальной и разветвленной цепью, олефины, нафтены и ароматики. Кроме того, образуются низкокипящие углеводороды, в том числе легкие олефины и алканы, среди которых особенно пропан и бутаны представляют собой ценные продукты. Кроме того, этан и метан образуются в качестве сопутствующих продуктов.
В соответствии с технологической схемой объединенного процесса синтеза, где непрореагировавший синтез-газ со стадии разделения вниз по потоку (downstream) от секции синтеза бензина возвращают на стадию синтеза оксигенатов, где олефины, присутствующие в рециркулирующем газе, легко гидрируются на катализаторе синтеза метанола. Степень рециркуляции синтез-газа на стадию синтеза оксигенатов влияет, в свою очередь, на состав получаемого бензина, поскольку, несмотря на высокую степень рециркуляции, получают бензиновый продукт, имеющий сравнительно низкое среднее число атомов С (среднее число атомов углерода в углеводородных соединениях), поскольку последующая реакция метилирования олефинов на этой стадии затруднена.
Катализатор, используемый для конверсии оксигенатов, обычно выбирают из цеолитов. Предпочтительными типами являются такие, которые имеют мольное отношение диоксида кремния к оксиду алюминия, по меньшей мере, 12 и размеры формируемых пор до 12-членных колец, предпочтительно 10-членных. Примеры таких цеолитов включают ZSM-5, ZSM-11, ZSM-12, ZSM-23, ZSM-35 и ZSM-38. Способы их получения хорошо известны специалистам в данной области техники, и эти катализаторы имеются в свободной продаже. Особенно предпочтителен катализатор марки ZSM-5 в своей водородной форме, то есть HZSM-5.
Известно также применение других алюмосиликатов и силикоалюмофосфатов для конверсии оксигенатов в бензиновые смеси.
В зависимости от объемной скорости подачи и состава оксигената фактически можно достигнуть полной конверсии исходного сырья. Рабочее давление в технологических схемах объединенного процесса синтеза бензина варьирует в диапазоне от 25 до 150 бар. Самостоятельный, т.е. необъединенный, процесс синтеза бензина может протекать при давлении в интервале от нескольких бар, предпочтительно при давлении 5 бар или более. Выход бензиновой смеси в результате конверсии оксигенатов зависит, среди прочего, от рабочей температуры. Типичная рабочая температура реактора для синтеза бензина лежит в диапазоне 250-500°С, предпочтительно около 300-450°С.
Конверсия оксигенатов в углеводороды (бензин) является сильно экзотермической. Например, конверсия химически чистого метанола в бензин обычно приводит к повышению адиабатической температуры примерно до 600°С. Следовательно, в адиабатическом реакторе для синтеза бензина необходимо разбавлять оксигенат для того, чтобы избежать чрезмерного повышения температуры процесса. Это может быть достигнуто путем создания зоны для рециркулирования промежуточных продуктов из легких углеводородов и/или непрореагировавших компонентов синтез-газа вокруг бензинового реактора (см. ранее указанные ссылки на Yurchak и Topp-Jorgensen).
Высшие спирты по отношению к индивидуальному метанолу, используемому в процессе синтеза бензина, были изучены с точки зрения их влияния на конверсию метанола и состава суммарного продукта (распределение продуктов) на цеолитах. Главным образом были изучены смеси метанола и высших спиртов, содержащие весомую мольную долю высших спиртов.
В патенте США No. 4,076,761 говорится о том, каким образом можно получить бензин в соответствии со способом, в котором уголь газифицируют для получения синтез-газа, используемого в двухстадийном процессе синтеза бензина, протекающего при давлении 1-50 атмосфер. Этот двухстадийный способ синтеза бензина включает в себя стадию синтеза метанола, где синтез-газ конвертируется сначала в метанол и примеси, предпочтительно смесь из непрореагировавшего синтез-газа, спиртов, простых эфиров и соединений углеводорода, после которой проводят стадию синтеза бензина, в результате которой неразветвленные углеводороды и оксигенаты (спирты и простые эфиры) превращаются в полезные компоненты бензина.
Этот способ осуществляют предпочтительно без разделения первичных продуктов, образовавшихся между этими стадиями синтеза, поскольку установлено, что вторая стадия реакционного процесса нечувствительна к загрязняющим примесям (простым эфирам, высшим спиртам и углеводородам), содержащимся в полученном метаноле, и к наличию в них непрореагировавшего синтез-газа. В этом документе также упоминается о том, что на стадии синтеза метанола можно использовать катализаторы, позволяющие улучшить конверсию оксида углерода за счет образования промежуточных оксигенатов, таких как простой диметиловый эфир и высшие спирты.
Это позволяет получить максимальный эффект при осуществлении указанного способа за счет практически полной конверсии оксида углерода в оксигенат.
В многочисленных патентных документах, например патентах США US 4,752,622 и 4,668,656, патентной заявке Японии JP 59098024 А2 и европейской патентной заявке ЕР 0110357, описан процесс синтеза высших спиртов из синтез-газа для смешивания их в бензиновом коллекторе.
В зависимости от состава синтез-газа, используемого в качестве подпитки или исходного сырья для объединенного процесса синтеза бензина, корректировки для благоприятного протекания процесса могут происходить как снаружи реакционной зоны до введения порции синтез-газа в контур объединенного процесса синтеза, так внутри реакционной зоны между проведением/при проведении стадий синтеза, описанных выше. Корректировка состава синтез-газа может включать в себя корректировки, полученные посредством реакции конверсии водяным паром, на основании чего можно повышать отношение водорода к монооксиду углерода в случае, если прибавляют воду в стадию процесса, активную в реакции конверсии водяным паром, или же можно удалять один или несколько компонентов реакционной смеси с помощью адсорбционных или мембранных модулей.
В патенте США US 4,481,305 говорится о том, как можно эффективно проводить конверсию синтез-газа, полученного в результате газификации угля, в бензиновые продукты при проведении объединенного двустадийного процесса синтеза, в котором на первой стадии синтеза из синтез-газа получают метанол и простой диметиловый эфир, а на второй стадии синтеза из метанола и/или простого диметилового эфира получают бензиновые продуты. СО2, образовавшийся на стадии синтеза оксигенатов, удаляют из синтез-газа в стадии удаления с одновременным удалением кислых компонентов газа (H2S, COS и CO2), присутствующих в объединенном потоке свежей порции синтез-газа и возращенного на рециркуляцию непрореагировавшего синтез-газа. С целью поддержания низкого расхода газа на совместной стадии получения оксигенатов и удаления их них высокосернистых компонентов газа создают самостоятельный внутренний контур вокруг секции синтеза бензина. Воду прибавляют в заданном количестве для того, чтобы обеспечить максимальный выход продукции оксигенатов.
Обе стадии синтеза проводят каталитическим методом с применением подходящих общеизвестных специалистам в данной области катализаторов. Во всех вышеупомянутых технологических схемах часть непрореагировавшего синтез-газа после разделения его на бензиновую или спиртовую фракцию может быть возвращена в точку подачи свежего синтез-газа, что позволяет повысить суммарную степень конверсии синтез-газа. В соответствии с патентом США US 4,481,305 разделенный поток рециркулированного неконвертированного синтез-газа смешивается с эффлюентом, выходящим из секции синтеза оксигенатов, для того чтобы снизить количество газа, проходящее через секцию синтеза оксигенатов. Однако непрореагировавший синтез-газ может также, по меньшей мере, частично, быть направлен вниз по потоку в секции синтеза бензина для дальнейшей его переработки, причем в этом случае производство бензина включено в технологическую схему совместного синтеза.
Li-Min Tau и др. сообщали в журнале "Fuel Processing Technology", 33 (1993), 1, что чистый пропанол имеет более высокую реакционную способность по сравнению с чистым метанолом в реакции конверсии углеводородов на катализаторе типа ZSM-5 при температуре 300°С.
Сообщалось также R. Le Van Mao и др. в журнале Energy & Fuels, 1989, 3, 620, что чистый бутанол при температуре 470°С превращается в углеводородную фракцию С5+ с повышенным выходом на катализаторе ZSM-5, по сравнению с чистым метанолом.
В другом ссылочном документе R. Le Van Мао и др., Applied Catalysis, 34 (1987), 163-179, сообщают об исследовании реакционной способности этанола на различных катализаторах типа ZSM-5 (модифицированных и немодифицированных). Катализатор ZSM-5 испытывали при температуре 400°С при объемной скорости подачи сырья на массу катализатора в час (WHSV) 2,4 г/(г-час). Более высокая степень конверсии была отмечена по метанолу, по сравнению с подачей в качестве сырья чистого этанола, однако пониженный выход был получен для мольной фракции смеси, содержащей 77 мол.% метанола/23 мол.% этанола.
Было также установлено (R. Le Van Мао и др.), что состав суммарного продукта, полученный в результате конверсии пропанола, н-бутанола и изобутанола, почти приближался к составу суммарного продукта, полученного при конверсии чистого метанола. Было также высказано предположение о том, что смеси этанола/метанола и высших спиртов, образуемые в предыдущей стадии в результате конверсии синтез-газа, можно было бы объединить со стадией получения этилена, используя при этом их же модифицированный Zn катализатор ZSM-5.
Еще в одном источнике литературы (R. Le Van Мао и др., Energy & Fuels, 1989, 3, 620) говорится о том, что применение модифицированного Zn катализатора ZSM-5 для конверсии смеси спиртов с 1-4 атомами углерода в высококачественный бензиновый продукт приводит к снижению содержания дурола при применении такой смеси спиртов по сравнению с чистым метанолом.
В этом же источнике приводятся результаты сравнительного исследования конверсии указанной смеси из высших спиртов в метаноле на немодифицированном катализаторе ZSM-5. Пробу смеси, содержащую 35 мол.% метанола, 40 мол.% этанола, 17 мол.% пропанола и 9 мол.% 1-бутанола испытывали при температуре 470°С и полученные данные сравнивали с результатами конверсии чистого метанола. Было установлено, что выход углеводородной фракции C5+ был выше при подаче в качестве сырья смешанных спиртов по сравнению с чистым метанолом.
Было установлено Т. Mole (J. Catalysis, 84, 423-434), что добавка 6,5% смеси н/изо-пропанола и трет-бутанола ускоряет конверсию водного метанола (2,75 мас./мас.) при 280°С. В публикации сообщалось, что степень конверсии доходила до примерно 20%, но ничего не говорилось о выходе целевого продукта C5+ при 100% конверсии. При введении добавки этанола было установлено, что она не ведет к увеличению степени конверсии метанола. Это, как указывает Mole, противоречит данным Ono и Mori (J. Chem. Soc. Faraday Trans. 1. Vol.77, p.2209, 1981), которые обнаружили, что этилен, который является промежуточным продуктом синтеза этанола, совместно катализирует конверсию метанола.
Эта информация в некотором роде распространяется на температурный режим и подачу спиртов, поэтому нельзя получить полной картины в отношении реакционной способности и выхода углеводородов при добавлении спиртов, более высших, чем метанол, на катализаторах типа ZSM-5. Нигде не сообщалось, что побочный продукт, содержащийся в восстановленном метанольном продукте (главным образом этанол), приносит пользу в результате улучшенной реакционной способности бензину на цеолитсодержащем катализаторе. Не установлено также влияние добавления ничтожно малых количеств спиртов, более высших, чем этанол.
Langner (Appl. Catalysis, 2, p.289, 1982) показал, что добавление ничтожных количеств спиртов резко сокращает так называемый индукционный период, т.е. период нахождения их в потоке при заданной температуре и давлении, прежде чем произойдет конверсия из метанола в углеводороды.
Нельзя установить никакой связи между поведением переходного состояния кинетической среды (реагента, промежуточного продукта и продукта, контактирующего с катализатором), пока не установится конверсия метанола в углеводороды внутри цеолитных пор, и поведением состояния равновесия сразу же после начала конверсии метанола в углеводороды, если только картина процесса может быть установлена на определенной модели. Однако такой определенной модели не существует.
Для описания процесса конверсии оксигенатов в углеводороды предпочтительно применение комплексных кинетических моделей. Состав конечного суммарного продукта, полученного в результате конверсии оксигената, включает более 50 компонентов, а выход бензиновых продуктов и их распределение связаны с рабочими условиями проведения процесса и составом реакционной среды. Однако, вообще говоря, на выход бензина оказывает отрицательное влияние повышение рабочей температуры процесса синтеза.
Таким образом, основная проблема, имеющая отношение к конверсии оксигенатов в бензиновый продукт, касается управления тепловым режимом.
Характерной особенностью цеолитов и связанных с синтезом бензина катализаторов, описанных выше, является то, что при их применении имеют место два разных типа их деактивации. Один тип деактивации катализатора касается формирования углеродистых отложений, как правило, называемых коксом, на поверхности катализатора, который удаляют с катализатора после катализаторного цикла (продолжительность работы катализатора) при применении процедуры регенерации. Специалисты в данной области хорошо знают, что высокие температуры ускоряют коксообразование, в результате чего происходит потеря активности катализатора. Наряду с деактивацией катализатора, коксовые отложения также являются причиной потери углеродного потенциала, в результате чего снижается выход ценного продукта.
Под продолжительностью цикла работы катализатора понимается промежуток времени, когда катализатор демонстрирует необходимую каталитическую активность. По мере того как происходит дезактивация катализатора в результате образования коксовых отложений, количество активной части катализатора, необходимой для конверсии оксигенатов в бензин, снижается. Поэтому важно не допустить прохода (т.е. истечения неконвертированных) оксигенатов, поскольку их присутствие затруднит стадию разделения для получения целевого бензина. После такой продолжительности цикла катализатор должен быть восстановлен путем выжигания кокса. Процесс с коротким циклом активности катализатора подразумевает обязательное применение дорогостоящего реактора, например, с непрерывной регенерацией катализатора, циркулирующего между реактором и регенератором, или обязательное применение нескольких параллельно расположенных реакторов с частым переключением режима работы (синтез-регенерация) и оборудованных комплексным управлением. Увеличение цикла активности катализатора благоприятно влияет на технологический процесс, повышая его эффективность, и приводит к финансовой экономии.
Другой тип дезактивации катализатора представляет собой необратимое деалюминирование структуры катализатора. С течением времени этот тип дезактивации приводит к низкой производительности катализатора, и в конечном счете его следует заменять свежим катализатором. Рабочая температура проведения процесса также оказывает огромное влияние на скорость деалюминирования структуры катализатора.
Таким образом, помимо негативного влияния на выход требуемого продукта, вызванного чрезмерно высокими температурами реакции, управление тепловым режимом также играет важную роль в отношении как обратимой, так и необратимой дезактивации катализатора.
Решения, относящиеся к проблеме, связанной с управлением тепловым режимом, описанные в патенте США US 4,481,305, включают корректировку внутреннего и/или внешнего рециркулирования газа, с тем чтобы ограничить повышение температуры на стадии синтеза бензина, индивидуально задаваемой используемым типом катализатора. Корректировка степени рециркулирования, в свою очередь, влияет на состав подаваемого сырья. Другие традиционные средства корректировки состава компонентов подаваемого сырья включают в себя изменение рабочей температуры процесса синтеза оксигенатов, давления, количества добавляемой воды в процесс и скорости рециркулирирующего газа для получения синтез-газа, вводимого в объединенный процесс синтеза.
Сосредотачивая внимание на реакторе синтеза бензина, состав входящего потока сырья, содержащего оксигенат, первоначально вызывает выделение теплоты реакции, поэтому в адиабатическом реакторе-конвертере разность температур (ΔT) между входом и выходом тесно связана с концентрацией на входе.
Продукт, полученный со стадии синтеза оксигенатов, не учитывая неконвертированный синтез-газ, упоминается далее в описании как восстановленный продукт.
Чем относительно большее количество (в расчете на постоянное содержание атомов углерода) простых эфиров, высших спиртов и углеводородов содержится в восстановленном продукте, полученном на первой стадии синтеза, тем меньше выделяется теплоты реакции на количество бензинового продукта, выходящего со стадии синтеза бензина. Соответственно, если образуется меньше теплоты реакции на моль бензинового продукта, то выход бензина повышается и/или снижается необходимость регулирования температуры во время синтеза бензина.
Следует соблюдать минимальную температуру на входе в реактор, так как для цеолитов, применяемых при синтезе бензина, характерно то, что, если эта температура ниже определенного нижнего ее граничного значения, глубина конверсии в полезные составляющие бензина недопустимо низка.
Каталитические реакторы, используемые в традиционном способе синтеза бензина, следовательно, должны соответствовать требованиям, предъявляемым к управлению тепловым режимом, описанным выше. В то же время реактор должен быть в состоянии выдерживать рабочие условиях во время регенерации катализатора.
Реакторы с псевдоожиженным слоем катализатора без сомнения отвечают требованиям к управлению тепловым режимом, поскольку температура подаваемого сырья может быть при широком интервале концентрации восстановленного продукта скорректирована так, чтобы она на выходе не превышала интервал максимальных значений температуры. Этот тип реактора, однако, лучше всего подходит при работе реактора при низком давлении и требует применения катализатора наивысшей механической прочности.
Адиабатические реакторы представляют собой реакторы, которые не имеют внутренней терморегуляции, поэтому выделившуюся теплоту реакции следует регулировать путем надлежащей корректировки добавками состава загружаемого сырья. Однако адиабатические реакторы могут быть в свою очередь легко приспособлены для целей регенерации катализатора при нормальном режиме работы без риска механического износа. Кроме того, адиабатические реакторы дешевле, чем любой другой тип реактора.
Реакторы с охлаждаемой средой могут быть использованы с ограничением механической стабильности конструкции во время циклов их работы, переключаясь попеременно с обычного режима в режим регенерации и обратно. Охлаждаемые реакторы работают, как правило, с кипящей средой во взаимосвязи между теплопередачей и слоем катализатора, отводя тем самым теплоту реакции из реакционной зоны. Предпочтительной кипящей средой является вода, так как вода химически стабильна и чаще всего пар, образованный в результате отвода теплоты реакции, может быть использован непосредственно для средств обогрева. С другой стороны, под практическим ограничением, применяемым к давлению, подразумевается то, что температура кипящей воды выше 325°С почти никогда не встречается. Применение кипящей воды с более высокими температурами вплоть до температуры около 340°С является традиционным, однако дорогостоящим. Известно применение других теплоносителей, но в целом все эти решения являются более дорогостоящими.
Эффективность или, другими словами, насколько режим работы приближен к изотермическим условиям, зависит от механического расположения элементов, экзотермичности (которая может быть выражена через повышение температуры адиабатического слоя), кинетики и теплопроводящих свойств катализатора и реакционной среды. В общем, можно сказать, что охлаждаемые реакторы, где проводят экзотермические реакции, демонстрируют более низкие максимальные температуры, чем адиабатические реакторы, поскольку температура охлаждения ниже адиабатической температуры на выходе.
Закалочные, или с охлаждением между слоями катализатора, реакторы являются модификациями типа адиабатических реакторов, которые требуют регулирования скорости потока и его температуры в целях соблюдения заданным граничным значениям температуры. Если рассматривать всю технологическую схему объединенного процесса синтеза, скорость газового потока, проходящего через стадию синтеза бензина, является величиной, зависимой как от скорости газа, рециркулирующего на стадию синтеза оксигенатов, так и скорости (скоростей) газа, рециркулирующего вокруг стадии синтеза бензина. Иначе говоря, степень рециркуляции газовых потоков, как внутренняя, так и внешняя, отражается на скорости потока газа на стадии синтеза бензина и должна быть определена таким образом, чтобы для оптимальной конверсии синтеза в оксигенаты, на стадии синтеза оксигенатов, рабочая температура на стадии синтеза бензина, будь то адиабатический, охлаждаемый, внутреннего охлаждения или закаленный реактор, была в температурном диапазоне от самой низкой температуры до температуры верхних пределов. Сокращение расхода газа на стадии реакции бензина улучшит процесс экономии путем снижения размеров оборудования и стоимости коммунальных услуг при эксплуатации этого процесса.
Задачей данного изобретения является создание способа, при осуществлении которого оксигенаты, включающие в свой состав другие высшие спирты С3+ и метанол, превращаются в углеводородные продукты, которые можно использовать в качестве компонентов высококачественного бензина.
Кроме того, задачей настоящего изобретения является создание улучшенного способа конверсии синтез-газа в высокотоварные бензиновые продукты при высоком их выходе.
Еще одна задача данного изобретения направлена на осуществление процесса синтеза бензина в реакторе, охлаждаемом кипящей водой, который способен выдерживать рабочий режим на протяжении всего цикла его работы, а также во время регенерации катализатора.
Краткое изложение сущности изобретения
Данное изобретение, таким образом, относится к способу синтеза углеводородных компонентов бензина, характеризующемуся тем, что он включает каталитическую конверсию на стадии синтеза бензина оксигенатсодержащего сырья, содержащего метанол и/или простой диметиловый эфир и смесь, содержащую в пересчете на общий оксигенатный состав, по меньшей мере, 0,05 мас.% высших спиртов С3+ и/или их оксигенатных эквивалентов, в углеводородные компоненты бензина.
Описание чертежей
На Фиг.1 показан вариант осуществления способа.
На Фиг.2 показано размещение катализатора в варианте осуществления изобретения.
На Фиг.3 показан вариант осуществления способа, включающего стадию разделения.
На Фиг.4а и 4b показана конверсия метанола и высших спиртов при различных скоростях подачи потока.
На Фиг.5а и 5b показан выход, полученный при конверсии метанола и высших спиртов.
На Фиг.6а и 6b показаны результаты хроматографического анализа, полученные для смеси метанола и высших спиртов.
На Фиг.7а и 7b показана степень конверсии смеси метанола и высших спиртов.
На Фиг.8а и 8b показан выход продукта из смеси метанола и высших спиртов.
На Фиг.9а и 9b показаны зависимости температуры при 50% конверсии от концентрации высших спиртов.
Подробное описание изобретения
Данное изобретение относится к технологии синтеза бензина, осуществляемого при проведении типичных стадий протекания процесса, а также к синтезу продуктов, осуществляемому с точки зрения аппаратно-технологического оформления в виде объединенного процесса синтеза.
В настоящее время установлено, что синергический эффект стадий синтеза продукции объединенного процесса синтеза бензина имеет место в случае, когда содержание высших спиртов С3+, в пересчете на общий оксигенатный состав поступающего на стадию синтеза бензина, составляет, по меньшей мере, 0,05 мас.%, что позволяет снизить скорости рециркулирования через стадию синтеза бензина и/или повысить суммарный выход бензина, за счет чего, в свою очередь, улучшаются экономические показатели процесса синтеза бензина.
Оказалось совсем неожиданным, что эффект синергизма в объединенном процессе синтеза оксигенатов и бензина возникает тогда, когда на стадии синтеза оксигенатов образуется достаточное количество высших спиртов. Поддерживая постоянный объем выпуска продукции и качество бензина, скорость питающего потока, поступающего на стадию синтеза оксигенатов, таким образом, значительно снижается, что позволяет существенно снизить его температуру на входе стадии синтеза бензина. Еще более удивительным оказывается то, что этот эффект синергизма преобладает при довольно низких концентрациях высших спиртов С3+, составляющих по меньшей мере 0,05% в пересчете на общий оксигенатный состав, поступающий на стадию синтеза бензина.
Было установлено, что при осуществлении конверсии смесей высших спиртов С3+ на цеолитных катализаторах, таких как ZSM-5, температура, при которой достигают заданной степени конверсии (1-99%) их в углеводороды, существенно ниже температуры, при которой достигают такой же степени конверсии при применении в качестве сырья химически чистого метанола или метанола, в котором присутствует некоторое количество сопутствующих продуктов: этанола, пропанола и бутанола, сохраняя при этом сопоставимое качество углеводородных продуктов.
В частности, было неожиданно установлено, что эффект нелинейной зависимости лежит в основе этого явления, при котором низкое содержание высших спиртов С3+ в интервале от 0,05 до 1 мас.% обеспечивает достижение этого эффекта. Этот эффект достигается путем проведения объединенного процесса синтеза, например, если высшие спирты совместно образуются на стадии синтеза оксигенатов, а также при проведении синтеза бензина, который включает самостоятельные стадии протекания процесса с совместной подачей высших спиртов С3+ или путем получения на отдельной установке оксигената, содержащего высшие спирты С3+.
Кроме того, было неожиданно установлено, что уровень снижения температуры, обусловленный присутствием высших спиртов С3+ в сырье, содержащем оксигенаты, является самым высоким, если оксигенатное сырье содержит от 5 мас.% до 15 мас.% высших спиртов С3+.
Далее было установлено, что сравнительно низкое содержание прежде всего этанола не ускоряют конверсию метанола в углеводороды в такой же степени, как это делают высшие спирты С3+, так что содержание высших спиртов С3+ в восстановленном продукте должно быть больше 0,05 мас.% в пересчете на общий оксигенатный состав для того, чтобы получить в данном случае этот эффект.
Восстановленный продукт содержит оксигенаты (высшие спирты С3+), образованные на стадии синтеза оксигенатов, метанол и в предпочтительном варианте включает в свой состав простой диметиловый эфир и высшие эфиры, необязательно также углеводороды. Было установлено, что добавление только этанола при высоких уровнях (30%) ускоряет конверсию метанола, но приводит к пониженному выходу продукта, тогда как смеси спиртов, содержащие этанол наряду с другими высшими спиртами, превосходят любой из индивидуальных компонентов восстановленного продукта как по степени конверсии, так и по выходу.
Присутствие малых количеств высших спиртов С3+, т.е. содержание их в количестве от 0,05 до 1 мас.% в пересчете на общий оксигенатный состав, в восстановленном продукте, при подаче его в реактор синтеза бензина имеет преимущество, заключающееся в том, что оно:
(1) позволяет использовать пониженную температуру на входе в реактор синтеза бензина и
(2) приводит к снижению роста адиабатической температуры при полной конверсии.
Это в свою очередь приводит к повышенному выходу продукта С5+ как в адиабатическом реакторе, так и в реакторе охлаждаемого типа. С другой стороны, при поддержании уровня температуры на выходе из реакционной зоны допускается повышенная концентрация восстановленного продукта в потоке исходного сырья, поступающего на стадию синтеза бензина, то есть допускается рост повышенной адиабатической температуры, в результате чего обеспечивается снижение суммарной скорости подачи в реактор синтеза бензина. При применении реактора с петлевой конфигурацией за счет этого снижается количество газа, который должен быть возвращен в рецикл для обеспечения регулирования уровня температуры.
Таким образом, если питающий поток, поступающий на стадию синтеза бензина, содержит малые количества спиртов С3+, т.е. от 0,05 до 1 мас.% в пересчете на общий оксигенатный состав, то это позволяет получить вышеупомянутые преимущества.
Присутствие высших спиртов С3+ в восстановленном продукте обеспечивает снижение рабочей температуры стадии синтеза бензина. Хотя традиционно температура потока, входящего на стадию синтеза бензина, обычно составляет минимальное значение 350°С, присутствие высших спиртов С3+ в количестве 0,05 мас.% или более в пересчете на общий оксигенатный состав приводит к тому, что стадию синтеза бензина можно проводить при более низкой минимальной температуре потока на входе в реакционную зону, по меньшей мере, на 20°С ниже, чем используют традиционно. Рабочий минимальный диапазон температуры можно снизить, например, с 350°С до 320-330°С.
Снижение рабочей температуры до таких значений имеет особое преимущество, поскольку такой температурный режим позволяет использовать реакционные аппараты типа реакторов, охлаждаемых кипящей водой, которые обеспечивают охлаждение температуры процесса так, что минимальная его температура имеет значение ниже 340°С. В предпочтительном варианте температура кипящей воды составляет около 325°С или ниже этого значения. Для проведения традиционных процессов синтеза бензина обычно требуются реакторы, которые могут работать при более высоких температурах, например в интервале от 350-400°С.
Обеспечение в реакторе минимальной температуры порядка 350°С приведет к установлению давления кипящей воды до значения более 165 бар, что делает реактор этого типа экономически невыгодным.
Данное изобретение относится также к улучшенному способу конверсии синтез-газа в объединенном процессе синтеза оксигенатов и бензина, при этом улучшение этого способа достигается путем получения на стадии синтеза оксигенатов восстановленного продукта с содержанием спиртов С3+, по меньшей мере, 0,05 мас.% в пересчете на общий оксигенатный состав. Синергетический эффект наблюдается в объединенной системе синтеза при вышеупомянутых условиях, приводящих к снижению скорости возвращенного на рецикл потока газа, и в особенности скорости потока газа, проходящего через стадию синтеза оксигенатов.
Снижением скорости рециркулирования вокруг стадии синтеза бензина достигается надлежащая степень влияния, которое оказывают высшие спирты С3+, образованные на стадии синтеза оксигената, в том смысле, что снижается, таким образом, нижний предел температуры на стадии синтеза бензина. В свою очередь, стадия синтеза оксигената извлекает выгоду за счет дополнительного получения высших спиртов, что приводит к более высокой степени конверсии синтез-газа за проход через эту стадию и, таким образом, к более высокому выходу оксигенатной продукции.
Объединенный процесс синтеза бензина включает в себя следующие стадии:
- синтез-газ с объемным соотношением водорода к монооксиду углерода, например, в интервале от 0,1 до 6 подают в секцию синтеза, содержащую реакционную зону, в которой протекают две основных стадии конверсии: стадия синтеза оксигената, за которой следует стадия синтеза бензина, при этом место подачи сырья может находиться в любом удобном для проведения процесса месте, например до входа потока на стадию синтеза оксигенатов;
- на стадии синтеза оксигената синтез-газ превращают в восстановленный продукт, содержащий метанол, высшие спирты, и в том числе предпочтительно простой диметиловый эфир и простые эфиры высших спиртов, и также необязательно углеводороды; вытекающий поток продукта (эффлюент), кроме того, содержит неконвертированный синтез-газ и инертные газы. Стадия синтеза оксигенатсодержащего сырья может быть разделена на ступени неполного синтеза оксигенатов, которые могут включать в себя любые традиционно используемые типы реакторов и располагаться последовательно и/или параллельно;
- на стадии синтеза бензина оксигенатную фракцию восстановленного продукта дегидратируют до соединений, кипящих в диапазоне бензина (углеводородные компоненты), при высоком их выходе с образованием совместно полезных легких (газообразных) продуктов и мизерных количеств метана и этана, легкие продукты далее отделяют, по меньшей мере, частично от непрореагировавшего синтез-газа. Пригодные для применения типы реакторов синтеза бензина включают в свой состав адиабатические, с охлаждением между слоями катализатора, или закалочные, и охлаждаемые реакторы, и они могут быть разделены на одну или несколько секций и расположены последовательно и/или параллельно общеизвестным в данной области техники способом.
Типы реакторов, которые особенно подходят для синтеза бензина, включают в себя охлаждаемые типы реакторов, в которых охлаждение происходит за счет образования пара из кипящей воды.
Инертные газы, содержащиеся в газе, подаваемом на синтез, и низшие парафины, образованные в реакции синтеза и не растворенные на стадии разделения, должны быть очищены продувочным газом в надлежащем месте синтеза. Расход потока продувочного газа может составлять ничтожное количество (<10%) по сравнению со свежим синтез-газом, поступающим в контур синтеза, что свидетельствует о высокой глубине превращения реагентов синтез-газа в бензин, или же он может составлять количество, которое затем можно использовать в последовательной переработке.
Неконвертированный синтез-газ может быть возвращен рециркуляцией в любое место производственной линии в направлении вверх от стадии синтеза оксигенатов, или в секцию получения синтез-газа, или в любое место в стадии синтеза оксигенатов и/или стадии синтеза бензина. Если соотношение внутреннего и внешнего рециркуляционных потоков поддерживается постоянным, то на стадии синтеза оксигенатов проводят такую же степень гидрирования нежелательных олефинов, что обеспечивает выход продукта сопоставимого/аналогичного углеводородного состава. В связи с этим нет никакого другого различия между внешним и внутренним рециклом в том смысле, что внутренний рецикл включает в себя меньшее количество стадий неполного синтеза оксигенатов, чем внешний.
Необязательно блоки введения воды/пара и удаления CO2 располагают в секции совместного синтеза, что обеспечивает оптимальное применение реагентов конверсии синтез-газа в бензин. Это технологическое оформление является предпочтительным, когда заданное отношение водорода к монооксиду углерода составляет значение около 1 или ниже, а оксигенатная фракция содержит простой диметиловый эфир и/или высшие эфиры. В этом случае термодинамический потенциал конверсии в оксигенаты может существенно повышаться. Эти аспекты обсуждаются в патенте США US 4,481,305.
Содержание высших спиртов С3+ на входе в реактор синтеза бензина выше 0,05 мас.% в пересчете на общий оксигенатный состав в восстановленном продукте, и количество неконвертированного синтез-газа, рециркулированного на стадию синтеза оксигенатов и/или стадию синтеза бензина, должно быть скорректировано так, чтобы обеспечить возможность функционирования реактора конверсии бензина при температурах выше нижних и не превышающих верхних предельных значений температуры, задаваемых по катализатору.
В соответствии с настоящей технологией предлагается также улучшенный способ получения бензина путем создания рецикла восстановленного продукта вокруг стадии синтеза оксигената и/или синтеза бензина таким образом, чтобы концентрация оксигената и углеводорода на входе в реактор синтеза бензина позволяла реактору функционировать в заданном цикле при температурах в интервале нижних и верхних предельных значений температуры, устанавливаемых в соответствии с потребностями к выходу бензина.
В объеме данного изобретения также предлагается способ превращения метанола в углеводороды при повышенном их выходе и/или пониженной скорости дезактивации катализатора, если высшие спирты, содержащиеся в потоке исходного сырья, поступающего на стадию синтеза бензина, составляют в интервале 0,05-1 мас.% высших спиртов С3+ в пересчете на общий оксигенатный состав. Высшие спирты могут поступать или со стадии синтеза оксигенатов в виде смеси (объединенного процесса синтеза), или же они могут поступать из самостоятельной стадии синтеза, не входящей (т.е. не совмещенной) в стадию синтеза бензина, или же высшие спирты С3+ можно вводить и просто подавать совместно с исходным сырьем в стадию синтеза бензина.
Общеизвестно в данной области производства, что катализаторы, используемые в синтезе бензина, вообще очень активны в реакции этерификации спиртов. Таким образом, при воздействии на катализатор синтеза бензина любых смесей спиртов и простых эфиров необходимо сразу же обеспечить равновесное состояние путем контактирования с кислотным катализатором синтеза бензина.
Следовательно, следует понимать, что в способе настоящего изобретения касательно содержания высших спиртов в восстановленном продукте, содержащем оксигенат или смеси оксигенатов, количество высших спиртов С3+, связанных в виде простых эфиров, также подсчитывается и поэтому его следует рассматривать как долю высших спиртов С3+, присутствующих в восстановленном продукте. Иными словами, производные простых эфиров высших спиртов С3+ считаются в качестве эквивалентов высших спиртов С3+. Оксигенатсодержащая смесь представляет собой целевую фракцию оксигената, присутствующую в питающем потоке стадии синтеза бензина, образующегося в результате совместной подачи оксигената и/или полученного отдельно и/или полученного в объединенном процессе синтеза (т.е. восстановленный продукт).
В случае когда высшие спирты, необходимые для осуществления способа в соответствии с настоящим изобретением, получают путем добавления или совместной подачи высших спиртов в последовательно протекающий и объединенный процесс синтеза, то высшие спирты можно предпочтительно вводить на стадии синтеза оксигенатов. В этом случае также целесообразно добавление этанола. Таким образом, даже несмотря на то, что этанол сам по себе не оказывает благоприятного эффекта на реакцию конверсии оксигенатов в углеводороды, которыми являются высшие спирты С3+, этанол оказывает благоприятное влияние на образование высших спиртов С3+ в стадии синтеза оксигенатов. Общеизвестно в данной области, что этанол является промежуточным продуктом в процессе образования высших спиртов и других оксигенатов из синтез-газа и что добавление спиртов, содержащих, по меньшей мере, одну С-С связь, и простых эфиров таких спиртов значительно усиливает образование высших спиртов (см., например, K.J.Smith и R.В.Anderson, Journal of Catalysis 85 (1984) 428; A.M.Hilmen и др., Applied Catalysis A, 169 (1998) 355; R.G.Herman, Catalysis Today 55 (2000) 233).
Иными словами, хотя введение этанола и/или его простых эфиров не оказывает непосредственно благоприятного эффекта в реакции превращения оксигенатов в углеводороды, которые представляют собой высшие спирты С3+, введение этанола и/или его эфиров в стадию синтеза оксигенатов действительно ускоряет образование высших спиртов С3+, которые оказывают благоприятное действие в реакции конверсии оксигенатов в целевые углеводороды. Следовательно, еще одной задачей настоящего изобретения является создание способа превращения этанола в ценные углеводородные продукты путем введения потока этанолсодержащего материала в стадию синтеза оксигенатов.
Введение в стадию синтеза бензина смесей, содержащих этанол для ускорения образования высших спиртов, является особенно важным моментом настоящего изобретения, поскольку такие смеси можно получить из восстанавливаемых источников энергии (возобновляемых источников энергии), таких как источники продуктов сельскохозяйственной и лесной промышленности и сопутствующие продукты промышленной, сельскохозяйственной и лесной переработки и бытовые и коммунальные отходы, которые находят практическое применение в относительно крупном масштабе путем брожения или бактериальными процессами с выходом так называемого биоэтанола. Биоэтанол приобретает важное значение в качестве компонента смеси с бензином благодаря его способности снижать выброс диоксида углерода в окружающую среду.
В качестве компонента бензиновой смеси этанол должен практически не содержать воды для предотвращения разделения фаз. В соответствии с данными Ullmann (Ullmann' s Encyclopedia of Industrial Chemistry, 6th Ed., 2002) необходимо, чтобы чистота биоэтанола составляла 99,5%. Одним из недостатков в производстве биоэтанола такой высокой степени чистоты является то, что перегонка требует большого расхода энергии. По данным Ullmann установка для производства этанола в качестве компонента моторного топлива имеет суммарное потребление энергии от 1,1 до 1,6 МДж на литр этанола.
В одном из вариантов осуществления настоящего изобретения водный этанол, например, полученный путем ферментации биомассы или бактериологическими методами, в предпочтительном варианте можно вводить в стадию синтеза оксигенатов последовательно осуществляемого или совмещенного синтеза бензина. В объединенном процессе синтеза бензина особенно предпочтительно осуществлять введение водного этанола при низких отношениях водорода к монооксиду углерода в синтез-газе, получаемом обычно газификацией твердых топлив или тяжелой нефти. В таких случаях предпочтительно вводить определенное количество пара в синтез-газ с целью достижения оптимального стехиометрического соотношения водорода и монооксида углерода на стадии синтеза оксигенатов за счет реакции конверсии водяным газом, показанной в уравнении (2). Таким образом, введение водного этанола одновременно служит как для корректировки соотношения водорода и монооксида углерода, так и для ускорения образования высших спиртов С3+.
В этом варианте осуществления изобретения предлагается также способ эффективной утилизации водного этанола, полученного, например, путем ферментации биомассы, что позволяет сократить энергозатраты и снизить себестоимость оборудования для перегонки водного этанола-сырца в топливный этанол, не говоря уже об экономии средств на инфраструктуры, например как нефтеперерабатывающие заводы и бензозаправочные станции, имеющие отношение к производству этанол-бензиновой смеси.
Многочисленные катализаторы синтеза метанола обладают способностью к гидрированию альдегидов, кетонов и карбоновых кислот и простых их алкиловых эфиров до спиртов, которые составляют легко конвертируемую группу производных кислородсодержащего соединения по сравнению с альдегидами и кетонами. Таким образом, потоки, содержащие альдегиды, кетоны и карбоновые кислоты и их простые эфиры, можно также использовать в стадии синтеза оксигенатов для ускорения образования высших спиртов С3+.
Катализаторы, пригодные для применения в стадии синтеза оксигенатов для получения высших спиртов, включают в себя катализаторы, содержащие смесь ZnO и Cr2O3, Cu/ZnO, сульфиды переходных металлов, например MoS2 и Сu-содержащие оксидные комплексы, каждый промотированный щелочью, а также смесь ZnO и ZrO2, промотированную редокситом и сильным основанием, Pd и Cu-катализаторы на основе диоксида циркония и оксидов редкоземельных металлов и катализаторы на основе благородных металлов. В частности, катализаторы на основе Cu и/или ZnO можно использовать для конверсии синтез-газа в смеси метанола и высших спиртов.
В соответствии с данным изобретением предпочтительными катализаторами высших спиртов являются такие, которые имеют низкую чувствительность к присутствию CO2 и рабочую температуру в диапазоне функционирования катализатора, присутствующего в оксигенате, т.е. в интервале температуры от 200 до 350°С. Выход высших спиртов в синтезе высшего спирта может быть относительно небольшим. В предпочтительном варианте выход углеводородов ниже С5 является небольшим. В предпочтительном варианте если активность катализатора в отношении продукции высших спиртов является низкой, то желательно, чтобы содержание высших спиртов в восстановленном или смешанном оксигенате было исключительно небольшим.
Катализатор, активный в синтезе высших спиртов, может быть размещен в отдельном реакторе последовательно или параллельно в стадии синтеза оксигенатов, но его можно также успешно размещать в любом реакторе вместе с одним или несколькими другими катализаторами синтеза оксигенатов.
Фиг.1 служит в качестве иллюстрации данного изобретения, раскрываемого выше в одном из его вариантов осуществления. Теплообменники и компрессоры не показаны.
Синтез-газ 10, полученный, например, в секции получения синтез-газа, вводят в замкнутый контур объединенного синтеза бензина, содержащий реактор синтеза оксигенатов 25, реактор синтеза бензина 35 и блок разделения 55. В предпочтительном варианте синтез-газ 10 вводят сразу же в место входа потока в реактор синтеза оксигенатов 25, хотя можно использовать другие места подачи сырья, например наличие большего количества переходов, чем между индивидуальными стадиями синтеза оксигенатов. Необязательно внешний рециркуляционный поток 110, полученный из блока разделения 55, смешивают с синтез-газом 10 и полученную газовую смесь 20 направляют в реактор синтеза оксигенатов 25. Внутренний рециркуляционный поток 100, полученный из блока разделения 55, может быть введен в восстановленный продукт, содержащий оксигенаты.
В реактор синтеза оксигенатов 25, который может включать один или несколько реакторов, выбранных из любого общеизвестного в данной области типа реакторов, загружают один или несколько катализаторов, которые обеспечивают конверсию синтез-газа в восстановленный продукт, содержащий, по меньшей мере, 0,05 мас.% высших спиртов С3+ в пересчете на общую массу оксигената.
Выходящий поток (эффлюент) 30 из реактора синтеза оксигенатов 25, содержащий восстановленный продукт, может быть смешан с рециркуляционным газом 100 из блока разделения 55, с получением общего питающего потока, подаваемого в реактор синтеза бензина 35. Содержание оксигенатов вообще скорректировано так, чтобы обеспечить конверсию на стадии синтеза бензина в диапазоне температур, определенном по нижним и верхним граничным значениям температуры, о которых говорилось ранее.
Поток продуктов 50 (эффлюент), выходящий из реактора синтеза бензина 35, содержащий углеводородные компоненты бензина и, кроме того, легкие углеводородные продукты, проходит в блок разделения 55. Блок разделения 55 включает средства для разделения неконвертированного синтез-газа от бензиновых продуктов, легких углеводородных продуктов и воды и извлечения ценных продуктов из продувочного газа при его присутствии. Блок разделения 55 может также включать в себя узел для перегонки для получения бензинового продукта.
В одном варианте технологического оформления предлагаемого изобретения блок разделения 55 может содержать 3-фазовый сепаратор, узел промывки продувочного газа и фракционирования продуктов в топливный газ 80. Топливный газ представляет собой продувочный газ, необязательно с извлеченными из него ценными продуктами, который смешан с растворенным газом, сжиженный углеводородный газ LPG 70 представляет собой легкий углеводородный продукт, необязательно подвергаемый дальнейшей переработке для того, чтобы гидрогенизировать долю присутствующих в нем олефинов, и бензин 60 представляет собой высококипящие углеводороды, полученные в качестве основного продукта.
Разделенный поток непрореагировавших реагентов синтез-газа 90 без обработки его продувочным газом возвращают затем рециклом необязательно сначала в секцию получения синтез-газа через линию 120 и в реактор синтеза оксигенатов 25 через линию 110 и/или в реактор синтеза бензина 35 через линию 100.
Реактор синтеза оксигенатов 25 может включать один или несколько реакторов синтеза, где может протекать синтез оксигенатов. Катализаторы, используемые в синтезе оксигенатов, могут быть размещены в одном или нескольких реакторах синтеза оксигенатов на одном или нескольких уровнях температуры и с одним или несколькими местами подачи синтез-газа. Катализатор(ы) или фракции, контактирующие с ним, помимо того, что должны быть активны в образовании метанола из синтез-газа, также активны и в катализе высших спиртов С3+.
Предпочтительно также присутствие катализатора, активного в образовании простых эфиров в секции синтеза оксигената, при этом катализаторы размещены или смешаны так, чтобы восстановленный продукт включал в себя, по меньшей мере, метанол, простой диметиловый эфир и высшие спирты С3+. В предпочтительном варианте применение рецикла 100 вокруг стадии синтеза бензина 35 снижает необходимость применения рецикла газа вокруг стадии синтеза оксигената, если достигается удовлетворительная степень конверсии синтез-газа в оксигенаты.
Необязательно, катализаторы можно размещать или смешивать таким образом, чтобы восстановленный продукт, кроме того, включал в свой состав простые эфиры высших спиртов и углеводороды. Примеры применения таких комбинаций катализаторов многочисленны, и возможные технологические схемы или размещения таких комбинаций превышают объем настоящего изобретения. Один из примеров технологического оформления показан на Фиг.2.
На Фиг.2 показан пример технологической схемы размещения катализаторов. Охладители не показаны, поскольку их размещение не имеет никакого отношения к описанному процессу. Катализаторы могут быть размещены в одном или нескольких реакторах с применением наиболее удобного расположения.
В этом варианте осуществления изобретения показаны три стадии синтеза оксигенатов. Синтез-газ 10 превращается в метанол в первой стадии синтеза оксигенатов 2 с применением катализатора синтеза метанола, такого как коммерчески доступный МK 121, который производит фирма Haldor Topsoe A/S, который представляет собой тип оксидных катализаторов, содержащий Cu/ZnO. Первый вытекающий оксигенатный поток 3, содержащий метанол, затем передают из первой стадии синтеза оксигената 2 на вторую стадию синтеза оксигената 4, содержащую катализаторы, пригодные для дальнейшей конверсии непрореагировавших реагентов синтез-газа, а часть метанола направляют во второй вытекающий оксигенатный поток 5, содержащий среди других реагентов простой диметиловый эфир. В качестве примера таких катализаторов могут служить алюмооксидные катализаторы или алюмосиликатные катализаторы, например коммерчески доступные DMK-10 производства фирмы Haldor Topsoe A/S. Второй вытекающий оксигенатный поток 5 из второй стадии синтеза оксигенатов 4, включающий смесь метанола, диметилового эфира и неконвертированные реагенты синтез-газа, затем конвертируют в третьей стадии синтеза оксигенатов 6 с получением третьего вытекающего оксигенатного потока 7, содержащего смесь метанола, простого диметилового эфира, высшие спирты С3+, простые эфиры высших спиртов С3+ и неконвертированные реагенты синтез-газа. Пригодные для применения катализаторы включают в свой объем вышеуказанные катализаторы DMK-10, промотированные щелочью ZnO/Cr2O3 и Cu/ZnO, размещенные, например, слоями поочередно или в виде смесей.
Предусматривается также применение нескольких возможностей обхода. Байпасные потоки 8, 9 и 11 могут служить в качестве средства охлаждения и/или корректировки состава исходного сырья, подаваемого в реакторы с нисходящим потоком, за счет чего обеспечивается повышенная глубина конверсии. Синтез-газ 10 может быть введен во вторую стадию синтеза оксигенатов 4 через байпасную линию 8 или же альтернативном варианте непосредственно введен в третью стадию синтеза оксигенатов 6 через байпасную линию 9. Кроме того, некоторая часть вытекающего потока 3 из первой стадии синтеза оксигенатов 2 может обойти вторую стадию синтеза оксигената 4 и введена в питающий поток (т.е. во второй вытекающий поток оксигенатов 5 на третьей стадии синтеза оксигенатов 6. Эти байпасные контуры имеют преимущество в том, что они служат в качестве средств охлаждения и/или корректировки состава сырья, подаваемого в реакторы нисходящего типа, за счет чего обеспечивается улучшение конверсии, как уже упоминалось выше.
Корректировка соотношения компонентов в синтез-газе может включать в себя корректировку, обеспечиваемую реакцией конверсии водяным газом (паром), в результате которой можно повысить соотношение водорода и монооксида углерода, если воду вводят в стадию процесса, активную в реакции синтеза водяного газа, или же за счет одного или нескольких компонентов, которые могут быть удалены абсорбционными или мембранными элементами.
Фиг.3 иллюстрирует еще один вариант осуществления изобретения. В этом варианте теплообменники и компрессоры не показаны. Стадия разделения описана подробно, чтобы показать размещение блока разделения (14) внутри контура синтеза. Численные обозначения, приведенные в треугольниках, являются точками отсчета, упоминаемыми в Примерах 4-6.
Каменноугольный газ 10, полученный путем газификации угля, который содержит синтез-газ, смешивают с рециркуляционным газом и подвергают очистке от кислых газов 11 (AGR), при которой удаляют кислые содержащие серу соединения и диоксид углерода. Вытекающий поток из стадии удаления кислого газа 11 направляют на стадию синтеза оксигената 12 для получения оксигенатов, например смеси метанола и высших спиртов. Воду 13 вводят в этот процесс в виде жидкости или пара, выше по потоку от стадии синтеза оксигенатов 12 для корректировки полученного состава непрореагировавшего синтез-газа на выходе стадии синтеза оксигената.
В этом конкретном варианте установка AGR по очистке кислых газов расположена внутри контура объединенного процесса синтеза. Другая установка AGR может быть расположена на линии подачи угольного газа в качестве альтернативы или в дополнение к установке AGR внутри контура объединенного процесса синтеза. Эти альтернативные технологические схемы размещения могут быть рассмотрены по экономическим соображениям, но для демонстрации эффективности процесса конверсии и эффектов, связанных со степенью рециркуляции, этот метод представляется самым выгодным в смысле конверсии.
Кроме того, возможно, потребуется дополнительная стадия очистки от серусодержащих соединений, например как удаление мелкодисперсных сернистых соединений путем пропускания через соответствующий слой обычного абсорбента, размещенный выше стадии синтеза оксигената 12, который не показан на Фиг.3. Вытекающий поток оксигенатов, полученный в стадии синтеза оксигенатов 12, подается на стадию синтеза бензина 13 для синтеза бензина. Вытекающий поток из стадии синтеза бензина 13 направляют в парожидкостный VLL сепаратор 14 для отделения бензина-сырца 16 и воды 15.
Полученный бензин-сырец, который содержит пропан и бутан и растворенные газы, направляют в секцию перегонки для фракционирования с получением бензиновой фракции (а также пропана и бутана, которые можно считать как совместно полученные продукты). Олефины, присутствующие в бензине-сырце, могут быть гидрогенизированы. Компоненты бензина могут быть извлечены из продувочного газа.
В предпочтительном варианте осуществления изобретения зона стадии синтеза оксигенатов расположена так, чтобы уровень температуры вытекающего потока (эффлюента) продуктов из этой стадии был достаточным, чтобы отпадала необходимость его нагрева или охлаждения перед поступлением на стадию синтеза бензина.
Данное изобретение продемонстрировано далее нижеследующими примерами его осуществления.
В примерах термин ВС используется для обозначения высших спиртов и их эквивалентов.
Примеры
Пример 1
Проводят серию экспериментов в кварцевом реакторе, имеющем внутренний диаметр 4 мм. Для этого 250 мг цеолитного катализатора типа HZSM-5 (с размером частиц от 150-300 мкм) смешивают с 500 мг диоксида кремния, SiC и загружают в реактор. Используют пять различных вариантов подачи сырья, показанных в Таблице 1.
Реакционный процесс проводят при атмосферном давлении и температуре в интервале от 250 до 370°С и скорости потока 60 нмл/мин и 105 нмл/мин соответственно, что соответствует среднечасовой скорости подачи сырья (WHSV) 1,4 (стандартной для промышленного производства) и расходу 2,45 г/г катализатора ч.
На Фиг.4а и 4b показаны результаты суммарной конверсии метанола и простого диметилового эфира в зависимости от изотермической рабочей температуры процесса, и на Фиг.5а и 5b показан выход углеводородных продуктов фракции C5+ в зависимости от изменения рабочей температуры изотермической реакции.
Как можно видеть из данных, приведенных на Фиг.4 и 5, показатели степени конверсии метанола, а также его выход в зависимости от изменения температуры снимали в каждом эксперименте. На этих чертежах степень конверсии определяется следующей формулой:
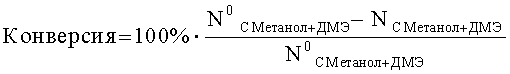
где:
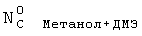 означает общее количество атомов углерода, присутствующих в метаноле и ДМЭ в исходном сырье, а
означает общее количество атомов углерода, присутствующих в метаноле и ДМЭ в исходном сырье, а
NC Метанол+ДМЭ означает общее количество атомов углерода, присутствующего в метаноле и ДМЭ в полученном продукте.
Выход продукта определяется как % доля атомов углерода, полученная из метанола, ДМЭ или высших спиртов, которые присутствуют в указанном продукте или группе продуктов.
В соответствии с данными, приведенными на этих чертежах, можно видеть, что степень конверсии метанола повышается, если в метанольное сырье не прибавляют ни этанол, ни изопропанол, ни 1-бутанол, в то время как выход компонентов углеводородов C5+ увеличивается только при добавлении к нему высших спиртов С3+. Из Фиг.5 можно видеть, что выход продукта в зависимости от температуры является величиной, не зависимой от высшего спирта, вводимого при температуре, превышающей температуру, при которой конвертируются все высшие спирты и ДМЭ. Можно также отметить, что этанол, несмотря на свой промотирующий конверсию эффект, снижает выход бензиновых компонентов в целевом продукте. Оказывается также, что спирты, содержащие большее число атомов углерода, чем этанол, т.е. высшие спирты С3+, демонстрируют как эффект, ускоряющий конверсию, так и эффект, повышающий выход целевого продукта.
Результаты исследований, проведенных Le Van Мао и др., свидетельствующие о том, что состав суммарного продукта, полученного в результате конверсии пропанола и бутанола, близок к составу суммарного продукта, полученного из реакции конверсии метанола, подтверждены путем анализа (см. Фиг.6а и 6b, которые показывают результаты хроматографического анализа по распределению продуктов, полученных из метанола и смеси, состоящей из 70 мол.% метанола и 30 мол.% высших спиртов (Примеры исходного сырья 1-4).
Пример 2
Этот пример демонстрирует один из основополагающих принципов настоящего изобретения, а именно полученный эффекта снижения температурного режима, при котором происходит реакция конверсии.
Повторяют методику Примера 1. Однако поддерживая концентрацию метанола на уровне 7 мол.% в смеси его с азотом, к ней добавляют еще смесь высших спиртов (ВС) определенного состава, приведенного в Таблице 2. Смесь высших спиртов вводят при различных нормах расхода, определяемых в расчете на мас.% метанольного сырья в интервале значений от 0,1 до 35 мас.% ВС. Этанол не подпадает под определение высших спиртов С3+, но включен в эту таблицу в целях сравнения.
Аналогичную смесь высших спиртов можно получить при проведении конверсии синтез-газа в соответствии с патентом США US 4,668,656. Объемные скорости подачи составляют 60 нмл/мин и 150 нмл/мин, что соответствует среднечасовой скорости подачи метанола 1,4 и 3,5 г/г катализатора ч.
Полученные показатели степени конверсии метанола и высших спиртов, а также их выход в зависимости от температуры приведены для каждого эксперимента на Фиг.7а, 7b, 8а и 8b. Для характеристики степени конверсии и выхода продуктов используют определения, приведенные в Примере 1.
На Фиг.7а и 7b показаны результаты конверсии смеси метанола и высших спиртов в зависимости от рабочей температуры в изотермических условиях процесса. Результаты проведения конверсии метанола-сырца (обозначенного на указанных фигурах как "сырец"), описанной в сравнительном Примере 3, отражены наряду результатами, полученными при конверсии смеси, включающей в свой состав высшие спирты (ВС).
На Фиг.8а и 8b показан выход продуктов С5+, в том числе метанола-сырца, в зависимости от рабочей температуры в изотермических условиях процесса.
Как можно видеть на кривых зависимости на обоих этих чертежах, заметный эффект возникает при введении даже незначительного количества высших спиртов в метанольное сырье. Рабочая температура может быть снижена примерно на 20-30°С например с 350°С до температуры от 320 до 330°С, в зависимости от доли высших спиртов по сравнению с метанольным сырьем без или в присутствии побочных продуктов традиционного состава и уровня. Как видно на Фиг.8а и 8b, выход как функция температуры не зависит от смеси высших спиртов, вводимых выше указанного диапазона температуры, где конвертируются все реагенты оксигенатного сырья.
Пример 3 (Сравнительный)
Этот пример не имеет отношения к данному изобретению. Он служит для демонстрации того, что проведение объединенного процесса синтеза оксигенатов, как описано в патенте США US 4,076,761, в котором стадия синтеза оксигенатов представляет собой синтез метанола, содержащего побочные продукты, не приведет к эффектам, необходимым для выполнения задачи настоящего изобретения.
Повторяют методику вышеуказанного эксперимента. Однако раствор чистого метанола заменяют раствором метанола-сырца, полученным при добавлении в него высших спиртов, приведенных в Таблице 3. Полученный смешанный раствор метанола-сырца представляет собой типичный состав, выходящий из известной в данной области установки производства метанола.
Как видно из результатов, приведенных на Фиг.7а, 7b, 8а и 8b, в составе, обозначенном "сырец", степень конверсии метанола, если в нем присутствует стандартная концентрация и распределение высших спиртов, не отличима от степени конверсии чистого метанола.
На основе вышеизложенных результатов эффект снижения температуры показан на Фиг.9а и 9b. Температура, при которой достигают 50% конверсии, является произвольно выбранной для иллюстрации наблюдаемого эффекта снижения температуры реакции при добавлении высших спиртов. Эта температура установлена методом интерполяции данных Фиг.7а и 7b. Температурный эффект реакции при других степенях конверсии может отличаться от таковых, показанных на Фиг.9а и 9b. На Фиг.9а и 9b видно, что рабочая температура может снижаться при очень малых концентрациях вводимых высших спиртов.
Как показывают данные, этот температурный эффект сохраняется и наблюдается при очень малой концентрации вводимых высших спиртов. При содержании высших спиртов С3+, по меньшей мере, 0,05 мас.% в пересчете на общую массу оксигената этот температурный эффект ярко выражен. Максимальный температурный эффект реакции наблюдается при содержании в оксигенатном сырье около 10 мас.% введенных ВС.
Как можно видеть, этот эффект в большей степени воспроизводим при более высокой среднечасовой скорости подачи сырья WHSV. Температура, необходимая для достижения 50% конверсии, выше в случае более высокой среднечасовой скорости подачи сырья WHSV, но эффект, получаемый в результате снижения температуры реакции, сохраняется.
При применении сравнительных Примеров 4, 5 и 6 далее продемонстрировано, что в объединенном процессе синтеза с максимальным эффектом, достигнутым в соответствии с патентом США US 4,076,761, необходимая степень рециркуляции для фиксированного выхода бензина (температура на выходе) существенно выше по сравнению со способом данного изобретения.
В целях получения сопоставимого качества сырого бензинового продукта кратность внутренней и внешней рециркуляций должна оставаться постоянной. Снижение показателя кратности рециркуляции(ий) снижает падение давления в объединенном процессе синтеза и тем самым продолжительность работы и размер рециркуляционного(ых) компрессор(ов) и нагрузку на теплообменники. Это обеспечивает получение экономически более эффективного способа синтеза.
Пример 4 (Сравнительный)
Данный пример представляет собой сравнительный пример, основанный на материальном балансе, который не рассматривается в объеме настоящего изобретения, но служит для сравнения с известными решениями в данной области техники. Этот способ представляет собой объединенный процесс синтеза оксигенатов и бензина, характеризуемый отводом CO2 из внутреннего рециркулирующего потока, в котором оксигенат представляет собой смесь метанола, содержащую обычную мольную концентрацию побочных продуктов, а именно 487 мол. ч./млн этанола, 75 мол. ч./млн 1-пропанола, 32 мол. ч./млн 2-пропанола, 40 мол. ч./млн 1-бутанола и 11 мол. ч./млн 2-бутанола, как показано в Таблице 3.
Питающий газовый поток (100 кмоль/ч), например обычный каменноугольный газ, содержащий 37,48 мол.% Н2, 45,39 мол.% СО, 15,95 мол.% СО2, 0,6 мол.% N2 и 0,58 мол.% содержащих S соединений, при давлении 55 бар направляют реакционную петлю синтеза бензина, показанную на Фиг.3. В целях обеспечения надлежащей утилизации синтез-газа, используемого в качестве исходного сырья, целевая минимальная суммарная глубина конверсии синтез-газа в оксигенаты установлена на уровне 96%, а выход продуктов бензина установлен на уровне 78%.
Присутствие обычной концентрации побочных продуктов в метаноле позволяет обеспечить температуру на входе в реактор 350°С с целью получения стабильной конверсии.
В соответствии с этим был создан способ на основе того, что простое равновесие пар-жидкость-жидкость (VLL) при 40°С обеспечивает отделение непрореагировавшего синтез-газа от бензинового продукта-сырца и воды, образуемой в объединенном процессе синтеза, и применение адиабатического реактора синтеза бензина. В результате были получены минимальный показатель скорости внешнего рецикла, необходимый для удовлетворения технологических целей при одновременном соблюдении эффективности конверсии синтез-газа, предельные значения выхода бензина и температуры бензина в качестве ограничивающих условий.
Найденные минимальные скорости рециркуляции составляли кратность 3,2 подпитки для внешнего рецикла и 3,6 подпитки для внутреннего рецикла.
В нижеследующих примерах показано, что соотношение между внутренним и внешним рециклами оставалось соответственно постоянным (коэффициент внешней/внутренний рециркуляции = 3,2/3,6=0,89) для сравнения сопоставимого качества сырого бензинового продукта, полученного в сепараторе ниже по потоку.
Составы, полученные в различных зонах процесса, указанные численными обозначениями в треугольниках, показанных на Фиг.3, приведены ниже в Таблице 4.
Пример 5 (сравнительный)
Данный пример представляет результаты по материальному балансу в синтезе, который используют не для иллюстрации настоящего изобретения, а в качестве сравнения. Этот способ представляет собой повторение Примера 4, за исключением того, что синтез оксигенатов представляет собой в настоящий момент совместный синтез метанола и диметилового эфира.
Допустимая температура на входе в реактор синтеза бензина не изменяется при изменении состава сырья по сравнению с предыдущим Примером 4.
Составы в позициях на диаграмме, показанной на Фиг.3, перечислены ниже в Таблице 5.
Было найдено, что минимальная величина необходимых рециклов составляет 2,4 для внешнего рецикла (задаваемая по горячей точке катализатора) и 2,7 для внутреннего рецикла.
Эффективность конверсии синтез-газа превосходит эффективность, полученную в Примере 4, а именно 98%. В действительности, величину внешнего рецикла можно было бы уменьшить, что позволяет также улучшить качество сырого бензинового продукта, полученного в сепараторе. Однако сумма отношений между внутренним и внешним рециклами в отношении состава продуктов должна в любом случае оставаться в основном такой же для соответствия температурному диапазону реактора.
Пример 6
Это еще один пример, который иллюстрирует преимущества, полученные в результате применения настоящего изобретения. В синтезе оксигенатов осуществляют совмещенный процесс получения метанола и простого диметилового эфира с последующим проведением совмещенного процесса синтеза метанола и высших спиртов.
Те же целевые показатели по эффективности конверсии и выходу заданы в способе, приведенном в Примере 4 и проиллюстрированном на Фиг.3.
Составы в позициях на диаграмме, показанной на Фиг.3, перечислены ниже в Таблице 6.
Было найдено, что минимальный показатель необходимых рециклов составляет 1,12 для внешнего рецикла и 1,28 для внутреннего рецикла, соблюдая при этом постоянство показателя степени рециркулирования. Эффективность конверсии синтез-газа превосходит эффективность, полученную в Примере 4, а именно 98%.
Минимальный показатель внешнего рецикла, найденный в Примере 6, оказался низким даже при уровне выше нуля в этом конкретном процессе. Возможно было бы предпочтительным размещать реакторы в секции синтеза оксигенатов для того, чтобы полностью предотвратить внешнее рециркулирование, если вводится поправка по критерию эффективности конверсии.
Как ясно продемонстрировано в этом примере, конкретная технологическая схема объединенного синтеза оксигенатов, в результате которой образуются высший спирт, и синтеза бензинового продукта приводит к резкому сокращению скоростей рециркуляции, необходимых для получения надлежащей эффективности конверсии и выходов бензина.
Пример 7
Этот пример иллюстрирует еще один вариант осуществления настоящего изобретения, описанный выше, относящийся, в частности, к синергетическим эффектам, которые достигаются при совместной подаче потока сырого водного биоэтанола на участок синтеза оксигенатов объединенного процесса синтеза бензина.
Те же целевые показатели по эффективности и выходу заданы в способе, приведенном в Примере 4 и проиллюстрированном на Фиг.3.
Составы в позициях на диаграмме, показанной на Фиг.3, перечислены ниже в Таблице 7.
Оказалось, что минимальный показатель необходимых рециклов составляет 1,10 для внешнего рецикла и 1,23 для внутреннего рецикла, соблюдая при этом постоянство показателя степени рециркулирования. Эффективность конверсии синтез-газа превосходит эффективность, полученную в Примере 4, а именно 98%.
Параллельно Примеру 6 минимальный показатель внешнего рецикла, установленный в Примере 7, оказался низким даже при уровне выше нуля в этом конкретном процессе. Возможно было бы предпочтительным размещать реакторы в секции синтеза оксигенатов для того, чтобы полностью предотвратить внешнее рециркулирование, если вводится поправка на критерий эффективности конверсии.
Как продемонстрировано выше, конкретная совместная подача потока, содержащего этанол, на стадию синтеза оксигенатов, производящая совместно высший спирт, в конечном итоге поступающая в реактор синтеза бензина, приводит к дальнейшему снижению скоростей рециркуляции, необходимых для получения требуемой эффективности конверсии синтез-газа и выхода бензина.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ УГЛЕВОДОРОДНЫХ ПРОДУКТОВ | 2010 |
|
RU2524957C2 |
| СПОСОБ ПОЛУЧЕНИЯ УГЛЕВОДОРОДОВ ИЗ СИНТЕЗ-ГАЗА | 2010 |
|
RU2543482C2 |
| КАТАЛИЗАТОР И СПОСОБ ПОЛУЧЕНИЯ ВЫСОКООКТАНОВЫХ БЕНЗИНОВ С НИЗКИМ СОДЕРЖАНИЕМ БЕНЗОЛА И ДУРОЛА | 2010 |
|
RU2440189C1 |
| СПОСОБ ПОЛУЧЕНИЯ УГЛЕВОДОРОДНЫХ ПРОДУКТОВ | 2008 |
|
RU2473665C2 |
| СПОСОБ ПРЕВРАЩЕНИЯ ТРУДНО КОНВЕРТИРУЕМЫХ ОКСИГЕНАТОВ В БЕНЗИН | 2006 |
|
RU2428455C2 |
| ДЕГИДРИРОВАНИЕ СМЕШАННЫХ СПИРТОВ | 2006 |
|
RU2412141C2 |
| КАТАЛИЗАТОР И СПОСОБ СОВМЕСТНОЙ ПЕРЕРАБОТКИ НИЗКООКТАНОВЫХ УГЛЕВОДОРОДНЫХ ФРАКЦИЙ И АЛИФАТИЧЕСКИХ СПИРТОВ И/ИЛИ ДИМЕТИЛОВОГО ЭФИРА | 2010 |
|
RU2429910C1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕНЗИНОВ С РАСПРЕДЕЛЕНИЕМ ПОТОКОВ ОКСИГЕНАТА И ДВУХ ОЛЕФИНСОДЕРЖАЩИХ ФРАКЦИЙ | 2020 |
|
RU2747866C1 |
| СПОСОБ УВЕЛИЧЕНИЯ ВЫХОДА ЖИДКОГО УГЛЕВОДОРОДНОГО ПРОДУКТА | 2020 |
|
RU2747864C1 |
| СПОСОБ УВЕЛИЧЕНИЯ ВЫХОДА ЖИДКОГО УГЛЕВОДОРОДНОГО ПРОДУКТА | 2020 |
|
RU2747931C1 |
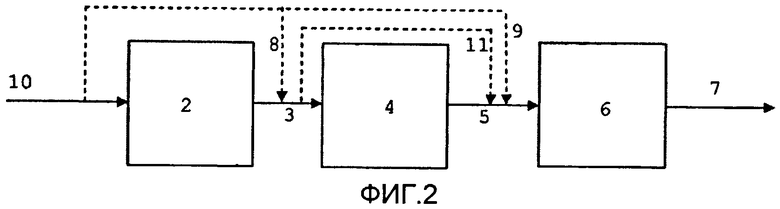
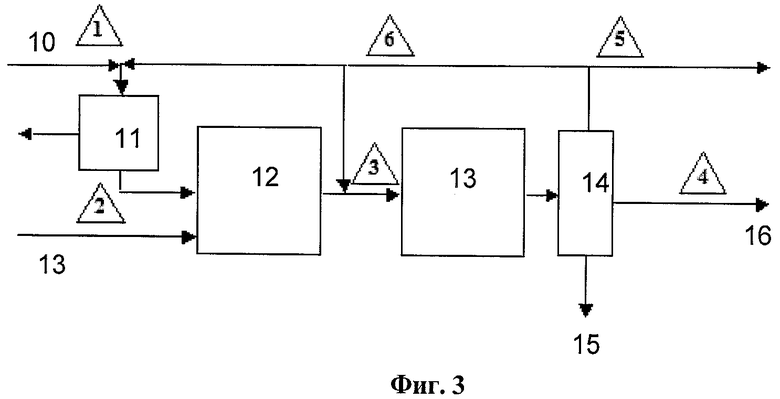
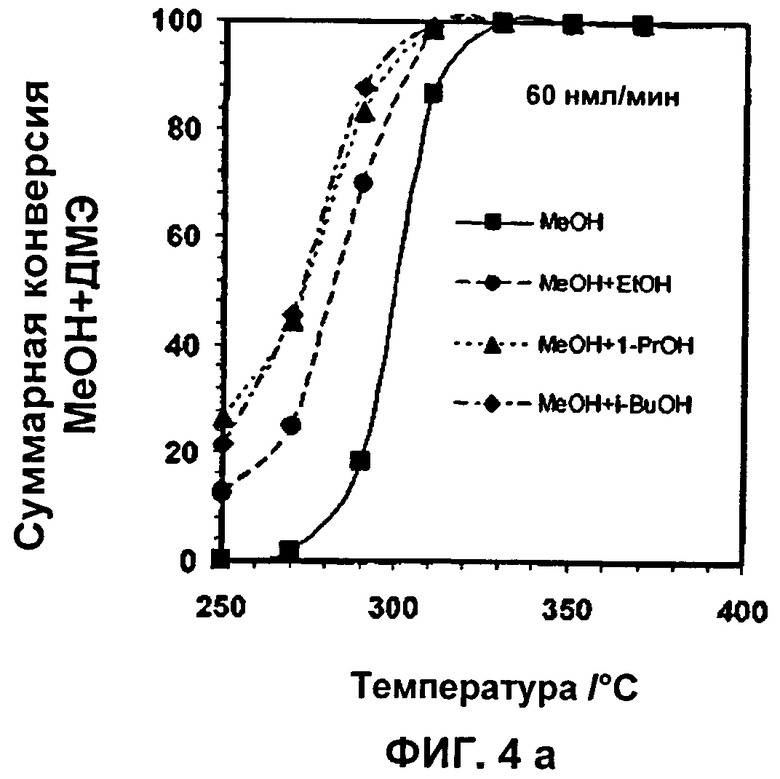
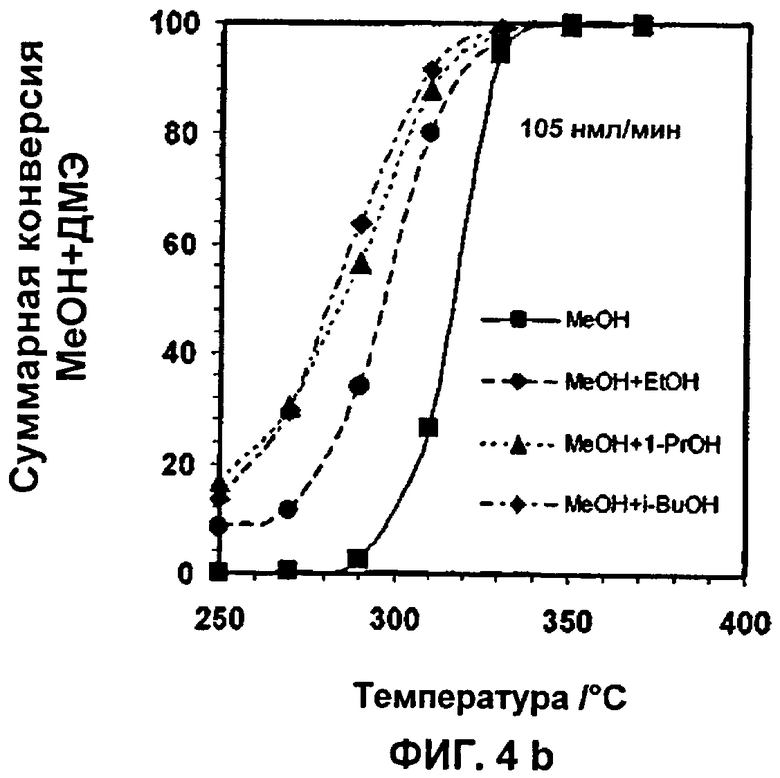
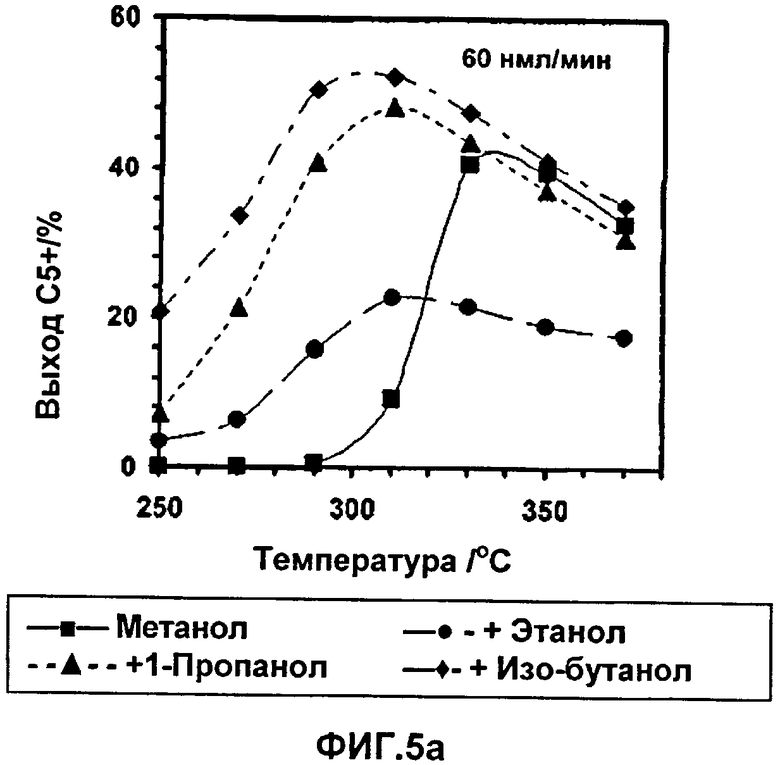
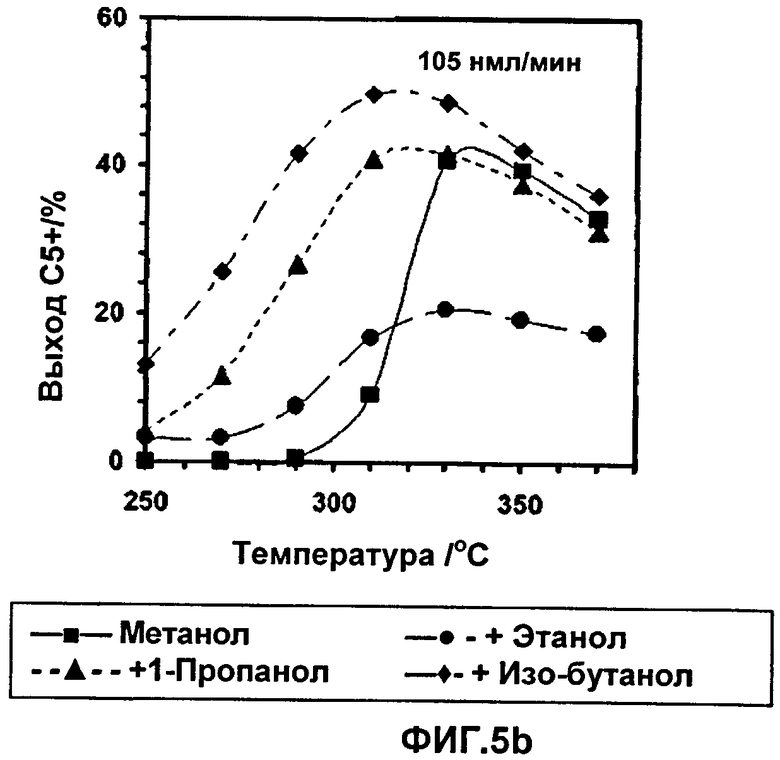
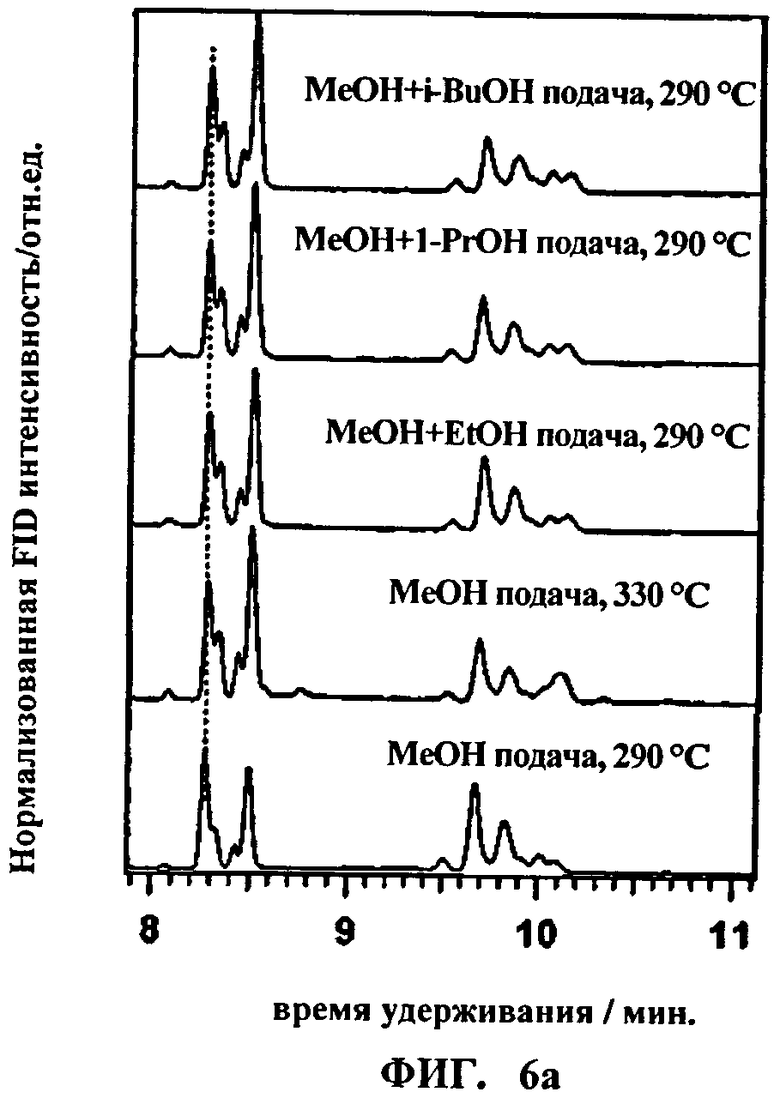

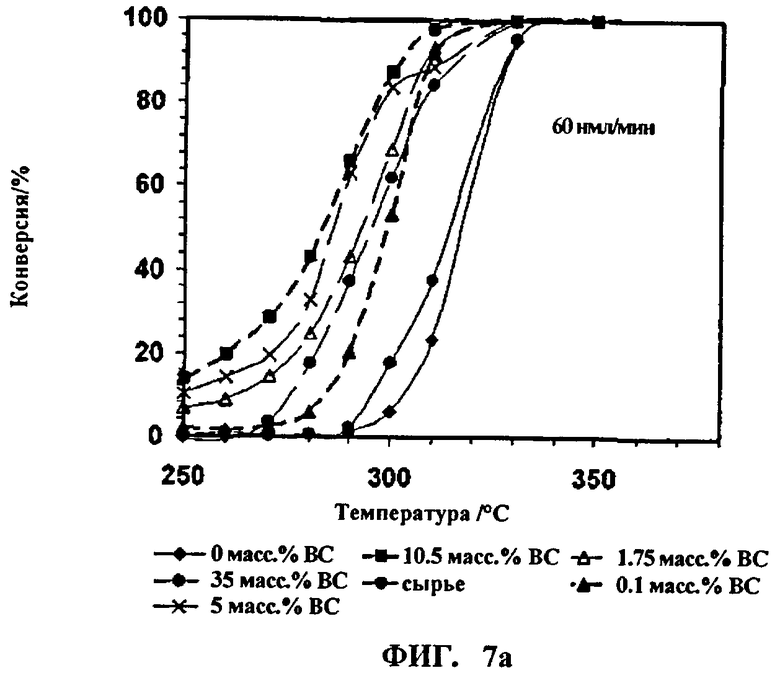
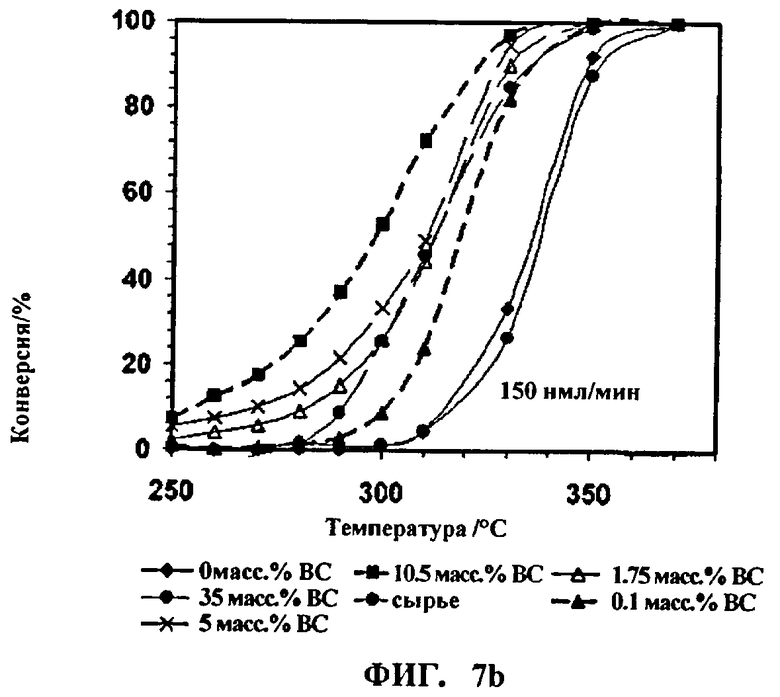
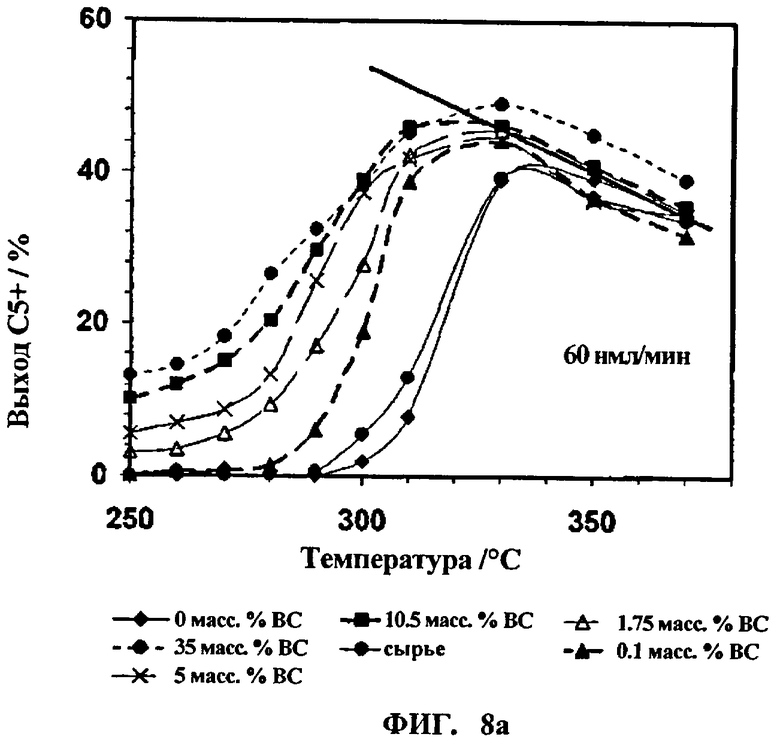
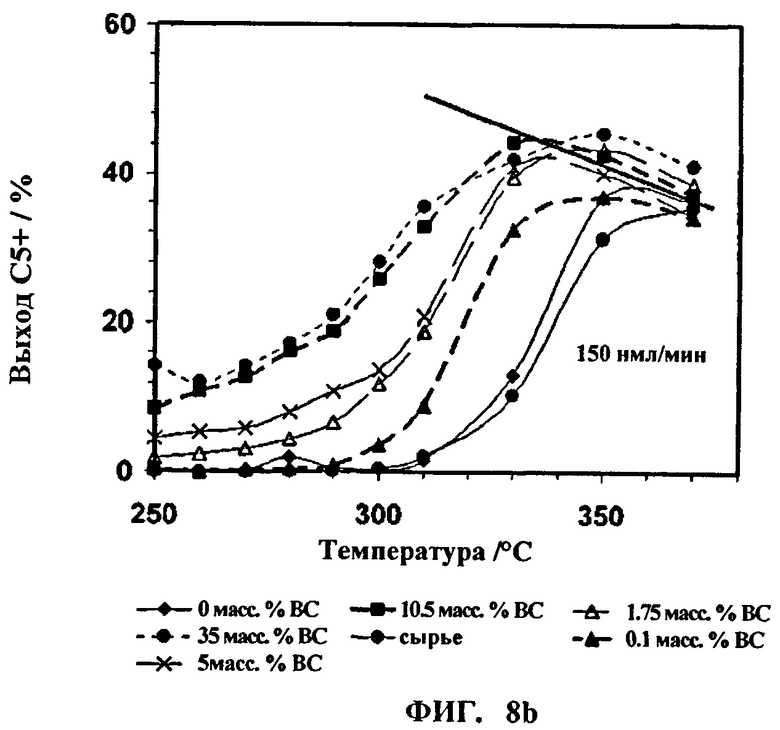
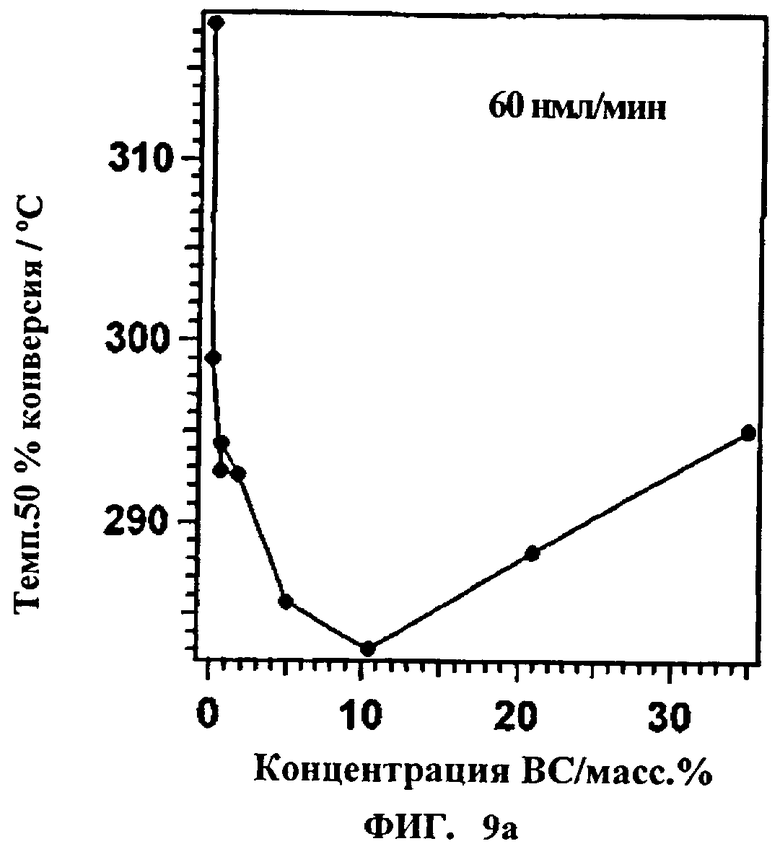
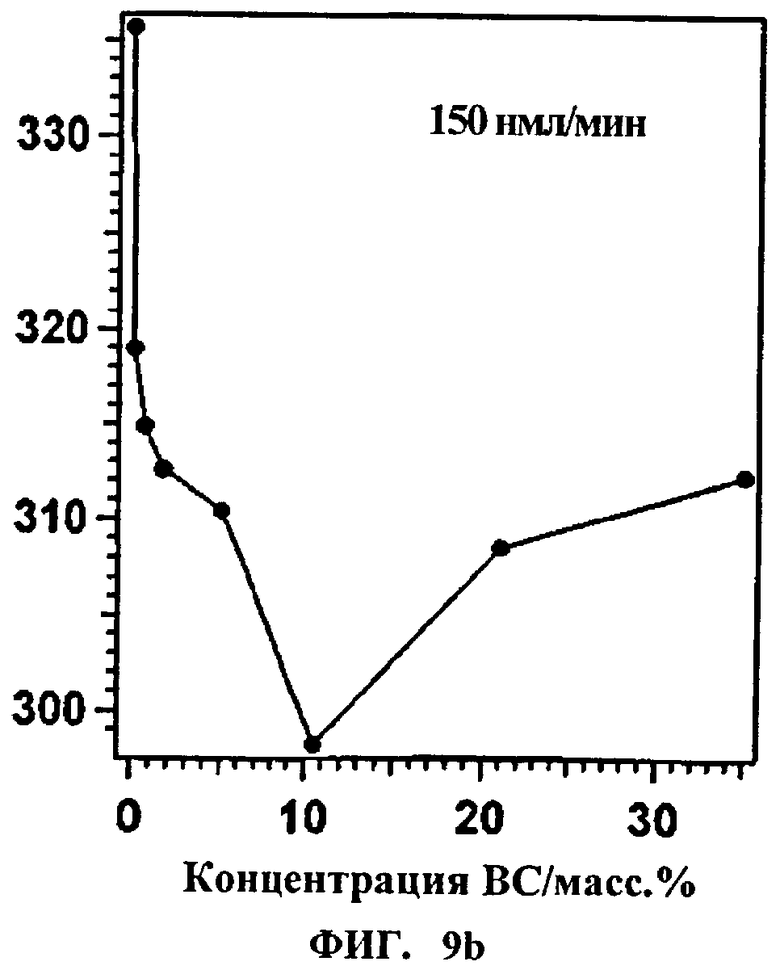
Изобретение относится к синтезу богатой бензиновой фракции из оксигенатов. Изобретение касается способа синтеза углеводородных компонентов бензина, включающего каталитическую конверсию на стадии синтеза бензина оксигенатсодержащего сырья, полученного в результате каталитической конверсии синтез-газа, поданного в одну или несколько стадий синтеза оксигенатов, оксигенатсодержащее сырье содержит метанол и/или простой диметиловый эфир и смесь, содержащую в пересчете на общий оксигенатный состав 0,05-1 мас.% одного или нескольких оксигенатов, выбранных из группы пропанола, бутанола, пентанола, гексанола, простого диметилового эфира и простых эфиров высших спиртов С3+ и/или их оксигенатных эквивалентов, в углеводородные компоненты бензина и, по меньшей мере, на одну из стадий синтеза оксигенатов совместно подают один или несколько оксигенатсодержащих потоков, содержащих метанол, высшие спирты и/или их простые эфиры и дополнительно, при необходимости, содержащих оксигенаты, выбранные из группы альдегидов и кетонов, карбоновых кислот и их сложных алкилэфиров. Изобретение также касается другого способа синтеза углеводородных компонентов бензина. Технический результат - конверсия оксигенатов в ценные углеводородные продукты. 2 н. и 11 з.п. ф-лы, 7 пр., 7 табл., 15 ил.
1. Способ синтеза углеводородных компонентов бензина, включающий каталитическую конверсию на стадии синтеза бензина оксигенатсодержащего сырья, полученного в результате каталитической конверсии синтез-газа, поданного в одну или несколько стадий синтеза оксигенатов, оксигенатсодержащее сырье содержит метанол и/или простой диметиловый эфир и смесь, содержащую в пересчете на общий оксигенатный состав 0,05-1 мас.% одного или нескольких оксигенатов, выбранных из группы пропанола, бутанола, пентанола, гексанола, простого диметилового эфира и простых эфиров высших спиртов С3+ и/или их оксигенатных эквивалентов, в углеводородные компоненты бензина и, по меньшей мере, на одну из стадий синтеза оксигенатов совместно подают один или несколько оксигенатсодержащих потоков, содержащих метанол, высшие спирты и/или их простые эфиры и дополнительно, при необходимости, содержащих оксигенаты, выбранные из группы альдегидов и кетонов, карбоновых кислот и их сложных алкилэфиров.
2. Способ по п.1, в котором, по меньшей мере, один из оксигенатсодержащих потоков содержит этанол и воду.
3. Способ по п.2, в котором, по меньшей мере, один из оксигенатсодержащих потоков содержит сырой водный этанол, полученный из возобновляемого сырья.
4. Способ по любому из пп.2 или 3, в котором оксигенатсодержащее сырье подвергают фазовому разделению на две фракции, в частности богатую оксигенатом жидкую фракцию, содержащую метанол и смесь высших спиртов С3+, и обедненную оксигенатом газовую фракцию, содержащую непрореагировавший синтез-газ, при этом богатую оксигенатом жидкую фракцию затем превращают в углеводородные компоненты бензина.
5. Способ по п.1, в котором катализатор синтеза оксигенатов содержит оксид алюминия, алюмосиликат и/или цеолит, а также содержит Cu и/или ZnO.
6. Способ по п.1, в котором синтез-газ подают на стадию удаления кислого газа перед его конверсией в оксигенатсодержащее сырье.
7. Способ по п.1, в котором основную часть углеводородных компонентов, содержащих составляющие компоненты бензин и воду, разделяют, и равновесный поток, содержащий непрореагировавший синтез-газ, получают на указанной стадии разделения и часть его возвращают рециркуляцией на стадию синтеза оксигенатов и/или стадию синтеза бензина.
8. Способ по п.1, в котором фракцию подаваемого синтез-газа пропускают байпасом, по меньшей мере, в одну или несколько стадий синтеза оксигенатов.
9. Способ по п.5, в котором фракцию подаваемого синтез-газа пропускают байпасом, по меньшей мере, в одну или несколько стадий синтеза оксигенатов.
10. Способ по п.1, в котором воду вводят, по меньшей мере, на одной или нескольких стадиях синтеза оксигенатов.
11. Способ по п.1, в котором поток, содержащий высшие спирты или эквиваленты, подают совместно на стадию синтеза бензина.
12. Способ по п.1, в котором стадию синтеза бензина проводят в реакторе, охлаждаемом кипящей водой.
13. Способ синтеза углеводородных компонентов бензина, включающий каталитическую конверсию на стадии синтеза бензина оксигенатсодержащего сырья, полученного в результате каталитической конверсии синтез-газа, поданного в одну или несколько стадий синтеза оксигенатов, оксигенатсодержащее сырье содержит метанол и/или простой диметиловый эфир и смесь, содержащую в пересчете на общий оксигенатный состав 5-15 мас.% одного или нескольких оксигенатов, выбранных из группы пропанола, бутанола, пентанола, гексанола, простого диметилового эфира и простых эфиров высших спиртов С3+ и/или их оксигенатных эквивалентов, в углеводородные компоненты бензина и, по меньшей мере, на одну из стадий синтеза оксигенатов совместно подают один или несколько оксигенатсодержащих потоков, содержащих метанол, высшие спирты и/или их простые эфиры и дополнительно, при необходимости, содержащих оксигенаты, выбранные из группы альдегидов и кетонов, карбоновых кислот и их сложных алкилэфиров.
| Bernd E | |||
| Langer, Reactions of methanol on zeolites with different pore structures, Applied Catalysis, 2(1982) 289-302 | |||
| Li-Min Tau and Burton H | |||
| Davis, Isotopic tracer studies of the conversion of alcohol mixtures with a high silica ZSM-5 catalyst, Fuel Processing Technology, 33 (1993)1-12 | |||
| Raymond Le Van Мао and Gerald P | |||
| McLaughlin, Conversion of |
Авторы
Даты
2012-04-20—Публикация
2007-11-20—Подача