Область техники, к которой относится изобретение
Настоящее изобретение касается способа превращения этилбензола и способа получения п-ксилола. Более конкретно настоящее изобретение касается способа превращения этилбензола, содержащегося в C8 ароматических углеводородах, гидрированием и деэтилированием и способа получения п-ксилола путем превращения этилбензола, содержащегося в C8 ароматических углеводородах, гидрированием и деэтилированием, и разделения п-ксилола после изомеризации ксилола.
Уровень техники
Среди изомеров ксилола наиболее важным является п-ксилол. В настоящее время п-ксилол применяют в качестве исходного для получения терефталевой кислоты, которая является мономером для сложных эфиров, которые вместе с нейлонами оцениваются как важнейшие полимеры, потребность в которых в последние годы является высокой, особенно в Азии.
Обычно п-ксилол получают из смеси C8 ароматических углеводородов, получаемой реформингом нафты, за которым следует экстракция или дистилляция ароматических углеводородов, или получаемой обработкой крекированного газолина, получаемого термальным разложением нафты в качестве побочного продукта при экстракции или дистилляции ароматических углеводородов. Хотя состав смеси C8 ароматических углеводородов сильно варьируется, обычно она содержит от 10 до 40% этилбензола по весу, от 12 до 25% п-ксилола по весу, от 30 до 50% м-ксилола по весу и от 12 до 25% о-ксилола по весу. Так как смесь C8 ароматических углеводородов обычно содержит высококипящие компоненты, имеющие не менее 9 атомов углерода, высококипящие компоненты удаляют дистилляцией и полученную смесь C8 ароматических углеводородов подвергают стадии разделения п-ксилола для отделения и извлечения п-ксилола. Однако, так как точки кипения п-ксилола и м-ксилола составляют 138,4°C и 139°C соответственно и разница между ними, таким образом, составляет только около 1°C, извлечение п-ксилола дистилляцией не является очень эффективным при промышленном производстве. Таким образом, п-ксилол обычно отделяют кристаллизацией с применением разницы между точками плавления или адсорбционным разделением с применением разницы степени адсорбции на цеолитном адсорбенте. C8 ароматические углеводороды после стадии разделения, которая дает низкий выход п-ксилола, поступают на стадию изомеризации, на которой ксилолы изомеризуются до п-ксилола, обычно, на цеолитном катализаторе в концентрации, близкой к термодинамической равновесной концентрации. После удаления низкокипящих побочных продуктов дистилляцией полученную углеводородную смесь смешивают с вышеописанной свежей смесью C8 ароматических углеводородов и полученную смесь повторно используют на дистилляционной колонне, на которой высококипящие продукты, имеющие не менее 9 атомов углерода, удаляют дистилляцией, за которой следует новое разделение и выделение п-ксилола на стадии разделения п-ксилола. Эта циклическая последовательность в работе цитируется как "цикл разделения-изомеризации".
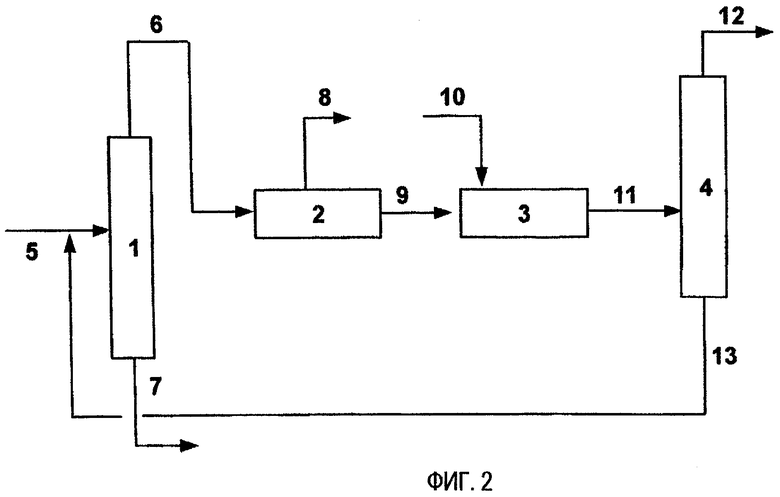
Фиг. 2 показывает схему производственного процесса этого "цикла разделения-изомеризации". Этот "цикл разделения-изомеризации" содержит стадию 1 разделения дистилляцией высококипящих компонентов, на которой извлекаются C8 ароматические углеводороды, которые содержатся в смешанном C8 ароматическом углеводородном сырье (которое цитируется в работе как "свежее сырье"), полученном после установки реформинга и подобного, и в возвратном сырье после стадии изомеризации, и из смеси удаляют высококипящие компоненты; стадию 2 разделения п-ксилола, на которой в качестве конечного продукта выделяют п-ксилол; стадию 3 изомеризации ксилола, на которой проводят изомеризацию ксилолов и конверсию этилбензола в C8 ароматическое углеводородное сырье (которое цитируется в работе как "рафинированный ксилол"), имеющее низкую концентрацию п-ксилола; и стадию 4 дистилляционного разделения низкокипящих компонентов, на которой разделяют и извлекают низкокипящие компоненты, такие как бензол и толуол, которые получают как побочные продукты на стадии изомеризации. Сначала смешанное C8 ароматическое углеводородное сырье подают на стадию 1 дистилляционного разделения высококипящих компонентов по линии питания, обозначенной как поток 5, и высококипящие компоненты удаляют по линии, обозначенной как поток 7. Смесь C8 ароматических углеводородов, из которой были удалены высококипящие компоненты, поступает на стадию 2 разделения п-ксилола по трубопроводу подачи, обозначенному как поток 6, и п-ксилол в качестве конечного продукта отделяют и извлекаю из смеси по трубопроводу, обозначенному как поток 8. Смесь C8 ароматических углеводородов, имеющая низкую концентрацию п-ксилола, поступает на стадию 3 изомеризации ксилола по трубопроводу, обозначенному как поток 9, на которой этилбензол превращают в бензол или ксилол через C8 нафтеновый парафин, как описано ниже, и рафинированный ксилол, имеющий низкую концентрацию п-ксилола, изомеризуют для получения п-ксилола в концентрации, близкой к концентрации термодинамического равновесия. Водород или водородсодержащий газ для стадии изомеризации также подают по трубопроводу, обозначенному как поток 10. C8 ароматические углеводороды со стадии изомеризации, содержащие побочные продукты, подают на стадию 4 дистилляционного разделения низкокипящих продуктов по трубопроводу, обозначенному как поток 11, на которой низкокипящие компоненты, такие как бензол и толуол, которые получают в качестве побочных продуктов на стадии изомеризации, разделяют и удаляют по трубопроводу, обозначенному как поток 12. Обогащенную п-ксилолом рецикловую смесь, содержащую высококипящие компоненты, подают на стадию 1 дистилляционного разделения высококипящих компонентов по трубопроводу, обозначенному как поток 13. На этой стадии 1 дистилляционного разделения высококипящих компонентов высококипящие компоненты удаляют, и полученный продукт опять возвращают на стадию 2 разделения п-ксилола. Существует воплощение, в котором в «цикл разделения-изомеризации» включают одну дистилляционную колонну для одновременного получения o-ксилола.
Как описано выше, C8 ароматическое углеводородное сырье, поступающее в «цикл разделения-изомеризации», содержит значительное количество этилбензола. Однако в вышеописанном «цикле разделения-изомеризации» этилбензол не удаляют и оставляют в цикле, что приводит к накоплению этилбензола. Если этилбензол удаляют каким-либо способом для предотвращения его накопления, этилбензол в количестве, соответствующем степени его удаления, циркулирует в «цикле разделения-изомеризации». Если количество циркулирующего этилбензола уменьшают, общее количество циркулирующего материала также уменьшается так, что снижаются коммуникационные затраты после стадии разделения п-ксилола, что является очень выгодным с экономической точки зрения. Другими словами, когда количества циркулирующих материалов являются равными, может достигаться увеличение выхода п-ксилола в степени, соответствующей уменьшению концентрации этилбензола.
Существует два обычных способа удаления этилбензола. Один представляет собой способ реформинга, в котором этилбензол изомеризуют до ксилола одновременно с изомеризацией ксилола на стадии изомеризации. Другой представляет собой способ деалкилирования, в котором этилбензол переводят в бензол гидрированием и деалкилированием на стадии изомеризации ксилола, и затем бензол отделяют дистилляцией на последующей стадии дистилляционного разделения. Однако степень конверсии этилбензола при применении способа изомеризации составляет от около 20 до 30% максимально из-за равновесия между этилбензолом и ксилолом. В противоположность, поскольку реакция деалкилирования обычно является неравновесной реакцией, степень конверсии этилбензола может быть высокой при применении способа деалкилирования. Следовательно, в настоящее время этилбензол обычно удаляют способом деалкилирования. Однако, даже если система функционирует с высокой степенью конверсии этилбензола на стадии изомеризации и даже если этилбензол удаляют на максимально возможном уровне, количество этилбензола, поступающего на стадию разделения п-ксилола, не может быть уменьшено до уровня ниже, чем первоначальное содержание этилбензола в сырье, поскольку смешанное C8 ароматическое углеводородное сырье, поступающее в «цикл разделения-изомеризации», содержит этилбензол.
Патентные источники 1 и 2 раскрывают способы, в которых количество этилбензола, поступающего в «цикл разделения-изомеризации», снижают предварительным деэтилированием большей части этилбензола, содержащегося в свежем сырье, с образованием бензола в одну стадию и отделением бензола дистилляцией для того, чтобы снизить количество этилбензола, поступающего в «цикл разделения-изомеризации» практически до нуля. Однако в способах, конкретно описанных в работе, необходимо удалить высококипящие компоненты дистилляционным разделением до реакции деалкилирования для того, чтобы снизить концентрацию высококипящих компонентов, имеющих не менее 9 атомов углерода, для предотвращения снижения каталитической активности.
Фиг. 3 показывает схему производственного процесса, показывающую режим применения этих способов. Стадию 15, на которой этилбензол предварительно деэтилируют в одну стадию, стадию 16 дистилляционного разделения, на которой бензол, полученный деэтилированием этилбензола, удаляют дистилляционным разделением, и стадию 14 дистилляционного разделения высококипящих компонентов, на которой снова вводят высококипящие компоненты, изначально содержащиеся в смешанном C8 ароматическом углеводородном сырье. То есть для защиты катализатора, который применяют на стадии деэтилирования, высококипящие компоненты, содержащиеся в смешанном C8 ароматическом углеводородном сырье, вводимом по трубопроводу, обозначенному как поток 5, которые действуют как каталитический яд, отделяют дистилляцией по трубопроводу, обозначенному как поток 18, и дистиллятную фракцию вводят на стадию 15 деэтилирования/изомеризации ксилола по трубопроводу, обозначенному как поток 17. Водород или газ, содержащий водород, также подают на стадию деэтилирования по трубопроводу, обозначенному как поток 19. Смешанное C8 ароматическое углеводородное сырье, в котором этилбензол деэтилировали с высокой степенью конверсии и которое содержит побочные продукты, подают на стадию 16 дистилляционного разделения низкокипящих компонентов по трубопроводу, обозначенному как поток 20. Низкокипящие компоненты, такие как бензол и толуол, которые получаются на стадии деэтилирования, отделяют и удаляют по трубопроводу, обозначенному как поток 21, и высококипящие компоненты подают в вышеописанный «цикл разделения-изомеризации» по трубопроводу, обозначенному как поток 22. Однако, в этом случае, поскольку высококипящие компоненты стадии дистилляционного разделения 14 и низкокипящие компоненты стадии дистилляционного разделения 16 вновь объединяют, коммуникационные затраты повышаются так, что возникает проблема, в которой достоинство введения данных стадий снижается.
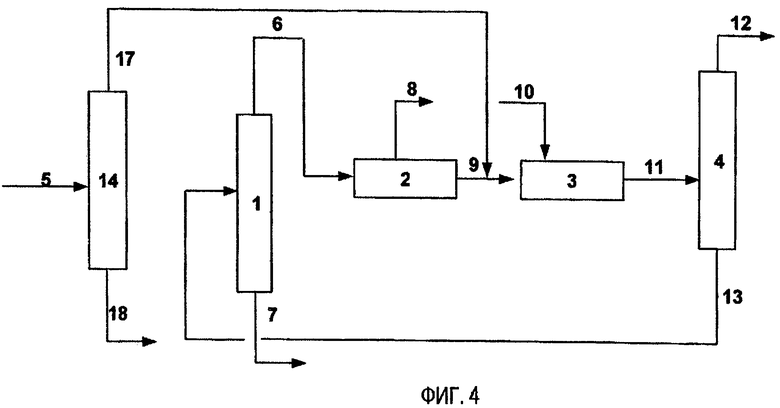
Необходимо сказать, что в вышеописанном режиме затраты на новое строительство с нулевого цикла для стадии деэтилирования также являются необходимыми. Таким образом, в патентном источнике 4 раскрывается способ для получения п-ксилола, в котором на стадии изомеризации ксилола исходного «цикла разделения-изомеризации» вводят катализатор, имеющий способность активно деэтилировать этилбензол, дополнительно к способности изомеризовать ксилол. В этом способе, как показано на Фиг. 4, свежее сырье, обозначено как поток 17, смешивают с рафинированным ксилолом из стадии разделения п-ксилола, обозначенного как поток 9, и смесь напрямую вводят на стадию изомеризации 3 для деэтилирования этилбензола с высокой степенью конверсии, за которой следует удаление низкокипящих компонентов, содержащих бензол на стадии 4 дистилляционного разделения низкокипящих компонентов. После этого рецикловый материал, обозначенный как поток 13, который имеет очень низкую концентрацию этилбензола и п-ксилола, подают на стадию 1 дистилляционного разделения высококипящих компонентов и на стадию 2 разделения п-ксилола. Этот способ называют прямым способом подачи. В соответствии с этим способом может достигаться увеличение выхода п-ксилола с относительно небольшими вложениями в оборудование, поскольку этот способ может реализовываться простой модификацией оборудования, такой как увеличение количества катализатора, применяемого для стадии изомеризации ксилола или заменой катализатора на катализатор, имеющий высокую активность, без самостоятельной организации оборудования для проведения стадии деэтилирования. Однако в патентном источнике 4 описано, что в случаях, когда в свежем топливе содержатся высококипящие компоненты, имеющие не менее 9 атомов углерода, высококипящие компоненты должны предварительно удаляться дистилляционным разделением для предотвращения снижения активности катализатора. Следовательно, даже в этом способе необходимым является проведение стадии 14 дистилляционного отделения высококипящих компонентов для того, чтобы капиталовложения в оборудование и увеличение коммуникационных затрат благодаря введению этой стадии стали очевидными.
В целом, для проведения превращения этилбензола с хорошим выходом поднимают температуру реакции или вводят материал во взаимодействие с катализатором, имеющим высокую активность. Поскольку степень конверсии этилбензола возрастает, происходит снижение выхода ксилола. Потери состоят в основном из (1) потерь при превращении ксилола в толуол в процессе реакции трансалкилирования между бензолом и ксилолом, при этом бензол получается при деэтилировании этилбензола. Другие потери представляют собой (2) потери при превращении ксилола в толуол и триметилбензол в процессе реакции диспропорционирования ксилола и (3) потери при превращении ксилола в неароматические соединения, такие как циклопарафины, н-парафины и изо-парафины в процессе внутриядерного гидрирования ксилола. Далее, поскольку бензол, полученный дистилляционным разделением, загрязнен неароматическими соединениями, которые получаются в процессе реакции внутриядерного гидрирования, дополнительно необходимо проводить экстракционную обработку на установке, такой как сульфолановая установка, что является экономически невыгодным, так как происходит увеличение коммуникационных затрат из-за удорожания обработки на стадии экстракции.
Патентный источник 3 раскрывает применение материала, содержащего C9 и C10 ароматические углеводороды, которые представляют собой высококипящие компоненты, и превращение этилбензола на стадии изомеризации ксилола, но он не раскрывает применение этилтолуола в качестве C9+ ароматического углеводорода и его превращение. Более конкретно в примере патентного источника 3 описывают, что превращение этилбензола проводят с применением сырья, содержащего C9+ ароматические углеводороды в количестве менее чем 0,01% по весу, и что в результате этой реакции получают продукты реакции, содержащие C9+ ароматические углеводороды в количестве 0,1% по весу и 0,2% по весу, соответственно. В соответствии с объяснением в этом литературном источнике по поводу побочных реакций, в которые вовлекаются C9+ ароматические углеводороды, предполагают, что увеличение количества C9+ ароматических углеводородов происходит из-за побочных реакций, таких как образование триметилбензола и диэтилбензола в реакциях диспропорционирования ксилола и этилбензола и образование метилэтилбензола и диметилэтилбензола в реакциях трансалкилирования этилбензола и ксилола. Патентный источник 3 также раскрывает в качестве дополнительного случая способ, в котором специально прибавляют толуол с целью снижения потерь ксилола в реакции диспропорционирования между ксилолами. Однако поскольку специально прибавляемый толуол представляет собой ценное и важное сырье для разнообразного применения, то есть применяется в качестве основы газолина с высоким октановым числом, в качестве растворителя, в качестве исходного для стадии диспропорционирования и так далее, толуол является нежелательным компонентом для прибавления в материал, если вообще возможным, если существует другой способ снижения потерь ксилола.
Патентный источник 1: JP-A-1-56626
Патентный источник 2: US-B-6342649
Патентный источник 3: US-B-5977429
Патентный источник 4: JP-A-8-143483.
Сущность изобретения
Задачи изобретения
Задачей настоящего изобретения является обеспечение способа превращения этилбензола, при котором этилбензол в материале, содержащем C8 ароматические углеводороды, превращают в бензол с высокой степенью конверсии.
Другой задачей настоящего изобретения является обеспечение экономически выгодного способа, в котором степень конверсии этилбензола является высокой и потери ксилола являются низкими, когда этилбензол в материале, содержащем C8 ароматические углеводороды, превращают в бензол и одновременно проводят изомеризацию ксилола.
Еще одной задачей изобретения является обеспечение способа извлечения бензола с высокой чистотой из реакционного продукта после реакции превращения этилбензола в материал, содержащий C8 ароматические углеводороды, и изомеризации ксилола.
Способы решения поставленных задач
После интенсивного изучения изобретатели нашли, что вышеуказанные задачи могут решаться путем создания сырья, содержащего этилтолуол, и введением этого сырья во взаимодействие с сильнокислым катализатором, высокоустойчивым к каталитическим ядам, в присутствии H2, и таким образом решить задачи настоящего изобретения.
То есть настоящее изобретение состоит из:
(1) Способа превращения этилбензола, содержащего стадию взаимодействия смешанного C8 ароматического углеводородного сырья, содержащего этилбензол, с катализатором(ами) кислотного типа, содержащим, по меньшей мере, один металл, выбранный из группы, состоящей из металлов группы VII и VIII, в присутствии H2 для превращения этилбензола в бензол; в случае C9-C10 ароматического углеводородного сырья, включающего этилтолуол, этилтолуол будет превращаться в толуол при превращении этилбензола.
(2) Способа по п. (1), также содержащего дистилляционное отделение бензола, полученного этой реакцией, и извлечение бензола с чистотой не менее 99,8% по весу.
(3) Способа получения п-ксилола, содержащего стадии: обработки смешанного C8 ароматического углеводородного сырья, содержащего этилбензол и ксилол, по пп. (1) или (2) для изомеризации ксилола вместе с превращением этилбензола в бензол; и
отделения п-ксилола от полученного продукта реакции.
(4) Способ получения п-ксилола, содержащий:
первоначальную стадию деэтилирования/изомеризации ксилола путем взаимодействия смешанного C8 ароматического углеводородного сырья по п. (3) для изомеризации ксилола вместе с превращением этилбензола в бензол;
стадию отделения п-ксилола от продукта реакции, полученного на первоначальной стадии деэтилирования/изомеризации ксилола;
стадию изомеризации ксилола, содержащегося в остатке после разделения на второй стадии изомеризации ксилола; и
повторное отделение п-ксилола от продукта реакции второй стадии изомеризации ксилола.
(5) Способ получения п-ксилола, содержащий:
стадию деэтилирования/изомеризации ксилола - взаимодействия смешанного C8 ароматического углеводородного сырья, содержащего этилбензол и ксилол по п. (3), для изомеризации ксилола вместе с превращением этилбензола в бензол;
стадию отделения п-ксилола от реакционного продукта, полученного на стадии деэтилирования/изомеризации п-ксилола; и
стадию повторного применения остатка после отделения, полученного на стадии отделения, и применение остатка на стадии деэтилирования/изомеризации ксилола.
(6) Способ получения п-ксилола с применением оборудования для получения п-ксилола для проведения первой стадии деэтилирования/изомеризации ксилола, стадии отделения п-ксилола и второй стадии изомеризации ксилола по п. (4), в котором оборудование содержит обводной трубопровод, который не проходит через первую стадию деэтилирования/изомеризации ксилола и где смешанное C8 ароматическое углеводородное сырье смешивают с C9-C10 ароматическими углеводородами, содержащими этилтолуол, и это сырье применяют для стадии разделения п-ксилола, как требуется.
Влияние изобретения
В соответствии с настоящим изобретением потери ксилола могут быть уменьшены, и этилбензол может быть гидрирован и деэтилирован, и превращен в бензол с высоким выходом проведения превращения этилбензола в бензол с одновременной изомеризацией ксилола на стадии изомеризации, где содержащий C9, C10 ароматические углеводороды этилтолуол смешивают со смешанным C8 ароматическим углеводородным сырьем, содержащим этилбензол, и где полученное сырье взаимодействует с катализатором(ами) кислотного типа, содержащим, по меньшей мере, один металл, выбранный из группы, состоящей из металлов, принадлежащих группе VII и VIII, в присутствии H2. Кроме этого этилтолуол в сырье превращают в полезный толуол посредством реакции деэтилирования, и толуол может быть извлечен в качестве конечного побочного продукта.
Кроме этого по настоящему изобретению из реакционного продукта, полученного превращением этилбензола в сырье, содержащее С8 ароматические углеводороды, может быть выделен бензол с высокой степенью чистоты. На основании этого бензол может быть получен в качестве конечного продукта после извлечения без стадии экстрагирования.
Краткое описание чертежей
Фиг. 1 представляет схему концептуального представления, показывающую направление потоков, когда обводной трубопровод не проходит через первую стадию деэтилирования/изомеризации ксилола, в оборудовании для получения п-ксилола для проведения первой стадии деэтилирования/изомеризации п-ксилола, стадии разделения п-ксилола и второй стадии изомеризации п-ксилола.
Фиг. 2 представляет схему концептуального представления, показывающую направление потока "цикла разделения-изомеризации" для обычного получения п-ксилола, в который не включена стадия деэтилирования.
Фиг. 3 представляет схему концептуального представления, показывающую направление потока "цикла разделения-изомеризации" для обычного получения п-ксилола, в который включена стадия деэтилирования.
Фиг. 4 представляет схему концептуального представления, показывающую направление потока при прямом способе подачи, в который не включена стадия деэтилирования, свежее сырье смешивают с рафинированным ксилолом и полученный смешанный материал подают на стадию изомеризации ксилола, на которой происходит высокоэффективное деэтилирование этилбензола.
Лучшие варианты воплощения изобретения
Настоящее изобретение характеризуется тем, что при проведении реакции деэтилирования этилбензола смешанное C8 ароматическое углеводородное сырье, содержащее этилбензол, которое подается, содержит этилтолуол. Обычно этилтолуол содержится в высококипящих компонентах сырья, содержащего C8 ароматические углеводороды, которое подают в качестве сырья для цикла "разделения-изомеризации", в количестве от 5 до 15% по весу. Следовательно, при применении стадии деэтилирования дистилляционная колонна для дистилляционного разделения высококипящих компонентов может быть исключена. Фиг. 1 показывает предпочтительный режим потока для проведения настоящего изобретения, и стадия 14 дистилляционного разделения высококипящих компонентов, показанная на фиг. 3 и 4, показывающая направление потока в существующем уровне техники, может быть исключена.
То есть в соответствии с настоящим изобретением при проведении реакции деэтилирования этилбензола в сырье, которое подают на стадию деэтилирования, одновременно протекает реакция деэтилирования этилтолуола, содержащегося в подаваемом сырье, содержащем C9 и C10 ароматические углеводороды, которая превращает его в толуол, таким образом этилтолуол может применяться для получения толуола. Таким образом, в отличие от существующего уровня техники, представленного патентным источником 3, дополнительное прибавление полезного толуола, который имеет многочисленные применения, не является необходимым. Кроме этого, так как реакция диспропорционирования ксилола и реакция трансалкилирования между бензолом, получаемым при деэтилировании этилбензола, и ксилолом, которые являются причиной вышеописанных потерь ксилола, являются равновесными реакциями, влияние этих побочных реакций снижается при наличии толуола, получаемого при деэтилировании этилтолуола, таким образом снижаются потери ксилола.
Катализатор, который применяют в способе по настоящему изобретению, представляет собой катализатор кислотного типа, полученный пропиткой твердой кислоты установленным металлом(ами), описанным ниже. В качестве твердой кислоты могут выступать цеолиты кислотного типа. Среди цеолитов кислотного типа, которые могут применяться в настоящем изобретении, находятся пентасильные цеолиты, такие как пентасил (MFI типа) цеолит, имеющий поры 10-членного кислородного кольца (например, смотри пример 1 на страницах 4-5 патента JP-B-60-35284 и пример 1 на странице 7 патента JP-B-46-10064). Что касается цеолитов, могут применяться как природные цеолиты, так и синтетические цеолиты, и синтетические цеолиты являются предпочтительными. Такой пентасильный цеолит сам по себе, так же как способ его получения являются хорошо известными, и пример синтетического способа конкретно описан в примерах ниже. Каталитическая производительность цеолитов сильно варьируется в зависимости от композиции, особенно от молярного соотношения оксидов кремния/алюминия (молярного соотношения SiO2/Al2O3) и от размера их кристаллов, даже когда структура цеолита является аналогичной.
Предпочтительный интервал молярного соотношения оксидов кремния/алюминия цеолитов также варьируется в зависимости от структуры цеолита. Например, в случае синтетического пентасильного цеолита предпочтительное молярное соотношение оксидов кремния/алюминия составляет от 10 до 70, более предпочтительно от 20 до 55. Это молярное соотношение может достигаться контролем соотношения компонентов при получении цеолита. Кроме этого молярное соотношение оксидов кремния/алюминия может быть увеличено удалением алюминиевой составляющей цеолитной структуры с помощью водного раствора кислоты, такой как хлороводородная кислота, или хелатирующим алюминий агентом, таким как этилендиаминтетрауксусная кислота (ЕДТА). Наоборот, обработкой цеолита водным раствором нитрата алюминия, водным раствором алюмината натрия или подобными алюминий может вводиться в структуру цеолита для снижения молярного соотношения оксидов кремния/алюминия, для достижения предпочтительного соотношения оксидов кремния/алюминия. Соотношение оксидов кремния/алюминия легко определяют атомно-абсорбционной спектрометрией, способом дифракции флуоресцентных рентгеновских лучей, ICP (спектрометрией индуктивно-связанной плазмы) и подобными.
Поскольку синтетические цеолиты обычно представляют собой порошок, предпочтительным является сформовать цеолит. Примеры способов формования включают способ компрессионного формования, вальцевого формования и способ экструзии. Среди этих способов формования способ экструзии является предпочтительным. В способе экструзии связывающее вещество(а), такое как золь оксида алюминия, гель оксида алюминия, бентонит и/или каолин, также как и поверхностно-активное вещество(а), такие как додецилбензолсульфонат натрия, Спан (торговая марка) и/или Твин (торговая марка), прибавляют по требованию в качестве вспомогательных веществ и замешиваются с порошком.
По требованию применяют устройство, такое как мешалка. Кроме этого в зависимости от металла(ов), который прибавляют к катализатору, при формовании к цеолиту прибавляют оксид(ы) металла, такой как оксид алюминия, титана и/или подобные для увеличения количества металла(ов), присутствующих в катализаторе и/или для повышения дисперсии. Замешанный продукт экструдируют через экран. В промышленности применяют экструдер. Замешанный продукт, экструдированный через экран, имеет форму лапши. Размер формованного продукта определяется размером пор экрана. Предпочтительно применять экран с диаметром пор от 0,2 до 1,5 мм. Сформованный продукт в форме лапши, экструдированный через экран, предпочтительно обрабатывают Марумелизером (торговая марка) для закругления концов. Приготовленный таким образом формованный продукт предпочтительно высушивают при температуре от 50 до 250°C. После высушивания формованный продукт предпочтительно обжигают при температуре от 250 до 600°C, более предпочтительно от 350 до 600°C.
Приготовленный таким образом формованный продукт затем подвергают ионообменной обработке для придания кислотности. Примеры способов придания кислотности включают способ, в котором формованный продукт подвергают ионообменной обработке с соединениями, содержащими ион аммония (например, NH4Cl, NH4NO3, (NH4)2SO4 и подобные), для введения ионов NH4 в ионообменные узлы цеолита, и затем ионы NH4 обменивают на ионы водорода высушиванием и запеканием цеолита; и способ, в котором ионы водорода напрямую вводят в ионообменные узлы цеолита обработкой цеолита соединением(ями), содержащим кислоту (например, HCl, HNO3, H3PO4 и подобные). Поскольку последний способ может разрушить структуру цеолита, предпочтительным является предыдущий способ, то есть предпочтительной является обработка соединением(ями), содержащим ион аммония. В качестве альтернативы твердая кислотность может вводиться путем введения двухвалентных и/или трехвалентных ионов металлов в ионообменные узлы цеолита. Примеры двухвалентных ионов металлов включают: Mg2+, Ca2+, Sr2+ и Ba2+. Примеры трехвалентных ионов металлов включают ионы редкоземельных металлов, таких как Ce3+, La3+ и подобные. Способ, в котором вводят ионы двухвалентных и/или трехвалентных металлов, и способ, в котором вводят ионы аммония или напрямую вводят ионы водорода, могут применяться в комбинации, и эта комбинация может быть более предпочтительной в некоторых случаях. Ионообменную обработку проводят способом серийного изготовления или поточным способом, в котором носитель, такой как цеолит, обрабатывают раствором, содержащим ионы, обычно водным раствором. Температура обработки варьируется от комнатной температуры до 100°C.
После ионообменной обработки наносят, по меньшей мере, один металл, выбранный из металлов группы VII и VIII. Присутствие H2 в каталитической реакционной системе и присутствие в катализаторе активного относительно гидрирования металла(ов), может предотвращать изнашивание катализатора в процессе времени. Предпочтительные примеры активных по отношению к гидрированию металлов включают: платину, палладий, рений и подобные. Предпочтительное количество наносимого металла варьируется в зависимости от металла. Например, в случае платины предпочтительные количества составляют от 0,005 до 0,5% по весу, более предпочтительные от 0,01 до 0,3% по весу. В случае палладия предпочтительные количества составляют от 0,05 до 1% по весу. В случае рения предпочтительные количества составляют от 0,01 до 5,0% по весу, более предпочтительные от 0,1 до 2% по весу. Большое количество наносимого гидрирующего металла не является предпочтительным, поскольку ароматические углеводороды гидрируются в ядро. С другой стороны, если количество наносимого гидрирующего металла является слишком маленьким, подача водорода в реакцию деэтилирования является недостаточной, что приводит к изнашиванию катализатора. Таким образом, тип выбираемого металла(ов) и их комбинаций, а также количество металла(ов) должно регулироваться соответствующим образом в зависимости от целевой характеристики. Способ нанесения металла(ов) содержит погружение катализатора в раствор, обычно водный раствор, содержащий по меньшей мере один из (металлов): платины, палладия и рения. В качестве соединения(ий), содержащего компонент платины, могут применяться: хлорплатиновая кислота, хлорплатинат аммония и/или подобные. В качестве соединения, содержащего компонент палладия, могут применяться: ацетат палладия, ацетилацетонат палладия, хлорид палладия, нитрат палладия и/или подобные. В качестве соединения(ий), содержащего компонент рения, могут применяться: перрениевая кислота, перренат аммония и/или подобные.
Приготовленный таким образом катализатор перед применением предпочтительно высушивают при температуре от 50 до 250°C в течение не менее 30 минут и предпочтительно обжигают при температуре от 350 до 600°C в течение не менее 30 минут.
В качестве катализатора может применяться индивидуально один тип катализатора или два или более типов катализаторов могут применяться в комбинации.
Каталитическая реакция с применением катализатора, полученного как описано выше, может проводиться различными способами, которые сами по себе являются хорошо известными в уровне техники. Реакцию можно проводить с помощью одного из способов: способом с фиксированным слоем (катализатора), способом с подвижным слоем (катализатора) и способом с псевдоожиженным слоем (катализатора). Среди этих способов особенно предпочтительным является способ с фиксированным слоем из-за легкости проведения. В этих реакционных способах катализатор может применяться в следующих реакционных условиях: температура реакции от 200 до 500°C, предпочтительно от 250 до 450°C; давление реакции от атмосферного до 10 МПа, предпочтительно от 0,3 до 2 МПа; среднечасовая скорость подачи сырья (WHSV), которая выражает время контакта, составляет от 0,1 до 50 ч-1, предпочтительно от 0,5 до 20,0 ч-1. Реакцию проводят в присутствии H2, и молярное соотношение H2 к сырью составляет от 0,5 до 10 моль/моль, предпочтительно от 1,5 до 5,0 моль/моль. Водород H2, который должен присутствовать в реакционной системе, вводят в реакционную систему в виде газообразного водорода. Сырье может быть либо в жидком, либо в газообразном (агрегатном) состоянии.
Этилтолуол, который должен содержаться в сырье, может быть любым из п-этилтолуола, м-этилтолуола и о-этилтолуола или может быть смесью изомеров. Общее количество этих этилтолуолов, содержащихся в сырье, предпочтительно составляет не менее 1% по весу, более предпочтительно не менее 3% по весу, еще более предпочтительно не менее 5% по весу. Что касается верхней границы, обычно предпочтительным является количество не более 20% по весу, более предпочтительно не более 15% по весу. Как упоминалось выше, поскольку C8 ароматические углеводороды, полученные реформингом или фракционной дистилляцией нафты, содержат этилтолуол, этот этилтолуол может применяться сам по себе. Следовательно, установка дистилляционной колонны для удаления высококипящих компонентов, которая является необходимой в традиционном способе, может быть исключена.
Этилтолуол, который должен содержаться в сырье, может быть введен прибавлением этилтолуола к сырью. В случаях, когда этилтолуол прибавляют к сырью, этилтолуол может прибавляться к сырьевому материалу индивидуально или в виде смеси этилтолуола и других C9-C10 ароматических углеводородов.
В соответствии со способом по настоящему изобретению, в котором применяют вышеописанный катализатор кислого типа, поскольку этилтолуол, содержащийся в сырье, может быть деэтилирован со степенью конверсии не менее 50% по весу, в более предпочтительном воплощении не менее 70% по весу и в особенно предпочтительном воплощении не менее 80% по весу, может быть получено большое количество толуола, полезного для снижения потерь ксилола, даже в случае применения сырья, имеющего низкую концентрацию этилтолуола.
Кроме этого бензол, получаемый в качестве побочного продукта в реакции деалкилирования этилбензола, обычно отделяют дистилляционным разделением, таким как сульфолановая стадия. Однако в случаях, когда применяют вышеописанный катализатор кислого типа, поскольку образование неароматических компонентов, таких как циклогексан, метилциклопентан, н-гексан и подобных, которые имеют точки кипения, относительно близкие к точке кипения бензола, и, соответственно, являются трудноотделимыми способом дистилляционного разделения, является низким, бензол с высокой чистотой может быть получен дистилляционным разделением с исключением экстракции.
Равенство для подсчета чистоты бензола в качестве конечного продукта, отделяемого от образовавшейся жидкой смеси продукта реакции дистилляцией, описано, например, в патенте JP-A-2002-504946 и описано ниже. В настоящем изобретении термин "чистота бензола" обозначает чистоту бензола, рассчитанную с помощью этого равенства для расчета чистоты бензола в качестве конечного продукта.
Рассчитанная чистота конечного продукта бензола = ([концентрация бензола]/a+b+c+d+[концентрация бензола]) * 100(%)), где a-d представляют собой следующие величины:
a=0,1 * [концентрация н-C6 парафина]
b=0,7 * [концентрация метилциклопентана]
c=1,0 * [концентрация циклогексана]
d=1,0 * [концентрация C7 нафтенового парафина]
В случаях, когда в качестве металла, содержащегося в катализаторе кислого типа, применяют рений, так как его гидрирующая способность является относительно мягкой, и, таким образом, потери ароматических соединений из-за разложения при ядерном гидрировании являются небольшими, образование вышеописанных примесей, имеющих точки кипения, относительно близкие к точке кипения бензола, является относительно низким. В результате подсчитанная чистота конечного продукта бензола составляет не менее 99,8% по весу. Таким образом, бензол получают в качестве продукта химической градации дистилляционным разделением без дальнейшей очистки, такой как стадия экстракции. С другой стороны, толуол, получаемый в реакции деалкилирования этилтолуола, извлекают дистилляцией, и он может применяться как основа для газолина, растворитель или сырье для получения бензола реакцией диспропорционирования.
В соответствии с настоящим изобретением не только этилбензол превращают в бензол применением вышеописанного способа превращения этилбензола с применением смешанного C8 ароматического углеводородного сырья, содержащего этилбензол и ксилол, но ксилол также могут изомеризовать (стадия превращения этилбензола в бензол и изомеризации ксилола цитируется как "стадия деэтилирования/изомеризации ксилола" или "первая стадия деэтилирования/изомеризации ксилола". При этом может быть получен не только продукт реакции, в котором степень конверсии этилбензола является высокой, но и потери ксилола также являются низкими. П-ксилол может быть получен отделением п-ксилола от этого продукта реакции. Отделение п-ксилола от продукта реакции может проводиться способами, которые сами по себе являются хорошо известными, например, криогенным разделением или адсорбционным разделением, применяющим разницу в степени адсорбции на цеолитном адсорбенте.
Кроме этого в настоящем изобретении рафинированный ксилол, который представляет собой остаток после вышеописанного разделения п-ксилола, который имеет низкую концентрацию п-ксилола, может быть подвергнут изомеризации ксилола на второй стадии изомеризации ксилола. Способ изомеризации, вводимый на этой второй стадии изомеризации ксилола, не ограничивается, и изомеризация ксилола может проводиться с помощью традиционного способа или может проводиться стадия, аналогичная вышеописанной стадии "деэтилирования/изомеризации ксилола". Из продукта реакции, полученного на этой второй стадии изомеризации ксилола, опять может быть выделен п-ксилол. Второй остаток после разделения п-ксилола может быть повторно использован смешиванием со смешанным C8 ароматическим углеводородным сырьем или может быть повторно использован введением его на вторую стадию изомеризации ксилола вместе с первым остатком после разделения, тем самым образуя "цикл разделения/изомеризации".
Кроме этого по настоящему изобретению п-ксилол может быть получен введением стадии деэтилирования/изомеризации ксилола, на которой превращают этилбензол и изомеризуют ксилол с применением смешанного C8 ароматического углеводородного сырья, содержащего этилбензол и ксилол; эта стадия деэтилирования/изомеризации ксилола аналогична вышеописанной первой стадии деэтилирования/изомеризации ксилола, отделением п-ксилола от полученного продукта реакции и повторного применения остатка после разделения введением остатка на вышеуказанную стадию деэтилирования/изомеризации ксилола. Этот способ также может применяться в вышеуказанном способе с прямой подачей. То есть п-ксилол могут разделять снова смешиванием со смешанным C8 ароматическим углеводородным сырьем, содержащим этилтолуол, полученный при исключении дистилляционного отделения высококипящих компонентов, с рафинированным ксилолом после разделения п-ксилола, подачей смеси на стадию изомеризации ксилола, на которой вводят вышеописанный катализатор кислого типа для деэтилирования этилбензола и изомеризации ксилола, и повторным отделением п-ксилола от полученного продукта реакции. То есть в случаях, когда на стадии изомеризации вводят вышеуказанный катализатор кислого типа, стадия 14 разделения высококипящих компонентов может отменяться на фиг. 4, показывающей схему концептуального представления обычного способа прямой подачи.
В случаях, когда проводят вышеуказанную первую стадию деэтилирования/изомеризации ксилола, стадию разделения п-ксилола и вторую стадию изомеризации ксилола, и в случаях, когда к этому прибавляют "цикл разделения/изомеризации", при включении этих стадий предпочтительным является обеспечение обводного трубопровода в оборудовании для получения п-ксилола, такого как обводной трубопровод 23 на стадии деэтилирования/xизомеризации ксилола, как показано на фиг. 1.
Это необходимо, поскольку даже в случае остановки стадии деэтилирования для периодического технического обслуживания или при аварийном выключении, нет необходимости останавливать весь последовательный "цикл разделения-изомеризации" путем изменения пути доставки смешанного C8 ароматического углеводородного сырья на подачу по обводному трубопроводу, таким образом снижение производства п-ксилола может быть уменьшено насколько это возможно. Кроме этого в случаях, когда вышеописанную стадию деэтилирования/изомеризации ксилола применяют как стадию изомеризации ксилола, поскольку одновременно происходит конверсия этилбензола, содержащегося в смешанном C8 ароматическом углеводородном сырье, этилбензол может превращаться с высокой степенью конверсии, несмотря на тот факт, что первая стадия деэтилирования/изомеризации ксилола исключается, и кроме этого, поскольку потери ксилола являются низкими, и может проводиться изомеризация ксилола, влияние исключения первой стадии деэтилирования/изомеризации ксилола может быть снижено насколько это возможно.
Примеры
1. Получение пентасильного цеолита
В 698,6 г воды растворяют 54,2 г водного раствора гидроксида натрия (содержание NaOH: 48,0% по весу, содержание H2O: 52,0% по весу, Toagosei Co., Ltd.) и 16,6 г порошкообразной винной кислоты (содержание винной кислоты: 99,7% по весу, содержание H2O: 0,3% по весу, CaHC Co., Ltd.). К этому раствору прибавляют 9,9 г раствора алюмината натрия (содержание Al2O3: 13,4% по весу, содержание Na20: 13,8% по весу, содержание H2O 43,9% по весу Sumitomo Chemical Co., Ltd.) и смесь перемешивают до образования гомогенного раствора. К этому смешанному раствору медленно прибавляют 111,5 г гидратированной кремниевой кислоты (содержание SiО2: 89,4% по весу, содержание Al2O3: 2,4% по весу, содержание Na20: 1,6% по весу, Нипсил VN-3, Nihon Silica Co., Ltd.) при перемешивании для приготовления водной реакционной смеси в форме гомогенной суспензии. Композиционное соотношение (молярное соотношение) этой реакционной смеси следующее:
SiO2/Al2O3: 77
OH-/SiO2: 0,3002
A/Al2O3: 5,14 (A: соль винной кислоты)
H2O/SiO2: 25.
Реакционную смесь помещают в 1000 мл автоклав, автоклав герметически закрывают и проводят реакцию при 160°C в течение 72 часов при перемешивании со скоростью 250 об/мин. После окончания реакции реакционную смесь промывают дистиллированной водой, проводят последовательное фильтрование 5 раз; полученный продукт высушивают в течение ночи при около 120°C.
Анализ полученного продукта проводят рентгеноструктурным анализом на оборудовании с применением медной камеры и Kα-лучей, который показывает, что полученный продукт представляет собой пентасильный цеолит.
Флуоресцентный рентгеноструктурный анализ этого пентасильного цеолита показывает, что его молярное соотношение оксидов кремния/алюминия составляет 49,0.
2. Получение катализатора
(1) Получение катализатора A (применение катализатора A не включается в область притязаний настоящего изобретения).
К синтезированному таким образом пентасильному цеолиту в количестве 10 г в единицах абсолютного стандарта сухости (рассчитанного из потери веса при прокаливании после запекания при 500°C в течение 20 минут) прибавляют гидратированный оксид алюминия (производства Sumitomo Chemical Co., Ltd.), имеющий псевдобемитную структуру, в количестве 30 г в единицах абсолютного стандарта сухости, и 60 г золя оксида алюминия (Al2O3 содержание: 10% по весу, производство Nissan Chemical Industries, Ltd.), и смесь должным образом смешивают, затем смесь высушивают в сушилке при 120°C до тех пор, пока смесь не примет консистенцию жидкой глины. Полученную вымешанную смесь экструдируют через экран, имеющий диаметр пор 1,2 мм. Экструдированный сформованный продукт высушивают в течение ночи при 120°C. После этого температуру медленно поднимают от 350 до 540°C, и продукт обжигают при 540°C в течение 2 часов. Двадцать грамм этого сформованного продукта пентасильного цеолита помещают в водный раствор, содержащий 11 весовых частей NH4Cl и 5 весовых частей CaCl2 на 100 весовых частей, в единицах абсолютного стандарта сухости, сформованного продукта пентасильного цеолита, и соотношение твердое вещество-жидкость доводят до 2,0 кг/л прибавлением чистой воды, затем смесь инкубируют при 80°C в течение 1 часа. Сформованный продукт затем партиями промывают по 6 раз чистой водой. Полученный таким образом сформованный продукт ионообменного пентасильного цеолита высушивают в течение ночи при 120°C. Перед применением продукта в каталитической реакции катализатор обрабатывают пропусканием газообразного сульфида водорода при 250°C в течение 2 часов и затем обжигают при 540°C в течение 2 часов на воздухе для получения катализатора A.
(2) Получение катализатора B
Получают сформованный продукт, содержащий пентасильный (MFI) цеолит и проводят ионообмен с ионами аммония и кальция аналогично способу получения катализатора A. 20 г высушенного сформованного продукта пентасильного цеолита после ионообмена погружают в 40 мл водного раствора перрениевой кислоты, содержащей 80 мг Re в единицах Re при комнатной температуре, смесь оставляют стоять в течение 2 часов. Смесь перемешивают с интервалами каждые 30 минут и после отсасывания жидкости продукт высушивают при 120°C. Перед применением продукта в каталитической реакции, катализатор обрабатывают продуванием газообразным сульфидом водорода при 250°C в течение 2 часов и затем обжигают при 540°C в течение 2 часов и получают катализатор В. Анализ на Re, присутствующий в катализаторе B, проводят ICP спектрометрией и находят, что количество Re составляет 2010 весовых м.д. в единицах Re.
Пример 1, сравнительный пример 1
Вышеописанные катализаторы A и B помещают в реакционные колбы соответственно и проводят тестовые реакции. Композиции применяемых 4 типов сырьевых материалов показаны в таблице 1 ниже. Анализ композиций сырьевых материалов и продуктов реакции проводят с применением 3 газовых хроматографов, снабженных водородно-пламенным детектором. Применяют следующие делительные колонки:
(1) Газовые компоненты (компоненты от метана до н-бутана в газе):
Среда: Юнипак S (торговая марка), 100-150 меш.
Колонка: нержавеющая сталь; длина: 4 м; внутренний диаметр: 3 мм N2: 1,65 кг/см2-G.
Температура: 80°C.
(2) Компоненты в жидкости с температурами кипения, близкими к температуре кипения бензола (от метана до н-бутана, растворенные в жидкости, и от 2-метилбутана до бензола, которые являются жидкими компонентами):
Среда: 25% полиэтилен гликоль 20M/носитель "Shimalite" 60-80 меш.
Колонка: нержавеющая сталь; длина: 12 м; внутренний диаметр: 3 мм.
N2: 2,25 кг/см2-G.
Температура: от 68 до 180°C, скорость увеличения температуры 2°C/мин.
(3) Компоненты с температурами кипения, более высокими, чем температура кипения бензола (от бензола до компонентов тяжелых фракций)
Капиллярная колонка с плавленым оксидом кремния Spelco wax: длина: 60 м; внутренний диаметр: 0,32 мм; толщина пленки 0,5 мкм линейная скорость He: 23 см/сек.
Температура: от 67°C при скорости увеличения температуры 1°C/мин и от 80 до 200°C при скорости увеличения температуры 2°C/мин.
Состав сырьевых материалов (единицы - весовые %)
"EB" обозначает этилбензол, "PX" обозначает п-ксилол, "MX" обозначает м-ксилол, "OX" обозначает о-ксилол и "ET" обозначает этилтолуол. "C9+" обозначает соединения, имеющие не менее 9 атомов углерода. Материалы от A до D представляют собой имитации сырья, подаваемого на стадию деэтилирования перед "циклом разделения-изомеризации". Материал E представляет собой имитацию смешанного ароматического углеводородного сырья, содержащего этилтолуол и соединения, имеющие не менее 9 атомов углерода, для способа прямой подачи.
7,5 г катализатора A или B помещают в реакционную колбу и проводят реакцию с вышеописанными сырьевыми материалами в следующих условиях:
Условия реакции:
WHSV(ч-1): 4,2.
Температура реакции (°C): 405.
Давление реакции (МПа): 0,9.
H2/сырье(моль/моль):3,5.
Результаты тестов показаны в таблице 2.
Из результатов примера 1 видно, что выход ксилола увеличивается при взаимодействии сырья, содержащего этилтолуол, с цеолитным катализатором кислого типа, включающего рений, который является активным гидрирующим металлом. Предполагают, что это происходит из-за того, что толуол, который получают деалкилированием этилтолуола, ингибирует протекание реакции трансалкилирования между ксилолом и бензолом (который получают деэтилированием этилбензола), которая является побочной реакцией и приводит к потери ксилола. Кроме этого прибавление ET в количестве 1% к сырью увеличивает выход на 0,2% (если сравнивать сравнительный пример 1-B и пример 1-C). Это улучшение выхода имеет очень большой экономический эффект при промышленном производстве, в котором обрабатывается большое количество сырья, то есть несколько тонн сырья в час. Кроме этого продукт реакции, полученный в примере 1, имеет низкую концентрацию этилбензола и высокую концентрацию п-ксилола. То есть видно, что этот способ является очень выгодным для получения п-ксилола в "цикле разделения-изомеризации", особенно в способе, в котором на стадии разделения п-ксилола применяют адсорбционное разделение с применением адсорбента на основе цеолита.
Из результатов сравнительного примера 1-A видно, что при применении катализатора (катализатор A), который не включает активного гидрирующего металла, активность этилбензола и этилтолуола в реакции деэтилирования была низкой.
Пример 2
Аналогично получению катализатора B 20 г сухого сформованного продукта пентасильного цеолита погружают в 40 мл водного раствора хлорплатиновой кислоты, содержащего 4 мг Pt в единицах Pt при комнатной температуре, и смесь оставляют стоять в течение 2 часов. Смесь перемешивают с интервалами каждые 30 минут, и после отсасывания жидкости продукт высушивают в течение ночи при 120°C. Перед применением продукта в каталитической реакции катализатор обрабатывают продуванием газообразным сульфидом водорода при 250°C в течение 2 часов и затем обжигают при 540°C в течение 2 часов на воздухе и получают катализатор C. Анализ на Pt, присутствующую в катализаторе C, проводят ICP спектрометрией и находят, что количество Pt составляет 169 весовых м.д. в единицах Pt.
В реакционную колбу помещают 7,5 г катализатора C и проводят реакцию с вышеописанным сырьевым материалом D в тех же условиях, что и в примере 1. Результаты показаны в таблице 3.
Пример 3
В 40 мл водного раствора хлорида палладия, содержащего 40 мг Pd в единицах Pd, погружают 20 г высушенного сформованного продукта пентасильного цеолита, который содержит ионообменные ионы аммония и кальция и который был приготовлен аналогично катализатору B; смесь оставляют стоять в течение 2 часов. Смесь перемешивают с интервалами каждые 30 минут и после отсасывания жидкости продукт высушивают при 120°C. Перед применением продукта в каталитической реакции катализатор обрабатывают продуванием газообразным сульфидом водорода при 250°C в течение 2 часов и затем обжигают при 540°C в течение 2 часов, и получают катализатор D. Анализ на Pd, присутствующий в катализаторе D, проводят ICP спектрометрией и находят, что количество Pd составляет 1480 весовых м.д. в единицах Pd.
В реакционную колбу помещают 7,5 г катализатора D и проводят реакцию с вышеописанным сырьевым материалом D в тех же условиях, что и в примере 1. Результаты показаны в таблице 3.
Пример 4
В 40 мл водного раствора нитрата никеля, содержащего 40 мг Ni в единицах Ni погружают 20 г высушенного сформованного продукта пентасильного цеолита, который содержит ионообменные ионы аммония и кальция и который был приготовлен аналогично катализатору B, смесь оставляют стоять в течение 2 часов. Смесь перемешивают с интервалами каждые 30 минут и после отсасывания жидкости продукт высушивают при 120°C. Перед применением продукта в каталитической реакции катализатор обрабатывают продуванием газообразным сульфидом водорода при 250°C в течение 2 часов и затем обжигают при 540°C в течение 2 часов и получают катализатор Е. Анализ на Ni, присутствующий в катализаторе Е, проводят ICP спектрометрией и находят, что количество Ni составляет 1680 весовых м.д. в единицах Ni.
В реакционную колбу помещают 7,5 г катализатора E и проводят реакцию с вышеописанным сырьевым материалом D в тех же условиях, что и в примере 1. Результаты показаны в таблице 3.
(Единицы: весовые %)
Пример 5
В 40 мл водного раствора оксида рения, содержащего 200 мг Re в единицах Re, погружают 20 г высушенного сформованного продукта пентасильного цеолита, который содержит ионообменные ионы аммония и кальция и который был приготовлен аналогично катализатору B, смесь оставляют стоять в течение 2 часов. Смесь перемешивают с интервалами каждые 30 минут и после отсасывания жидкости продукт высушивают при 120°C. Перед применением продукта в каталитической реакции катализатор обрабатывают продуванием газообразным сульфидом водорода при 250°C в течение 2 часов и затем обжигают при 540°C в течение 2 часов и получают катализатор F. Анализ на Re, присутствующий в катализаторе F, проводят ICP спектрометрией и находят, что количество Re составляет 4800 весовых м.д. в единицах Re.
В реакционную колбу помещают 7,5 г катализатора B или катализатора F и проводят реакцию с вышеописанным сырьевым материалом Е в условиях, показанных ниже. Результаты показаны в таблице 4.
Условия реакции:
WHSV (ч-1): 5,3.
Температура реакции (°C): 390.
Давление реакции (МПа): 0,9.
H2/сырье (моль/моль): 2,5.
(Единицы: весовые %)
Из таблицы 4 видно, что чем больше количество применяемого рения, тем выше извлечение ксилола. Сырьевой материал E представляет собой имитацию сырья, которое применяют при прямом способе подачи, исключая удаление C9+. Видно, что катализатор также является эффективным в способе прямой подачи.
Пример 6
Концентрации неароматических соединений в реакционном растворе измеряют способом, который позволяет проводить детальный анализ неароматических соединений (условия анализа описаны в (2) в примере 1) для реакционных растворов, полученных при применении катализаторов B и D в примере 3, соответственно. В результате, как показано ниже в таблице 5, концентрации циклогексана и метилциклопентана, которые загрязнены примесями, имеющими точки кипения близко к точке кипения бензола, были ниже в примере 1, в котором применяют катализатор B, и рассчитанная чистота конечного продукта бензола (чистота бензола), которую считают по равенству для расчета чистоты бензола, описанному ниже, является высокой и составляет не менее 99,8% по весу в примере 1.
(Единицы: весовые %)
Рассчитанная чистота конечного продукта бензола = ([концентрация бензола]/a+b+c+d+[концентрация бензола]) * 100(%)), где a-d обозначают следующее:
a=0,1 * [концентрация n-C6 парафинов]
b=0,7 * [концентрация метилциклопентана]
c=1,0 * [концентрация циклогексана]
d=1,0 * [концентрация C7 нафтеновых парафинов].
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения изомеров ксилола | 1974 |
|
SU890971A3 |
| УЛУЧШЕННЫЙ КАТАЛИЗАТОР ПРЕВРАЩЕНИЯ ЭТИЛБЕНЗОЛА В СПОСОБЕ ИЗОМЕРИЗАЦИИ КСИЛОЛА | 2016 |
|
RU2727190C2 |
| СПОСОБ КАТАЛИТИЧЕСКОЙ ИЗОМЕРИЗАЦИИ С*008-АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 1991 |
|
RU2094419C1 |
| СПОСОБ ИЗОМЕРИЗАЦИИ УГЛЕРОДНОГО СКЕЛЕТА ОЛЕФИНОВ (ВАРИАНТЫ) | 1998 |
|
RU2186756C2 |
| ИЗОМЕРИЗАЦИЯ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ С ИСПОЛЬЗОВАНИЕМ СИСТЕМЫ ДВОЙНОГО КАТАЛИЗАТОРА | 2012 |
|
RU2564526C1 |
| СПОСОБ КАТАЛИТИЧЕСКОЙ ИЗОМЕРИЗАЦИИ НЕРАВНОВЕСНОЙ СМЕСИ C- АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 1996 |
|
RU2125977C1 |
| СПОСОБЫ УВЕЛИЧЕНИЯ СУММАРНОГО ВЫХОДА АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ И КСИЛОЛОВ В КОМПЛЕКСЕ ПРОИЗВОДСТВА АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 2016 |
|
RU2691987C1 |
| КАТАЛИЗАТОР И СПОСОБ КОНВЕРСИИ УГЛЕВОДОРОДОВ | 2012 |
|
RU2570427C1 |
| СИНТЕТИЧЕСКИЙ КРИСТАЛЛИЧЕСКИЙ АЛЮМОСИЛИКАТ КАК КОМПОНЕНТ КАТАЛИЗАТОРА ДЛЯ КАТАЛИТИЧЕСКИХ ПРЕВРАЩЕНИЙ УГЛЕВОДОРОДОВ | 1994 |
|
RU2083281C1 |
| СПОСОБ ПРЕВРАЩЕНИЯ СМЕСЕЙ, СОДЕРЖАЩИХ АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ C В ИЗОМЕРЫ КСИЛОЛА | 2004 |
|
RU2354640C2 |

Изобретение относится к способу превращения этилбензола, включающий стадию введения смешанного С8 ароматического углеводородного сырья, содержащего этилбензол, в контакт с катализатором(ами), содержащими, по меньшей мере, один металл, выбранный из металлов Группы VII и VIII в присутствии Н2 для превращения указанного этилбензола в бензол. При этом указанное сырье содержит С9-С10 ароматические углеводороды, содержащие этилтолуол в количестве не менее 1% по весу и не более 20% по весу, где указанный этилтолуол превращают в толуол одновременно с указанным превращением этилбензола. Также изобретение относится к четырем вариантам способа получения п-ксилола, которые используют в качестве составляющей стадии отмеченный выше способ превращения этилбензола. Использование настоящего изобретения позволяет наряду с превращением этилбензола в бензол превращать этилтолуол в толуол. 5 н. и 12 з.п. ф-лы, 5 табл., 6 пр., 4 ил.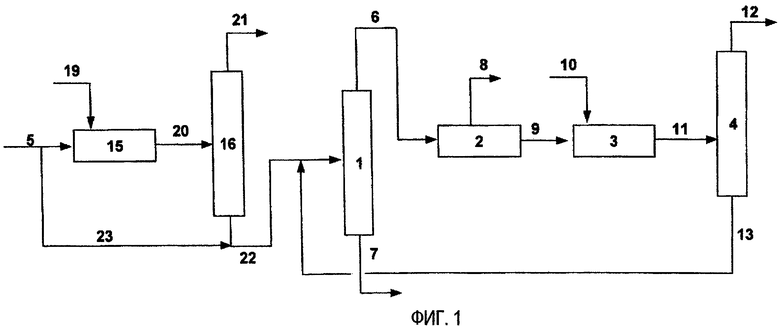
1. Способ превращения этилбензола, включающий стадию введения смешанного С8 ароматического углеводородного сырья, содержащего этилбензол, в контакт с катализатором(ами), содержащими, по меньшей мере, один металл, выбранный из металлов Группы VII и VIII в присутствии Н2 для превращения указанного этилбензола в бензол, где указанное сырье содержит С9-С10 ароматические углеводороды, содержащие этилтолуол в количестве не менее 1 вес.% и не более 20 вес.%, где указанный этилтолуол превращают в толуол одновременно с указанным превращением этилбензола.
2. Способ по п.1, где указанный этилтолуол в указанном сырье имеет концентрацию не менее 1 вес.%.
3. Способ по п.2, где указанный этилтолуол в указанном сырье имеет концентрацию не менее 3 вес.%.
4. Способ по п.3, где указанный этилтолуол в указанном сырье имеет концентрацию не менее 5 вес.%.
5. Способ по п.1, где указанный этилтолуол в указанном сырье превращают со степенью конверсии не менее 50%.
6. Способ по п.1, где указанный катализатор кислого типа содержит, по меньшей мере, один металл, выбранный из группы, состоящей из платины, палладия и рения.
7. Способ по п.6, где указанный катализатор кислого типа содержит рений.
8. Способ по п.7, где содержание указанного рения в указанном катализаторе кислого типа составляет от 0,01 вес.% до 5 вес.%.
9. Способ по п.8, где содержание указанного рения в указанном катализаторе кислого типа составляет от 0,1 вес.% до 2 вес.%.
10. Способ по п.1, дополнительно содержащий дистилляционное разделение бензола, получаемого в реакции, и выделение бензола с чистотой не менее 99,8 вес.%.
11. Способ по п.1, где указанный катализатор кислого типа представляет собой пентасильный цеолит, имеющий молярное соотношение оксидов кремния/алюминия от 10 до 70.
12. Способ получения п-ксилола, включающий стадии:
обработки смешанного С8 ароматического углеводородного сырья, содержащего этилбензол и ксилол, указанным способом по любому из пп.1-11 для изомеризации указанного ксилола вместе с превращением указанного этилбензола в бензол; и
отделения п-ксилола от полученного продукта реакции.
13. Способ получения п-ксилола, включающий:
первую стадию деэтилирования/изомеризации ксилола, на которой происходит обработка смешанного С8 ароматического углеводородного сырья, содержащего этилбензол и ксилол, указанным способом по п.12 для изомеризации указанного ксилола вместе с превращением указанного этилбензола в бензол;
стадию отделения п-ксилола от продукта реакции, полученного на указанной первой стадии деэтилирования/изомеризации ксилола;
стадию обработки ксилола, содержащегося в остатке после разделения на второй стадии изомеризации ксилола, для изомеризации указанного ксилола; и
повторное отделение п-ксилола от продукта реакции указанной второй стадии изомеризации ксилола.
14. Способ по п.13, где указанная вторая стадия изомеризации ксилола включает введение указанного остатка после разделения в контакт с катализатором(ами) кислотного типа, содержащего, по меньшей мере, один металл, выбранный из группы, состоящей из металлов Группы VII и VIII в присутствии H2.
15. Способ получения п-ксилола, включающий:
стадию деэтилирования/изомеризации ксилола, на которой происходит обработка смешанного С8 ароматического углеводородного сырья, содержащего этилбензол и ксилол, указанным способом по п.12 для изомеризации указанного ксилола вместе с превращением указанного этилбензола в бензол;
стадию отделения п-ксилола от продукта реакции, полученного на указанной стадии деэтилирования/изомеризации ксилола; и
стадию повторного применения остатка после разделения, полученного на стадии разделения применением указанного остатка на указанной стадии деэтилировании/изомеризации ксилола.
16. Способ по п.15, дополнительно включающий стадию повторного применения указанного остатка после разделения смеси путем смешивания указанного остатка с указанным смешанным С8 ароматическим углеводородным сырьем и обработки полученной смеси на указанной стадии деэтилирования/изомеризации ксилола.
17. Способ получения п-ксилола с использованием оборудования для получения п-ксилола для проведения указанной первой стадии деэтилирования/изомеризации ксилола, стадии разделения п-ксилола и второй стадии изомеризации ксилола, которые цитируются по п.13 или 14, где указанное оборудование содержит обводной трубопровод, который не проходит через указанную первую стадию деэтилирования/изомеризации ксилола, и где указанное смешанное С8 ароматическое углеводородное сырье, смешанное с указанными С9-С10 ароматическими углеводородами, содержащими этилтолуол, подают на указанную стадию разделения п-ксилола, как требуется.
| US 6504076 B1, 07.01.2003 | |||
| US 5763720 A, 09.06.1998 | |||
| US 5032561 A, 16.07.1991 | |||
| Способ окисления боковых цепей ароматических углеводородов и их производных в кислоты и альдегиды | 1921 |
|
SU58A1 |
| СПОСОБ КАТАЛИТИЧЕСКОЙ ИЗОМЕРИЗАЦИИ НЕРАВНОВЕСНОЙ СМЕСИ C- АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 1996 |
|
RU2125977C1 |
| СЕЛЕКТИВНАЯ ИЗОМЕРИЗАЦИЯ КСИЛОЛОВ И КОНВЕРСИЯ ЭТИЛБЕНЗОЛА | 2000 |
|
RU2233260C2 |
| US 4341622 A, 27.07.1982 | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Способ крашения тканей | 1922 |
|
SU62A1 |
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| US 4973784 A, 27.11.1990. | |||
Авторы
Даты
2012-04-27—Публикация
2007-03-28—Подача