Изобретение относится к области офтальмологии и может быть использовано для лечения пролиферативной диабетической ретинопатии.
Известен способ лечения пролиферативной диабетической ретинопатии (S.Rizzo, F.Patelli, D.R.Chow - "Vitreo-retinal surgery", Essentials in ophthalmology. Springer, 2009, pages - 31-36, 95-97), согласно которому осуществляется установка 3-х портов 25 G в нижненаружном сегменте - для ирригации, верхненаружном - для витреотома, верхневнутреннем - для эндоосветителя, введение инструментов через соответствующие порты в полость глаза. Далее световодом освещаются волокна стекловидного тела и витреотомом удаляются его передние слои. Затем с помощью витреотома удаляют средние и кортикальные слои стекловидного тела. Выводят витреотом из полости глаза, поднимают насадку с линзой. Вводят эндовитреальный шпатель, опускают насадку с линзой, перенастраивают операционный микроскоп и положение насадки с линзой над поверхностью глаза. При замене инструмента необходимо заново фокусировать и перенастраивать операционный микроскоп и положение насадки с линзой над поверхностью глаза. Во время смены инструмента происходит частичная разгерметизация полости глаза, через открытый порт происходит неконтролируемый отток жидкости из полости глаза. Это вызывает значительные перепады внутриглазного давления. Далее, с помощью эндовитреального шпателя отслаивают участок эпиретинальной мембраны (ЭРМ) от подлежащей сетчатки. После чего выводят эндовитреальный шпатель и вводят эндовитреальный пинцет. С помощью эндовитреального пинцета осуществляют подтягивание участка ЭРМ и разделение соединительнотканных перемычек между ЭРМ и сетчаткой. Затем выводят эндовитреальный пинцет. Вводят эндовитреальные ножницы, с помощью которых отсекают участок отслоенной ЭРМ. Затем выводят эндовитреальные ножницы и вводят эндовитреальный шпатель. Последовательность действий повторяют до полного удаления ЭРМ.
Однако данный метод имеет ряд существенных недостатков. Значительная операционная травма тканей глаза из-за неоднократной смены хирургических инструментов, необходимых для удаления ЭРМ по методике прототипа. Имеют место большие амплитуды перепадов внутриглазного давления (ВГД) в полости глазного яблока при смене инструментов, что связано с разгерметизацией полости глаза и интенсивным турбулентным оттоком жидкости через порт для введения инструментов. Это вызывается несоответствием между объемом эвакуируемой через порт жидкости и ее поступлением через канюлю ирригации. Перепады ВГД способствуют развитию таких интраоперационных осложнений, как кровотечение, нарушение кровообращения в сосудистой оболочке, цилиарном теле и сетчатке, что увеличивает время восстановления гомеостаза глазного яблока, физиологических условий функционирования после операционного лечения, время реабилитации. Изменение пространственного взаиморасположения сетчатки и эпиретинальных структур, возникающие из-за перепадов ВГД, затрудняет манипуляции хирурга после перенастройки операционного микроскопа и насадки с линзой. Необходимость неодкратной перенастройки операционного микроскопа и насадки с линзой из-за расфокуссировки изображения, возникающей при смене инструментов. Это вызывает дискомфорт и значительное перенапряжение органа зрения хирурга. Значительная длительность операции во времени требует длительной анестезии, увеличивается риск развития индивидуальных побочных эффектов анестезии.
Техническим результатом является одновременное уменьшение травматичности операции, амплитуды перепадов ВГД в полости глазного яблока, предотвращение изменения пространственного взаиморасположения сетчатки и эпиретинальных структур, возникающего из-за перепадов ВГД при смене хирургических инструментов и разгерметизации полости глаза; уменьшение необходимости неоднократной перенастройки операционного микроскопа и насадки с линзой, предотвращение интраоперационных осложнений в виде кровотечения, гипотонии, уменьшение времени операции, объема анестезиологического пособия, риска развития индивидуальных побочных эффектов анестезии у больных, длительно страдающих сахарным диабетом, имеющих тяжелый коморбидный фон, их более быстрая зрительная и социальная реабилитация, повышение удобства в работе хирурга.
Способ заключается в установке портов, введении световода и инструментов, проведении витрэктомии, отслаивании участка ЭРМ, отгибании его, разрезании и удалении его витреотомом, отличающийся тем, что совмещают продольную ось порта для витреотома с направлением на край ЭРМ, образуя ось хирургического воздействия (ОХВ), совмещают продольную ось витреотома с линией продольной симметрии ЭРМ, образуя плоскость хирургического воздействия (ПХВ), подводят под ретинальную поверхность ЭРМ наружную поверхность наконечника витреотома, осуществляют асинхронные колебательные движения вокруг центра колебаний с соотношением положительной амплитуды к отрицательной в интервале от 1,5 до 1,0; центр колебательного движения перемещают вдоль наружной криволинейной поверхности ЭРМ, за каждый этап дискретного движения наконечник витреотома перемещают вдоль ОХВ и в ПХВ вперед на 2-3 мм, затем назад на 1-2 мм; причем наконечник витреотома продвигают по ретинальной поверхности ЭРМ к противоположному краю ЭРМ, увеличивая площадь отслаиваемой ретинальной поверхности ЭРМ, начиная формирование прямолинейного тоннеля; в режиме вакуума 200-300 мм рт.ст. осуществляют фиксацию верхней стенки тоннеля ЭРМ в окне витреотома и подтягивание ЭРМ вверх, затем снижают уровень вакуума до нуля и снова перемещают наконечник витреотома вдоль ОХВ и в ПХВ вперед до формирования тоннеля длиной 4-5 мм; подводят наконечник витреотома под наружную границу тоннеля, окно наконечника витреотома приводят в соприкосновение с верхней стенкой тоннеля, затем в режиме резания наконечник витреотома продвигают вдоль тоннеля в ЭРМ, разделяя ЭРМ на два равных лоскута, край каждого из лоскутов ЭРМ отгибают витреотомом на угол 20-30 градусов относительно поверхности сетчатки, на режиме вакуума 200-300 мм рт.ст. край каждого лоскута ЭРМ фиксируют наконечником витреотома и осуществляют его подтягивание, отслаивая ЭРМ от поверхности сетчатки, отслоенный фрагмент ЭРМ удаляют витреотомом в режиме резания, в аналогичной последовательности удаляют остальные фрагменты ЭРМ.
Автором разработана совокупность существенных отличительных признаков, изложенных в формуле изобретения, которая является необходимой и достаточной для однозначного достижения заявленного технического результата.
Способ поясняется чертежами Фиг.1, Фиг.2.
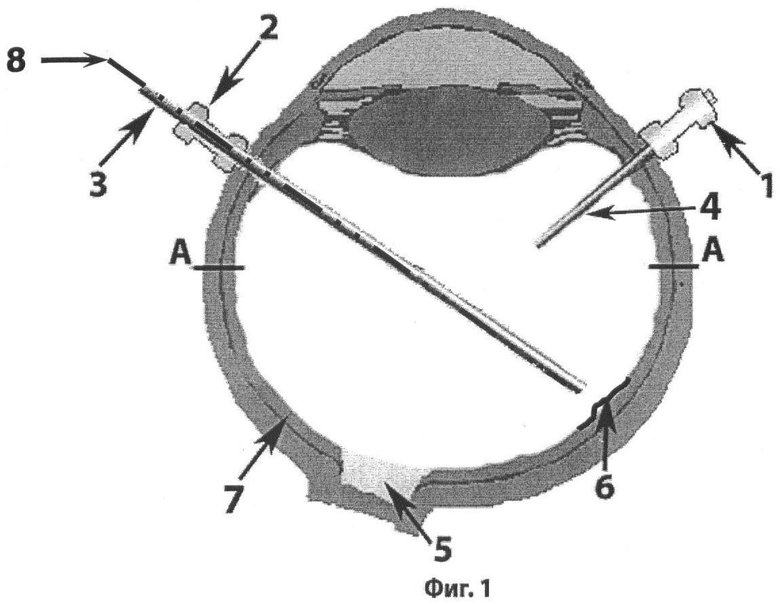
Фиг.1 - фронтальное сечение глазного яблока. На фигуре обозначены: 1 - порт для эндоосветителя; 2 - порт для витреотома; 3 - витреотом; 4 - эндоосветитель; 5 - диск зрительного нерва; 6 - эпиретинальная мембрана (ЭРМ); 7 - сетчатка; 8 - ось хирургического воздействия (ОХВ); 9 - сосудистые аркады.
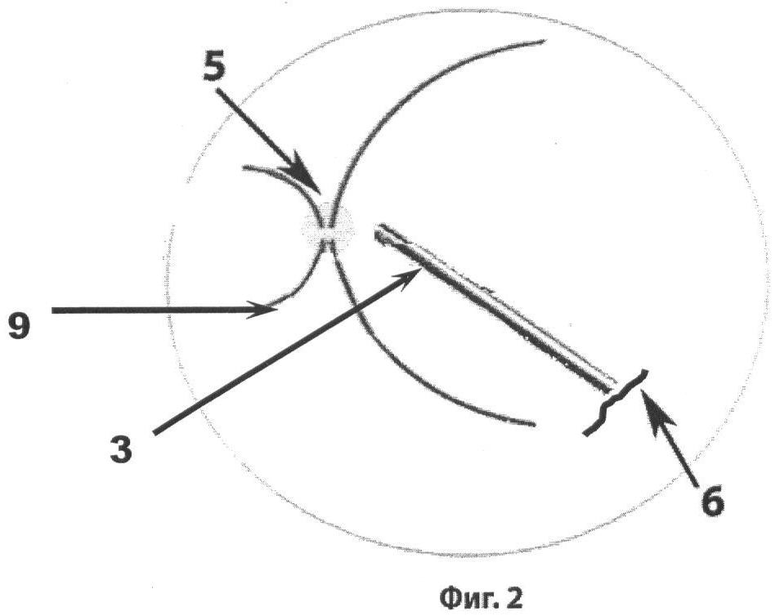
Фиг.2 - А-А - сечение фиг.1.
Способ осуществляется следующим образом.
После обработки операционного поля устанавливают блефаростат.
В нижненаружном квадранте поверхности глазного яблока отмеряют ровно четыре миллиметра от лимба до плоской части цилиарного тела специальным циркулем или обратным концом одноразового троакара 25 G. Согласно дистальной точке отмеченного расстояния от лимба до плоской части цилиарного тела осуществляют прокол троакаром 25 G строго перпендикулярно касательной, проходящей через дистальную точку, отмеченную циркулем до середины длины металлического стилета троакара, затем производят вкручивающие движения до полного введения троакара с портом в полость глаза. Затем пинцет для завязывания швов устанавливают в специальный желобок порта и отделяют стилет троакара от порта, при этом порт 25 G остается в полости глаза. В установленный порт помещают канюлю ирригации, предварительно выпустив из ирригационной системы воздух, путем активного слива ирригационной жидкости через канюлю. Аналогичным образом устанавливают порты 1, 2 в верхненаружном и верхневнутреннем квадрантах для эндоосветителя 1 и витреотома 2 соответственно.
На поверхность роговицы наносят вискоэластик шприцом с канюлей. В полость глаза через порты вводят витреотом 3 и эндоосветитель 4, опускают насадку с линзой и фокусируют изображение глазного дна по глубине и четкости, при этом рабочее расстояние насадки с линзой 90 дптр от поверхности роговицы до поверхности линзы составляет 5 мм. Освещая волокна стекловидного тела эндоосветителем 7 проводят удаление передних и средних и кортикальных слоев стекловидного тела. Затем продольную ось порта, через который введен витреотом, совмещают с направлением на край ЭРМ 6, путем манипуляции витреотомом 3 и ориентируются на наконечник витреотома, который при правильной совмещении продольной оси порта 2 с направлением на край ЭРМ 6 должен оказаться напротив наименее спаянного с сетчаткой края ЭРМ, так образуется ОХВ 8. Затем совмещают продольную ось витреотома с линией продольной симметрии ЭРМ, образуя ПХВ. Подводят под ретинальную поверхность ЭРМ наружную поверхность наконечника витреотома, осуществляют асинхронные колебательные движения вокруг центра колебаний. Соотношение положительной амплитуды к отрицательной в интервале от 1,5 до 1,0. Центр колебательного движения перемещают вдоль наружной криволинейной поверхности ЭРМ, за каждый этап дискретного движения; при этом за каждое колебательное движение наконечник витреотома перемещают вдоль ОХВ и в ПХВ вперед на 2-3 мм, затем назад на 1-2 мм. Причем наконечник витреотома продвигают по ретинальной поверхности ЭРМ к противоположному краю ЭРМ, увеличивая площадь отслаиваемой ретинальной поверхности ЭРМ, формируют прямолинейный тоннель. В режиме вакуума 200-300 мм рт.ст. осуществляют фиксацию верхней стенки тоннеля ЭРМ в окне витреотома и подтягивание ЭРМ вверх, затем снижают уровень вакуума до нуля и снова перемещают наконечник витреотома вдоль ОХВ и в ПХВ вперед, пока не будет сформирован тоннель длиной 4-5 мм. Подводят наконечник витреотома под наружную границу тоннеля, окно наконечника витреотома приводят в соприкосновение с верхней стенкой тоннеля, затем в режиме резания наконечник витреотома продвигают вдоль тоннеля в ЭРМ, разделяя ЭРМ на 2 равных лоскута, край каждого из лоскутов ЭРМ затем отгибают витреотомом на угол 20-30 градусов относительно поверхности сетчатки, на режиме вакуума 200-300 мм рт.ст. край лоскута ЭРМ фиксируют наконечником витреотома и осуществляют его подтягивание, отслаивая ЭРМ от поверхности сетчатки, выделенный фрагмент ЭРМ удаляют витреотомом в режиме резания, в аналогичной последовательности удаляют остальные фрагменты ЭРМ.
Автором проведена большая работа по обоснованию интервалов параметров, приведенных в формуле изобретения.
Соотношение положительной амплитуды к отрицательной в интервале от 1,5 до 1,0 при формировании тоннеля выведен эмпирически на основе большого опыта использования данного способа. При соотношении более 1,5 существует угроза повреждения ткани сетчатки, формирования в ней микроразрывов из-за сильного натяжения участков сетчатки, интимно спаянных с ЭРМ, при манипуляции наконечником витреотома в пространстве между ЭРМ и сетчаткой. При соотношении менее 1,0 значительно увеличивается время, необходимое для атравматичного расслоения спаек между ЭРМ и сетчаткой, что, естественно, требует большего объема анестезиологического пособия и увеличивает время манипулирования инструментами в полости глаза, поэтому увеличивается степень травматизации тканей глаза.
При формировании тоннеля, кроме колебательных движений, наконечник витреотома перемещают вперед на 2-3 мм и назад на 1-2 мм за каждый этап дискретного движения. При параметре перемещения наконечника витреотома вперед более 3 мм существует угроза повреждения ткани сетчатки наконечником витреотома, так как резко снижается контроль за перемещением наконечника в пространстве между ЭРМ и сетчаткой, и ощущение глубины наконечника витреотома, так как поверхность ЭРМ непрозрачна, а значит, отсутствует четкий визуальной контроль за манипуляциями витреотомом. При параметре перемещения наконечника витреотома менее 1 мм значительно увеличивается время формирования тоннеля, что также требует большего объема анестезии, увеличивает суммарную травматичность операции.
Параметр общей длины формируемого тоннеля, равный 4-5 мм, является оптимальным, поскольку складывается из параметров продвижения витреотома вперед и назад (2-3 мм и 1-2 мм), он является достаточным и безопасным, так как во время манипуляций хирург четко контролирует свои действия и отсутствует угроза интраоперационных осложнений.
Параметр разделения ЭРМ именно на 2 лоскута подтвержден практикой использования метода, дихотомический принцип разделения и удаления ЭРМ наиболее приемлем, поскольку создает удобную площадку для работы витреотомом, при большем количестве лоскутов значительно уменьшается площадь свободного края отслоенной и разделенной поверхности ЭРМ, что затрудняет работу с ней наконечника витреотома из-за уменьшения площади точки фиксации окна витреотома к поверхности лоскута, при осуществлении следующего этапа способа - аспирации края лоскута, его подтягивания и удаления.
Угол отгибания лоскута 20-30 градусов также выведен эмпирически и обоснован практикой применения способа в клинике. При меньшем угле отгибания наклон поверхности ЭРМ недостаточен для интимного и эффективного контакта с наконечником витреотома, поэтому возникают значительные затруднения в аспирации, подтягивании и удалении фрагмента ЭРМ. Угол наклона лоскута более 30 градусов, напротив, делает поверхность отгибаемого фрагмента слишком плоской, следовательно, аспирация, подтягивание и удаление фрагмента в этой ситуации значительно затруднены.
Параметры вакуума 200-300 мм рт.ст. (режим аспирации) оптимальны и подтверждены на практике, так, при параметрах вакуума более 300 мм рт.ст. слишком грубое и значительное засасывание края фрагмента ЭРМ в окно витреотома затрудняет подтягивание вверх поверхности ЭРМ из-за возникающего дефицита свободной площади фрагмента ЭРМ, а при параметрах вакуума менее 200 мм рт.ст. аспирация края фрагмента становится неэффективной, так как сила вакуума, необходимая для удержания края ЭРМ в окне витреотома, меньше силы, прилагаемой для подтягивания края ЭРМ вверх.
Технический результат обеспечивается тем, что отсутствие необходимости смены инструментов, низкие амплитуды перепадов внутриглазного давления в полости глаза уменьшают время, травматичность операции и объем анестезиологического пособия, поддерживают стабильность интерфейса структур сетчатки и рабочего конца инструмента в ПХВ, что является профилактикой интраоперационных осложнений; оптимальные параметры колебательных движений (1,0-1,5), длины формируемого тоннеля (4-5 мм), параметров вакуума (200-300 мм рт.ст.), четкая и координированная, методичная последовательность движений позволяют эффективно удалять ЭРМ и обеспечить быструю реабилитацию пациентов после операции.
Способ поясняется следующими клиническими примерами.
Пример 1. Пациентка К., 68 лет. Обратилась с жалобами на снижение зрения на правом глазу. Страдает сахарным диабетом более 15 лет. При обследовании острота зрения правого глаза составила 0.05, коррекция улучшения не давала. ВГД - 18 мм рт.ст. Биомикроскопически: роговица и влага передней камеры прозрачные, строма радужки субатрофична, в хрусталике выраженные помутнения в корковых слоях и субкапсулярно. Выраженная деструкция стекловидного тела в виде нитей и шварт. Офтальмоскопически: ДЗН бледно-розовый, границы четкие, на поверхности сетчатки имеются фиброглиальные разрастания в виде мембраны, распространяющейся от ДЗН к верхневисочной сосудистой аркаде, макулярная область имеет складчатый рельеф. Тракционная отслойка сетчатки в верхнем, верхненаружном сегментах, по всей поверхности сетчатки определяются микрогеморрагии, большое количество твердых экссудатов. В-скан: OD - выраженная деструкция стекловидного тела в виде нитей и веретен гиперэхогенных, тракционная отслойка сетчатки в верхнем и верхненаружном сегментах, высота отслойки - 1,4 мм.
При обследовании острота зрения левого глаза составила 0,5 с коррекцией. Биомикроскопически: роговица и влага передней камеры прозрачные, передняя камера средней глубины, строма радужки субатрофична. Субкапсулярные помутнения хрусталика. Умеренная деструкция стекловидного тела. Офтальмоскопически: ДЗН бледно-розовый, границы четкие, по всей поверхности сетчатки определяются микрогеморрагии, твердые экссудаты, деформация сосудов по типу «сосисок». В-скан: деструкция стекловидного тела в виде зерен. Оболочки прилежат.
Диагноз OD: Пролиферативная диабетическая ретинопатия. Тракционная отслойка сетчатки. Деструкция и помутнение стекловидного тела Осложненная катаракта. Миопия слабой степени.
OS - Препролиферативная диабетическая ретинопатия. Деструкция стекловидного тела. Осложненная катаракта. Миопия слабой степени.
Выполнено комбинированное хирургическое вмешательство: факоэмульсификация катаракты, удаление эпиретинальной мембраны согласно способу, заявленному в изобретении.
После установки портов и введения инструментов в полость глазного яблока совместили продольную ось порта для витреотома с направлением на край ЭРМ, образовав ось хирургического воздействия (ОХВ), совместили продольную ось витреотома с линией продольной симметрии ЭРМ, образовав плоскость хирургического воздействия (ПХВ), подвели под ретинальную поверхность ЭРМ наружную поверхность наконечника витреотома, осуществляли асинхронные колебательные движения вокруг центра колебаний, с соотношением положительной амплитуды к отрицательной 1,5, центр колебательного движения перемещали вдоль наружной криволинейной поверхности ЭРМ за каждый этап дискретного движения; при этом за каждое колебательное движение наконечник витреотома перемещали вдоль ОХВ и в ПХВ вперед на 2 мм, затем назад на 1 мм; причем наконечник витреотома продвигали по ретинальной поверхности ЭРМ к противоположному краю ЭРМ, увеличивая площадь отслаиваемой ретинальной поверхности ЭРМ, формировали прямолинейный тоннель; в режиме вакуума 200 мм рт.ст. осуществляли фиксацию верхней стенки тоннеля ЭРМ в окне витреотома и подтягивание ЭРМ вверх, затем снижали уровень вакуума до нуля и снова перемещали наконечник витреотома вдоль ОХВ и в ПХВ вперед, пока не был сформирован тоннель длиной 4 мм; подводили наконечник витреотома под наружную границу тоннеля, окно наконечника витреотома приводили в соприкосновение с верхней стенкой тоннеля, затем в режиме резания наконечник витреотома продвигали вдоль тоннеля в ЭРМ, разделяя ЭРМ на 2 равных лоскута, край каждого из лоскутов ЭРМ затем отгибали витреотомом на угол 20 градусов относительно поверхности сетчатки, на режиме вакуума 200 мм рт.ст. край лоскута ЭРМ фиксировали наконечником витреотома и осуществляли его подтягивание, отслаивая ЭРМ от поверхности сетчатки, выделенный фрагмент ЭРМ удаляли витреотомом в режиме резания, в аналогичной последовательности удаляли остальные фрагменты ЭРМ.
При контроле через месяц зрение правого глаза 0,06 sph-1.0 cyl ax=0.1.
ВГД 17 мм рт.ст. Офтальмоскопически: сетчатка прилежит, полость стекловидного тела прозрачная.
Пример 2. Пациентка Б., 56 лет. Обратилась с жалобами на снижение зрения на левом глазу. Страдает сахарным диабетом более 8 лет. При обследовании острота зрения правого глаза составила 0.01, коррекция улучшения не давала. ВГД - 20 мм рт.ст. Биомикроскопически: роговица и влага передней камеры прозрачные, строма радужки субатрофична, в капсульном мешке имплантированная интраокулярная линза центрирована, фиброз капсульного мешка. Выраженная деструкция стекловидного тела в виде нитей. Офтальмоскопически: ДЗН бледно-розовый, границы четкие, на поверхности сетчатки имеется эпиретинальная мембрана, распространяющаяся от нижневисочной сосудистой аркады к диску зрительного нерва и макулярной области. Тракционная отслойка сетчатки в нижнем, нижненаружном сегментах, по всей поверхности сетчатки определяются микрогеморрагии, большое количество твердых экссудатов. В-скан: OS - выраженная деструкция стекловидного тела в виде нитей и зерен гиперэхогенных, тракционная отслойка сетчатки в нижнем и нижненаружном сегментах, высота отслойки - 1,1 мм.
При обследовании острота зрения правого глаза составила 0,6 с коррекцией. Биомикроскопически: роговица и влага передней камеры прозрачные, передняя камера средней глубины, строма радужки субатрофична. В капсульном мешке имплантированная интраокулярная линза центрирована, фиброз капсульного мешка хрусталика. Умеренная деструкция стекловидного тела. Офтальмоскопически: ДЗН бледно-розовый, границы четкие, по всей поверхности сетчатки определяются микрогеморрагии, твердые экссудаты. В-скан: деструкция стекловидного тела в виде зерен. Оболочки прилежат.
Диагноз OS: Пролиферативная диабетическая ретинопатия. Тракционная отслойка сетчатки. Деструкция и помутнение стекловидного тела Артифакия. Простой миопический астигматизм слабой степени.
OD - Препролиферативная диабетическая ретинопатия. Деструкция стекловидного тела. Артифакия. Простой миопический астигматизм слабой степени.
Выполнено хирургическое вмешательство - удаление эпиретинальной мембраны согласно способу, заявленному в изобретении.
После установки портов и введения инструментов в полость глазного яблока совместили продольную ось порта для витреотома с направлением на край ЭРМ, образовав ось хирургического воздействия (ОХВ), совместили продольную ось витреотома с линией продольной симметрии ЭРМ, образовав плоскость хирургического воздействия (ПХВ), подвели под ретинальную поверхность ЭРМ наружную поверхность наконечника витреотома, осуществляли асинхронные колебательные движения вокруг центра колебаний, с соотношением положительной амплитуды к отрицательной 1,0, центр колебательного движения перемещали вдоль наружной криволинейной поверхности ЭРМ за каждый этап дискретного движения; при этом за каждое колебательное движение наконечник витреотома перемещали вдоль ОХВ и в ПХВ вперед на 3 мм, затем назад на 2 мм; причем наконечник витреотома продвигали по ретинальной поверхности ЭРМ к противоположному краю ЭРМ, увеличивая площадь отслаиваемой ретинальной поверхности ЭРМ, формировали прямолинейный тоннель; в режиме вакуума 300 мм рт.ст. осуществляли фиксацию верхней стенки тоннеля ЭРМ в окне витреотома и подтягивание ЭРМ вверх, затем снижали уровень вакуума до нуля и снова перемещали наконечник витреотома вдоль ОХВ и в ПХВ вперед, пока не был сформирован тоннель длиной 5 мм; подводили наконечник витреотома под наружную границу тоннеля, окно наконечника витреотома приводили в соприкосновение с верхней стенкой тоннеля, затем в режиме резания наконечник витреотома продвигали вдоль тоннеля в ЭРМ, разделяя ЭРМ на 2 равных лоскута, край каждого из лоскутов ЭРМ затем отгибали витреотомом на угол 30 градусов относительно поверхности сетчатки, на режиме вакуума 300 мм рт.ст. край лоскута ЭРМ фиксировали наконечником витреотома и осуществляли его подтягивание, отслаивая ЭРМ от поверхности сетчатки, выделенный фрагмент ЭРМ удаляли витреотомом в режиме резания, в аналогичной последовательности удаляли остальные фрагменты ЭРМ.
При контроле через месяц зрение левого глаза 0,01 cyl - 0,75 ax 85=0.2
ВГД 19 мм рт.ст. Офтальмоскопически: сетчатка прилежит, полость стекловидного тела прозрачная.
Использование предлагаемого изобретения в ФГУ МНТК «Микрохирургия глаза им. акад. С.Н.Федорова» позволяет значительно уменьшить травматичность и время операции, амплитуды перепадов ВГД в полости глазного яблока, предотвратить изменения пространственного взаиморасположения сетчатки и эпиретинальных структур, возникающего из-за перепадов ВГД при смене хирургических инструментов и разгерметизации полости глаза; уменьшить необходимость неоднократной перенастройки операционного микроскопа и насадки с линзой, предотвратить интраоперационные осложнения в виде кровотечения, гипотонии, уменьшить объем анестезиологического пособия, риск развития индивидуальных побочных эффектов анестезии у больных, длительно страдающих сахарным диабетом, имеющих тяжелый коморбидный фон, и добиться более быстрой зрительной и социальной реабилитации.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ УДАЛЕНИЯ ЭПИМАКУЛЯРНЫХ МЕМБРАНОПОДОБНЫХ СТРУКТУР В ХИРУРГИИ ПРОЛИФЕРАТИВНОЙ ДИАБЕТИЧЕСКОЙ РЕТИНОПАТИИ | 2011 |
|
RU2451499C1 |
| СПОСОБ УСТРАНЕНИЯ И ПРОФИЛАКТИКИ ИНТРАОПЕРАЦИОННОГО КРОВОТЕЧЕНИЯ В ХИРУРГИИ ПРОЛИФЕРАТИВНОЙ ДИАБЕТИЧЕСКОЙ РЕТИНОПАТИИ | 2011 |
|
RU2452440C1 |
| Способ поэтапной хромовитрэктомии при далекозашедшей стадии пролиферативной диабетической ретинопатии с применением суспензии "Витреоконтраст" | 2017 |
|
RU2662903C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО УДАЛЕНИЯ ЭПИРЕТИНАЛЬНЫХ МЕМБРАН В УСЛОВИЯХ СИЛИКОНОВОЙ ТАМПОНАДЫ | 2009 |
|
RU2405510C1 |
| Способ хирургического лечения идиопатической эпиретинальной мембраны | 2017 |
|
RU2644296C1 |
| Способ хирургического лечения макулярного разрыва с применением аутологичной кондиционированной плазмы | 2023 |
|
RU2816630C1 |
| Способ удаления эпиретинального фиброза при наличии адгезии в внутренней пограничной мембране | 2024 |
|
RU2838939C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ С НАЧАЛЬНЫМИ ПРИЗНАКАМИ ЭПИРЕТИНАЛЬНОЙ МЕМБРАНЫ | 2015 |
|
RU2571710C1 |
| Способ пилинга внутренней пограничной мембраны (ВПМ) сетчатки | 2020 |
|
RU2751284C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПАЦИЕНТОВ С ПРОЛИФЕРАТИВНОЙ ВИТРЕОРЕТИНОПАТИЕЙ НА ФОНЕ САХАРНОГО ДИАБЕТА | 2017 |
|
RU2675463C1 |
Изобретение относится к области офтальмологии и может быть использовано для лечения пролиферативной диабетической ретинопатии. Устанавливают порты, вводят световод, проводят витрэктомию, отслаивают участка эпиретинальной мембраны (ЭРМ), отгибают его, разрезают витреотомом. При этом совмещают продольную ось порта для витреотома с направлением на край ЭРМ, образуя ось хирургического воздействия (ОХВ), совмещают продольную ось витреотома с линией продольной симметрии ЭРМ, образуя плоскость хирургического воздействия (ПХВ). Подводят под ретинальную поверхность ЭРМ наружную поверхность наконечника витреотома, осуществляют асинхронные колебательные движения вокруг центра колебаний с соотношением положительной амплитуды к отрицательной в интервале от 1,5 до 1,0; центр колебательного движения перемещают вдоль наружной криволинейной поверхности ЭРМ, за каждый этап дискретного движения наконечник витреотома перемещают вдоль ОХВ и в ПХВ вперед на 2-3 мм, затем назад на 1-2 мм; причем наконечник витреотома продвигают по ретинальной поверхности ЭРМ к противоположному краю ЭРМ, увеличивая площадь отслаиваемой ретинальной поверхности ЭРМ, начиная формирование прямолинейного тоннеля; в режиме вакуума 200-300 мм рт.ст. осуществляют фиксацию верхней стенки тоннеля ЭРМ в окне витреотома и подтягивание ЭРМ вверх, затем снижают уровень вакуума до нуля и снова перемещают наконечник витреотома вдоль ОХВ и в ПХВ вперед до формирования тоннеля длиной 4-5 мм; подводят наконечник витреотома под наружную границу тоннеля, окно наконечника витреотома приводят в соприкосновение с верхней стенкой тоннеля, затем в режиме резания наконечник витреотома продвигают вдоль тоннеля в ЭРМ, разделяя ЭРМ на два равных лоскута, край каждого из лоскутов ЭРМ отгибают витреотомом на угол 20-30 градусов относительно поверхности сетчатки, на режиме вакуума 200-300 мм рт.ст. край каждого лоскута ЭРМ фиксируют наконечником витреотома и осуществляют его подтягивание, отслаивая ЭРМ от поверхности сетчатки, отслоенный фрагмент ЭРМ удаляют витреотомом в режиме резания, в аналогичной последовательности удаляют остальные фрагменты ЭРМ. Способ позволяет достичь одновременного уменьшения травматичности операции, амплитуды перепадов ВГД в полости глазного яблока, предотвращения изменений пространственного взаиморасположения сетчатки и эпиретинальных структур, возникающего из-за перепадов ВГД при смене хирургических инструментов и разгерметизации полости глаза. 2 пр., 2 ил.
Способ лечения пролиферативной диабетической ретинопатии, заключающийся в установке портов, введении световода и инструментов, проведении витрэктомии, отслаивании участка эпиретинальной мембраны (ЭРМ), отгибании его, разрезании и удалении его витреотомом, отличающийся тем, что совмещают продольную ось порта для витреотома с направлением на край ЭРМ, образуя ось хирургического воздействия (ОХВ), совмещают продольную ось витреотома с линией продольной симметрии ЭРМ, образуя плоскость хирургического воздействия (ПХВ), подводят под ретинальную поверхность ЭРМ наружную поверхность наконечника витреотома, осуществляют асинхронные колебательные движения вокруг центра колебаний с отношением положительной амплитуды к отрицательной в интервале от 1,5 до 1,0; центр колебательного движения перемещают вдоль наружной криволинейной поверхности ЭРМ, за каждый этап дискретного движения наконечник витреотома перемещают вдоль ОХВ и в ПХВ вперед на 2-3 мм, затем назад на 1-2 мм; причем наконечник витреотома продвигают по ретинальной поверхности ЭРМ к противоположному краю ЭРМ, увеличивая площадь отслаиваемой ретинальной поверхности ЭРМ, начинают таким образом формирование прямолинейного тоннеля; в режиме вакуума 200-300 мм рт.ст. осуществляют фиксацию верхней стенки тоннеля ЭРМ в окне витреотома и подтягивание ЭРМ вверх, затем снижают уровень вакуума до нуля и снова перемещают наконечник витреотома вдоль ОХВ и в ПХВ вперед до формирования тоннеля длиной 4-5 мм; подводят наконечник витреотома под наружную границу тоннеля, окно наконечника витреотома приводят в соприкосновение с верхней стенкой тоннеля, затем в режиме резания наконечник витреотома продвигают вдоль тоннеля в ЭРМ, разделяя ЭРМ на два равных лоскута, край каждого из лоскутов ЭРМ отгибают витреотомом на угол 20-30° относительно поверхности сетчатки, на режиме вакуума 200-300 мм рт.ст. край каждого лоскута ЭРМ фиксируют наконечником витреотома и осуществляют его подтягивание, отслаивая ЭРМ от поверхности сетчатки, отслоенный фрагмент ЭРМ удаляют витреотомом в режиме резания, в аналогичной последовательности удаляют остальные фрагменты ЭРМ.
| DANIEL A | |||
| et al | |||
| Retinal detachment - principles and practice// Oxford university press | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| СПОСОБ ХИРУРГИЧЕСКОГО УДАЛЕНИЯ ЭПИРЕТИНАЛЬНЫХ МЕМБРАН В УСЛОВИЯХ СИЛИКОНОВОЙ ТАМПОНАДЫ | 2009 |
|
RU2405510C1 |
| СПОСОБ УДАЛЕНИЯ ЭПИРЕТИНАЛЬНОЙ МЕМБРАНЫ | 2007 |
|
RU2335269C1 |
| ШАРАФЕТДИНОВ И.Х | |||
| и др | |||
| Хирургическое лечение эпимакулярных фиброзов в условиях силиконовой тампонады / Сб | |||
| научных статей науч.-практ | |||
| конф | |||
| современной технологии лечения витреоретинальной | |||
Авторы
Даты
2012-05-27—Публикация
2011-03-01—Подача