Текст описания приведен в факсимильном виде.















































































| название | год | авторы | номер документа |
|---|---|---|---|
| ТЕРАПЕВТИЧЕСКИЕ DLL4-СВЯЗЫВАЮЩИЕ БЕЛКИ | 2010 |
|
RU2570639C2 |
| АНТИТЕЛО ПРОТИВ cMet И ЕГО ПРИМЕНЕНИЕ ДЛЯ ОПРЕДЕЛЕНИЯ И ДИАГНОСТИКИ РАКА | 2010 |
|
RU2582265C2 |
| АНТИТЕЛА ПРОТИВ VEGF И ИХ ПРИМЕНЕНИЯ | 2010 |
|
RU2567639C2 |
| АНТИТЕЛА К CXCR4 И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ РАКА | 2009 |
|
RU2573897C2 |
| НОВОЕ АНТИТЕЛО ДЛЯ ДИАГНОСТИКИ И (ИЛИ) ПРОГНОЗИРОВАНИЯ РАКА | 2011 |
|
RU2651513C2 |
| АНТИ-TIGIT АНТИГЕНСВЯЗЫВАЮЩИЕ БЕЛКИ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2729379C1 |
| НОВЫЕ АНТИТЕЛА, ИНГИБИРУЮЩИЕ ДИМЕРИЗАЦИЮ С-МЕТ, И ИХ ПРИМЕНЕНИЯ | 2008 |
|
RU2552161C2 |
| АНТИТЕЛО ПРОТИВ MUC1 | 2019 |
|
RU2792347C2 |
| АНТИ-αvβ8 АНТИТЕЛА И КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2812478C2 |
| НОВОЕ АНТИТЕЛО К CXCR4 И ЕГО ПРИМЕНЕНИЕ ДЛЯ ВЫЯВЛЕНИЯ И ДИАГНОСТИКИ РАКА | 2012 |
|
RU2636345C2 |


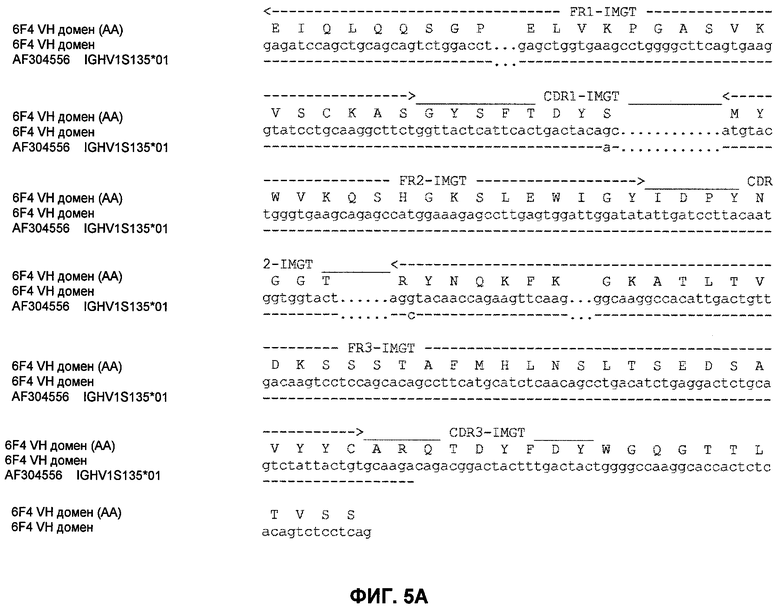
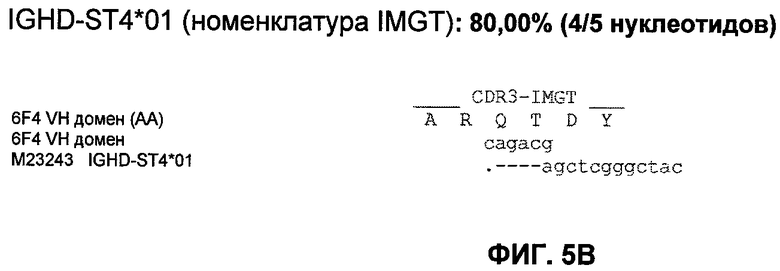
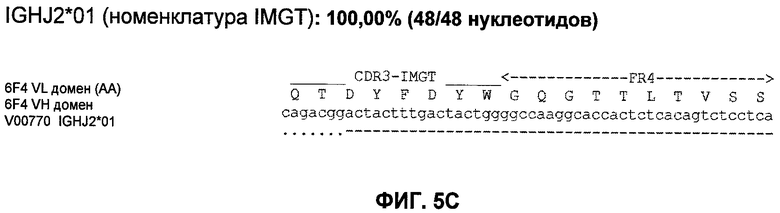
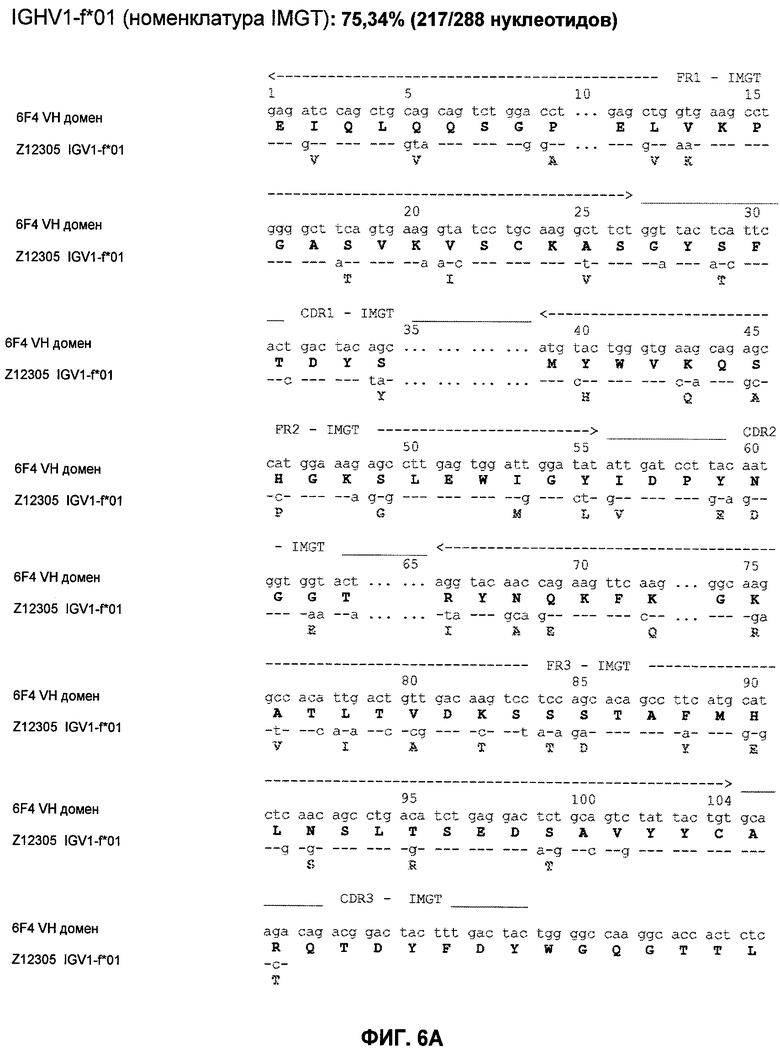
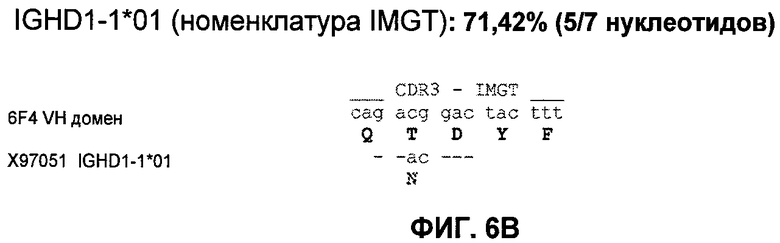
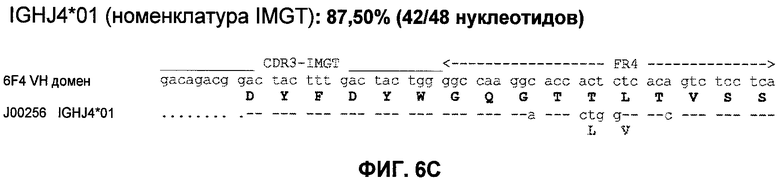

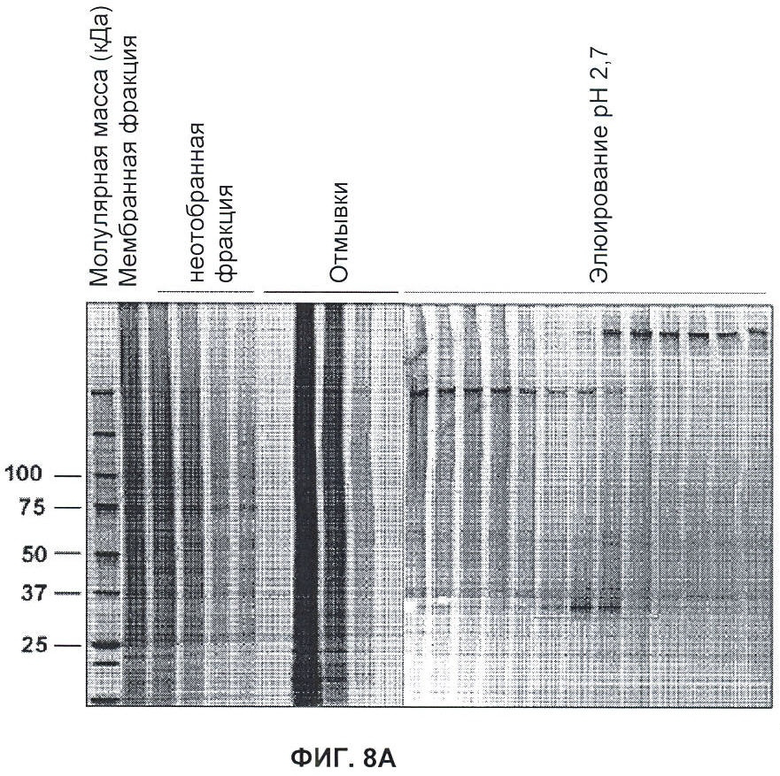
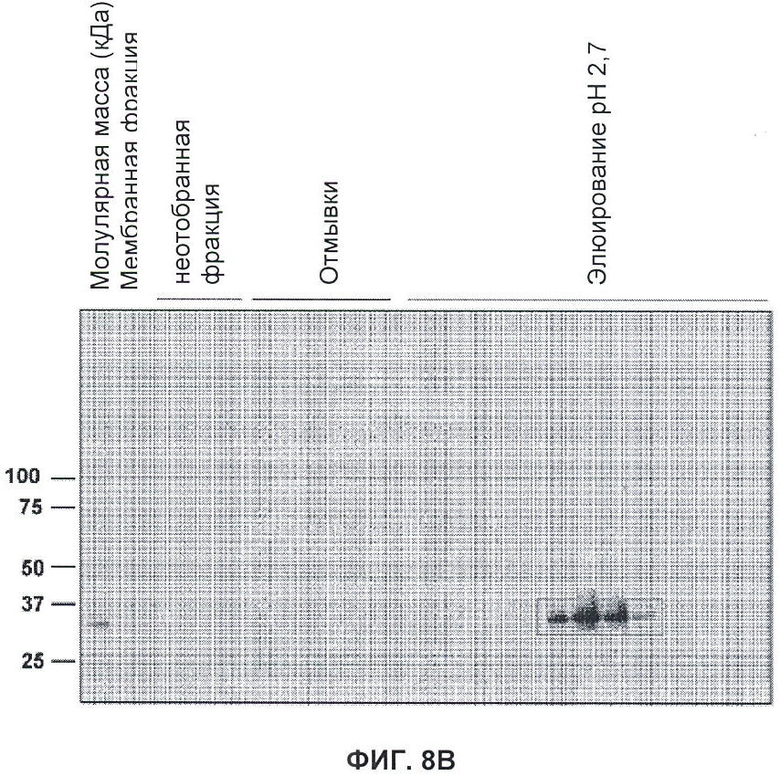

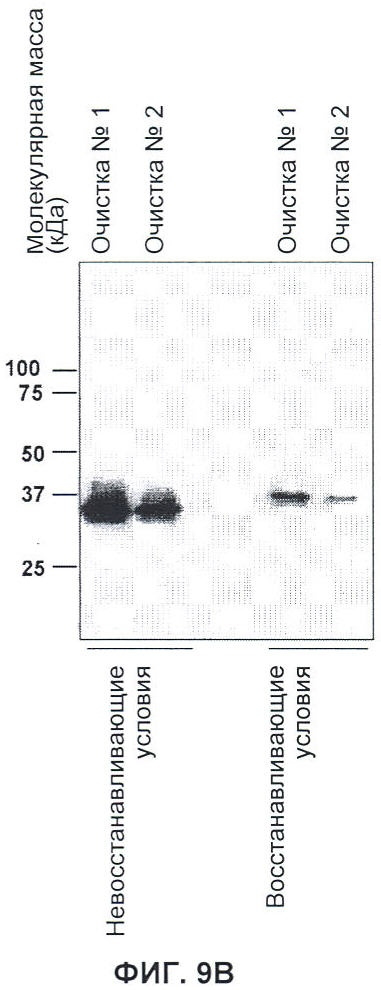
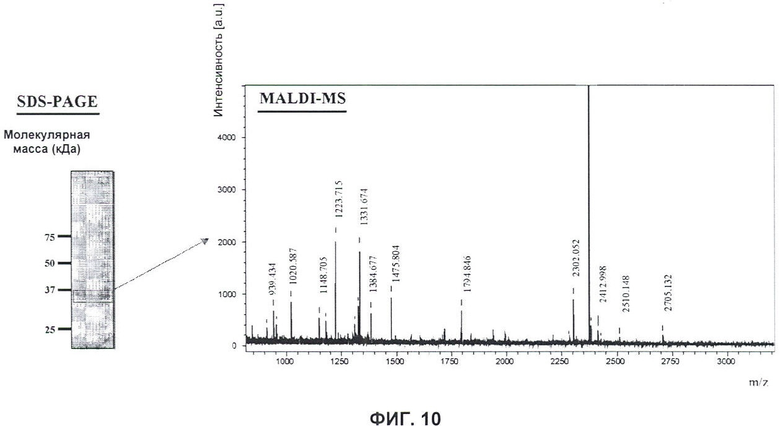
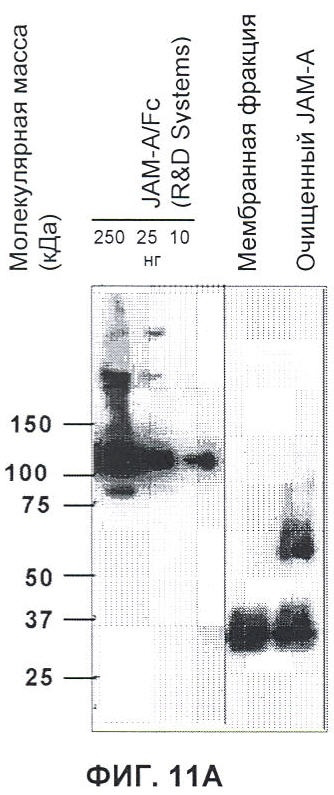
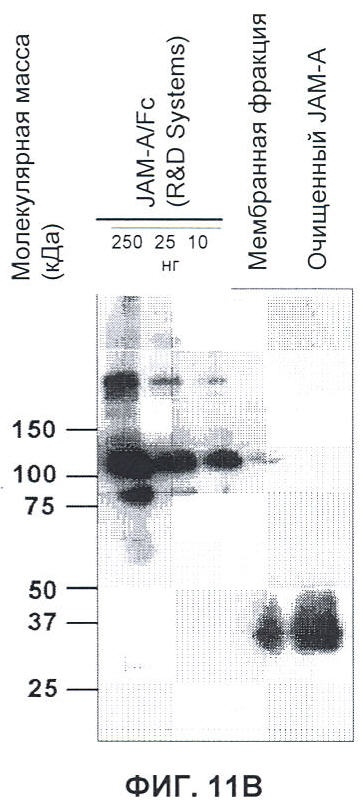
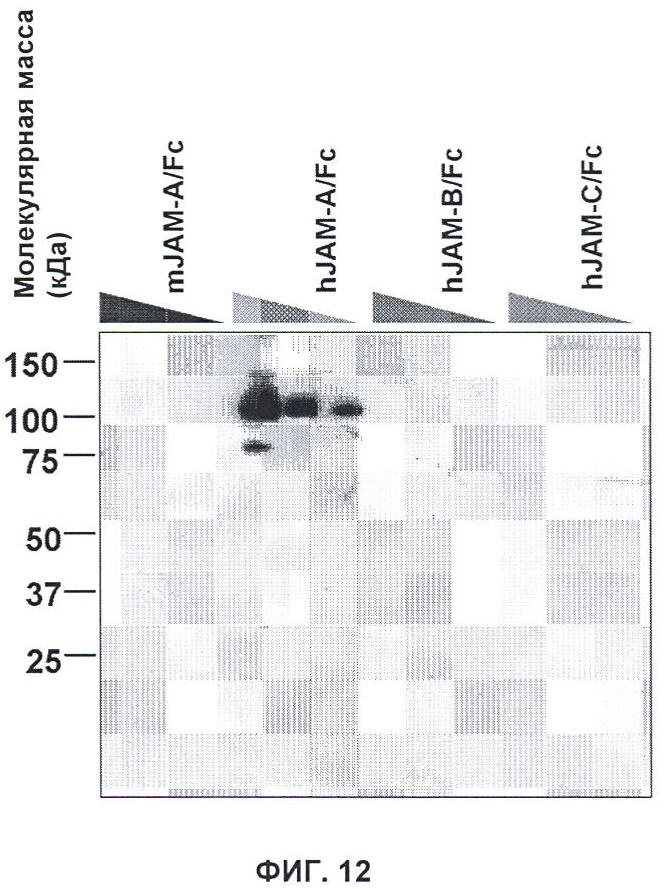
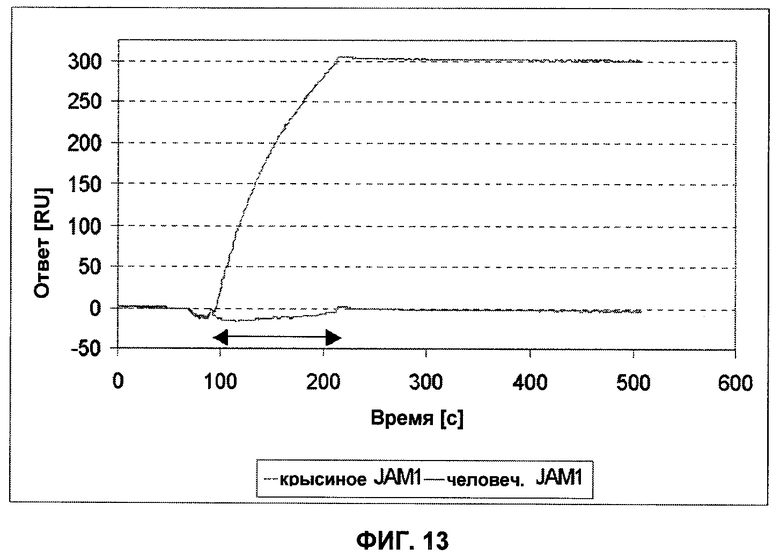
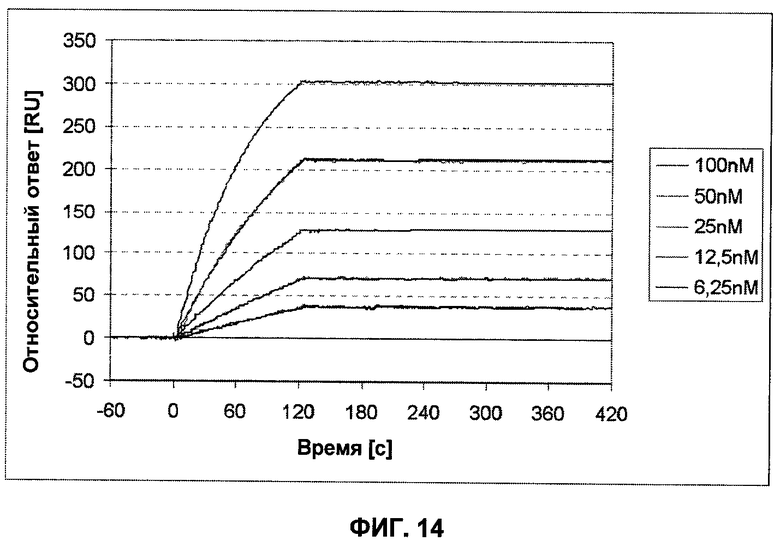
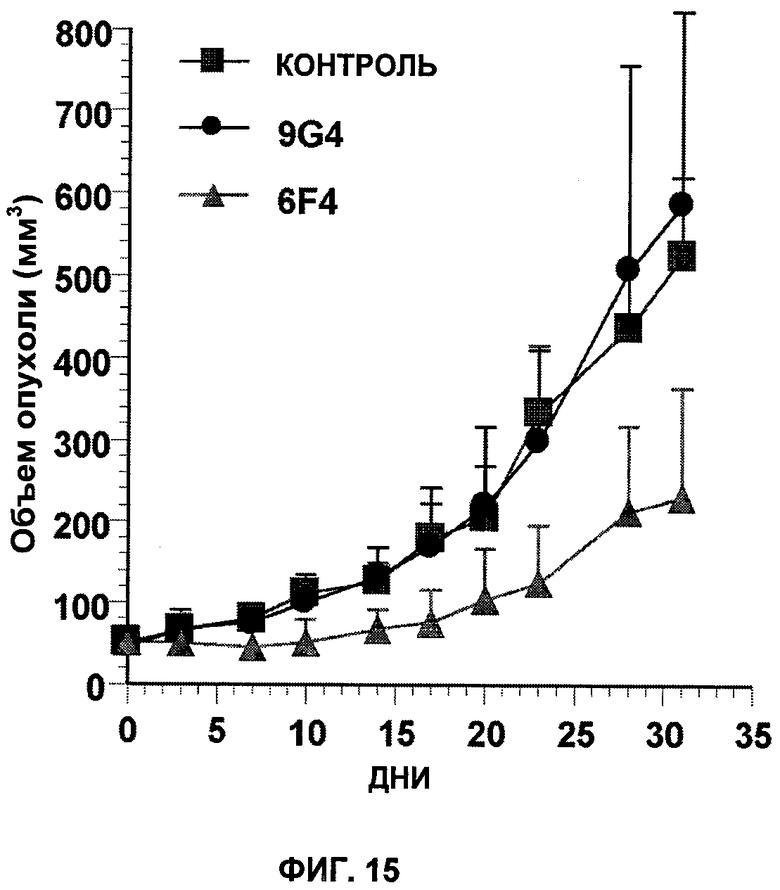


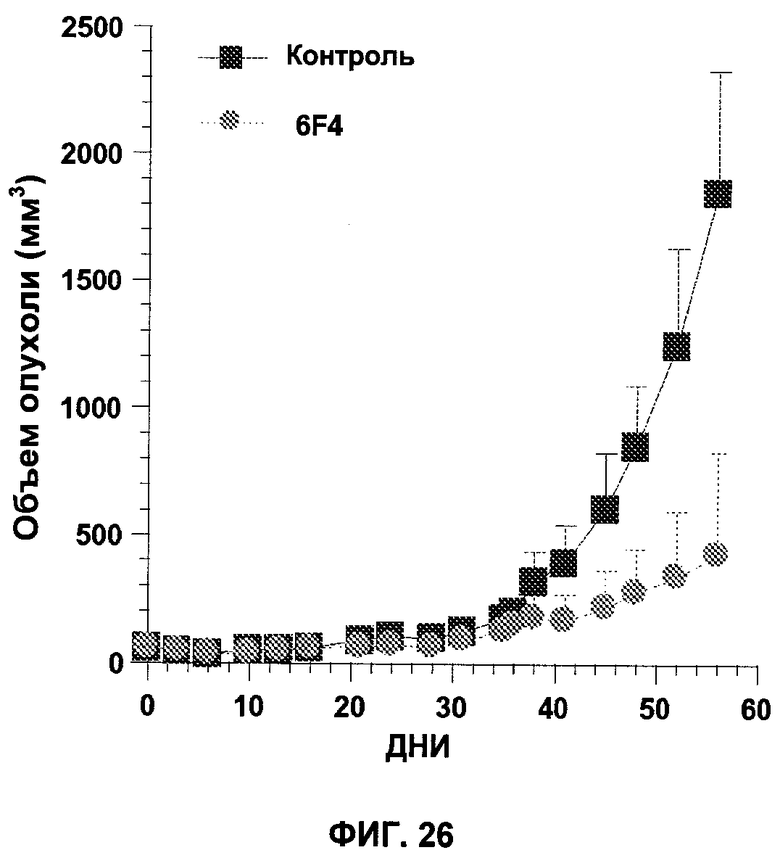
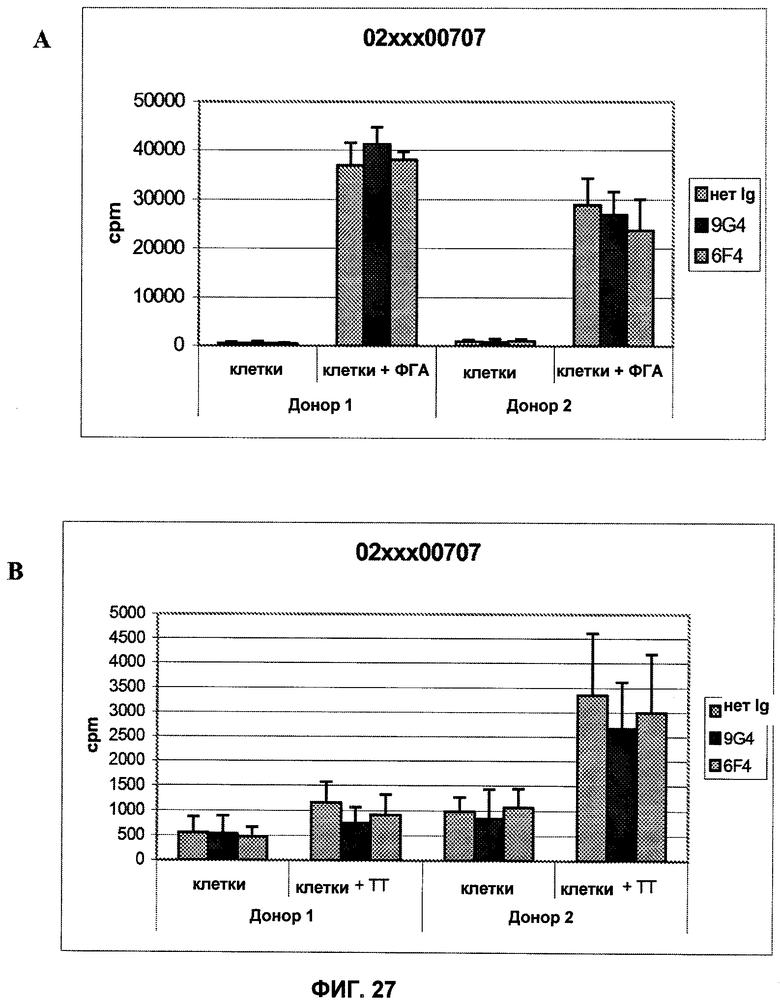
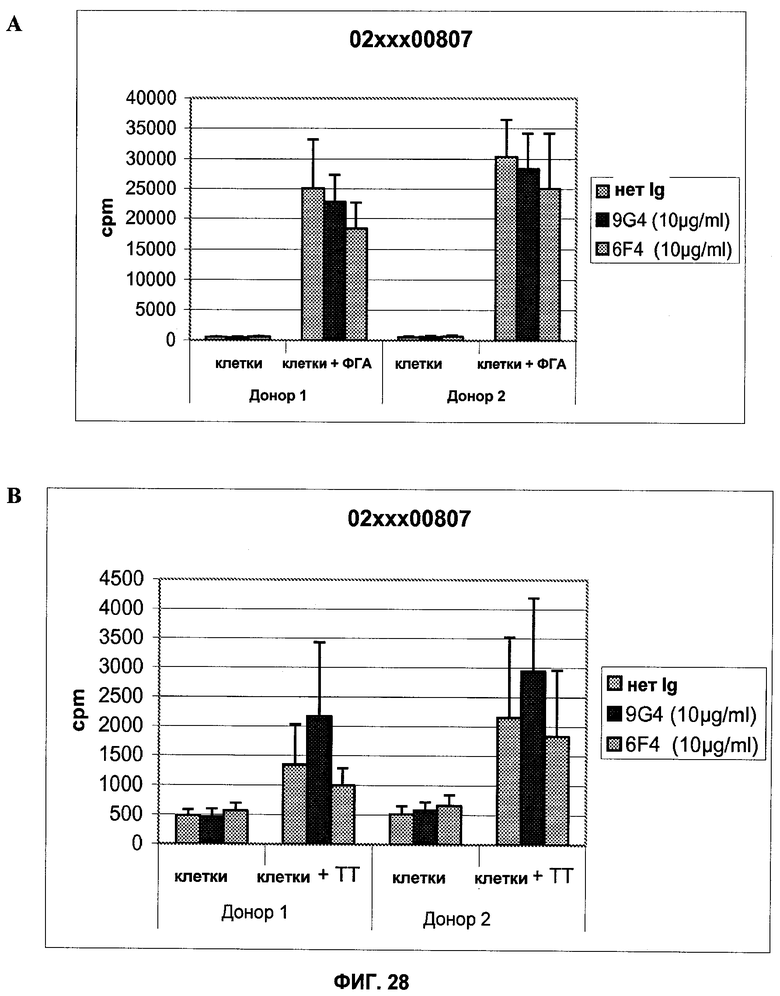
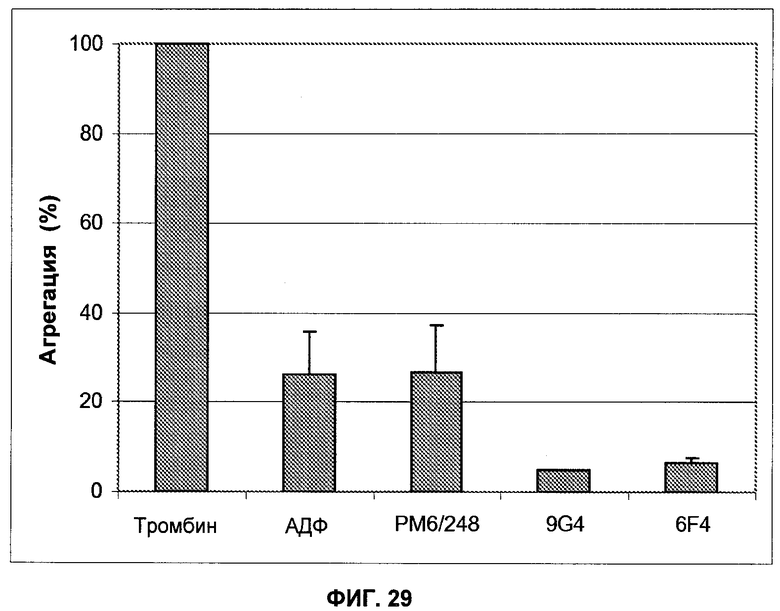

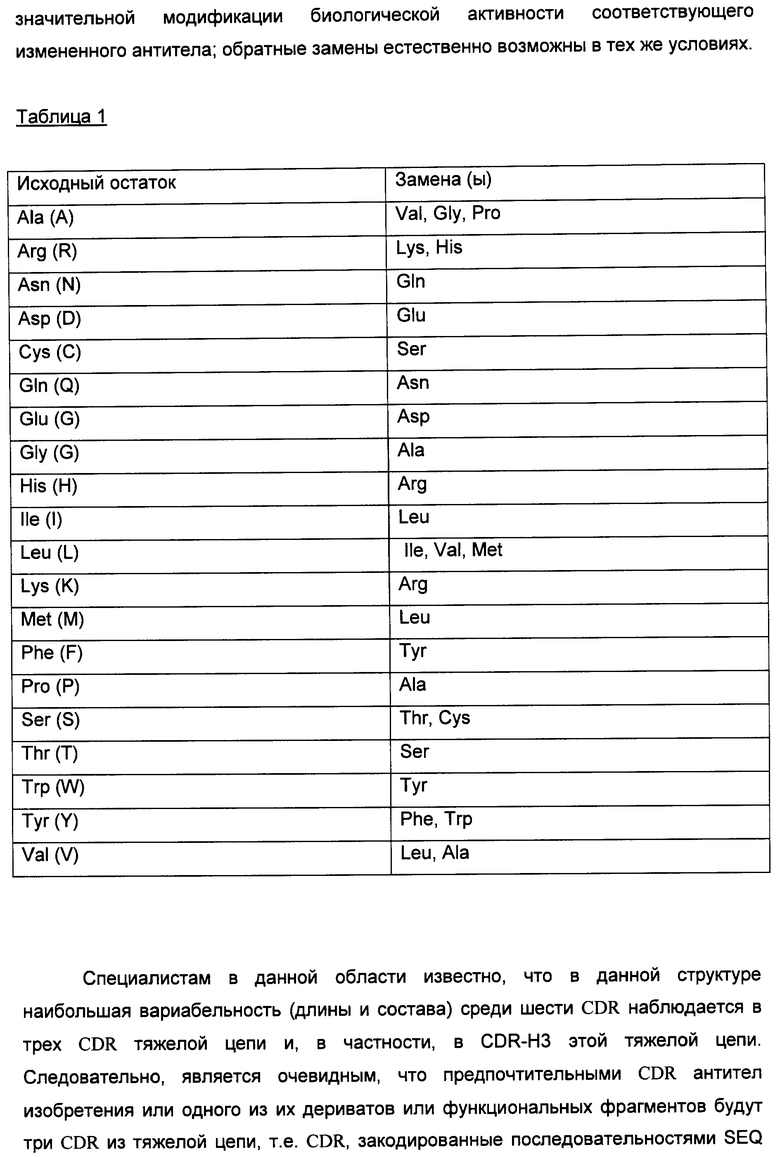
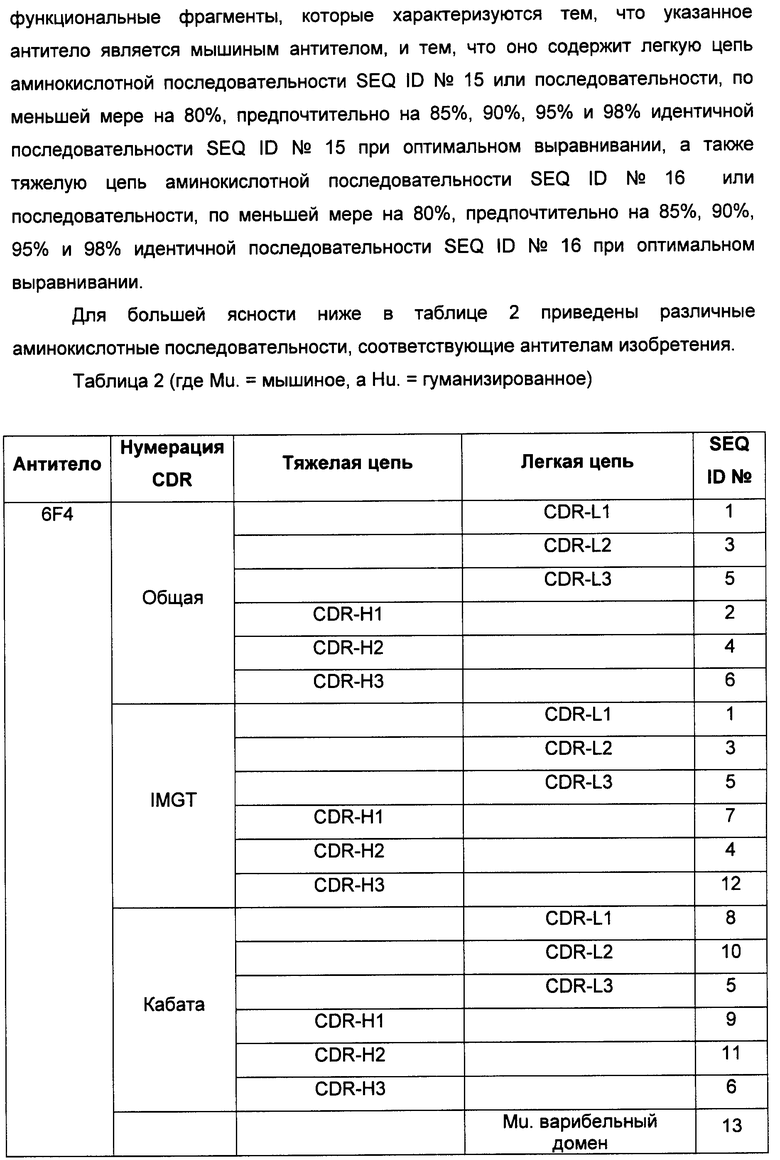
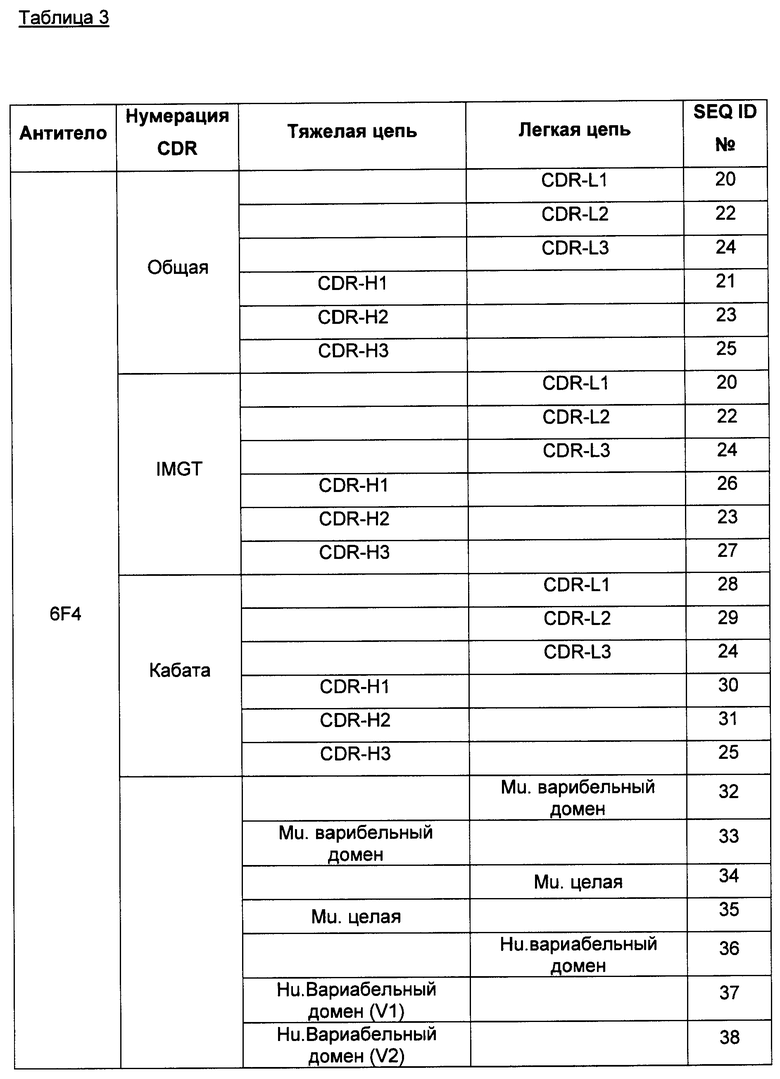
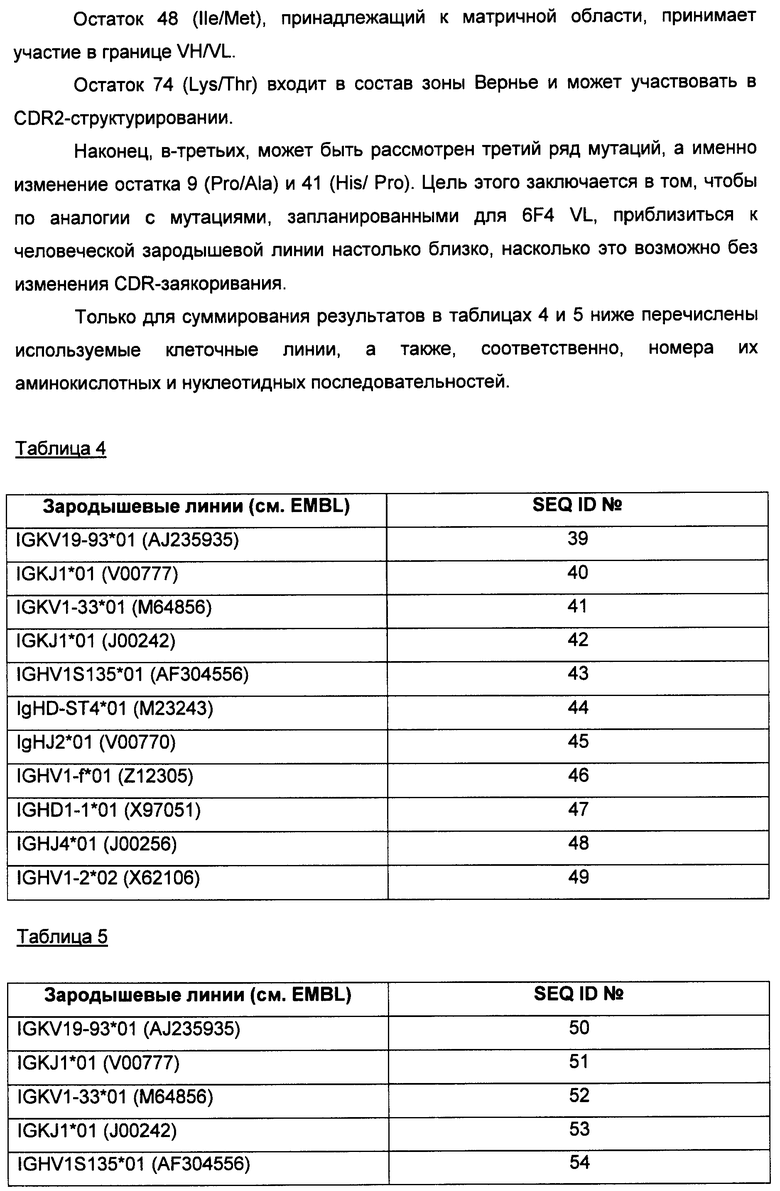
Настоящее изобретение относится к области иммунологии и биотехнологии. Предложены: антитело или его функциональный фрагмент к белку JAM-A, гибридома, секретирующая его, нуклеиновая кислота, вектор экспрессии и клетка-хозяин, способ получения антитела и композиция. Рассмотрено применение антитела или его функционального фрагмента к белку JAM-A. Использование изобретения обеспечивает новые антитела к белку JAM-A, что может найти дальнейшее применение в лечении или профилактике заболеваний, связанных с пролиферацией опухолевых клеток, экспрессирующих белок JAM-A. 9 н. и 25 з.п. ф-лы, 31 ил., 5 табл., 19 пр.
1. Изолированное антитело или его функциональный фрагмент, способное ингибировать пролиферацию опухолевых клеток, экспрессирующих JAM-А, in vitro и/или in vivo, которое характеризуется тем, что содержит CDR, имеющие последовательности SEQ ID №1, 2, 3, 4, 5 и 6.
2. Антитело или его функциональный фрагмент по п.1, характеризующееся тем, что оно представляет собой моноклональное антитело.
3. Антитело или его функциональный фрагмент по п.1, характеризующееся тем, что оно содержит тяжелую цепь, содержащую следующие три CDR, соответственно CDR-H1, CDR-H2 и CDR-H3, где:
CDR-H1 содержит последовательность SEQ ID №2, 7 или 9;
CDR-H2 содержит последовательности SEQ ID №4 или 11; и
CDR-H3 содержит последовательности SEQ ID №6 или 12.
4. Антитело или его функциональный фрагмент по п.1, характеризующееся тем, что оно содержит тяжелую цепь, содержащую CDR-H1 последовательности SEQ ID №7, CDR-H2 последовательности SEQ ID №4 и CDR-H3 последовательности SEQ ID №12.
5. Антитело или его функциональный фрагмент по п.1, характеризующееся тем, что оно содержит тяжелую цепь, содержащую CDR-H1 последовательности SEQ ID №9, CDR-H2 последовательности SEQ ID №11 и CDR-H3 последовательности SEQ ID №6.
6. Антитело или его функциональный фрагмент по п.1, характеризующееся тем, что оно содержит легкую цепь, содержащую следующие три CDR, соответственно CDR- L1, CDR-L2 и CDR-L3, где:
CDR-L1 содержит последовательность SEQ ID №1 или 8;
CDR-L2 содержит последовательность SEQ ID №3 или 10; и
CDR-L3 содержит последовательность SEQ ID №5.
7. Антитело или его функциональный фрагмент по п.1, характеризующееся тем, что оно содержит легкую цепь, содержащую CDR-L1 последовательности SEQ ID №1, CDR-L2 последовательности SEQ ID №3 и CDR-L3 последовательности SEQ ID №5.
8. Антитело или его функциональный фрагмент по п.1, характеризующееся тем, что оно содержит легкую цепь, содержащую CDR-L1 последовательности SEQ ID №8, CDR-L2 последовательности SEQ ID №10 и CDR-L3 последовательности SEQ ID №5.
9. Антитело или его функциональный фрагмент по п.1, характеризующееся тем, что оно содержит легкую цепь, содержащую следующие три CDR:
CDR-L1 последовательности SEQ ID №1;
CDR-L2 последовательности SEQ ID №3; и
CDR-L3 последовательности SEQ ID №5, а также тяжелую цепь, содержащую следующие три CDR:
CDR-H1 последовательности SEQ ID №7;
CDR-H2 последовательности SEQ ID №4; и
CDR-H3 последовательности SEQ ID №12.
10. Антитело или его функциональный фрагмент по п.1, характеризующееся тем, что оно содержит легкую цепь, содержащую следующие три CDR:
CDR-L1 последовательности SEQ ID №8;
CDR-L2 последовательности SEQ ID №10; и
CDR-L3 последовательности SEQ ID №5, а также тяжелую цепь, содержащую следующие три CDR:
CDR-H1 последовательности SEQ ID №9;
CDR-H2 последовательности SEQ ID №11, и
CDR-H3 последовательности SEQ ID №6.
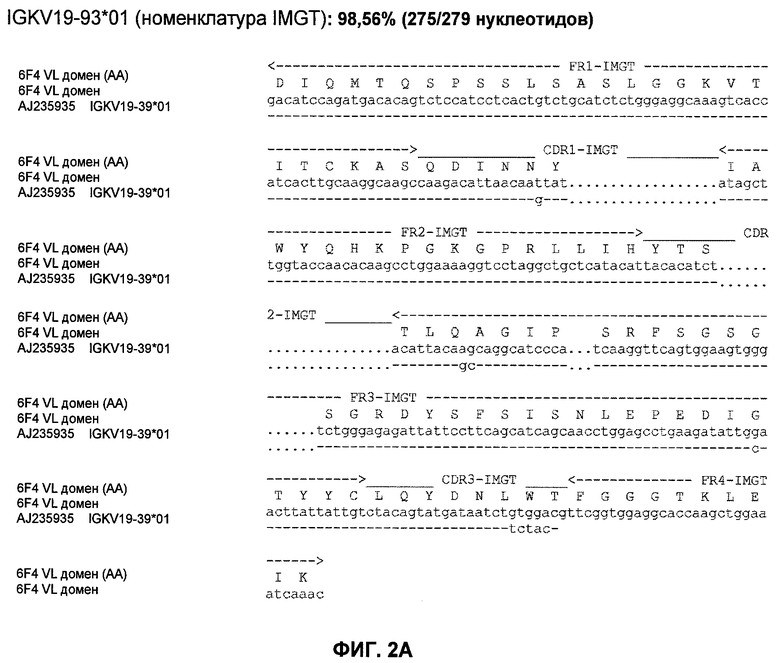
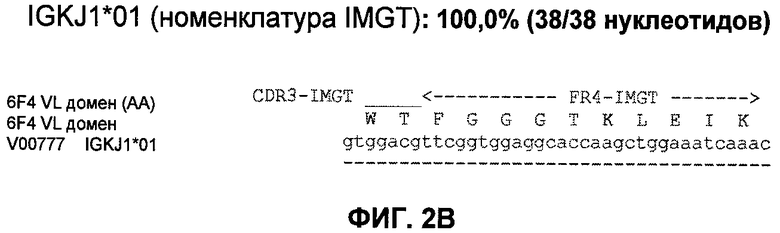
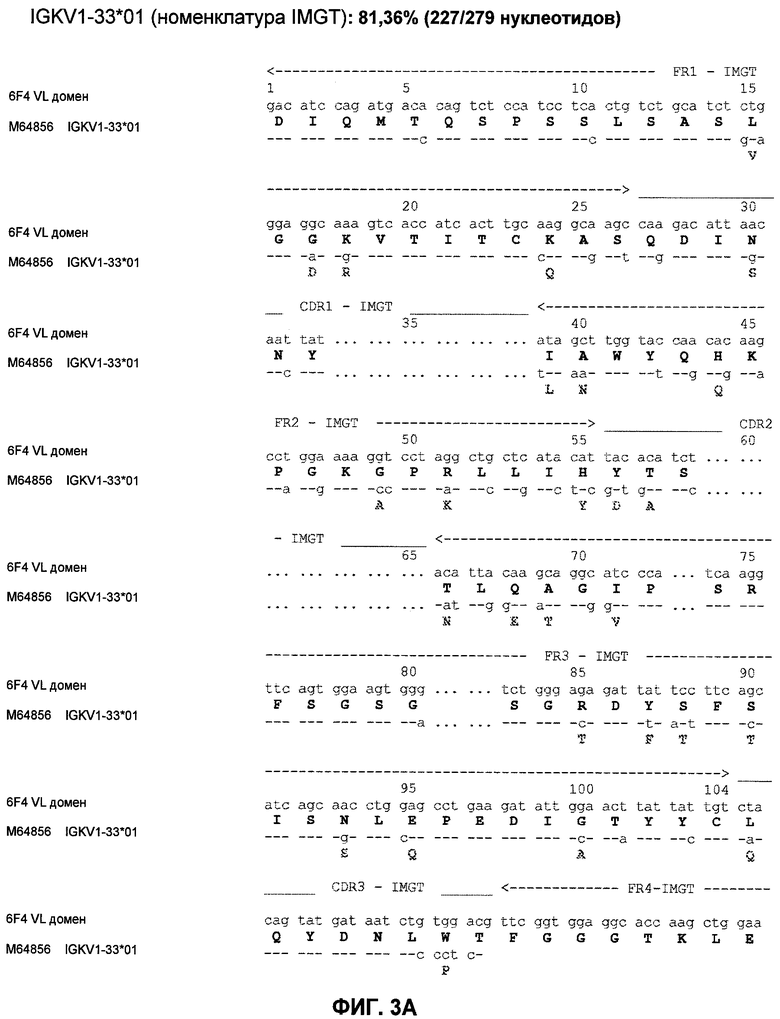
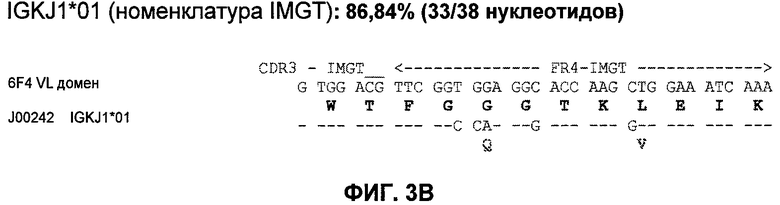
11. Антитело или его функциональный фрагмент по п.1, характеризующееся тем, что оно содержит последовательность вариабельного домена легкой цепи, содержащую аминокислотную последовательность SEQ ID №13, а также тем, что оно содержит последовательность вариабельного домена тяжелой цепи, содержащую аминокислотную последовательность SEQ ID №14.
12. Гуманизированное антитело или его функциональный фрагмент по п.1, характеризующееся тем, что оно содержит последовательность вариабельного домена легкой цепи, содержащую аминокислотную последовательность SEQ ID №17, а также тем, что оно содержит последовательность вариабельного домена тяжелой цепи, содержащую аминокислотную последовательность SEQ ID №18 или 19.
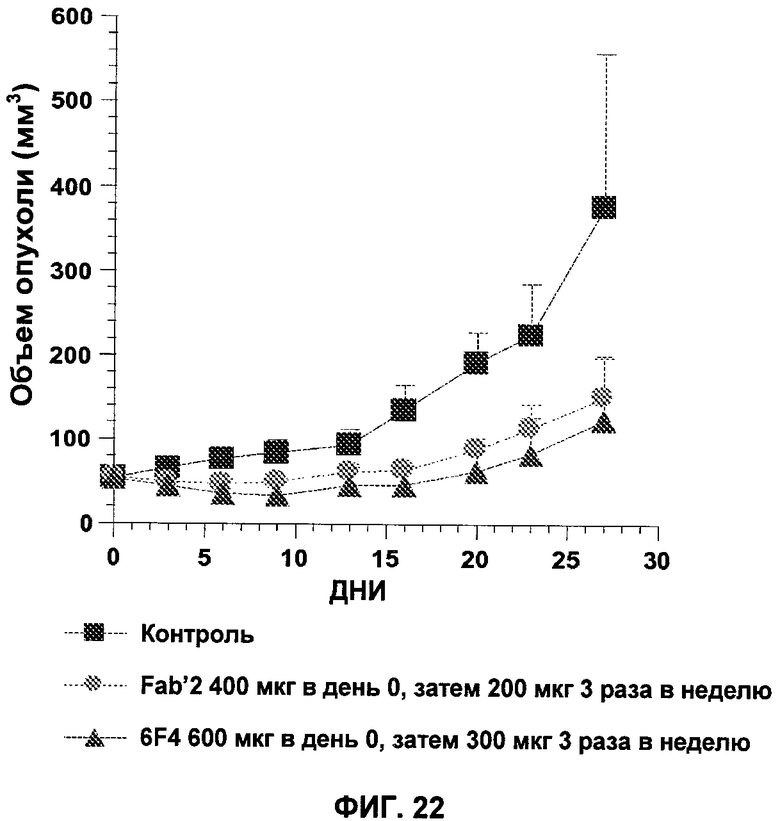
13. Антитело или его функциональный фрагмент по п.1, характеризующееся тем, что указанный функциональный фрагмент выбран среди фрагментов Fv, Fab, (Fab')2, Fab', scFv, scFv-Fc и димерных антител или любого фрагмента, время полужизни которого увеличено, такого как ПЭГилированные фрагменты.
14. Антитело или его функциональный фрагмент по п.1, характеризующееся тем, что указанное антитело является мышиным антителом, и тем, что оно содержит легкую цепь аминокислотной последовательности SEQ ID №15, а также тяжелую цепь аминокислотной последовательности SEQ ID №16.
15. Антитело или его функциональный фрагмент по п.1, характеризующееся тем, что указанное антитело является химерным антителом, которое содержит константные области легкой цепи и тяжелой цепи, полученные из антитела от вида, гетерологичного мыши.
16. Химерное антитело или его функциональный фрагмент по п.15, характеризующееся тем, что указанный гетерологичный вид является человеком.
17. Гуманизированное антитело или его функциональный фрагмент по п.16, характеризующееся тем, что константные области легкой цепи и тяжелой цепи, полученные из человеческого антитела, являются лямбда- или каппа- и гамма-1, гамма-2 или гамма-4 областями соответственно.
18. Мышиная гибридома, секретирующая антитело по п.1, зарегистрированная в Национальной коллекции культур микроорганизмов (CNCM, Институт Пастера, Париж, Франция) под номером I-3646.
19. Антитело, способное ингибировать пролиферацию опухолевых клеток, экспрессирующих JAM-A, in vitro и/или in vivo, которое характеризуется тем, что содержит CDR, имеющие последовательности SEQ ID №1, 2, 3, 4, 5 и 6, секретируемое гибридомой по п.18.
20. Антитело или его функциональный фрагмент по любому из пп.1-19 или 21, характеризующееся тем, что оно может специфично связываться с белком JAM-A (соединительной адгезионной молекулой-А).
21. Антитело или его функциональный фрагмент по п.20, характеризующееся тем, что Kd для белка JAM-A составляет от примерно 1 нМ до 1 пМ, более предпочтительно от 10 пМ до 40 пМ.
22. Изолированная нуклеиновая кислота, характеризующаяся тем, что она выбрана среди следующих нуклеиновых кислот:
a) нуклеиновой кислоты, ДНК или РНК, кодирующей антитело или его функциональный фрагмент по одному из пп.1-17 и 19-21; и
b) нуклеиновой кислоты, комплементарной нуклеиновой кислоте, определенной в пункте а).
23. Вектор экспрессии для экспрессии антитела по п.1, содержащий нуклеиновую кислоту по п.22.
24. Клетка-хозяин, содержащая вектор по п.23.
25. Способ получения антитела или его функционального фрагмента по одному из пп.1-17 и 19-21, характеризующийся наличием следующих этапов:
a) культивирование в среде и в культуральных условиях, подходящих для клетки-хозяина по п.24; и
b) выделение полученного таким образом указанного антитела или одного из его функциональных фрагментов из культуральной среды или из указанных культивируемых клеток.
26. Антитело или его функциональный фрагмент по одному из пп.1-17 и 19-21 для применения в качестве противоопухолевого лекарства.
27. Композиция, способная ингибировать пролиферацию опухолевых клеток, экспрессирующих JAM-A, содержащая в качестве активного ингредиента соединение, состоящее из антитела или его функционального фрагмента по одному из пп.1-17, 19-21 и 26 в эффективном количестве.
28. Композиция по п.27, характеризующаяся тем, что она как комбинированный продукт для применения в одновременной, раздельной или отсроченной форме также содержит противоопухолевое антитело иное, чем антитело, направленное против белка JAM-A.
29. Композиция по п.27, характеризующаяся тем, что она как комбинированный продукт для применения в одновременной, раздельной или отсроченной форме также содержит цитотоксический/цитостатический агент.
30. Композиция по одному из пп.27-29 для применения в качестве лекарства.
31. Применение антитела или его функционального фрагмента по одному из пп.1-17, 19-21 и 27, и/или композиции по любому из пп.28-33 для изготовления лекарства для профилактики или лечения заболевания, связанного с пролиферацией опухолевых клеток, экспрессирующих JAM-А.
32. Применение по п.31 для изготовления лекарства для профилактики или лечения рака.
33. Применение по п.32, характеризующееся тем, что указанный рак является раком, выбранным среди рака простаты, остеосаркомы, рака легких, рака молочной железы, рака эндометрия, множественной миеломы, рака яичников, рака поджелудочной железы и рака толстой кишки.
34. Применение по п.33, характеризующееся тем, что указанный рак является раком, выбранным среди эстроген-зависимого рака молочной железы, немелкоклеточного рака легкого, рака толстой кишки и рака поджелудочной железы.
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| BAZZONI G | |||
| et al | |||
| Homophilic Interaction of Junctional Adhesion Molecule, J | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| NAIK M.U | |||
| and NAIK U.P | |||
| Junctional adhesion molecule-A-induced endothelial cell migration on vitronectin is integrin αβ | |||
Авторы
Даты
2012-05-27—Публикация
2007-11-23—Подача