Настоящее изобретение относится к способу получения замещенных орто-хлорбромбензолов, применимых в качестве промежуточных продуктов при получении сельскохозяйственных химикатов, таких как фунгициды и/или гербициды.
1-Бром-2,3-дихлорбензол и 2-бром-1,3-дихлорбензол являются ценными промежуточными продуктами для получения бензонорборненовых фунгицидов, таких как (9-изопропил-1,2,3,4-тетрагидро-1,4-метанонафталин-5-ил)-амид 3-дифторметил-1-метил-1Н-пиразол-4-карбоновой кислоты, фунгицид, описанный в WO 04/35589 и WO 06/37632. 9-Изопропил-1,2,3,4-тетрагидро-1,4-метанонафталин-5-иламин можно получить из 1-бром-2,3-дихлорбензола или 2-бром-1,3-дихлорбензола, как описано в публикации ЕРА 05027072,7 в примерах 2b, 2d, 5 и 6b. 9-Изопропил-1,2,3,4-тетрагидро-1,4-метанонафталин-5-иламин можно использовать для получения (9-изопропил-1,2,3,4-тетрагидро-1,4-метанонафталин-5-ил)-амида 3-дифторметил-1-метил-1Н-пиразол-4-карбоновой кислоты путем амидирования 3-дифторметил-1-метил-1Н-пиразол-4-карбоновой кислоты, как описано в WO 04/35589.
Бром-2-хлор-4-фторбензол является ценным промежуточным продуктом для получения гербицидов, как описано в JP-6-2114-921.
Сельскохозяйственные химикаты обычно выпускают в больших количествах. Например, фунгицид хлороталонил выпускали в 2005 г. в количестве, составляющем более 23000 метрических тонн и гербицид атразин - в количестве, составляющем более 68000 метрических тонн.
Опубликованы несколько методик получения замещенных орто-хлорбромбензолов. Указанные соединения можно получить с помощью так называемой реакции Зандмейера, по которой аминогруппа замещается бромом через соль диазония (как описано в публикации Recueil des Travaux Chimiques des Pays-Bas et de la Belgique, 1932, 51, 98-113; JP-6-2114-921 и Journal of Organic Chemistry (1977), 42 (14), 2426-31) или путем прямого бромирования ароматических соединений, при котором атом водорода замещается бромом (как описано в публикации Recueil des Travaux Chimiques des Pays-Bas, 1962, 81, 365-379).
Реакция Зандмейера для получения замещенных орто-хлорбромбензолов представляет собой двустадийную методику: превращение анилина в соль диазония (диазотирование) с последующей заменой диазогруппы на бром (бромирование). Однако выход этой реакции сильно зависит от положения и природы дополнительных заместителей ароматического кольца и бывает и плохим, и очень хорошим.
Диазотирование замещенных орто-хлоранилинов обычно проводят в кислых реакционных средах при температурах около 0°C с использованием неорганического нитрита для количественного получения солей диазония в качестве промежуточных продуктов. Полученную холодную реакционную смесь медленно прибавляют к водному раствору, обладающему большой концентрацией бромида меди (I). Указанная методика описана в публикациях Recueil des Travaux Chimiques des Pays-Bas et de la Belgique, 1932, 51, 98-113 и JP-6-2114-921. В обоих примерах используют эквимолярное количество бромида меди (I). Хотя выходы искомых замещенных орто-хлорбромбензолов являются хорошими, указанная методика обладает значительными недостатками, делающими ее мало подходящей для крупномасштабного производства. Во-первых, необходимы два реактора для проведения реакций: один для стадии диазотирования и второй для стадии бромирования, это значительно увеличивает производственные расходы. Во-вторых, необходимость использования эквимолярных количеств дорогостоящего бромида меди (I), а также крупномасштабного удаления содержащих медь водных отходов значительно увеличивает производственные расходы. В третьих, эта схема реакций обладает низкой производительностью, поскольку диазотирование обычно необходимо проводить в разбавленных средах. Кроме того, во многих случаях образовавшиеся соли диазония плохо растворимы в водной среде. Поэтому актуальной задачей является использование твердой соли диазония, оставшейся в реакторе для проведения реакции после проведения стадии диазотирования.
Обращенная схема прибавления, т.е. прибавление кислого раствора бромида меди (I) к смеси, содержащей соль диазония, не очень подходит для крупномасштабного производства, поскольку при этом выделяются тепло и газ, что трудно регулировать.
Разработана модифицированная реакция Зандмейера, которая приводит к более простой технологической схеме. В отличие от описанной выше методики, в которой для получения соли диазония необходим неорганический нитрит в кислых водных реакционных средах, в ней можно использовать органический нитрит, такой как трет-бутилнитрит или изопентилнитрит, в качестве мягкого диазотирующего реагента in situ. Указанную реакцию проводят, как однореакторную реакцию с использованием бромида меди (I) в качестве бромирующего реагента и она описана в публикации Doyle et al. in Journal of Organic Chemistry (1977), 42 (14), 2426-31. Хотя в методике, описанной в публикации Doyle et al., стадию диазотирования и стадию бромирования можно проводить в одном реакторе и также необходимо эквимолярное количество бромида меди (I), что приводит к указанным выше недостаткам, кроме того, в методике, описанной в публикации Doyle et al., используют 1,5 экв. органического нитрита; при крупномасштабном производстве такое большое количество органического нитрита приводит к необходимости использования дополнительных мер по обеспечению безопасности и усложняет регенерацию органического растворителя, что приводит к более высоким производственным расходам.
Прямое бромирование ароматических соединений также не вполне подходит для крупномасштабного производства замещенных орто-хлорбромбензолов. При использовании этой методики образуются другие изомеры, являющиеся нежелательными примесями. Если 1-бром-2,3-дихлорбензол получают из орто-дихлорбензола, как описано в публикации Recueil des Travaux Chimiques des Pays-Bas, 1962, 81, 365-379, то основным образующимся изомером является нежелательный 1-бром-3,4-дихлорбензол; искомый продукт, 1-бром-2,3-дихлорбензол, составляет лишь 7% продуктов реакции.
В основу настоящего изобретения была положена задача разработки способа получения замещенных орто-хлорбромбензолов, в котором исключены недостатки известных способов, указанных выше, и который делает возможным получение этих соединений с высокими выходами и высокого качества экономически привлекательным и легким в осуществлении путем.
В соответствии с этим, настоящее изобретение относится к способу получения соединений формулы I
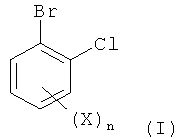
в которой Х обозначает фтор, хлор, бром или йод и n равно 1, 2, 3 или 4, который включает реакцию соединения формулы II
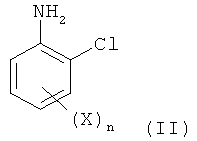
в которой заместители являются такими, как определено для формулы I, с неорганическим нитритом в кислой водной среде в присутствии бромида и содержащего медь катализатора, способ осуществляют в виде однореакторной реакции.
Способ, предлагаемый в настоящем изобретении, является особенно подходящим для получения соединений формулы I, в которой Х обозначает хлор. Способ, предлагаемый в настоящем изобретении, является особенно подходящим для получения соединений формулы I, в которой n равно 1 или 2, более предпочтительно - 1. Способ, предлагаемый в настоящем изобретении, является особенно подходящим для получения соединений формулы I, в которой Х обозначает хлор и n равно 1. Способ, предлагаемый в настоящем изобретении, является особенно подходящим для получения 1-бром-2,3-дихлорбензола или 2-бром-1,3-дихлорбензола.
Неорганические нитриты, подходящие для способа, предлагаемого в настоящем изобретении, являются нитриты щелочных металлов, например натрия нитрит или калия нитрит, нитриты щелочноземельных металлов, например магния нитрит или кальция нитрит или их смеси. Предпочтительными неорганическими нитритами являются нитриты щелочных металлов, наиболее предпочтительным неорганическим нитритом является натрия нитрит.
Количества неорганического нитрита, подходящие для способа, предлагаемого в настоящем изобретении, составляют, например, от 1 до 3 экв., предпочтительно - от 1,0 до 1,5 экв., наиболее предпочтительно - от 1,0 до 1,2 экв.
Подходящими источниками бромида являются бромистоводородная кислота, неорганические бромиды или их смеси. Подходящими неорганическими бромидами являются бромиды щелочных металлов, например бромид натрия или бромид калия, или бромиды щелочноземельных металлов, например бромид магния или бромид кальция; предпочтительными неорганическими бромидами являются бромиды щелочных металлов, наиболее предпочтительным неорганическим бромидом является бромид натрия.
Полные количества бромида, подходящие для способа, предлагаемого в настоящем изобретении, составляют, например, от 2,5 до 8 экв., предпочтительно - от 3 до 6 экв., наиболее предпочтительно - от 3 до 5 экв.
Подходящими содержащими медь катализаторами являются ионы меди (I), ионы меди (II), металлическая медь или их смеси. Подходящими источниками ионов меди (I) являются бромид меди (I) или оксид меди (I); предпочтительным является бромид меди (I). Подходящими источниками ионов меди (II) являются бромид меди (II), сульфат меди (II) или оксид меди (II); предпочтительным является бромид меди (II) или сульфат меди (II). Подходящим источником металлической меди является порошкообразная медь.
В одном варианте осуществления настоящего изобретения ионы меди (I) и/или ионы меди (II) применяют в качестве содержащих медь катализаторов.
В другом варианте осуществления настоящего изобретения ионы меди (I) применяют в качестве содержащего медь катализатора.
В другом варианте осуществления настоящего изобретения ионы меди (II) применяют в качестве содержащего медь катализатора.
В еще одном варианте осуществления настоящего изобретения металлическую медь применяют в качестве содержащего медь катализатора.
Подходящими количествами содержащих медь катализаторов являются, например, от 0,01 до 2 экв., предпочтительно - от 0,05 до 1 экв., более предпочтительно - от 0,05 до 0,5 экв., еще более предпочтительно - от 0,05 до 0,2 экв., наиболее предпочтительно - от 0,05 до 0,1 экв. Более предпочтительный вариант осуществления настоящего изобретения, в котором используют от 0,05 до 0,2 экв. содержащего медь катализатора является особенно подходящим для крупномасштабного производства, поскольку образуются лишь небольшие количества содержащих соли меди отходов.
В контексте настоящего изобретения "водная среда" предпочтительно означает жидкую реакционную среду, в которой основным компонентом является вода. Эдукты, продукты, реагенты или промежуточные продукты можно растворить, суспендировать или эмульгировать в указанной водной среде.
Кислотами, подходящими для применения в способе, предлагаемом в настоящем изобретении, являются неорганические кислоты, в которых анионом является бром или инертный анион, такие как бромистоводородная кислота или серная кислота, органические кислоты, такие как уксусная кислота или их смеси. Предпочтительной кислотой является бромистоводородная кислота.
Количества кислоты, подходящие для способа, предлагаемого в настоящем изобретении, составляют, например, от 1,5 до 5 экв., предпочтительно - от 1,5 до 4,0 экв., наиболее предпочтительно - от 2,6 до 4,0 экв.
Способ, предлагаемый в настоящем изобретении, предпочтительно осуществлять при температуре в диапазоне от 10 до 100°C, более предпочтительно - при температуре в диапазоне от 30 до 100°C, еще более предпочтительно - при температуре в диапазоне от 30 до 100°C, наиболее предпочтительно - при температуре в диапазоне от 35 до 65°C.
В одном варианте осуществления настоящего изобретения после образования продукта реакции реакционную смесь нагревают до температуры, превышающей температуру плавления продукта реакции. Этот вариант осуществления настоящего изобретения можно использовать для получения 1-бром-2,3-дихлорбензола, который обладает температурой плавления, равной около 60°C. При нагревании реакционной смеси после образования 1-бром-2,3-дихлорбензола до 65°C первоначально твердый продукт, находящийся в водной суспензии, превращается в расплавленную жидкость, и его легко отделить путем разделения фаз.
Специалист в данной области техники должен понимать, что искомый замещенный бензол можно экстрагировать из водной реакционной суспензии путем прибавления подходящего не смешивающегося с водой ароматического органического растворителя, такого как толуол, или галогенированного алифатического растворителя, такого как метиленхлорид или хлороформ, или алифатического органического растворителя, предпочтительно - (цикло)алифатического углеводорода, такого как гексан или циклогексан. Затем органическую фазу можно извлечь из реакционной смеси путем разделения фаз и продукт можно выделить путем отгонки органического растворителя.
Длительность проведения реакции в способе, предлагаемом в настоящем изобретении, предпочтительно составляет от 1 до 24 ч, более предпочтительно - от 2 до 16 ч, еще более предпочтительно - от 2 до 5 ч.
В контексте настоящего изобретения "однореакторная реакция" означает, что способ диазотирования и бромирования, предлагаемый в настоящем изобретении, проводят без замены реактора. В одном варианте осуществления настоящего изобретения обработку продукта реакции проводят в дополнительном реакторе, например в реакторе, подходящем для вакуумной перегонки, если продукт реакции очищают с помощью вакуумной перегонки.
Прибавление неорганического нитрита к соединению формулы II в кислой водной среде в присутствии бромида и содержащего медь катализатора приводит к тому, что промежуточный арилдиазоний является короткоживущим и вступает в реакцию in situ с образованием соединения формулы I в том же реакторе без выделения промежуточного арилдиазония.
В одном варианте осуществления настоящего изобретения неорганический нитрит прибавляют к смеси соединения формулы II, бромида и содержащего медь катализатора в кислой водной среде. В частности, в этом варианте осуществления в указанной смеси соединение формулы II, бромид и содержащий медь катализатор содержатся в соответствующих полных количествах, необходимых для использования в способе, предлагаемом в настоящем изобретении.
В этом варианте осуществления особенно предпочтительно, если этот неорганический нитрит прибавляют в виде водного раствора.
В другом варианте осуществления настоящего изобретения неорганический нитрит прибавляют к смеси соединения формулы II в кислой водной среде в виде смеси, содержащей неорганический нитрит, бромид и содержащий медь катализатор.
В еще одном варианте осуществления настоящего изобретения неорганический нитрит прибавляют к смеси соединения формулы II и бромида в кислой водной среде в виде смеси, содержащей неорганический нитрит и содержащий медь катализатор.
В еще одном варианте осуществления настоящего изобретения неорганический нитрит прибавляют к смеси соединения формулы II и содержащего медь катализатора в кислой водной среде в виде смеси, содержащей неорганический нитрит и бромид.
Соединения формулы II являются известными или их можно получить по методикам, аналогичным известным в данной области техники.
Настоящее изобретение иллюстрируется с помощью приведенных ниже примеров.
Пример Р1. Получение 1-бром-2,3-дихлорбензола (соединение А1)
32,7 г 2,3-Дихлоранилина (0,20 моля) прибавляют к смеси 21,4 г NaBr (0,20 моля, 1,0 экв.), 110,0 г 48% водного раствора HBr (0,66 моля, 3,3 экв.) и 70 мл воды при 30-45°C. Смесь перемешивают в течение 15 мин при 30-45°C и затем нагревают до 60°C. Затем прибавляют 2,9 г Cu(I)Br (0,02 моля, 0,10 экв.) и смесь перемешивают в течение 15 мин при 60°C. После этого водный раствор NaNO2 (40% водный раствор, 37,6 г, 0,22 моля, 1,1 экв.) прибавляют путем введения под поверхность в течение 2 ч при 60-65°C. Реакционную смесь перемешивают в течение 30 мин при 60-65°C. Органическую фазу, содержащую продукт реакции, отделяют от водной фазы и охлаждают до температуры окружающей среды, что приводит к затвердеванию продукта реакции. Оставшуюся жидкость отбрасывают и неочищенный продукт дважды промывают с помощью 10 мл воды и сушат в вакууме. Получают 44,0 г (89% от теоретического выхода) 1-бром-2,3-дихлорбензола в виде светло-коричневого твердого вещества (чистота: 91%). Для дополнительного изучения неочищенный продукт очищают с помощью вакуумной перегонки (130°C/20 мм рт.ст.). Получают 38,0 г (84% от теоретического выхода) чистого 1-бром-2,3-дихлорбензола в виде белого кристаллического вещества.
Пример Р2. Получение 1-бром-2,3-дихлорбензола (соединение А1)
32,7 г 2,3-Дихлоранилина (0,20 моля) прибавляют к смеси 168,5 г 48% водного раствора HBr (1,0 моля, 5,0 экв.) и 40 мл воды при 30-40°C. Смесь перемешивают в течение 15 мин при 30-40°C и затем нагревают до 45°C. Затем прибавляют 2,9 г Cu(I)Br (0,02 моля, 0,10 экв.) и смесь перемешивают в течение 15 мин при 45°C. После этого водный раствор NaNO2 (40% водный раствор, 35,6 г, 0,21 моля, 1,0 экв.) прибавляют путем введения под поверхность в течение 2 ч при 45°C. Реакционную смесь перемешивают в течение 30 мин при 45°C. После этого реакционную смесь нагревают до 60-65°C. Органическую фазу, содержащую продукт реакции, отделяют от водной фазы и охлаждают до температуры окружающей среды, что приводит к затвердеванию продукта реакции. Оставшуюся жидкость отбрасывают и неочищенный продукт дважды промывают с помощью 10 мл воды и сушат в вакууме. Получают 40,0 г (80% от теоретического выхода) 1-бром-2,3-дихлорбензола в виде светло-коричневого твердого вещества (чистота: 90%).
Пример Р3. Получение 1-бром-2,3-дихлорбензола (соединение А1)
32,7 г 2,3-Дихлоранилина (0,20 моля) прибавляют к смеси 21,4 г NaBr (0,20 моля, 1,0 экв.), 110,0 г 48% водного раствора HBr (0,66 моля, 3,3 экв.) и 70 мл воды при 30-40°C. Смесь перемешивают в течение 15 мин при 30-40°C и затем нагревают до 45°C. Затем прибавляют 5,1 г CuSO4·5H2O (0,02 моля, 0,10 экв.) и смесь перемешивают в течение 15 мин при 45°C. После этого водный раствор NaNO2 (40% водный раствор, 37,6 г, 0,22 моля, 1,1 экв.) прибавляют путем введения под поверхность в течение 2 ч при 45°C. Реакционную смесь перемешивают в течение 30 мин при 45°C. После этого реакционную смесь нагревают до 60-65°C. Органическую фазу, содержащую продукт реакции, отделяют от водной фазы и охлаждают до температуры окружающей среды, что приводит к затвердеванию продукта реакции. Оставшуюся жидкость отбрасывают и неочищенный продукт дважды промывают с помощью 10 мл воды и сушат в вакууме. Получают 44,0 г (83% от теоретического выхода) 1-бром-2,3-дихлорбензола в виде светло-коричневого твердого вещества (чистота: 85%).
Пример Р4. Получение 1-бром-2,3-дихлорбензола (соединение А1)
163 г 2,3-Дихлоранилина (1,0 моля) прибавляют к смеси 3250 г 30% водного раствора HBr (12,0 моля) и 25,4 г порошкообразной меди с частицами размером примерно 45 мкм при 35-37°C. Смесь перемешивают в течение 15 мин при 35-37°C. Затем 766 г водного раствора NaNO2 (40% водный раствор, 4,44 моля) прибавляют путем введения под поверхность в течение 3 ч при 35°C. Одновременно с прибавлением нитрита натрия прибавляют 489 г 2,3-дихлоранилина (3,0 моля) в течение 2,5 ч при такой же температуре. Прибавление дихлоранилина начинают через 15 мин после начала прибавления нитрита натрия. После окончания прибавления всех веществ реакционную смесь перемешивают в течение 30 мин при 35°C. Затем реакционную смесь нагревают до 60-65°C. Органическую фазу, содержащую продукт реакции, отделяют от водной фазы. Оставшуюся жидкость отбрасывают и неочищенный продукт дважды промывают с помощью 200 мл воды. 792,2 г неочищенного твердого 1-бром-2,3-дихлорбензол получают (87,7% от теоретического выхода) чистотой 86,2%).
В соответствии с приведенными выше примерами можно получить следующие соединения формулы I:
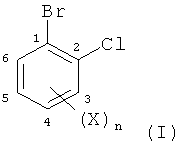
Способ, предлагаемый в настоящем изобретении, позволяет получать замещенные орто-хлорбромбензолы регулируемым образом, с высоким выходом, с высокой степенью региоселективности и с низкими затратами.
Способ, предлагаемый в настоящем изобретении, при желании позволяет получать замещенные орто-хлорбромбензолы без использования органического растворителя.
Исходные вещества для способа, предлагаемого в настоящем изобретении, отличаются легкой доступностью и простотой применения, а также являются недорогими.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДИНИТРИЛОВ ФЕНИЛМАЛОНОВОЙ КИСЛОТЫ | 2003 |
|
RU2324678C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПИРАЗОЛОВ | 2008 |
|
RU2459807C2 |
| СИНТЕЗ ЗАМЕЩЕННЫХ КОНДЕНСИРОВАННЫХ С ГЕТЕРОЦИКЛОМ ГАММАКАРБОЛИНОВ | 2019 |
|
RU2795581C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛИЧЕСКИХ ДИКЕТОНОВ | 2005 |
|
RU2384562C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 3-ПИРИДИЛМЕТИЛ АММОНИЙ БРОМИДОВ | 2009 |
|
RU2549896C2 |
| СПОСОБ ПРОИЗВОДСТВА 2,3-ДИХЛОРПИРИДИНА | 2005 |
|
RU2359960C2 |
| СПОСОБ ПОЛУЧЕНИЯ АНИЛИНОВЫХ ПРОИЗВОДНЫХ И 3-МЕТИЛ-7-НИТРО-3Н-ИЗОБЕНЗОФУРАН-1-ОН | 2001 |
|
RU2270186C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЦИЛИРОВАННЫХ 1,3-ДИКАРБОНИЛЬНЫХ СОЕДИНЕНИЙ | 2000 |
|
RU2248347C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФТОРСОДЕРЖАЩИХ СОЕДИНЕНИЙ | 1997 |
|
RU2175958C2 |
| ПРОИЗВОДНЫЕ УРАЦИЛА, ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ ПОДАВЛЕНИЯ РОСТА СОРНЯКОВ | 2000 |
|
RU2259359C2 |
Изобретение относится к способу получения соединений формулы I
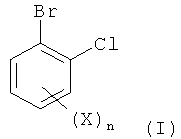 , в которой X обозначает фтор, хлор, бром или йод и n равно 1, 2, 3 или 4, который включает реакцию соединения формулы II
, в которой X обозначает фтор, хлор, бром или йод и n равно 1, 2, 3 или 4, который включает реакцию соединения формулы II
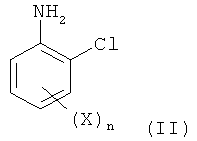 , в которой заместители являются такими, как определено для формулы I, с неорганическим нитритом в кислой водной среде в присутствии бромида и содержащего медь катализатора, способ осуществляют в виде однореакторной реакции. Использование настоящего способа позволяет получать указанные соединения с высокими выходами и высокого качества экономически привлекательным и легким в осуществлении путем. 11 з.п. ф-лы, 4 пр., 1 табл.
, в которой заместители являются такими, как определено для формулы I, с неорганическим нитритом в кислой водной среде в присутствии бромида и содержащего медь катализатора, способ осуществляют в виде однореакторной реакции. Использование настоящего способа позволяет получать указанные соединения с высокими выходами и высокого качества экономически привлекательным и легким в осуществлении путем. 11 з.п. ф-лы, 4 пр., 1 табл.
1. Способ получения соединений формулы I
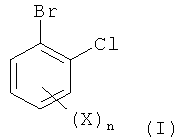
в которой X обозначает фтор, хлор, бром или йод и n равно 1, 2, 3 или 4, который включает реакцию соединения формулы II
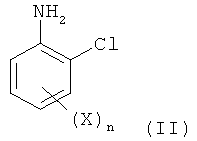
в которой заместители являются такими, как определено для формулы I, с неорганическим нитритом в кислой водной среде в присутствии бромида и содержащего медь катализатора, способ осуществляют в виде однореакторной реакции.
2. Способ по п.1, в котором X обозначает хлор.
3. Способ по п.1, в котором n равно 1.
4. Способ по п.1, в котором соединение формулы I представляет собой 1-бром-2,3-дихлорбензол или 2-бром-1,3-дихлорбензол.
5. Способ по п.1, в котором соединение формулы I представляет собой 1-бром-2,3-дихлорбензол.
6. Способ по п.1, в котором используют от 0,01 до 2 экв. содержащего медь катализатора.
7. Способ по п.1, в котором ионы меди (I) и/или ионы меди (II) применяют в качестве содержащего медь катализатора.
8. Способ по п.1, в котором содержащий медь катализатор представляет собой тонкоизмельченную металлическую медь.
9. Способ по п.1, который осуществляют при температуре от 10 до 100°С.
10. Способ по п.1, в котором неорганический нитрит прибавляют к смеси соединения формулы II, бромида и содержащего медь катализатора в кислой водной среде.
11. Способ по п.1, в котором неорганический нитрит прибавляют в виде водного раствора.
12. Способ по п.1, в котором растворимый в органическом растворителе замещенный бензол формулы I извлекают из водной реакционной фазы путем прибавления к ней подходящего органического растворителя с последующим разделением фаз.
| Способ крашения тканей | 1922 |
|
SU62A1 |
| BELETSKAYA еt al | |||
| FIRST EXAMPLE OF CATALYTIC SANDMEYER REACTION // XVI | |||
| FECHEM CONFERENCE ON ORGANOMETALLIC CHEMISTRY, 08.09.2005, P.172, retrieved from the Internet: http://comc16.chem.elte.hu/pdffiles/Posters/Poster171_180.pdf | |||
| BELETSKAYA et al | |||
| CATALYTIC SANDMEYER BROMINATION // SYNTHESIS, 12.07.2007, №16, | |||
Авторы
Даты
2012-06-20—Публикация
2007-10-08—Подача