Область техники
Настоящее изобретение связано с фармацевтическими композициями, содержащими гуманизированное моноклональное антитело, распознающее дифференцировочный антиген CD6 лейкоцитов, способный вызывать апоптоз в опухолевых клетках, которые пригодны для лечения В-клеточной хронической лимфоцитарной лейкемии.
Описание предшествующего уровня техники
Терапевтическая значимость моноклональных антител (мАТ) была доказана на практике. В частности, в случае раковых заболеваний мАТ принадлежат к современным инструментам, используемым для терапии пациентов с различными видами раковых заболеваний (Weiner, L.M. et al. (2006) Hum Antibodies 15(3): 103; Imai, K. et al. (2006) Nat Rev Cancer 6(9):714).
Апоптоз представляет собой природный биологический механизм клеточной смерти; однако апоптоз может быть вызван терапевтическими средствами. Апоптоз представляет собой важный путь контроля роста опухолевых клеток и является механизмом действия, заявленным для некоторых лекарственных препаратов, включая мАТ, для терапевтического применения у пациентов, страдающих от некоторых видов раковых заболеваний. В медицинской онкологии поэтому становится важным поиск лекарственных соединений, способных вызывать клеточную смерть через апоптоз (Cartron, G. et al. (2004) Blood 104:2635).
Одной из современных проблем здравоохранения являются лимфопролиферативные синдромы, в частности В-клеточная хроническая лимфоцитарная лейкемия (B-CLL). B-CLL представляет собой наиболее распространенную лейкемию в западном мире, и на сегодняшний день не существует лекарственных средств, избавляющих от нее (Chiorazzi, N. et al. (2005) N Engl J Med 352(8):804; Herishanu, Y. et al. (2005) Transfus Apher Sd 32(1):85). В настоящий момент одним из важных методов лечения таких пациентов является применение мАТ, способных удалять опухолевые клетки (Robak, T. (2005) Transfus Apher Sci 32(1):33). Однако основным недостатком этого подхода, основанного на использовании специфических мАТ к CD52 и CD20, является то, что он имеет очень ограниченный противоопухолевый терапевтический эффект, при этом также вызывая уничтожение нормальных лимфоцитов индивидуума (Nuckel, H. et al. (2005) Eur J Pharmacol 514(2-3):217; Cartron, G. et al. (2004) Blood 104:2635). Отсутствие специфического распознавания вызывает продолжительную лимфопению, составляющую фактор риска частого возникновения инфекций у пациентов, получающих лечение, которые уже и так к ним восприимчивы вследствие собственных характеристик этого ракового заболевания (Boye, J. et al. (2003) Ann Oncol 14(4):520; Cartron, G. et al. (2004) Blood 104:2635; Potter, M.(1999) 12(4):359; Ravandi, F. et al. (2006) Cancer Immunol Immunother 55(2): 197).
Опухолевые клетки пациентов с B-CLL экспрессируют маркеры клеточной поверхности, характерные для нормальных В-лимфоцитов (например, CD19 и CD20). Конкретно, возникновение опухолевых клеток ассоциируют с В-лимфоцитами периферической крови, которые коэкспрессируют дифференцировочный антиген CD5 лейкоцитов (Herishanu, Y. et al. (2005) Transfus Apher Sci 32(1):85). CD5 является отличительным маркером для B-CLL, но не определяющим, поскольку он может представлять собой второстепенный маркер субпопуляции опухолевых клеток, и еще не доказано, происходят ли эти клетки из костного мозга, или источник их находится вне костного мозга (Caligaris-Cappio, F. et al. (2004) Hematol Oncol Clin N Am 18:849).
Дифференцировочный антиген CD6 лейкоцитов является мало известной и слабо охарактеризованной молекулой. CD6 представляет собой поверхностный гликопротеин, экспрессируемый преимущественно Т-лимфоцитами. В основном полагают, что CD6 в этих клетках является рецептором, выполняющим костимулирующие функции, но лежащий в основе механизм остается неизвестным (Aruffo, A. et al. (1997) Immunol Today 18(10):498; Patel, D.D. (2000) J Biol Regul Homeost Agents 2000 14(3):234). Его экспрессия в зрелых тимоцитах ассоциирована с их устойчивостью к апоптозу в процессе созревания лимфоцитов в этом лимфоидном органе (Singer, N.G. et al. (2002) Int Immunol. 14(6):585).
Интересно, что молекула CD6 экспрессируется в минорной субпопуляции В-лимфоцитов периферической крови здоровых индивидуумов, однако сведения о происхождении и функциональных характеристиках этих клеток очень ограничены. Кроме того, мононуклеарные клетки периферической крови пациентов с B-CLL также экспрессируют молекулу CD6. Полагают, что молекула CD6 коэкспрессируется с молекулой CD5, но в отличие от нее в итоге CD6 обнаруживали только в образцах пациентов с B-CLL.
Кроме того, распознавание молекулы CD5 специфическими моноклональными антителами вызывает апоптоз в опухолевых клетках пациентов с B-CLL, но только у части из них (Pers, J.O. et al. (2002) Leukemia 16:44).
Молекулу CD6 распознает мышиное мАТ ior-t1A. В предшествующем исследовании образцов пациентов с B-CLL было найдено, что мышиное мАТ ior-t1A ингибирует апоптоз, вызываемый анти-IgM антителом в В-лимфоцитах (Osorio, L. M. et al. (1997) Blood, 89(8):2833). С другой стороны, терапевтические композиции этого мышиного мАТ к CD6 обладают лечебным эффектом в отношении псориаза (Montero, E. et al. (1999) Autoimmunity 29(2): 155).
Впоследствии с помощью генно-инженерных методов (ЕР 0699755) была получена гуманизированная версия этого мышиного моноклонального антитела к CD6 человека, названная T1h (ЕР 0807125).
Авторы обнаружили, что гуманизированное мАТ T1h распознает молекулы CD6, экспрессируемые на опухолевых клетках периферической крови и, неожиданно, также на клетках костного мозга пациентов с B-CLL. Более того, мАТ T1h также распознает опухолевые клетки, которые не экспрессируют молекулу CD5, что делает CD6 опухолевым маркером, включающим CD5-субпопуляцию. Более того, гуманизированное моноклональное мАТ T1h вызывает апоптоз опухолевых клеток пациентов с В-клеточной хронической лимфоцитарной лейкемией, но не нормальных лимфоцитов.
Новизна настоящего изобретения состоит в создании терапевтических композиций, содержащих анти-CD6 моноклональные антитела, для применения их у пациентов с лимфопролиферативными синдромами и, в частности, у пациентов с В-клеточной хронической лимфоцитарной лейкемией. К удивлению, распознавание молекулы CD6 гуманизированным моноклональным антителом T1h вызывает апоптотическую смерть опухолевых клеток пациентов с лимфопролиферативными синдромами, экспрессирующими молекулу CD6, и, в частности, опухолевых В-лимфоцитов пациентов с В-клеточной хронической лимфоцитарной лейкемией, что позволяет использовать мАТ T1h для терапии этого типа опухолей. В дополнение, воздействие мАТ T1h может сенсибилизировать злокачественные клетки к действию цитотоксических лекарственных средств, что может способствовать комбинированному применению гуманизированного моноклонального антитела T1h вместе с радиационной терапией, химиотерапевтическими агентами или другими биопрепаратами.
Подробное описание изобретения
Настоящее изобретение связано с терапевтическими композициями моноклональных антител, которые распознают антиген CD6 человека, эффективными для лечения пациентов с лимфопролиферативными заболеваниями. Более конкретно, настоящее изобретение включает в себя применение фармацевтических композиций, содержащих гуманизированное моноклональное антитело T1h, которое распознает дифференцировочный антиген CD6 лейкоцитов человека, и их использование для диагностики и лечения В-клеточной хронической лимфоцитарной лейкемии.
Термин «гуманизированное моноклональное антитело» относится к моноклональному антителу, полученному методами генной инженерии, как описано в патенте № 0699755 (Европейский патентный бюллетень). Объектом настоящего изобретения является терапевтическая композиция, содержащая гуманизированное мАТ T1h (которое получено из гибридомы IOR-T1A с депозитарным номером ЕСАСС 96112640 и способно вызывать апоптоз злокачественных клеток пациентов с В-клеточной хронической лимфоцитарной лейкемией посредством распознавания молекулы CD6) отдельно или совместно с любым из агентов, выбранных из группы:
химиотерапевтических агентов, таких как флударабин;
моноклональных антител, специфичных к поверхностным молекулам злокачественных лимфоцитов, таких как анти-CD20 антитела.
Фармацевтические композиции по настоящему изобретению также содержат подходящий наполнитель, который может представлять собой физиологический буферный раствор, и их можно вводить путем инъекций в пределах дозировок от 0,05 до 1 мг/кг веса тела. С другой стороны, настоящее изобретение связано с диагностическим реагентом, содержащим анти-CD6 моноклональное антитело, для применения в диагностике В-клеточной хронической лимфоцитарной лейкемии.
1. Создание фармацевтических композиций, содержащих гуманизированное моноклональное антитело T1h к CD6 человека
Гуманизированное моноклональное антитело T1h к CD6 человека получали из гибридомы IOR-T1A с депозитарным № ЕСАСС 96112640, как описано в ЕР 0807125 А2. Фармацевтическая композиция по настоящему изобретению содержит гуманизированное моноклональное антитело T1h, кроме того, эта композиция содержит в качестве подходящего вспомогательного наполнителя физиологический буферный раствор, аналогичный другим растворам, используемым в составах с моноклональными антителами для внутривенного применения, как описано в ЕР 0807125. Композицию по настоящему изобретению вводят путем инъекций в диапазоне дозировок от 0,05 до 1 мг/кг веса тела.
2. Характеристика специфического распознавания гуманизированного моноклонального антитела T1h
Мононуклеарные клетки периферической крови и клетки костного мозга пациентов с В-клеточной хронической лимфоцитарной лейкемией окрашивали FITC-конъюгированным мАТ к CD19 человека. После этого клетки инкубировали со следующими моноклональными антителами: конъюгированным с биотином моноклональным антителом к CD6 человека (T1h) или конъюгированным с PE-Cy5 антителом к CD5 человека (Pharmingen) или конъюгированным с биотином антителом к CD20 человека (Ритуксимаб-Rx). Связывание биотинилированных антител детектировали с помощью стрептавидина, конъюгированного с PE-Cy5.5. На проточном цитофлуориметре FACScan собирали, по меньшей мере, 10000 живых клеток. Мертвые клетки исключали окрашиванием пропидия иодидом.
3. Характеристика противоопухолевого действия гуманизированного моноклонального антитела T1h на клетки пациентов с В-клеточной хронической лимфоцитарной лейкемией.
Мононуклеарные клетки периферической крови здоровых индивидуумов и пациентов с В-клеточной хронической лимфоцитарной лейкемией обрабатывали in vitro 0,1 мкг/мл гуманизированным моноклональным антителом T1h или изотипическим контролем (моноклональным антителом R3h) в течение 18 часов при 37°С и 5% СО2. Затем клетки промывали и инкубировали с аннексином-V, конъюгированным с FITC, в течение 10 минут при комнатной температуре. После этого клетки окрашивали пропидия иодидом (PI) и собирали на проточном цитофлуориметре FACScan. Апоптотические клетки определяли как клетки аннексин-V+/PI-.
ПРИМЕРЫ
Нижеследующие примеры предназначены для иллюстрации изобретения. Гуманизированное моноклональное антитело T1h к CD6 человека получали из гибридомы IOR-T1A с депозитарным № ЕСАСС 96112640, как описано в ЕР 0807125 А2.
Пример 1: Гуманизированное моноклональное антитело T1h к CD6 человека распознает злокачественные клетки из периферической крови пациентов с В-клеточной хронической лимфоцитарной лейкемией.
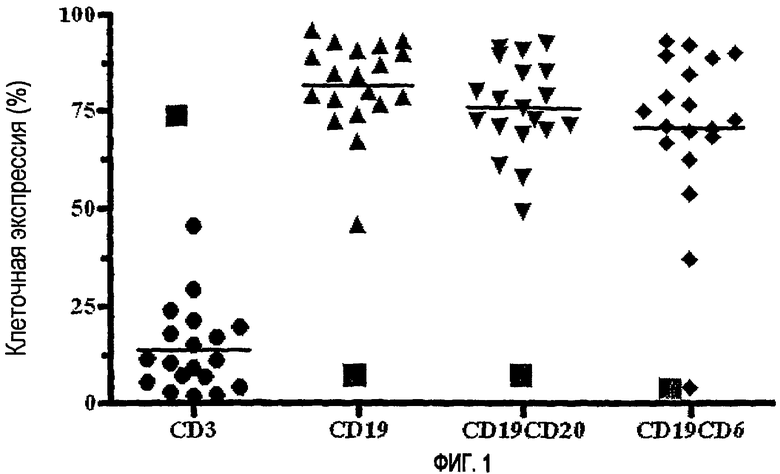
Была проведена оценка распознавания мАТ T1h мононуклеарных клеток периферической крови 19 пациентов с В-клеточной хронической лимфоцитарной лейкемией и определена экспрессия молекулы CD6 на В-клетках, ограниченных экспрессией маркеров CD19 и CD20. Более того, было проведено сравнение экспрессии этих клеточных маркеров с образцами от здоровых индивидуумов (фигура 1). Исследование проводили с помощью проточной цитофлуориметрии, используя FACScan для анализа образцов. Нормальные значения указаны в виде красных сплошных квадратов на фигуре 1.
Пример 2: Гуманизированное моноклональное антитело T1h к CD6 человека распознает злокачественные клетки из костного мозга пациентов с В-клеточной хронической лимфоцитарной лейкемией.
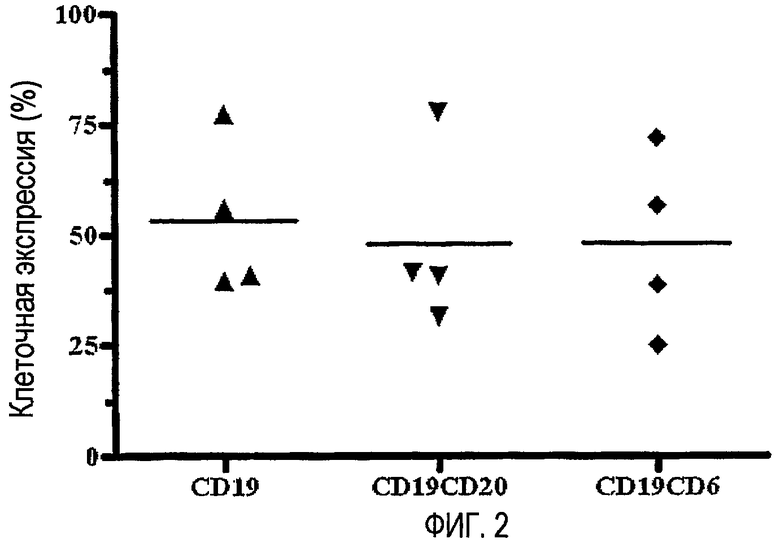
Была проведена оценка распознавания мАТ T1h мононуклеарных клеток периферической крови 4 пациентов с В-клеточной хронической лимфоцитарной лейкемией и определена экспрессия молекулы CD6 на В-клетках, ограниченных экспрессией маркеров CD19 и CD20. Более того, было проведено сравнение экспрессии этих клеточных маркеров с образцами от здоровых индивидуумов (фигура 2). Исследование проводили с помощью проточной цитофлуориметрии, используя FACScan для анализа образцов.
Пример 3: Гуманизированное моноклональное антитело T1h к CD6 человека распознает злокачественные клетки пациентов с В-клеточной хронической лимфоцитарной лейкемией, которые не экспрессируют молекулу CD5.
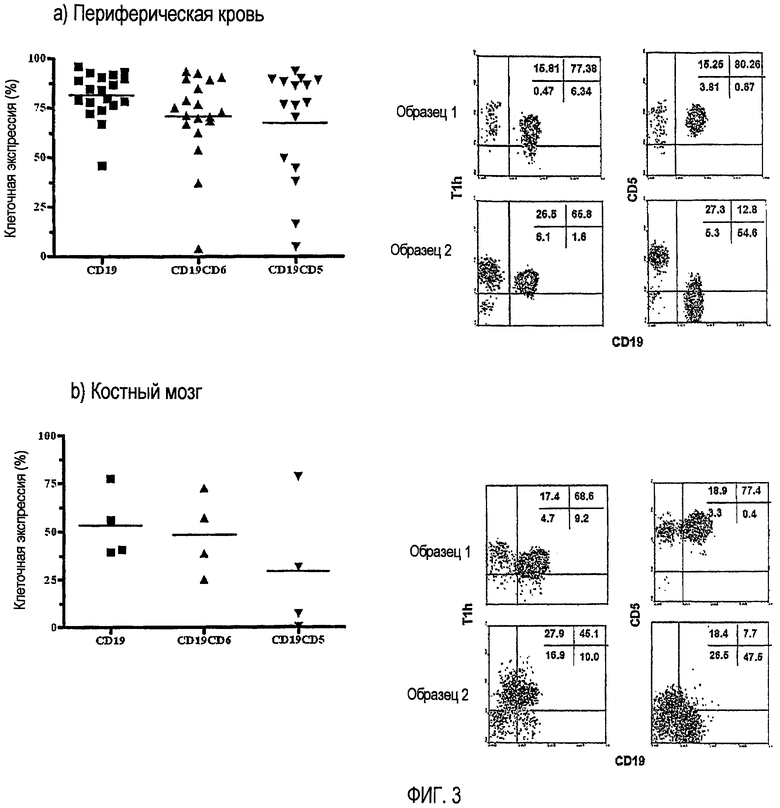
Была проведена оценка распознавания мАТ T1h мононуклеарных клеток периферической крови (фигура 3а) и клеток костного мозга (фигура 3b) пациентов с В-клеточной хронической лимфоцитарной лейкемией и определена коэкспрессия молекул CD6 и CD5 в злокачественных клетках. Образец 1 представляет пациента с опухолевыми клетками CD6+CD5+, а образец 2 представляет пациента с опухолевыми клетками CD6+CD5-. Исследование проводили с помощью проточной цитофлуориметрии, используя FACScan для анализа образцов.
Пример 4: Гуманизированное моноклональное антитело T1h вызывает апоптотическую клеточную смерть злокачественных клеток пациентов с В-клеточной хронической лимфоцитарной лейкемией.
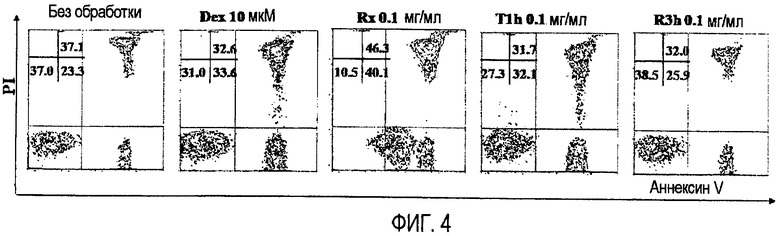
Была проведена оценка способности гуманизированного моноклонального антитела T1h вызывать апоптотическую клеточную смерть злокачественных клеток пациентов с В-клеточной хронической лимфоцитарной лейкемией. После инкубации in vitro опухолевых клеток с гуманизированным моноклональным антителом T1h был определен процент апоптотических клеток по нижеследующим критериям: клетки положительно окрашивались аннексином-V и не окрашивались пропидия иодидом. В качестве положительных контролей использовали дексаметазон (Dex) и ритуксимаб (Rx, анти-CD20 моноклональное антитело). В качестве отрицательного контроля использовали гуманизированное моноклональное антитело R3h (изотип IgG1; специфичное к рецептору эпидермального фактора роста человека). Результаты (фигура 4) сравнивали с клетками, не получавшими воздействие (без обработки). Исследование проводили с помощью проточной цитофлуориметрии, используя FACScan для анализа образцов.
Краткое описание чертежей
Фигура 1:
На фигуре 1 представлена экспрессия CD6, определенная с помощью гуманизированного моноклонального антитела T1h, в мононуклеарных клетках периферической крови пациентов с В-клеточной хронической лимфоцитарной лейкемией. Потенциальный специфичный к опухоли антиген.
Фигура 2:
На фигуре 2 представлена экспрессия CD6, определенная с помощью гуманизированного моноклонального антитела T1h, в клетках костного мозга пациентов с В-клеточной хронической лимфоцитарной лейкемией. Потенциальный специфичный к опухоли антиген.
Фигура 3:
На фигуре 3 представлена экспрессия CD6, определенная с помощью гуманизированного моноклонального антитела T1h, в мононуклеарных клетках периферической крови пациентов с В-клеточной хронической лимфоцитарной лейкемией, у которых отсутствует экспрессия молекулы CD5.
Фигура 4:
На фигуре 4 представлена индукция апоптотической клеточной смерти злокачественных клеток пациентов с В-клеточной хронической лимфоцитарной лейкемией с помощью гуманизированного моноклонального антитела T1h.
Группа изобретений относится к области медицины и касается фармацевтических композиций, способных вызывать апоптоз опухолевых клеток для диагностики и лечения В-клеточной хронической лимфоцитарной лейкемии. Сущность изобретений включает фармацевтические композиции для лечения В-клеточной хронической лимфоцитарной лейкемии, включающие в качестве активного компонента гуманизированное моноклональное антитело Tlh из секретирующей гибридомы IOR-TIA с депозитарным № ЕСАСС 96112640, распознающее дифференцировочный антиген CD6 лейкоцитов. Диагностический реагент также включает данное антитело. Преимущество группы изобретений заключается в увеличении специфической активности. 5 н. и 6 з.п. ф-лы, 4 пр., 4 ил.
1. Фармацевтическая композиция, пригодная для диагностики В-клеточной хронической лимфоцитарной лейкемии, где композиция содержит гуманизированное моноклональное антитело, распознающее дифференцировочный антиген CD6 лейкоцитов, способное вызывать апоптоз в опухолевых клетках, и подходящий наполнитель, в которой гуманизированное моноклональное антитело к CD6 является гуманизированным антителом T1h из секретирующей гибридомы IOR-T1A с депозитарным № ЕСАСС 96112640.
2. Фармацевтическая композиция по п.1, в которой подходящим наполнителем является физиологический буферный раствор.
3. Фармацевтическая композиция, пригодная для лечения В-клеточной хронической лимфоцитарной лейкемии, где композиция содержит гуманизированное моноклональное антитело, распознающее дифференцировочный антиген CD6 лейкоцитов, способное вызывать апоптоз в опухолевых клетках, и подходящий наполнитель, в которой гуманизированное моноклональное антитело к CD6 является гуманизированным антителом T1h из секретирующей гибридомы IOR-T1A с депозитарным № ЕСАСС 96112640.
4. Фармацевтическая композиция по п.3, содержащая гуманизированное антитело T1h, которое вызывает апоптоз злокачественных В-лимфоцитов, отдельно или совместно с любым из агентов, выбранных из группы химиотерапевтических агентов, моноклональных антител, специфических к поверхностным молекулам злокачественных лимфоцитов.
5. Фармацевтическая композиция по п.4, в которой химиотерапевтическим агентом является флударабина фосфат.
6. Фармацевтическая композиция по п.4, в которой моноклональным антителом, специфичным к поверхностным молекулам злокачественных лимфоцитов, является анти-СD20 антитело.
7. Фармацевтическая композиция по п.3, в которой подходящим наполнителем является физиологический буферный раствор.
8. Фармацевтическая композиция по пп.3-7, где композиция обладает терапевтическим эффектом в пределах дозировок анти-СD6 моноклонального антитела от 0,05 до 1 мг/кг веса тела.
9. Диагностический реагент, содержащий гуманизированное антитело T1h из секретирующей гибридомы IOR-T1A с депозитарным № ЕСАСС 96112640, для применения в диагностике В-клеточной хронической лимфоцитарной лейкемии.
10. Применение гуманизированного антитела T1h из секретирующей гибридомы IOR-T1A с депозитарным № ЕСАСС 96112640 для диагностики В-клеточной хронической лимфоцитарной лейкемии.
11. Применение гуманизированного антитела T1h из секретирующей гибридомы IOR-T1A с депозитарным № ЕСАСС 96112640 для лечения В-клеточной хронической лимфоцитарной лейкемии.
| GHOBRIAL L.M | |||
| et al | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Proc | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| OSORIO L.M | |||
| et al | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
Авторы
Даты
2012-06-27—Публикация
2007-12-24—Подача