Изобретение относится к применению производных пурина для изготовления лекарственного препарата, предназначенного для лечения патологий, при которых наблюдается дефицит баланса между клеточным делением и апоптозом, более точно, в случаях, когда повышенный апоптоз является причиной патологии.
Также изобретение относится к некоторым производным пурина.
Патологии, при которых наблюдается дефицит баланса между клеточным делением и апоптозом, представляют собой хроническую лимфоцитарную лейкемию и заболевания почек, такие как поликистоз почек.
Хроническая лимфоцитарная лейкемия, ХЛЛ (CLL), представляет собой разнородную группу заболеваний, характеризующихся накоплением CD5+ моноклональных В клеток в крови, костном мозге и кроветворных органах.
Это заболевание, при котором моноклональные В клетки не подвергаются, либо подвергаются лишь в небольшой степени естественному апоптозу (клеточная смерть) и лишь небольшое количество В клеток участвует в клеточном цикле. В этом смысле данное заболевание существенно отличается от заболеваний, при которых обнаруживается непрекращающаяся избыточная пролиферация моноклональных клеток, при которой моноклональные клетки в большой степени участвуют в клеточном цикле, а устойчивость клеток к апоптозу (клеточной смерти) представляет собой феномен вторичной патогенности.
Как правило, различают несколько типов ХЛЛ, включая В-клеточную хроническую лимфоцитарную лейкемию и Т-клеточную хроническую лимфоцитарную лейкемию. Под термином ХЛЛ обычно понимается В-клеточная лимфоцитарная лейкемия (В-ХЛЛ).
В-клеточная хроническая лимфоцитарная лейкемия, обозначаемая как В-ХЛЛ, представляет собой заболевание, при котором В лимфоциты, ответственные за аккумуляцию В лимфоцитов лимфоидной морфологии, экспрессируют мембранные антигены, характерные для данного заболевания, такие как молекулы CD5 и CD23, вызывая гиперлимфоцитоз крови, недостаточность костного мозга, а также полиаденопатию лимфоузлов.
В-ХЛЛ была охарактеризована как отдельная биологическая разновидность с различным сценарием развития.
Классификация стадий по Бинету позволяет выделить три этапа развития болезни: А, В и С.
В 41% случаев на стадии А болезнь далее непосредственно переходит в стадии В и С.Критериями для неблагоприятного прогноза, помимо других биологических параметров, являются время удвоения лимфоцитов менее 6 месяцев, увеличение уровня содержания растворимых CD23 или увеличение активности сывороточной тимидинкиназы. Полностью установленные генетические параметры неблагоприятного прогноза включают немутированные формы болезни (гены тяжелых цепей иммуноглобулина в герминальном положении 14q32), аномальная делеция хромосом 11q и 17р, или дополнительные хромосомные аномалии типа 12+. Для пациентов, являющихся носителями В-ХЛЛ с подобными биологическими показателями, наблюдается быстрое прогрессирование заболевания: так, в 50% случаев для пациентов с немутированной формой прогрессирование составляет 24 месяца;
в 50% случаев для пациентов с аномалиями 17р-, 11q- или 12q+ прогрессирование составляет 15 месяцев.
Несмотря на то, что лечение на данный момент в первую очередь приводит к ремиссии заболевания, для всех пациентов наблюдается рецидив и на данный момент ХЛЛ рассматривается как неизлечимое заболевание.
Важным вопросом в настоящее время является выявление на стадии А заболевания пациентов с высокой степенью вероятности прогрессирования болезни к более тяжелой степени.
Лучшая терапия первого ряда для В-ХЛЛ еще не определена.
Аналоги пурина, в частности флударабин, остаются наиболее хорошо изученными в отношении В-ХЛЛ. Флударабин сам по себе приводит к отклику на более высоком уровне по сравнению с комбинированным лекарственным лечением, которое включает алкилирующие вещества и кортикотерапию. Флударабин вызывает более полную гематологическую ремиссию (от 7 до 40%), по сравнению с комбинированной терапией типа CHOP или CAP (хлораминофен).
Несмотря на то, что флударабин приводит к лучшему ответу, в целом достижения в области повышения общего уровня выживаемости остаются крайне незначительными. Основные терапевтические усилия заключаются в сочетании флударабина с подходящей химиотерапией, например флударабин и циклофосфамид, особенно в случаях устойчивых форм заболевания. Средняя продолжительность жизни для пациентов, устойчивых к действию флударабина, составляет только 12 месяцев. Тем не менее, токсичность лечения, в частности гематологическая токсичность, при таких сочетаниях повышается.
У 50% пациентов, подвергавшихся комбинированному лечению флударабином и циклофосфамидом, обнаруживается заражение. Официально зарегистрированный сепсис или пневмопатия были обнаружены во время лечения у 25% пациентов, незарегистрированные случаи повышения температуры и/или госпитализации составляют другие 25%.
Революционные изменения в терапии произошли благодаря использованию антител. При терапии В-ХЛЛ применяют два антитела: ритуксимаб и алемтузумаб. В случае В-ХЛЛ активность ритуксимаба снижена вследствие невысокой экспрессии в мишени, CD20 антигене, на В лимфоцитах ХЛЛ. Ритуксимаб применяют при В-ХЛЛ совместно с аналогами пурина и/или циклофосфамидом (общий ответ 59% получен в случае комбинации флударабина/циклофосфамида/ритуксимаба для пациентов, не восприимчивых к воздействию флударабина, включя только 5% полного ответа).
Активность алемтузумаба, направленная против антигенов, экспрессирующихся на лейкоцитах и лейкемических В лимфоцитах ХЛЛ, с очень гетерогенной плотностью мембраны антигена, снижена вследствие его высокой иммунодепрессивной активности и высокой частотой возникновения цитомегаловирусных и оппортунистических инфекций во время или после лечения: антитела проявляют высокую Т иммунодепрессивную активность. Гематологический ответ к алемтузумабу составляет 33%; антитела способны разрушать клональные В лимфоциты крови и костного могза, однако оказывают лишь незначительное воздействие на лимфатические узлы. Указанные особенности ограничивают использование антител при таких симптомах. Радиоиммунотерапия с анти-С020 телами совместно с иттрием-90 (Цевалин) приводит к низкому проценту ремиссии В-ХЛЛ и приводит к существенной миелосупрессии.
В патенте US 6812232 описаны аналоги пурина, аналогичные заявленным в данном изобретении, обладающие способностью ингибировать пролиферацию клеток. По существу, избыточная пролиферация клеток в случае ХЛЛ была остановлена.
В заявке на патент WO 2005/02584 описано применение росковитина, предпочтительно его абсолютной (R)-конфигурации, для лечения хронической лимфоцитарной лейкемии, в частности, В-клеточной хронической лимфоцитарной лейкемии.
Росковитин представляет собой пурин приведенной ниже формулы:
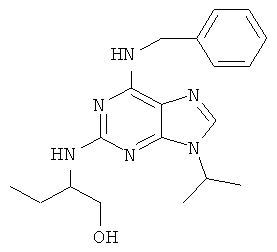
Было обнаружено, что производные росковитина обладают гораздо большей активностью по сравнению с росковитином при лечении патологий, для которых наблюдается нарушение баланса между клеточным делением и апоптозом, помимо этого, производные росковитина, в некоторых случаях, характеризуются лучшей растворимостью.
Так, в изобретении предлагается применение, по меньшей мере, одного соединения приведенной ниже формулы I:
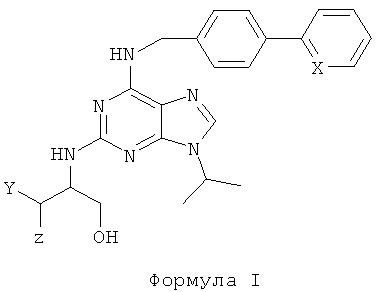
где:
- Х представляет собой С или N,
- Y представляет собой СН3 или ОН, и
- Z представляет собой Н или СН3,
либо одной из его фармацевтически приемлемых солей, гидратов, сложных эфиров или изомеров,
для изготовления лекарственного препарата, предназначенного для лечения патологий, при которых наблюдается нарушение баланса между клеточным делением и апоптозом.
В первом воплощении изобретения патологией является хроническая лимфоцитарная лейкемия.
Более конкретно, патология представляет собой В-клеточную хроническую лейкемию.
Во втором воплощении изобретения, патология представляет собой заболевание почек, более конкретно поликистоз почек.
Предпочтительной солью, применяемой для изготовления лекарственного препарата для лечения патологий, при которых наблюдается нарушение баланса между клеточным делением и апоптозом, является оксалат одного из соединений формулы I.
Предпочтительно, по меньшей мере, одно из применяемых соединений характеризуются формулой 1-1, которая соответствует формуле I, где Х представляет собой N:
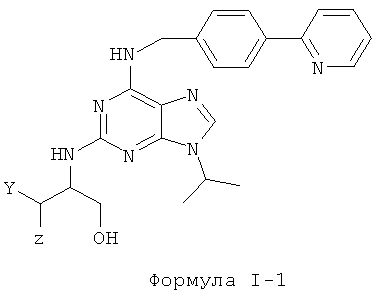
Причина заключается в том, что, как будет показано ниже, активность веществ на клеточных моделях хронической лимфоцитарной лейкемии и поликистоза почек больше примерно в 4-5 раз, а растворимость в водной среде больше примерно в 5-10 раз по сравнению с аналогичными соединениями, где Х представляет собой С.
Более предпочтительно, чтобы, по меньшей мере, одно используемое соединение характеризовалось формулой I-II, которая соответствует формуле I, где Х представляет собой N, a Y представляет собой ОН:
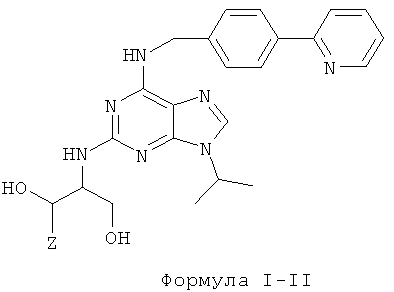
Соединения, обладающие структурой I-II, проявляют активность, сравнимую с таковой для I-I производных, однако их растворимость в водной среде еще больше.
Более конкретно, в первом предпочтительном воплощении, по меньшей мере, одно из соединений, применяемых для изготовления лекарственного препарата для лечения указанных патологий, представляет собой соединение формулы I, где Х является N, Y является СН3, a Z является Н. Данное соединение представляет собой абсолютную (R)-конфигурацию и характеризуется приведенной ниже формулой Ia:
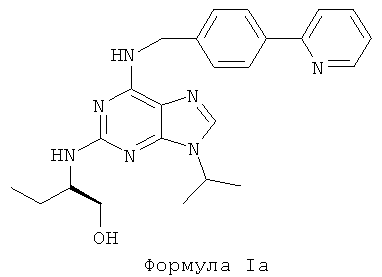
Во втором предпочтительном воплощении изобретения, по меньшей мере, одно соединение представляет собой абсолютную (S)-конфигурацию. Данное соединение характеризуется формулой Ib:
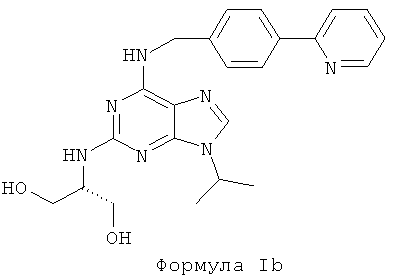
Данное открытие явилось совершенно неожиданным, поскольку в известном уровне техники, главным образом, соединения с абсолютной (Реконфигурацией рассматривались как обеспечивающие наилучшие результаты.
В третьем предпочтительном воплощении изобретения, по меньшей мере, одно соединение формулы Ia или Ib находится в форме его оксалатной соли.
В четвертом предпочтительном воплощении изобретения, по меньшей мере, одно соединение, применяемое для изготовления лекарственного препарата для лечения патологий, при которых наблюдается нарушение баланса между клеточным делением и апоптозом, представляет собой соединение формулы I, где Х представляет собой С, Y представляет собой СН3, a Z является Н. Данное соединение характеризуется приведенной ниже формулой Ic:
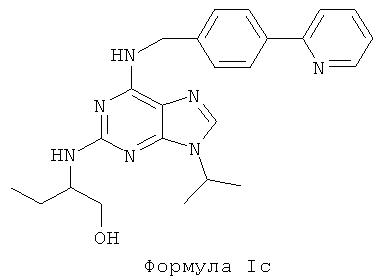
Данное соединение может использоваться как в виде абсолютной (S)-конфигурации, либо абсолютной (R)-конфигурации, так и в виде смеси этих конфигураций.
В пятом предпочтительном воплощении изобретения, по меньшей мере, одно используемое соединение представляет собой соединение формулы I, где Х является N, Y является ОН, а Z представляет собой Н. Данное соединение характеризуется формулой Id:
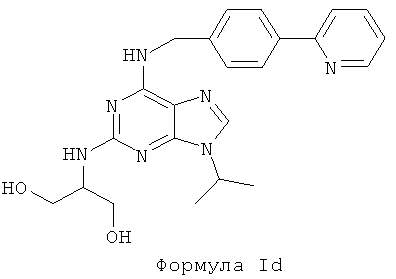
Соединение Id можно получить способом, описанным ниже в Примере 1.
Пример 1: Получение соединения Id
Данное соединение получают в три стадии, начиная с дихлорпурина согласно следующей схеме:
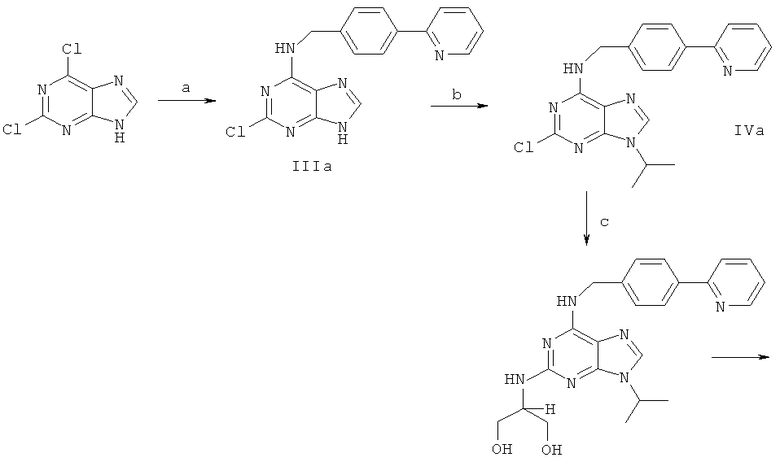
Реагенты и условия:
а: 4-(2-пиридил)бензиламин, н-BuOH, 110°C; b: 2-бромпропан, K2CO3, ДМСО; с: серинол, нагрев 160°С, 8 ч.
Стадия 1: 2-хлор-6-[4-(2-пиридил)фенилметиламино]пурин (IIIa)
4-(2-пиридил)бензиламин (2,0 г, 1,05 ммоль) и 3 мл NEt3 добавляли к раствору 2,6-дихлорпурина (2,3 г, 10 ммоль) в 20 мл н-BuOH. После нагревания при 110°С в течение 3 ч, смесь охлаждали до 20°С, отфильтровывали осадок, промывали 5 мл холодного бутанола и далее сушили под вакуумом. Выход = 85%. Т.пл. > 250°C. 1H ЯМР (d6-ДМСО): δ 4,80 (s, 2H, CH2); 7,20 (m, 1H, Hпиридил); 7,45 (d, 2H, Hфенил); 7,72 (m, 2H, Hпиридил); 7,95 (m, 3Н, Hфенил и Н-8), 8,54 (d, 1H, J=4,8 Hz, Hпиоидил).
Стадия 2: 2-хлор-9-изопропил-6-[4-(2-пиридил)фенилметил-амино]пурин (IVa)
K2CO3 (3,5 г, 24 ммоль) и 1,9 мл (20 ммоль) 2-бромпропана добавляли к раствору 2-2-хлор-6-[4-(2-пиридил)фенилметиламино]пурина (8 ммоль) в 10 мл ДМСО при температуре 18-20°C. После перемешивания при температуре 18-20°С в течение 5 часов снова добавляли 2-бромпропан (0,5 мл) и перемешивание продолжали при 20°C в течение 5 часов. После добавления 50 мл холодной (5°C) воды, смесь экстрагировали EtOAc (3 раза по 10 мл), органические фазы промывали солевым раствором (3 раза по 10 мл) и сушили над Na2SO4. Производное IVa кристаллизовали путем выпаривания растворителя. Далее производное растирали с 2 мл 2-пропанола и отфильтровывали.
Выход 86%. 1H ЯМР (CDCl3): δ 1,58 (d, 6H); 4,79 (гепт., 1Н); 4,85 (широкая s, 2Н); 6,59 (широкая s, 1Н); 7,20-7,23 (m, 1Н); 7,49 (d, 2H); 7,73-7,71 (m, 2H); 7,79 (s, 1Н); 7,98 (d, 2H); 8,71 (d, 1Н).
Стадия 3: 2-(1,3-дигидроксипроп-2-иламино)-6-[4-(2-пиридил)фенилметил амино]-9-изопропилпурин Id
Смесь соединения IVa (10 ммоль) и серинола (2-аминопропан-1,3-диол) (2 мл) нагревали в атмосфере N2 при 160°С в течение 8 ч. После охлаждения до 20°C, добавили 20 мл воды и смесь экстрагировали EtOAc (4 раза по 10 мл) Органический раствор промыли водой 2 раза по 20 мл, осушили и упарили. Производное Id кристаллизовали путем растирания с Et2O.
Т.пл. 114-117°C. Выход 74%. 1Н ЯМР (CDCl3) δ 1,52 (d, 6H); 3,78 (m, 4H); 3,96 (m, 1Н); 4,55 (гепт, 1Н); 4,76 (s, 2H); 5,40 (s, 1Н); 6,20 (s, 1Н); 7,12 (m, 1Н); 7,38 (d, 2H); 7,48 (s, 1Н); 7,62 (m, 2H); 7,90 (d, 2H); 8,60 (d, 1Н).
В шестом предпочтительном воплощении изобретения, по меньшей мере, одно используемое соединение представляет собой соединение формулы I, где Х является N, Y представляет собой СН3, Z является СН3. Данное соединение характеризуется следующей формулой Ie:
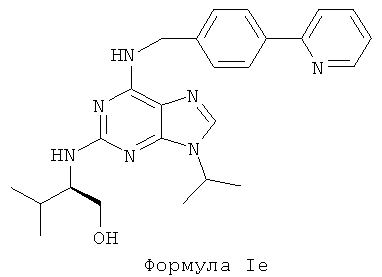
В седьмом предпочтительном воплощении изобретения, по меньшей мере, одно используемое соединение представляет собой оксалатную соль соединения формулы Ie. Данное соединение характеризуется следующей формулой If:
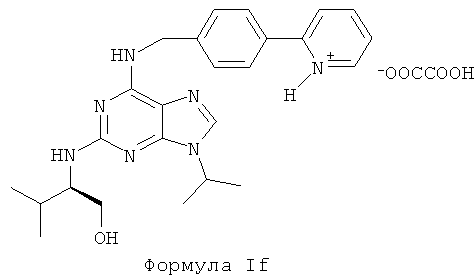
Следует отметить, что один из атомов азота в пурине может участвовать в образовании соли, что соответствует соединению одной молекулы пурина с двухосновной кислотой.
В восьмом предпочтительном воплощении изобретения, по меньшей мере, одно используемое соединение является соединением формулы Ig:
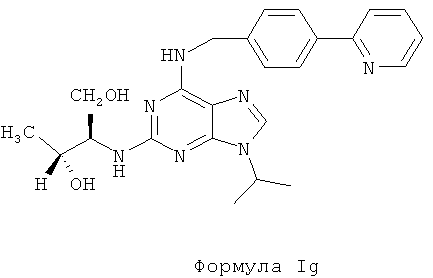
Данное соединение представляет собой (1R,2R)-2-(1,3-дигидроксибут-2-иламино)-6-[4-(2-пиридил)фенилметиламино]-9-изопропилпурин Ig.
Данное соединение получают таким же способом, как и продукт Id, заменяя, однако, в последней стадии аминопропандиол на L-треонинол или (1R, 2R)-2-аминобутан-1,3-диол.
Характеристики соединения, измеренные с помощью ЯМР:
ЯМР: 1,2 (d, 3Н); 1,4 (d, 6Н); 3,70 (m, 4H); 4,10 (m, 1H), 4,52 (гепт, 1Н); 4,72 (широкая s, 2Н); 5,50 (s, 1H); 6,2 (широкая s, 1H); 7,15 (m, 1H); 7,4 (d, 2H); 7,42 (s, 1H); 7,55 (m, 2H); 7,85 (d, 2H); 8,60 (d, 1H).
В девятом предпочтительном воплощении изобретения, по меньшей мере одно используемое соединение представляет собой соединение формулы Ih, приведенной ниже:
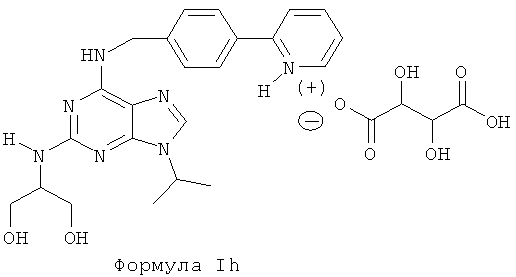
Следует отметить, что один из атомов азота в пурине может участвовать в образовании соли, что соответствует соединению одной молекулы пурина с двухосновной кислотой. Можно использовать три изомера винной кислоты.
Данное соединение является 2-(1,3-дигидроксипроп-2-иламино)-6-[4-(2-пиридил)фенилметиламино]-9-изопропилпиридин тартратом (Ih).
Данное соединение получают следующим способом: 2,1 ммоль винной кислоты, растворенной в изопропаноле (1 мл), добавляют к раствору, нагретого до 70-80°С, 2 ммоль Id в растворе изопропанола (1 мл). После охлаждения, тартрат Id выделяют фильтрацией.
Соли, такие как фумараты или гидрохлориды, гидраты и сложные эфиры соединений формулы Ia, Id и Ig, а также изомеры соединений формулы Ic и Ig также можно с успехом использовать.
В частности, сложные эфиры соединений формулы I также входят в объем изобретения.
Предпочтительными сложными эфирами соединения формулы I являются эфиры карбоновых кислот, такие как ацетиловые эфиры, эфиры никотиновой кислоты, а также эфиры аминокислот L-формы или D.
Другие предпочтительные сложные эфиры образованы из аминокислот, таких как валин или лейцин.
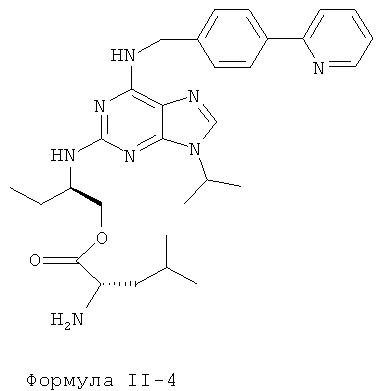
Наиболее предпочтительные сложные эфиры характеризуются нижеприведенными формулами II-1-II-4:
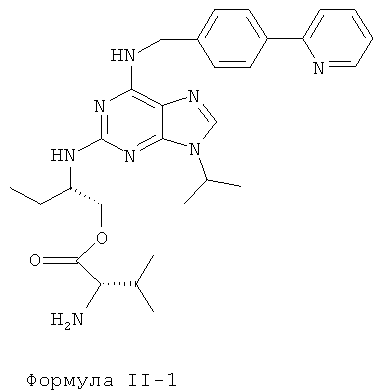
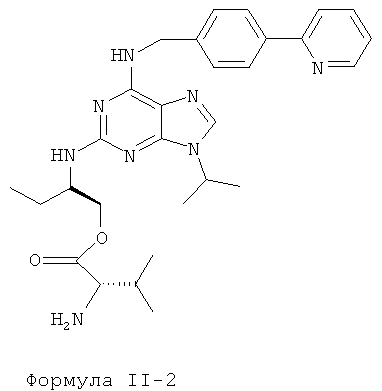
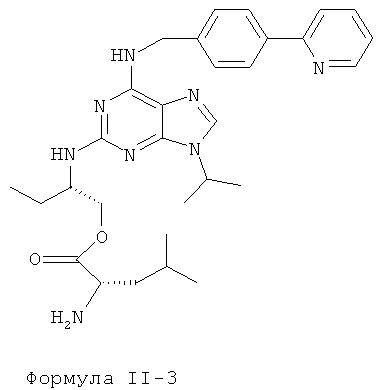
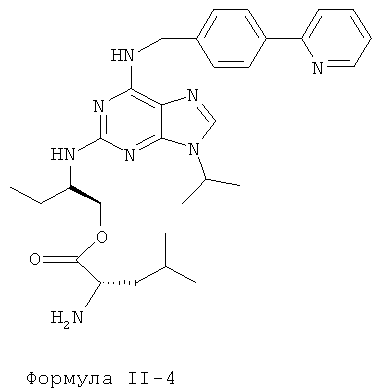
Данные эфиры являются веществами-предшественниками (пролекарствами) продуктов формулы I.
Их применение для изготовления лекарственных препаратов, предназначенных для лечения патологий, при которых наблюдается нарушение баланса между клеточным делением и апоптозом, также является объектом изобретения.
Для лучшего понимания сущности изобретения, а также его особенностей и преимуществ, ниже приведены поясняющее описание и ссылки на фигуры:
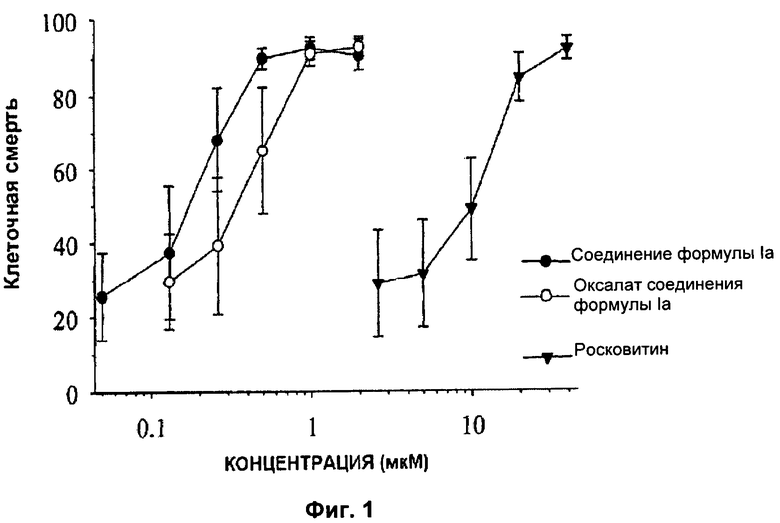
- на Фиг.1 показана стимуляция клеточной смерти соединением формулы Ia и оксалатной соли соединения формулы Ia в клетках хронической лимфоцитарной лейкемии, по сравнению со стимуляцией клеточной смерти росковитином.
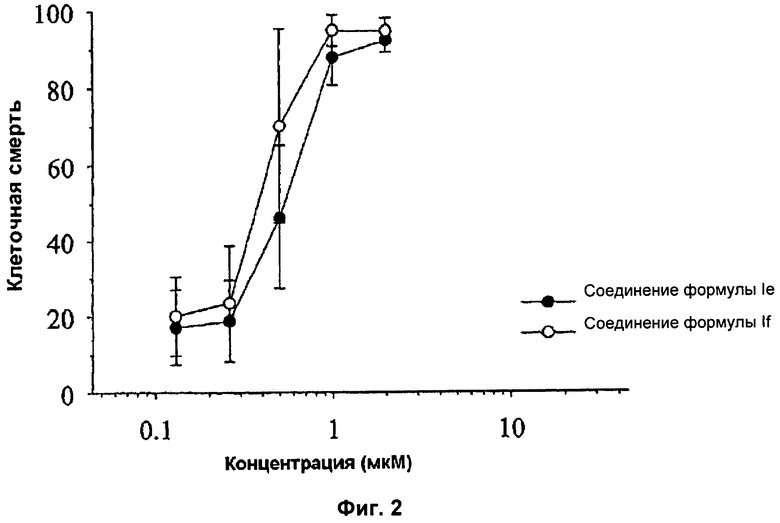
- на Фиг.2 показана стимуляция клеточной смерти соединениями формулы Ie и If в клетках хронической лимфоцитарной лейкемии.
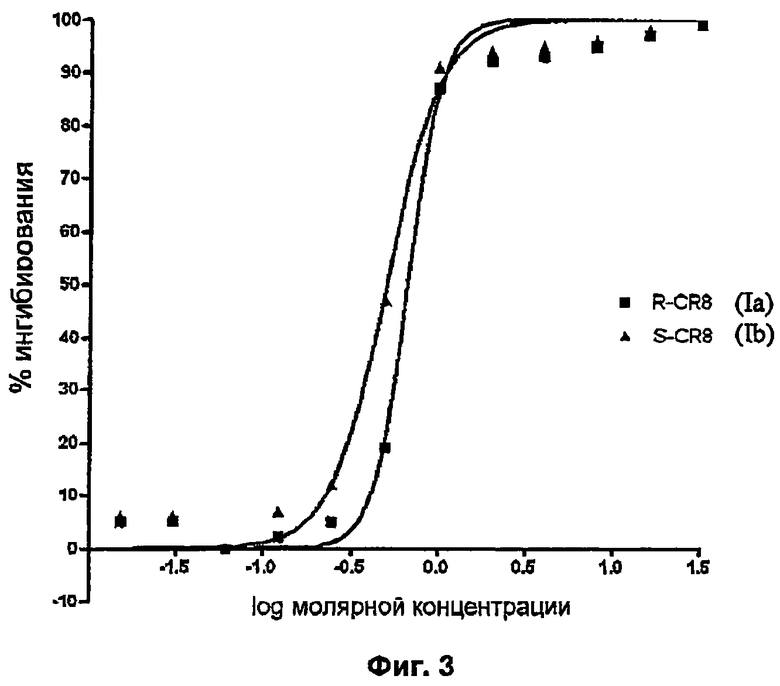
- на Фиг.3 показано ингибирование пролиферации клеток MDCK (клетки Мадин-Дарби почек собак) соединениями (Ib) и (Ia).
Действие росковитина и соединения формулы Ia, а также оксалатной соли исследовали в анализах киназной активности при различных концентрациях.
Исследования выполняли следующим образом:
Буферные растворы:
Буфер А: 10 мМ MgCl2, 1 мМ ЭГТА (этиленгликольтетрауксусная кислота), 1 мМ ДТТ (дитиотреитол), 25 мМ трис-HCl рН 7,5, 50 мкг гепарина/мл.
Буфер С: 60 мМ глицерофосфата, 15 мМ п-нитрофенилфосфата, 25 мМ МОПС (3-N-морфолинпропансульфоновая кислота) (pH 7,2), 5 мМ ЕГТА, 15 мМ MgCl2, 1 мМ ДТТ, 1 мМ ванадата натрия, 1 мМ фенилфосфата.
Подготовка и анализ киназной активности:
Киназную активность анализировали в буфере А или C при 30°C и конечной концентрации АТФ 15 мкМ. Контроль выполняли с соответствующим разведениями диметилсульфоксидом.
CDK1/циклин В (овоциты морской звезды N-фаза, нативные) и CDK5/p25 (человеческий, рекомбинантный) получали и анализировали как описано в работе Leclerc S. et al., J. Biol. Chem., 2001, 276, 251-60. Исследование проводили с 1 мг гистона Н1/мл в присутствии 15 мкМ [γ-33P] АТФ (3000 Кюри/моль; 10 мКюри/мл) в конечным объеме 30 мкл. После инкубирования при 30°C в течение 30 мин наносили аликвоты надосадочной жидкости по 25 мкл на кусочки фосфоцеллюлозной бумаги Р8 Whatman размером 2,5×3 см, а затем, спустя 20 секунд, фильтры промывали 5 раз в растворе 10 мл фосфорной кислоты/литр. Фильтры далее считали в присутствии 1 мл сцинтилляционной жидкости ACS (Amersham). CDK2/циклин А и CDK2/циклин Е (человеческий, рекомбинантный, экспрессирующийся в клетках насекомых) анализировали как и CDK1. CDK9/циклин Т (человеческий, рекомбинантный, экспрессирующийся в клетках насекомых) анализировали как и CDK1/циклин В, с фрагментом pRB (АА773-928) (3,5 мкг/анализ) в качестве субстрата.
GSK-3 α/β (мозг свиньи, природный, аффинно-очищенный) анализировали подобно CDK1/циклин В, но в буфере А и со специфическим GSK-3 субстратом (GS-1: YRRAAVPPSPSLSRHSSPHQSpEDEEE) (Bach S. et al, J. Biol. Chem, 2005, 280, 31208-19).
СК1δ/е (мозг свиньи, природный, аффинно очищенный) анализировали подобно CDKI/циклин В, но в буфере А и со специфическим субстратом RRKHAAIGSpAYSITA(ReinhardtJ. et al., Protein Expr.&Purif., 2007, 54, 101-9).
DYRK1A (человеческий, рекомбинантный, экспрессирующийся в клетках кишечной палочки) анализировали подобно CDK1/циклин В.
Средние значения ингибирующей концентрации IC50 рассчитывались из кривых доза/ответ и перечислены в единицах мкМ в Таблице 1, приведенной ниже.
Как видно из Таблицы 1, в случае всех протеинкиназ, соединение формулы Ib, его (S)-конфигурация проявляет ингибирующую активность для различных киназ, схожую с активностью росковитина, которая немного ниже активности соединения формулы Ia, по сравнению с абсолютной R-конфигурацией его гомолога.
Однако, неожиданно было обнаружено, что соединение формулы Ia и его оксалатная соль, а также соединения формулы Ie и If, которые тестировали на В-клетках с хронической лимфоцитарной лейкемией, взятых у пациентов с таким типом хронической лимфоцитарной лейкемией, проявляют активность в отношении стимуляции апоптоза клеток ХЛЛ гораздо большую, примерно в 50-100 раз, по сравнению с активностью росковитина, как это видно из Фиг.1 и 2.
Кроме того, действие соединений Ia, Ib, Ic, Id, Ie и If, а также оксалатной соли соединения Ia на стимуляцию клеточной смерти В2 лимфоцитов, взятых у пациентов, оказалось сравнимым с действием (R)-росковитина.
В2 лимфоциты представляют собой лимфоциты, участвующие в В2-клеточной хронической лимфоцитарной лейкемии.
Жизнеспособность клеток определяли по восстановлению 3-(4,5-диметилтиазол-2-ил)-5-(3-карбоксиметоксифенил)-2-(4-сульфофенил)-2Н-тетразолиума (MTS).
Клеточную смерть определяли путем измерения уровня активности лактатдегидрогеназы (LDH), высвобождаемой во время клеточного лизиса. Два этих процесса подробно описаны в источнике «Ribas J. and Boix J., Cell differentiation, caspase inhibition, and macromolecular synthesis blockage, but not BCL-2 or BCL-XL proteins protect SH-SY5Y cells from apoptosis triggered by two inhibitory drugs. Exp.Cell Res., 2004, 295, 9-24».
Полученные результаты приведены ниже в Таблице 2:
Величины, приведенные в Таблице 2, являются средней ингибирующей концентрацией IC50, выраженной в мкМ.
Действие соединений Ib и Id по настоящему изобретению при заболевании почечный поликистоз также исследовали на линии клеток Мадин-Дарби почек собак (MDCK) в сравнении с росковитином. Соединения Ib и Id в 50-60 раз более активны по сравнению с росковитином.
Растворимость соединений по изобретению в воде, где Х является N, как было сказано, в 5-10 превышает растворимость соединения, где Х является С.
Так, соединение формулы Ic, где Х является С, обладает растворимостью в воде равной 0,5 мкг/мл, в то время как соответствующее ему соединение, где Х представляет собой N, т.е. соединение формулы Ia, обладает растворимостью в воде 3,3 мкг/мл.
Соединения формулы Ib-Ih, по существу, также являются объектом настоящего изобретения.
Сложные эфиры соединений формулы I также являются объектом настоящего изобретения.
Предпочтительными сложными эфирами соединения формулы I являются эфиры карбоновых кислот, такие как ацетиловые эфиры, эфиры никотиновой кислоты, а также эфиры аминокислот L-формы или D.
Предпочтительные сложные эфиры образованы из аминокислот, таких как валин или лейцин.
Наиболее предпочтительные сложные эфиры характеризуются формулами II-1-II-4, приведенными ниже:
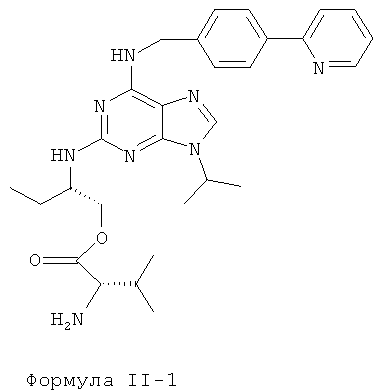
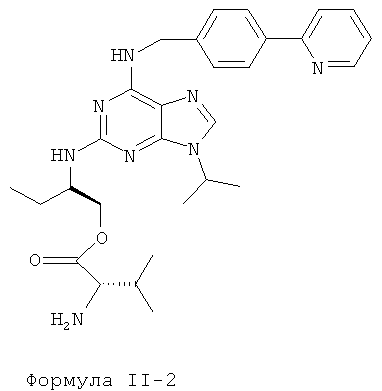
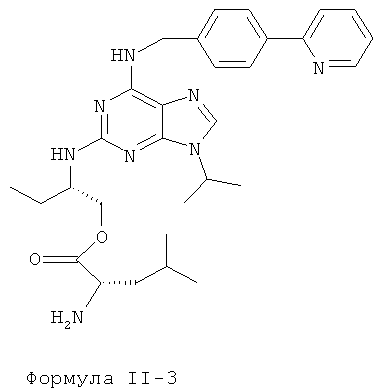
Данные эфиры являются веществами-предшественниками (пролекарствами) продуктов формулы I.
Так, соединения по изобретению, являются особенно эффективными для использования при изготовлении лекарственных препаратов, предназначенных для лечения хронической лимфоцитарной лейкемии. Они также являются особенно применимыми для введения согласно способу лечения пациентов с хронической лимфоцитарной лейкемией.
Данные соединения также являются особенно эффективными для использования при изготовлении лекарственных препаратов для лечения почечных заболеваний и, в частности, поликистоза почек. Также, они являются особенно применимыми для введения согласно способу лечения пациентов с заболеваниями почек, в частности, поликистозом почек.
Специалисты в данной области техники могут легко определить, что соединения по изобретению могут быть использованы в виде смеси одного соединения с другим, двух или нескольких соединений, а также в сочетании с другими соединениями, обладающими терапевтической активностью при лечении хронической лимфоцитарной лейкемии или почечных заболеваний, таких как поликистоз почек, и/или в сочетании с любыми фармацевтически приемлемыми вспомогательными веществами при изготовлении лекарственных препаратов, при этом подобные сочетания и смеси также входят в объем изобретения.
Соединения (II) и (III), раскрытые в WO 9805335 (см. таблицу 1 на стр.30 и таблицу 3 на стр.40) по структуре наиболее близки соединениям по настоящему изобретению.
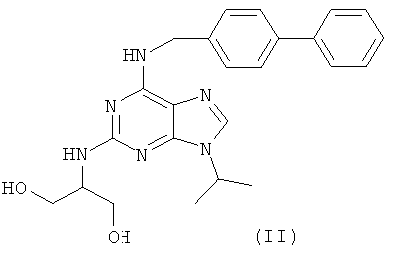
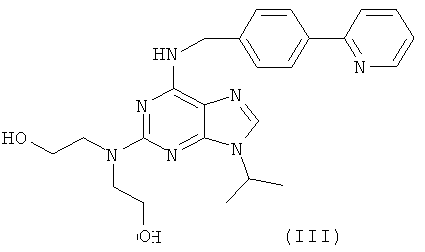
Ниже в таблице 3 приведены данные сравнительного анализа ингибирующей активности соединений (II) и (III) и соединений по изобретению в отношении киназ.
Приведенные данные показывают, что
- соединения по изобретению превосходят известное соединение (II) в ингибировании киназы CDK5, которая вовлечена в развитие поликистоза почек,
- соединения по изобретению превосходят известное соединение (III) в отношении селективности к киназе GSK-3 (аффинность к этой киназе вызывает вредный побочный эффект, поскольку она является канцерогеном).
В анализе на линии клеток Мадин-Дарби почек собак (MDCK), которая является клеточной моделью для поликистоза почек, проведенном как описано выше в настоящем описании, соединение (Ib) (S-CR8) проявило себя как более эффективное по сравнению с соединением структуры (Ia) (R-CR8). Результаты представлены на Фиг.3. Полученные результаты являются тем более неожиданными, поскольку для известного ингибитора киназ, используемого для сравнения, росковитина, энантиомер (R), наоборот, является существенно более активным по сравнению с S энантиомером.
Авторы изобретения также проводили сравнительные испытания Ia и Ib в отношении хронической лимфоцитарной лейкемии.
Способность выбранных ингибиторов киназ индуцировать клеточную гибель тестировали на выделенных лимфоцитах, полученных от пациентов с хронической лимфоцитарной лейкемией, не получавших предварительного лечения (n=5). Жизнеспособность клеток измеряли, используя проточную цитометрию, чтобы исключить аннексии V- и PI (пропидиум иодид)-положительные клетки с последующей 24 часовой обработкой ингибитором. Значения IC50, вычисленные на основании кривых зависимости "доза-эффект", приведены в µ моль. В указанном испытании соединение (Ib) оказалось в 2 раза более эффективным чем соединение (Ia). Для Ia IC50 составляла 0,18 µ моль, тогда как для Ib IC50 составляла 0,09 µ моль.
Изобретение относится к химико-фармацевтической промышленности, а именно к применению производных пурина при изготовлении лекарственных препаратов, предназначенных для лечения хронической лимфоцитарной лейкемии и поликистоза почек. Изобретение обеспечивает получение соединений, обладающих большей активностью в отношении лимфоцитарной лейкемии и поликистоза почек. 4 н. и 4 з.п. ф-лы, 3 ил., 1 пр., 3 табл.
1. Применение по меньшей мере одного соединения, выбранного среди следующих соединений:
соединения формулы Id:
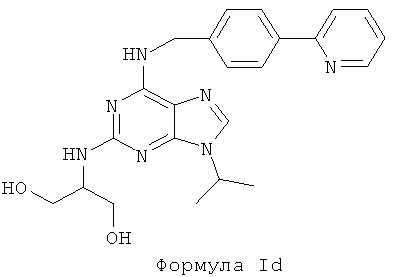
или одной из его фармацевтически приемлемых солей, гидратов или сложных эфиров,
соединения формулы Ie:

или одной из его фармацевтически приемлемых солей, гидратов или сложных эфиров,
соединения формулы Ig:

или одной из его фармацевтически приемлемых солей или гидратов,
и соединения формулы Ib:
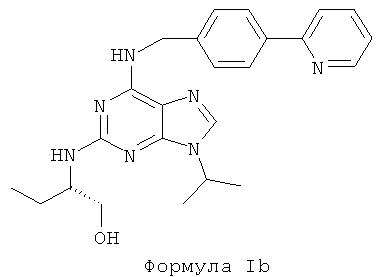
или одной из его фармацевтически приемлемых солей, гидратов или сложных эфиров,
при изготовлении лекарственного препарата, предназначенного для лечения хронической лимфоцитарной лейкемии или поликистоза почек.
2. Применение по п.1, отличающееся тем, что хроническая лимфоцитарная лейкемия представляет собой B-клеточную хроническую лимфоцитарную лейкемию.
3. Применение по любому из пп.1 или 2, отличающееся тем, что фармацевтически приемлемая соль представляет собой оксалат или тартрат, либо гидрохлорид или фумарат.
4. Применение по любому из пп.1-3, отличающееся тем, что по меньшей мере одно соединение представляет собой соединение формулы Ib:

или одну из его фармацевтически приемлемых солей, гидратов или сложных эфиров.
5. Применение по п.4, отличающееся тем, что по меньшей мере одно соединение представляет собой оксалат соединения формулы Ib.
6. Соединение формулы Ib:

или одна из его солей, гидратов или сложных эфиров.
7. Соединение формулы Id:

или одна из его солей, гидратов или сложных эфиров
или формулы Ie:

или его соли, гидраты или сложные эфиры,
или формулы If:

или формулы Ig:

или одна из его солей, гидратов или сложных эфиров,
или формулы Ih:

8. Соединение, отличающееся тем, что оно имеет формулы II-1 или II-3, приведенные ниже:


| WO 03022805 A2, 20.03.2003 | |||
| WO 9805335 A1, 12.02.1998 | |||
| WO 03002565 A1, 09.01.2003 | |||
| WO 2005016528 A2, 24.02.2005 | |||
| JP 11335298 A, 07.12.1999. |
Авторы
Даты
2013-12-10—Публикация
2008-09-12—Подача