Настоящее изобретение относится к новым соединениям, способу получения этих соединений и относящихся к ним промежуточных соединений, применению соединений и фармацевтическим композициям, содержащим их. Эти соединения полезны в терапии, в частности, для лечения боли, тревоги и депрессии.
Дельта (δ) рецептор был идентифицирован как рецептор, играющий роль во многих функциях организма, таких как ноцицептивная, моторная и сердечно-сосудистая системы, а также в регулировании эмоций. Поэтому лиганды δ рецептора могут найти потенциальное применение в качестве анальгетиков, анксиолитиков и/или гипотензивных агентов. Также было показано, что лиганды δ рецептора обладают иммуномодулирующими активностями.
В настоящее время точно идентифицированы по меньшей мере три разные популяции опиоидных рецепторов (µ, δ и κ), и все три выявлены как в центральной, так и в периферической нервной системах многих видов, включая человека. При активации одного или более чем одного из этих рецепторов в различных моделях на животных наблюдались аналгезия и седативное действие. В общем, селективные лиганды δ рецептора обладают преимуществами по сравнению с неселективными лигандами опиоидных рецепторов, вызывая менее значительные побочные эффекты.
Многие соединения, представляющие собой δ-агонисты, идентифицированные в предшествующем уровне техники, обладают множеством недостатков, которые заключаются в том, что соединения имеют плохую фармакокинетику и не оказывают ни анксиолитического, ни аналитического действия при введении системными путями.
В РСТ публикации WO 01/74806 описаны некоторые δ-агонисты.
Однако все еще существует необходимость в улучшенных δ-агонистах.
Авторы изобретения неожиданно обнаружили, что некоторые соединения проявляют одно или более чем одно улучшенное свойство, то есть улучшенные эффективность в качестве δ-агонистов, эффективность in vivo, фармакокинетику, биодоступность, стабильность in vitro, стабильность in vivo, проникновение в головной мозг и/или более низкую токсичность.
В настоящей заявке описан N-(2-гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамид.
Далее в настоящей заявке описан N-(2-гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамид, его фармацевтически приемлемые соли, его пролекарства, его сольваты и/или их смеси.
Кроме того, в настоящей заявке описан трет-бутил-4-((4-(N-(2-гидроксиэтил)-N-метилкарбамоил)фенил)(хинолин-8-ил)метилен)пиперидин-1-карбоксилат.
Кроме того, в настоящей заявке описан N-(2-гидроксиэтил)-N-метил-4-((пиперидин-4-илиден)(хинолин-8-ил)метил)бензамид.
Кроме того, в настоящей заявке также описаны способы получения N-(2-гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамида, трет-бутил-4-((4-(N-(2-гидроксиэтил)-N-метилкарбамоил)фенил)(хинолин-8-ил)метилен)пиперидин-1-карбоксилата и N-(2-гидроксиэтил)-N-метил-4-((пиперидин-4-илиден)(хинолин-8-ил)метил)бензамида.
Кроме того, в настоящей заявке также описана фармацевтическая композиция, содержащая N-(2-гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамид, его фармацевтически приемлемые соли, его пролекарства, его сольваты и/или их смеси совместно с фармацевтически приемлемым носителем.
Кроме того, в настоящей заявке также описан способ лечения боли, депрессии, тревоги, тревожной депрессии и/или болезни Паркинсона у теплокровного животного, включающий введение указанному животному, нуждающемуся в таком лечении, терапевтически эффективного количества N-(2-гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамида, его фармацевтически приемлемых солей, его пролекарств, его сольватов и/или их смесей.
Признаки и преимущества настоящего изобретения могут быть более легко понятны средним специалистам в данной области техники после прочтения следующего подробного описания. Следует понимать, что некоторые признаки изобретения, которые по причинам ясности изложения описаны выше и ниже в контексте отдельных воплощений, также могут быть объединены с образованием одного воплощения. Наоборот, различные признаки изобретения, которые из соображений краткости описаны в контексте одного воплощения, также могут быть объединены с образованием их субкомбинаций.
Если не оговорено особо в данном описании изобретения, ссылки, сделанные в единственном числе, также могут включать множественное число. Например, термины, которые указывают на неопределенное количество, могут относиться либо к одному, либо к одному или более чем к одному.
Подразумевают, что воплощения, определенные в данном описании изобретения как типичные, являются иллюстративными и не ограничивающими.
Если не указано особо, предполагают, что любой гетероатом с ненасыщенными валентностями имеет достаточное количество атомов водорода для насыщения валентностей.
Определения, сформулированные в данном описании изобретения, имеют преимущественное значение перед определениями, сформулированными в любом патенте, патентной заявке и/или публикации патентной заявки, которые могут быть включены в данное описание изобретения путем ссылки.
"Теплокровное животное" включает человека.
Термин "защищенный" означает, что соединение, на которое ссылаются как на защищенное, защищено аминозащитной группой. Например, защищенный N-(2-гидрокси-этил)-N-метил-4-(пиперидин-4-илиден-хинолин-8-ил-метил)-бензамид представляет собой N-(2-гидрокси-этил)-N-метил-4-(пиперидин-4-илиден-хинолин-8-ил-метил)-бензамид, который имеет по меньшей мере одну аминогруппу, защищенную аминозащитной группой.
Термин "аминозащитная группа" относится к общепризнанным в данной области техники группировкам, способным присоединяться к аминогруппе для предотвращения участия аминогруппы в реакциях, происходящих с каким-либо другим участком молекулы, содержащей аминогруппу.
Подходящие аминозащитные группы включают, например, аминозащитные группы, описанные в "Protective Groups in Organic Synthesis" (2nd edition, John Wiley & Sons, 1991), но не ограничиваются ими. Аминозащитная группа может, например, представлять собой защитную группу уретанового типа (которую также называют карбаматной защитной группой), включая, без ограничения, арилалкилоксикарбонильные группы, такую как, например, бензилоксикарбонил, и алкоксикарбонильные группы, такие как, например, метоксикарбонил и трет-бутоксикарбонил. Типично аминозащитная группа представляет собой трет-бутоксикарбонил.
В одном из аспектов настоящего изобретения предложен N-(2-гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамид, его фармацевтически приемлемые соли, его пролекарства, его сольваты и их смеси.
В одном из воплощений соединение по настоящему изобретению может быть выбрано из N-(2-гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамида, его фармацевтически приемлемых солей, его сольватов и их смесей.
В другом воплощении соединение по настоящему изобретению может быть выбрано из N-(2-гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамида, его фармацевтически приемлемых солей и их смесей.
В дополнительном воплощении соединение по настоящему изобретению может быть выбрано из N-(2-гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамида.
Также будет понятно, что некоторые соединения по настоящему изобретению могут существовать как в сольватированных, например гидратированных, так и в несольватированных формах. Кроме того, будет понятно, что настоящее изобретение охватывает все такие сольватированные формы этого соединения.
В объем изобретения также входят соли этого соединения. В общем, фармацевтически приемлемые соли соединения по настоящему изобретению могут быть получены с использованием стандартных методик, хорошо известных в данной области техники, например путем взаимодействия достаточно основного соединения, например алкиламина, с подходящей кислотой, например HCl или уксусной кислотой, способной предоставить физиологически приемлемый анион. Также возможно получение соответствующей соли щелочного металла (такого как натрий, калий или литий) или щелочно-земельного металла (такого как кальций) путем обработки соединения по настоящему изобретению, имеющего подходящий кислый протон, такого как карбоновая кислота или фенол, одним эквивалентом гидроксида или алкоксида (такого как этоксид или метоксид) щелочного металла или щелочно-земельного металла, либо подходящего основного органического амина (такого как холин или меглумин) в водной среде с последующей очисткой традиционными методами.
В одном из воплощений описанное выше соединение может быть превращено в фармацевтически приемлемую соль или ее сольват, в частности соль присоединения кислоты, такую как гидрохлорид, гидробромид, фосфат, ацетат, фумарат, малеат, тартрат, цитрат, метансульфонат или п-толуолсульфонат.
Соединения по настоящему изобретению полезны в лечении, в особенности для лечения различных болевых состояний, таких как, например, хроническая боль, невропатическая боль, острая боль, раковая боль, боль, вызванная ревматоидным артритом, мигрень, висцеральная боль и так далее. Однако этот список не следует понимать как исчерпывающий.
Соединения по настоящему изобретению полезны при лечении тревоги, такой как, например, паническое расстройство, паническое расстройство без агорафобии, паническое расстройство с агорафобией, агорафобия без панического расстройства в анамнезе, специфическая фобия, социальная фобия, социальное тревожное расстройство, обсессивно-компульсивное расстройство, расстройства, связанные со стрессом, посттравматическое стрессовое расстройство, острое стрессовое расстройство, расстройство генерализованной тревоги или расстройство генерализованной тревоги, обусловленное общим медицинским состоянием.
По меньшей мере одно воплощение настоящего изобретения полезно для лечения депрессии, такой как, например, тревожная депрессия, большое депрессивное расстройство, дистимическое расстройство, биполярная депрессия и/или биполярная мания, биполярное расстройство I типа с маниакальными, депрессивными или смешанными эпизодами или без них, биполярное расстройство II типа, циклотимическое расстройство, расстройство настроения, обусловленное общим медицинским состоянием, маниакальные эпизоды, ассоциируемые с биполярным расстройством, и смешанные эпизоды, ассоциируемые с биполярным расстройством.
Соединения по изобретению полезны для лечения диареи, депрессии, тревоги и/или расстройств, связанных со стрессом, таких как посттравматические стрессовые расстройства, паническое расстройство, расстройство генерализованной тревоги, социальная фобия и обсессивно-компульсивное расстройство, недержания мочи, преждевременной эякуляции, различных психических заболеваний, кашля, отека легких, различных желудочно-кишечных расстройств, например запора, функциональных желудочно-кишечных расстройств, таких как синдром раздраженного кишечника и функциональная диспепсия, болезни Паркинсона и других моторных расстройств, травматического повреждения головного мозга, удара, для защиты сердца после инфаркта миокарда, для лечения повреждения спинного мозга и привыкания к чрезмерному употреблению лекарственных средств, включая лечение алкогольной, никотиновой, опиоидной и иной наркотической зависимости, а также для расстройств симпатической нервной системы, например гипертензии.
Соединения по изобретению полезны в качестве иммуномодуляторов, в особенности при аутоиммунных заболеваниях, таких как артрит, при трансплантациях кожи, трансплантациях органов и для подобных хирургических нужд, при коллагенозах, различных аллергиях, для применения в качестве противоопухолевых агентов и противовирусных агентов.
Соединения по изобретению полезны при болезненных состояниях, при которых имеет место или в которые вовлечена дегенерация или дисфункция опиоидных рецепторов. Это может включать применение меченных изотопами вариантов соединений по изобретению в диагностических методиках и при осуществлении визуализации, например позитронной эмиссионной томографии (ПЭТ).
Соединения по изобретению полезны в качестве болеутоляющего агента для применения во время общей анестезии и для анестезиологического пособия с мониторингом. Комбинации агентов с различными свойствами часто применяют для достижения баланса эффектов, необходимых для поддержания состояния анестезии (например, амнезии, аналгезии, мышечной релаксации и седативного эффекта). В такую комбинацию включают ингаляционные анестезирующие средства, снотворные средства, анксиолитики, миелорелаксанты и опиоиды.
В объем изобретения входит применение любого соединения, определенного выше, для изготовления лекарственного средства.
Также в объем изобретения входит применение любого соединения по изобретению для изготовления лекарственного средства для лечения боли, включая, без ограничения, острую боль, хроническую боль, невропатическую боль, боль в спине, раковую боль и висцеральную боль.
Также в объем изобретения входит применение любого соединения по изобретению для изготовления лекарственного средства для лечения тревоги, включая, без ограничения, паническое расстройство, паническое расстройство без агорафобии, паническое расстройство с агорафобией, агорафобию без панического расстройства в анамнезе, специфическую фобию, социальную фобию, социальное тревожное расстройство, обсессивно-компульсивное расстройство, посттравматическое стрессовое расстройство, острое стрессовое расстройство, расстройство генерализованной тревоги или расстройство генерализованной тревоги, обусловленное общим медицинским состоянием.
Также в объем изобретения входит применение любого соединения по изобретению для изготовления лекарственного средства для лечения депрессии, такой как, например, большое депрессивное расстройство, дистимическое расстройство, биполярная депрессия и/или биполярная мания, биполярное расстройство I типа с маниакальными, депрессивными или смешанными эпизодами или без них, биполярное расстройство II типа, циклотимическое расстройство, расстройство настроения, обусловленное общим медицинским состоянием, маниакальные эпизоды, ассоциируемые с биполярным расстройством, и смешанные эпизоды, ассоциируемые с биполярным расстройством.
Также в объем изобретения входит применение любого соединения по изобретению для изготовления лекарственного средства для лечения тревожной депрессии.
Также в объем изобретения входит применение любого соединения по изобретению для изготовления лекарственного средства для лечения болезни Паркинсона.
Также в объем изобретения входит применение любого из соединений по настоящему изобретению для изготовления лекарственного средства для лечения любого из состояний, рассмотренных выше.
Дополнительным аспектом изобретения является способ лечения субъекта, страдающего от любого из состояний, рассмотренных выше, при котором пациенту, нуждающемуся в таком лечении, вводят эффективное количество соединения по настоящему изобретению.
Таким образом, согласно изобретению предложено соединение или его фармацевтически приемлемые соль или сольват, такие как определено выше, для применения в лечении.
В контексте настоящего описания изобретения термин "лечение" также включает "профилактику", если нет конкретных указаний обратного. Термин "терапевтический" и "терапевтически" следует толковать соответственно. Термин "лечение" в контексте настоящего изобретения также охватывает введение эффективного количества соединения по настоящему изобретению для облегчения либо ранее существовавшего болезненного состояния, острого или хронического, либо рецидивирующего состояния. Это определение также охватывает профилактическое лечение для предотвращения рецидивирующих состояний и непрерывное лечение для хронических расстройств.
В еще одном воплощении соединение по настоящему изобретению или фармацевтическую композицию либо препарат, содержащие по меньшей мере одно соединение по настоящему изобретению, можно вводить одновременно, совместно, последовательно или раздельно с по меньшей мере одним другим фармацевтически активным соединением, выбранным из нижеследующего:
(1) антидепрессантов, включая, например, агомелатин, амитриптилин, амоксапин, бупропион, циталопрам, кломипрамин, дезипрамин, доксепин, дулоксетин, элзасонан, эсциталопрам, флувоксамин, флуоксетин, гепирон, имипрамин, ипсапирон, мапротилин, нортриптилин, нефазодон, пароксетин, фенелзин, протриптилин, рамелтеон, ребоксетин, робалзотан, сертралин, сибутрамин, тионизоксетин, транилципромаин, тразодон, тримипрамин, венлафаксин и их эквиваленты, и фармацевтически активный(е) изомер(ы): и метаболит(ы), но не ограничиваясь ими;
(2) атипичных антипсихотических средств, включая, например, кветиапин и его фармацевтически активный(е) изомер(ы) и метаболит(ы), но не ограничиваясь ими;
3) антипсихотических средств, включая, например, амисулприд, арипипразол, азенапин, бензизоксидил, бифепрунокс, карбамазепин, клозапин, хлорпромазин, дебензапин, дивалпроекс, дулоксетин, эсзопиклон, галоперидол, илоперидон, ламотригин, локсапин, мезоридазин, оланзапин, палиперидон, перлапин, перфеназин, фенотиазин, фенилбутилпиперидин, пимозид, прохлорперазин, рисперидон, сертиндол, сульпирид, супроклон, тиоридазин, трифлуоперазин, триметозин, вальпроат, вальпроевую кислоту, зопиклон, зотепин, зипразидон и их эквиваленты и фармацевтически активный(е) изомер(ы) и метаболит(ы), но не ограничиваясь ими;
(4) анксиолитиков, включая, например, алнеспирон, азапироны, бензодиазепины, барбитураты, такие как адиназолам, альпразолам, балезепам, бентазепам, бромазепам, бротизолам, буспирон, клоназепам, клоразепат, хлордиазепоксид, ципразепам, диазепам, дифенгидрамин, эстазолам, фенобам, флунитразепам, флуразепам, фосазепам, лоразепам, лорметазепам, мепробамат, мидазолам, нитразепам, оксазепам, празепам, квазепам, реклазепам, траказолат, трепипам, темазепам, триазолам, улдазепам, золазепам и их эквиваленты, и фармацевтически активный(е) изомер(ы), и метаболит(ы), но не ограничиваясь ими;
(5) противосудорожных средств, включая, например, карбамазепин, вальпроат, ламотрогин, габапентин и их эквиваленты, и фармацевтически активный(е) изомер(ы), и метаболит(ы), но не ограничиваясь ими;
(6) лекарственных средств для лечения болезни Альцгеймера, включая, например, донезепил, мемантин, такрин и их эквиваленты, и фармацевтически активный(е) изомер(ы), и метаболит(ы), но не ограничиваясь ими;
(7) лекарственных средств для лечения болезни Паркинсона, включая, например, депренил, L-допа, Requip, Mirapex, ингибиторы МАОВ (моноаминооксидазы Б) (то есть селегин и расагилин), ингибиторы сотР (катехол-O-метилтрансферазы) (то есть Тасмар), ингибиторы A-2, ингибиторы обратного захвата дофамина, антагонисты NMDA (N-метил-D-аспартат), агонисты никотина, агонисты дофамина и ингибиторы нейрональной синтазы оксида азота и их эквиваленты, и фармацевтически активный(е) изомер(ы), и метаболит(ы), но не ограничиваясь ими;
(8) лекарственных средств для лечения мигрени, включая, например, алмотриптан, амантадин, бромкриптин, буталбитал, каберголин, дихлоральфеназон, элетриптан, фроватриптан, лизурид, наратриптан, перголид, прамипексол, ризатриптан, ропинирол, суматриптан, золмитриптан, зомитриптан и их эквиваленты, и фармацевтически активный(е) изомер(ы), и метаболит(ы), но не ограничиваясь ими;
(9) лекарственных средств для лечения удара, включая, например, абциксимаб, активазу, NXY-059, цитиколин, кробенетин, десмотеплазу, репинотан, траксопродил и их эквиваленты, и фармацевтически активный(е) изомер(ы), и метаболит(ы), но не ограничиваясь ими;
(10) лекарственных средств для лечения недержания мочи, включая, например, дарафенацин, фалвоксат, оксибутинин, пропиверин, робалзотан, солифенацин, толтеродин и их эквиваленты, и фармацевтически активный(е) изомер(ы), и метаболит(ы), но не ограничиваясь ими;
(11) лекарственных средств для лечения невропатической боли, включая, например, габапентин, лидодерм, прегаблин и их эквиваленты, и фармацевтически активный(е) изомер(ы), и метаболит(ы), но не ограничиваясь ими;
(12) лекарственных средств для лечения ноцицептивной боли, включая, например, целекоксиб, эторикоксиб, лумиракоксиб, рофекоксиб, валдекоксиб, диклофенак, локсопрофен, напроксен, парацетамол и их эквиваленты, и фармацевтически активный(е) изомер(ы), и метаболит(ы), но не ограничиваясь ими;
(13) лекарственных средств для лечения бессонницы, включая, например, агомелатин, аллобарбитал, алонимид, амобарбитал, бензоктамин, бутабарбитал, капурид, хлораль, клоперидон, клоретат, декскламол, эсзопиклон, этхлорвинол, этомидат, глутетимид, галазепам, гидроксизин, меклоквалон, мелатонин, мефобарбитал, метаквалон, мидафлур, низобамат, пентобарбитал, фенобарбитал, пропофол, рамелтеон, ролетамид, триклофос, секобарбитал, залеплон, золпидем и их эквиваленты, и фармацевтически активный(е) изомер(ы), и метаболит(ы), но не ограничиваясь ими, и
(14) стабилизаторов настроения, включая, например, карбамазепин, дивалпроекс, габапентин, ламотригин, литий, оланзапин, кветиапин, вальпроат, вальпроевую кислоту, верапрамил и их эквиваленты, и фармацевтически активный(е) изомер(ы), и метаболит(ы), но не ограничиваясь ими.
В таких комбинированных продуктах используют соединения по настоящему изобретению в диапазоне доз, раскрытом в данном описании изобретения, и другое фармацевтически активное соединение или соединения в согласованных диапазонах доз и/или в дозах, описанных в релевантой публикации.
При применении для лечения теплокровного животного, такого как человек, соединение по изобретению можно вводить в форме традиционной фармацевтической композиции любым путем, включая пероральный, внутримышечный, подкожный, местный, интраназальный, внутрибрюшинный, интраторакальный, внутривенный, эпидуральный, интратекальный, интрацеребровентрикулярный или инъекцией в суставы.
В одном из воплощений изобретения путь введения может быть пероральным, внутривенным или внутримышечным.
"Терапевтически эффективное количество" и/или диапазон доз для соединений по настоящему изобретению могут быть определены средним специалистом в данной области техники по известным критериям, включающим возраст, массу и реакцию индивидуального пациента, и интерпретирован в контексте заболевания, которое следует лечить и/или предотвратить. Количества типичных (однократной или разделенной) доз для млекопитающего могут составлять от примерно 0,05 до примерно 300 мг/кг в сутки.
Однако конкретный уровень дозы и частоту дозирования для каждого конкретного субъекта могут варьировать, и обычно они зависят от множества факторов, включая, например, биодоступность соединений по настоящему изобретению во вводимой форме; метаболическую стабильность и продолжительность действия конкретных соединений по настоящему изобретению; вид, возраст, массу тела, общее состояние здоровья, пол и диету субъекта; способ и время введения; скорость экскреции; лекарственную комбинацию и тяжесть конкретного состояния, а также любые другие факторы, обычно рассматриваемые лечащим врачом при определении индивидуального режима и уровня дозировки, который является наиболее подходящим для конкретного пациента, но не ограничиваясь ими.
Также предложена фармацевтическая композиция, содержащая соединение по настоящему изобретению, его сольваты или его фармацевтически приемлемую соль совместно с фармацевтически приемлемым носителем.
В частности, предложена фармацевтическая композиция, содержащая соединение по настоящему изобретению, его сольваты или его фармацевтически приемлемую соль совместно с фармацевтически приемлемым носителем для лечения, более конкретно для лечения боли и тревоги.
Кроме того, предложена фармацевтическая композиция, содержащая соединение по настоящему изобретению, его сольваты или его фармацевтически приемлемую соль совместно с фармацевтически приемлемым носителем для применения при любом из состояний, рассмотренных выше.
Кроме того, предложена фармацевтическая композиция, содержащая соединение по настоящему изобретению, его сольваты или его фармацевтически приемлемую соль совместно с фармацевтически приемлемым носителем для лечения депрессии.
Инертные фармацевтически приемлемые носители для приготовления фармацевтических композиций из соединений по настоящему изобретению могут быть либо твердыми, либо жидкими. Препараты в твердой форме включают порошки, таблетки, дисперсные гранулы, капсулы, облатки и суппозитории.
Твердым носителем может быть одно или более чем одно вещество, которые также могут действовать в качестве разбавителей, корригентов, солюбилизаторов, смазывающих веществ, суспендирующих агентов, связывающих веществ или разрыхлителей таблеток; носитель также может представлять собой инкапсулирующий материал.
В порошках носитель представляет собой тонкоизмельченное твердое вещество, которое находится в смеси с тонкоизмельченным соединением по изобретению или активным компонентом. В таблетках активный компонент смешан с носителем, имеющим необходимые связующие свойства, в подходящих пропорциях и спрессован в желаемую форму до желаемого размера.
Для приготовления суппозиторных композиций низкоплавкий воск, такой как смесь глицеридов жирных кислот и масла какао, сначала расплавляют и в нем диспергируют активный ингредиент, например, путем перемешивания. Затем расплавленную гомогенную смесь выливают в формы подходящего размера и оставляют стоять до охлаждения и затвердевания.
Подходящими носителями являются карбонат магния, стеарат магния, тальк, лактоза, сахар, пектин, декстрин, крахмал, трагакант, метилцеллюлоза, карбоксиметилцеллюлоза натрия, низкоплавкий воск, масло какао и тому подобное.
Термин композиция также предназначен для включения препарата активного компонента с инкапсулирующим материалом в качестве носителя, обеспечивающим получение капсулы, в которой активный компонент (с другими носителями или без них) окружен носителем, который таким образом находится в ассоциации с ним. Аналогичным образом охвачены облатки.
Таблетки, порошки, облатки и капсулы можно применять в твердых лекарственных формах для перорального введения.
Композиции в жидкой форме включают растворы, суспензии и эмульсии. Например, стерильные водные или водно-пропиленгликолевые растворы активных соединений могут представлять собой жидкие препараты, подходящие для парентерального введения. Жидкие композиции также могут быть приготовлены в виде раствора в водно-полиэтиленгликолевом растворе.
Водные растворы для перорального ведения могут быть приготовлены путем растворения активного компонента в воде и добавления, если требуется, подходящих красителей, корригентов, стабилизаторов и загустителей. Водные суспензии для перорального применения могут быть изготовлены путем диспергирования тонкоизмельченного активного компонента в воде вместе с вязким материалом, таким как натуральные синтетические камеди, смолы, метилцеллюлоза, карбоксиметилцеллюлоза натрия и другие суспендирующие агенты, известные в области приготовления фармацевтических препаратов.
В зависимости от пути введения фармацевтическая композиция будет предпочтительно содержать от 0,05 до 99 мас.%, (процент по массе), более предпочтительно от 0,10 до 50 мас.%, соединения по изобретению, причем все проценты по массе рассчитаны по отношению к общей массе композиции.
В дополнительном аспекте настоящего изобретения предложен способ получения соединений по настоящему изобретению.
В одном из воплощений изобретения предложен способ получения N-(2-гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамида, включающий взаимодействие N-(2-гидроксиэтил)-N-метил-4-(пиперидин-4-илиден-хинолин-8-ил-метил)бензамида с 4-тиазолкарбоксальдегидом в присутствии восстановителя, такого как триацетоксиборогидрид натрия или борогидрид натрия.
В другом воплощении изобретения предложен способ получения N-(2-гидрокси-этил)-N-метил-4-(пиперидин-4-илиден-хинолин-8-ил-метил)бензамида, включающий взаимодействие защищенного 4-(бром-{4-[(2-гидрокси-этил)-метил-карбамоил]-фенил}-метилен)-пиперидина с 8-хинолинбороновой кислотой с образованием защищенного N-(2-гидрокси-этил)-N-метил-4-(пиперидин-4-илиден-хинолин-8-ил-метил)-бензамида и снятие защиты с указанного защищенного N-(2-гидрокси-этил)-N-метил-4-(пиперидин-4-илиден-хинолин-8-ил-метил)-бензамида.
В конкретном воплощении указанный защищенный 4-(бром-{4-[(2-гидрокси-этил)-метил-карбамоил]-фенил}-метилен)-пиперидин защищен группой трет-Boc по положению 1 пиперидина.
В конкретном воплощении указанный защищенный N-(2-гидрокси-этил)-N-метил-4-(пиперидин-4-илиден-хинолин-8-ил-метил)-бензамид защищен группой трет-Boc по положению 1 пиперидина.
В дополнительном воплощении изобретения предложен способ получения защищенного 4-(бром-{4-[(2-гидрокси-этил)-метил-карбамоил]-фенил}-метилен)-пиперидина, включающий взаимодействие 2-(метиламино)этанола с защищенным 4-[бром-(4-карбокси-фенил)-метилен]-пиперидином.
В конкретном воплощении указанный защищенный 4-(бром-{4-[(2-гидрокси-этил)-метил-карбамоил]-фенил}-метилен)-пиперидин защищен группой трет-Boc по положению 1 пиперидина.
В конкретном воплощении указанный защищенный 4-[бром-(4-карбокси-фенил)-метилен]-пиперидин защищен группой трет-Boc по положению 1 пиперидина.
Другое воплощение относится к способу получения защищенного N-(2-гидрокси-этил)-N-метил-4-(пиперидин-4-илиден-хинолин-8-ил-метил)-бензамида, включающий взаимодействие защищенного 4-(бром-{4-[(2-гидрокси-этил)-метил-карбамоил]-фенил}-метилен)-пиперидина с 8-хинолинбороновой кислотой.
Еще одно другое воплощение относится к способу снятия защиты с защищенного N-(2-гидрокси-этил)-N-метил-4-(пиперидин-4-илиден-хинолин-8-ил-метил)-бензамида с образованием N-(2-гидрокси-этил)-N-метил-4-(пиперидин-4-илиден-хинолин-8-ил-метил)-бензамида.
Еще одно дополнительное воплощение относится к взаимодействию N-(2-гидрокси-этил)-N-метил-4-(пиперидин-4-илиден-хинолин-8-ил-метил)-бензамида с тиазол-4-карбальдегидом с образованием N-(2-гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамида.
В одном из воплощений указанный защищенный N-(2-гидрокси-этил)-N-метил-4-(пиперидин-4-илиден-хинолин-8-ил-метил)-бензамид защищен группой трет-Boc по положению 1 пиперидина.
В другом воплощении указанный защищенный 4-(бром-{4-[(2-гидрокси-этил)-метил-карбамоил]-фенил}-метилен)-пиперидин защищен группой трет-Boc по положению 1 пиперидина.
Еще одно дополнительное воплощение относится к способу получения N-(2-гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамида, включающий взаимодействие 2-(метиламино)этанола с 4-((1-(трет-бутоксикарбонил)пиперидин-4-илиден)бромметил)бензойной кислотой с образованием трет-бутил-4-((4-(N-(2-гидроксиэтил)-N-метилкарбамоил)фенил)бромметилен)пиперидин-1-карбоксилата; взаимодействие трет-бутил-4-((4-(N-(2-гидроксиэтил)-N-метилкарбамоил)фенил)бромметилен)пиперидин-1-карбоксилата с 8-хинолинбороновой кислотой с образованием трет-бутил-4-((4-(N-(2-гидроксиэтил)-N-метилкарбамоил)фенил)(хинолин-8-ил)метилен)пиперидин-1-карбоксилата; снятие защиты с трет-бутил-4-((4-(N-(2-гидроксиэтил)-N-метилкарбамоил)фенил)(хинолин-8-ил)метилен)пиперидин-1-карбоксилата с образованием N-(2-гидроксиэтил)-N-метил-4-((пиперидин-4-илиден)(хинолин-8-ил)метил)бензамида и взаимодействие N-(2-гидроксиэтил)-N-метил-4-((пиперидин-4-илиден)(хинолин-8-ил)метил)бензамида с тиазол-4-карбальдегидом с образованием N-(2-гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамида.
Другое воплощение относится к трет-бутил-4-((4-(N-(2-гидроксиэтил)-N-метилкарбамоил)фенил)(хинолин-8-ил)метилен)пиперидин-1-карбоксилату.
Еще одно другое воплощение относится к N-(2-гидроксиэтил)-N-метил-4-((пиперидин-4-илиден)(хинолин-8-ил)метил)бензамиду.
В общем, соединение по изобретению может быть получено в соответствии со следующими ниже схемами и общими сведениями, известными специалисту в данной области техники, и/или в соответствии со способами, изложенными в следующих ниже примерах. Растворители, температуры, давления и другие условия реакций могут легко быть выбраны средним специалистом в данной области техники. Исходные материалы имеются в продаже или могут быть легко приготовлены специалистом в данной области техники. При получении соединений могут быть использованы комбинаторные методы, например, в тех случаях, когда промежуточные соединения обладают подходящими для этих методов группами.
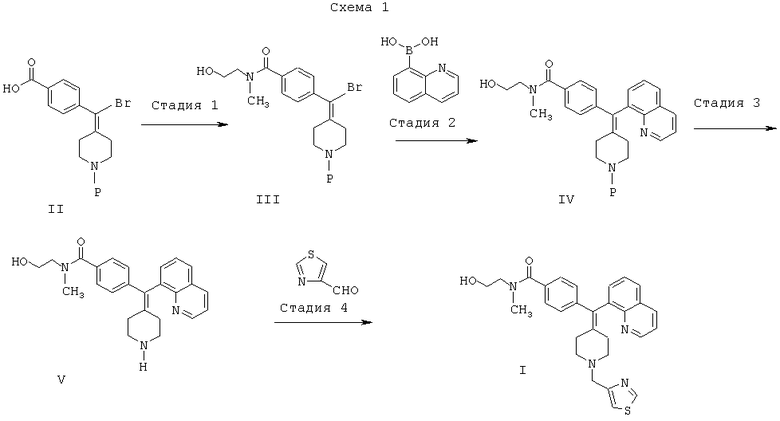
где P представляет собой аминозащитную группу.
Стадия 1
Соединения формулы III могут быть получены путем взаимодействия соединения формулы II, которое может быть приготовлено способом, изложенным в WO 2001/074806 для соединения 5, с 2-(метиламино)этанолом в присутствии катализатора, такого как, например, N-метилморфолин и диметиламинопиридин; растворителя, такого как, например, DMF (диметилформамид) и ацетонитрил; и подходящего связывающего реагента, такого как, например, тетрафторборат O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония, гидрохлорид N-(3-диметиламинопропил)-N'-этилкарбодиимида и карбонилдиимидазол.
Стадия 2
Соединения формулы IV могут быть получены путем сочетания соединения формулы III с 8-хинолнинбороновой кислотой в присутствии катализатора, такого как, например, дигидро-дихлор-бис(ди-трет-бутил-фосфинито-kP)палладат(2-), ацетат палладия (II), PdCl2dppf ([1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий(II)) и (PdCl2(PPh3)2; основания, такого как, например, карбонат калия, карбонат цезия, гидроксид натрия и гидроксид калия; растворителя, такого как, например, изопропиловый спирт и ацетонитрил/вода, при повышенных температурах; и, возможно, с последующей очисткой с помощью Si-Тиола (Si-Thiol), который имеется в продаже от SiliCycle, Inc. Quebec, Canada, в растворителе, таком как, например, тетрагидрофуран. Далее, соединения формулы IV, возможно, могут быть подвергнуты кристаллизации из растворителя.
Стадия 3
Соединения формулы V могут быть получены путем обработки соединений формулы IV кислотой, такой как, например, соляная кислота, в присутствии растворителя, такого как, например, диоксан, дихлорметан, метанол/дихлорметан и эфир/диоксан, возможно с последующей обработкой основанием, таким как, например, метоксид натрия в растворителе, таком как, например, метанол.
Стадия 4
Соединения формулы I могут быть получены путем взаимодействия соединения формулы V с 4-тиазолкарбоксальдегидом в присутствии подходящего борогидридного реагента, такого как, например, триацетоксиборогидрид натрия, в растворителе, таком как, например, дихлорэтан, тетрагидрофуран/метанол и дихлорэтан/метанол.
Более конкретно, соединение по настоящему изобретению и промежуточные соединения, используемые для его получения, могут быть получены синтетическими путями, как проиллюстрировано на следующей ниже схеме 2.
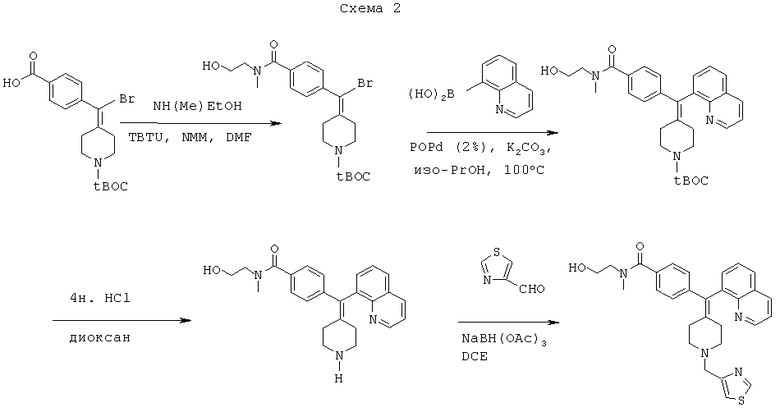
Сокращения:
TBTU - тетрафторборат O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония,
POPd - дигидро-дихлор-бис(ди-трет-бутил-фосфинито-kP)палладат(2-),
NMM - N-метилморфолин,
DCE - дихлорэтан.
Еще более конкретно, соединение по настоящему изобретению и промежуточные соединения, используемые для его получения, могут быть получены синтетическими путями, как проиллюстрировано на следующей ниже схеме 3.
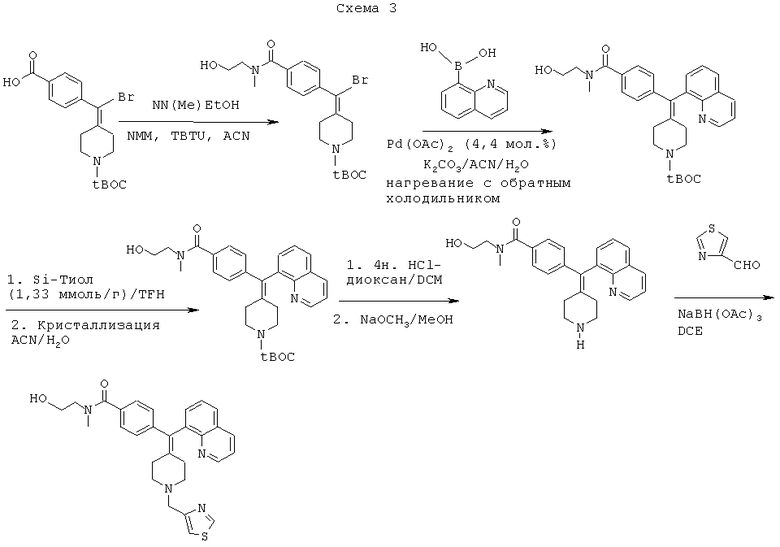
Сокращения:
TBTU - тетрафторборат O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония,
NMM - N-метилморфолин,
ACN - ацетонитрил,
Pd(OAc)2 - ацетат палладия (II),
K2CO3 - карбонат калия,
THF - тетрагидрофуран,
DCM - дихлорметан,
NaOCH3 - метоксид натрия,
MeOH - метанол,
NaBH(OAc)3 - триацетоксиборогидрид натрия,
DCE - дихлорэтан.
БИОЛОГИЧЕСКАЯ ОЦЕНКА И СВОЙСТВА
Было обнаружено, что соединения по изобретению являются активными в отношении δ рецепторов теплокровного животного, например человека. В частности, было установлено, что соединения по изобретению являются эффективными лигандами δ рецепторов. Приведенные ниже анализы in vitro доказывают эти неожиданные действия, особенно активность и эффективность соединений как агонистов, что продемонстрировано в функциональном анализе δ рецепторов человека. Эта особенность может быть связана с активностью in vivo и может не находиться в линейной корреляции с аффинностью связывания. В этих анализах in vitro соединения тестируют на их активность в отношении δ рецепторов и получают IC50 для определения селективной активности конкретного соединения в отношении δ рецепторов. В данном контексте IC50 обычно относится к концентрации соединения, при которой наблюдалось 50%-ное вытеснение стандартного радиоактивного лиганда δ рецептора.
Активности соединения в отношении κ (каппа) и µ рецепторов также измеряют в аналогичном анализе.
Модели in vitro
Культура клеток
Клетки человека 293S, экспрессирующие клонированные κ, δ и µ рецепторы человека и резистентные к неомицину, выращивают в суспензии при 37°C и 5% CO2 во встряхиваемых колбах, содержащих DMEM (модифицированная Дульбекко среда Игла) без кальция, 10% FBS (сыворотка плода коровы), 5% BCS, 0,1% Pluronic F-68 и 600 мкг/мл генетицина.
Получение мембран
Клетки осаждают центрифугированием и ресуспендируют в лизирующем буфере (50 мМ Tris трис(гидроксиметил)аминометан, pH 7,0, 2,5 мМ EDTA (этилендиаминтетрауксусная кислота) с PMSF (фенилметилсульфонилфторид), добавляемым непосредственно перед применением до 0,1 мМ из 0,1 M исходного раствора в этаноле), инкубируют на льду в течение 15 мин, затем гомогенизируют с помощью политрона в течение 30 с. Суспензию центрифугируют при 1000 g (максимум) в течение 10 мин при 4°C. Супернатант оставляют на льду, а осадки ресуспендируют и центрифугируют, как раньше. Супернатанты после обоих центрифугирований объединяют и центрифугируют при 46000 g (максимум) в течение 30 мин. Осадки ресуспендируют в холодном Tris буфере (50 мМ Tris/Cl, pH 7,0) и снова центрифугируют. Конечные осадки ресуспендируют в буфере для мембран (50 мМ Tris, 0,32 M сахарозы, pH 7,0). Аликвоты (1 мл) в полипропиленовых пробирках замораживают в смеси сухого льда с этанолом и хранят при -70°C до применения. Концентрации белка определяют модифицированным анализом Лоури с додецилсульфатом натрия.
Анализы связывания лиганда
Аффинности связывания соединений в отношении κ, δ или µ рецепторов определяют путем измерения их активностей в отношении вытеснения радиолиганда, связывающегося с рецепторами, в мембранах с использованием формата SPA (анализ сцинтилляционной близости). Соединения растворяют в DMSO (диметилсульфоксид), выполняют 3-кратные серийные разведения с использованием DMSO для 11 концентраций и переносят по 2 мкл на лунку в белый 96-луночный планшет для анализа.
Клеточные мембраны с κ, δ или µ рецепторами оттаивают при 37°C, охлаждают на льду, пропускают 3 раза через иглу 25 калибра и затем смешивают с суспензией PVT SPA шариков, покрытых агглютинином ростков пшеницы (PVT-WGA SPA) в буфере для связывания (50 мМ Tris, 3 мМ MgCl2, 1 мг/мл BSA (бычий сывороточный альбумин), pH 7,4, который хранят при 4°C после фильтрования через 0,22 м фильтр). После выдерживания на льду в течение 30 мин 100 мкл смеси мембран и SPA шариков добавляют в каждую лунку 96-луночного планшета, содержащую 2 мкл разведенного соединения.
Радиолигандами для анализа связывания являются 125I Deltorphin II для δ рецептора, [3H]-U69593 для κ рецептора и [125I]-энкефалин для µ рецептора соответственно. Для определения неспецифического связывания применяют налоксон. Реакцию связывания инициируют добавлением радиолигандов (100 мкл/лунка), разведенных в буфере для связывания, в планшет для анализа, содержащий соединения, мембраны и SPA шарики. Конечные концентрации лигандов составляют 40 пМ для 125I Deltorphin II, 0,6 нМ для [3H]-U69593 и 0,1 нМ для [125I]-энкефалина. Планшеты, содержащие смеси для связывания, оставляют при встряхивании и комнатной температуре на период времени от 60 до 120 мин. После вращения на центрифуге при 2000 оборотах в минуту в течение 5 мин с помощью Topcount Reader (Perkin-Elmer Instrument) измеряют радиоактивность в каждой лунке планшетов. Общее (ТВ) и неспецифическое (NS) связывание определяют в отсутствие и в присутствии 10 мкМ налоксона соответственно.
Функциональные анализы
Активность соединений как агонистов измеряют путем определения степеней, до которых соединения стимулируют связывание GTP[γ]35S (гуанозинтрифосфат) с комплексом мембран рецептор-G-белки. Значения EC50 и Emax соединений определяют из анализа кривых концентрация - ответ.
Соединения растворяют в DMSO, выполняют 3-кратные серийные разведения с использованием DMSO для 11 концентраций и переносят по 2 мкл на лунку в белый 96-луночный планшет для анализа.
Клеточные мембраны с κ, δ или µ рецепторами оттаивают при 37°C, охлаждают на льду, пропускают 3 раза через иглу 25 калибра и затем смешивают с суспензией PVT SPA шариков, покрытых агглютинином ростков пшеницы (PVT-WGA SPA) в буфере для GTPγS анализа (50 мМ HEPES (N-2-гидроксиэтил-пиперазин-N-2-этансульфоновая кислота), 150 мМ NaCl, 5 мМ MgCl2, 1 мМ EGTA (этиленгликоль-тетрауксусная кислота), 0,2 мМ DTT (дитиотреитол), 1 мг/мл BSA, pH 7,4). После выдерживания на льду в течение 30 мин, 100 мкл смеси мембран и SPA шариков добавляют в каждую лунку 96-луночного планшета, содержащую 2 мкл разведенного соединения.
GTP[γ]35S разводят буфером для GTPγS анализа до концентрации 0,2 нМ, смешивают с 20 мкМ GDP (гуанозиндифосфат) и добавляют 100 мкл смеси в каждую лунку планшета для анализа, содержащего соединения, мембраны и SPA шарики. После встряхивания при комнатной температуре в течение 45-60 мин планшеты вращают на центрифуге при 2000 оборотах в минуту в течение 5 мин и путем измерения радиоактивности на Topcount Reader (Perkin-Elmer Instrument) определяют активности связывания GTP[γ]35S.
Анализ данных
Специфическое связывание (SB) рассчитывали как TB-NS, a SB в присутствии различных тестируемых соединений выражали как процент от контрольного SB. Значения IC50 и коэффициента Хилла (nн) для лигандов при вытеснении специфично связанного радиолиганда рассчитывают с помощью Excel Fit. Значения К рассчитывали из уравнения Ченга-Прусоффа (Cheng-Prussoff). Среднее±S.E.M (стандартная ошибка среднего).
ФИЗИЧЕСКИЕ СВОЙСТВА И МЕТАБОЛИЗМ И ФАРМАКОКИНЕТИЧЕСКИЕ СВОЙСТВА ЛЕКАРСТВЕННОГО СРЕДСТВА in vitro
На основании испытаний с использованием следующих ниже анализов обнаружено, что соединение по изобретению достигает одного или более желаемых физических свойств, а также метаболических и фармакокинетических свойств лекарственного средства in vitro.
Растворимость
Термодинамическую растворимость соединения(ий) по настоящему изобретению определяли путем перемешивания известного количества соединения при 25°C в течение 24 часов в фосфатном буфере с концентрацией 100 мМ при pH 7,4. Затем отбирали аликвоту насыщенного раствора и измеряли его концентрацию при помощи жидкостной хроматографии/тандемной масс-спектрометрией (ЖХ/МС/МС). Экспериментальные условия и инструментальные параметры ЖХ/МС/МС подробно описаны в разделе, посвященном ЖХ/МС/МС.
LogD
Определение logD было основано на принципе "встряхивание-колба". Соединение(я) по настоящему изобретению суспендировали в октанол-насыщенном буферном растворе и обрабатывали ультразвуком для содействия растворению. Для удаления какого-либо нерастворившегося материала раствор фильтровали. После отбора первоначального образца объем раствора доводят до 10 мл и добавляют известный объем октанола, насыщенного буфером. Двухфазный раствор смешивают и затем разделяют центрифугированием. Затем из нижнего слоя (водного слоя) отбирают второй образец. Оба образца, которые представляли собой растворные концентрации соединения до и после добавления октанола, анализировали при помощи ЖХ/МС/МС. Определенные концентрации использовали для расчета значения logD.
Метаболическая стабильность
Метаболическую стабильность соединения(й) по настоящему изобретению in vitro определяли с использованием микросом печени человека в качестве источника фермента. Соединения (конечная концентрация 1 мкМ) инкубируют с микросомами печени человека и NADPH (никотинамидадениндинуклеотидфосфат). В различные моменты с начала инкубирования отбирают образцы и анализируют их при помощи ЖХ/МС/МС для определения потери исходного соединения. Собственный клиренс (CLint) определяли на основе скорости элиминирования исходного соединения первого порядка.
Анализ ЖХ/МС/МС
Все образцы in vivo подвергали количественному ЖХ/МС/МС анализу с использованием системы Micromass Quattro Ultima MS/MS (Waters, Milford, MA), оснащенной ВЭЖХ системой Shimadzu LC-10 (Shimadzu Scientific Systems, Columbia, MD) и автоматическим пробоотборником CTC-Pal (Leap Technologies, Carrboro, NC). Конкретные ЖХ/МС условия, которые были использованы, суммированы ниже:
hERG АНАЛИЗ
Соединение может быть протестировано на ингибирование K+ канала, кодируемого геном hERG человека (human ether-a-go-go-related gene), с использованием электрофизиологической системы со средней пропускной способностью (medium-throughput) на основе планарной матрицы (lonWorks™ HT). Подробное описание этого анализа, сделанное Bridelan-Taylor et al., было опубликовано в Journal of Pharmacological and Toxicological Methods (54 (2006), pages 189-199), который включен здесь путем ссылки на описание lonWorks™ HT. Результаты этого испытания представлены в таблице ниже.
Метод Геллера-Сейфтера (Geller-Siefter) - тревожная модель
В конфликтном тесте голодных животных тренируют нажимать на рычажный пресс для получения пищи в стандартной оперантной камере при двух условиях. Согласно первому условию, рассматриваемому как неподавляемый компонент, пища доставляется в среднем после 17 нажимов на рычажный пресс (также называется как VR17 график подкрепления). Согласно второму условию, рассматриваемому как подавляемый компонент, обозначаемому мигающими огнями внутри оперантной камеры, пища также доставляется в среднем после 17 нажимов на рычажный пресс, но дополнительно на пол клетки при отдельном VR17 графике подается электрический ток. Ежедневные сеансы состоят из 5 чередующихся презентаций компонента каждого типа: подавляемого (продолжительностью 3 мин) и неподавляемого (продолжительностью 2 мин). Количество нажимов на рычажный пресс, издаваемых при подавляемом компоненте, очевидно низкое по сравнению с неподавляемым компонентом. Седативные агенты, такие как диазепам, увеличивают количество нажимов на рычажный пресс, которые животные сделают при подавляемом компоненте в определенном интервале доз, но не оказывают воздействие на количество нажимов на рычажный пресс, производимых при неподавляемом компоненте. Некоторые соединения по изобретению в этом тесте обладают анксиолитическим профилем.
В следующей ниже таблице представлены некоторые из биологических данных для соединения по изобретению, измеренные с помощью одного или более чем одного анализа, описанного выше.
ПРИМЕРЫ
Далее изобретение будет раскрыто более подробно с помощью следующих ниже примеров, описывающих способы, посредством которых соединения по настоящему изобретению могут быть получены, очищены, проанализированы и подвергнуты биологическому тестированию и которые нельзя толковать, как ограничивающие данное изобретение.
Все значения температуры приведены в градусах Цельсия (°C). Если не оговорено особо, операции проводили при комнатной температуре или температуре окружающей среды (18-25°C).
Если не отмечено особо, коммерческие реагенты, используемые при получении соединения примера и промежуточных соединений, применяли в том виде, в котором они были приобретены, без дополнительной очистки.
Если не отмечено особо, растворители, используемые при получении соединения примера и промежуточных соединений, имели безводные товарные сорта, и их применяли без дополнительной сушки или очистки.
В данном описании изобретения использованы следующие сокращения: водн.: водный; CH2Cl2: дихлорметан, DMF: диметилформамид; EtOAc: этилацетат; ч: час(ы); ВЭЖХ: высокоэффективная жидкостная хроматография; HCl: соляная кислота; изо-PrOH: изопропиловый спирт; K2CO3: карбонат калия; MeOH: метанол; NaHCO3: бикарбонат натрия; Na2SO4: сульфат натрия; NH3: аммиак; POPd: дигидро-дихлор-бис(ди-трет-бутил-фосфинито-kP)палладат (2-); мин: минуты; МС: масс-спектр; ЯМР: ядерный магнитный резонанс и TBTU: тетрафторборат O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония.
Пример 1
N-(2-Гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамид
1А. трет-Бутиловый эфир 4-(бром-{4-[(2-гидрокси-этил)-метил-карбамоил]-фенил}-метилен)-пиперидин-1-карбоновой кислоты.
N-Метилморфолин (6,7 мл, 60,6 ммоль) и трет-бутиловый эфир 4-[бром-(4-карбокси-фенил)-метилен]-пиперидин-1-карбоновой кислоты (полученный, как описано в WO 2001074806 для соединения 5) (20,0 г, 50,5 ммоль) в DMF (240 мл) обрабатывали TBTU (17,8 г, 55,6 ммоль) под азотом. После перемешивания в течение 10 мин добавляли 2-(метиламино)этанол (5,3 мл, 65,7 ммоль) и раствор перемешивали в течение 2 ч. Реакционную смесь разбавляли EtOAc (350 мл), промывали 2%-ной лимонной кислотой, 3%-ным NaHCO3 и рассолом. Водные промывки экстрагировали EtOAc (50 мл). Объединенные органические фазы сушили над Na2SO4, а затем концентрировали в вакууме до получения твердого вещества. После перемешивания в смеси гексанов в течение 5 ч белое твердое вещество собирали фильтрованием и сушили под высоким вакуумом, получая 21,0 г (92%) 1A. 1H ЯМР (500,333 МГц, CDCl3): δ 7.44 (d, J=8.0 Гц, 2H), 7.32 (d, J=8.0 Гц, 2H), 3.91 (br s, 2H), 3.74 (br s, 2H), 3.54 (t, J=5.8 Гц, 3H), 3.34 (t, J=5.7 Гц, 2H), 3.09 (s, 3H), 3.01 (br s, 1H), 2.64 (t, J=5.9 Гц, 2H), 2.23 (t, J=5.8 Гц, 2H), 1.47 (s, 9H). МС ИЭР+ (масс-спектрометрия с ионизацией электрораспылением) 453.1.
1Б. трет-Бутиловый эфир 4-({4-[(2-гидрокси-этил)-метил-карбамоил]-фенил}-хинолин-8-илметилен)-пиперидин-1-карбоновой кислоты.
Соединение 1А (4,0 г, 8,8 ммоль), 8-хинолинбороновую кислоту (3,0 г, 17,6 ммоль), POPd (0,088 г, 0.18 ммоль) и K2CO3 (3,6 г, 26 4 ммоль) в изо-PrOH (90 мл) перемешивали в течение 20 ч под азотом на предварительно нагретой до 100°C масляной бане. Реакционную смесь фильтровали через целит и концентрировали. Полученный материал очищали хроматографией на силикагеле (градиент 2-5% МеОН в CH2Cl2) с получением желтого твердого вещества 1Б (3,27 г, 74%). 1H ЯМР (500,333 МГц, CDCl3): δ 8,91 (dd, J=4.0, 1.6 Гц, 1H), 8.13 (dd, J=8.2, 1.5 Гц, 1H), 7.74 (dt, J=9.5, 3.5 Гц, 1H), 7.50 (d, J=2.5 Гц, 2H), 7.37-7.33 (m, 5H), 3.86 (br s, 2H), 3.68 (br s, 2H), 3.59 (br s, 2H), 3.52-3.43 (m, 3H), 3.34-3.23 (m, 2H), 3.03 (s, 3H), 2.57-2.52 (m, 2H), 2.01 (dd, J=19.3, 7.6 Гц, 2H), 1.44 (s, 9Н). МС ИЭР+ 502,2.
1В. N-(2-Гидрокси-этил)-N-метил-4-(пиперидин-4-илиден-хинолин-8-илметил)-бензамид.
Соединение 1Б (4,7 г, 9,3 ммоль) обрабатывали 4н. HCl в диоксане (30 мл). Через 10 мин смесь декантировали и твердое вещество перемешивали в эфире (40 мл) в течение 2 ч. Затем эфир декантировали и оставшееся желтое твердое вещество сушили под высоким вакуумом с получением 3,7 г 1В (100%). 1H ЯМР (300,132 МГц, DMSO, 90°C): δ 8.98 (s, 1H), 8.47 (d, J=8.1 Гц, 1H), 7.96 (d, J=6.6 Hz, 1H), 7.69-7.57 (m, 3H), 7.38 (d, J=8.0 Гц, 2H), 7.29 (d, J=8.3 Гц, 2H), 3.53 (t, J=5.8 Гц, 2H), 3.36 (t, J=5.7 Гц, 2H), 3.23 (t, J=6.0 Гц, 2H), 3.07 (t, J=6.0 Гц, 2H), 2.92 (s, 3H), 2.63 (t, J=6.0 Гц, 2H), 2.15 (t, J=6.0 Гц, 2H). ВП МС (времяпролетная масс-спектрометрия) ИЭР+ 402,17.
1Г. N-(2-Гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)-пиперидин-4-илиден)метил)бензамид.
Соединение 1В (3,3 г, 8,3 ммоль) и 4-тиазолкарбоксальдегид (1,4 г, 12,4 ммоль) в дихлорэтане (16 мл) перемешивали под азотом в течение 30 мин. Добавляли триацетоксиборогидрид натрия (5,3 г, 24,9 ммоль) и реакционную смесь перемешивали в течение 20 ч. Смесь разбавляли CH2Cl2 (20 мл) и промывали насыщенным водным NaHCO3. Органическую фазу сушили над Na2SO4 и концентрировали. После колоночной хроматографии (120 г силикагеля, элюирование 4% 7н. NH3/MeOH в CH2Cl2) получали 2,01 г 1Г в виде твердого белого вещества (49%). 1H ЯМР (500,333 МГц, CDCl3): δ 8 90 (dd, J=4.1, 1.7 Гц, 1Н), 8.76 (d, J=1.9 Гц, 1Н), 8.11 (dd, J=8.0, 1.5 Гц, 1Н), 7.72 (dd, J=7.3, 2.3 Гц, 1H), 7.51-7.46 (m, 2Н), 7.37-7.33 (m, 3H), 7.31-7.29 (m, 2H), 7.18 (s, 1H), 3.85 (s, br, 2H), 3.76 (s, 2H), 3.67 (br s, 2Н), 3 26 (br s, 1Н), 3.02 (s, 3Н), 2.78-2.71 (m, 1H), 2.67-2.52 (m, 4H), 2.46-2.37 (m, 1H), 2.14-2.04 (m, 2H). ВП МСЭ+ 499,21.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ N-ФЕНИЛПИРРОЛИДИНИЛМЕТИЛПИРРОЛИДИНАМИДЫ И ИХ ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ В КАЧЕСТВЕ МОДУЛЯТОРОВ РЕЦЕПТОРА Н3 ГИСТАМИНА | 2008 |
|
RU2477721C2 |
| ПРОИЗВОДНЫЕ 4-(ФЕНИЛ-ПИПЕРАЗИНИЛ-МЕТИЛ)-БЕНЗАМИДА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2002 |
|
RU2297412C2 |
| ПРОИЗВОДНЫЕ 1-[М-КАРБОКСАМИДО(ГЕТЕРО)АРИЛ-МЕТИЛ]-ГЕТЕРОЦИКЛИЛ-КАРБОКСАМИДА | 2013 |
|
RU2644761C2 |
| ФЕНОКСИЗАМЕЩЕННЫЕ ПИРИМИДИНЫ ДЛЯ ИСПОЛЬЗОВАНИЯ В КАЧЕСТВЕ МОДУЛЯТОРОВ ОПИОИДНЫХ РЕЦЕПТОРОВ | 2010 |
|
RU2554870C2 |
| Замещенные производные N-[2-(4-феноксипиперидин-1-ил)-2-(1,3-тиазол-5-ил)этил]бензамида и N-[2-(4-бензилоксипиперидин-1-ил)-2-(1,3-тиазол-5-ил)этил]бензамида в качестве антагонистов P2X7 рецептора | 2017 |
|
RU2755705C2 |
| ЗАМЕЩЕННЫЕ N-ФЕНИЛБИПИРРОЛИДИНКАРБОКСАМИДЫ И ИХ ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2008 |
|
RU2477719C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ АНТАГОНИСТ Р2Х РЕЦЕПТОРА И ФАКТОР НЕКРОЗА ОПУХОЛИ α | 2004 |
|
RU2350354C2 |
| АМИНОМЕТИЛХИНОЛОНЫ, ПОЛЕЗНЫЕ ПРИ ЛЕЧЕНИИ JNK-ОПОСРЕДОВАННОГО РАССТРОЙСТВА | 2012 |
|
RU2629111C2 |
| НОВЫЕ 4-АМИНО-N-ГИДРОКСИБЕНЗАМИДЫ В КАЧЕСТВЕ ИНГИБИТОРОВ HDAC ДЛЯ ЛЕЧЕНИЯ РАКА | 2012 |
|
RU2591190C2 |
| ИНГИБИТОРЫ КАТЕХОЛ-О-МЕТИЛТРАНСФЕРАЗЫ И ИХ ПРИМЕНЕНИЕ ПРИ ЛЕЧЕНИИ ПСИХОТИЧЕСКИХ РАССТРОЙСТВ | 2011 |
|
RU2586974C2 |
Изобретение относится к N-(2-гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамиду, его фармацевтически приемлемой соли и/или их смеси, а также к его применению в фармацевтической композиции, способе лечения для применения в лечении боли, тревоги, депрессии, тревожной депрессии или болезни Паркинсона. Также изобретение относится к способам получения N-(2-гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамида и его промежуточных соединений. 10 н. и 2 з.п. ф-лы, 1 табл., 1 пр.
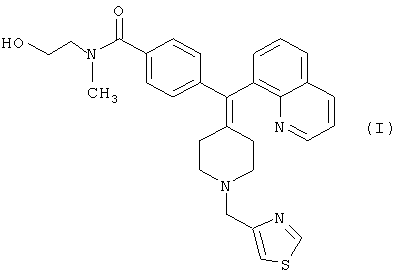
1. N-(2-гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамид, его фармацевтически приемлемая соль или их смесь.
2. Соединение по п.1 для применения в качестве лекарственного средства для лечения боли, тревоги, депрессии, тревожной депрессии или болезни Паркинсона.
3. Применение соединения по п.1 в изготовлении лекарственного средства для лечения боли, тревоги, депрессии, тревожной депрессии или болезни Паркинсона.
4. Фармацевтическая композиция, содержащая терапевтически эффективное количество соединения по п.1 и фармацевтически приемлемый носитель, для применения в лечении боли, тревоги, депрессии, тревожной депрессии или болезни Паркинсона.
5. Способ лечения боли, тревоги, депрессии, тревожной депрессии или болезни Паркинсона у теплокровного животного, включающий стадию введения указанному животному, нуждающемуся в таком лечении, терапевтически эффективного количества соединения по п.1.
6. Способ получения N-(2-гидрокси-этил)-N-метил-4-(пиперидин-4-илиден-хинолин-8-ил-метил)-бензамида, включающий:
взаимодействие защищенного 4-(бром-{4-[(2-гидрокси-этил)-метил-карбамоил]-фенил}-метилен)-пиперидина с 8-хинолинбороновой кислотой с образованием защищенного N-(2-гидрокси-этил)-N-метил-4-(пиперидин-4-илиден-хинолин-8-ил-метил)-бензамида и
снятие защиты с указанного защищенного N-(2-гидрокси-этил)-N-метил-4-(пиперидин-4-илиден-хинолин-8-ил-метил)-бензамида.
7. Способ получения защищенного 4-(бром-{4-[(2-гидрокси-этил)-метил-карбамоил]-фенил}-метилен)-пиперидина, включающий:
взаимодействие 2-(метиламино)этанола с защищенным 4-[бром-(4-карбокси-фенил)-метилен]-пиперидином.
8. Способ получения защищенного N-(2-гидрокси-этил)-N-метил-4-(пиперидин-4-илиден-хинолин-8-ил-метил)-бензамида, включающий:
взаимодействие защищенного 4-(бром-{4-[(2-гидрокси-этил)-метил-карбамоил]-фенил}-метилен)-пиперидина с 8-хинолинбороновой кислотой.
9. Способ по любому из пп.6-8, где указанный защищенный 4-[бром-(4-карбокси-фенил)-метилен]-пиперидин, указанный защищенный 4-(бром-{4-[(2-гидрокси-этил)-метил-карбамоил]-фенил}-метилен)-пиперидин и указанный защищенный N-(2-гидрокси-этил)-N-метил-4-(пиперидин-4-илиден-хинолин-8-ил-метил)-бензамид каждый независимо защищен группой трет-Вос по положению 1 пиперидина.
10. Способ получения N-(2-гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамида, включающий:
взаимодействие 2-(метиламино)этанола с 4-((1-(трет-бутоксикарбонил)пиперидин-4-илиден)бромметил)бензойной кислотой с образованием трет-бутил-4-((4-(N-(2-гидроксиэтил)-N-метилкарбамоил)фенил)бромметилен)пиперидин-1 -карбоксилата;
взаимодействие трет-бутил-4-((4-(N-(2-гидроксиэтил)-N-метилкарбамоил)фенил)бромметилен)пиперидин-1-карбоксилата с 8-хинолинбороновой кислотой с образованием трет-бутил-4-((4-(N-(2-гидроксиэтил)-N-метилкарбамоил)фенил)(хинолин-8-ил)метилен)пиперидин-1-карбоксилата;
снятие защиты с трет-бутил-4-((4-(N-(2-гидроксиэтил)-N-метилкарбамоил)фенил)(хинолин-8-ил)метилен)пиперидин-1-карбоксилата с образованием N-(2-гидроксиэтил)-N-метил-4-((пиперидин-4-илиден)(хинолин-8-ил)метил)бензамида и
взаимодействие N-(2-гидроксиэтил)-N-метил-4-((пиперидин-4-илиден)(хинолин-8-ил)метил)бензамида с тиазол-4-карбальдегидом с образованием N-(2-гидроксиэтил)-N-метил-4-(хинолин-8-ил(1-(тиазол-4-илметил)пиперидин-4-илиден)метил)бензамида.
11. Трет-бутил-4-((4-(N-(2-гидроксиэтил)-N-метилкарбамоил)фенил)-(хинолин-8-ил)метилен)пиперидин-1-карбоксилат.
12. N-(2-гидроксиэтил)-N-метил-4-((пиперидин-4-илиден)(хинолин-8-ил)метил)бензамид.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| YONG-ZHONG WEI et al.,:"N,N-Diethyl-4-(phenylpiperidin-4-ylidenemethyl)benzamide: A Novel, Exceptionally Selective, Potent δ Opioid Receptor Agonist with Oral Bioavailability and Its Analogues", J.Med.Chem., 2000, vol.43, p.3895-3905 | |||
| ПРОИЗВОДНЫЕ ПИПЕРИДИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 1997 |
|
RU2193029C2 |
Авторы
Даты
2012-06-27—Публикация
2007-10-19—Подача