ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Область изобретения
Изобретение относится к группе замещенных N-фенилпирролидинилметилпирролидинамидов. Соединения данного изобретения являются модуляторами рецепторов H3 и, следовательно, пригодны для использования в качестве фармацевтических средств, в особенности для лечения и/или профилактики различных заболеваний, модулируемых рецепторами H3, включая заболевания, связанные с центральной нервной системой. Кроме того, настоящее изобретение также относится к способам получения замещенных N-фенилпирролидинилметилпирролидинамидов и их промежуточных соединений.
Описание уровня техники
Гистамин является распространенной молекулой-мессенджером, высвобождаемой мастоцитами, энтерохромаффин-подобными клетками и нейронами. Физиологическое действие гистамина опосредовано четырьмя фармакологически определяемыми рецепторами (H1, H2, H3 и H4). Все гистаминовые рецепторы имеют семь трансмембранных доменов и относятся к суперсемейству рецепторов, связанных с G-белком (GPCR).
Рецептор Н1 был первым членом семейства гистаминовых рецепторов, которые удалось определить фармакологически, в процессе разработки классических антигистаминов (антагонистов), например дифенгидрамина и фексофенадина. Несмотря на то что антагонизм рецептора Н1 в иммунной системе обычно используется для лечения аллергических реакций, рецептор Н1 также экспрессируется в различных периферических тканях и центральной нервной системе (ЦНС). В головном мозге Н1 участвует в контроле бодрствования, настроения, аппетита и секреции гормонов.
Рецептор Н2 также экспрессируется в ЦНС, где он может модулировать несколько процессов, в том числе когнитивную функцию. Вместе с тем антагонисты рецепторов Н2 в основном разрабатывались для улучшения состояния при язвах желудка за счет ингибирования опосредованной гистаминами секреции желудочной кислоты париетальными гландулоцитами. К классическим Н2 антагонистам относятся циметидин, ранитидин и фамотидин.
Следует также отметить, что функция рецепторов Н4 еще точно не установлена, но она может затрагивать иммунное регулирование и воспалительные процессы.
Рецепторы Н3 также были фармакологически идентифицированы в ЦНС, сердце, легких и желудке. Рецептор Н3 существенно отличается от других гистаминовых рецепторов, демонстрируя низкую гомологию последовательности (Н1: 22%, H2: 21%, H4: 35%). Н3 является пресинаптическим ауторецептором на гистаминовых нейронах в головном мозге, а также пресинаптическим гетерорецептором в не содержащих гистамина нейронах в центральной и периферической нервной системах. Кроме гистамина Н3 также модулирует высвобождение и/или синтез других нейтротрансмиттеров, в том числе ацетилхолина, дофамина, норэпинефрина и серотонина. Особенно важно отметить, что опосредованная Н3 пресинаптическая модуляция высвобождения гистамина обеспечивает активное регулирование рецепторов Н1 и Н2 в головном мозге. Модулируя множество каналов передачи сигналов нейротрансмиттера, Н3 может участвовать в самых различных физиологических процессах. В самом деле, результаты обширных доклинических исследований показывают, что Н3 играет определенную роль в когнитивной функции, цикле сон-бодрствование и энергетическом гомеостазе.
Модуляторы функции Н3 могут использоваться для лечения ожирения и расстройств центральной нервной системы (шизофрении, болезни Альцгеймера, синдрома дефицита внимания с гиперактивностью, болезни Паркинсона, депрессии и эпилепсии), расстройств сна (нарколепсии и бессонницы), сердечно-сосудистых заболеваний (острого инфаркта миокарда), заболеваний органов дыхания (астма), а также желудочно-кишечных расстройств. См., в общем случае, Hancock, Biochem. Pharmacol. 2006 Apr. 14;71(8):1103-13 и Esbenshade et al. Mol Interv. 2006 Apr.; 6(2):77-88, 59.
Недавно было установлено, что соединения, которые в определенной мере структурно связаны с соединениями настоящего изобретения, являются антагонистами рецептора меланинконцентрирующего гормона (МСН), см., в особенности, патент США № 7223788. При этом следует отметить, что не раскрывается информация об активности соединений, представленных в настоящем документе, в отношении сайта рецептора Н3.
Все приведенные здесь источники включаются в настоящий документ полностью путем ссылки на них.
Таким образом, целью настоящего изобретения является предоставить группу замещенных N-фенилпирролидинилметилпирролидинамидов в качестве селективных лигандов рецепторов Н3 для лечения регулируемых рецептором Н3 нарушений ЦНС.
Также целью настоящего изобретения является предоставить способы получения замещенных N-фенилпирролидинилметилпирролидинамидов, как раскрыто в настоящем документе.
Иные цели и другие области применения настоящего изобретения станут очевидны из детального описания, следующего ниже.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Неожиданно был обнаружено, что соединения формулы (I) можно использовать в качестве антагонистов и/или обратных агонистов рецепторов Н3. Также следует отметить, что соединения формулы I не охватываются информацией, представленной в патенте США № 7223788. Более того, неожиданно в настоящее время было установлено, что соединения формулы (I) проявляют селективную активность только в отношении рецепторов Н3 и проявляют низкую активность в отношении сайта рецептора МСН-1, причем этот аспект изобретения становится еще более очевидным из приведенного ниже подробного изложения.
Итак, в соответствии с практикой настоящего изобретения, предлагается соединение формулы (I):
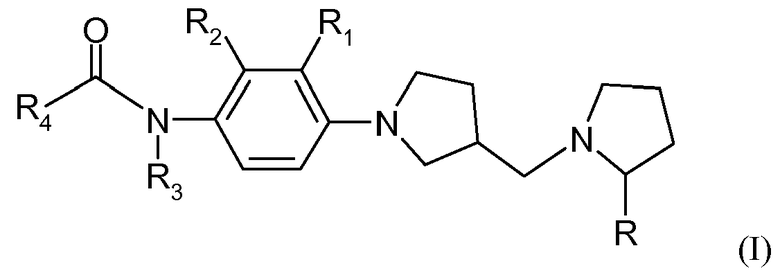
где R, R1, R2 и R3 являются одинаковыми или различными и, независимо друг от друга, выбираются из водорода, (C1-C4)алкила или CF3;
R4 выбирается из группы, включающей фенил, циклогексил, пиридинил, фуранил, изоксазолил, хинолинил, нафтиридинил, индолил, бензоимидазолил, бензофуранил, хроманил, 4-оксо-4H-хроменил, 2,3-дигидробензофуранил, бензо[1,3]диоксолил и 2,5-диоксо-2,3,4,5-тетрагидро-1H-бензо[е]][1,4]диазепинил; где указанный R4 необязательно один или более раз замещен заместителем, выбираемым из группы, включающей галоген, гидрокси, (C1-C4)алкил, (C1-C4)алкокси, CF3, гидроксиметил, 2-гидроксиэтиламино, метоксиэтиламид, бензилоксиметил, пиперидинил, N-ацетилпиперидинил, пирролил, имидазолил и 5-оксо-4,5-дигидропиразолил.
Настоящее изобретение также включает различные соли соединений формулы (I), в том числе различные энантиомеры или диастереомеры соединений формулы (I).
В других аспектах настоящего изобретения также предлагаются различные фармацевтические композиции, содержащие одно или более соединений формулы (I), а также их терапевтическое применение для купирования различных заболеваний, отчасти и/или полностью опосредованных рецепторами H3.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Используемые в настоящем документе термины имеют следующие значения:
Используемое в настоящем документе выражение «(C1-C6)алкил» включает метильную и этильную группы, а также линейные или разветвленные пропильную, бутильную, пентильную и гексильную группы. Конкретными алкильными группами являются метильная, этильная, н-пропильная, изопропильная и трет-бутильная. Производные выражения, такие как «(C1-4)алкокси», «(C1-4)тиоалкил», «(C1-4)алкокси (C1-4)алкил», «гидрокси(C1-4)алкил», «(C1-4)алкилкарбонил», «(C1-4)алкоксикарбонил(C1-4)алкил», «(C1-4)алкоксикарбонил», «амино(C1-4)алкил», «(C1-4)алкиламино», «(C1-4)алкилкарбамоил(C1-6)алкил», «(C1-4)диалкилкарбамоил)(C1-4)алкил», «моно- или ди-(C1-4)алкиламино(C1-4)алкил», «амино(C1-4)алкилкарбонил», «дифенил(C1-4)алкил», «фенил(C1-4)алкил», «фенилкарбоил(C1-4)алкил» и «фенокси(C1-4)алкил», следует толковать соответствующим образом.
Используемое в настоящем документе выражение «циклоалкил» включает все известные циклические радикалы. Характерные примеры «циклоалкила» включают, без ограничения, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил и им подобные. Производные обозначения, такие как «циклоалкокси», «циклоалкилалкил», «циклоалкиларил», «циклоалкилкарбонил», следует толковать соответствующим образом.
Используемое в настоящем документе выражение «(C2-6)алкенил» включает этенильную, а также линейные и разветвленные пропенильную, бутенильную, пентенильную и гексенильную группы. Аналогичным образом, выражение «(C2-6)алкинил» включает этинильную и пропинильную группы, а также линейные и разветвленные бутинильную, пентинильную и гексинильную группы
Используемое в настоящем документе выражение «(C1-4)ацил» имеет такое же значение, что и «(C1-6)алканоил», которое может быть также структурно представлено как «R-CO-», где R - (C1-3)алкил, в соответствии с приведенным в настоящем документе определением. Кроме того, «(C1-5)алкилкарбонил» имеет то же значение, что и (C1-4)ацил. В частности, «(C1-4)ацил» означает формильную, ацетильную или этаноильную, пропаноильную, н-бутаноильную и пр. группы. Производные выражения, такие как «(C1-C4)ацилокси» и «(C1-C4)ацилоксиалкил», следует толковать соответствующим образом.
Используемое здесь выражение «(C1-C6)перфторалкил» означает, что все атомы водорода в указанной алкильной группе замещены атомами фтора. Конкретными примерами являются трифторметильная и пентафторэтильная и линейные или разветвленные гептафторпропильная, нонафторбутильная, ундекафторпентильная и тридекафторгексильная группы. Производное выражение «(C1-C6)перфторалкил» следует толковать соответствующим образом.
Используемое в настоящем документе выражение «(C6-C10)арил» означает замещенный или незамещенный фенил или нафтил. Конкретные примеры замещенного фенила или нафтила включают o-, п-, м-толил, 1,2-, 1,3-, 1,4-ксилил, 1-метилнафтил, 2-метилнафтил и т.д. «Замещенный фенил» или «замещенный нафтил» также включает любые возможные заместители, далее определяемые в настоящем документе или хорошо известные специалистам. Производное выражение «(C6-C10)арилсульфонил» следует толковать соответствующим образом.
Используемое в настоящем документе выражение «(C6-C10)арил(C1-C4)алкил» означает, что (C6-C10)арил, определяемый в настоящем документе, присоединен к (C1-C4)алкилу, в соответствии с приведенным в настоящем документе определением. Характерными примерами являются бензил, фенилэтил, 2-фенилпропил, 1-нафтилметил, 2-нафтилметил и им подобные.
Используемое в настоящем документе выражение «гетероарил» включает все известные ароматические радикалы, содержащие гетероатом. К характерным 5-членным гетероарильным радикалам относятся фуранил, тиенил или тиофенил, пирролил, изопирролил, пиразолил, имидазолил, оксазолил, тиазолил, изотиазолил и им подобные. К характерным 6-членным гетероарильным радикалам относятся пиридинил, пиридазинил, пиримидинил, пиразинил, триазинил и им подобные радикалы. К характерным примерам бициклических гетероарильных радикалов относятся бензофуранил, бензотиофенил, индолил, хинолинил, изохинолинил, циннолил, бензимидазолил, индазолил, пиридофуранил, пиридотиенил и им подобные радикалы.
Используемое в настоящем документе выражение «гетероцикл» включает все известные циклические радикалы, содержащие восстановленный гетероатом. К характерным 5-членным гетероциклическим радикалам относятся тетрагидрофуранил, тетрагидротиофенил, пирролидинил, 2-тиазолинил, тетрагидротиазолил, тетрагидрооксазолил и им подобные радикалы. К показательным 6-членным гетероциклическим радикалам относятся пиперидинил, пиперазинил, морфолинил, тиоморфолинил и им подобные радикалы. Различные другие гетероциклические радикалы включают, без ограничений, азиридинил, азепанил, диазепанил, диазабицикло[2.2.1]гепт-2-ил и триазоканил и им подобные.
«Галоген» или «гало» означает хлор, фтор, бром или иод.
Используемый здесь термин «пациент» означает теплокровных животных, например, крыс, мышей, собак, кошек, морских свинок и приматов, таких как люди.
Используемое в настоящем документе выражение «фармацевтически приемлемый носитель» обозначает нетоксичный растворитель, диспергатор, эксципиент, вспомогательное или другое вещество, которое смешивают с соединением, составляющим предмет настоящего изобретения, чтобы образовать фармацевтическую композицию, то есть дозированную форму, которую можно вводить пациенту. Одним из примеров такого носителя является фармацевтически приемлемое масло, обычно используемое для парентерального введения.
Используемый в настоящем документе термин «фармацевтически приемлемые соли» означает, что соли соединений настоящего изобретения могут использоваться в лекарственных препаратах. Вместе с тем, и другие соли могут быть полезны в получении соединений в соответствии с настоящим изобретением или их фармацевтически приемлемых солей. К подходящим фармацевтически приемлемым солям соединений настоящего изобретения относятся кислотно-аддитивные соли, которые могут образоваться, например, при смешении раствора соединения в соответствии с настоящим изобретением с раствором фармацевтически приемлемой кислоты, например хлористоводородной кислоты, бромистоводородной кислоты, азотной кислоты, сульфаминовой кислоты, серной кислоты, метансульфоновой кислоты, 2-гидроксиэтансульфоновой кислоты, п-толуолсульфоновой кислоты, фумаровой кислоты, малеиновой кислоты, гидроксималеиновой кислоты, яблочной кислоты, аскорбиновой кислоты, янтарной кислоты, глутаровой кислоты, уксусной кислоты, пропионовой кислоты, салициловой кислоты, коричной кислоты, 2-феноксибензойной кислоты, гидроксибензойной кислоты, фенилуксусной кислоты, бензойной кислоты, щавелевой кислоты, лимонной кислоты, винной кислоты, гликолевой кислоты, молочной кислоты, пировиноградной кислоты, малоновой кислоты, угольной кислоты или фосфорной кислоты. Могут также образовываться кислые соли металлов, например моногидроортофосфат натрия и гидросульфат калия. Кроме того, получаемые таким образом соли могут представлять собой моно- или дизамещенные кислые соли и могут быть по существу безводными гидратированными. Более того, если соединения настоящего изобретения несут кислотную функцию, то к подходящим фармацевтически приемлемым их солям могут быть отнесены соли щелочных металлов, например соли натрия или калия, соли щелочноземельных металлов, например соли кальция или магния, и соли, образованные подходящими органическими лигандами, например, четвертичные аммониевые соли.
Используемый в настоящем документе термин «пролекарство» имеет общепринятое значение в данной области. Одно такое определение включает фармакологически неактивное химическое вещество, которое, метаболизируясь или химически преобразуясь под воздействием билогической системы, такой как система млекопитающих, конвертируется в фармакологически активное вещество.
Выражение «стереоизомеры» является общим термином, используемым для всех изомеров индивидуальных молекул, которые отличаются только пространственной ориентацией своих атомов. К ним, как правило, относятся зеркальные изомеры, которые обычно существуют при наличии, по крайней мере, одного центра асимметрии (энантиомеры). Если соединения, составляющие предмет настоящего изобретения, обладают двумя или более центрами асимметрии, они могут также существовать в форме диастереоизомеров, кроме того, некоторые индивидуальные молекулы могут существовать в форме геометрических изомеров (цис/транс). Аналогичным образом, соединения настоящего изобретения могут существовать в смеси двух или более структурно различающихся форм, которые находятся в состоянии быстрого равновесия, общеизвестных как таутомеры. К характерным примерам таутомеров относятся кето-енольные таутомеры, фенол-кето таутомеры, нитрозо-оксимные таутомеры, имино-енаминовые таутомеры и пр. Следует понимать, что все такие изомеры и их смеси в любой пропорции попадают в объем настоящего изобретения.
Используемые в настоящем документе обозначения «R» и «S» применяются как широко употребляемые в органической химии для указания специфической конфигурации хирального центра. Обозначение «R» (rectus, правый) относится к конфигурации хирального центра с расположением старших по рангу групп по часовой стрелке (от группы с наибольшим рангом к группе с другим наименьшим), если смотреть вдоль связи в направлении группы, наименьшей по старшинству. Обозначение «S» (sinister, левый) относится к конфигурации хирального центра с расположением старших по рангу групп против часовой стрелки (от группы с наибольшим рангом к группе с другим наименьшим), если смотреть вдоль связи в направлении группы, наименьшей по старшинству. Старшинство групп определяется правилами последовательности, причем приоритет, в первую очередь, основан на атомном номере (в порядке убывания атомных номеров). Перечень и обсуждение старшинства групп приводится в работе Stereochemistry of Organic Compounds, Ernest L. Eliel, Samuel H. Wilen and Lewis N. Mander, editors, Wiley-Interscience, John Wiley & Sons, Inc., New York, 1994.
Кроме системы (R)-(S), в настоящем документе может также применяться более старая система D-L для обозначения абсолютной конфигурации, особенно в отношении аминокислот. В данной системе формула проекции Фишера ориентируется таким образом, чтобы атом углерода с номером 1 основной цепи находился в верхней части. Префикс «D» используется для описания абсолютной конфигурации изомера, в котором функциональная (определяющая) группа находится справа от углерода хирального центра, а «L» - для изомера, в котором она расположена слева.
Используемый в настоящем документе термин «сольват» означает агрегат, состоящий из иона или молекулы растворенного вещества с одной или несколькими молекулами растворителя. Аналогичным образом, «гидрат» означает агрегат, состоящий из иона или молекулы растворенного вещества с одной или несколькими молекулами воды.
В широком смысле предполагается, что термин «замещенный» включает все допустимые заместители органических соединений. В приведенном в настоящем документе ряде конкретных осуществлений термин «замещенный» означает замещенный одним или несколькими заместителями, которые независимым образом выбираются из группы, включающей (C1-C6)алкил, (C2-C6)алкенил, (C1-C6)перфторалкил, фенил, гидрокси, CO2H, эфир, амид, (C1-C6)алкокси, (C1-C6)тиоалкил, (C1-C6)перфторалкокси, -NH2, Cl, Br, I, F, -NH низший алкил и -N(низший алкил)2. Вместе с тем, в указанных осуществлениях может также использоваться любой другой из подходящих заместителей, известных специалистам в данной области.
«Терапевтически эффективное количество» означает количество соединения, эффективное для лечения названного заболевания, расстройства или состояния.
Термин «лечение» означает:
(i) профилактику заболевания, расстройства или состояния у пациента, который может быть предрасположен к заболеванию, расстройству и/или состоянию, однако, его наличие еще не было диагностировано;
(ii) подавление заболевания, расстройства или состояния, то есть замедление его развития;
(iii) облегчение заболевания, расстройства или состояния, то есть регрессия заболевания, расстройства и/или состояния.
Итак, в соответствии с настоящим изобретением, предлагается соединение формулы I:

где
R, R1, R2 и R3 являются одинаковыми или различными и, независимо друг от друга, выбираются из водорода, (C1-C4)алкила или CF3;
R4 выбирается из группы, включающей фенил, циклогексил, пиридинил, фуранил, изоксазолил, хинолинил, нафтиридинил, индолил, бензоимидазолил, бензофуранил, хроманил, 4-оксо-4H-хроменил, 2,3-дигидробензофуранил, бензо[1,3]диоксолил, 2,5-диоксо-2,3,4,5-тетрагидро-1H-бензо[е]][1,4]диазепинил; где указанный R4 необязательно один или более раз замещен заместителем, выбираемым из группы, включающей галоген, гидрокси, (C1-C4)алкил, (C1-C4)алкокси, CF3, гидроксиметил, 2-гидроксиэтиламино, метоксиэтиламид, бензилоксиметил, пиперидинил, N-ацетилпиперидинил, пирролил, имидазолил и 5-оксо-4,5-дигидропиразолил.
Настоящее изобретение также включает различные соли соединений формулы (I), в том числе различные энантиомеры или диастереомеры соединений формулы (I). Как отмечено выше и в конкретных примерах, приводимых ниже, все соли, которые могут быть образованы, включая фармацевтически приемлемые соли, являются частью настоящего изобретения. Как было отмечено также выше и в продолжение настоящего документа, все возможные энантиомерные и диастереомерные формы соединений формулы (I) являются частью настоящего изобретения.
В одном осуществлении предлагаются соединения формулы (I) настоящего изобретения, где R и R2 представляют собой метил; R1 и R3 представляют собой водород.
Еще в одном осуществлении настоящего изобретения раскрываются соединения формулы (I), где R4 представляет собой фенил, который необязательно замещен одной или несколькими группами, выбираемыми из фтора, метила, гидроксиметила, N-ацетилпиперидинила, имидазолила или 5-оксо-4,5-дигидропиразолила.
Еще в одном осуществлении настоящего изобретения раскрываются соединения формулы (I), где R4 представляет собой пиридинил, который необязательно замещен один или более раз хлором, 2-гидроксиэтиламином, метоксиэтиламидом, бензилоксиметилом или пирролилом.
Еще в одном осуществлении настоящего изобретения также раскрываются соединения формулы (I), где R4 представляет собой хинолинил, нафтиридинил, индолил, бензоимидазолил или бензофуранил, и где R4 необязательно замещен один или более раз хлором, гидрокси, метилом или метокси.
Еще в одном осуществлении настоящего изобретения раскрываются соединения формулы (I), где R4 представляет собой хроманил, 4-оксо-4H-хроменил или 2,3-дигидробензофуранил, где указанный R4 необязательно замещен один или более раз гидрокси или метилом.
Еще в одном осуществлении настоящего изобретения также раскрывается соединение формулы (I), где R4 представляет собой бензо[1,3]диоксолил или 2,5-диоксо-2,3,4,5-тетрагидро-1H-бензо[е]][1,4]диазепинил.
В одном осуществлении настоящего изобретения конкретные соединения формулы (I) выбираются без ограничения из группы, в которую входят следующие соединения:
(2S,3R)-3-фтор-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид;
(2S,3R)-5-фтор-2-метил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид;
4-гидроксиметил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид;
4-имидазол-1-ил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид;
4-(1-ацетилпиперидин-3-ил)-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид;
N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}-4-(3-метил-5-оксо-4,5-дигидропиразол-1-ил)бензамид;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид (2S,3R)-циклогексанкарбоновой кислоты;
5-хлор-6-(2-гидроксиэтиламино)-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}никотинамид;
2-[(2-метоксиэтил)амид] 5-({2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид)пиридин-2,5-дикарбоновой кислоты;
N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}-6-пиррол-1-илникотинамид;
6-бензилоксиметил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}никотинамид;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид (2S,3R)-фуран-3-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид (2S,3R)-3,5-диметилизоксазол-4-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 7-хлор-4-гидроксихинолин-3-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 4-гидрокси-7-метил-[1,8]нафтиридин-3-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 1H-индол-6-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 5-метокси-1H-индол-2-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 2-метил-1H-бензоимидазол-5-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 6-метоксибензофуран-2-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 3,4-дигидрокси-2,2-диметилхроман-6-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 6-метил-4-оксо-4H-хромен-2-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 2,3-дигидробензофуран-5-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид бензо[1,3]диоксол-5-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 2,5-диоксо-2,3,4,5-тетрагидро-1H-бензо[e][1,4]диазепин-8-карбоновой кислоты.
Все вышеперечисленные соединения могут также включать, где это возможно, соответствующие соли, в том числе их фармацевтически приемлемые соли.
В дополнительном аспекте настоящего изобретения можно перечислить следующие соединения, охватываемые, без ограничения, соединением формулы (I) настоящего изобретения:
(2S,3R)-3-фтор-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид
(2S,3R)-5-фтор-2-метил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид;
4-гидроксиметил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид;
4-имидазол-1-ил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид;
4-(1-ацетилпиперидин-3-ил)-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид;
N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}-4-(3-метил-5-оксо-4,5-дигидропиразол-1-ил)бензамид;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид (2S,3R)-циклогексанкарбоновой кислоты;
5-хлор-6-(2-гидроксиэтиламино)-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}никотинамид;
2-[(2-метоксиэтил)амид] 5-({2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид)пиридин-2,5-дикарбоновой кислоты;
N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}-6-пиррол-1-илникотинамид;
6-бензилоксиметил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}никотинамид;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид (2S, 3R)-фуран-3-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид (2S, 3R)-3,5-диметилизоксазол-4-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 7-хлор-4-гидроксихинолин-3-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 4-гидрокси-7-метил-[1,8]нафтиридин-3-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 1H-индол-6-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 5-метокси-1H-индол-2-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 2-метил-1H-бензоимидазол-5-карбоновой кислоты;
Все возможные соли вышеперечисленных соединений, в том числе фармацевтически приемлемые соли, также являются частью настоящего изобретения.
Еще в одном аспекте настоящего изобретения можно перечислить следующие соединения, входящие в объем настоящего изобретения:
(2S,3R)-3-фтор-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид
(2S,3R)-5-фтор-2-метил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид;
4-гидроксиметил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид;
4-имидазол-1-ил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид;
4-(1-ацетилпиперидин-3-ил)-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид;
N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}-4-(3-метил-5-оксо-4,5-дигидропиразол-1-ил)бензамид;
5-хлор-6-(2-гидроксиэтиламино)-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}никотинамид;
2-[(2-метоксиэтил)амид] 5-({2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид)пиридин-2,5-дикарбоновой кислоты;
N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}-6-пиррол-1-илникотинамид; и
6-бензилоксиметил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}никотинамид;
Все возможные соли вышеперечисленных соединений, в том числе фармацевтически приемлемые соли, также являются частью настоящего изобретения.
Еще в одном аспекте настоящего изобретения соединение настоящего изобретения может быть представлено конкретной стереоизомерной формой формулы (II):
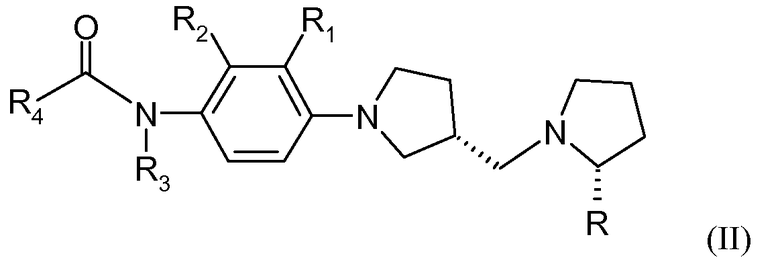
где R, R1, R2 R3 и R4 представлены в соответствии с определениями выше.
Соединения настоящего изобретения могут быть синтезированы любым из известных специалистам способов. В частности, некоторые исходные материалы, используемые при получении соединений настоящего изобретения, являются известными или коммерчески доступными. Соединения настоящего изобретения и некоторые исходные соединения также могут быть получены способами, используемыми для получения аналогичных соединений, как сообщается в литературе, а также как описано далее в настоящем документе. Например, как указано выше, некоторые из соединений с аналогичной структурой раскрыты в патенте США № 7223788. См. также R. C. Larock, “Comprehensive Organic Transformations,” VCH publishers, 1989.
Также хорошо известно, что в различных органических реакциях может возникать необходимость защитить реакционноспособные функциональные группы, например, аминогруппы, чтобы избежать их нежелательного участия в реакциях. Обычные защитные группы могут использоваться в соответствии со стандартными методами, которые известны специалистам в области, например, см. T.W. Greene and P. G. M. Wuts в "Protective Groups in Organic Chemistry" John Wiley and Sons, Inc., 1991. Например, подходящие аминозащитные группы включают, без ограничения, сульфонил (напр., тозил), ацил (напр. бензилоксикарбонил или т-бутоксикарбонил) и арилалкил (напр., бензил), которые могут быть впоследствии удалены гидролизом или гидрированием, в зависимости от случая. Другие подходящие аминозащитные группы включают трифторацетил [-C(=O)CF3], который может быть удален катализируемым основаниями гидролизом, или твердофазная полимерно-связанная бензильная группа, такая как связанная с полимером Меррифилда 2,6-диметоксибензильная группа (линкер Элмана) или 2,6-диметокси-4-[2-(полистирилметокси)этокси]бензил, который может быть удален кислотно-катализируемым гидролизом, например с ТФК.
Более конкретно, описанные в настоящем документе соединения и различные предшественники, использованные для них, могут быть синтезированы при помощи следующих способов, указанных на схемах 1-3, где R, R1, R2, R3 и R4 соответствуют определениям, приведенным для формулы I, если не указано иное.
Например, на схеме 1 приведен пример получения промежуточного соединения (8), которое получают в соответствии с способами, описанными в Bioorg. Med. Chem. 2004, 12 (10), 2603.
Схема 1
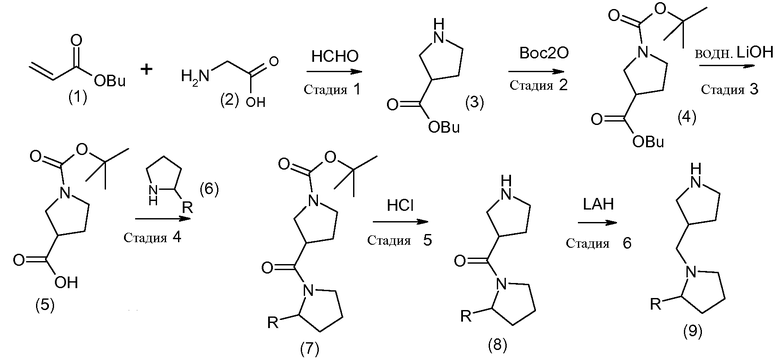
На стадии 1 схемы 1 α-аминоуксусная кислота (2) конденсируется с бутилакрилатом (1) в присутствии формальдегида до образования бутилового эфира пирролидин-3-карбоновой кислоты (3). Данная реакция обычно может быть проведена в подходящем органическом растворителе, таком как толуол, при температурах образования флегмы. Однако также могут применяться различные другие подходящие условия, известные специалистам.
На стадии 2 схемы 1 атом азота промежуточного соединения (3) подходящим образом защищают, например, посредством реакции с ангидридом трет-бутилугольной кислоты для защиты азота трет-бутилоксикарбонильной группой с образованием промежуточного соединения (4). Подобные реакции также могут проводиться с использованием способов, известных специалистам в данной области. Следует понимать, что для достижения тех же результатов могут использоваться любые другие известные защитные группы, позволяющие получать надлежащим образом защищенное промежуточное соединение (4).
На стадии 3 схемы 1 проводится реакция промежуточного соединения (4) с подходящим реагентом, таким как, например, основание, такое как гидроксид лития, в подходящем растворителе, таком как метанол, с образованием промежуточного соединения карбоновой кислоты (5). Такой гидролиз эфира также можно провести в кислотных условиях и/или по существу нейтральных условиях с использованием различных известных кислот и/или кислых веществ, а также силильных соединений, известных специалистам.
На стадии 4 схемы 1 кислотное промежуточное соединение (5) реагирует с замещенным пирролидином формулы (6), где R соответствует определению в данном документе. Подобная реакция сочетания может проводиться в присутствии таких реагентов, как комбинация N-метилморфолина, 1-гидроксибензотриазола и гидрохлорида EDC в присутствии подходящего органического растворителя, такого как дихлорметан. Тем не менее, может использоваться и любой другой способ, позволяющий провести подобное превращение.
На стадии 5 схемы 1 с промежуточного соединения (7) удаляются защитные группы с образованием промежуточного соединения (8), например с помощью хлористоводородной кислоты в присутствии подходящего растворителя, такого как метанол. Опять же, на данной стадии можно использовать любые известные специалистам способы и/или реагенты, которые позволят удалить защитные группы.
Наконец, на стадии 6 схемы 1 промежуточное соединение (8) подвергают восстановительным условиям для получения искомого промежуточного соединения (9). На данной стадии могут применяться различные способы восстановления, позволяющие преобразовать карбонильную группу в метиленовую. Например, промежуточное соединение (8) подвергают восстановительным условиям в присутствии литийалюмогидрида в органическом растворителе, таком как тетрагидрофуран, и получают промежуточное соединение (9).
Аналогично, энантиомерно чистую форму промежуточного соединения (9) можно получить с помощью подходящих исходные веществ в соответствии со способами, показанными на схеме 1. Конкретные примеры энантиомерно обогащенных соединений, составляющих предмет настоящего изобретения, показаны ниже.
На схеме 2 приведен пример получения промежуточного аминофенилпирролидинилметилпирролидина формулы (12), где R, R1 и R2 соответствуют определению в настоящем документе.
Схема 2
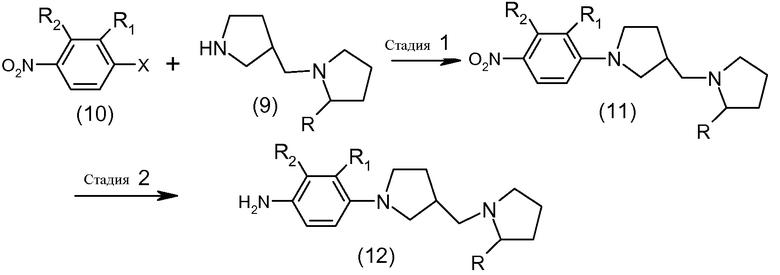
На стадии 1 схемы 2 надлежащим образом замещенный нитробензол формулы (10), где X обозначает приемлемую уходящую группу, например, Cl, F, Br или трифлат (OTf), конденсируется с [1,3']-пирролидинилметилпирролидином формулы (9) для получения промежуточного соединения формулы (11). Такие реакции восстановления также могут проводиться с использованием любого известного в данной области способа. Например, такая реакция замещения может проводиться в полярном растворителе, таком как ДМСО, в присутствии такого основания, как карбонат калия, при комнатной температуре или при температуре, превышающей комнатную.
На стадии 2 схемы 2 промежуточное соединение формулы (11) восстанавливается путем гидрирования или другими известными химичекими способами, например путем использования двухлористого олова в хлористоводородной кислоте, для образования основного промежуточного соединения (12).
Схема 3 содержит пример получения соединений формулы (I) настоящего изобретения с использованием способа А или способа В, в зависимости от доступности необходимой карбоновой кислоты формулы R4-CO2H, либо в форме самой кислоты или ее хлорангидрида, где R, R1, R2 и R4 описаны в настоящем документе, а R3 - атом водорода.
В способе А схемы 3 хлорангидрид формулы (13) может реагировать с промежуточным соединением (12) в любых условиях, известных специалистам в области. Как правило, такие условия предусматривают, среди прочих, реакцию хлорангидрида с промежуточным соединением формулы (12) в подходящем органическом растворителе, например, таком как дихлорметан, в присутствии подходящего основания, например пиридина. Такие реакции обычно проводятся при пониженных температурах, например около 0°C, однако в определенных ситуациях могут также применяться температуры окружающей среды и повышенные температуры, в зависимости от природы хлорангидрида и промежуточного соединения (12).
Схема 3
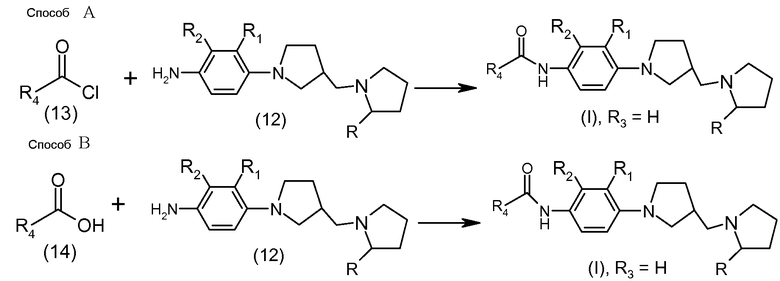
Аналогичным образом, в способе В схемы 3 карбоновая кислота формулы (14) может вступать в реакцию с промежуточным соединением формулы (12) при различных условиях реакции, которые известны специалистам в области. Например, кислота формулы (14) реагирует с промежуточным соединением формулы (12) при пониженной температуре в присутствии подходящих реагентов, например смеси N-метилморфолина, 1-гидроксибензотриазола и EDC.
Как уже отмечалось выше в настоящем документе, соединения настоящего изобретения можно без труда превращать в соли. В частности, соединения настоящего изобретения являются основными, и такие соединения полезны в форме свободного основания или в форме фармацевтически приемлемой кислотно-аддитивной соли такого соединения. Кислотно-аддитивные соли могут явиться более удобной формой при использовании, и на практике использование соли по существу сводится к использованию формы свободного основания. Кислоты, которые могут быть использованы для получения кислотно-аддитивных солей, включают предпочтительно те, которые при реакции со свободным основанием образуют фармацевтически приемлемые соли, то есть соли, анионы которых не токсичны для пациента в фармацевтических дозах солей, так чтобы положительный ингибирующий эффект, присущий свободным основаниям, не разрушался побочными эффектами, приписываемыми анионам. Несмотря на то что фармацевтически приемлемые соли указанного основного соединения являются предпочтительными, все кислотно-аддитивные соли полезны в качестве источников форм свободного основания, даже если конкретная соль как таковая необходима только в качестве промежуточного продукта, как, например, в случае, когда соль образуется только в целях очистки и идентификации или когда она используется в качестве промежуточного соединения в получении фармацевтически приемлемой соли путем ионно-обменных процессов.
В другом аспекте осуществления настоящего изобретения, при помощи соединения настоящего изобретения можно лечить конкретные заболевания, расстройства или состояния, включая, среди прочего, расстройства сна (конкретные примеры включают, среди прочего, нарколепсию, нарушение циркадного ритма сна, обструктивное апноэ во сне, синдром периодических движений конечностей и синдром беспокойных ног, чрезмерную сонливость и дремоту, являющиеся побочным эффектом лекарственного средства, и т.д.), неврологические расстройства (среди конкретных примеров можно назвать, среди прочего, деменцию, болезнь Альцгеймера, рассеянный склероз, эпилепсию и невропатическую боль), невропсихологичские и когнитивные расстройства (конкретные примеры включают, без ограничения, шизофрению, синдром гиперактивности с дефицитом внимания, болезнь Альцгеймера, депрессию, сезонные аффективные расстройства и когнитивные нарушения).
Как показано ниже в конкретных примерах настоящего документа, соединения формулы (I) связываются с рецепторами Н3 и проявляют обратный агонизм по отношению к функциональной активности Н3. Поэтому соединения настоящего изобретения могут применяться для терапии заболеваний или состояний, которые облегчаются лигандами рецептора Н3. Более конкретно, соединения настоящего изобретения являются лигандами рецептора Н3, которые модулируют функцию рецептора Н3, выступая в качестве антагонистов активности рецептора. Кроме того, соединения настоящего изобретения могут выступать в качестве обратных агонистов, которые ингибируют базальную активность рецептора, или же могут выступать антагонистами, которые полностью блокируют действие агонистов, активирующих рецептор. Более того, соединения настоящего изобретения могут также быть частичными агонистами, которые частично блокируют, или частично активируют рецептор Н3, или могут быть агонистами, которые активируют рецептор. Таким образом, соединения настоящего изобретения могут действовать как антагонисты, обратные агонисты и/или частичные агонисты в зависимости от функционального результата, гистаминового тонуса и/или состояния тканей. Соответственно, дифференциальная активность этих соединений может допускать их использование для облегчения множества патологических состояний, которые были конкретно перечислены выше.
Так, одним аспектом настоящего изобретения является способ лечения заболевания у пациента, причем указанное заболевание выбирается из группы, включающей нарушение, связанное с расстройством сна, деменцию, болезнь Альцгеймера, рассеянный склероз, когнитивное расстройство, синдром гиперактивности с дефицитом внимания и депрессию, включающий введение данному пациенту терапевтически эффективного количества соединения формулы (I).
Для специалиста в данной области очевидно, что патологии и патологические состояния, явно указанные в настоящем документе, призваны не ограничивать, но скорее иллюстрировать эффективность соединений, составляющих предмет настоящего изобретения. Так, необходимо понимать, что соединения настоящего изобретения могут быть использованы для облегчения любого заболевания, вызванного эффектами рецепторов H3. Иными словами, как было отмечено выше, соединения настоящего изобретения являются модуляторами рецепторов H3 и могут эффективно вводиться для облегчения болезненного состояния, которое полностью или частично опосредовано рецепторами H3.
Все различные осуществления соединений настоящего изобретения могут быть использованы в способе лечения различных патологических состояний, как описано в настоящем документе. Как сформулировано в настоящем документе, соединения, используемые в способе настоящего изобретения, способны противодействовать эффектам рецептора H3 и, таким образом, смягчать действие и/или состояния, вызванные активностью рецептора H3.
В еще одном осуществлении способа настоящего изобретения соединения настоящего изобретения могут вводиться любыми известными способами. В особенности, соединения настоящего изобретения могут вводиться перорально, внутримышечно, подкожно, ректально, интратрахеально, интраназально, интраперитонально или местно.
В заключение, еще в одном осуществлении настоящего изобретения также предлагается фармацевтическая композиция, содержащая фармацевтически приемлемый носитель и соединение формулы (I), включая энантиомеры, стереоизомеры и таутомеры указанного соединения и его фармацевтически приемлемые соли, сольваты или производные, причем указанное соединение имеет общую структуру, показанную в формуле I, как описано в настоящем документе.
Как описано в настоящем документе, фармацевтические композиции настоящего изобретения отличаются ингибирующим H3 действием и, таким образом, применимы при лечении любого заболевания, состояния или расстройства, вызванного у пациента эффектами H3. Вновь, как описано выше, все предпочтительные осуществления соединений настоящего изобретения, как раскрыто в настоящем документе, могут быть использованы при получении фармацевтических композиций, как описано в настоящем документе.
Предпочтительно, фармацевтические композиции настоящего изобретения представлены в дозированных формах, таких как таблетки, пилюли, капсулы, порошки, гранулы, стерильные парентеральные растворы или суспензии, дозируемые аэрозоли и жидкие распыляемые растворы, капли, ампулы, автоинжекторные устройства или суппозитории, предназначенные для перорального, интраназального, сублингвального или ректального введения или введения посредством ингаляции или инсуффляции. В качестве альтернативы эти композиции могут иметь форму, оптимальную для введения 1 раз в неделю или 1 раз в месяц; например нерастворимая соль активного соединения, такая как соль деканоата, может быть приспособлена для получения депо для внутримышечных инъекций. Возможно использование разрушающегося полимера, содержащего активный ингредиент. Для получения твердых композиций, таких как таблетки, основное действующее вещество смешивают с фармацевтическим носителем, например обычными для таблеток ингредиентами, такими как кукурузный крахмал, лактоза, сахароза, сорбит, тальк, стеариновая кислота, стеарат магния, дикальция фосфат или смолы, а также другими фармацевтическими разбавителями, такими как вода, чтобы образовать твердую предварительную композицию, содержащую гомогенную смесь соединения, составляющего предмет данного изобретения, или его фармацевтически приемлемую соль. Когда такие предварительные композиции называют гомогенными, подразумевается, что активный ингредиент перемешан равномерным образом во всем составе, и композицию можно разделить на обладающие равной эффективностью единичные дозированные формы, например таблетки, пилюли и капсулы. Затем эту твердую предварительную композицию делят на единичные дозированные формы описанного выше типа, содержащие от 0,1 до примерно 500 мг активного ингредиента, составляющего предмет настоящего изобретения. Ароматизированные единичные дозированные формы содержат от 1 до 100 мг, например 1, 2, 5, 10, 25, 50 или 100 мг активного ингредиента. Таблетки и пилюли новой композиции могут быть покрыты оболочкой или сформированы иным образом, чтобы обеспечить дозированную форму пролонгированного действия. Например, таблетка или пилюля может содержать внутренний и внешний дозированные компоненты, когда последний образует оболочку, заключающую в себе первый компонент. Два компонента могут быть разделены энтеральным слоем, который предотвращает разрушение в желудке и позволяет внутреннему компоненту в неразрушенном состоянии попасть в двенадцатиперстную кишку, или чтобы его высвобождение произошло с задержкой. В качестве таких энтеральных слоев или покрытий могут использоваться разнообразные вещества, в том числе ряд полимерных кислот и смесей полимерных кислот с такими веществами, как шеллак, цетиловый спирт и ацетилцеллюлоза.
Жидкие формы, в которых новые соединения, составляющие предмет настоящего изобретения, могут вводиться перорально или при помощи инъекции, включают водные растворы, сиропы с подходящим ароматизатором, водные и масляные суспензии и ароматизированные эмульсии со съедобным маслом, например хлопковым, кунжутным, кокосовым или арахисовым маслом, а также эликсиры и аналогичные фармацевтические носители. К подходящим диспергирующим или суспендирующим веществам для водных суспензий относятся синтетические и натуральные смолы, например трагакант, аравийская камедь, альгинат, декстран, натрий карбоксиметилцеллюлоза, метилцеллюлоза, поливинилпирролидон или желатин.
Фармацевтические композиции настоящего изобретения могут вводиться любыми известными специалистам способами. В целом фармацевтические композиции настоящего изобретения могут вводиться перорально, внутримышечно, подкожно, ректально, интратрахеально, интраназально, интраперитонально или местно. Предпочтительными способами введения фармацевтических композиций настоящего изобретения являются пероральный и интраназальный пути. Любой из известных способов введения лекарственных препаратов пероральным или интраназальным путем может использоваться для введения фармацевтических композиций настоящего изобретения.
При лечении различных патологических состояний, описанных в настоящем документе, подходящие дозы составляют примерно от 0,01 до 250 мг/кг в день, предпочтительно примерно от 0,05 до 100 мг/кг в день, а в особенности примерно от 0,05 до 20 мг/кг в день. Соединения могут вводиться в соответствии со схемой 1-4 раза в день.
Настоящее изобретение далее иллюстрируется следующими примерами, которые приводятся для целей пояснения и никоим образом не ограничивают объем настоящего изобретения.
Примеры (общая часть)
Реакции, как правило, проводят в атмосфере азота. Растворители высушивают над сульфатом магния и выпаривают под вакуумом на роторном испарителе. Анализы ТСХ выполняются на пластинках с силикагелем EM Science 60 F254 с визуализацией УФ излучением. Флэш-хроматография выполняется на колонках Alltech, предварительно заполненных силикагелем. Спектры 1H ЯМР записываются на частоте 300 МГц на спектрометре Gemini 300 или Varian VXR 300 и определяются в дейтерированном растворителе, таком как DMSO-D6 или CDCl3, если не указано иное. Величины химического сдвига указаны в миллионных долях (мд) относительно тетраметилсилана (TMS) в качестве внутреннего стандарта. ЖХ/МС записывается на Micromass Platform LCZ.
Используемые в примерах и последующих препаратах термины имеют следующие указанные значения: «кг» означает килограмм, «г» - грамм, «мг» - миллиграмм, «мкг» - микрограмм, «пг» - пикограмм, «ф» - фунт, «у» - унция, «моль» - моль, «ммоль» - миллимоль, «мкмоль» - микромоль, «нмоль» - наномоль, «л» - литр, «мл» - миллилитр, «мкл» - микролитр, «гал» - галлон, «°С» - градусы Цельсия, «Rf» - коэффициент удерживания, «тп» или «т.п.» - точка плавления, «разл.» - разложение, «тк» или «т.к.» - точка кипения, «мм Hg» - давление в миллиметрах ртутного столба, «см» - сантиметр, «нм» - нанометр, «абс.» - абсолютный, «конц.» - концентрированный, «с» - концентрация в г/мл, «ТГФ» - тетрагидрофуран, «ДМФ» - диметилформамид, «НМП» - 1-метил-2-пирролидинон, «солевой раствор» - насыщенный водный раствор хлорида натрия, «М» - молярность, «мМ» - миллимолярность, «мкМ» - микромолярность, «нМ» - наномолярность, «Н» - нормальность, «ТСХ» - тонкослойная хроматография, «ВЭЖХ» - высокоэффективная жидкостная хроматография, «МСВР» - масс-спектр с высоким разрешением, «П.П.В.» - потери при высушивании, «мкКи» - микрокюри, «в/б» - внутрибрюшинно, «в.в.» - внутривенно, безв. - безводный, вод. - водный, мин. - минута, ч. - час, д. - день, нас. - насыщенный, с - синглет, д - дублет, т - триплет, к - квартет, м - мультиплет, дд - дублет дублетов, ш. - широкий, ЖХ - жидкостный хроматограф, МС - масс-спектрограф, ЭСИ/МС - ионизация электрораспылением/масс-спектрограф, ВУ - время удерживания, М - молекулярный ион.
Промежуточное соединение (i)
Трет-бутиловый эфир (2S,3S)-3-(2-метилпирролидин-1-карбонил)пирролидин-1-карбоновой кислоты
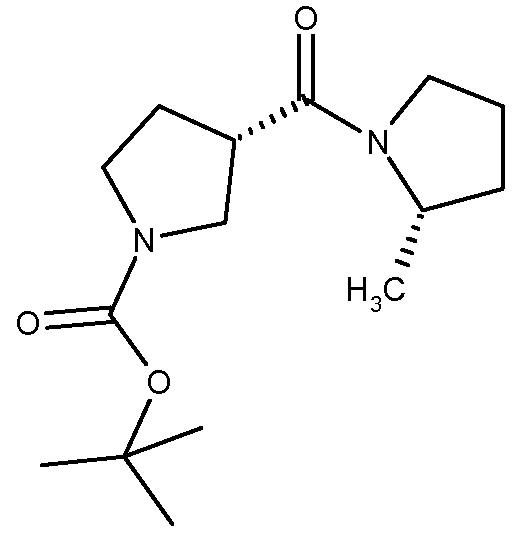
1-трет-бутиловый эфир (3S)-пирролидин-1,3-дикарбоновой кислоты (приобретен в Astatech, Inc, 0,5 г, 2,3 ммоль) растворяли в ДХМ (20 мл) и полученный раствор охлаждали на ледяной бане. К данному раствору добавляли последовательно раствор (S)-2-метилпирролидина (приобретен в Advanced Asymmetric, Inc., 235 мг, 2,76 ммоль, 1,2 эквив.) в 1 мл ДХМ, N-метилморфолин (700 мг, 6,9 ммоль, 3 эквив.), 1-гирдоксилбензотриазол (HOBT) (404 мг, 3 ммоль, 1,3 эквив.) и затем EDC.HCl (576 мг, 3 ммоль, 1,3 эквив.). Полученный прозрачный раствор светло-коричневого цвета перемешивали при комнатной температуре в течение ночи. Анализ ТСХ (10% MeOH в ДХМ) и ЖХ/МС показал пик продукта при времени удерживания 3,238 мин с МС 227 (M-t-Bu). Реакционную смесь гасили насыщенным водным раствором бикарбоната натрия (10 мл) и 10 мл ДХМ. Два слоя разделяли, и водный слой экстрагировали дихлорметаном (15 мл × 2). Объединенные экстракты ДХМ промывали последовательно бикарбонатом натрия (10 мл) и солевым раствором (10 мл), сушили (безводный карбонат калия), фильтровали и концентрировали под вакуумом до получения искомого соединения, 0,65 г (100% выход), в виде густой маслянистой жидкости.
ЖХ/МС: Tr=3,238 мин.; МС: 227 (M-tBu).
1H ЯМР (300 МГц, CDCl3), δ (мд): 4,40 (м, 1H), 3,95-3,20 (м, 6H), 2,65-2,00 (м, 5H), 1,95 (м, 1H), 1,65 (с, 9H), 1,35 (м, 2H).
Промежуточное соединение (ii)
(2S,3S) (2-метилпирролидин-1-ил)пирролидин-3-илметанон
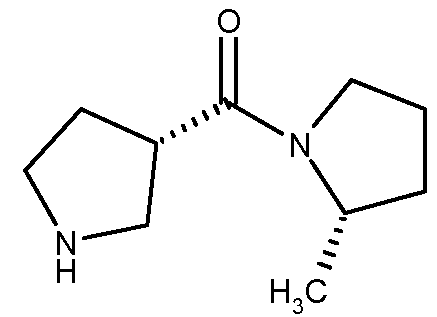
Трет-бутиловый эфир (2S, 3S)-3-(2-метилпирролидин-1-карбонил)пирролидин-1-карбоновой кислоты, полученный в соответствии с описанным выше способом (~ 2,3 ммоль) обрабатывали 3 мл 4M HCl в диоксане при температуре в диапазоне от 0°C до комнатной температуры в течение ночи. Анализ ЖХ/МС показал пик продукта при t=1,219 с МС 183. Пик исходного материала обнаружен не был. Избыток реагента удаляли продувкой реакционной смеси сухим азотом, проходящим через колонку с гидроксидом калия, для поглощения хлористого водорода в течение 1 часа. Растворитель отгоняли выпариванием под высоким вакуумом. Остаток продолжали сушить под высоким вакуумом в течение 2 ч до получения гидрохлоридной соли искомого соединения в виде полутвердого вещества, 0,85 г, с неопределенным числом гидратации. ЖХ/МС: T=1,219 мин, МС: 183 (M+H).
Промежуточное соединение (iii)
(2S,3S)-2-метил-1-пирролидин-3-илметилпирролидин
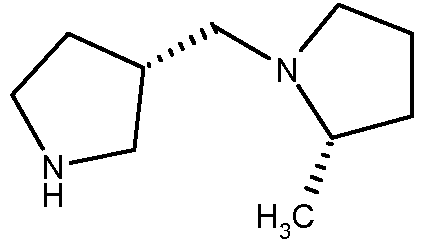
К раствору (2S, 3S)-(2-метилпирролидин-1-ил)пирролидин-3-илметанона (2,3 ммоль, полученного в соответствии с описанным выше способом ) в сухом ТГФ (6 мл) добавляли по каплям раствор 2M BH3SMe2 в ТГФ (2M в ТГФ, 5 мл, 10 ммоль, 4 эквив.). Смесь нагревали при кипении с обратным холодильником в течение 2 часов. После охлаждения раствора до комнатной температуры добавляли 5 мл метанола и перемешивали в течение 2 ч при комнатной температуре. Растворитель выпаривали до сухого состояния для получения искомого продукта в виде полутвердого вещества. Анализ ЖХ/МС показал пик молекулярного иона искомого соединения 169 (M+H) при времени удерживания 1,742 мин.
Промежуточное соединение (iv)
(2S,3R)-2-метил-1-[1-(3-метил-4-нитрофенил)пирролидин-3-илметил]пирролидин
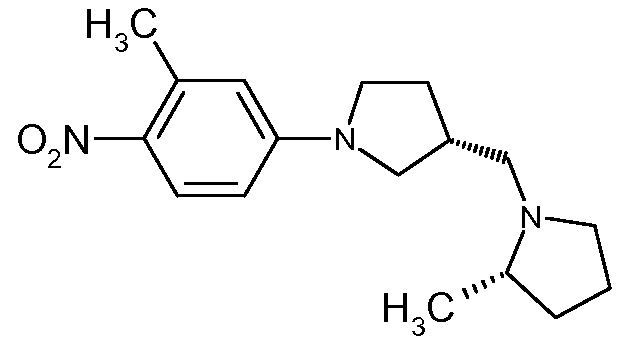
(2S,3S)-2-метил-1-пирролидин-3-илметилпирролидин (2 ммоль) растворяли в безводном ДМСО (10 мл). К данному раствору добавляли 5-фтор-2-нитротолуол (620 мг, 4 ммоль, 2 эквив.), с последующим добавлением порошкообразного карбоната калия (1,1 г, 8 ммоль, 4 эквив.). Суспензию нагревали на масляной бане до 85oC (температура бани) в течение 4 ч, когда исходный материал был израсходован, как показал анализ ЖХ/МС. МС показал 304 (основной пик).
К данной суспензии добавляли 5 мл воды и 10 мл ДХМ. Два слоя разделяли, и водный слой экстрагировали дихлорметаном (10 мл × 2). Объединенные экстракты ДХМ последовательно промывали бикарбонатом натрия (10 мл) и солевым раствором (10 мл × 2), сушили (безводный карбонат калия), фильтровали и концентрировали под вакуумом. Неочищенный продукт очищали на силикагелевой колонке, элюируя 0-2% MeOH в ДХМ, до получения искомого соединения в виде твердого вещества желтого цвета после сушки. МС: 304 (M+1).
1H ЯМР (300 МГц, CDCl3), δ (мд): 8,08 (д, 9,2 Гц, 1H), 6,36 (дд, 9,2, 2,8 Гц, 1H), 6,28 (д, 2,2 Гц, 1H), 3,6 (м, 1H), 3,4 (м, 2H), 3,20 (м, 1H), 3,05 (м, 1H), 2,78 (м, 2H) 2,62 (с, 3H), 2,40-1,60 (м, 8H), 1,45 (м, 1H), 1,08 (д, 6,2 Гц, 3H).
Промежуточное соединение (v)
(2S,3R)-2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламин
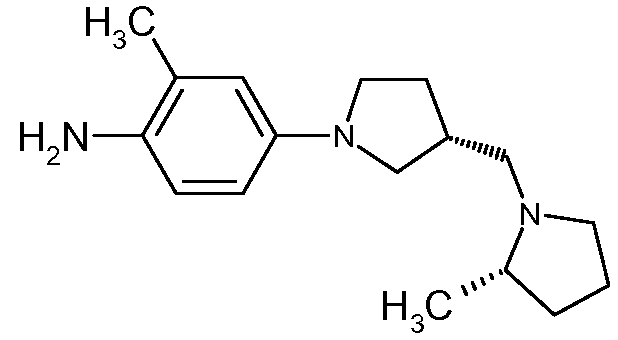
Раствор (2S, 3R)-2-метил-1-[1-(3-метил-4-нитрофенил)пирролидин-3-илметил]пирролидина (0,3 г, 1 ммоль) в MeOH (15 мл) деаэрировали и надували азотом. В данный раствор добавляли Pd-C (10%, 30 мг). Данную смесь перемешивали под давлением H2 при комнатной температуре в течение ночи. Анализ ТСХ (10% MeOH в ДХМ) и ЖХ/МС показал, что реакция завершилась и пик продукта был отмечен при t=1,458 мин, m/z: 274 (M). Смесь пропускали через слой целита и промывали метанолом. Фильтрат концентрировали до сухого состояния с дальнейшей сушкой под высоким вакуумом до получения искомого соединения в виде жидкости красновато-коричневого цвета после сушки под высоким вакуумом.
Пример 1
{2-Метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 2-метил-1H-бензоимидазол-5-карбоновой кислоты
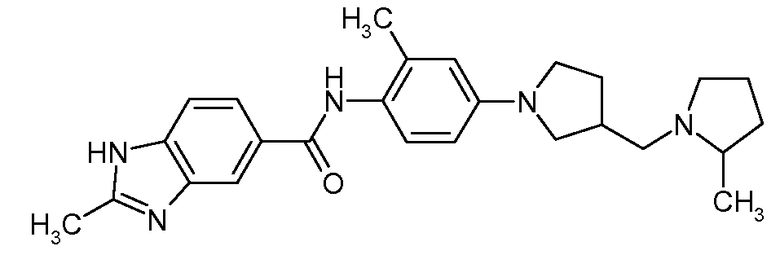
2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламин (27 мг, 0,1 ммоль) и 2-метил-1H-бензоимидазол-5-карбоновую кислоту (17,6 мг, 0,1 ммоль) растворяли в смеси, содержащей 3 мл дихлорметана и 1 мл деметилформамида. К данному раствору затем добавляли N-метилморфолин (33 мкл, 0,3 ммоль), 1-гидроксибензотриазол (17,6 мг, 0,13 ммоль) и 1-(3-диметиламинопропил)-3-этилкарбодиимид (22 мг, 0,123 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 20 ч. В результате выпаривания и ВЭЖХ-ОФ получали 25 мг искомого соединения с трифторуксусной кислотой в виде соли (46%). МС: 432,5 (M+H).
Пример 2
5-Хлор-6-(2-гидроксиэтиламино)-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}никотинамид
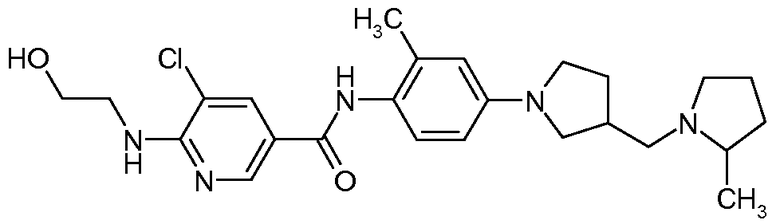
Искомое соединение получали способом, по существу аналогичным примеру 1, путем сочетания 2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 5-хлор-6-(2-гидроксиэтиламино)никотиновой кислотой. МС: 472,3 (M+H).
Пример 3
{2-Метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 7-хлор-4-гидроксихинолин-3-карбоновой кислоты
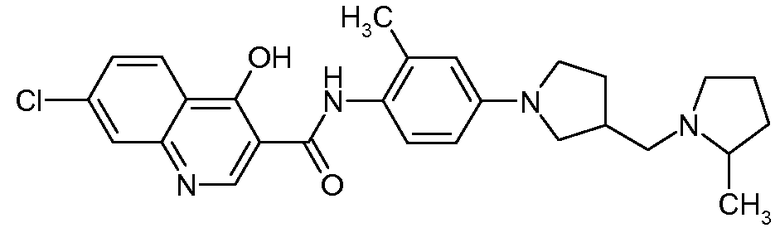
Искомое соединение получали способом, по существу аналогичным примеру 1, путем сочетания 2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 7-хлор-4-гидроксихинолин-3-карбоновой кислотой. МС: 479,2 (M+H).
Пример 4
N-{2-Метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}-6-пиррол-1-илникотинамид
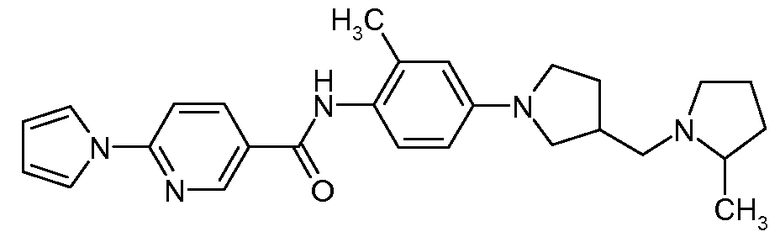
Искомое соединение получали способом, по существу аналогичным примеру 1, путем сочетания 2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 6-пиррол-1-илникотиновой кислотой. МС: 444,5 (M+H).
Пример 5
{2-Метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 2,3-дигидробензофуран-5-карбоновой кислоты
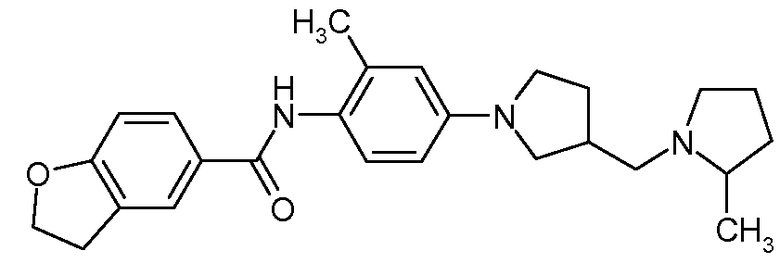
Искомое соединение получали способом, по существу аналогичным примеру 1, путем сочетания 2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 2,3-дигидробензофуран-5-карбоновой кислотой. МС: 420,3 (M+H).
Пример 6
6-Бензилоксиметил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}никотинамид
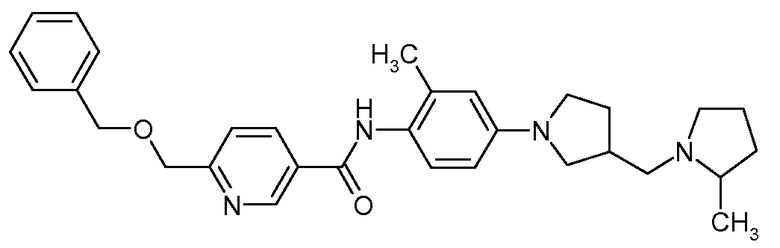
Искомое соединение получали способом, по существу аналогичным примеру 1, путем сочетания 2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 6-бензилоксиметилникотиновой кислотой. МС: 499,3 (M+H).
Пример 7
{2-Метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид бензо[1,3]диоксол-5-карбоновой кислоты
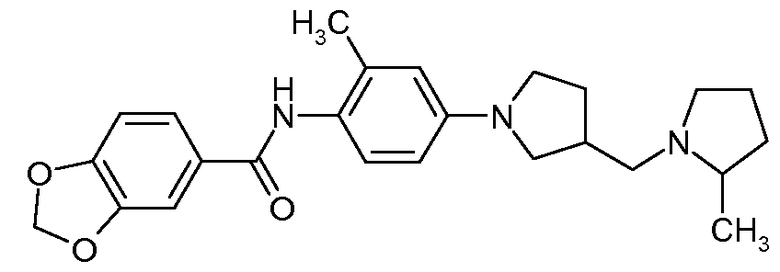
Искомое соединение получали способом, по существу аналогичным примеру 1 путем сочетания 2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с бензо[1,3]диоксол-5-карбоновой кислотой. МС: 422,5 (M+H).
Пример 8
{2-Метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 1H-индол-6-карбоновой кислоты
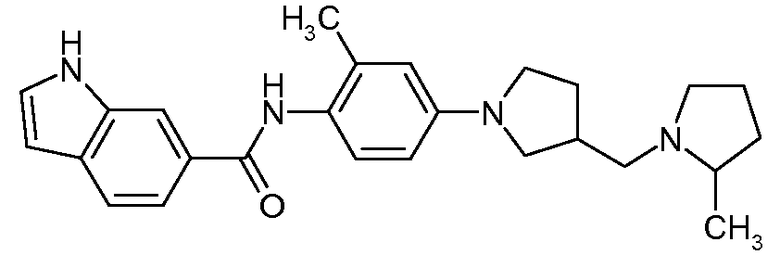
Искомое соединение получали способом, по существу аналогичным примеру 1, путем сочетания 2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 1H-индол-6-карбоновой кислотой. МС: 417,5 (M+H).
Пример 9
4-Имидазол-1-ил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид
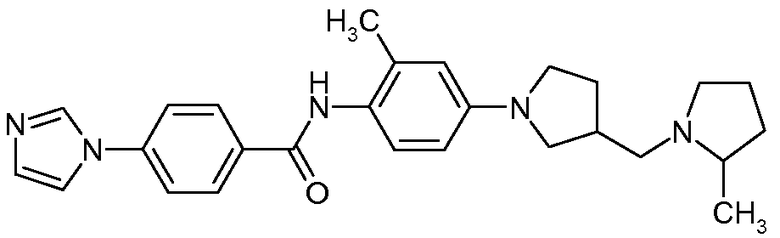
Искомое соединение получали способом, по существу аналогичным примеру 1, путем сочетания 2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 4-имидазол-1-илбензойной кислотой. МС: 444,3 (M+H).
Пример 10
4-(1-Ацетилпиперидин-3-ил)-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид
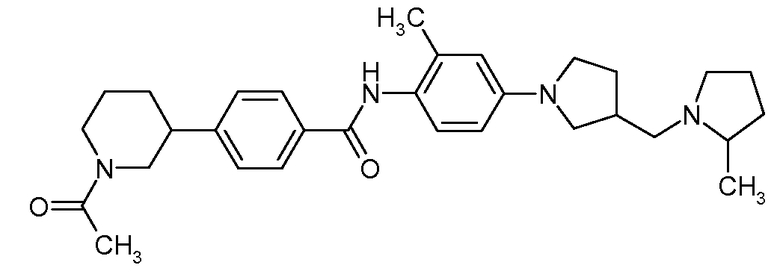
Искомое соединение получали способом, по существу аналогичным примеру 1, путем сочетания 2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 4-(1-ацетилпиперидин-3-ил)бензойной кислотой. МС: 503,3 (M+H).
Пример 11
4-Гидроксиметил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид
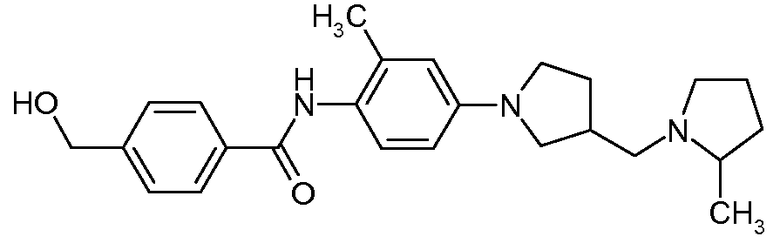
Искомое соединение получали способом, по существу аналогичным примеру 1, путем сочетания 2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 4-гидроксиметилбензойной кислотой. МС: 408,5 (M+H).
Пример 12
{2-Метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 5-метокси-1H-индол-2-карбоновой кислоты
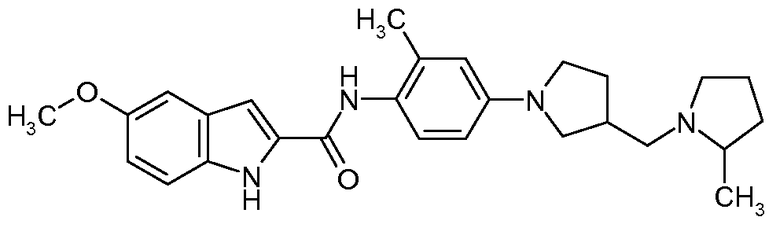
Искомое соединение получали способом, по существу аналогичным примеру 1, путем сочетания 2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 5-метокси-1H-индол-2-карбоновой кислотой. МС: 447,5 (M+H).
Пример 13
{2-Метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 2,5-диоксо-2,3,4,5-тетрагидро-1H-бензо[e][1,4]диазепин-8-карбоновой кислоты
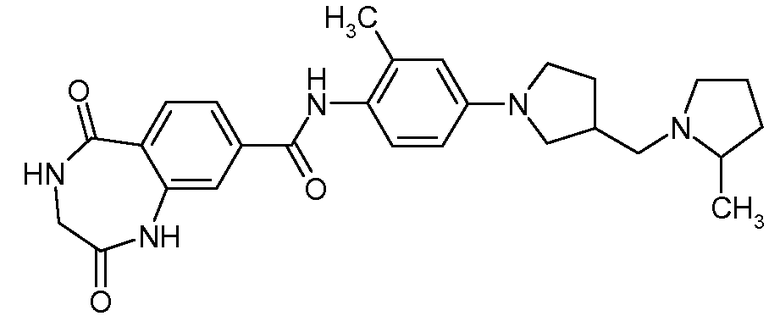
Искомое соединение получали способом, по существу аналогичным примеру 1, путем сочетания 2-метил-4-(3-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 2,5-диоксо-2,3,4,5-тетрагидро-1H-бензо[e][1,4]диазепин-8-карбоновой кислотой. МС: 476,3 (M+H).
Пример 14
2-[(2-Метоксиэтил)амид] 5-({2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид) пиридин-2,5-дикарбоновой кислоты
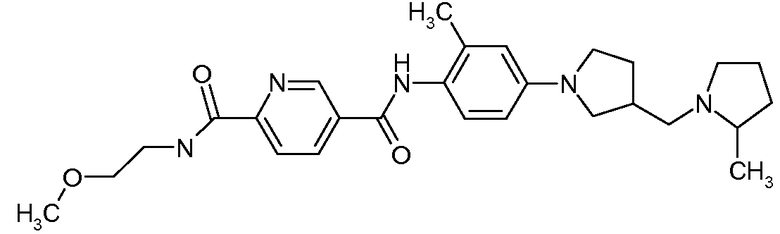
Искомое соединение получали способом, по существу аналогичным примеру 1, путем сочетания 2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 2-[(2-метоксиэтил)амид] пиридин-2,5-дикарбоновой кислоты. МС: 480,3 (M+H).
Пример 15
{2-Метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 6-метоксибензофуран-2-карбоновой кислоты
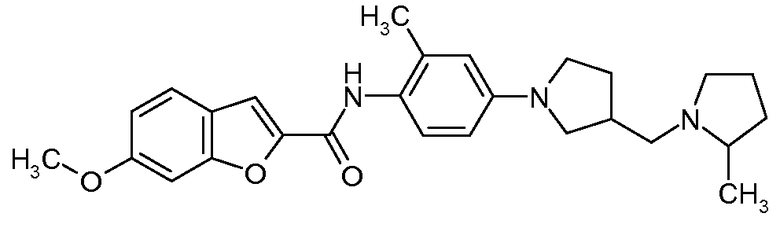
Искомое соединение получали способом, по существу аналогичным примеру 1, путем сочетания 2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 6-метоксибензофуран-2-карбоновой кислотой. МС: 448,5 (M+H).
Пример 16
{2-Метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 3,4-дигидрокси-2,2-диметилхроман-6-карбоновой кислоты
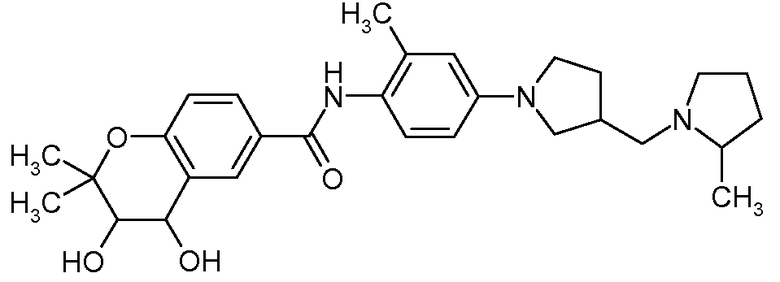
Искомое соединение получали способом, по существу аналогичным примеру 1, путем сочетания 2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 3,4-дигидрокси-2,2-диметилхроман-6-карбоновой кислотой. МС: 494,6 (M+H).
Пример 17
{2-Метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 4-гидрокси-7-метил-[1,8]нафтиридин-3-карбоновой кислоты
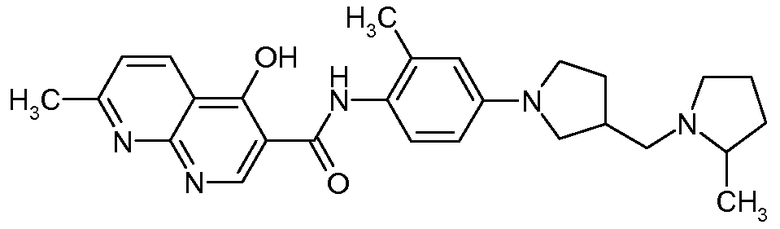
Искомое соединение получали способом, по существу аналогичным примеру 1, путем сочетания 2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 4-гидрокси-7-метил-[1,8]нафтиридин-3-карбоновой кислотой. МС: 460,6 (M+H).
Пример 18
N-{2-Метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}-4-(3-метил-5-оксо-4,5-дигидропиразол-1-ил)бензамид
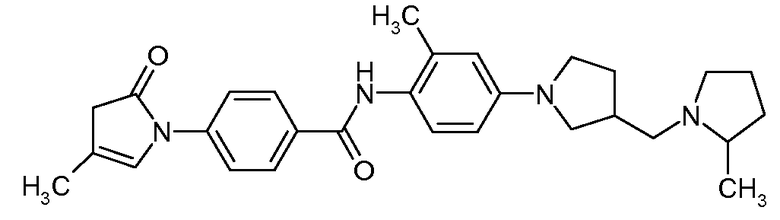
Искомое соединение получали способом, по существу аналогичным примеру 1, путем сочетания 2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 4-(3-метил-5-оксо-4,5-дигидропиразол-1-ил)бензойной кислотой. МС: 474,6 (M+H).
Пример 19
{2-Метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 6-метил-4-оксо-4H-хромен-2-карбоновой кислоты
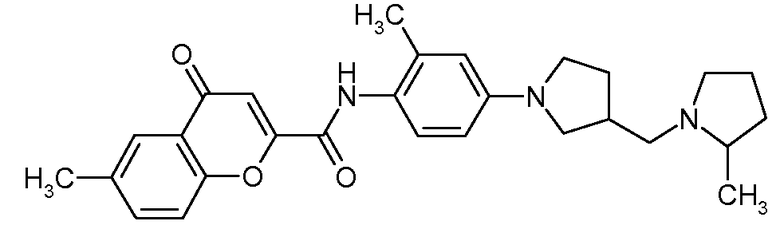
Искомое соединение получали способом, по существу аналогичным примеру 1, путем сочетания 2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 6-метил-4-оксо-4H-хромен-2-карбоновой кислотой. МС: 460,3 (M+H).
Пример 20
(2S,3R)-5-Фтор-2-метил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид
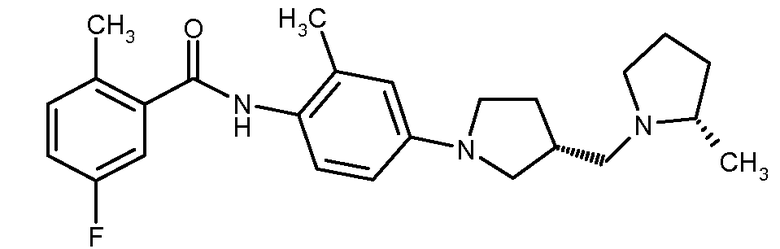
(2S,3R)-2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламин (92 мг, 0,34 ммоль) растворяли в ДХМ (4 мл) и пиридине (1 мл). Раствор охлаждали на ледяной бане. В этот раствор добавляли раствор 5-фтор-2-метилбензоилхлорида (от Alfa Aesar, 0,48 г, 2,77 ммоль, 1,6 эквив.) в ДХМ (2 мл). Раствор перемешивали при комнатной температуре в течение 2 ч. Реакция была признана завершенной, когда анализ ТСХ (10% MeOH в ДХМ) и ЖХ/МС не обнаруживали ИМ при 274, но отмечали только пик продукта при 410,2 и времени удерживания 3,02 мин. К смеси добавляли полимерсвязанный диэтилентриамин (4 ммоль/г, 0,12 г) и перемешивали при комнатной температуре в течение 30 мин, затем фильтровали и промывали ДХМ. Растворитель выпаривали до сухого состояния, повторно растворяли в ДХМ и водном растворе NaHCO3. Два слоя разделяли, и водный слой экстрагировали дихлорметаном (10 мл × 2). Объединенные экстракты ДХМ промывали последовательно бикарбонатом натрия (5 мл) и солевым раствором (5 мл × 2), сушили (безводный карбонат калия), пропускали через слой силикагеля (самоупакованный, ~10 г), промывали ДХМ (без продукта) и затем 10% MeOH в ДХМ (в присутствии продукта). Раствор концентрировали под вакуумом для получения неочищенного продукта, который очищали на силикагелевой колонке, элюируя от 0 до 10% MeOH в ДХМ, до получения 48 мг (34% выход) искомого соединения в виде полутвердого вещества. ЖХ/МС: T=3,020 мин, МС: 410,2.
1H ЯМР (300 МГц, CDCl3), δ (мд): 7,49 (м, 1H), 7,23 (м, 1H), 7,11 (м, 2H), 6,41 (м, 1H), 3,70 (м, 2H), 3,57 (т, 6,2 Гц, 1H), 3,39 (м, 2H), 3,32 (м, 1H), 3,16 (м, 1H), 3,06 (м, 1H), 2,95 (м, 2H), 2,65 (м, 1H), 2,62 (с, 1H), 2,61 (с, 3H), 2,49 (м, 1H), 2,38 (с, 3H), 2,05 (м, 2H), 1,90 (м, 2H), 1,80 (м, 1H), 1,40 (д, 6,5 Гц, 3H).
Пример 21
(2S,3R)-3-фтор-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид

Искомое соединение получали способом, по существу аналогичным примеру 20, путем сочетания (2S, 3R)-2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 3-фторбензоилхлоридом при выходе 39%.
ЖХМС: RT = 2,949 мин, МС: 396,20 (M+H).
1H ЯМР (CDCl3, 300 МГц), δ (мд): 7,87 (д, 7,7 Гц, 1H), 7,62 (м, 2H), 7,45 (м, 2H), 7,20 (м, 1H), 6,39 (м, 1H), 3,73 (м, 1H), 3,57 (т, 6,2 Гц, 1H), 3,59 (м, 1H), 3,40-3,19 (м, 3H), 3,07 (м, 2H), 2,82-2,68 (м, 3H), 2,36 (м, 1H), 2,25 (с, 3H), 2,15 (м, 2H), 2,11-1,80 (м, 3H), 1,43 (д, 6,4 Гц, 3H).
Пример 22
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид (2S,3R)-фуран-3-карбоновой кислоты
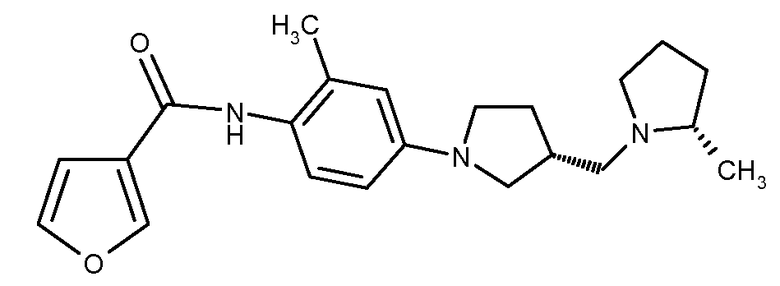
Искомое соединение получали способом, по существу аналогичным примеру 20, путем сочетания (2S, 3R)-2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 3-фуроилхлоридом при выходе 35%.
ЖХМС: RT=2,502 мин, МС: 368,2 (M+H).
1H ЯМР (CD3OD, 300 МГц), δ (мд): 8,16 (шс, 1H), 7,61 (шс, 1H), 7,08 (д, 8,4 Гц, 1H), 6,90 (шс, 1H), 6,49 (м, 2H), 3,58 (м, 2H), 3,55-3,27 (м, 3H), 3,08-2,92 (м, 2H), 2,70 (м, 1H), 2,35 (м, 3H), 2,28 (с, 3H), 2,15 (м, 2H), 2,08 (м, 2H), 1,87 (м, 1H), 1,70 (м, 1H), 1,40 (д, 6,4 Гц, 3H).
Пример 23
{2-метил-4-[3-(2-метилпирролидин-1-ил-метил)пирролидин-1-ил]фенил}амид (2S,3R)-3,5-диметилизоксазол-4-карбоновой кислоты
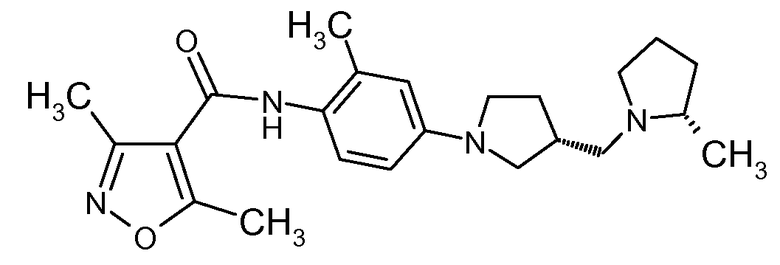
Искомое соединение получали способом, по существу аналогичным примеру 20, путем сочетания (2S, 3R)-2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с 3,5-диметилизоксазол-4-карбонилхлоридом при выходе 50%.
ЖХМС: RT=2,521 мин, МС: 397,3 (M+H).
1H ЯМР (CD3OD, 300 МГц), δ (мд): 7,46 (ш, 1H), 6,92 (ш, 1H), 6,39 (м, 1H), 3,56 (м, 1H), 3,38 (м, 2H), 3,03 (м, 2H), 2,70 (м, 1H), 2,65 (с, 3H), 2,44 (с, 3H), 2,25 (с, 3Н), 2,68 (м, 3H), 2,15 (м, 3H), 2,08 (м, 2H), 1,87 (м, 1H), 1,70 (м, 1H), 1,30 (д, 6,4 Гц, 3H).
Пример 24
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид (2S,3R)-циклогексанкарбоновой кислоты
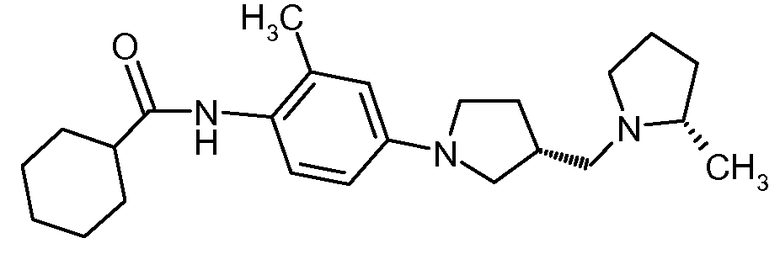
Искомое соединение получали способом, по существу аналогичным примеру 20, путем сочетания (2S, 3R)-2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламина с циклогексанкарбонилхлоридом при выходе 45%.
ЖХМС: RT=2,972 мин, МС: 384,2 (M+H).
Биологические примеры
Пример 25
В настоящем примере продемонстрирована эффективность соединений настоящего изобретения в качестве лигандов рецепторов Н3. Известно, что соединения настоящего изобретения вытесняют радиолиганд [3H]-метилгистамин, который связывается с мембранами клеток млекопитающих, экспрессирующих рецепторы Н3 макак-резусов (Macacca Mulatta). Эти соединения обладают константами аффинности (Ki) к Н3 резусов в интервале от 1 мкМ до <1 нМ. Кроме того, посредством анализа связывания радиолиганда GTPγS было показано, что соединения настоящего изобретения ингибируют конститутивную функциональную активность Н3 резуса в клеточных мембранах. Такое ингибирование связывания радиоактивного лиганда GTPγS, опосредованное базальными Н3 резусов, показывает, что соединения настоящего изобретения могут применяться в качестве обратных агонистов. Эти соединения снижают уровень связывания радиоактивного лиганда GTPHγS рецепторов Н3 резусов на 0-40% ниже базальных уровней.
Мембраны Н3 резусов получали из клеточной линии Flp-In T-REx 293 (Invitrogen), стабильно трансфицированной pcDNA5/FRT/TO (Invitrogen), содержащей рецептор Н3 макаки-резуса (Macacca Mulatta) из 445 аминокислот. (Genbank #AY231164). Стабильно трансфицированные культуры амплифицировали в колбах для культивирования тканей с помощью стандартных методов культивирования тканей и индуцировали для экспрессии Н3 резуса посредством воздействия 500 нг/мл тетрациклина (Cellgro) в течение 24 часов. После индукции клетки отделяли от колб с помощью Cell Stripper (Cellgro). Клетки центрифугировали (1000 × g, 5 мин) и осадок замораживали на бане этанол-сухой лед, с тем чтобы разрушить клеточные мембраны. Замороженный осадок клеток ресуспендировали в 5 мМ HEPES (pH 7,4, Invitrogen) при концентрации собранных клеток 10 мл/1000 см2. Суспензию клеток отсасывали иглой 18 размера (2-3x), а потом иглой 23 размера (2-3x), чтобы в еще большей степени разрушить клеточные мембраны. Суспензию клеток центрифугировали (40 000 × g, 30 мин). Осадок клеточных мембран ресуспендировали в 5 мМ HEPES (pH 7,4, Invitrogen) при конечной концентрации белка 10 мг/мл. Мембраны Н3 резуса хранили под жидким азотом до использования их для анализа связывания [3H]-метилгистамина и радиоактивного лиганда GTPγS.
Анализ связывания радиоактивного лиганда Н3 резуса проводили с использованием мембран рецептора Н3 резуса (полученных как описано выше), [3H]-метилгистамина (Perkin Elmer) и гранул WGA SPA (сцинтилляционный анализ сближения с использованием агглютинина из проростков пшеницы) (Amersham). Анализ проводили в 96-ячеечном планшете Opti-Plates (Packard). В каждой реакции использовали 50 мкл мембран Н3 резуса (20-30 мкг суммарного белка), 50 мкл гранул WGA SPA (0,1 мкг) и 50 мкл 83 Ки/ммоль [3H]-метилгистамина (конечная концентрация 2 нМ) и 50 мкл исследуемого соединения. Соединения настоящего изобретения и/или носитель разбавляли буфером связывания из исходных растворов 10 мМ в DMSO. Планшеты для анализа запечатывали TopSeal (Perkin Elmer) и перемешивали на шейкере (25°C, 1 час). Планшеты для анализа считывали на сцинтилляционном счетчике TopCount (Packard). Анализ результатов проводили посредством трансформации Хилла, и значения Ki определяли по уравнению Ченга-Прусоффа. Наблюдаемые данные по связыванию для нескольких репрезентативных соединений настоящего изобретения приведены в таблице 1.
Пример 26
Данный пример иллюстрирует селективную аффиность соединений настоящего изобретения в отношении рецепторов Н3 и демонстрирует низкую активность в отношении сайта МСН-1 рецептора.
Аффинность Н3 соединений настоящего изобретения измеряли в соответствии с методами, приведенными в примере 25.
Активность соединений настоящего изобретения в сайте рецептора MCH-1, при ее наличии, измеряли в соответствии с методами, описанными ниже.
Испытываемые соединения: Соединения настоящего изобретения хранились в 96-ячеечных планшетах для микротитрования (1 мкл, 10 мМ, 100% DMSO). Каждый из испытываемых образцов разбавляли 249 мкл 100% DMSO (разбавление 1:250). Испытываемые соединения дополнительно разбавляли 1:4 (0,1% DMSO) во время анализа, в результате конечная концентрация испытываемого соединения составляла 10 мкМ.
Отрицательный контроль: 40 мкМ MCH-1 в аналитическом буфере с 0,4% DMSO переносили в планшеты микротитрования для разбавления с целью контроля, что обеспечило конечную концентрацию 10 мкМ.
Холостой контроль: Аналитический буфер, содержащий 0,4% DMSO, переносили в планшеты микротитрования для разбавления, с тем чтобы провести холостой опыт.
Порядок проведения анализа: Фильтровальные планшеты с 250 мл 0,5% раствора PEI в ячейке инкубировали 2 часа при комнатной температуре. PEI удаляли вакуумным фильтрованием перед отбором пипеткой (Univac Polyfiltronic/Whatman). Раствор соединения, приготовленный выше (50 мкл), или MCH-1 (отрицательный контроль) или буфер/DMSO (положительный контроль) добавляли в 96-ячеечный круглодонный планшет для микротитрования. Затем добавляли 50 мкл раствора лиганда с [125J], после чего приливали 100 мкл мембранной суспензии. Ячейки закрывали крышками и инкубировали 60 мин при 25°C. Образцы переносили в фильтровальную планшету GF/B. Реакционную смесь удаляли вакуумным фильтрованием, промывали 4 × 300 мкл промывным буфером, охлажденным до температуры замерзания, и раствор после промывки удаляли вакуумным фильтрованием. Резиноподобный слой на дне планшета затем удаляли, и фильтры осушали в течение ночи при комнатной температуре. Добавляли 25 мкл сцинтилляционной смеси, и планшеты запечатывали, после чего добавляли рамки для планшетов и инкубировали в течение 1 часа при комнатной температуре. Затем измеряли уровень радиоактивности, стандартные параметры для 125J, 30 с на ячейку. На основе этого определяли процент ингибирования связывания лиганда.
Результаты: Как правило, соединения настоящего изобретения демонстрировали значение ki для связывания с рецептором Н3 резуса в интервале от примерно 100 нМ до менее 5 нМ, тогда как процент ингибирования связывания лиганда рецептором MCH-1 был менее 35% при концентрации 10 мкМ. Данный сравнительный пример показывает, что соединения настоящего изобретения могут быть более чем в тысячу раз более селективными на сайте рецептора Н3, чем на сайте рецептора МСН-1.
Пример 27
Настоящий пример иллюстрирует исследование эффективности соединений настоящего изобретения в увеличении бодрствования в моделях животных.
Самцы крыс Спраг-Доули (Charles River, France) весом 250 ± 10 г получали анестезию ZoletilR 50 (60 мг/кг в/б) и фиксировались в стереотаксическом устройстве. Кортикальные электроды (небольшие винтовые электроды из нержавеющей стали диаметром 0,9 мм) ввинчивали в кость над сенсомоторной частью коры головного мозга (1,5 мм латерально по отношению к медиальному шву и 1,5 мм за фронтально-теменным швом), зрительной частью коры (1,5 мм латерально к медиальному шву и 1,5 мм перед затылочно-теменным швом), а также над мозжечком (электрод сравнения). Кортикальные электроды подключали к разъему (Winchester, 7-проводников) и фиксировались зубным цементом к черепу.
Через три недели послеоперационного восстановления животных помещали в плексигласовые цилиндры (60 см диаметром) со свободным доступом к пище и воде. Температуру в помещении поддерживали на постоянном уровне (21 ± 1°C), и освещение поддерживали с 07.00 ч до 19.00 ч. Регистрацию показаний у крыс проводили с 10.00 ч до 16.00 ч в течение трех последовательных дней: контрольный день (D1), день приема лекарства (D2) и день после приема лекарства (D3). Носитель (D1 и D3) или лекарство (D2) вводили за 15 мин до регистрации.
Активность сенсомоторной и зрительной части коры регистрировали посредством сравнения со стандартным электродом, помещенным над корой мозжечка. Выделяли три стадии:
- бодрствование (Б), которое характеризовалось быстрой электрической кортикальной активностью с низким напряжением (ECoG);
- сон НБДГ (небыстрое движение глаз или медленноволновой сон: МВС), который характеризовался ростом электрической кортикальной активности; формирование медленных волн высокой амплитуды со всплесками сонного веретена;
- сон БДГ (быстрое движение глаз или парадоксальный сон: ПС), который характеризовался гиперсинхронизацией тета-ритма в зрительной области.
Анализ сигнала ECoG проводили автоматически посредством компьютерной системы, распознающей различные фазы сна с помощью последовательного спектрального анализа десятисекундных периодов (программное обеспечение Deltamed “Coherence”).
Соединения настоящего изобретения растворяли в 0,6% MTC твина и вводили перорально (п/о). Объем инъекции составлял 0,5 мл/100 г веса тела.
Два вида анализа использовали для количественного определения эффектов воздействия соединений настоящего изобретения на переменные сна-бодрствования: анализ одночасового периода и анализ шестичасового периода.
Результаты выражены в минутах (часовой период анализа) или в процентах от контрольных значений (100%). Статистический анализ данных проводили с использованием t-критерия Стьюдента для парных значений, с тем чтобы определить значимые отклонения от контрольных значений.
Пример 28
Тест стресс-индуцированных ультразвуковых вокализаций у взрослых крыс
Настоящий пример иллюстрирует исследование эффективности соединений настоящего изобретения в качестве антидепрессантов в моделях животных.
Использованная процедура была адаптирована на основе методики, описанной в работе Van Der Poel A.M, Noach E.J.K, Miczek K.A (1989) Temporal patterning of ultrasonic distress calls in the adult rat: effects of morphine and benzodiazepines. Psychopharmacology 97:147-8. Крыс во время сеанса обучения помещали в клетку с решетчатым полом из нержавеющей стали (MED Associates, Inc., St. Albans, VT). Четыре удара электрическим током (0,8 мА, 3 с) производили каждые 7 с, а затем регистрировали ультразвуковые сигналы (UV, 22 кГц) с помощью системы Ultravox (Noldus, Wageningen, The Netherlands) в течение 2 мин. Модифицированный ультразвуковой детектор (модель Mini-3 bat), связанный с микрофоном, использовали для преобразования ультразвукового сигнала в слышимый звук. Затем сигнал фильтровали и передавали на компьютер, где программное обеспечение Ultravox регистрировало каждый всплеск UV, который продолжался более 10 мс. Крыс отбирали по продолжительности их UV (> 40 с), и проводили тест, в течение 4 ч после обучения. Для проведения теста крыс помещали в ту же клетку, где проводили обучение. Производили один удар электрическим током (0,8 мА, 3 с), после чего регистрировали UV (продолжительность и частоту) в течение 2 мин с использованием системы Ultravox. Соединения настоящего изобретения вводили п/о за 60 мин до тестирования.
Пример 29
Тест принудительного плавания у крыс
Настоящий пример дополнительно иллюстрирует исследование эффективности соединений настоящего изобретения в качестве антидепрессантов в моделях животных.
Процедура представляет собой модификацию подхода, описанного в работе Porsolt et al. (1977) Depression: a new animal model sensitive to antidepressant treatments. Nature 266:730-2. Крыс помещали в отдельный стеклянный цилиндр (40 см высотой, 17 см в диаметре), содержащий воду (21°C), налитую до высоты 30 см. Проводили два сеанса плавания (15-минутный сеанс обучения с последующим через 24 часа 6-минутным тестом). После каждого сеанса плавания крыс помещали под нагревательную лампу во избежание гипотермии. Продолжительность состояния неподвижности измеряли в ходе 6-минутного теста. Соединения настоящего изобретения вводили п/о дважды (через 15 мин после сеанса обучения и за 60 мин до теста).
Несмотря на то, что настоящее изобретение проиллюстрировано некоторыми из приведенных выше примеров, их не следует толковать как ограничивающие его объем, а напротив, как отмечалось выше в настоящем документе, данное изобретение распространяется и на родственные области. Возможны различные модификации и осуществления, не отклоняющиеся от основной идеи и объема настоящего изобретения.
Изобретение относится к замещенным N-фенил-пирролидинилметилпирролидинамидам формулы (I):
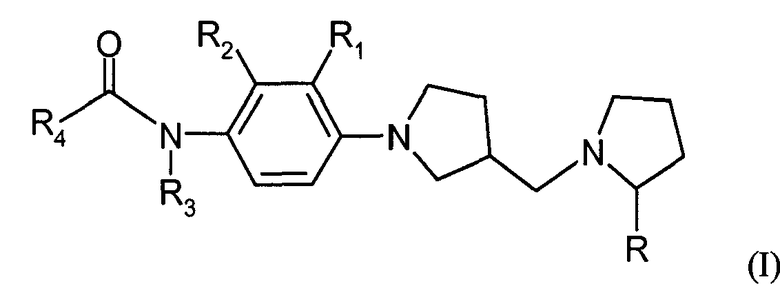
где R, R1, R2 и R3 являются одинаковыми или различными и, независимо друг от друга, означают Н, (С1-С4)алкил, CF3; R4 означает фенил, циклогексил, пиридинил, фуранил, изоксазолил, хинолинил, нафтиридинил, индолил, бензоимидазолил, бензофуранил, хроманил, 4-оксо-4Н-хроменил, 2,3-дигидробензофуранил, бензо[1,3]диоксолил и 2,5-диоксо-2,3,4,5-тетрагидро-1Н-бензо[е]][1,4]диазепинил; где указанный R4 необязательно один или более раз замещен заместителем, выбираемым из галогена, гидрокси, (C1-C4)алкила, (C1-C4)алкокси, CF3, гидроксиметила, 2-гидроксиэтиламино, метоксиэтиламида, бензилоксиметила, пиперидинила, N-ацетилпиперидинила, пирролила, имидазолила, 5-оксо-4,5-дигидропиразолила или его фармацевтически приемлемой соли, энантиомеру, диастереомеру. Соединения обладают моделирующей активностью в отношении рецептора Н3 гистамина, что позволяет использовать их для получения фармацевтической композиции. 3 н. и 7 з.п. ф-лы, 1 табл., 3 сх., 29 пр.
1. Соединение формулы (I)
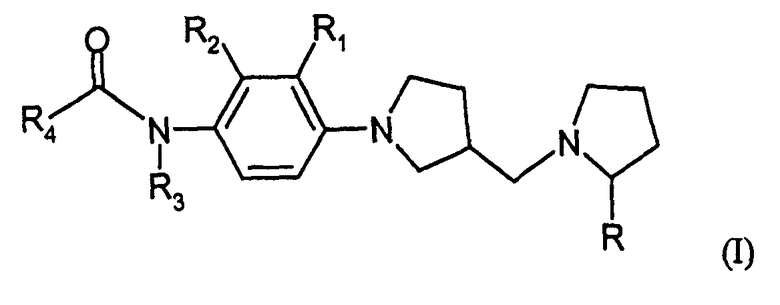
где R, R1, R2 и R3 являются одинаковыми или различными и независимо друг от друга выбираются из водорода, (С1-С4)алкила или CF3;
R4 выбирается из группы, включающей фенил, циклогексил, пиридинид, фуранил, изоксазолил, хинолинил, нафтиридинил, индолил, бензоимидазолил, бензофуранил, хроманил, 4-оксо-4Н-хроменил, 2,3-дигидробензофуранил, бензо[1,3]диоксолил и 2,5-диоксо-2,3,4,5-тетрагидро-1Н-бензо[е]][1,4]диазепинил; где указанный R4 необязательно один или более раз замещен заместителем, выбираемым из группы, включающей галоген, гидрокси, (C1-C4)алкил, (C1-C4)алкокси, CF3, гидроксиметил, 2-гидроксиэтиламино, метоксиэтиламид, бензилоксиметил, пиперидинил, N-ацетилпиперидинил, пирролил, имидазолил и 5-оксо-4,5-дигидропиразолил; или его фармацевтически приемлемая соль или энантиомер или диастереомер.
2. Соединение по п.1, где
R и R2 представляют собой метил;
R1 и R3 представляют собой водород; и
R4 представляет собой фенил, который необязательно замещен одной или несколькими группами, выбираемыми из фтора, метила, гидроксиметила, N-ацетилпиперидинила, имидазолила или 5-оксо-4,5-дигидропиразолила;
или
R4 представляет собой пиридинил, который необязательно замещен один или более раз хлором, 2-гидроксиэтиламино, метоксиэтиламидом, бензилоксиметилом или пирролилом; или
R4 представляет собой хинолинил, нафтиридинил, индолил, бензоимидазолил или бензофуранил, и где R4 необязательно замещен один или более раз хлором, гидрокси, метилом или метокси; или
R4 представляет собой хроманил, 4-оксо-4Н-хроменил или 2,3-дигидробензофуранил, где указанный R4 необязательно замещен один или более раз гидрокси или метилом; или
R4 представляет собой бензо[1,3]диоксолил или 2,5-диоксо-2,3,4,5-тетрагидро-1Н-бензо[е]][1,4]диазепинил.
3. Соединение по п.1, выбираемое из группы, в которую входят:
(2S,3R)-3-фтор-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид;
(2S,3R)-5-фтор-2-метил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид;
4-гидроксиметил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид;
4-имидазол-1-ил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид;
4-(1-ацетилпиперидин-3-ил)-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}бензамид;
N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]-фенил}-4-(3-метил-5-оксо-4,5-дигидропиразол-1-ил)бензамид;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид (23,3R)-циклогексанкарбоновой кислоты;
5-хлор-6-(2-гидроксиэтиламино)-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1- ил]фенил}никотинамид;
2-[(2-метоксиэтил)амид] 5-({2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид)пиридин-2,5-дикарбоновой кислоты;
N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}-6-пиррол-1-илникотинамид;
6-бензилоксиметил-N-{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}никотинамид;
{2-метил-4-[3-(2-метил-пирролидин-1-илметил)пирролидин-1-ил]фенил}амид (2S,3R)-фуран-3-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид (23,3R)-3,5-диметилизоксазол-4-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 7-хлор-4-гидроксихинолин-3-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 4-гидрокси-7-метил-[1,8]нафтиридин-3-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фениламид 1H-индол-6-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 5-метокси-1Н-индол-2-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 2-метил-1Н-бензоимидазол-5-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 6-метоксибензофуран-2-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 3,4-дигидрокси-2,2-диметилхроман-6-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 6-метил-4-оксо-4Н-хромен-2-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 2,3-дигидробензофуран-5-карбоновой кислоты;
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]-фенил}амид бензо[1,3]диоксол-5-карбоновой кислоты; и
{2-метил-4-[3-(2-метилпирролидин-1-илметил)пирролидин-1-ил]фенил}амид 2,5-диоксо-2,3,4,5-тетрагидро-1Н-бензо[е][1,4]диазепин-8-карбоновой кислоты
или их фармацевтически приемлемая соль.
4. Фармацевтическая композиция, обладающая модулирующей активностью в отношении рецептора Н3 гистамина, содержащая соединение формулы (I) по любому из пп.1-3 или его фармацевтически приемлемую соль или его энантиомер или стереоизомер, в комбинации по меньшей мере с одним фармацевтически приемлемым эксципиентом, разбавителем или носителем.
5. Применение соединения формулы (I) по любому из пп.1-3 необязательно в комбинации с фармацевтически приемлемым носителем для получения фармацевтической композиции для лечения заболевания, выбираемого из группы, включающей нарушение, связанное с расстройством сна, деменцию, болезнь Альцгеймера, рассеянный склероз, когнитивное расстройство, синдром гиперактивности с дефицитом внимания и депрессию.
6. Применение по п.5, где расстройство сна выбирается из группы, включающей нарколепсию, нарушение циркадного ритма сна, обструктивное апноэ во сне, синдром периодических движений конечностей и синдром беспокойных ног, чрезмерную сонливость и дремоту, вызванные побочным эффектом лекарственного средства.
7. Применение по п.5, где заболеванием является когнитивное расстройство.
8. Применение по п.5, где заболеванием является болезнь Альцгеймера.
9. Применение по п.5, где заболеванием является депрессия.
10. Применение по п.5, где заболеванием является деменция.
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| ПОЛИЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ СВОЙСТВАМИ АНТАГОНИСТА РЕЦЕПТОРА H, И СПОСОБ ЛЕЧЕНИЯ С ЕГО ПРИМЕНЕНИЕМ | 2001 |
|
RU2301231C2 |
Авторы
Даты
2013-03-20—Публикация
2008-10-14—Подача