Изобретение относится к области медицинской техники, а именно к ортопедической стоматологии, и может быть использовано при изготовлении внутрикостных имплантатов путем нанесения на их металлическую основу многослойных плазменных покрытий с последующей ионно-лучевой модификацией.
Известен способ изготовления внутрикостных стоматологических имплантатов с биоактивным покрытием [патент РФ №2074674, МПК: A61F 2/28], включающий изготовление из металла или сплава универсальным способом (токарная, фрезерная и др. методы обработки или с помощью специальных электрофизических методов) основы имплантата цилиндрической, пластинчатой или трубчатой формы, нанесение на основу имплантата методом плазменного напыления системы покрытий из четырех слоев - двух слоев титана или гидрида титана различной дисперсности и толщины, третьего слоя из механической смеси титана или гидрида титана, или гидроксиапатита с соотношением соответственно 60-80 мас.% и 20-40 мас.% и наружного слоя - гидроксиапатита.
Недостатком данного изобретения является невысокая биосовместимость и хрупкость покрытия.
Известен способ изготовления имплантата для замены костной ткани [патент РФ №2025132, МПК A61F 2/28], согласно которому на имплантат, выполненный из металлического или металл-керамического сплава в виде штифта, наносят трехслойное покрытие, при этом первый слой содержит биостекло на основе фосфата кальция с добавлением оксидов металлов, второй слой - смесь фосфата кальция и гидроксиапатита, а промежуточный слой содержит фосфат кальция.
Однако многокомпонентная система покрытий (СаР-стекло, гидроксиапатит кальция, трикальцийфосфат и добавки оксидов металлов) с различными коэффициентами термического расширения не способствует прочному закреплению слоев покрытия (особенно первого слоя) с металлической основной имплантата, покрытие также не обладает высокой биоактивностью.
Наиболее близким к предлагаемому изобретению является способ изготовления внутрикостного стоматологического имплантата с плазмонапыленным многослойным биоактивным покрытием [патент РФ №2146535, МПК A61L 27/00, А61С 8/00], состоящий в напылении плазменным методом на титановую основу имплантата системы покрытий различной дисперсности и толщины, состоящей из пяти слоев: первых двух из титана или гидрида титана, последующих двух слоев из смеси титана или гидрида титана с гидроксиапатитом кальция, отличающихся содержанием компонентов в слоях, и наружного, пятого слоя из гидроксиапатита кальция. Напыление ведут послойно при различных режимах, обеспечивающих плавный переход от компактной структуры титановой основы имплантата через многослойную систему переходного покрытия к тонкому биологически активному поверхностному пористому слою.
Однако при плазменном напылении биоактивного порошка теряются многие исходные химические свойства, что приводит к недостаточной биоактивности покрытия. Кроме того, покрытие является хрупким, что не позволяет использовать его при изготовлении высоконагруженных имплантатов.
Задача изобретения заключается в повышении биоактивности и механической прочности имплантата.
Техническим результатом является образование в поверхностном слое системы покрытий имплантата большого количества упрочняющих фаз, препятствующих развитию усталостных трещин и выходу их на поверхность, а также образование на поверхности системы покрытий тонкой беспористой наноразмерной алмазоподобной пленки, способствующей быстрому росту костной ткани.
Поставленная задача решается тем, что в способе изготовления внутрикостного имплантата, включающем пескоструйную обработку поверхности имплантата частицами оксида алюминия, послойное напыление плазменным методом на основу имплантата системы биосовместимых покрытий из смеси порошков титана или гидрида титана и гидроксиапатита кальция, при этом первым слоем напыляют титан или гидрид титана дисперсностью 3-5 мкм с дистанцией напыления 70-80 мм и толщиной 5-10 мкм, вторым слоем - титан или гидрид титана дисперсностью 50-100 мкм с дистанцией напыления 100 мм, толщиной 15-20 мкм, третьим слоем напыляют смесью титана или гидрида титана дисперсностью 50-100 мкм и гидроксиапатита кальция дисперсностью 5-10 мкм, с соотношением 70-80 и 30-20 мас.% соответственно, с дистанцией напыления 90-100 мм и толщиной слоя 30-50 мкм, четвертым слоем - смесь титана или гидрида титана дисперсностью 50-100 мкм и гидроксиапатита кальция дисперсностью 20-40 мкм, с соотношением 50-60 и 50-40 мас.% соответственно, с дистанцией напыления 80-85 мм и толщиной 30-50 мкм, пятым слоем напыляют гидроксиапатит кальция дисперсностью 40-70 мкм с дистанцией напыления 70 мм и толщиной слоя 20-30 мкм, согласно предлагаемому техническому решению, многослойную систему биосовместимых покрытий облучают в вакуумной среде углеводородного газа высокоэнергетическими ионами инертного газа с энергией 40-130 кэВ и дозой облучения 2000-5000 мкКл/см2.
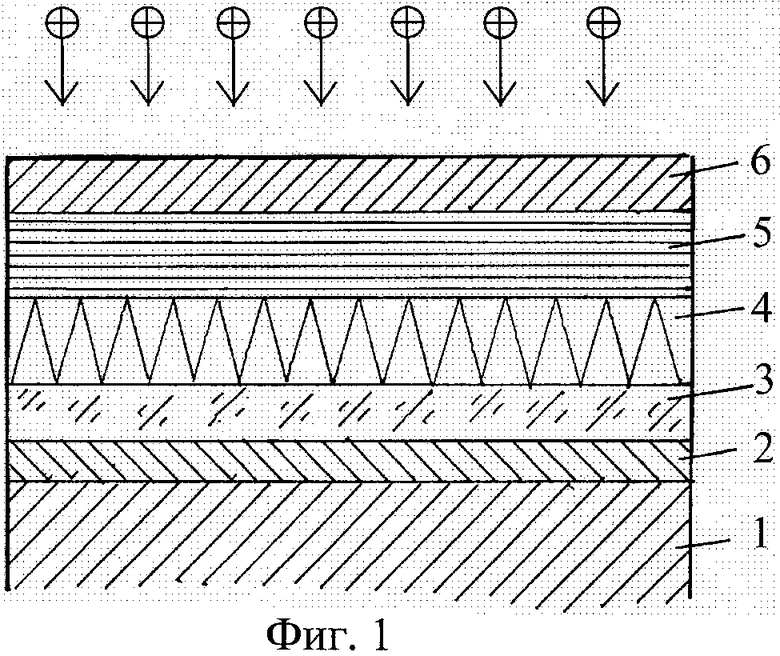
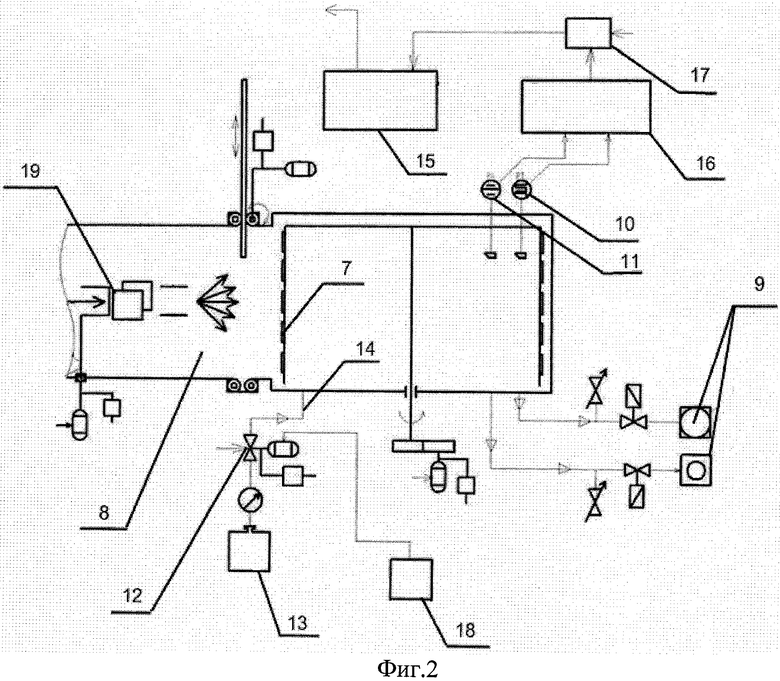
Изобретение поясняется чертежами, где на фиг.1 представлена схема послойного формирования покрытий, на фиг.2 - схема ионно-лучевой обработки системы покрытий.
Предлагаемый способ изготовления стоматологического имплантата осуществляют следующим образом (см. фиг.1). Перед напылением поверхность основы металлического имплантата 1 подвергают пескоструйной обработке частицами оксида алюминия, затем наносят первый слой 2 толщиной 5-10 мкм из порошка титана или гидрида титана дисперсностью 3-5 мкм с расстояния 70-80 мкм; второй слой 3 толщиной 15-20 мкм напыляют титаном или гидридом титана дисперсностью 50-100 мкм с дистанцией напыления 100 мм; третий слой 4 толщиной 30-50 мкм - смесью титана или гидрида титана (70-80 мас.%) и гидроксиапатита кальция (30-20 мас.%) дисперсностью 50-100 мкм и 5-10 мкм соответственно, с расстояния 90-100 мм; четвертый слой 5 толщиной 30-50 мкм - смесью титана или гидрида титана (50-60 мас.%) с гидроксиапатитом кальция (50-40 мас.%) дисперсностью 50-100 мкм и 20-40 мкм, с дистанцией напыления 80-85 мм и пятый слой 6 толщиной 20-30 мкм напыляют гидроксиапатитом кальция дисперсностью 40-70 мкм с расстояния 70 мм, соответственно. Напыление осуществляют плазменным методом в атмосфере в струе защитного газа, например аргона, при этом расход плазмообразующего газа составляет 20-40 л/мин. Скорость перемещения плазмотрона при напылении 80-700 мм/мин, ток плазменной дуги составляет 450-540 А, напряжение дуги 30 В, скорость вращения детали 110-160 об/мин.
Затем изделие с многослойной системой покрытий закрепляют на барабане 7 (см. фиг.2) в установке ионно-лучевого легирования, например «Везувий-5» (Мейер Дж. Эриксон Л. «Ионное легирование полупроводников» 1970 г. М.: Мир). В объеме приемной камеры 8 установки откачивают давление до 10-6 мм рт.ст. с помощью высоковакуумных насосов 9, которое фиксируют ионизационным датчиком высокого вакуума 10 и вакуумметром 11. Далее, по команде оператора, в камеру 8 через игольчатый клапан 12 из баллона 13 по герметичному трубопроводу 14 в объем приемной камеры 8 подают реакционный углеводородный газ, например оксид углерода (СО) или углеводорода (СН), при этом давление в камере по средствам ЭВМ 15 (автоматически) изменяют в сторону повышения, но не более 10-4 мм рт.ст., что фиксируется ионизационным датчиком высокого вакуума 10 и вакуумметром 11. Сигнал с датчика высокого вакуума 10 поступает на электронный блок 16, где происходит сравнение полученных значений вакуума с заданной величиной. Далее сигнал через устройство сопряжения с объектом 17 (УСО) передается на ЭВМ и уже затем на источник питания привода 18 игольчатого клапана 12. Данный процесс повторяется постоянно с целью поддержания заданной величины давления в объеме приемной камеры 8 установки. Далее изделие с многослойной системой покрытий, находящееся на барабане 7 в приемной камере 8, облучают ионами инертного газа с энергией 40-130 кэВ и интегральной дозой 2000-5000 мкКл/см2, например ионами аргона (Ar) или неона (Ne) (см. табл.1, 2), которые образуются в разрядной камере ионного источника 19 за счет ионизации паров рабочего вещества в дуговом разряде и вытягиваются из него при помощи электрода.
Облучение изделий осуществляют в среде газа, например CO, CH, являющегося источником углерода, необходимого для синтеза на поверхности изделий углеродсодержащей наноразмерной алмазоподобной полимерной пленки. При ионно-лучевой обработке в поверхностном слое адсорбированных углеродсодержащих фрагментов происходят процессы ионизации и диссоциации молекул, приводящие к возникновению заряженных радикалов, процесс сшивания которых стимулируется энергетическим воздействием ионно-лучевой обработки и контролируется поступлением электронов из нижележащего металла. По мере увеличения толщины заполимеризовавшегося слоя поступление электронов к поверхности реакции затрудняется и при достижении толщины порядка длины туннелирования электронов рост алмазоподобной полимерной пленки прекращается. Наиболее интенсивно процесс роста протекает на участках заполимеризовавшегося слоя с меньшей толщиной и порами, что обеспечивает высокую равномерность и беспористость пленки.
Облучение многослойных биосовместимых покрытий высокоэнергетическими ионами инертного газа, например Ar, He, Xe, Rn, Kr, Ne, являющимися химически не активными с металлом, обеспечивает максимальную прочность сцепления покрытия с соседними слоями и с подложкой, за счет ионного перемешивания фрагментов адсорбированной на поверхности покрытий полимерной пленкой с приповерхностным слоем металла. Облучение высокоэнергетическими ионами инертного газа способствует появлению на многослойном покрытии равномерной алмазоподобной беспористой полимерной пленки, обладающей высокой химической инертностью и механической прочностью, способствующей быстрому росту костной ткани. После облучения системы покрытий в структуре образуется большое количество упрочняющих фаз, препятствующих развитию усталостных трещин. При введении в костную ткань такого имплантата с алмазоподобным покрытием наблюдается эффективное прорастание кости в поры покрытия, что обеспечивает прочное закрепление имплантата и длительное его функционирование в организме.
В таблицах 1, 2 представлены характеристики получаемого покрытия в зависимости от дозы и энергии облучения, соответственно.
мкКл/см2
Q, кгс/мм2
Из таблиц 1, 2 видно, что наиболее оптимальными диапазонами энергии и дозы облучения, при котором покрытия обладают высокой механической прочностью, являются значения 40-130 кэВ, 2000-5000 мкКл/см2, соответственно.
При ионно-лучевом облучении покрытий с энергетическим воздействием менее 40 кэВ процесс сшивки полимерной углеродсодержащей пленки происходит менее эффективно, т.к. ионам недостаточно энергетического воздействия, необходимого для разрыва химических связей атомов кристаллической решетки нижележащего металла, а при облучении с энергетическим воздействием более 130 кэВ внедряемые ионы из-за большой глубины проникновения затрудняют выход электронов на поверхность покрытий к месту синтеза углеродсодержащей полимерной пленки, что приводит к уменьшению механической прочности покрытий.
Таким образом, предлагаемое техническое решение позволяет повысить механическую прочность и биоактивность покрытия за счет образования на нем алмазоподобной беспористой наноразмерной химически инертной пленки, активно стимулирующей рост костной ткани и обладающей высокой твердостью.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИЗГОТОВЛЕНИЯ ВНУТРИКОСТНОГО ИМПЛАНТАТА С ИОННО-ЛУЧЕВОЙ МОДИФИКАЦИЕЙ | 2013 |
|
RU2530568C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВНУТРИКОСТНОГО СТОМАТОЛОГИЧЕСКОГО ИМПЛАНТАТА С УГЛЕРОДНЫМ НАНОПОКРЫТИЕМ | 2014 |
|
RU2571559C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВНУТРИКОСТНОГО СТОМАТОЛОГИЧЕСКОГО ИМПЛАНТАТА С УГЛЕРОДНЫМ НАНОПОКРЫТИЕМ | 2012 |
|
RU2490032C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВНУТРИКОСТНОГО СТОМАТОЛОГИЧЕСКОГО ИМПЛАНТАТА | 2013 |
|
RU2525737C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВНУТРИКОСТНОГО СТОМАТОЛОГИЧЕСКОГО ИМПЛАНТАТА С ПЛАЗМОНАПЫЛЕННЫМ МНОГОСЛОЙНЫМ БИОАКТИВНЫМ ПОКРЫТИЕМ | 1998 |
|
RU2146535C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВНУТРИКОСТНЫХ ИМПЛАНТАТОВ С БИОАКТИВНЫМ ПОКРЫТИЕМ | 2013 |
|
RU2530573C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВНУТРИКОСТНЫХ ИМПЛАНТАТОВ | 2010 |
|
RU2443434C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВНУТРИКОСТНЫХ ИМПЛАНТАТОВ С МНОГОСЛОЙНЫМ ПОКРЫТИЕМ | 2013 |
|
RU2526252C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВНУТРИКОСТНЫХ ИМПЛАНТАТОВ С АНТИМИКРОБНЫМ ЭФФЕКТОМ | 2013 |
|
RU2512714C1 |
| Способ изготовления дентального имплантата с использованием композитного нанопокрытия | 2018 |
|
RU2765921C1 |
Изобретение относится к области медицины, а именно к ортопедической стоматологии, и может быть использовано при изготовлении внутрикостных имплантатов путем нанесения на их металлическую основу многослойных плазменных покрытий с последующей ионно-лучевой модификацией. Предлагаемый способ изготовления внутрикостного имплантата включает пескоструйную обработку поверхности имплантата частицами оксида алюминия, послойное напыление плазменным методом на основу имплантата системы биосовместимых покрытий различной дисперсности и толщины, состоящей из пяти слоев: первых двух из титана или гидрида титана, последующих двух слоев из смеси титана или гидрида титана с гидроксиапатитом кальция, отличающихся содержанием компонентов в слоях, и пятого слоя из гидроксиапатита кальция, после чего многослойную систему биосовместимых покрытий облучают в вакуумной среде углеводородного газа высокоэнергетическими ионами инертного газа с энергией 40-130 кэВ и дозой облучения 2000-5000 мкКл/см2. Способ обеспечивает повышение биоактивности и механической прочности имплантата. 2 табл., 2 ил.
Способ изготовления внутрикостного стоматологического имплантата с ионно-лучевой модификацией плазмонапыленного многослойного биосовместимого покрытия, включающий пескоструйную обработку поверхности имплантата частицами оксида алюминия, послойное напыление плазменным методом на основу имплантата системы биосовместимых покрытий из смеси порошков титана или гидрида титана и гидроксиапатита кальция, при этом первым слоем напыляют титан или гидрид титана дисперсностью 3-5 мкм с дистанцией напыления 70-80 мм и толщиной 5-10 мкм, вторым слоем - титан или гидрид титана дисперсностью 50-100 мкм с дистанцией напыления 100 мм, толщиной 15-20 мкм, третьим слоем напыляют смесью титана или гидрида титана дисперсностью 50-100 мкм и гидроксиапатита кальция дисперсностью 5-10 мкм, с соотношением 70-80 и 30-20 мас.% соответственно, с дистанцией напыления 90-100 мм и толщиной слоя 30-50 мкм, четвертым слоем -смесь титана или гидрида титана дисперсностью 50-100 мкм и гидроксиапатита кальция дисперсностью 20-40 мкм, с соотношением 50-60 и 50-40 мас.% соответственно, с дистанцией напыления 80-85 мм и толщиной 30-50 мкм, пятым слоем напыляют гидроксиапатит кальция дисперсностью 40-70 мкм с дистанцией напыления 70 мм и толщиной слоя 20-30 мкм, отличающийся тем, что многослойную систему биосовместимых покрытий облучают в вакуумной среде углеводородного газа высокоэнергетическими ионами инертного газа с энергией 40-130 кэВ и дозой облучения 2000-5000 мкКл/см2.
| СПОСОБ ИЗГОТОВЛЕНИЯ ВНУТРИКОСТНОГО СТОМАТОЛОГИЧЕСКОГО ИМПЛАНТАТА С ПЛАЗМОНАПЫЛЕННЫМ МНОГОСЛОЙНЫМ БИОАКТИВНЫМ ПОКРЫТИЕМ | 1998 |
|
RU2146535C1 |
| JP 2005034333 A, 10.02.2005 | |||
| KR 100809574 B1, 04.03.2008 | |||
| УСТРОЙСТВО ДЛЯ ПОГЛОЩЕНИЯ ИЗ ГАЗОВ ВОДЯНЫХ И ДРУГИХ ПАРОВ | 1926 |
|
SU6030A1 |
| Аппарат для цинкования железных листов | 1924 |
|
SU1402A1 |
| СПОСОБ ПЛАЗМЕННОЙ ОБРАБОТКИ ПОВЕРХНОСТИ ИЗДЕЛИЯ | 2007 |
|
RU2340703C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОСТРУКТУРИРОВАННЫХ ПЛЕНОЧНЫХ ПОКРЫТИЙ (ВАРИАНТЫ) | 2008 |
|
RU2371513C1 |
Авторы
Даты
2012-08-20—Публикация
2011-03-17—Подача