Изобретение относится к медицине, в частности к препаратам, ускоряющим ранозаживление.
Создание современных ранозаживляющих средств продиктовано высоким уровнем травматизма в России, когда каждый десятый житель страны ежегодно подвергается травмам. Уровень пострадавших резко возрастает в результате террористических актов, проведения военных действий и при возникновении природных катаклизмов. В любом случае травматизм, как повреждающий фактор, приводит к нарушению функций организма. Кроме того, высокая резистентность микроорганизмов, инфицирующих раны, усложняет процесс ранозаживления. Поэтому разработка новых современных препаратов, обладающих ранозаживляющим и антимикробным действием, является актуальной.
Ранозаживление является сложным процессом, протекание которого требует баланса микроэлементов, антиоксидантов, матриксных металлопротеиназ и других факторов. Одним из металлов, дефицит которого тормозит ранозаживление, является медь [13]. В последнее время в качестве средств для лечения поражений кожи стали использовать препараты на основе высокодисперсных порошков металлов. Так, разработана повязка на основе наночастиц серебра. Среди препаратов такого класса, популярных, например, в США, являются торговые марки Acticoat, Nucryst. По данным исследователей, указанные препараты ускоряют заживление ожогов, ран, экземы, угревой сыпи [16, 17]. К отечественным препаратам на основе высокодисперсных соединений металлов, обладающих лечебным эффектом, относятся магнитные суппозитории на основе высокодисперсного феррита бария [4].
В качестве аналогов представленного изобретения можно привести ранозаживляющие препараты с наночастицами (НЧ) магния и наночастицами железа, описанные в патентах №2296571, №2306141 [5, 6].
Интерес к нанообъектам связан с пониманием отличия их физико-химических и биологических свойств как от свойств массивных металлических объектов, так и свойств отдельных атомов. Проведенные исследования по влиянию наночастиц металлов на биосистемы позволили выявить их уникальные свойства [3, 7]:
1) наночастицы металлов в 7-50 раз менее токсичны, чем металлы в ионной форме;
2) наночастицы оказывают пролонгированное действие благодаря своей способности осуществлять роль депо элементов в организме;
3) наночастицы, введенные в биотических дозах, стимулируют обменные процессы в организме;
4) наночастицы обладают полифункциональным действием.
В научной литературе имеется много сведений о перспективности применения хитозанов различной структуры в качестве ранозаживляющих агентов [1, 2, 10, 11, 12, 14].
Зависимость ранозаживляющих свойств хитозана, нетоксичного биодеградируемого полимера природного происхождения, от его основных характеристик - молекулярной массы (М.м.) и степени деацетилирования (СД), установлена нами ранее [1, 2].
Наночастицы (НЧ) хитозана также обладают биологической активностью и способны влиять на физиологические процессы в организме. Так, показано, что НЧ хитозана обладают способностью стимулировать пролиферацию лимфоцитов и, таким образом, оказывать положительное влияние на заживление ран [15].
Биологические эффекты НЧ хитозана не являются однозначными. Известно, например, что некоторые НЧ хитозана проявляют высокий цитотоксический эффект на различных культурах клеток опухоли в опытах in vitro [14].
Известно также, что хитозан связывает ионы различных металлов и, в частности, имеет высокое сродство к ионам меди. При этом наблюдается изменение свойств хитозана [14].
Поэтому использование наночастиц различной химической природы в составе ранозаживляющих средств представляется перспективным направлением фармации и медицины.
Задачей данного изобретения является создание современных ранозаживляющих препаратов полифункционального действия, обеспечивающих высокий уровень ранозаживления и обладающих антимикробным эффектом.
Поставленная задача решается тем, что разработаны фармацевтические композиции, ускоряющие ранозаживление и обладающие антимикробной активностью на основе наночастиц меди. Для приготовления препаратов, ускоряющих ранозаживление, использованы наночастицы меди в концентрационном интервале, %: 2×10-5-2×10-2.
Предпочтительно медьсодержащие наночастицы имеют следующие характеристики: наночастицы меди имеют размер частиц 33.8÷103 нм; толщину оксидной пленки 6÷10 нм, фазовый состав: кристаллическая медь 67÷96%, меди оксида CuO - 4÷33%; более окисленные наночастицы меди имеют размер частиц 77÷124 нм, фазовый состав: кристаллическая медь 0.5÷3.3÷23%, CuO - 27.1÷90% и Cu2O - 9.05÷69.5%.
Изобретение относится также к комбинированным препаратам, которые дополнительно содержат производные хитозана, представляющие собой производные низкомолекулярных хитозанов: O-сульфохитозан и N-сульфосукциноил-N-карбоксиметилхитозан, или наночастицы хитозана.
В качестве основы разработанных препаратов предпочтительно используют метилцеллюлозу (МЦ-100), а также Твин-80, глицерин; в качестве консерванта более предпочтительно применяют нипагин. Предпочтительно заявляемые препараты представляют собой мази следующего состава (в г):
1) наночастицы меди - 0.00002-0.002; вазелиновое масло - 10.0-15.0; метилцеллюлоза (МЦ -100) - 3.0-4.0; Твин-80 - 2.0-3.0; нипагин - 0.1-0.3; вода очищенная до 100.0;
2) наночастицы меди - 0.00002-0.002; хитозан - 0.005-0.05; вазелиновое масло - 10.0-15.0; метилцеллюлоза (МЦ -100) - 3.0-4.0; Твин-80 - 2.0-3.0; нипагин - 0.1-0.3; вода очищенная до 100.0;
3) наночастицы меди - 0.00002-0.002; наночастицы хитозана - 0.01-0.0002, вазелиновое масло - 10.0-15.0; метилцеллюлоза (МЦ - 100) - 3.0-4.0; Твин-80 - 2.0-3.0; нипагин - 0.1-0.3; вода очищенная до 100.0.
В другом варианте изобретения предлагается фармацевтическая композиция, ускоряющая ранозаживление и включающая действующее вещество и основу, которая в качестве действующего вещества содержит производное хитозана, которое выбирают из группы, включающей низкомолекулярные производные хитозана или наночастицы хитозана. Производные низкомолекулярных хитозанов - O-сульфохитозан и N-сульфосукциноил-N-карбоксиметилхитозан - синтезированы нами из исходного хитозана СД 89% и М.м. 56 кДа и 200 кДа. Наночастицы хитозана синтезированы из хитозана М.м. 10 кДа, СД 89%. Размер наночастиц хитозана составляет 60-106 нм. Наночастицы хитозана имеют дзета-потенциал 38-42 мВ.
В наиболее предпочтительных вариантах изобретения препараты имеют следующий состав, г:
I.
II.
III.
Комбинированные мази:
IV.
V.
Ниже предствленные схемы иллюстрируют способы осуществления наиболее предпочтительных вариантов изобретения.
I. Состав
Этап 1. Подготовка геля МЦ
Приготовление геля на МЦ-100.
Нипагин растворяли в воде при нагревании (80-90°С). Далее в полученный теплый раствор (60°С) добавляли МЦ-100 и оставляли набухать в течение 1 часа.
Этап 2. Приготовление вазелиновой суспензии наночастиц меди
Точную навеску нанопорошка меди помещали в вазелиновое масло и диспергировали на ультразвуковом диспергаторе УЗДН-А в режиме 44 кГц, 0.5А по следующей схеме: 20 секунд озвучивания - 2 минуты перерыв (3 цикла).
Этап 3. Введение наночастиц меди в основу
К подготовленному гелю МЦ, полученному на первом этапе, прибавляли твин-80 и эмульгировали в течение 10-15 минут на мешалке фирмы MLW (модель ER-10) со скоростью 300 об/мин. К вазелиновой суспензии наночастиц меди добавляли равное количество полученного геля и перемешивали с помощью мешалки фирмы MLW (модель ER-10), со скоростью 300 об/мин, следя за тем, чтобы в полученной массе не появлялись пузырьки воздуха. Далее постепенно добавляли оставшееся количество геля, каждый раз тщательно перемешивая.
II. Состав
Этап 1. Подготовка геля МЦ
Нипагин растворяли в 2/3 рассчитанного объема воды, очищенной при нагревании (80-90°С). В полученный теплый раствор (60°С) добавляли МЦ-100 и оставляли набухать в течение 1 часа. В оставшемся объеме воды (1/3) растворяли навеску производных низкомолекулярных хитозанов.
Этап 2. Введение низкомолекулярных хитозанов
Полученный раствор низкомолекулярных хитозанов добавляли к гелю МЦ и тщательно перемешивали с помощью мешалки фирмы MLW (модель ER-10), со скоростью 300 об/мин, избегая появления пузырьков воздуха.
III. Состав
Этап 1. Подготовка геля
Нипагин растворяли в 2/3 рассчитанного объема воды, очищенной при нагревании (80-90°С), далее в полученный теплый раствор (60°С) добавляли МЦ-100 и оставляли набухать в течение 1 часа.
Этап 2. Введение наночастиц хитозана
В оставшейся объем воды (1/3) водили водную суспензию наночастиц хитозана, добавляли к приготовленному гелю и осторожно перемешивали с помощью мешалки фирмы MLW (модель ER-10), со скоростью 300 об/мин, избегая появления пузырьков воздуха.
IV. Состав
Этап 1. Подготовка геля МЦ
Нипагин растворяли в 2/3 рассчитанного объема воды, очищенной при нагревании (80-90°С). В полученный теплый раствор (60°С) добавляли МЦ-100 и оставляли набухать в течение 1 часа. В оставшемся объеме воды (1/3) растворяли навеску производных низкомолекулярных хитозанов.
Этап 2. Введение низкомолекулярных хитозанов
Полученный раствор низкомолекулярных хитозанов добавляли к гелю МЦ и тщательно перемешивали с помощью мешалки фирмы MLW (модель ER-10), со скоростью 300 об/мин, избегая появления пузырьков воздуха.
Этап 3. Приготовление вазелиновой суспензии наночастиц меди
Точную навеску нанопорошка меди помещали в вазелиновое масло и диспергировали на ультразвуковом диспергаторе УЗДН-А в режиме 44 кГц, 0.5А по следующей схеме: 20 секунд озвучивания - 2 минуты перерыв (3 цикла).
Этап 4. Введение вазелиновой суспензии наночастиц меди
К вазелиновой суспензии наночастиц меди добавляли полученный на втором этапе гель и перемешивали с помощью мешалки фирмы MLW (модель ER-10), со скоростью 300 об/мин, следя за тем, чтобы в полученной массе не появлялись пузырьки воздуха.
V. Состав
Этап 1. Подготовка геля
Нипагин растворяли в 2/3 рассчитанного объема воды, очищенной при нагревании (80-90°С). Далее в полученный теплый раствор (60°С) добавляли МЦ-100 и оставляли набухать в течение 1 часа.
Этап 2. Введение наночастиц хитозана
В оставшийся объем воды (1/3) вводили водную суспензию наночастиц хитозана, добавляли к приготовленному гелю и осторожно перемешивали с помощью мешалки фирмы MLW (модель ER-10), со скоростью 300 об/мин, избегая появления пузырьков воздуха.
Этап 3. Приготовление вазелиновой суспензии наночастиц меди
Точную навеску нанопорошка меди помещали в вазелиновое масло и диспергировали на ультразвуковом диспергаторе УЗДН-А в режиме 44 кГц, 0.5А по следующей схеме: 20 секунд озвучивания - 2 минуты перерыв (3 цикла).
Этап 4. Введение наночастиц меди в основу
К вазелиновой суспензии наночастиц меди добавляли полученный на втором этапе гель и перемешивали с помощью мешалки фирмы MLW (модель ER-10), со скоростью 300 об/мин, следя за тем, чтобы в полученной массе не появлялись пузырьки воздуха.
Для состава I, IV, V полученный продукт представляет собой мазь белого цвета, однородную по составу, без механических включений, с очень слабым специфическим запахом.
Для состава II, III полученный продукт представляет собой бесцветный, прозрачный гель, однородный по составу, без механических включений, без запаха. Производные низкомолекулярных хитозанов - O-сульфохитозан и N-сульфосукциноил-N-карбоксиметилхитозан - синтезированы нами из исходного хитозана СД 89% и М.м. 56 кДа и 200 кДа. Наночастицы хитозана синтезированы из хитозана М.м. 10 кДа, СД 89%. Размер наночастиц хитозана составляет 60-106 нм. Наночастицы хитозана имеют дзета-потенциал 38-42 мВ.
I. Физико-химические характеристики наночастиц меди
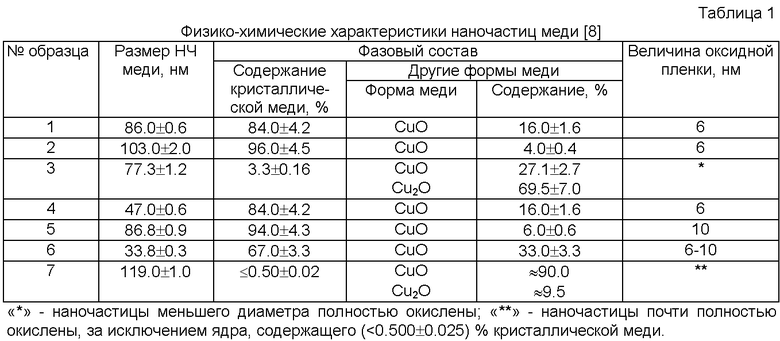
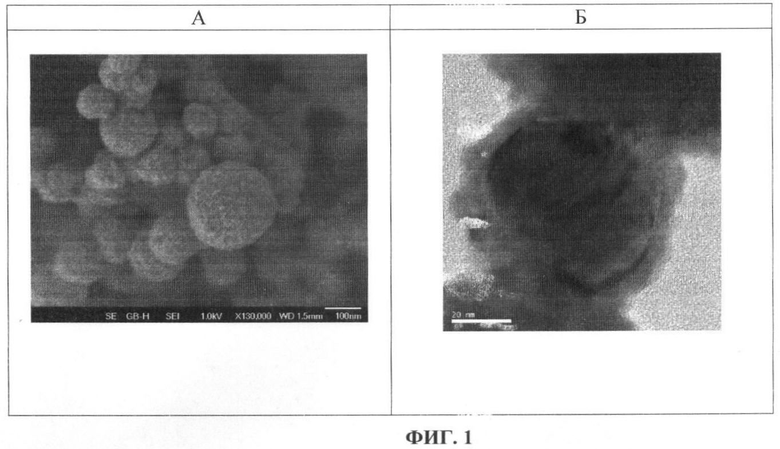
В состав мази вводили наночастицы одного из образцов меди, которые отличаются между собой размером, фазовым составом и толщиной оксидной пленки на поверхности наночастиц (таблица 1). На ФИГ.1 (А и Б) представлены фотографии наночастиц меди образца №2, полученные методами электронной сканирующей микроскопии (А) и просвечивающей электронной микроскопии (Б). Видно, что наночастицы меди образца №2 представляют собой монокристаллические структуры круглой правильной формы, покрытые полупрозрачной пленкой меди оксида (Б).
Основные физико-химические характеристики наночастиц меди представлены в таблице 1 [8].
По диаграммам распределения частиц по размерам и кривым накопления частот установлено, что средний размер наночастиц меди укладывается в диапазон от 33.8 нм (образец №6) до 103.8 нм (образец №2). Размер наночастиц меди образца №3 составляет 77.3 нм, образца №7 - 119,0 нм. Наночастицы меди различаются по фазовому составу. Так, содержание кристаллической меди в ядре наночастиц меди образца №6 составляет 67%, образцов №5 и №2 94% и 96% соответственно.
В наночастицах меди образцов меди №3 и №7 содержание кристаллической меди мало и составляет 3.3% и 0.5% соответственно.
Толщина оксидной пленки на поверхности наночастиц меди меняется в пределах 6-10 нм. При хранении наночастиц в герметичной таре, заполненной инертным газом, величина оксидной пленки практически остается постоянной. При хранении в обычных условиях, т.е. в отсутствие инертного газа, степень окисленности частиц изменяется. Поэтому обычно перед приготовлением мазей проводилось повторное определение степени окисленности наночастиц.
Состав оксидной пленки на поверхности наночастиц меди образцов №1, №2, №4, №5, №6 одинаков и представлен CuO. В то же время в состав оксидной пленки наночастиц меди образцов №3 и №7, помимо Cu (II) оксида, входит Cu (I) оксид.
Следовательно, наночастицы меди отличаются размером, фазовым составом, толщиной оксидной пленки.
II. Ранозаживляющая активность
II.1. Ранозаживляющее действие наночастиц меди с разными физико-химическими характеристиками в составе мази
Разработанные нами мази с наночастицами меди, имеющие физико-химические характеристики, описанные в таблице 1, ежедневно наносили на поверхность полнослойных ран первоначальной площадью 60 мм2 в количестве 0.2 г. В качестве эталонного препарата использовали заводские мази «Солкосерил» и «Левомеколь», которые наносили на раны тем же путем, в том же количестве и по той же схеме лечения. Во всех вариантах опытов ежедневно регистрировали изменение площади ран и по кинетическим кривым изменения площади ран рассчитывали скорость натяжения ран и оценивали время полного заживления ран. Действие препаратов изучали на белых мышах-самках весом 18-20 г линии SHK, находящихся на общевиварийном рационе кормления [1]. Экспериментальные исследования на животных проводили в соответствии с инструкциями, рекомендуемыми нашим институтом, 1987 г. и «The Guide for the Care and Use of Laboratory Animals (National Academy Press Washington, D.C. 1996)».
Пример 1. Влияние мази с наночастицами меди образца №5 и образца №7 на кинетику заживления ран
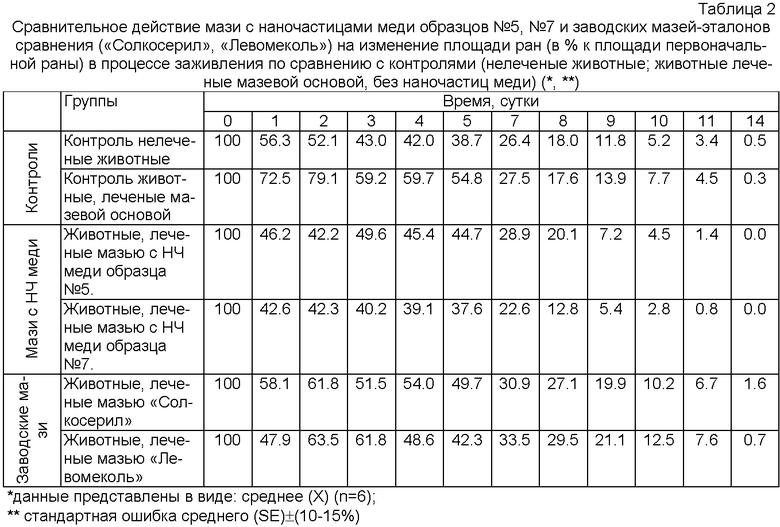
В таблице 2 представлены данные по изменению площади ран в процессе их заживления: нелеченых животных (контроль 1), леченых мазевой основой без наночастиц меди (контроль 2), леченых мазями с наночастицами меди образца №5, образца №7, а также леченых заводскими мазями «Солкосерил» и «Левомеколь», взятыми в качестве эталона сравнения.
Исследование заживления ран позволило установить, что экспериментальные полнослойные раны в двух контрольных группах и группах, леченых мазями-эталонами «Солкосерил» и «Левомеколь», через 14 суток после нанесения ран имели площадь 0.3-1.6% к первоначальной площади раны. В то же время при лечении полнослойных ран мазями с наночастицами меди раны полностью заживают через 14 суток после их нанесения.
Следовательно, по влиянию на время полного заживления разработанные нами мази имеют преимущество по сравнению с мазями-эталонами «Солкосерилом» и «Левомеколем».
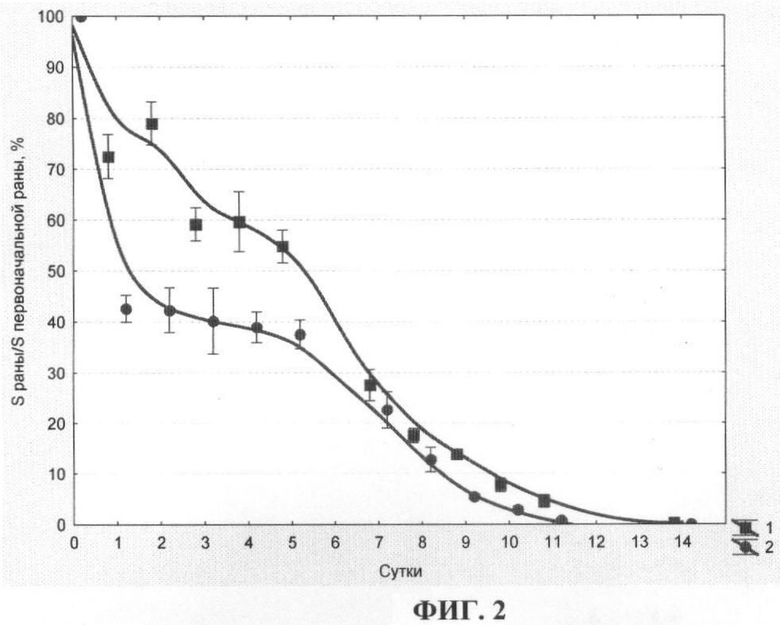
На ФИГ.2 представлены кинетические кривые изменения площади экспериментальных полнослойных ран при действии мазевой основы без наночастиц (кривая 1), при действии мази с наночастицами меди образца №7 (кривая 2). Кинетика изменения площади ран в процессе лечения мазями с наночастицами меди свидетельствует об эффективном влиянии мазей на течение раневого процесса.
Пример 2. Влияние мази с наночастицами меди на удельную скорость первичного натяжения экспериментальных полнослойных ран
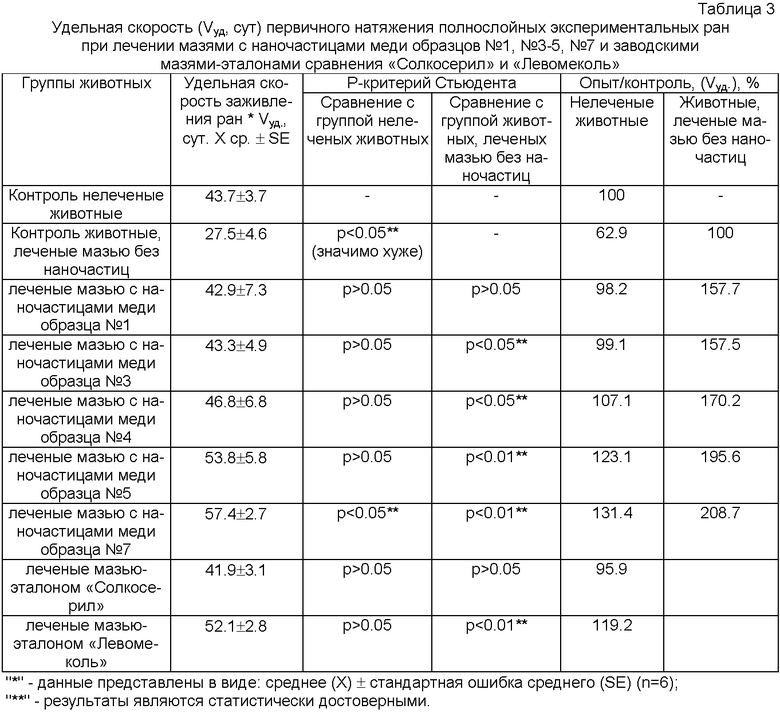
Для оценки эффективности влияния разработанных нами мазей с наночастицами меди на течение раневого процесса мы провели расчет удельных скоростей первичного натяжения ран: [Vуд=(So-S1)/t], где So - площадь исходной раны, S1 - площадь раны через сутки после операции, t - время между измерениями площадей (в сутках). Данные по изменению скорости первичного натяжения ран при лечении мазями с наночастицами меди представлены в таблице 3. Результаты исследования показывают, что мази, содержащие наночастицы меди образца №5 и образца №7, по-разному влияют на удельную скорость натяжения ран. Мази с наночастицами меди образца №5 и образца №7 увеличивают скорость первичного натяжения ран на 23.1 и 31.4% соответственно по сравнению со скоростью первичного натяжения ран нелеченых животных и в 2.0 раза по сравнению со скоростью натяжения ран животных, леченых мазевой основой. Мази с наночастицами меди образца №1 и образца №3 не изменяют показатель удельной скорости натяжения ран по сравнению с нелечеными животными и увеличивают удельную скорость натяжения ран на 57% по сравнению со скоростью натяжения ран животных, леченых мазевой основой. Мазь-эталон «Солкосерил» практически не изменяет показатель удельной скорости натяжения ран по сравнению с нелечеными животными, мазь-эталон «Левомеколь» ускоряет заживление ран на 19.2%. Следовательно, по эффективности воздействия на скорость первичного натяжения ран мази с наночастицами меди имеют преимущество по сравнению с мазями-эталонами «Солкосерилом» и «Левомеколем».
Пример 3. Влияние мазей на кинетику изменения площади ран в процессе заживления в зависимости от концентрации наночастиц меди образца №2 в препарате
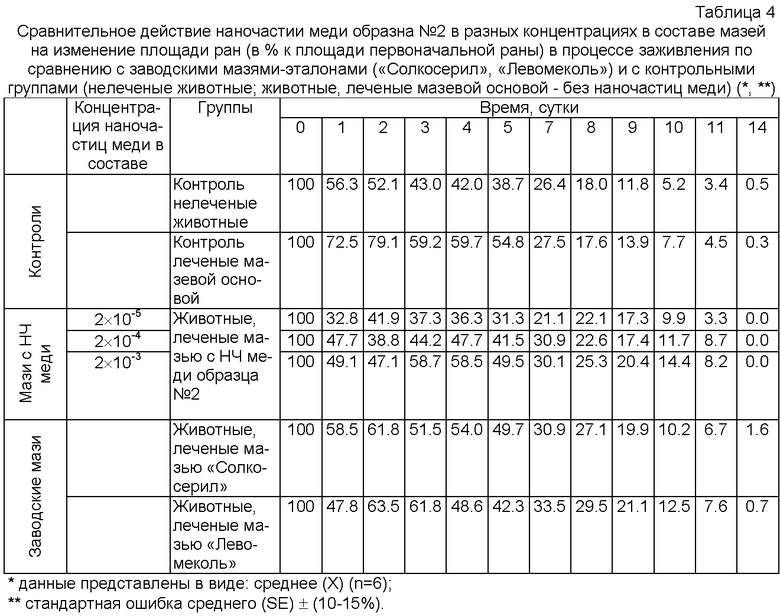
Для установления концентрационной зависимости влияния наночастиц меди в составе мази на кинетику заживления ран были использованы наночастицы меди образца №2 в следующих концентрациях, в %: 2×10-5, 2×10-4, 2×10-3. Результаты исследований представлены в таблице 4. Результаты показывают, что мази с наночастицами меди образца №2 в изученном интервале доз обладают ранозаживляющей активностью, ускоряя ранозаживление практически в течение всего периода заживления ран. Сравнение эффективности разработанных нами мазей с мазями-эталонами на изменение площади ран в процессе заживления показало, что при лечении мазями с наночастицами меди полное заживление ран наблюдается через 14 суток, в то время как при лечении заводской мазью «Солкосерил» и заводской мазью «Левомеколь» размеры незаживших ран через 14 суток составляют 1.6 и 0.7% (по сравнению с исходными ранами) соответственно. Следует также отметить, что в изученном интервале концентраций наибольшим эффектом обладает мазь с меньшей концентрацией наночастиц.
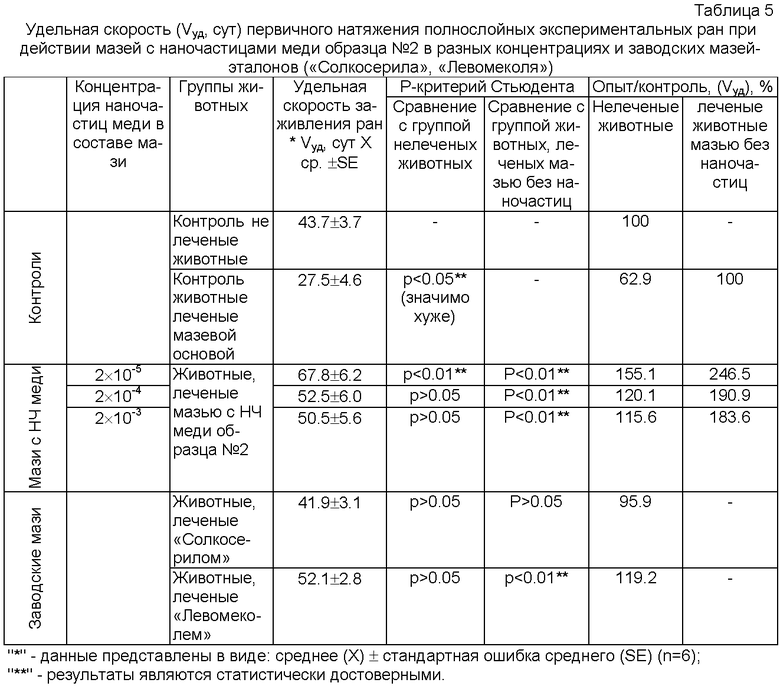
Пример 4. Удельная скорость первичного натяжения экспериментальных полнослойных ран при лечении мазями с наночастицами меди образца №2 в разных концентрациях
Учитывая эффективное влияние разработанных нами мазей с наночастицами меди на течение раневого процесса, был проведен расчет удельной скорости первичного натяжения ран при лечении мазями, содержащими наночастицы меди в разных концентрациях. Результаты представлены в таблице 5. Нами установлено, что при концентрациях наночастиц меди образца №2 в составе мази, в %: 2×10-5, 2×10-4, 2×10-3 наблюдается увеличение скорости первичного натяжения ран на 55.1%, на 20.1%, на 15.6% по сравнению с контролем (не леченые животные) соответственно и на 146.5%, 90.9% и 83.6% по сравнению со скоростью натяжения ран животных, леченых мазевой основой. При сравнении эффективности действия наночастиц меди с мазями-эталонами «Солкосерилом» и «Левомеколем» установлено, что мазь «Левомеколь» ускоряет заживление ран на 19.2% по сравнению с нелеченым контролем, а мазь «Солкосерил» уменьшает удельную скорость первичного натяжения ран на 4.1%.
Следовательно, мази с наночастицами меди образца №2 в концентрациях, в %: 2×10-5, 2×10-4, 2×10-3 увеличивают скорость первичного натяжения ран. При этом мазь с наночастицами меди в концентрации 2×10-5% проявляет более высокую ранозаживляющую активность, чем мази с наночастицами меди в концентрациях, в %: 2×10-4 и 2×10-3.
II.2. Ранозаживляющее сочетанное действие наночастиц меди с разными физико-химическими характеристиками и производными низкомолекулярных хитозанов, а также с наночастицами хитозана в составе мази
Разработанные нами комбинированные мази с наночастицами меди образцов №1 и №2, имеющими физико-химические характеристики, описанные в таблице 1, с производными низкомолекулярных хитозанов, а также с наночастицами хитозана, ежедневно наносили на поверхность полнослойных ран первоначальной площадью 60 мм2 в количестве 0.2 г. В качестве эталонного препарата использовали заводские мази: «Солкосерил» и «Левомеколь», которые наносили на раны тем же путем, в том же количестве и по той же схеме лечения, что и разработанные нами комбинированные мази. Во всех вариантах опытов ежедневно регистрировали изменение площади ран и по кинетическим кривым изменения площади ран рассчитывали скорость натяжения ран и оценивали время полного заживления ран. Действие препаратов изучали на белых мышах-самках весом 18-20 г линии SHK, находящихся на общевиварийном рационе кормления [1].
Пример 5. Влияние мази с производными низкомолекулярных хитозанов на удельную скорость первичного натяжения полнослойных экспериментальных ран
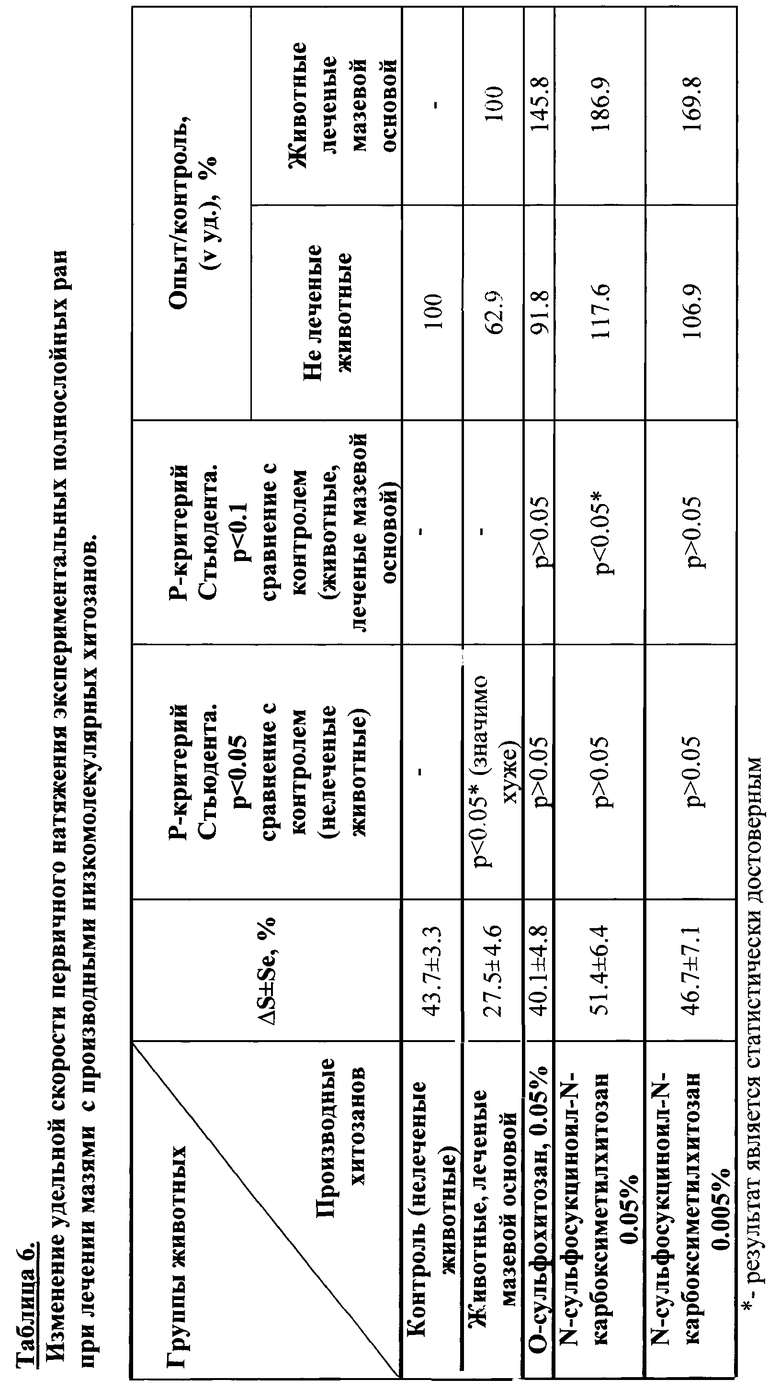
Для исследования выбраны производные низкомолекулярных хитозанов: O-сульфохитозан и N-сульфосукциноил-N-карбоксиметилхитозан, синтезированные нами из исходного хитозана СД 89% М.м. 56 кДа и 200 кДа. Результаты исследований представлены в таблице 6.
O-сульфохитозан в составе мази в концентрации 0.05% уменьшает удельную скорость первичного натяжения ран на 8.2% по сравнению с контролем (нелечеными животными) и увеличивает скорость на 45.8% по сравнению с результатами лечения животных мазевой основой.
N-сульфосукциноил-N-карбоксиметилхитозан в составе мази в концентрации 0.05% способствует увеличению удельной скорости ранозаживления на 17.6% по сравнению с контролем (нелечеными животными) и достоверному увеличению удельной скорости ранозаживления на 86.9% по сравнению с животными, лечеными мазевой основой.
N-сульфосукциноил-N-карбоксиметилхитозан в составе мази в концентрации 0.005% способствует увеличению удельной скорости ранозаживления на 69.8% по сравнению с животными, лечеными мазевой основой, и на 6.9% по сравнению с контролем (нелечеными животными).
Пример 6. Влияние мази с наночастицами хитозана на удельную скорость первичного натяжения экспериментальных полнослойных ран
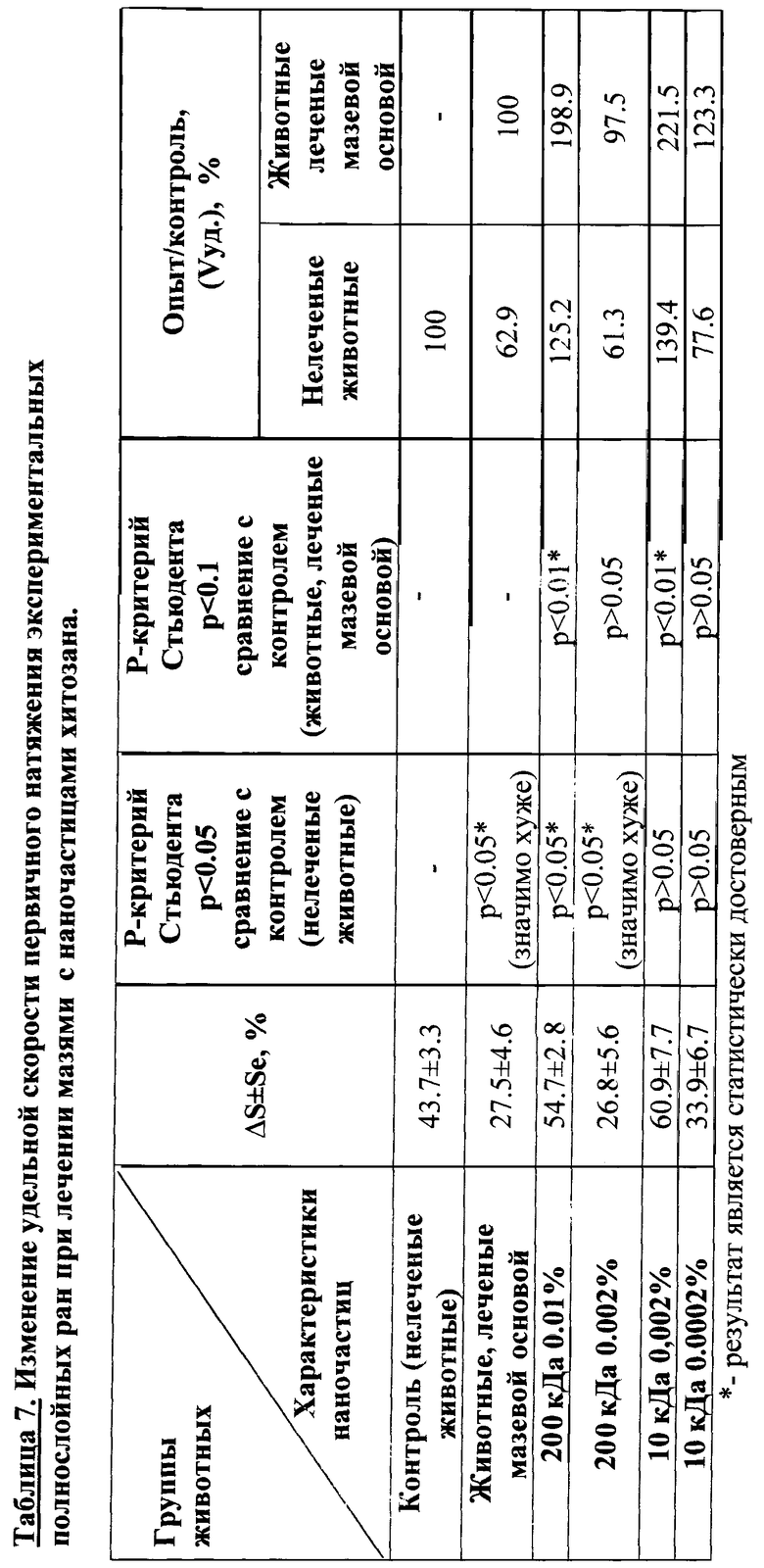
В таблице 7 представлены данные по влиянию наночастиц хитозана в составе мази на удельную скорость первичного натяжения экспериментальных полнослойных ран. Для исследования использованы наночастицы хитозана, синтезированные из низкомолекулярного хитозана М.м. 200 кДа, введенные в мазь в концентрациях, в %: 0.01 и 0.002, а также наночастицы хитозана, синтезированные из низкомолекулярного хитозана М.м. 10 кДа, введенные в мазь в концентрациях, в %: 0.002 и 0.0002.
Видно, что при лечении ран мазью с наночастицами хитозана происходит изменение удельной скорости ранозаживления. Лечение мазью с наночастицами хитозана, синтезированными из хитозана М.м. 200 кДа, в концентрации 0.01% в составе мази способствует достоверному увеличению удельной скорости ранозаживления на 25.2% по сравнению с контролем (нелечеными животными) и на 98.9% по сравнению с животными, лечеными мазевой основой. Уменьшение концентрации наночастиц хитозана в мази до концентрации 0.002% замедляет заживление ран, уменьшая удельную скорость ранозаживления на 39.7% по сравнению с контролем (нелечеными животными) и на 2.5% по сравнению с животными, лечеными мазевой основой. Мазь с наночастицами хитозана, синтезированными из хитозана М.м. 10 кДа, в концентрации 0.002% способствует увеличению удельной скорости ранозаживления на 39.4% по сравнению с контролем (нелечеными животными) и достоверному увеличению скорости в 2.2 раза по сравнению с животными, лечеными мазевой основой. Лечение ран мазью с наночастицами хитозана, синтезированными из хитозана М.м. 10 кДа, в концентрации 0.0002% в составе мази приводит к уменьшению удельной скорости ранозаживления на 22.4% по сравнению с контролем (нелечеными животными) и увеличению удельной скорости ранозаживления на 23.3% по сравнению с животными, лечеными мазевой основой.
Пример 7. Влияние комбинированной мази с наночастицами меди и производными низкомолекулярных хитозанов на удельную скорость первичного натяжения экспериментальных полнослойных ран
Учитывая ранозаживляющий эффект мазей, содержащих модифицированные наночастицы меди, мазей, содержащих производные хитозанов, нами были разработаны мази комбинированного состава, включающие как наночастицы меди, так и производные низкомолекулярных хитозанов. Результаты исследований по влиянию комбинированных мазей на удельную скорость первичного натяжения ран представлены на ФИГ.4 и ФИГ.5.
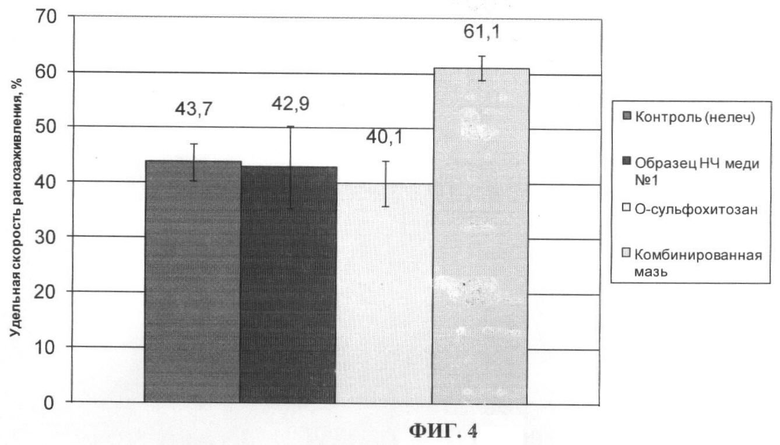
На ФИГ.4 представлены данные по изменению удельной скорости ранозаживления при лечении комбинированной мазью, содержащей наночастицы меди образца №1 в концентрации 0.002% и производное низкомолекулярных хитозанов - O-сульфохитозан в концентрации 0.05%. Лечение комбинированной мазью приводит к достоверному увеличению удельной скорости ранозаживления в 1.5 раза по сравнению с группой, леченой мазью с O-сульфохитозаном, в 1.4 раза по сравнению с группой, леченой мазью с наночастицами меди образца №1 и в 1.4 раза по сравнению с контрольной группой (нелеченые животные)
При лечении комбинированной мазью, содержащей наночастицы меди образца №1 в концентрации 0.002% и производное низкомолекулярных хитозанов - O-сульфохитозан в концентрации 0.05%, усиление эффекта ранозаживления происходит за счет синергизма действия компонентов органической (O-сульфохитозан) и неорганической (наночастицы меди) природы, способствуя увеличению удельной скорости заживления ран.
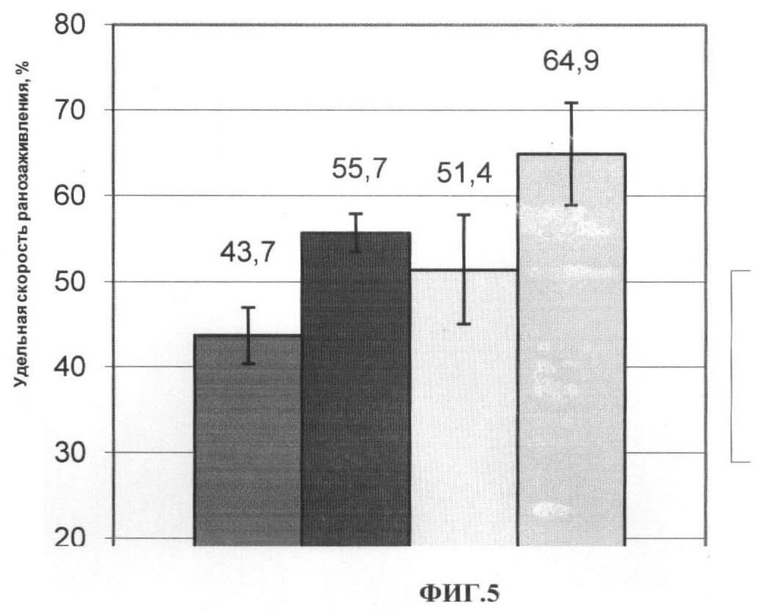
На ФИГ.5 представлены данные по изменению удельной скорости ранозаживления ран при лечении комбинированной мазью, содержащей наночастицы меди образца №2 в концентрации 0.002% и производное низкомолекулярных хитозанов - N-сульфосукциноил-N-карбоксиметилхитозан в концентрации 0.05%. Лечение комбинированной мазью приводит к увеличению удельной скорости ранозаживления на 26% по сравнению с мазью, содержащей N-сульфосукциноил-N-карбоксиметилхитозан в концентрации 0.05%, на 16.5% по сравнению с мазью, содержащей наночастицы меди образца №2 и на 48.5% по сравнению с контрольной группой (нелеченые животные).
При лечении комбинированной мазью, содержащей наночастицы меди образца №2 в концентрации 0.002% и производное низкомолекулярных хитозанов - N-сульфосукциноил-N-карбоксиметилхитозан, усиление эффекта ранозаживления происходит за счет синергизма действия компонентов органической (N-сульфосукциноил-N-карбоксиметилхитозан) и неорганической (наночастицы меди) природы, способствуя увеличению скорости заживления ран.
Учитывая ранозаживляющий эффект мазей, содержащих модифицированные наночастицы меди, мазей, содержащих наночастицы хитозанов, нами были разработаны мази комбинированного состава, включающие как наночастицы меди, так и наночастицы низкомолекулярных хитозанов. Результаты исследований по влиянию комбинированных мазей на удельную скорость первичного натяжения ран представлены на ФИГ. 6.
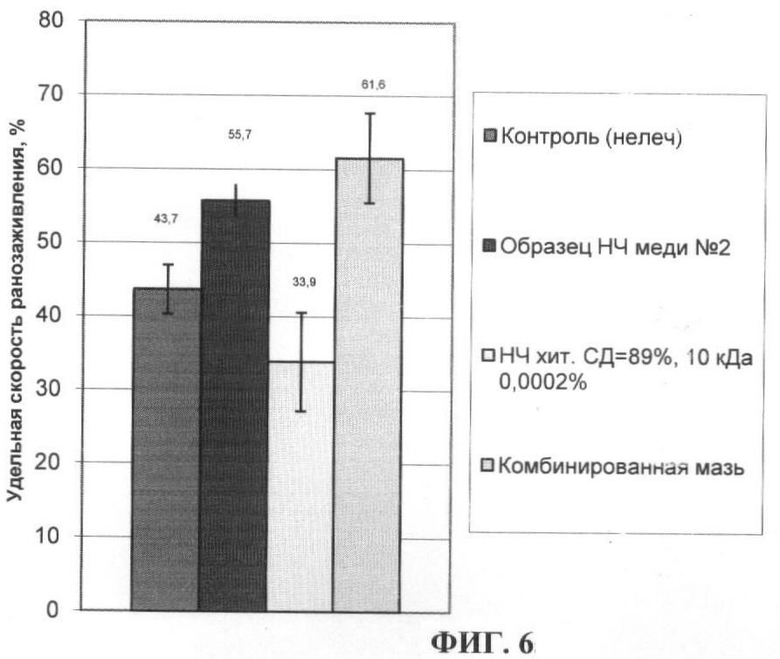
На ФИГ.6 представлены данные по изменению удельной скорости ранозаживления при лечении комбинированной мазью, содержащей наночастицы меди образца №2 в концентрации 0.002% и наночастицы хитозанов, синтезированные из хитозана СД 89% и М.м. 10 кДа, в концентрации 0.0002% в составе мази. Лечение комбинированной мазью увеличивает удельную скорость ранозаживления на 10.5% по сравнению с группой, леченой мазью с наночастицами меди образца №2, увеличивает удельную скорость ранозаживления на 81.7% по сравнению с группой, леченой мазью с наночастицами хитозана, и на 40.9% по сравнению с контрольной группой (нелеченые животные).
При лечении комбинированной мазью, содержащей НЧ хитозана и НЧ меди образца №2, усиление эффекта ранозаживления происходит за счет синергизма действия компонентов органической (наночастицы хитозана) и неорганической (наночастицы меди) природы, способствуя увеличению скорости заживления ран.
III. Антимикробная активность мазей с наночастицами меди
В стерильные чашки Петри одинакового диаметра с ровным плоским дном разливается среда, пригодная для выращивания тест-микробов: Staphylococcus albus (St. albus) и Escherichia coli AB 1157 (E. coli АВ1157). Состав среды роста микроорганизмов (в г): пептон - 10, дрожжевой экстракт - 5, натрия хлорида - 5, агар-агар - 20 в 1 л дистиллированной воды. После застывания агар-агара в чашки Петри высевают тест-культуру микроорганизмов. Посев проводят равномерно и одинаково во все чашки из предварительно подготовленной суспензии. Плотность засева должна быть достаточной для роста сплошного газона. Чашки растирают стерильным шпателем. Образцы наночастиц меди с разными физико-химическими характеристиками помещали на бумажные глицериновые диски в количестве 5 мг/диск, эталон сравнения для образцов нанопорошков стрептомицин в количестве 100 мкг/диск. Разработанные нами мази с наночастицами меди и мази-эталоны: «Солкосерил» и «Левомеколь», помещали на бумажные диски в количестве 50 мг/диск. Диски раскладывали на поверхности агара в предварительно подготовленные чашки Петри, засеянные тест-культурами. Далее чашки Петри на сутки ставили в термостат при температуре 37°С. Через сутки чашки вынимали из термостата и фотографировали. Если испытуемый образец оказывает влияние на рост тест-микроба, то образуется зона задержки роста клеток. По площади зоны задержки роста (мм2) оценивали интенсивность влияния испытуемого образца на тест-микробы [9].
Пример 9. Оценка антимикробной активности наночастиц меди дискодиффузионным методом
Образцы наночастиц меди с разными физико-химическими характеристиками в концентрации 5 мг/диск помещали на диск, эталон сравнения - стрептомицин помещали на диск в концентрации 100 мкг. Диски раскладывали на чашки Петри с агаром, засеянные тест-культурами: St. albus и E.coli AB 1157. Антимикробную активность наночастиц меди и эталонов сравнения - стрептомицина оценивали по величине зон задержки роста бактерий.
Результаты исследования приведены в таблице 8. Нами установлено, что образцы наночастиц меди обладают антибактериальной активностью в отношении клеток тест-культур как грамположительных, так и грамотрицательных микроорганизмов. Однако существуют различия в эффективности действия наночастиц. Видно, что площади зон задержки роста бактерий более выражены при действии наночастиц меди в отношении клеток тест-культуры St. albus no сравнению с клетками Е. coli AB1157. Причем наночастицы образцов меди по-разному влияют на бактерии: наибольшее антимикробное действие на клетки тест-культуры St. albus оказывают наночастицы меди образцов №5 и №6, а на клетки тест-культуры Е. coli AB1157 - наночастицы меди образца №4. Наименее выраженным антибактериальным действием в отношении клеток тест-культуры St. albus обладают наночастицы меди образцов №1 и №2, а в отношении клеток тест-культуры Е. coli AB1157 - наночастицы меди образца №1. Наночастицы образцов №3 и №7 обладают одинаковым антимикробным действием в отношении клеток тест-культур. В этих исследованиях в качестве эталона сравнения использовали классический антибиотик - стрептомицин в концентрации 100 мкг/диск. Антимикробная активность антибиотика в этой концентрации соизмерима с антимикробным действием наночастиц меди.
Следовательно, наночастицы меди (7 образцов) независимо от их размеров и структуры обладают антимикробным действием, незначительно отличаясь друг от друга по эффективности.
Пример 10. Антимикробное действие мазей с наночастицами меди образца №2, мазей с наночастицами меди образца №1, мази с O-сульфохитозаном, мази с наночастицами хитозана, комбинированной мази с наночастицами меди образца №2 и O-сульфохитозаном, комбинированной мази с наночастицами меди образца №2 и наночастицами хитозана, заводских мазей-эталонов сравнения «Солкосерила» и «Левомеколя» по показателю зон задержки роста клеток тест-культур St. albus и Е. coli AB1157
Разработанные нами мази с наночастицами меди образца №2 в концентрациях, в %: 2×10-2, 2×10-3, 2×10-4, 2×10-5, мазь с наночастицами меди образца №1 в концентрации 2×10-3%, мазь с O-сульфохитозаном в концентрации 0.05%, мазь с наночастицами хитозана в концентрации 0.0002%, комбинированная мазь с наночастицами меди образца №2 в концентрации 2×10-3% и с O-сульфохитозаном в концентрации 0.05%, комбинированная мазь с наночастицами меди образца №2 в концентрации 2×10-3% и с наночастицами хитозана в концентрации 0.0002% наносили на диски в количестве 0.2 г/диск. Диски помещали на чашки Петри с агаром, засеянные тест-культурами: St. albus и E. coli АВ 1157. Оценивали антимикробную активность разработанных мазей и заводских мазей-эталонов «Солкосерила», «Левомеколя» по величине зоны задержки роста бактерий.
Результаты приведены в таблице 9 и ФИГ.3. Наши исследования показали, что разработанные нами мази с наночастицами меди образца №2, в концентрациях, в %: 2×10-2, 2×10-3, 2×10-4, 2×10-5, мазь с наночастицами меди образца №1 в концентрации 2×10-3%, мазь с O-сульфохитозаном в концентрации 0.05%, мазь с наночастицами хитозана в концентрации 0.0002%, комбинированная мазь с наночастицами меди образца №2 в концентрации 2×10-3% и O-сульфохитозаном в концентрации 0.05%, комбинированная мазь с наночастицами меди образца №2 в концентрации 2×10-3% и наночастицами хитозана в концентрации 0.0002% обладают антимикробным действием, о чем свидетельствует образование зон задержки роста клеток тест-культуры St. albus площадью от 34.2 мм2 (мазь с O-сульфохитозаном в концентрации 0.05%) до 88.6 мм2 (комбинированная мазь с наночастицами меди образца №2 в концентрации 2×10-3% и O-сульфохитозаном в концентрации 0.05%) и зон задержки роста клеток тест-культуры Е. coli AB1157 площадью от 22.3 мм2 (мазь с O-сульфохитозаном в концентрации 0.05%) до 29.1 мм2 (мазь с наночастицами меди в концентрации 2×10-2%). Сравнение антимикробного действия разработанных нами мазей с действием заводских мазей-эталонов показало, что зоны задержки роста клеток тест-культур St. Albus и Е. coli AB1157 при нанесении на диски заводских мазей-эталонов сравнения «Солкосерила» и «Левомеколя» выше.
Следовательно, разработанные нами мази разного состава, содержащие наночастицы меди, производные низкомолекулярных хитозанов и наночастиц из них, а также комбинированные мази обладают антимикробным действием в отношении клеток тест-культур грамположительных и грамотрицательных микроорганизмов.
КРАТКОЕ ОПИСАНИЕ ФИГУР
ФИГ.1. (А): (СЭМ)* изображение наночастиц меди образца №2,
(Б): (ПЭМ)** изображение наночастиц меди образца №2.
*(СЭМ) - сканирующая электронная микроскопия,
**(ПЭМ) - просвечивающая электронная микроскопия.
На ФИГ.1 представлены фотографии наночастиц меди образца №2, полученные методами сканирующей электронной микроскопии (А) и просвечивающей электронной микроскопии (Б). Видно, что наночастицы меди образца №2 представляют собой монокристаллические структуры круглой правильной формы (А), покрытые полупрозрачной пленкой меди оксида (Б).
ФИГ.2. Кинетические кривые изменения площади экспериментальных полнослойных ран при действии мазевой основы без наночастиц (кривая 1), при действии мази с наночастицами меди образца №7 (кривая 2).
На ФИГ.2 представлены кинетические кривые изменения площади экспериментальных полнослойных ран при действии мазевой основы без наночастиц (кривая 1) и при действии мази с наночастицами меди образца №7 (кривая 2). Видно, что кинетика изменения площади ран в процессе лечения мазями с наночастицами меди свидетельствует об эффективном влиянии мазей на течение раневого процесса.
ФИГ.3. Фото чашек Петри при исследовании антимикробной активности наночастиц меди (образец №2), эталонов сравнения - мазей «Солкосерил» и «Левомеколь» дискодиффузионным методом.
А-В Мазь с наночастицами меди образца №2 в концентрациях, в %: 2×10-3 (диск №1), 0 (диск №2), 2×10-4 (диск №3), 2×10-5 (диск №4);
С-D Эталон сравнения - заводская мазь «Солкосерил»;
Е-F Эталон сравнения -заводская мазь «Левомеколь».
На ФИГ.3 представлены фотографии чашек Петри, засеянные тест-культурой Staph.albus (фотографии А, С, Е) и тест-культура E.coli 1157 (фотографии В, D, F). Рядом с чашками Петри расположены крышки с маркерами, на которых нанесены номера дисков. На фотографиях А и В представлены чашки Петри, на поверхности которых расположены диски, с дозировано найденной мазью в количестве 0.2 г с наночастицами меди образца №2 в концентрациях, в %: 2×10-3 (диск №1), 0 (диск №2), 2×10-4 (диск №3), 2×10-5 (диск №4). На фотографиях С и D представлены чашки Петри, на поверхности которых расположены диски, с дозировано нанесенной мазью «Солкосерил» в количестве 0.2 г. На фотографиях Е и F представлены чашки Петри, на поверхности которых расположены диски, с дозировано нанесенной мазью «Левомеколь» в количестве 0.2 г. Видно, что разработанные нами мази, содержащие наночастицы меди в разных концентрациях, обладают антимикробным действием в отношении клеток тест-культур грамположительных и грамотрицательных микроорганизмов.
ФИГ.4. Изменение удельной скорости ранозаживления при лечении комбинированной мазью, содержащей производное низкомолекулярных хитозанов - O-сульфохитозан и наночастицы меди образца №1 по сравнению с мазью, содержащей наночастицы меди образца №1, мазью, содержащей производное низкомолекулярных хитозанов - O-сульфохитозан, и контролем (нелеченые животные).
На ФИГ.4 представлены данные по изменению удельной скорости ранозаживления контрольной группы (нелеченые животные), группы, леченной мазью с наночастицами меди образца №1 в концентрации 0.002%, группы, леченной гелем с O-сульфохитозаном в концентрации 0.05%, и группы, леченной комбинированной мазью, содержащей наночастицы меди образца №1 в концентрации 0.002% и производное низкомолекулярных хитозанов - O-сульфохитозан в концентрации 0.05%. Видно, что лечение комбинированной мазью приводит к увеличению удельной скорости ранозаживления в 1.5 раза по сравнению с группой, леченой мазью с O-сульфохитозаном, в 1.4 раза по сравнению с группой, леченой мазью с наночастицами меди образца №1, и в 1.4 раза по сравнению с контрольной группой (нелеченые животные).
ФИГ.5. Изменение удельной скорости ранозаживления при лечении комбинированной мазью, содержащей производное низкомолекулярных хитозанов-N-сульфосукциноил-N-карбоксиметилхитозан и наночастицы меди образца №2, по сравнению с мазью, содержащей наночастицы меди образца №2, мазью, содержащей производное низкомолекулярных хитозанов - N-сульфосукциноил-N-карбоксиметилхитозан, и контролем (нелеченые животные).
На ФИГ.5 представлены данные по изменению удельной скорости ранозаживления контрольной группы (нелеченые животные), группы, леченной мазью с наночастицами меди образца №2 в концентрации 0.002%, группы, леченной гелем с N-сульфосукциноил-N-карбоксиметилхитозаном в концентрации 0.05%, и группы, леченной комбинированной мазью, содержащей наночастицы меди образца №2 в концентрации 0.002% и производное низкомолекулярных хитозанов - N-сульфосукциноил-N-карбоксиметилхитозан в концентрации 0.05%. Видно, что лечение комбинированной мазью приводит к увеличению удельной скорости ранозаживления на 26% по сравнению с мазью, содержащей N-сульфосукциноил-N-карбоксиметилхитозан в концентрации 0.05%, на 16.5% по сравнению с мазью, содержащей наночастицы меди образца №2, и на 48.5% по сравнению с контрольной группой (нелеченые животные).
ФИГ.6. Изменение удельной скорости ранозаживления при лечении комбинированной мазью, содержащей наночастицы меди образца №2 и наночастицы хитозана, синтезированные из хитозана СД 89% и М.м. 10 кДа, в концентрации 0.0002% в составе мази по сравнению с мазью, содержащей наночастицы меди образца №2, мазью, содержащей наночастицы хитозана, синтезированные из хитозана СД 89% и М.м. 10 кДа, и контролем (нелеченые животные).
На ФИГ.6 представлены данные по изменению удельной скорости ранозаживления контрольной группы (нелеченые животные), группы, леченной мазью с наночастицами меди образца №2 в концентрации 0.002%, группы, леченной гелем с наночастицами хитозана, синтезированными из хитозана СД 89% и М.м. 10 кДа, в концентрации 0.0002%, и группы, леченной комбинированной мазью, содержащей наночастицы меди образца №2 в концентрации 0.002% и наночастицы хитозана, синтезированные из хитозана СД 89% и М.м. 10 кДа, в концентрации 0.0002%. Видно, что лечение комбинированной мазью увеличивает удельную скорость ранозаживления на 10.5% по сравнению с группой, леченой мазью с наночастицами меди образца №2, увеличивает удельную скорость ранозаживления на 81.7% по сравнению с группой, леченой мазью с наночастицами хитозана, и на 40.9% по сравнению с контрольной группой (нелеченые животные).
ЛИТЕРАТУРА
1. Алексеева Т.П., Рахметова А.А., Богословская О.Д., Ольховская И.П., Левов А.Н., Ильина А.В., Варламов В.П., Байтукалов Т.А., Глущенко Н.Н. Ранозаживляющие свойства хитозана и его N-сульфосукциноилпроизводных. // Известия РАН. Серия биологическая. - 2010. - №3. - с.1-7.
2. Байтукалов Т.А., Богословская О.А., Ольховская И.П., Глущенко Н.Н., Овсянникова М.Н., Лопатин С.А., Варламов В.П. Регенерирующая активность и антибактериальное действие низкомолекулярного хитозана. // Известия Академии Наук. Серия биологическая. - 2005. - №6. - с.659-663.
3. Глущенко Н.Н., Богословская О.А., Ольховская И.П. Физико-химические закономерности биологического действия высокодисперсных порошков металлов. // Химическая физика. - 2002. - Т.21. - №4. - с.79-85.
4. Завадский С.П., Черкасова О.Г., Харитонов Ю.Я. Критерии контроля качества и свойства магнитных ректальных суппозиториев. // Хим. - фарм. журнал. - 2000. - №10.
5. Патент на изобретение №2296571. Ранозаживляющий состав и способ его получения. Байтукалов Т.А., Глущенко Н.Н., Богословская О.А., Ольховская И.П., Фолманис Г.Э., Арсентьева И.П. Заявка №2006120516. Приоритет изобретения 14 июня 2006 г. Зарегистрировано в Государственном реестре изобретений Российской Федерации 10 апреля 2007 г.
6. Патент на изобретение №2306141. Препарат, ускоряющий ранозаживление. Байтукалов Т.А., Глущенко Н.Н., Богословская О.А., Ольховская И.П., Лейпунский И.О., Жигач А.Н., Шафрановский Э.А. Заявка №2005141039. Приоритет изобретения 28 декабря 2005 г.Зарегистрировано в Государственном реестре изобретений Российской Федерации 20 сентября 2007 г.
7. Публикации 1977-2011 г. см. на Интернет-сайте: http//www.nanobiology.narod.ru
8. Рахметова А.А, Алексеева Т.П., Богословская О.А, Лейпунский И.О., Ольховская И.П, Жигач А.Н., Глущенко Н.Н. Ранозаживляющие свойства наночастиц меди в зависимости от их физико-химических характеристик. // Российские нанотехнологии. - 2010. - Том 5. - №3-4. - с.102-107.
9. Справочник по микробиологическим и вирусологическим исследованиям. / Под ред. Биргера М.О. - М.: Медицина, 1973. - 455 с.

| название | год | авторы | номер документа |
|---|---|---|---|
| ПРЕПАРАТ, УСКОРЯЮЩИЙ ЗАЖИВЛЕНИЕ РАН | 2010 |
|
RU2440122C1 |
| ПРЕПАРАТ, УСКОРЯЮЩИЙ РАНОЗАЖИВЛЕНИЕ | 2005 |
|
RU2306141C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕТЕРОГЕННОГО ФЕРМЕНТНОГО ПРЕПАРАТА НА ОСНОВЕ ФИЦИНА И НИЗКОМОЛЕКУЛЯРНОГО ХИТОЗАНА | 2021 |
|
RU2769243C1 |
| N,O-(2,3-ДИГИДРОКСИПРОПИЛ)ХИТОЗАНИЛ-БОРАТ, ОБЛАДАЮЩИЙ АНТИБАКТЕРИАЛЬНЫМ, ИММУНОМОДУЛИРУЮЩИМ И АНТИТОКСИЧЕСКИМ ДЕЙСТВИЕМ | 2014 |
|
RU2547843C1 |
| АНТИМИКРОБНЫЕ АГЕНТЫ | 2010 |
|
RU2446810C2 |
| АНТИАГРЕГАНТНОЕ СРЕДСТВО | 2017 |
|
RU2647366C1 |
| КОЖНАЯ МАЗЬ | 2007 |
|
RU2362568C1 |
| ГИДРОГЕЛЬ НА ОСНОВЕ КОМПЛЕКСНОЙ СОЛИ ХИТОЗАНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2015 |
|
RU2617501C1 |
| Катализатор для селективного окисления арабинозы в арабоновую кислоту и способ селективного окисления арабинозы в арабоновую кислоту с использованием этого катализатора | 2021 |
|
RU2778517C1 |
| СПОСОБ ВЫРАЩИВАНИЯ РАСТЕНИЙ С ИСПОЛЬЗОВАНИЕМ НАНОЧАСТИЦ МЕТАЛЛОВ И ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2015 |
|
RU2612319C1 |

Изобретение относится к области медицины. Препарат представляет собой раствор низкомолекулярных хитозанов в гидрогеле, содержащем метилцеллюлозу (МЦ-100) и нипагин. Препарат представляет собой диспергированную суспензию наночастиц меди, размер частиц 33.8÷103 нм; толщина оксидной пленки 6÷10 нм и фазовый состав: кристаллическая медь 67÷96%, и меди оксид CuO - 4÷33%, или более окисленные наночастицы меди, имеющие следующие характеристики: размер частиц 77÷119 нм и фазовый состав: кристаллическая медь 0.5÷3.3%, CuO - 27.1÷90.0% и Cu2O - 9.05÷69.50, в гидрогеле, содержащем метилцеллюлозу (МЦ-100), твин-80, нипагин и раствор низкомолекулярных хитозанов, суспензию наночастиц хитозана. Изобретение обладает высоким ранозаживляющим эффектом и антимикробным действием. 15 з.п. ф-лы, 9 табл., 6 ил., 10 пр.
1. Фармацевтическая композиция, ускоряющая ранозаживление и обладающая антимикробной активностью и включающая действующее вещество и основу, которая в качестве действующего вещества включает наночастицы меди, при этом наночастицы меди имеют следующие характеристики: размер частиц 33,8÷103 нм; толщину оксидной пленки 6÷10 нм и фазовый состав: кристаллическая медь 67÷96%, и меди оксид CuO - 4÷33% или размер частиц 77÷119 нм, фазовый состав: кристаллическая медь 0,5÷3,3%, CuO - 27,1÷90% и Cu2O - 9,05÷69,5, и содержатся в концентрации от 0,00002 до 0,002%.
2. Фармацевтическая композиция по п.1, которая дополнительно содержит производные низкомолекулярных хитозанов.
3. Фармацевтическая композиция по п.1, которая дополнительно содержит наночастицы хитозана.
4. Фармацевтическая композиция по п.1, которая содержит в качестве основы метилцеллюлозу МЦ-100 и воду.
5. Фармацевтическая композиция по п.4, которая дополнительно содержит вазелиновое масло, Твин-80 и консервант.
6. Фармацевтическая композиция по п.5, которая содержит в качестве консерванта нипагин при следующем соотношении компонентов, г на 100 г композиции:
7. Фармацевтическая композиция по п.2, которая содержит в качестве производных низкомолекулярных хитозанов O-сульфохитозан или N-сульфосукциноил-N-карбоксиметилхитозан и в качестве основы метилцеллюлозу МЦ-100 и воду.
8. Фармацевтическая композиция по п.7, которая дополнительно содержит вазелиновое масло, Твин-80 и консервант.
9. Фармацевтическая композиция по п.8, которая содержит в качестве консерванта нипагин при следующем соотношении компонентов, г на 100 г композиции:
10. Фармацевтическая композиция по п.3, которая содержит в качестве наночастиц хитозана наночастицы, синтезированные из хитозана СД 89% и М.м. 10 кДа и в качестве основы метилцеллюлозу МЦ-100 и воду.
11. Фармацевтическая композиция по п.10, которая дополнительно содержит вазелиновое масло, Твин-80 и консервант.
12. Фармацевтическая композиция по п.11, которая содержит в качестве консерванта нипагин при следующем соотношении компонентов, г на 100 г композиции:
13. Фармацевтическая композиция по п.7, которая содержит в качестве производного хитозана O-сульфохитозан или N-сульфосукциноил-N-карбоксиметилхитозан и в качестве основы метилцеллюлозу МЦ-100 и воду.
14. Фармацевтическая композиция по п.13, которая содержит в качестве консерванта нипагин при следующем соотношении компонентов, г на 100 г композиции:
15. Фармацевтическая композиция по п.10, которая содержит в качестве наночастиц хитозана наночастицы, синтезированные из хитозана СД 89% и М.м. 10 кДа и в качестве основы метилцеллюлозу МЦ-100, воду и консервант.
16. Фармацевтическая композиция по п.19, которая содержит в качестве консерванта нипагин при следующем соотношении компонентов, г на 100 г композиции:
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Повозка с гусеничным движителем | 1946 |
|
SU69398A1 |
| RU 2008114711 A, 27.10.2009 | |||
| ГИДРОФИЛЬНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ОЖОГОВ (ВАРИАНТЫ) | 2008 |
|
RU2404745C2 |
| Мазь а.б.бланшея для лечения трофических язв | 1971 |
|
SU405549A1 |
| ПРОТИВОИНФЕКЦИОННЫЕ КОМПОЗИЦИИ В ВИДЕ ГИДРОГЕЛЯ | 2005 |
|
RU2379025C2 |
| СОСТАВ ДЛЯ АНТИСЕПТИЧЕСКОЙ ОБРАБОТКИ ТКАНЫХ МАТЕРИАЛОВ | 2009 |
|
RU2408755C1 |
| УСТРОЙСТВО ДЛЯ ДОБЫЧИ НЕФТИ | 1994 |
|
RU2083796C1 |
| ИЗДЕЛИЕ, ПОДВЕРГАЕМОЕ ВОЗДЕЙСТВИЮ ГОРЯЧЕГО АГРЕССИВНОГО ГАЗА, В ЧАСТНОСТИ, ДЕТАЛЬ ГАЗОВОЙ ТУРБИНЫ (ВАРИАНТЫ) И СПОСОБ ИЗГОТОВЛЕНИЯ ТЕПЛОИЗОЛЯЦИОННОГО СЛОЯ ДЛЯ ИЗДЕЛИЯ | 1998 |
|
RU2218447C2 |
| СПОСОБ КОМПЛЕКСНОГО, ПРИ НЕОБХОДИМОСТИ - СКРЫТОГО ПОИСКА И ОБНАРУЖЕНИЯ ВЗРЫВЧАТЫХ ВЕЩЕСТВ И ВЗРЫВООПАСНЫХ ПРЕДМЕТОВ | 2000 |
|
RU2186411C2 |
Авторы
Даты
2012-09-10—Публикация
2011-04-28—Подача